OPTIMASI DAN VALIDASI METODE ANALISIS TIMBAL (Pb) MENGGUNAKAN SPEKTROFOTOMETRI SERAPAN ATOM DAN APLIKASINYA DALAM PENETAPAN KADAR TIMBAL (Pb) PADA
SEDIAAN KAPSUL CACING OBAT
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Anak Agung Istri Yulianty Suryasmi NIM : 098114029
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
i
OPTIMASI DAN VALIDASI METODE ANALISIS TIMBAL (Pb) MENGGUNAKAN SPEKTROFOTOMETRI SERAPAN ATOM DAN APLIKASINYA DALAM PENETAPAN KADAR TIMBAL (Pb) PADA
SEDIAAN KAPSUL CACING OBAT
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Anak Agung Istri Yulianty Suryasmi NIM : 098114029
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
Karya ini kupersembahkan untuk :
Ida Sang Hyang Widhi Wasa
Ibu dan Aji yang begitu luar biasa memberi dukungan, doa, kasih sayang
Adik-adikku tersayang, Gungde Kurnia dan Gunggus Rifa
Keluarga besar dan teman-temanku
vii
PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa karena atas berkat kasih dan
karunia-Nya sehingga penulis dapat menyelesaikan penelitian serta penyusunan
skripsi yang berjudul “Optimasi dan Validasi Metode Analisis Timbal (Pb)
Menggunakan Spektrofotometri Serapan Atom dan Aplikasinya dalam Penetapan
Kadar Timbal (Pb) pada Sediaan Kapsul Cacing Obat”. Skripsi ini disusun untuk
memenuhi salah satu persyaratan memperoleh gelar Sarjana Farmasi (S. Farm.) di
Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Selama pelaksanaan penelitian dan penyusunan skripsi ini, penulis banyak
mendapatkan dukungan dari berbagai pihak. Maka dari itu, penulis ingin
mengucapkan terima kasih kepada:
1. Ipang Djunarko, M.Sc., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata
Dharma Yogyakarta.
2. C.M. Ratna Rini Nastiti, M.Pharm., Apt. selaku Ketua Program Studi Fakultas
Farmasi Sanata Dharma Yogyakarta.
3. Prof. Dr. Sri Noegrahati Apt, selaku dosen pembimbing yang telah memberikan
pengarahan, bantuan, nasihat, kritik, dan saran sejak awal penelitian hingga akhir
penyusunan skripsi ini.
4. Enade Perdana Istyastono, Ph.D., Apt. selaku dosen penguji atas segala masukan
dan bimbingannya.
5. Dra. M.M. Yetty Tjandrawati, M.Si., selaku dosen penguji atas segala masukan dan
6. Rini Dwiastuti, M.Sc., selaku dosen pembimbing akademik serta atas segala
bantuan dalam perijinan penggunaan laboratorium.
7. Bapak Sanjayadi atas segala ilmu dan bantuan yang diberikan.
8. Segenap dosen yang telah berkenan membagikan ilmu kepada penulis selama
belajar di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
9. Staf sekertariat Fakultas Farmasi Mas Dwi dan Mas Narto atas segala bantuannya.
10.Mas Bimo, Pak Parlan, Mas Kunto, Mas Kethul Ismadi, Mas Ottok dan seluruh
staf laboratorium Fakultas Farmasi atas segala bantuannya selama penelitian.
11.Teman seperjuangan skripsi: Jimmy Chua, Rachelia Octavia untuk perjuangan,
kesabaran, kebersamaan dan suka dukanya.
12.Teman seperjuangan skripsi bimbingan Ibu Prof. Dr. Sri Noegrohati Apt. : Topan
Pamungkas, Leonardus Nito, Ina Juni, Kristina Nety, Johanes Dharma.
13.Teman-teman di laboratorium lantai 4 : Agnes, Novia, Victor, Agus, Shinta,
Sasya, Metri, Febrin, Wisnu.
14.Teman-teman FST A 2009 dan seluruh angkatan 2009 atas dukungan,
kebersamaan dan suka duka yang diberikan, khususnya Wanda, Kenny, Putra,
Deny, Aldo, Mikhael, Danu, Jenny, Dina, Felix, Dinda, Raras, Hera, Lambang.
Semoga pengalaman yang telah kita lalui bersama bisa menjadi kenangan di masa
depan.
15.Teman-teman kos Dewi 2 atas kebersaaman, suka dukanya, khususnya kepada
ix
16.Semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah
membantu dalam pelaksanaan penelitian dan penyusunan skripsi.
Penulis menyadari bahwa masih banyak kekurangan dalam penelitian dan
penyusunan skripsi ini mengingat keterbatasan dan kemampuan penulis, sehingga
sangat diharapkan adanya masukan dan saran yang membangun untuk penulis.
Semoga skripsi ini dapat bermanfaat bagi pembaca dan berguna bagi dunia ilmu
pengetahuan.
DAFTAR ISI
Halaman
HALAMAN JUDUL ………... i
HALAMAN PERSETUJUAN PEMBIMBING………... ii
HALAMAN PENGESAHAN………... iii
PERNYATAAN KEASLIAN KARYA………... iv
LEMBAR PERSETUJUAN PUBLIKASI KARYA……….... v
HALAMAN PERSEMBAHAN………... vi
PRAKATA……… vii
DAFTAR ISI………... x
DAFTAR TABEL……….. xv
DAFTAR GAMBAR……….. xvi
DAFTAR LAMPIRAN………... xvii
INTISARI……… xviii
ABSTRACT……….. xix
BAB I. PENGANTAR………. 1
A. Latar Belakang………. 1
1. Permasalahan...………. 4
2. Keaslian Penelitian ……… 4
3. Manfaat Penelitian ……… 5
B. Tujuan Penelitian ……….. 5
1. Tujuan Umum... 5
xi
BAB II. PENELAAHAN PUSTAKA ………... 7
Obat Tradisional dan Kapsul………..……….... 7
1. Obat Tradisional... 7
2. Kapsul... 7
a. Keseragaman Bobot... 7
A. Pencemaran Logam Berat... 8
B. Timbal... 8
1. Prinsip Spektroskopi Serapan Atom... 11
2. Instrumentasi... 12
a. Sumber Sinar……….. 12
b. Tempat Sampel... 13
c. Monokromator... 13
d. Detektor... 14
e. Readout... 14
E. Validasi Metode Analisis………. 14
2. Kisaran (Range)... 16
3. Presisi……….... 16
4. Akurasi... 18
5. Limit of Detection (LOD)... 19
6.Limit of Quantitation (LOQ)... 19
F. Landasan Teori……….. 20
G. Hipotesis………... 21
BAB III. METODE PENELITIAN ……….………… 23
A. Jenis dan Rancangan Penelitian ………...…... 23
B. Variabel Penelitian dan Definisi Operasional ………... 23
1. Klasifikasi Variabel... 23
2. Definisi Operasional... 23
C. Bahan ………... 24
D. Alat ………... 24
E. Tata Cara Penelitian ……….. 25
1. Pengumpulan Sampel………... 25
2. Uji Keseragaman Bobot Kapsul... 25
3. Penimbangan Bobot Kering Sampel ……….. 25
4. Pencucian Alat-alat Gelas... 26
5. Preparasi Cuplikan Sediaan Kapsul Cacing Obat………. 26
a. Destruksi Basah (Wet Ashing)…....………. 26
b. Penyaringan……….. 27
xiii
a. Optimasi Tinggi Burner……… 27
b. Optimasi Untuk Perbandingan Bahan Bakar dan Udara…... 28
7. Pembuatan Larutan Baku Timbal (Pb)... 28
a. Larutan Stok (1000 µg/ml)……….... 28
b. Larutan Kerja……….... 28
8. Validasi Metode Analisis………. 29
9. Penetapan Kadar Timbal Sediaan Kapsul Cacing Obat... 29
F. Analisis Hasil...………... 30
c. Pengaruh Prosedur Analisis ………... 31
d. Limit of Quantitation……….………... 31
BAB IV. HASIL DAN PEMBAHASAN ………...……….. 32
A. Preparasi Sampel Kapsul Cacing Obat... 32
1. Pemilihan Sampel………... 32
2. Keseragaman Bobot Kapsul... 32
3. Destruksi... 33
C. Validasi Instrumen Analisis... 43
1. Linearitas... 43
2. Kisaran (Range)... 44
3. Limit of Detection (LOD)... 45
D. Validasi Metode Analisis………... 46
1. Presisi... 46
2. Akurasi………... 47
3. Pengaruh Prosedur Analisis terhadap Sampel... 48
4. Limit of Quantitation (LOQ)... 50
E. Penetapan Kadar... 51
BAB V. KESIMPULAN DAN SARAN ………... 52
A. Kesimpulan ………... 52
B. Saran ………. 52
DAFTAR PUSTAKA ………... 53
LAMPIRAN ………. 56
xv
DAFTAR TABEL
Halaman
Tabel I. Perbedaan Bobot Isi Kapsul... 7
Tabel II. Kategori Metode Analisis... 15
Tabel III. Persyaratan % RSD………... 17
Tabel IV. Persyaratan % Recovery………... 18
Tabel V. Kondisi Optimum Sistem SSA ………... 38
Tabel VI. Data Presisi………... 47
Tabel VII. Data Recovery ………... 47
Tabel VIII. Hasil Significant Test 3 Replikasi... 48
Tabel IX. Mean LOQ (Limit of Quantitation)... 50
DAFTAR GAMBAR
Halaman
Gambar 1. Bagan Hipotesis………... 22
Gambar 2. Larutan Hasil Destruksi………... 35
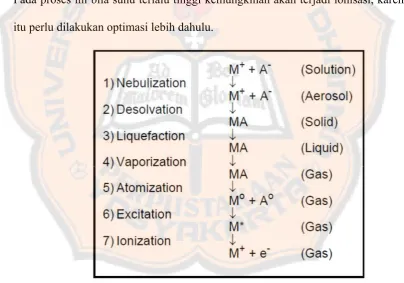
Gambar 3. Atomisasi Pada SSA ………... 37
Gambar 4. Proses Eksitasi... 38
Gambar 5. Resonance Lines Pb …... 39
Gambar 6. Ilustrasi Nyala Burner... 42
xvii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. COA Pb(NO3)2………... 57
Lampiran 2. Data Penimbangan Baku Timbal Pb(NO3)2………... 58
Lampiran 3. Data Keseragaman Bobot Kapsul………... 59
Lampiran 4. Data Penimbangan Bobot Kering ………... 61
Lampiran 5. Data Optimasi Spektroskopi Serapan Atom ……... 62
Lampiran 6. Polynomial Fit Program... 63
Lampiran 7. Perhitungan Regresi Linearitas... 64
Lampiran 8. Data Perhitungan Limit of Detection Menggunakan Powerfit... 66
Lampiran 9. Data Absorbansi 3 Replikasi Sampel Adisi (repetisi 3 kali) dan Data Recovery serta Contoh Perhitungannya... 68
Lampiran 10. Data Presisi dan Contoh Perhitungannya... 70
Lampiran 11. Data Pengaruh Prosedur Analisis terhadap Sampel... 71
Lampiran 12. Data Perhitungan Limit of Quantitation Menggunakan Powerfit... 78
Lampiran 13. Data Penetapan Kadar Sampel Kapsul Cacing Obat... 82
Lampiran 14. Significant test Kurva Baku Validasi dan Penetapan Kadar ... 84
INTISARI
Kapsul cacing obat merupakan obat bahan alam yang dipercaya berkhasiat mengobati penyakit tifus, diare, stroke dan trombosis serta berkhasiat sebagai antibakteri dan antipiretik. Kapsul cacing obat mengandung cacing tanah kering yang dikhawatirkan tercemar logam berat timbal apabila dalam pembudidayaannya tidak diperhatikan secara khusus.
Optimasi sistem spektrofotometri serapan atom dan validasi instrumen serta metode analisis dilakukan terlebih dahulu kemudian dilanjutkan dengan penetapan kadar logam berat timbal. Dalam kondisi optimum sistem SSA diperoleh validitas yang baik meliputi presisi dan akurasi yang memenuhi syarat, linearitas dengan koefisien korelasi sebesar 0,9992, Limit of Detection sebesar 0,1309 µg/mL, dan Limit of Quantitation sebesar 4,373 µ .
Kadar logam berat timbal (Pb) dalam sediaan kapsul cacing obat tanpa merek sebesar 12,647 µ , dimana kadar tersebut melebihi persyaratan BPOM
untuk obat bahan alam yaitu Pb ≤ 10,0 ppm µ , sedangkan pada sediaan kapsul cacing obat bermerek tidak terdapat cemaran logam berat timbal (Pb).
xix
ABSTRACT
Medicinal earth-worm capsule is a natural medicine with an antibacteria and antipiretic activity and believed to treat typhus, diarrhea, stroke, and thrombosis. Medicinal earth-worm capsule is made from dried earth-worm which has a risk of lead (Pb) contamination in the ground.
Optimization of atomic absorption spectrophotometry system and validation of both instrument and analysis method were did then the research was continued by the determination of lead heavy metal. When the system of AAS reached the optimum condition, the good validity included good precision and accuracy, linearity (with r = 0,9992), Limit of Detection 0,1309 µg/mL and Limit of Quantitation 4,373 were obtained.
Concentration of lead (Pb) on the medicinal earth-worm capsule without brand was 12,647 µ , which was higher than the concentration set by BPOM for
the natural medicine (Pb ≤ 10,0 ppm µ ). There was no lead (Pb) found in branded medicinal earth-worm capsule.
BAB I PENGANTAR
A. Latar Belakang
Penggunaan obat bahan alam cenderung terus meningkat dari tahun ke tahun, baik yang digunakan untuk meningkatkan kesehatan, maupun untuk pengobatan suatu penyakit. Hal ini tidak saja terjadi pada negara-negara berkembang seperti Indonesia, akan tetapi juga pada negara-negara maju. Dengan adanya kemajuan ilmu pengetahuan dan teknologi informasi, makin banyak hasil penelitian obat bahan alam dapat diakses dengan mudah melalui berbagai media elektronik, sehingga masyarakat dapat dengan mudah mendapatkan informasi terpercaya mengenai penggunaan obat bahan alam. Pengobatan dengan menggunakan obat bahan alam dipercaya berkhasiat serta efek samping yang ditimbulkan cenderung lebih ringan apabila dibandingkan dengan pengobatan menggunakan bahan kimia.
lainnya cacing tersebut dikeringkan di oven hingga kering lalu ditumbuk hingga halus dan dikonsumsi bubuk atau tepungnya. Ada juga yang dipanggang di api langsung sampai mengarang, kemudian arangnya ditumbuk sampai halus dan diseduh seperti teh (Ulfa, 2010).
Salah satu jenis cacing yang memilki khasiat, yaitu Lumbricus rubellus.
Di RRC, Korea, Vietnam, dan banyak tempat lain di Asia Tenggara, cacing jenis
Lumbricus rubellus sudah biasa digunakan sebagai obat sejak ribuan tahun lalu. Dalam pengobatan tradisional cina cacing Lumbricus rubellus ini cukup efektif dalam menyembuhkan pasien (Dina, 2012). Cacing Lumbricus rubellus memiliki enzim yang dikenal dengan lumbrokinase. Lumbrokinase memiliki efek sebagai fibrinolitik dan antitrombotik pada kasus trombosis (Verma dan Pulicherla, 2011). Selain itu cacing Lumbricus rubellus memiliki Lumbricin I yang memiliki aktivitas antibakteri (Cho, Park, Yoon dan Kim, 1998).
Dalam pembudidayaan cacing Lumbricus rubellus perlu diperhatikan media tumbuh yang digunakan serta pangan yang diberikan. Hal tersebut penting karena cacing tanah dapat menoleransi logam berat dalam konsentrasi yang cukup tinggi dan terjadi akumulasi logam berat di dalam jaringan cacing tanah (Ulfa, 2010). Penelitian ini merupakan satu rangkaian pengembangan dari penelitian
Chua (2013) mengenai “Pengaruh Pangan yang Dicemari Logam Berat Timbal
(Pb) terhadap Kadar Timbal pada Cacing Lumbricus rubellus” dan Endrastiana
(2013) mengenai “Pengaruh Fermentasi dengan Bakteri Lactobacillus terhadap
Timbal (Pb) yang Disemprotkan pada Daun Murbei yang Digunakan sebagai
Di pasaran beredar kapsul cacing obat yang berisi serbuk dari cacing
Lumbricus rubellus yang dikeringkan. Akan tetapi ada beberapa jenis kapsul cacing obat yang beredar dipasaran tidak memiliki izin dari BPOM. Maka hal ini menjadi suatu keraguan bagi peneliti terhadap pangan cacing dan proses dari pembuatan kapsul cacing ini. Apabila pembudidayaan cacing tanah yang tidak tepat pemberian pangannya, maka cemaran yang ada dipangan cacing tersebut kemungkinan dapat berpindah ke dalam tubuh cacing. Salah satunya adalah timbal yang ada didedaunan yang diambil dari tempat yang berpolusi. Polusi ini terutama polusi dari kendaraan bermotor. Bahan bakar bensin yang banyak digunakan oleh sebagian besar kendaraan di Indonesia mengandung zat tambahan TEL (tetra ethyl lead) yang digunakan untuk meningkatkan angka oktan dari bensin tersebut. TEL (timbal) ini akan ikut keluar ke udara bersama gas buang kendaraan bermotor dan mencemari udara disekitarnya (WHO, 2010).
Hal ini sungguh berbahaya terutama adanya cemaran dari logam berat timbal (Pb). Dampak dari timbal sendiri sangat mengerikan bagi manusia, utamanya bagi anak-anak. Di antaranya adalah timbal menurunkan tingkat kecerdasan, pertumbuhan dan pendengaran, menyebabkan anemia, dan dapat menimbulkan gangguan pemusatan perhatian dan gangguan tingkah laku. Pemaparan yang tinggi dapat menyebabkan kerusakan otak yang parah atau kematian (Albalak, 2001).
instrumen ini spesifik terhadap logam, dengan setiap logam memiliki garis resonansi tertentu dan lampu khusus untuk masing-masing logam. Sebelum penetapan kadar dilakukan optimasi dan validasi metode agar diperoleh kondisi optimum analisis serta diperoleh validitas yang baik terkait akurasi, presisi, linearitas, LOD dan LOQ.
1. Permasalahan
Berdasarkan latar belakang diatas, maka dapat disusun permasalahan sebagai berikut :
a. Apakah terdapat logam berat timbal dalam sediaan kapsul cacing obat yang berasal dari salah satu toko obat di Yogyakarta?
b. Apakah penetapan kadar logam berat timbal pada sediaan kapsul cacing obat menggunakan SSA memiliki validitas yang baik?
c. Berapa kadar logam berat timbal dalam sediaan kapsul cacing obat yang berasal dari salah satu toko obat di Yogyakarta dan apakah kadar logam berat timbal tersebut sesuai dengan persyaratan BPOM?
2. Keaslian penelitian
3. Manfaat penelitian
Hasil penelitian ini nantinya diharapkan mempunyai manfaat sebagai berikut :
a. Manfaat Teoretis. Menambah informasi bagi ilmu pengetahuan khususnya dalam bidang kefarmasian mengenai metode yang digunakan untuk analisis kadar logam berat (timbal) dalam kapsul cacing obat.
b. Manfaat Metodologi. Penelitian ini diharapkan dapat menjadi metode alternatif dalam penetapan kadar logam berat timbal pada suatu sediaan farmasetika.
c. Manfaat Praktis. Memberikan informasi tentang keamanan sediaan kapsul cacingobat yang tidak memiliki izin BPOM yang beredar di masyarakat.
B. Tujuan Penelitian 1. Tujuan umum
Mengetahui keamanan kapsul cacing obat dari salah satu toko obat di kota Yogyakarta yang digunakan sebagai obat tifus, diare, stroke dan trombosis serta berkhasiat sebagai antibakteri dan antipiretik.
2. Tujuan khusus
a. Mengetahui apakah terdapat logam berat timbal dalam sediaan kapsul cacing obat yang berasal dari salah satu toko obat di Yogyakarta.
c. Mengetahui berapa kadar logam berat timbal dalam sediaan kapsul cacing obat yang berasal dari salah satu toko obat di Yogyakarta dan mengetahui apakah kadar tersebut sesuai dengan persyaratan dari BPOM.
BAB II
PENELAAHAN PUSTAKA
A. Obat Tradisional dan Kapsul 1.Obat tradisional
Obat tradisional adalah obat jadi atau ramuan bahan alam yang berasal
dari tumbuhan, hewan, mineral, sediaan galenik atau campuran bahan tersebut
yang secara tradisional telah digunakan untuk pengobatan berdasarkan
pengalaman (Andalusia,Hidayat, dan Wahyuni, 2008).
2. Kapsul
Kapsul adalah bentuk sediaan obat terbungkus cangkang kapsul, keras
atau lunak. Cangkang kapsul dibuat dari Gelatin dengan atau tanpa zat tambahan
lain. Syarat kapsul harus memenuhi syarat sebagai berikut :
a. Keseragaman bobot untuk kapsul yang berisi obat kering. Timbang 20
kapsul, kemudian timbang lagi kapsul satu persatu. Keluarkan isi semua kapsul,
timbang seluruh bagian cangkang kapsul, hitung bobot isi kapsul dan bobot
rata-rata tiap isi kapsul. Perbedaan dalam persen bobot isi tiap kapsul terhadap bobot
rata-rata tiap isi kapsul tidak boleh lebih dari yang ditetapkan kolom A dan untuk
setiap 2 kapsul tidak lebih dari yang ditetapkan kolom B.
Tabel I. Perbedaan Bobot Isi Kapsul
Bobot rata-rata Isi Kapsul Perbedaan bobot isi kapsul dalam %
A B
120 mg ataukurang ± 10% ± 20%
Lebihdari 120 mg ± 7,5% ± 15%
B. Pencemaran Logam Berat
Pencemaran merupakan peristiwa adanya penambahan bermacam-macam
bahan sebagai aktivitas manusia ke dalam lingkungan, yang biasanya memberikan
pengaruh berbahaya bagi lingkungan. Pencemaran logam berat terhadap
lingkungan merupakan suatu proses yang erat hubungannya dengan penggunaan
logam tersebut oleh manusia. Logam digunakan pada alat-alat yang banyak
dipakai oleh manusia, misalnya peralatan rumah tangga, batu baterai, tempat
makanan, pipa-pipa logam, perhiasan, peralatan pertanian dan lain-lain.
Pencemaran logam dapat juga berasal dari proses produksi, misalnya pembakaran
batu bara, pemurnian minyak, pembangkit listrik (Buchari, Arka, Putra dan Sri,
2001).
C. Timbal 1. Definisi
Timbal atau yang kita kenal sehari-hari dengan timah hitam dan dalam
bahasa ilmiahnya dikenal denganPlumbum dan logam ini memiliki simbol kimia
timbal (Pb). Logam ini termasuk kedalam kelompok logam-logam golongan IV–A
pada tabel periodik unsur kimia. Mempunyai nomor atom (NA) 82 dengan massa
atom (MA) 207,2. Timbal adalah suatu logam berat berwarna kelabu kebiruan dan
lunak, dengan titik leleh 327°C dan titik didih 1.620°C. Pada suhu 550-600°C
timbal (Pb) menguap dan dengan oksigen dalam udara membentuk timbal oksida.
Bentuk oksidasi yang paling umum adalah timbal (II). Walaupun bersifat lunak
dalam air dingin dan air panas. Timbal (Pb) dapat larut dalam asam nitrat, asam
asetat dan asam sulfat pekat (Palar, 2004).
2. Keracunan timbal
Kelebihan timbale memberikan efek toksik multisistemik melalui
minimal tiga mekanisme, yaitu melalui aktivitas hambatan enzim, sebagai
konsekuensi ikatan pada gugus sulfuhidril (-SH); dengan mempengaruhi aksi
kation esensial, terutama kalsium, zat besi dan seng; dan dengan mengubah
struktur reseptor serta membrane sel (Katzung, 2004).
Gejala yang ditimbulkan pada keracunan Pb kronis, antara lain anoreksia,
lelah, malaise, sakit kepala, depresi, kelemahan otot kaki dan tangan, anemia,
neuropati perifer (Katzung, 2004).
Timbal mengakibatkan kerusakan reversible pada ginjal akibat
efeksampingnya terhadap tubulus proksimal. Hal ini akan mengganggu kerja
ginjal dalam mengabsorbsi glukosa, fosfat, dan asam amino. Efek jangka
panjangnya yaitu terjadi penurunan fungsi ginjal, termasuk atropi glomular,
fibrosis interstinal, dan sklerosis pembuluh darah (Manahan, 2003).
3. Batas maksimum
Suatu sediaan obat bahan alam dipersyaratkan tidak boleh mengandung
cemaran logam berat atau tidak melebihi batas maksimum yang diperbolehkan
D. Destruksi
Jaringan hewan dan tanaman, cairan biologis, dan komponen organik
biasanya diuraikan dengan destruksi basah. Destruksi basah dilakukan dengan
memanaskan asam atau campuran asam atau dengan pengabuan kering pada
temperatur tinggi (400-700 C°) pada tungku api. Pada destruksi basah, hasil
oksidasi dari zat organik akan menjadi karbon dioksida, air, dan zat lain yang
mudah menguap, yang didorong keluar, meninggalkan garam atau asam dari
konstituen inorganik. Pada pengabuan kering, oksigen atmosfer berfungsi sebagai
oksidan, zat organik dibakar, meninggalkan sisa inorganik. Bantuan oksidasi
dapat dilakukan setelah pengabuan kering (Christian, 2004).
1. Dry ashing (Destruksi kering)
Walaupun berbagai macam kombinasi pengabuan dan destruksi basah
digunakan dalam frekuensi yang hampir sama oleh analis organik dan material
biologik, pengabuan sederhana tanpa bantuan bahan kimia mungkin adalah teknik
yang paling banyak digunakan (Christian, 2004).
2. Wet ashing (Destruksi basah)
Destruksi basah dengan menggunakan campuran dari asam nitrat dan
asam perklorat adalah prosedur oksidasi yang paling sering dipakai. Biasanya
sejumlah kecil dari asam sulfat digunakan dengan volume asam nitrat yang lebih
besar (20-30 mL). Destruksi basah biasanya dilakukan dengan labu Kjehdahl.
Asam nitrat menghancurkan zat organik, tetapi tidak cukup panas untuk
menghancurkan senyawa organikyang tersisa. Campuran dipanaskan selama
asap SO3 putih terbentuk dan mulai berefluk dalam labu. Pada titik ini cairan akan
sangat panas, dan asam sulfat bereaksi terhadap sisa bahan organik. Destruksi
dilanjutkan sampai cairan jernih (Christian, 2004).
Campuran dari asam nitrat dan asam perklorat bisa digunakan. Asam
nitrat dipanaskan pertama, dan perhatian harus diberikan untuk mencegah
penguapan dari asam perklorat hingga hampir mengering atau ledakan keras akan
timbul, prosedur ini tidak direkomendasikan kecuali telah memiliki pengalaman
dalam prosedur destruksi. Asam perklorat tidak boleh ditambahkan langsung ke
material organik atau biologis. Selalu tambahkan asam nitrat pertama kali.
Ledakan dengan asam perklorat biasa dihubungkan dengan pembentukan
peroksida dan asam berubah warna menjadi gelap sebelum ledakan (Christian,
2004).
E. Spektroskopi Serapan Atom 1. Prinsip spektroskopi serapan atom
Spektroskopi serapan atom digunakan untuk analisis kuantitatif
unsur-unsur logam dalam jumlah sekelumit (trace) dan sangat kelumit (ultratrce). Cara
analisis ini memberikam kadar total unsur logam dalam suatu sampel dan tidak
tergantung pada bentuk molekul dari logam dalam sampel tersebut. Cara ini cocok
untuk analisis kelumit logam karena mempunyai kepekaan yang tinggi (batas
deteksi kurang dari 1 ppm), pelaksanaannya relatif sederhana, dan interferensinya
sedikit. Spektroskopi serapan atom didasarkan pada penyerapan energi sinar oleh
Dalam garis besarnya prinsip spektroskopi serapan atom sama saja dengan
spektrofotometri sinar tampak dan ultraviolet. Perbedaannya terletak pada bentuk
spektrum, cara pengerjaan sampel dan peralatannya(Gandjar dan Rohman, 2007).
Interaksi materi dengan berbagai energi seperti energi panas, energi
radiasi, energi kimia dan energi listrik selalu memberikan sifat-sifat yang
karakteristik untuk setiap unsur (atau persenyawaan) dan besarrnya perubahan
yang terjadi biasanya sebanding dengan jumlah unsur atau persenyawaan yang
terdapat didalamnya. Didalam kimia analisis yang mendasarkan pada proses
interaksi itu antara lain cara analisis spektrofotometri atom yang bisa berupa cara
emisi dan cara absorpsi (serapan) (Gandjar dan Rohman, 2007).
2. Instrumentasi
a. Sumber Sinar.Sumber sinar yang biasanya digunakan adalah lampu
katoda berongga (hollow cathode lamp). Lampu ini terdiri atas tabung kaca
tertutup yang mengandung suatu katoda dan anoda. Katoda berbentuk silinder
berongga yang terbuat dari logam atau dilapisi dengan logam tertentu. Tabung
logam ini diisi dengan gas mulia (neon atau argon) dengan tekanan rendah (10-15
torr). Neon biasanya lebih disukai karena memberikan intensitas pancaran lampu
yang lebih rendah. Salah satu kelemahan penggunaan lampu katoda berongga
adalah satu lampu digunakan untuk satu unsur, akan tetapi saat ini telah banyak
dijumpai suatu lampu katoda berongga kombinasi, yakni satu lampu dilapisi
beberapa unsur sehingga dapat digunakan untuk analisis beberapa unsur sekaligus
b. Tempat Sampel.Dalam analisis dengan spektrofotometri serapan atom,
sampel yang dianalisis harus diuraikan menjadi atom-atom netral. Ada berbagai
macam alat yang dapat digunakan untuk mengubah suatu sampel menjadi uap
atom-atom yaitu dengan nyala (flame) dan dengan tanpa nyala (flameless).
Nyala digunakan untuk mengubah sampel yang berupa padatan atau
cairan menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi. Nyala
biasanya berupa udara/asetilen, menghasilkan suhu ± 2500 oC. Dinitrogen
oksida/asetilen dapat digunakan untuk menghasilkan suhu sampai 3000 oC yang
diperlukan menguapkan garam-garam dari unusr-unsur seperti aluminium atau
kalsium (Watson, 2007).
Tanpa nyala (Flameless) digunakan karena teknik atomisasi dengan
nyala dinilai kurang peka karena atom gagal mencapai nyala, tetesan sampel yang
masuk ke dalam nyala terlalu besar, dan proses atomisasi kurang sempurna. Oleh
karena itu, muncullah suatu teknik atomisasi yang baru yakni atomisasi tanpa
nyala. Pengatoman dapat dilakukan dalam tungku dari grafit seperti tungku yang
dikembangkan oleh Masmann(Gandjar dan Rohman, 2007).
c. Monokromator. Monokromator digunakan untuk menyempitkan lebar
pita radiasi yang sedang diperiksa sehingga diatur untuk memantau panjang
gelombang yang sedang dipancarkan oleh lampu katode rongga. Hal ini
menghilangkan interferensi oleh radiasi yang dipancarkan dari nyala tersebut, dari
gas pengisi di dalam lampu katode rongga, dan dari unsur-unsur lain di dalam
Monokromator dimaksudkan untuk memisahkan dan memilih panjang
gelombang yang digunakan dalam analisis. Disamping sistem optik, dalam
monokromator juga terdapat suatu alat yang digunakan untuk memisahkan radiasi
resonansi dan kontinyu yang disebut dengan chopper (Watson, 2007).
d.Detektor.Detektor digunakan untuk mengukur intensitas cahaya yang
melalui tempat pengatoman. Biasanya digunakan tabung penggandaan foton. Ada
dua cara yang dapat digunakan dalam sistem deteksi yaitu memberikan respon
terhadap radiasi resonansi dan radiasi kontinyu serta memberikan respon terhadap
radiasi resonansi saja (Watson, 2007).
e. Readout.Readout merupakan suatu alat penunjuk atau dapat juga
diartikan sebagai sistem pencatatan hasil. Pencatatan hasil dilakukan dengan suatu
alat yang telah terkalibrasi untuk pembacaan suatu transmisi atau absorbsi. Hasil
pembacaan dapat berupa angka atau berupa kurva dari suatu recorder yang
menggambarkan absorbansi atau intensitas emisi(Gandjar dan Rohman, 2007).
F. Validasi Metode Analisis
Suatu metode perlu divalidasi atau direvalidasi apabila: sebelum
metodetersebut digunakan secara rutin; suatu metode yang telah divalidasi
dilakukanpada kondisi yang berbeda (misalnya pada alat yang karakteristiknya
berbeda);metodenya berubah dan perubahan itu di luar jangkauan metode semula;
kontrolkualitas menunjukkan metode tersebut berubah seiring berjalannya waktu;
denganmetode standar/baku) Validasi metode analisis dapat digunakan pada
analisissenyawa obat dan produk obat (Ahuja dan Rasmussen, 2007).
Menurut Snyder, Kirkland, dan Galjh. (2010), metode analisis
dapatdikelompokkan menjadi 4 kategori yaitu:
1. Kategori 1, merupakan metode analisis yang digunakan untuk
mengukurkomponen utama/jumlah besar (termasuk bahan pengawet) atau
bahan aktifobat dari suatu sediaan.
2. Kategori 2, merupakan metode analisis untuk penentuan impurities bahan
obatdan degradasi produk obat, termasuk penentuan kuantitatif dan uji batas.
3. Kategori 3, merupakan metode analisis yang digunakan untuk
menentukankarakteristik sediaan farmasi (misalnya disolusi).
4. Kategori 4, merupakan metode analisis untuk identifikasi secara kualitatif.
Setiap kategori metode analisis memiliki persyaratan validasi
yangberbeda-beda sepertitercantum pada tabel II berikut.
Tabel II. Kategori Metode Analisis(Snyder, Kirkland, dan Galjh, 2010)
1. Linearitas
Linearitas merupakan kemampuan suatu metode untuk memperoleh
hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada
kurva kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x).
Linearitas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi
yang berbeda-beda. Data yang diperoleh berupa nilai kemiringan (slope), intersep,
dan koefisien korelasi (Gandjar dan Rohman, 2007).
2. Kisaran (Range)
Kisaran atau range suatu metode merupakan interval konsentrasi analit
terendah dan tertinggi dalam suatu sampel yang mana telah memenuhi linearitas,
presisi dan akurasi dalam suatu metode. Kisaran-kisaran konsentrasi yang diuji
tergantung pada jenis metode dan kegunaannya. Untuk pengujian komponen
utama, maka konsentrasi baku harus diukur di dekat atau sama dengan konsentrasi
kandungan analit yang diharapkan (Gandjar dan Rohman, 2007).
3. Presisi
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
dapat dilihat sebagai simpangan baku relatif dari sejumlah sampel yang berbeda
signifikan secara statistik (Gandjar dan Rohman, 2007).
Menurut ICH, presisi dikategorikan menjadi 3 tingkatan yang berbeda
yaitu repeatibility, intermediate precision dan reproducibility.Repeatibility yaitu
ketepatan (precision) pada kondisi percobaan yang sama (berulang) baik
orangnya, peralatannya, tempatnya, maupun waktunya. Analisis Repeatibility
dapat dilakukan dengan membuat tiga konsentrasi yang berbeda-beda dengan tiga
kali replikasi masing-masing konsentrasi.Intermediate precision yaitu ketepatan
tempatnya, maupun waktunya.Reproducibilitymenggambarkanpresisi yang
diperolehantarlaboratorium(Chan,Lam, Lee dan Zhang, 2004).
Presisi mencakup simpangan baku, simpangan baku relatif (RSD) atau
koefisien variasi (CV), dan kisaran kepercayaan. Pengujian presisi pada validasi
metode sebagian besar menggunakan repeatibility dan intermediate precision.
Reproducibility biasanya dilakukan untuk membandingkan hasil uji antar
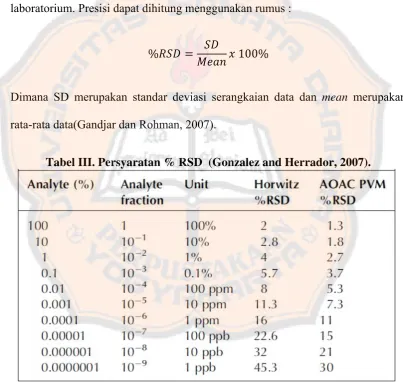
laboratorium. Presisi dapat dihitung menggunakan rumus :
% 100%
Dimana SD merupakan standar deviasi serangkaian data dan mean merupakan
rata-rata data(Gandjar dan Rohman, 2007).
4. Akurasi
Akurasi merupakan ketelitian metode analisis atau kedekatan antara nilai
terukur dengan nilai yang diterima baik nilai konvensi, nilai sebenarnya, atau nilai
rujukan. Akurasi diukur sebagai banyaknya analit yang diperoleh kembali pada
suatu pengukuran dengan melakukan spiking pada suatu sampel. Untuk pengujian
bahan obat, akurasi diperoleh dengan membandingkan hasil pengukuran dengan
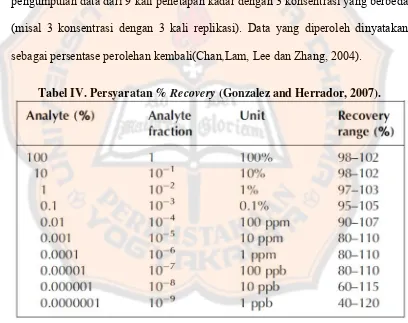
standard reference. Untuk mendokumentasikan akurasi, ICH merekomendasikan
pengumpulan data dari 9 kali penetapan kadar dengan 3 konsentrasi yang berbeda
(misal 3 konsentrasi dengan 3 kali replikasi). Data yang diperoleh dinyatakan
sebagai persentase perolehan kembali(Chan,Lam, Lee dan Zhang, 2004).
5. Limit of Detection (LOD)
LOD merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi
dan masih memberikan respon signifikan dibandingkan dengan blangko. LOD
dapat dihitung secara statistic melalui garis regresi linier dari kurva kalibrasi.
LOD dapat dihitung menggunakan rumus :
b Sa
LOD 3,3 (Ermer and Miller, 2005).
LOD seringkali diekspresikan sebagai suatu konsentrasi pada signal to noise
ratio, rasio yang digunakan biasanya 2 atau 3 dibanding 1. ICH mengenalkan
suatu konvensi metode signal to noise ini, dan dua metode pilihan lain untuk
menentukan LOD, yaitu metode non instrumental visual dan dengan metode
perhitungan. Metode non instrumental visual digunakan pada teknik kromatografi
lapis tipis dan pada metode titrimetri. LOD juga dapat dihitung berdasarkan pada
standar deviasi (SD) respon dan kemiringan (slope) kurva baku pada level yang
mendekati LOD sesuai dengan rumus. Standar deviasi respon dapat ditentukan
berdasarkan pada standar deviasi blanko, pada standar deviasi residual dari garis
regresi, atau standar deviasi intersep y pada garis regresi (Gandjar dan Rohman,
2007).
6. Limit of Quantitation (LOQ)
LOQ merupakan konsentrasi analit terendah dalam sampel yang dapat
ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi
operasional metode yang digunakan. Sebagaimana LOD, LOQ juga diekspresikan
merupakan aturan umum, meskipun demikian perlu diingat bahwa LOQ
merupakan suatu kompromi antara konsentrasi dengan presisi dan akurasi yang
dipersyaratkan. Jadi, jika konsentrasi LOQ menurun maka presisi juga menurun.
Jika presisi tinggi dipersyaratkan, maka konsentrasi LOQ yang lebih tinggi harus
dilaporkan(GandjardanRohman, 2007).
ICH mengenalkan suatu konvensi metode signal to noise ini, dan dua
metode pilihan lain untuk menentukan LOQ, yaitu metode non instrumental visual
dan dengan metode perhitungan. LOQ dapat dihitung berdasarkan pada standar
deviasi (SD) respon dan kemiringan (slope) kurva baku sesuai dengan rumus.
Standar deviasi respon dapat ditentukan berdasarkan pada standar deviasi blanko,
pada standar deviasi residual dari garis regresi, atau standar deviasi intersep y
pada garis regresi (Gandjar dan Rohman, 2007).
LOQ dapat dihitung secara statistic melalui garis regresi linier dari kurva
kalibrasi. LOQ dapat dihitung menggunakan rumus :
b Sa
LOQ 3,3 (Ermer and Miller, 2005).
G. Landasan Teori
Kapsul cacing obat merupakan obat bahan alam yang dipercaya
berkhasiat mengobati penyakit tifus, diare, berkhasiat sebagai antibakteri dan
antipiretik (Dina, 2012) serta mengobati stroke dan thrombosis (Verma dan
Pulicherla, 2011). Kapsul cacing obat mengandung cacing tanah kering
Lumbricus rubellus. Sediaan ini dikhawatirkan tercemar logam berat seperti
khusus. Apabila pangan yang diberikan diambil dengan sembarangan misalnya
dari pinggir jalan maka akan ada kemungkinan terdapat cemaran logam berat
salah satunya timbal.
Penggunaan cacing tanah kering sebagai obat biasanya dikemas dalam
bentuk kapsul. Kapsul cacing obata dalah bentuk sediaan obat terbungkus
cangkang kapsul, yang berisi obat kering (cacing kering). Sediaan kapsul cacing
obat yang dianalisis adalah produk yang tidak memiliki izin BPOM/tanpa merek
dan yang memiliki izin BPOM/bermerek.
Keberadaan timbale ini dapat dideteksi dengan menggunakan instrument
spektrofotometri serapan atom. Dimana instrument ini bias dengan spesifik
mendeteksi keberadaan timbale meski ada logam-logam lain yang dapat
mengganggu dari pembacaan alat ini (Beaty and Kerber, 1993). Destruksi yang
dipilih adalah destruksi basah karena keamanan dari pengerjaannya terjamin
dengan pelarut yang digunakan untuk destruksi adalah H2SO4 dan HNO3
(Christian, 2004). Untuk mendapatkan hasil yang optimal maka perlu dilakukan
optimasi sistem SSA. Optimasi yang dilakukan antara lain optimasi tinggi burner
dan optimasi untuk perbandingan bahan bakar dan udara. Selain itu juga perlu
dilakukan validasi metode agar hasil yang nantinya didapatkan valid.
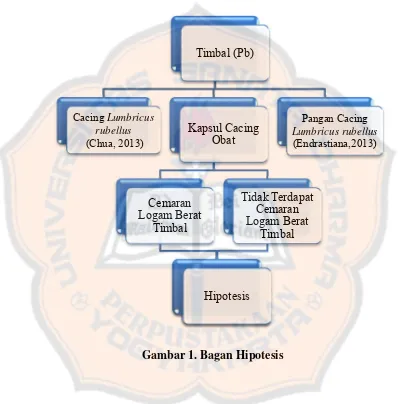
H. Hipotesis
1. Metode penetapan kadar logam berat timbal pada sediaan kapsul cacing obat
2. Terdapat cemaran logam berat timbal pada kapsul cacing obat yang berasal dari
salah satu toko obat di Yogyakarta.
Gambar 1. Bagan Hipotesis Timbal (Pb)
Cacing Lumbricus rubellus (Chua, 2013)
Kapsul Cacing Obat
Cemaran Logam Berat
Timbal
Tidak Terdapat Cemaran Logam Berat
Timbal
Hipotesis
Pangan Cacing Lumbricus rubellus
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan jenis penelitian eksperimental dengan
rancangan acak.
B. Variabel Penelitian dan Definisi Operasional 1. Klasifikasi variabel
a. Variabel bebas dalam penelitian ini adalah kadar seri larutan baku
Pb(NO3)2, tinggi burner, perbandingan bahan bakar dan udara.
b. Variabel tergantung dalam penelitian ini adalah aborbansi dari seri larutan
baku Pb(NO3)2, absorbansi dari sampel kapsul cacing obat dan parameter
optimasi serta parameter validasi yang dihasilkan.
c. Variabel pengacau terkendali dalam penelitian ini yaitu kualitas bahan
baku, pelarut dan sampel kapsul cacing obat yang digunakan.
2. Definisi operasional
a. Kapsul cacing obat adalah bentuk sediaan obat terbungkus cangkang kapsul,
yang berisi obat kering (cacing kering). Sediaan kapsul cacing obat yang
dianalisis adalah produk yang tidak memiliki izin BPOM dan tidak
b. Cemaran logam berat adalah cemaran logam berat timbal pada kapsul cacing
obat yang diukur dengan spektrofotometri serapan atom dan dinyatakan
dalam ppm (part per million). Dalam penelitian ini ppm yaitu µg/g.
c. Spektrofotometri serapan atom adalah spektrofotometri yang berprinsip pada
absorbsi cahaya oleh atom. Atom-atom menyerap cahaya tersebut pada
panjang gelombang tertentu, tergantung pada sifat unsurnya. Pada penelitian
ini dianalisis logam berat timbal pada resonance lines 283,3 nm.
C. Bahan
Bahan-bahan yang digunakan dalam penelitian ini antara lain sampel
sediaan kapsul cacing obat yang berasal dari salah satu toko obat di Yogyakarta,
asam bikromat 1% teknis (Laboratorium Kimia Organik Fakultas Farmasi
Universitas Sanata Dharma), Pb(NO3)2 p.a Merck®, H2SO4 p.a. Merck®, HNO3
p.a. Merck®, aquabidest (Laboratorium Kimia Analisis Instrumental Fakultas
Farmasi Universitas Sanata Dharma).
D. Alat
Alat-alat yang digunakan dalam penelitian ini antara lain alat-alat gelas
merek Pyrex®, hotplate merek LabTech®, seperangkat instrumen SSA merek
Perkin Elmer ® dengan tipe nyala udara : asetilen, neraca analitik dengan kepekaan
E. Tata Cara Penelitian 1. Pengumpulan sediaan kapsul cacing obat
Sediaan kapsul cacing obat diperoleh dari salah satu toko obat di
Yogyakarta. Sampel yang digunakan merupakan sampel dengan kode produksi
sama kemudian dilakukan uji keseragaman bobot.
2. Uji keseragaman bobot kapsul
Ditimbang 20 kapsul, kemudian ditimbang lagi kapsul satu persatu.
Semua isi kapsul dikeluarkan, kemudian ditimbang seluruh bagian cangkang
kapsul. Dihitung bobot isi kapsul dan bobot rata-rata tiap isi kapsul. Perbedaan
dalam persen bobot isi tiap kapsul terhadap bobot rata-rata tiap isi kapsul tidak
boleh lebih dari yang ditetapkan kolom A dan untuk setiap 2 kapsul tidak lebih
dari yang ditetapkan kolom B (Dirjen POM, 1979).
3. Penimbangan bobot kering sampel
Wadah dipanaskan dalam oven pada suhu 105oC selama 1 jam,
ditimbang kemudian dipanaskan kembali dalam oven pada suhu 105oC selama 1
jam. Cara ini dilakukan berulang kali sampai diperoleh bobot tetap. Bobot tetap
berarti selisih dua kali penimbangan sampel berturut-turut tidak lebih dari 0,5 mg
tiap g sisa yang ditimbang. Penimbangan bobot kering juga dilakukan terhadap
sampel yang digunakan. Ditimbang 1-2 g sampel kemudian lakukan seperti
prosedur diatas menggunakan wadah yang telah dikuantifikasi (Dirjen POM,
4. Pencucian alat-alat gelas
Alat-alat gelas yang akan digunakan untuk analisis, dibilas dengan asam
bikromat 1% dan H2SO4 kemudian didiamkan pada lemari asam selama 24 jam
lalu dibilas dengan aquabidest. Setelah kering, alat ini dimasukkan dalam kantong
plastik dan disimpan dalam ruang bebas debu. Sebelum digunakan, peralatan
dibilas dengan HNO3 1 M terlebih dahulu (AOAC, 2007).
5. Preparasi cuplikan sediaan kapsul cacing obat
a. Destruksi Basah (Wet Ashing). Ditimbang seksama 2,5 gram sampel
(bobot kering) dalam labu Erlenmeyer 50 mL (sebelumnya dicuci asam dan
dikeringkan). Ditambahkan 7,5 mL H2SO4 pekat diikuti oleh 12,5 mL HNO3 pekat
ke dalam erlenmeyer. Sampel dipanaskan di hot plate pada suhu ±130°C
(mendidih). Asap cokelat-kuning akan muncul. Setelah asap cokelat-kuning
tersebut hilang, maka akan mucul asap putih dari H2SO4. Hal ini menunjukkan
proses penguraian H2SO4 dan sampel akan berwarna lebih gelap. Dengan segera
erlenmeyer dipindahkan dari pemanas dan perlahan-lahan ditambahkan HNO3
pekat sedikit demi sedikit (catatan: suhu cairan dalam erlemenyer tidak boleh
turun hingga sama dengan suhu kamar). Erlenmeyer diletakkan kembali pada
pemanas dan HNO3 dididihkan lagi. Dilanjutkan sampai warna larutan menjadi
jernih, yaitu berwarna kuning jerami. Jika larutan itu masih gelap warnanya
ditambahkan HNO3 pekat kembali dan dididihkan lagi. Proses ini diulangi sampai
larutan tersebut jernih, kuning jerami dan ketika dimasukkan kedalam wadah yang
berisi es tidak terbentuk gumpalan minyak. Sampel dibiarkan mendingin sampai
b. Penyaringan. Penyaringan dilakukan dengan menggunakan corong
burner dan kertas Whatman No.42. Kertas saring dijenuhkan dengan HNO3 1 M
lalu diletakkan di bagian dalam corong. Corong diletakkan pada mulut labu hisap
yang sudah terhubung dengan vaccum. Sebanyak 5 mL HNO3 1 M dituangkan ke
dalam erlenmeyer yang berisi timbal hasil destruksi basah kemudian saring.
Prosedur ini dilakukan sebanyak tiga kali hingga tidak ada sampel yang tertinggal
di Erlenmeyer. Sebanyak 5 mL HNO3 1 M dituangkan melewati kertas saring tadi
untuk mengantisipasi adanya sampel yang tertinggal di kertas saring dan corong.
Lalu HNO3 1 M ditambahkan hingga batas tanda pada labu ukur 50 mL. Labu
ukur ditutup, lalu dikocok dan dipindahkan ke wadah plastik. Larutan siap
diujikan ke SSA pada kondisi optimum (dilakukan tiga kali replikasi) (AOAC,
2007).
6. Optimasi metode analisis
a. Optimasi Tinggi Burner. Tekanan bahan bakar dan gas pembawa
diatur sampai nyala api stokiometrik nyala berwarna kuning tipis. Tekanan
dinaikkan sampai nyala berpijar kuning kuat. Larutan Pb 5 ppm disiapkan dan
absorbansinya dicatat pada 283,3 nm dan λ diatur hingga absorbansi maksimum.
Tinggi burner diatur hingga cahaya tampak melalui ujungnya dengan tombol.
Aquabidest digunakan untuk autozero instrumen lalu diukur absorbansi dari
larutan Pb 5 ppm. Tinggi burner diturunkan secara bertahap dan absorbansinya
b. Optimasi untuk Perbandingan Bahan Bakar dan Udara. Digunakan
tipe nyala udara : asetilen dengan perbandingan 20:5 dan 20:10. Tekanan udara
dijaga konstan dan tekanan bahan bakar diatur bertahap dari kaya bahan bakar
hingga nyala kecil. Absorbansi Pb 5 ppm dicatat pada setiap penambahan.
Tekanan bahan bakar dipilih yang optimum dan tekanan udara diubah dengan cara
yang sama. Absorbansi vs tekanan udara diplot, dengan catatan satu dibuat
konstan. Setting tekanan bahan bakar dipilih yang optimum.
7. Pembuatan larutan baku timbal (Pb)
a. Larutan Stok (1000 µg/mL). Dilarutkan 0,3197 g Pb(NO3)2 dalam 50
mL HNO3 1M dalam labu takar 200 mL, kemudian ditambahkan HNO3 1M
hingga batas tanda pada labu. Konsentrasi 1000 µg/mL didapat dari:
207,2
331,2098 0,3197 /200
999,9982 μ /
b. Larutan Kerja. Disiapkan Pb 100 µg/mL (intermediet) dengan
mengencerkan 10 mL larutan stok hingga 100 mL dengan larutan HNO3 1M.
Kemudian dibuat seri kurva baku yaitu 0,1 ; 0,5 ; 1,0 ; 1,5 ; 2,0 ; 2,5 dan 3,0
µg/mL dari larutan intermediet. Kurva kalibrasi unsur Pb diperoleh dengan
mengukur serapan larutan standar unsur pada kondisi optimum. Kurva kalibrasi
diperoleh dengan membuat kurva antara konsentrasi terhadap serapan Pb.
8. Validasi metode analisis
Validasi metode analisis yang dilakukan meliputi presisi, recovery,
pengaruh prosedur analisis terhadap sampel dan Limit of Quantitation (LOQ).
Prosedur dari parameter-parameter tersebut adalah sebagai berikut : dibuat larutan
blangko yang berisi 2,5 g sampel kapsul cacing obat kemudian didestruksi dan
dilakukan penyaringan (seperti pada prosedur 5a dan 5b). Kemudian sebelum
proses destruksi ke dalam 2,5 g sampel ditambahkan 10 mL larutan standar
Pb(NO3)2 p.a dengan konsentrasi 2 ppm, 4 ppm, 6 ppm, 8 ppm dan 10 ppm.
Setelah didestruksi kemudian disaring dengan kertas Whatman no.42 dan diukur
absorbansinya menggunakan SSA pada kondisi optimum dengan resonance lines
283,3 nm. Dilakukan tiga kali replikasi.
9. Penetapan kadar logam berat timbal pada sediaan kapsul cacing obat Larutan sampel hasil destruksi dan penyaringan diambil kemudian
diencerkan dalam labu ukur 50 mL, setelah itu diukur absorbansinya
menggunakan SSA dengan kondisi optimum pada resonance lines 283,3 nm.
F. Analisis Hasil
1. Analisis hasil seri kurva baku atau validasi instrumen : a. Korelasi signal/linearitas
Linearitas ditentukan dari koefisien korelasi (r) yang diperoleh dari
persamaan regresi linear.
b. Sensitivitas/limit of detection LOD dapat dihitung dengan rumus:
3 ,3
Sa = standar deviasi dari intersep kurva baku, b adalah slope dari kurva
baku.
c. Kisaran (Range)
Kisaran diperoleh dengan cara melihat interval konsentrasi terendah dari
analit dan konsentrasi tertinggi analit yang telah memenuhi parameter
linearitas, presisi dan akurasi yang baik.
2. Analisis hasil dari validasi metode yaitu : a. Akurasi
Perolehan Kembali (recovery) = x 100%
b. Presisi
c. Pengaruh prosedur analisis terhadap sampel
Pengaruh prosedur analisis terhadap sampel dapat dilihat dengan plot kurva
baku standar dan kurva baku adisi kemudian kedua kurva tersebut
dibandingkan dengan significance tests.
d.Limit of Quantitation
LOQ dapat dihitung dengan rumus:
3,3
Sa = standar deviasi dari intersep kurva baku adisi, b adalah slope dari kurva
32 BAB IV
HASIL DAN PEMBAHASAN
A. Preparasi Sampel Kapsul Cacing Obat 1. Pemilihan sampel
Sampel yang digunakan pada penelitian ini merupakan kapsul cacing obat
yang diperoleh dari salah satu toko obat di Yogyakarta. Pengambilan sampel
dilakukan secara acak namun sebelumnya dipilih sampel dengan kode produksi
yang sama. Hal ini dilakukan untuk menjamin kesamaan kondisi sampel selama
satu proses produksi, distribusi dan penyimpanan hingga sebelum dilakukan
penetapan kadar cemaran logam berat timbal pada sampel tersebut. Kesamaan
kondisi sampel ini diharapkan dapat mencegah keragaman kadar yang akan
dihasilkan. Terdapat dua sampel yang digunakan yaitu sampel cacing obat
bermerek dan sampel cacing obat tanpa merek. Pada sampel kapsul cacing obat
bermerek terdapat no.registrasi dari BPOM, komposisi kapsul cacing obat, aturan
pakai dan peringatan. Namun, pada sampel kapsul cacing obat tanpa merek hanya
terdapat satu komposisi, yaitu mengandung ekstrak cacing Lumbricus rubellus.
Dari kedua sampel tersebut dapat dibandingkan kadar yang akan dihasilkan.
2. Keseragaman bobot kapsul dan penimbangan bobot kering
Setelah pemilihan sampel dilakukan uji keseragaman bobot kapsul
terhadap kapsul cacing obat. Penimbangan bobot kering dilakukan terhadap
sampel yang telah diuji keseragaman bobotnya. Penimbangan bobot kering
dan bahan dalam ruangan akan memberikan lembab (air) yang berasal dari udara
pada wadah/sampel yang akan digunakan. Karena itu perlu dilakukan
penimbangan bobot kering untuk mengetahui bobot yang sebenarnya dari wadah
atau sampel yang akan digunakan. Penimbangan bobot kering dilakukan dengan
melakukan penimbangan bobot berulang kali hingga diperoleh bobot tetap. Bobot
tetap yang dimaksud adalah bobot dengan selisih antara tiap penimbangan tidak
lebih dari 0,5 mg tiap gram sisa yang ditimbang. Prosedur ini dilakukan dengan
pemanasan dalam oven selama satu jam dengan suhu 105oC, kemudian
didinginkan dalam desikator. Desikator merupakan suatu wadah yang terbuat dari
bahan gelas yang kedap udara dan mengandung desikan yang dapat menyerap air.
Kadar air dari sampel kapsul cacing obat yaitu sebesar 0,16 %. Setelah didapatkan
bobot kering maka selanjutnya dilakukan proses destruksi.
3. Destruksi
Pada tahap preparasi sampel kapsul cacing obat, setelah serbuk ditimbang
dalam bobot keringnya dilakukan proses destruksi. Dalam penggunaan instrumen
SSA, sampel yang akan dianalisis harus tidak mengandung molekul atau senyawa
organik yang dapat menimbulkan jelaga (arang) dan tidak mengandung partikel
tidak larut yang dapat menyumbat saluran kapiler instrumen. Karena itu setiap
sampel yang akan diukur harus mengalami proses destruksi untuk menghilangkan
molekul-molekul organik. Molekul organik yaitu molekul yang secara umum
tersusun dari rantai karbon, seperti lemak, protein dan karbohidrat. Penggunaan
intrumen SSA melibatkan proses pembakaran pada suhu tinggi agar terjadi
karbon) yang ikut terbakar dapat menimbulkan noda jelaga (arang) pada
instrumen. Noda tersebut dapat terakumulasi dalam instrumen sehingga
menyebabkan penyumbatan dan kerusakan pada bagian-bagian di sekitar burner.
Destruksi sampel dilakukan dengan proses oksidasi menggunakan asam
pengoksidasi sehingga molekul organik yang ada pada sampel dapat teroksidasi
dan berubah menjadi fase gas dalam bentuk karbondioksida dan air. Destruksi
merupakan proses penghancuran bahan-bahan organik dalam sampel sehingga
ikatan antara senyawa organik dengan logam yang akan dianalisis terputus.
Terdapat dua cara destruksi yaitu destruksi basah (wet ashing) dan destruksi
kering (dry ashing). Pada destruksi basah biasanya digunakan kombinasi dari
beberapa pengoksidasi seperti asam nitrat, hidrogen peroksida, asam perklorat dan
katalis seperti asam sulfat, sedangkan destruksi kering menggunakan suhu
pemanasan yang tinggi.
Dalam penelitian ini digunakan destruksi basah karena untuk unsur dalam
konsentrasi rendah akan lebih dapat terbaca dibandingkan dengan destruksi kering
yang menggunakan suhu tinggi, pemanasan dengan suhu tinggi dikawatirkan
dapat mengakibatkan hilangnya unsur-unsur mikro tertentu. Menurut Palar (2004)
pada suhu 550-600°C timbal (Pb) menguap dan dengan oksigen dalam udara
membentuk timbal oksida. Saat proses destruksi kering terjadi pemanasan hingga
temperatur 500-550 oC, hal tersebut kemungkinan akan mengakibatkan
kehilangan Pb (Hseu, 2004). Selain itu pada destruksi kering digunakan wadah
yang terbuat dari silika atau porselin karena itu bisa terjadi proses adsorpsi
dihancurkan seluruhnya oleh asam. Hal tersebut membuat hasil yang diperoleh
menjadi tidak kuantitatif karena banyak unsur logam yang hilang.
Pada proses destruksi ditambahkan 7,5 mL H2SO4 pekat diikuti oleh 12,5
mL HNO3 pekat ke dalam erlenmeyer. Kemudian dipanaskan di hot plate pada
suhu ±130°C, pemanasan dilakukan untuk mempercepat proses oksidasi.
Mulainya proses oksidasi akan ditandai dengan munculnya gas kuning kecoklatan
dari larutan sampel. Apabila asam nitrat habis menguap ditandai dengan berhenti
atau berkurangnya gas kuning kecoklatan yang muncul, dan digantikan gas putih
yang menunjukkan adanya penguapan gas SO3 dari asam sulfat. Pada tahap ini,
larutan menjadi sangat panas sehingga terjadi penghancuran fragmen-fragmen
organik yang tersisa. Bila gas putih telah berhenti, dilakukan penambahan sedikit
asam nitrat untuk menjaga suasana oksidasi pada larutan di dalam erlenmeyer.
Pemanasan larutan di atas hot plate dilanjutkan sampai warna larutan menjadi
jernih. Jika warna larutan berubah menjadi hitam atau coklat yang menandakan
masih terdapat molekul organik pada sampel maka harus ditambahkan asam nitrat
kembali. Proses ini diulangi sampai larutan jernih dalam beberapa jam dan
penambahan asam nitrat tidak menimbulkan reaksi secara kasat mata pada sampel.
Pengoksidasi utama dari penelitian ini adalah HNO3 pekat, digunakan
HNO3 karena sifat logam (Pb) larut dalam HNO3. Asam nitrat pekat ditambahkan
sedikit demi sedikit karena apabila sekaligus sampel akan meluap. Penambahan
asam dalam jumlah banyak biasanya dapat dilakukan setelah sebagian besar
protein dan lemak yang mungikn terdapat dalam sampel teroksidasi. Penambahan
asam sulfat berfungsi sebagai katalis untuk mempercepat reaksi terputusnya
logam (Pb) dari senyawa organik yang ada di dalam sampel kapsul cacing obat.
Reaksi antara asam nitrat dan asam sulfat yang terjadi adalah sebagai berikut :
H2SO4
3Pb + 8HNO3 3Pb2+ + 6NO3- + 2NO + 4H2O (1)
Setelah proses destruksi, dilakukan proses penyaringan larutan sampel
kemudian diencerkan hingga 50 mL dengan asam nitrat 1 M. Larutan disaring
dengan kertas Whatman No.42 untuk menghilangkan pengotor dan substransi
tidak larut air yang tertinggal, agar tidak menyumbat instrumen pada proses
pengukuran.
Proses destruksi pada penelitian ini dilakukan selama ± 28 jam. Lamanya
proses destruksi bergantung pada jumlah molekul organik yang akan dioksidasi.
Penggunaan asam perklorat dapat mempercepat proses destruksi namun dapat
B. Optimasi Spektrofotometri Serapan Atom
Prinsip spektroskopi serapan atom adalah terjadinya penyerapan sumber
radiasi berupa sinar UV (200 – 400 nm) atau sinar tampak/visibel (400 – 800 nm)
di luar nyala, oleh atom-atom netral dalam keadaan gas yang berada dalam nyala.
Untuk menghasilkan atom-atom netral dilakukan proses atomisasi yaitu proses
penguraian atau pengubahan suatu molekul menjadi atom-atom netral dalam
keadaan gas, dimana diperlukan panas yang sesuai yang dihasilkan dari nyala api.
Pada proses ini bila suhu terlalu tinggi kemungkinan akan terjadi ionisasi, karena
itu perlu dilakukan optimasi lebih dahulu.
Gambar 3. Atomisasi Pada SSA (Beaty and Kerber, 1993)
Optimasi dilakukan bertujuan untuk memperoleh populasi atom pada
keadaan dasar yang paling banyak dalam nyala api yang dilewati oleh radiasi.
radiasi yang diserap makin banyak pula. Pada kondisi yang optimum akan
diperoleh serapan yang maksimum.
Gambar 4. Proses Eksitasi (Beaty and Kerber, 1993)
Parameter kondisi optimum spektroskopi serapan atom yang diperoleh dari
Fakultas MIPA UGM meliputi resonance lines, lebar celah monokromator, kuat
arus lampu katoda (Hollow Cathode Lamp), laju alir udara, laju alir asetilen dan
tinggi burner. Kondisi optimum yang digunakan dalam penelitian ini adalah
sebagai berikut :
Tabel V. Kondisi Optimum Sistem SSA
Parameter Kondisi Optimum
Resonance Lines 283,3 nm
Lebar Celah Monokromator 0,7 mm
Kuat Arus Lampu Katoda 10 mA
Laju Alir Udara 2 L/menit
Laju Alir Asetilen 3 L/menit
Tinggi Burner 1,2 cm
Resonance lines yang dipilih adalah 283,3 nm karena panjang gelombang
ini merupakan panjang gelombang paling kuat menyerap garis untuk transisi
elektronik dari tingkat dasar ke tingkat eksitasi. Apabila atom pada tingkat energi
dasar diberi energi yang sesuai maka energi tersebut akan diserap dan atom-atom
tersebut akan tereksitasi ke tingkat energi yang lebih tinggi. Pada keadaan
dengan melepas sejumlah energi dalam bentuk sinar. Karena itu setiap garis
mempunyai energi yang spesifik.
Gambar 5. Resonance Lines Pb (Beaty and Kerber, 1993)
Lebar celah yang digunakan pada penelitian ini adalah 0,7 mm. Lebar
celah dapat mengontrol gangguan spektra tertentu, misalnya garis-garis yang
terabsorpsi dari gas pengisi lampu katoda cekung, garis-garis yang tidak
terabsorpsi dari logam katoda, dan pita-pita molekul dalam nyala. Pengaturan
sinar yang masuk mengurangi gangguan ini, tetapi tidak seluruhnya efektif.
Lebar celah monokromator harus dipilih untuk mengoptimasi signal to
noise ratio. Lebar celah dalam spektrofotometri serapan atom harus kecil yang
diperlukan untuk mengisolasi garis spektra yang digunakan (garis resonansi).
Lebar celah yang sangat sempit diperlukan hanya bila spektra emisi sumber
radiasi adalah sangat kompleks.
Kuat arus lampu katoda pada kondisi optimum dalam penelitian ini yaitu
10 mA. Lampu katoda terdiri atas tabung kaca tertutup yang mengandung suatu
atau dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia
(neon atau argon) dengan tekanan rendah (10-15 torr) (Watson, 2007).
Bagian katoda yang berbentuk cekung dilapisi logam yang sesuai dengan
logam yang akan dianalisis. Anoda diberi tegangan sehingga bila sejumlah kecil
arus yang besarnya beberapa mA diberikan diantara katoda dan anoda akan
mengakibatkan gas argon yang ada di dalam tabung akan mengalami ionisasi,
akibatnya ion gas argon tersebut akan tertarik ke arah katoda (yang bermuatan
negatif) dengan kecepatan yang sangat tinggi dan terjadi tumbukan yang
mengakibatkan tereksitasinya atom-atom logam yang bersangkutan. Dalam hal ini
berlaku hukum emisi atom yang menyatakan bila atom mempunyai kelebihan
tenaga maka akan melepaskan kembali tenaga yang berupa sinar panjang
gelombang yang karakteristik. Dengan demikian sinar dari lampu katoda cekung
ini mempunyai spektrum yang spesifik sesuai dengan garis resonansinya yaitu
283,3 nm dengan kuat arus 10 mA.
Kuat arus lampu katoda cekung yang dianjurkan tergantung pada unsur
yang akan dianalisis dan bervariasi. Pemakaian kuat arus diusahakan seoptimal
mungkin, karena pemberian kuat arus yang terlalu rendah akan menyebabkan
intensitas lampu menjadi terlalu rendah sehingga energi yang diberikan juga
rendah.
Efisiensi lampu katoda cekung bergantung pada bentuk geometri dari
katodanya dan besarnya tegangan atau arus yang diberikan. Peningkatan
pemberian arus pada lampu katoda, pada umumnya akan meningkatkan
intensitas ini ada batasnya, karena hal sebaliknya mungkin saja terjadi, yaitu
pemberian arus yang terlalu tinggi akan mengakibatkan terjadinya peningkatan
jumlah atom-atom yang tidak tereksitasi dalam awan atom dan menyerap emisi
yang dipancarkan sehingga dapat terjadi apa yang disebut penyerapan dini dan hal
ini dapat mengurangi intensitas.
Tipe nyala untuk Pb yaitu udara : asetilen dengan suhu 2200 oC (Gandjar
dan Rohman, 2007). Laju alir asetilen-udara yang digunakan pada penelitian ini
sebagai bahan pembakar dan oksida untuk logam Pb adalah 3 L/menit dan 2
L/menit. Asetilen-udara berfungsi membawa sampel dalam bentuk larutan agar
masuk ke dalam sistem pengkabutan yang akan mengubah sampel larutan menjadi
aerosol halus (uap) yang siap masuk ke dalam sistem nyala untuk atomisasi.
Beberapa kelebihan gas pembakar dan oksidator asetilen-udara yaitu dapat
memberikan hasil yang maksimal, digunakan untuk berbagai unsur dan memiliki
sensitifitas dan kecermatan yang tinggi. Laju alir gas pembakar dan oksidator
yang dibutuhkan tergantung pada ukuran pembakar (burner dan
komponen-komponen sampel).
Atom-atom dalam nyala tidak merata distribusinya karena di dalam nyala
terdapat beberapa daerah panas. Untuk mengatasi hal ini maka dilakukan optimasi
Ilustrasi nyala pada burner :
Gambar 6. Ilustrasi Nyala Burner (Ulfa, 2010)
Larutan cuplikan masuk ke dalam daerah A dalam bentuk butir-butir
halus tercampur dengan udara-asetilen. Pada daerah B air akan menguap
disebabkan oleh konduksi dan radiasi panas dari daerah C. Dalam daerah C ini
terjadi penguapan dan penguraian menjadi atom. Pada daerah ini pula dimulai
proses serapan dan emisi. Atom yang berubah menjadi oksida dalam daerah C,
akan keluar melalui daerah D, setelah itu dibuang ke kuncup luar. Optimasi tinggi
C. Validasi Instrumen Analisis
Validasi instrumen analisis yang diteliti meliputi linearitas dan limit of
detection (LOD) atau sensitivitas. Kurva baku Fakultas MIPA UGM dibuat
dengan konsentrasi 1 ; 2 ; 4 ; 8 dan 10 ppm. Namun, karena diduga konsentrasi
sampel dibawah konsentrasi kurva baku Fakultas MIPA UGM kemudian dibuat
kurva baku dengan konsentrasi yang lebih rendah yaitu dengan konsentrasi 0,1 ;
0,5 ; 1,5 ; 2,0 ; 2,5 dan 3,0 ppm dalam 10 mL. Hal ini dilakukan untuk mencegah
terjadinya ekstrapolasi. Absorbansi yang diperoleh dari kedua kurva baku
kemudian diplot dengan konsentrasi sehingga dihasilkan persamaan regresi dan
dihitung parameter validasinya, seperti linearitas, kisaran (range) dan limit of
detection (LOD).
1. Linearitas
Linearitas merupakan salah satu parameter validasi yang
menggambarkan kemampuan suatu metode analisis untuk mendapatkan hasil uji
yang proporsional antara jumlah analit dengan respon yang dihasilkan. Linearitas
suatu metode ditunjukkan oleh besarnya koefisien korelasi (r) dari kurva baku.
Koefisien korelasi menggambarkan kedekatan dari suatu data terhadap regresi
yang terbentuk dari populasi data yang ada. Koefisien korelasi diperoleh dengan
membuat persamaan regresi linear y = bx + a, dimana y adalah absorbansi dari
senyawa uji, b adalah slope, x adalah konsentrasi dan a adalah intersep.
Persamaan regresi yang diperoleh dari kurva baku Fakultas Farmasi USD yaitu
kriteria penerimaan untuk koefisien korelasi yaitu ≥ 0,9985, sehingga dalam
penelitian ini parameter linearitas dapat dipenuhi.
Gambar 7. Kurva Baku Pb Fakultas Farmasi USD
2. Kisaran (Range)
Merupakan interval antara level terendah dan level tertinggi dari jumlah
analit dalam sampel yang digunakan dalam suatu metode analisis dan telah
memenuhi linearitas, presisi dan akurasi yang dapat diterima. Level terendah
dalam penelitian ini yaitu sebesar 0,1 ppm dan untuk level tertinggi sebesar 3
ppm. Dalam penelitian ini konsentrasi tersebut telah memenuhi linearitas, presisi
dan akurasi yang baik.
y = 0,0126x + 0,0027
3. Limit of Detection (LOD)
Suatu alat dapat dikatakan cukup sensitif apabila alat tersebut mampu
mendeteksi konsentrasi terkecil dari suatu analit, semakin kecil konsentrasi yang
bisa dideteksi semakin sensitif instrumen tersebut. LOD merupakan jumlah
terkecil analit dalam sampel yang dapat dideteksi dan masih memberikan respon
berbeda signifikan terhadap respon blangko. LOD dapat dihitung secara statistik
melalui garis regresi linear dari kurva kalibrasi. LOD dapat dihitung dengan
menggunakan rumus :
3,3
Sa merupakan standar deviasi dari intersep dan slope (b) merupakan kemiringan,
Sa dan b diperoleh dengan menggunakan Polynomial fit (Lampiran 6.).
Polynomial fit mampu menguji kesesuaian pemodelan hubungan sinyal detektor
dengan konsentrasi.
Dari kurva baku Pb Fakultas Farmasi USD diperoleh persamaan regresi
Y = 0,0126x + 0,0027 dan diperoleh Sa dan b untuk menghitung LOD. Sa sebesar
0,0005 dan b sebesar 0,0126, sehingga diperoleh LOD sebesar 0,1309 µg/mL.
Nilai LOD tersebut merupakan kadar analit terendah yang memberikan respon
berbeda signifikan dari respon blanko. Dari nilai LOD tersebut dapat ditentukan
nilai absorbansi terkecil dari sistem ini, yaitu dengan mensubstitusikan nilai x =
0,1309 µg/mL ke dalam persamaan regresi Y = 0,0126x + 0,0027, sehingga