BAB II
TINJAUAN PUSTAKA
1.1.Limbah Praktikum Kimia Analisis
Menurut Undang-Undang Republik Indonesia Nomor 23 Tahun 1997 tentang Pengelolaan Lingkungan Hidup, limbah adalah sisa suatu usaha dan/atau kegiatan. Limbah cair adalah limbah berupa cairan yang berasal dari hasil buangan dari bahan-bahan yang telah terpakai dari suatu proses produksi industri, domestik (rumah tangga), pertanian serta laboratorium yang tercampur (tersuspensi) dan terlarut didalam air.
a. Analisis Kualitatif
Analisis kualitatif dilakukan untuk mengidentifikasi unsur yang terdapat dalam suatu sampel, yang terdiri dari golongan kation, dan anion.
Analisis golongan kation meliputi :
1. Golongan I, disebut golongan asam klorida (Pb2+, Ag+, Hg2+)
2. Golongan II, disebut golongan hidrogen sulfida (As, Sn, Sb, Cu, Pb2+, Bi2+, Cd2+, Hg2+)
3. Golongan III, disebut golongan amonium sulfida (Al, Cr, Fe, Zn, MN, Co, dan Ni)
4. Golongan IV, disebut golongan amonium karbonat (Ba, Sr, dan Ca) 5. Golongan V, disebut golongan sisa (Mg, K, NH4+)
Analisis golongan anion
Perubahan spesifik dari sampel yang diuji, meliputi perubahan warna/terjadinya gas/bau dari sampel atas penambahan asam sulfat encer atau pekat. Analisis anion dilakukan dengan menambah larutan Na2CO3 jenuh, untuk menghilangkan logam berat. Hal ini menyebabkan logam-logam akan terlarutkan sebagai garam karbonat, sedangkan anion terlarut sebagai garam natrium. Analisis anion meliputi :
o Uji sulfat dengan HCl encer dan BaCl2 : jika terjadi endapan maka mengandung Sulfat (SO42-).
nitrit (NO2-), bromida (Br-), iodida (I-), dan arsenit (AsO32-). Jika warna ungu hilang pada pemanasan maka ada oksalat (COO)22-
o Uji untuk oksidator dengan HCl pekat dan MnCl2 jenuh : jika larutan coklat atau hitam maka ada nitrat (NO3-), klorat (ClO3), nitrit (NO2-), kromat (CrO42-), ferisianida, bromat (BrO3-), iodat, dan permanganat (MnO4-). Jika hasil uji negatif maka hanya sedikit nitrat dan nitrit.
o Uji dengan larutan perak nitrat : untuk menguji adanya tiosulfat (S2O32-), iodida (I-), klorida (Cl-), dan bromida (Br-).
b. Analisis Kuantitatif
Analisis kuantitatif dilakukan untuk penetapan banyaknya suatu zat tertentu (analit) yang ada dalam sampel. Analisis kuantitatif digolongkan dalam dua jenis yaitu :
1. Analisis Titrimetri (Volumetri)
Analisis ini berkaitan dengan pengukuran volume suatu larutan dengan konsentrasi yang diketahui, yang diperlukan untuk bereaksi dengan analit. Berdasarkan reaksi kimianya, titrimetri dikelompokkan dalam empat jenis yaitu :
a. Titrasi Asidi Alkalimetri (Reaksi Asam–Basa)
b. Titrasi Oksidasi-Reduksi (Reaksi Redoks)
Reaksi kimia yang melibatkan oksidasi-reduksi, seperti analisis iod bebas, analisis ion iodida (I-), analisis ion ferro (Fe2+)
c. Titrasi Argentometri (Reaksi Pengendapan)
Pengendapan kation perak dengan anion halogen pada suasana tertentu, seperti analisis ion kalium (K+) dalam KCl, analisis ion bromida (Br-), analisis ion iodida (I-)
d. Titrasi Kompleksometri (Reaksi Pembentukan Kompleks)
Suatu titrasi berdasarkan pembentukan senyawa kompleks antara kation dengan zat pembentuk kompleks, seperti analisis MgSo4, analisis ion kalsium (Ca2+), analisis ion alumunium (Al3+), analisis ion timbal (Pb2+)
2. Analisis Gravimetri
Analisis ini merupakan salah satu metode analisis kuantitatif suatu zat atau komponen yang telah diketahui dengan cara mengukur berat komponen dalam keadaan murni setelah melalui proses pemisahan. Analisis gravimetri dapat dilakukan dengan cara sebagai berikut : a) Penguapan, misalnya untuk menentukan kadar air, yaitu air kristal
atau air yang ada dalam suatu spesies.
c) Pengendapan, menggunakan pereaksi yang akan menghasilkan endapan dengan zat yang dianalisa sehingga mudah dipisahkan dengan cara penyaringan. Contohnya, Ag+ diendapkan sebagai AgCl, atau ion besi (Fe3+) diendapkan sebagai Fe(OH)3, yang setelah dipisahkan, dipijarkan dan ditimbang sebagai Fe2O3. Contoh lain yaitu:
BaCl2 (aq) + K2CrO4 (aq) BaCrO4 (s) + 2 KCl (aq) Contoh senyawa yang dapat diendapkan dan ditimbang dapat dilihat pada Tabel 2.1
Tabel 2.1 Senyawa yang dapat di endapkan dan di timbang pada Analisis Gravimetri
1.2.Koagulasi
ukuran yang sangat kecil, yaitu berkisar antara 10-7 cm sampai dengan 10-5 cm. Sifat partikel selalu dalam keadaan stabil, hal ini disebabkan karena muatan antar partikel sama sehingga terjadi gaya tolak menolak. Karena sifatnya tersebut, maka partikel koloid akan selalu menyebabkan kekeruhan dan sulit untuk dipisahkan dengan cara penyaringan maupun pengendapan. Salah satu cara untuk dapat memperbesar ukuran partikel tersebut adalah dengan menetralkan muatan partikel dengan jalan menambahkan larutan kimia tertentu, sehingga partikel-partikel koloid akan membentuk suatu gumpalan. Cara tersebut dinamakan koagulasi (Buchari,1981).
Senyawa kimia yang dapat digunakan sebagai bahan kogulan biasanya adalah senyawa yang mempunyai molekul berukuran besar dan mempunyai gugus reaktif disepanjang rantainya, misalnya selulosa, protein dan senyawa polimer lainnya (Prayudi & Susanto 2000). Bahan koagulan yang digunakan dalam proses pengendapan limbah cair adalah bahan koagulan utama dan bahan koagulan pendukung. Bahan koagulan utama termasuk tawas, ferosulfat, ferisulfat, feriklorida, dan bahan koagulan pendukung termasuk air kapur, soda abu, dan polyalumunium chlorida (Droste,R.L1975;Kiely,G.,1997).
Faktor-faktor yang mempengaruhi koagulasi
Proses koagulasi untuk pengolahan air dipengaruhi oleh beberapa faktor antara lain:
Nilai pH untuk proses koagulasi beragam, bergantung pada koagulan dan karakteristik air yang dipilih. Sebagai contoh, pH optimum untuk aluminium sulfat 5,5-7,5, untuk garam besi 5,0-8,5, sedangkan pH optimum untuk kitosan adalah pH 5 (Roussy et al., 2005).
b. Suhu
Dengan turunnya suhu, maka viskositas air semakin tinggi sehingga kecepatan flok untuk mengendap semakin turun. Penurunan suhu menyebabkan kecepatan reaksi berkurang, sehingga flok lebih sukar mengendap.
c. Konsentrasi koagulan
Konsentrasi koagulan akan berpengaruh pada banyaknya jumlah bahan kimia (koagulan) yang ditambahkan, sehingga proses pengendapan dari tiap konsentrasi akan bervariasi. Selain itu, hal ini akan berpengaruh terhadap tumbukan antar partikel yang akan membentuk flok-flok (Azamia 2012).
d. Kecepatan dan waktu pengadukan
Pengadukan ini diperlukan agar tumbukan antar partikel untuk netralisasi menjadi sempurna. Dalam proses koagulasi ini, pengadukan dilakukan dengan cepat. Air yang memiliki turbiditas yang rendah memerlukan pengadukan yang lebih banyak dibandingkan dengan air yang memiliki turbiditas yang tinggi.
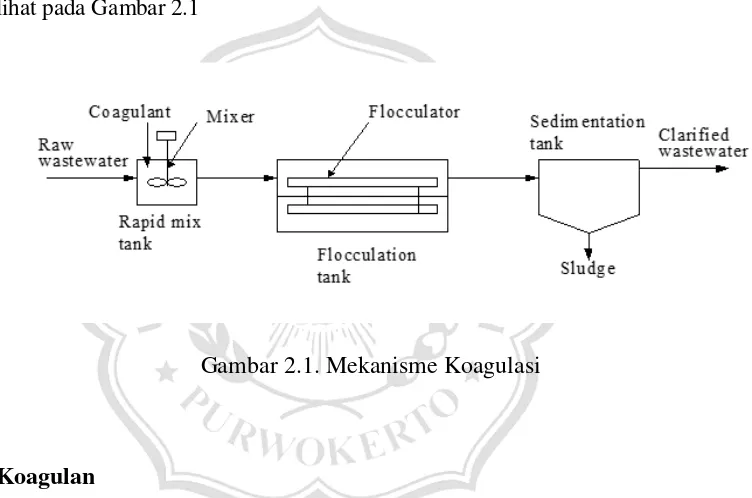
Mekanisme koagulasi ada dua jenis, yaitu sweep coagulation dan adsorption coagulation. Sweep coagulation ialah koagulasi yang dimana
partikel koloid yang tidak terlarut membentuk flok-flok yang ternetralkan oleh koagulan, sedangkan adsorption coagulation ialah koagulasi yang dimana muatan elektris partikel koloid diubah oleh molekul koagulan yang menempel pada permukaan koloid (Lilis.,2006). Mekanisme koagulasi dapat di lihat pada Gambar 2.1
Gambar 2.1. Mekanisme Koagulasi
1.3.Koagulan
Menurut Kawamura (1991), koagulan yang digunakan dapat dibedakan menjadi polimer anorganik dan polimer alami. Koagulan yang umum digunakan adalah koagulan kimia seperti alum sulfat, polyaluminium chloride, ferro sulfat (FeSO4), dan ferri khlorida (FeCl3).
Jenis-jenis Koagulan:
Alumunium sulfat (Al2(SO4)3.14H2O)
Alumunium sulfat biasanya disebut tawas, bahan ini sering dipakai karena efektif untuk menurunkan kadar karbonat. Tawas berbentuk kristal atau bubuk putih, larut dalam air, tidak larut dalam alkohol, tidak mudah terbakar, ekonomis, mudah didapat dan mudah disimpan. Penggunaan tawas memiliki beberapa keuntungan yaitu harga relatif murah dan sudah dikenal luas oleh operator water treatment. Namun tawas juga memiliki kerugian, yaitu umumnya dipasok dalam bentuk padatan, sehingga perlu waktu yang lama untuk proses pelarutan. Mekanisme reaksi yang terjadi adalah sebagai berikut:
Al2(SO4)3→2 Al+3 + 3SO4-2 H2O → H+ + OH -2Al+3 + 6 OH-→ 2 Al (OH)3
PAC (Poly Alumunium Chlorida)
Polimer alumunium merupakan jenis baru sebagai hasil riset dan pengembangan teknologi air. Sebagai dasarnya adalah alumunium yang berhubungan dengan unsur lain membentuk unit berulang dalam suatu ikatan rantai molekul yang cukup panjang, pada PAC unit berulangnya adalah Al-OH. Rumus empirisnya adalah Aln(OH)mCl3n-m, dimana : n = 2 2,7 <> 0 Dengan demikian PAC menggabungkan netralisasi dan kemampuan menjembatani partikel-partikel koloid sehingga koagulasi berlangsung efisien. Namun terdapat kendala dalam menggunakan PAC sebagai koagulan, yaitu perlu pengarahan dalam pemakaiannya karena bersifat higroskopis.
Karbon aktif
Aktivasi karbon bertujuan untuk memperbesar luas permukaan arang dengan membuka pori-pori yang tertutup sehingga memperbesar kapasitas adsorbsi. Pori-pori arang biasanya diisi oleh hidrokarbon dan zat-zat organik lainnya, yang terdiri dari persenyawaan kimia. Aktivasi yang ditambahkan akan meresap dalam arang dan membuka permukaan yang mula-mula tertutup oleh komponen kimia, sehingga luas permukaan yang aktif bertambah besar.
Jumlah karbon aktif yang digunakan untuk menyerap warna berpengaruh terhadap jumlah warna yang diserap.
Activated silica
Activated silica merupakan sodium silikat yang telah direaksikan dengan asam sulfat, alumunium sulfat, carbon dioxide, atau klorida. Sebagai koagulan, activated silica memberikan keuntungan antara lain meningkatkan laju reaksi kimia, menurunkan dosis koagulan, memperluas jangkauan pH optimum dan mempercepat serta memperkeras flok yang terbentuk. Umumnya digunakan bersama dengan koagulan alumunium dengan dosis 7 – 11% dari dosis alum.
Bentonic clay
Bentonic clay digunakan pada pengolahan air yang mengandung zat warna tinggi, kekeruhan rendah dan mineral yang rendah.(Romel.2013)
Bahan-Bahan Pembantu Koagulan
a. Penambahan alkalinitas, biasanya menggunakan kapur dan soda abu. b. Polielektrolit, untuk memperoleh koagulasi yang optimum seperti anionik,
kationik, dan poliamfolit.
1.4.Kitosan
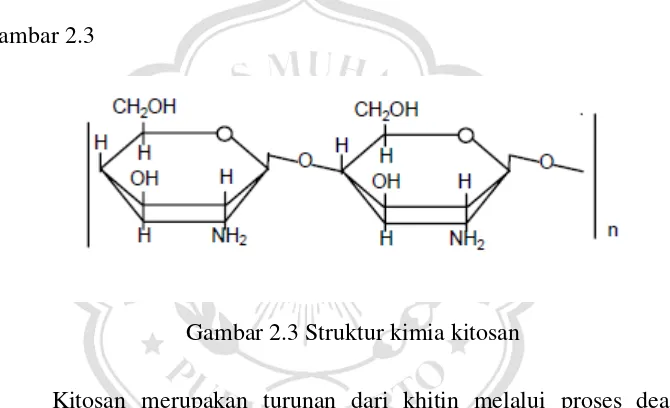
Kitosan (C6H11NO4) merupakan polimer dengan nama kimia 2-amino-2-deoksi-D-glukosa, mengandung gugus amino bebas dalam rantai karbonnya dan bermuatan positif. Gugus amina bebas inilah yang banyak memberikan kegunaan bagi kitosan. Kitosan berbentuk padatan amorf, merupakan salah satu dari sedikit polimer alami yang berbentuk polielektrolit kationik dalam larutan asam organik (Hirano.,1986). Struktur kimia kitosan disajikan pada Gambar 2.3
Gambar 2.3 Struktur kimia kitosan
Beberapa kegunaan kitosan antara lain sebagai berikut : 1. Membran penukar ion
2. Bahan pemurni air
3. Bahan baku benang untuk operasi plastik/bedah 4. Bahan powder untuk sarung tangan pembedahan 5. Koagulan dan flokulan
Penggunaan kitosan tergantung dari kualitasnya. Sebagai contoh kitosan dengan kualitas rendah dapat digunakan pada pemrosesan limbah cair industri, sedang kitosan dengan kemurnian tinggi dibutuhkan dalam bidang kesehatan, seperti bahan obat-obatan (Bastaman,1989). Sebagai bahan pemrosesan limbah cair, kitosan mampu menurunkan kadar COD, BOD, padatan tersuspensi, warna, kekeruhan dan mampu mengikat logam berat seperti Fe, Cu, Cd, Hg, Pb, Cr, Ni, Mn, Co, Zn dan lain lain (Bough,1976). Kitosan mempunyai gugus amino bebas sebagai polikationik, pengkhelat dan pembentuk dispersi dalam larutan asam asetat. Gugus amino bebas inilah yang memberikan banyak kegunaan pada kitosan (Knorr,1982).
Tabel 2.2 Standar mutu kitosan
Parameter Nilai
Ukuran partikel Dari bubuk smpai serpihan
Kadar air < 10%
Kadar abu < 2 %
Warna larutan Jernih
Derajat deasetilasi > 70 Viskositas:
- Rendah < 200 (cps)
- Medium 200 s/d 799 (cps)
- Tinggi 800 s/d 2000 (cps)
- Ekstra tinggi >2000 (cps) (Sumber : Protan Laboratories Inc)
Kelarutan kitosan dalam asam asetat dipengaruhi oleh suhu dan lamanya perendaman dalam NaOH. Asam asetat tergolong asam lemah golongan asam karboksilat yang mengandung gugus karboksil (-COOH). Gugus karboksil mengandung sebuah gugus karbonil dan gugus hidroksil. Titik didihnya mencapai 118˚C dan baunya sangat tajam (Fessenden &
dan reaksi kelarutan kitosan dengan asam asetat dapat di lihat pada Gambar 2.4 dan Gambar 2.5
Gambar 2.4 Reaksi pembentukan kitosan dari khitin.
Gambar 2.5 Reaksi kelarutan kitosan dengan asam asetat. Spesifikasi kitosan sebagai koagulan :
a. Kitosan merupakan senyawa polimer organik. b. Kitosan berbentuk padatan amorf berwarna kuning. c. Kitosan larut dalam larutan asam asetat.
d. Kitosan efektif pada pH 5.
f. Jika penambahan kitosan berlebihan, akan menambah nilai kekeruhan dan menurunkan nilai pH secara drastis namun tidak beracun, dan ramah lingkungan.
g. Kitosan mampu mengikat logam berat seperti Fe, Cu, Cd, Hg, Pb, Cr, Ni, Mn, Co, dan Zn.
1.5.Jar Test
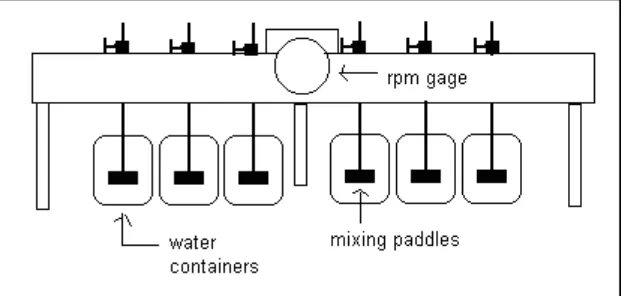
Jar test atau uji jar merupakan metode standar yang digunakan untuk
menguji proses koagulasi. Data yang didapat dengan melakukan jar test antara lain dosis optimum penambahan koagulan, lama pengendapan serta volume endapan yang terbentuk. Jar test yang dilakukan adalah untuk membandingkan kinerja koagulan yang digunakan untuk mendapatkan padatan yang tersuspensi. Metode ini dapat dilakukan untuk menentukan pH optimum, variasi dosis koagulan, alternatif kecepatan pengadukan atau menguji jenis koagulan yang berbeda (Hardina.,2012).
Pelaksanaan jar test ini dilakukan agar diketahui titik kekeruhan akhir pada penambahan kedua koagulan yang sesuai dengan baku mutu air bersih yang ditetapkan oleh Kep Menkes RI No.416/Menkes/Per/XI/1990. Konsentrasi koagulan yang optimum dapat ditentukan berdasarkan hasil jar test, yaitu konsentrasi yang memberikan kekeruhan akhir tepat dibawah 5
Gambar 2.6 Jar test
Faktor-faktor yang mempengaruhi percobaan dengan Jar-Test, adalah : 1. Bahan kimia yang dipakai untuk menurunkan kadar logam berat 2. Penambahan dosis Presipitan
3. pH