J u r n a l S a i n s F a r m a s i & K l i n i s
(p- ISSN: 2407-7062 | e-ISSN: 2442-5435)
diterbitkan oleh Ikatan Apoteker Indonesia - Sumatera Barat homepage: http://jsfkonline.org
ABSTRACT: Some herbal formulation containing α-mangostin as a marker compound in the pericarp
of the mangosteen (Garcinia mangostana L.) are marketed now in Indonesia. The determination of
the component of preparation both qualitatively and quantitatively is essential to ensure quality of the product. This research is aimed to develop a TLC (Thin Layer Chromatography)-densitometry method to analyze α-mangostin in the herbal drinks of mangosteen rind. The analysis was performed with TLC Scanner using Camag TLC Scanner 4 with Wincats software. Silica gel 60 F254 (Merck) plates (20x20 cm: 200 μm thickness) were used as stationary phase and mixture of chloroform and ethyl acetate (9:1,v/v) as a mobile phase. The developed chromatogram was scanned at 316 nm, the wavelength of maximum absorption for α-mangostin. At this condition, the Rf value of α-mangostin is 0.48. Regression analysis of the calibration data showed an excellent linear relationship between peak-area vs drug concentration. Linearity was found to be in the range of 50-400 µg/mL. The suitability of developed TLC densitometry method for estimation of α-mangostin was established by validating it as per the ICH guidelines. The limits of detection (LOD) and quantification (LOQ) for α-mangostin were found to be 54.38 μg/mL and 181.28 μg/mL. The developed method was found to be linear (r=0,99415), precise (RSD <1.28 % and < 2.39 % for intra-day and inter-day precision) and accurate (mean recovery of 90.04%). Results of the samples analysis showed that sample A does not contain α-mangostin, whereas sample B and C contain α-mangostin. The average concentrations obtained for samples B and C were 0.040% w/v and 0.118% w/v, respectively. The developed method has been successfully applied for the determination of α-mangostin in the herbal drinks of mangosteen rind.
ABSTRAK: Beberapa formulasi herbal yang mengandung α-mangostin sebagai senyawa penanda pada
kulit buah manggis (Garcinia mangostana L.) sekarang dipasarkan di Indonesia. Penentuan kadar
senyawa penanda secara kualitatif dan kuantitatif penting untuk memastikan kualitas produk. Penelitian ini bertujuan untuk mengembangkan metode Kromatografi Lapis Tipis (KLT) densitometri untuk menganalisis α-mangostin pada minuman herbal kulit buah manggis. Analisis dilakukan dengan TLC Scanner menggunakan Camag TLC Scanner 4 dengan software Wincats. Pelat silika gel 60 F254 (Merck) (ketebalan 20x20 cm: 200 μm) digunakan sebagai fase diam dan kloroform-etil asetat (9:1,v/v) sebagai fase gerak. Kromatogram yang dikembangkan dipindai pada 316 nm yaitu panjang gelombang serapan maksimum untuk α-mangostin. Pada kondisi ini, nilai Rf adalah 0,48. Analisis regresi data kalibrasi menunjukkan hubungan linier antara luas area di bawah puncak vs konsentrasi. Linearitas ditemukan berada pada kisaran 50-400 μg/mL. Kesesuaian metode KLT densitometri yang dikembangkan untuk estimasi α-mangostin ditetapkan dengan memvalidasinya sesuai dengan pedoman ICH. Batas deteksi (LOD) dan kuantifikasi (LOQ) untuk α-mangostin ditemukan 54,38 μg/mL dan 181,28 μg/mL. Metode yang dikembangkan ditemukan linier (r = 0,99415), tepat (RSD <1,28% dan <2,39% untuk presisi intra hari dan antar hari), dan akurat (rata-rata perolehan kembali 90,04%). Hasil analisis sampel menunjukkan bahwa sampel B dan C mengandung α-mangostin, sedangkan sampel A tidak. Rata-rata kadar yang diperoleh untuk sampel B dan C masing-masing adalah 0,040% b/v dan 0,188% b/v. Metode yang dikembangkan telah berhasil diterapkan untuk penentuan α-mangostin dalam minuman herbal kulit manggis.
Keywords:
α-mangostin; Garcinia mangostana L; herbal drinks; tlc densitometry.
Kata Kunci:
α-mangostin; Garcinia mangostana L; minuman herbal; KLT densitometri.
*Corresponding Author: Regina Andayani
Bagian Kimia Farmasi, Fakultas Farmasi Universitas Andalas,
Article History: Received: 15 Nov 2017 Accepted: 20 Nov 2017
Analisis α-Mangostin dalam Minuman Herbal
Kulit Buah Manggis (
Garcinia mangostana
L.) dengan
Metode Kromatografi Lapis Tipis-Densitometri
#(Analysis of α-mangostin in the herbal drinks of mangosteen rind (Garcinia mangostana L.) by thin layer chromatography-densitometric method)
Regina Andayani
*, & Friardi Ismed
Fakultas Farmasi Universitas Andalas#Makalah ini sudah dipresentasikan di dalam kegiatan Indonesian Conference on Contemporary Science & Clinical Pharmacy
(ICCSCP 2017) yang diselenggarakan di Padang pada 10-11 November 2017
Access this article
PENDAHULUAN
Saat ini pemanfaatan ekstrak tanaman sebagai minuman yang terbuat dari rempah - rempah dan tanaman obat mengalami peningkatan. Penyajiannya berupa minuman kesehatan, jamu, minuman ringan, jus dan sirup. Kulit buah manggis adalah salah satunya. Kulit buah manggis digunakan sebagai minuman kesehatan yang telah dijual di toko obat dan swalayan sebagai minuman herbal
[1]. Oleh karena itu, supaya produk-produk herbal tersebut dapat terjaga kualitas dan khasiatnya maka diperlukan suatu standardisasi baik pada bahan baku ataupun dalam bentuk sediaan ekstrak atau sediaan galenik. sehingga memenuhi persyaratan mutu, sebagaimana tercantum dalam Farmakope Herbal Indonesia [2,3].
Kulit buah manggis mengandung senyawa
α-mangostin yang merupakan derivat xanton, yang pertama
kali diisolasi oleh Schmid dari ekstrak kulit buah manggis
pada tahun 1855. Senyawa ini mempunyai berbagai aktifitas farmakologis seperti antioksidan, antitumor, antiinflamasi,
antialergi, antibakteri dan antijamur [1,4,5,6,7].
Pada penelitian sebelumnya, telah dilaporkan
metode analisis kuantitatif senyawa α-mangostin dalam
ekstrak kulit buah manggis dengan menggunakan berbagai metode analisis seperti spektrofotometri UV
[9,10], KLT (Kromatografi Lapis Tipis) densitometri [11,12], dan KCKT (Kromatografi Cair Kinerja Tinggi) [13,14,15]. Namun belum ada publikasi yang melaporkan pengembangan metode analisis alfa mangostin dalam dalam minuman herbal.
Penelitian ini bertujuan untuk mengidentifikasi dan menentukan kadar senyawa α-mangostin sebagai senyawa
penanda atau identitas yang diduga bertanggungjawab terhadap efek farmakologi dalam minuman herbal yang mengandung kulit buah manggis dengan metode KLT densitometri.
METODE PENELITIAN
Bahan
Standar α-mangostin yang diperoleh dari Wuxi
Gorunjie Natural-Pharma Co., Ltd (Jiangsu, China:
kemurnian 90,3 %). Pelarut kimia yang digunakan adalah metanol, kloroform dan etil asetat (Merck). Sampel
yang digunakan dipilih berdasarkan merek yang banyak dikonsumsi oleh masyarakat yang dibeli di beberapa apotek di kota Padang, yaitu minuman herbal kulit buah manggis merek A, B dan C. Alat-alat yang digunakan antara lain: Camag UV lamps 254 dan 366 nm, Camag TLC Scanner 4
dengan software Wincats, plat silika gel 60 F254 (Merck).
Persiapan Larutan Induk α-Mangostin 1000 µg/mL
Ditimbang seksama lebih kurang 10 mg standar
α-mangostin murni, dimasukkan ke dalam labu ukur 10 mL
lalu ditambahkan metanol sampai tanda batas. Kemudian dilakukan pengenceran sehingga diperoleh konsentrasi
α-mangostin standar 50, 100, 150, 300 dan 400 µg/mL.
Penyiapan Ekstrak Kulit Buah Manggis dari Sampel Sirup
Sampel A, B dan C, masing-masing dipipet 25 mL dan dimasukkan ke dalam corong pisah 100 mL. Ekstraksi dilakukan tiga kali berturut-turut tiap kalinya dengan 30 mL etil asetat. Kumpulan ekstrak diuapkan dengan rotary evaporator. Ekstrak kental yang didapat dimasukkan ke dalam labu ukur 10 mL dan ditambahkan metanol hingga
10 mL (sampai tanda batas). Selanjutnya dianalisis dengan
menggunakan metode KLT densitometri.
Pemeriksaan Organoleptis
Untuk mengetahui karakteristik sediaan cair kulit
manggis (parameter spesifik), maka identifikasi dilakukan
dengan cara pengamatan secara visual meliputi bentuk, bau, rasa dan warna dari sediaan sampel.
Penyiapan Fase Gerak
Fase gerak yang digunakan sesuai dengan Farmakope Herbal Indonesia tentang ekstrak kulit buah manggis yaitu kloroform dan etil asetat. Dimana perbandingan kloroforom dan etil asetat masing-masing 9 : 1 [16].
Kondisi Analisis
Analisis dilakukan dengan menotolkan standar
α-mangostin dan ketiga sampel dengan menggunakan pipet kapiler berukuran 2 µL pada plat KLT yang berukuran 10 x 5 cm dengan jarak tempuh eluen sejauh 8 cm dan jarak
totolan standar dengan sampel adalah 1 cm menggunakan alat CAMAG® Nanomat 4. Kemudian plat ini dimasukkan
ke chamber yang telah dijenuhkan terlebih dahulu dengan
fase gerak kloroform dan etil asetat (9:1). Chamber ditutup
dan dibiarkan fase gerak mencapai batas pengembangan.
Chamber dibuka dan plat KLT diambil untuk dikeringkan. Setelah dilihat di bawah lampu UV, ditentukan nilai Rf yang diperoleh dan dipindai dengan Camag TLC Scanner 4 pada panjang gelombang serapan maksimum. Nilai Rf yang baik adalah 0,2 - 0,8 [17,18].
Validasi Metode Analisis
Liniearitas dilakukan dengan menganalisis puncak kromatogram bercak dari beberapa tingkat konsentrasi
dari larutan standar (50, 100, 150, 300, dan 400 ppm) kemudian luas puncak (AUC) yang didapat diplot terhadap
konsentrasi standar menggunakan persamaan garis regresi
linier (y = a + bx). Linieritas ditentukan oleh harga r (koefisien kolerasi). Persamaan regresi ini dapat digunakan jika faktor korelasinya (r ) mendekati 1 [19,20,21].
Sensitifitas ditentukan dari perhitungan nilai Batas Deteksi/LOD dan Batas Kuantitasi/LOQ. Nilai LOD dan LOQ dapat ditentukan dari persamaan regresi dan
simpangan baku residual [19,20,21].
Presisi ditentukan dengan cara: larutan standar dengan berbagai tingkat konsentrasi (150 ppm, 300 ppm,
400 ppm) sebanyak tiga kali pengulangan ditotolkan pada
plat silika gel F254 pada hari yang sama untuk variabel intraday, kemudian tiga hari berturut-turut untuk variabel
interday. % RSD = (Standar Deviasi : Kadar rata-rata) x
100%. % RSD dinyatakan memenuhi validasi metode jika % RSD < 5% [19,20,21].
Akurasi metode ditentukan oleh pengujian recovery
(perolehan kembali) menggunakan metode baku standar (α-mangostin murni). Sampel yang telah diketahui kadarnya yaitu sampel C1 (278,8187 µg/mL) dipipet sebanyak 1 mL ditambah larutan standar α-mangostin (100 µg/mL) sebanyak 1 mL dicampur dalam vial kemudian ditotolkan sebanyak 2 µL dengan tiga kali pengulangan
pada plat. Nilai perolehan kembali dihitung dengan cara membandingkan konsentrasi terukur dengan konsentrasi sebenarnya. Perolehan kembali memenuhi syarat validasi metode jika % perolehan kembalinya dengan nilai rentang 85% - 115% [19,20,21].
Analisis kualitatif dan kuantitatif
Pelat KLT disiapkan dengan garis penotolan 1 cm dari tepi bawah dan 1 cm dari tepi atas dengan jarak
pengembangan 8 cm. Larutan standar α-mangostin dan larutan uji ditotolkan masing-masing 2 µL pada lempeng
KLT yang sama, dielusi dan dianalisis dengan metode yang
disusulkan. Sampel dinyatakan mengandung α-mangostin
jika bercak mempunyai nilai Rf dan densitogram yang
sama dengan α-mangostin standard. Luas area di bawah
puncak dimasukkan ke dalam persamaan regresi yang didapat dan dilakukan perhitungan kadar sampel.
HASIL DAN DISKUSI
Analisis dilakukan untuk memastikan bahwa produk minuman herbal kulit buah manggis mengandung bahan-bahan sesuai yang dicantumkan dalam etiketnya. Kalau produk jus manggis semestinya harus mengandung
senyawa penandanya yaitu α-mangostin. Senyawa penanda
merupakan salah satu parameter standar mutu ekstrak tumbuhan obat [3].
Pada penelitian ini dilakukan dengan menggunakan metode KLT densitometri karena cukup luas digunakan dengan hasil yang cukup memuaskan. Metode ini sederhana, mudah dilakukan, cukup teliti dan sensitif, serta dapat diterapkan untuk ekstrak kasar kulit buah manggis
yang mengandung α-mangostin [5]. Batas deteksi sistem
ini lebih rendah, kelinieran respon dan selektifitasnya lebih
tinggi [17,18].
Gambar 2. Spektrodensitogram senyawa α-mangostin
pada alat TLC Scanner
Gambar 3. Hasil KLT sampel dengan fase gerak
Kloro-form : Etil asetat (9:1) (S=standar α-mangostin; A, B, dan
Pemilihan pelarut etil asetat untuk proses ekstraksi cair-cair ini dikarenakan sifatnya semi polar sehingga dapat
menarik semua senyawa α-mangostin yang bersifat semi
polar di dalam larutan sampel [13].
Gambar 2 menunjukkan spektrodensitogram senyawa
α-mangostin standard pada plat KLT yang telah dielusi dengan fase gerak kloroform-etil asetat (9:1, v/v). Bercak
dipindai dengan TLC Scanner menghasilkan Rf 0,48 dan
Tabel 1. Parameter validasi untuk penentuan kadar
α-mangostin
Pa ra m e te r Hasil
Rentang linieritas (µg/mL) 50-400
Persamaan regresi y = 1326,1658 + 19,7647x Koefisien korelasi r = 0,99415
Batas deteksi (µg/mL) 54,38
Batas kuantisasi (µg/mL) 181,28
Tabel 2. Presisi dan akurasi intraday
I nt ra d ay ( n = 3 )
CA (µg/mL) CF (rata ± SD) KV (%) Akurasi (%)
150 169,50 ± 2,16 1,28 113,00 300 304,68 ± 2,20 0,72 101,56
400 389,16 ± 1,77 0,45 97,29
400
350
300
250
200
150
100
50
0
300
250
200
150
100
50
0
300
250
200
150
100
50
0 400
350
300
250
200
150
100
50
0 -0,20 -0,10 0,00 0,10 0,20 0,30
-0,20 -0,10 0,00 0,10 0,20 0,30
-0,40 -0,30 -0,20 -0,10 0,00 0,10 0,20 0,30 -0,40 -0,30 -0,20 -0,10 0,00 0,10 0,20 0,30 -0,20 -0,10 0,00 0,10 0,20 0,30
-0,20 -0,10 0,00 0,10 0,20 0,30
400
350
300
250
200
150
100
50
0
400
350
300
250
200
150
100
50
0
A
B
C
panjang gelombang serapan maksimum 316 nm.
Hasil identifikasi senyawa α-mangostin dalam sampel
uji menggunakan plat KLT silika gel F254, dengan fase
gerak kloroform : etil asetat (9:1) menunjukkan bahwa
sampel minuman herbal merek A tidak memiliki bercak
dengan nilai Rf yang sama dengan senyawa α-mangostin
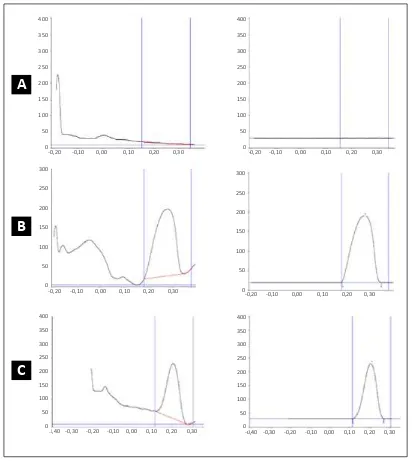
standar,seperti yang diperlihatkan oleh Gambar 3. Hal ini juga dibuktikan dengan hasil densitogram sampel A, seperti yang diperlihatkan oleh Gambar 4A, dimana hanya terbentuk garis datar dan tidak terdapat puncak pada densitogram 2 dimensi.
Hal ini dapat disebabkan produsen tidak mengikuti prosedur CPOTB (Cara Pembuatan Obat Tradisional yang
Baik) selama proses produksi sampel sehingga senyawa α-mangostin (senyawa xanton dengan gugus polifenol)
mengalami reaksi degradasi termal seperti reaksi oksidasi. Reaksi oksidasi dapat terjadi dengan suhu pemanasan yang terlalu tinggi atau waktu pemanasannya terlalu lama. Hal ini membantu terjadinya degradasi enzimatik oleh enzim
polifenol oksidase sehingga kandungan α-mangostin
hilang [22,23]. Dugaan lainnya, sampel minuman herbal kulit buah manggis merek A tidak mengandung ekstrak
Tabel 3. Presisi dan akurasi interday
I nte rd ay ( n = 3 )
CA (µg/mL) CF (rata ± SD) KV (%) Akurasi (%) 150 165,29 ± 2,16 2,39 110,19 300 302,94 ± 2,20 1,74 99, 45
400 389,22 ± 1,77 1,00 97,27
Tabel 4. Data perhitungan % recovery (akurasi)
Standar
ditambahkan AUC (Ct) Rata-rata AUC(Ct) Kadar Ct (µg/mL) Kadar Co (µg/mL) Recovery % Recovery
100 µg/mL
8518,9
8616,5 368,8563 278,8187 0,9004 90,04 8996,3
8334,4
AUC = Luas area; Ct = Konsentrasi sampel tambah standar; Co = Konsentrasi sampel awal
Tabel 5. Data kadar sampel B
Sampel Luas Puncak rata-rata
Konsentrasi
(µg/mL) % Kadar
% Kadar rata-rata B 1 6903,4 282,1916 0,045
0,040 B 2 5941,5 233,5140 0,037
B 3 6155,9 244,3633 0,039
Tabel 6. Data kadar sampel C
Sampel Luas Puncak rata-rata
Konsentrasi
(µg/mL) % Kadar
% Kadar rata-rata C 1 6836,933 278,8187 0,111
0,118 C 2 7417,233 298,6857 0,123
C 3 7229,600 308,1791 0,119
kulit buah manggis.
Sampel B dan sampel C memiliki bercak dengan Rf
yang sama dengan senyawa α-mangostin standar yaitu
0,48, dimana menurut literatur Rf yang baik adalah antara 0,2-0,8 [17]. Gambar 4B dan Gambar 4C menunjukkan densitogram ekstrak sampel B dan C dengan fase gerak
kloroform : etil asetat (9:1).
Secara kualitatif, dinyatakan bahwa sampel B dan
C mengandung senyawa α-mangostin. Oleh karena itu
proses analisis dilanjutkan ke tahap selanjutnya yaitu analisis kuantitatif.
Uji liniearitas dilakukan dengan menganalisis beberapa tingkat konsentrasi dari larutan standar (50 ppm, 100 ppm,
150 ppm, 300 ppm dan 400 ppm). Persamaan regresi linier
yang diperoleh dari kurva kalibrasi adalah y = 1326,1658
+ 19,7647x dengan koefisien korelasi kurva standar r = 0,99415. Nilai koefisien korelasi (r), mendekati 1, artinya
konsentrasi berbanding lurus dengan luas puncak, seperti yang diperlihatkan oleh Tabel 1.
Nilai LOD dan LOQ dari α-mangostin yang
didapat adalah 54,38 µg/mL dan 181,28 µg/mL. Tabel 1
menunjukkan hasil parameter validasi untuk penentuan
kadar α-mangostin, yang meliputi koefisien korelasi, batas
deteksi dan batas kuantisasi.
Presisi intraday dan interday telah dilakukan pada tiga
konsentrasi standar α-mangostin yaitu 150, 300 dan 400
ppm, dengan nilai %RSD untuk presisi intraday
berturut-turut 1,28 % ;0,72 % dan 0,45 %. Sedangkan presisi inter-day berturut-turut 2,39 % ; 1,74 % dan 1,00 %. Nilai rata-rata % RSD yang diperoleh ≤ 2 % sehingga memenuhi
REFERENSI
[1] Soetikno, J.S., Handayani, R., & Rahayu, R.D. (2016). Assay for antimicrobial activity of mangosteen rind extracts. Journal of Innovations in Pharmaceuticals and Biological Sciences, 3(1), 54–60. [2] Kemenkes, R.I. (2010), Suplemen I Farmakope Herbal Indonesia,
Jakarta: Kementerian Kesehatan Republik Indonesia.
[3] Parameter standar umum ekstrak tumbuhan obat. (2000). Jakarta: Departemen Kesehatan RI
[4] Liu, S. H., Lee, L. T., Hu, N. Y., Huange, K. K., Shih, Y. C., Munekazu, I., Li, J. M., Chou, T. Y., Wang, W. H., and Chen, T. S. (2012). Effects of alpha-mangostin on the expression of anti-inflammatory genes in U937 cells, Chinese Medicine, 7(19), 1–11.
[5] Jung, A.H., Su, B.N., Keller, W.J., Mehta, R.G., dan Kinghorn, A.D. (2006). Antioxidant xanthones from the pericarp of Garcinia mangostana (Mangosteen), Journal of Agricultural and Food Chemistry, 54(6), 2077–2082.
[6] Pasaribu, F., Sitorus, P., & Bahri, S. (2012). Uji ekstrak etanol kulit buah manggis terhadap penurunan kadar glukosa darah, Journal of Pharmaceutics and Pharmacology, 1(1), 1–8.
[7] Akao, Y., Nakagawa,Y., Iinuma, M., & Nozawa, Y. (2008). Anti cancer effects of xanthones from pericarps of mangosteen. International Journal of Molecular Sciences, 9, 355–370.
[8] National Center for Biotechnology Information. (2017). Alpha Mangostin. Retrieved August 12, 2017, from https://pubchem.ncbi. nlm.nih.gov/compound/5281650#section=Top [accessed [9] Pothitirat, W., & Gritsanapan.W. (2008). Quantitave Analysis of Total
Mangostins in Garcinia mangostana fruit rind. Journal of Health Research, 22(4), 161–166.
[10] Aisha A. F., Abu-Salah, K. M., Ismail, Z., & Majid, A. M. S. A. (2013). Determination of total xanthones in Garcinia mangostana fruit rind extracts by ultraviolet (UV) spectrophotometry. Journal of Medicinal Plants Research, 7(1), 29–35.
[11] Misra, H., Dwivedi, B. K., Mehta, D., Mehta, B. K., & Jain, D. C. (2009). Development and Validation of High Performance Thin-Layer Chromatographic Method for Determination of [alpha]-Mangostin in Fruit Pericarp of Mangosteen Plant (Garcinia mangostana L.) using Ultraviolet-Visible Detection. Records of Natural Products, 3(4), 178– 186.
[12] Agustina, R., Andayani, R., Dachriyanus. (2014). Development and validation of thin layer chromatographic method for determination of α-mangostin in young pericarp, ripe pericarp, and bark extract of Garcinia mangostana L. using TLC Densitometry. International Journal of Research in Pharmacutical Sciences, 5(4), 294–298. [13] Andayani, R., Wahyuni F. S., Wirasti Y., & Dachriyanus. (2015).
Development and validation of RP-HPLC method for quantitative estimation of α-mangostin in the rind extract and fractions of Garcinia mangostana L. and their citotoxic activity on T47D breast cancer cell line. International Journal of Pharmacy and Pharmaceutical Sciences, 7(2), 174–178.
[14] Khumsupan P, Sithisan P, Managit C, and Gritsanapan W. (2014). Simple quantitative analysis of α-mangostin in mangosteen rind extracts and their microparticle preparations using HPLC method. Journal of Chemical, Biologycal and Physical Sciences Sec. B, 4(4), 3406–3412.
[15] Walker, E. B. (2007). HPLC analysis of selected xanthones in mangosteen fruit. Journal of separation science, 30(9), 1229–1234. [16] Depkes RI. (2010). Suplemen I Farmakope Herbal Indonesia, Jakarta:
Kementerian Republik Indonesia.
[17] Gandjar, I. G., & Rohman, A. (2012). Analisis Obat secara Spektrofotometri dan Kromatografi. Yogyakarta: Pustaka Pelajar. [18] Gandjar, I. G., & Rohman, A. (2012). Kimia Farmasi Analisis.
Yogyakarta: Pustaka Pelajar.
[19] Harmita, H. (2012). Petunjuk pelaksanaan validasi metode dan Cara Perhitungannya. Pharmaceutical Sciences and Research (PSR), 1(3), 117–135.
[20] ICH. (2005). Validation of Analytical Procedures: Text and Methodology Q2(R1). http://www.ich.org/products/guidelines/ quality/quality-single/article/validation-of-analytical-procedures-text-and-methodology.html. [accessed 12.11.17]
[21] Borman, P. and Elder, D. (2017) Q2(R1) Validation of Analytical Procedures, in ICH Quality Guidelines: An Implementation Guide (eds A. Teasdale, D. Elder and R. W. Nims). New York: John Wiley & Sons, Inc.
[22] Rappoport, Z. (2003). Chemistry of Phenols. Chichester: John Wiley & Sons Ltd.
[23] Satong-aun, W., Assawarachan, R., & Noomhorm, A. (2011). The Influence of Drying Temperature and Extraction Methods on α-Mangostin in Mangosteen Pericarp. Journal of Food Science and Engineering, 1(2), 10–17.
Copyright © 2017 The author(s). You are free to share (copy and redistribute the material in any medium or format) and adapt (remix, transform, and build upon the material for any purpose, even commercially) under the following terms: Attribution — You must give appropriate credit, provide a link to the license, and indicate if changes were made. You may do so in any reasonable manner, but not in any way that suggests the licensor endorses you or your use; ShareAlike — If you remix, transform, or build upon the material, you must distribute your contributions under the same license as the original (https://creativecommons.org/licenses/by-sa/4.0/)
baik digunakan untuk analisis suatu senyawa [20,21]. Data pengukuran presisi intraday dan interday dapat dilihat pada
Tabel 2 dan 3.
Perolehan kembali (recovery) dilakukan dengan
penambahan larutan standar pada sampel dengan
konsentrasi 100 µg/mL. Didapatkan % perolehan kembali
dari hasil analisis sebesar 90,04%. Persentase perolehan kembali yang baik adalah memiliki rentang nilai 85% - 115% [20,21]. Dari hasil % recovery yang diperoleh pada penelitian ini menunjukkan bahwa nilainya berada pada rentang yang diperbolehkan. Jadi, dapat dibuktikan bahwa metode validasi ini memberikan hasil yang akurat, seperti yang tercantum di dalam Tabel 4.
Kemudian dilakukan pengukuran kadar α-mangostin
pada sampel dengan menggunakan perhitungan yang telah ditetapkan, didapatkan hasil akhir kadar rata-rata untuk
sampel B dan C sebesar 0,040% b/v dan 0,118% b/v,
seperti yang tercantum di dalam Tabel 5, dan Tabel 6.
KESIMPULAN
Analisis kandungan senyawa α-mangostin pada
minuman herbal kulit buah manggis dapat ditentukan dengan metode KLT densitometri menggunakan fase diam pelat silika gel 60 F254 dan fase gerak
kloroform-etil asetat (9:1, v/v). Metode KLT densitometri valid untuk penentuan kadar α-mangostin dengan hasil nilai parameter
validasi yang memenuhi persyaratan, dengan nilai r =
0,99415; LOD = 54,38 µg/mL dan LOQ 181,28 µg/mL;
nilai presisi di bawah 2% serta akurasi 90,04 %. Minuman herbal kulit buah manggis yang positif mengandung
![Gambar 1. Struktur kimia α-mangostin [8].](https://thumb-ap.123doks.com/thumbv2/123dok/2639868.1667004/2.595.325.510.85.172/gambar-struktur-kimia-a-mangostin.webp)