S K R I P S I
M J L i K
PEKHLiSTAKAAN *UNIVERS1TAS A i R L A N G G A "
S U R A B a V A
JEMY TANDRA
KK S
K KF F 74]/9r
Ta h
p
PENGARUH PEMBERIAN VITAMIN C
TERHADAP KADAR KOLESTEROL TOTAL
DAN KOLESTEROL HDL SERUM
MARMOT
(CAVIA PORCELLUS)
PENGARUH PEMBERIAN VITAMIN C TERHADAP KADAR
KOLESTEROL TOTAL DAN KOLESTEROL HDL
SERUM MARMOT {CAVIA PORCELLUS)
Dibuat untuk memenuhi syarat
mencapai gelar Sarjana Farmasi pada
Fakultas Farmasi Universitas Airlangga
1995
Oleh :
Jemy Tandra
059011243
Disetujui oleh pembimbing : SKRIPSI
DR. Purwanto
Pembimbing utama
Drs. Siswandono, MS Drs. Robby Sondakh, MS
KATA PENGANTAR
Puji syukur ke hadirat Tuhan Yang Maha Esa atas
segala rahmat dan karunia yang telah dilimpahkanNya kepada
saya, sehingga tugas skripsi saya telah terselesaikan,
guna memenuhi syarat dalam mencapai gelar Sarjana Farmasi
di Fakultas Farmasi Universitas Airlangga.
Dengan selesainya tugas skripsi ini, maka pada kesem-
patan ini saya ingin menyampaikan terima kasih yang sebe-
sar-besarnya kepada :
1. Bapak DR. Purwanto dari Laboratorium Kimia
Medisinal Fakultas Farmasi Universitas Airlangga
selaku pembimbing utama.
2. Bapak Drs. Siswandono, MS dari Laboratorium Kimia
Medisinal Fakultas Farmasi Universitas Airlangga
selaku pembimbing serta.
3. Bapak Drs. Robby Sondakh, MS dari Laboratorium
Kimia Medisinal Fakutas Farmasi Universitas Air
langga selaku pembimbing serta.
4. Bapak Ketua Jurusan Kimia Farmasi, Kepala Labora
torium Kimia Medisinal, Kepala Laboratorium
Kimia Analisis Farmasi dan Kepala Laboratorium
Sintesis Farmasi Fakultas Farmasi Universitas
5. Ibu Dra. Hamidah Shahab, Bapak Drs. IGK Artawan,
Bapak Drs. Soegiyanto, MS dan Ibu Dra. Soemiati,
MS selaku dosen penguji.
6. Pengelola Unit Penunjang Hewan Percobaan Fakul
tas Farmasi Universitas Airlangga yang telah
banyak memberikan bantuan dan fasilitas selama
penelitian ini.
7. Segenap karyawan Laboratorium Kimia Medisinal,
Laboratorium Kimia Analisis dan Laboratorium
Sintesis Farmasi yang telah memberikan bantuan
dalam penelitian ini. •
*
8. Keluarga tercinta yang senantiasa memberikan ban
tuan, dorongan dan mendampingi dalam suka dan
duka.
9. Semua pihak yang tidak dapat saya sebutkan satu
persatu.
Semoga semua pihak yang telah memberikan bantuan
kepada saya akan mendapat balasan dari Tuhan Yang Maha Esa
dan semoga skripsi ini dapat memberikan sumbangan yang
bermanfaat bagi masyarakat, khususnya mahasiswa Fakultas
Farmasi Universitas Airlangga.
Surabaya, Januari 1995
DAFTAR ISI
KATA PENGANTAR ... ii
DAFTAR ISI ... iv
DAFTAR GAMBAR ... vii
DAFTAR TABEL ... viii
DAFTAR LAMPIRAN ... ix
RINGKASAN ... x
BAB I. PENDAHULUAN ... 1
1. Latar Belakang Permasalahan ... 1
2. Permasalahan ... 5
3. Tujuan Penelitian ... 5
4. Hipotesis ... 5
5. Manfaat Penelitian ... 5
BAB II. TINJAUAN PUSTAKA ... 6
1. Tinjauan tentang Vitamin C ... 6
1.1. Sumber Vitamin C ... 6
1.2. Sifat Fisika Kimia Vitamin C ... 8
1.3. Stabilitas Vitamin C ... 9
1.4. Vitamin C dalam Tubuh ... '.... 10
2. Tinjauan tentang Kolesterol ... 11.
2.1. Sifat Fisika Kimia Kolesterol ... 11
2.2. Kolesterol dalam Tubuh ... 13
2.4. Faktor-faktor yang Mempengaruhi Kadar
Kolesterol dalam Darah .14
2.5. Kolesterol HDL ... .16
2.6. Ekskresi Kolesterol ...18
3. Tinjauan tentang Hewan Percobaan ...19
4. Tinjauan tentang Penentuan Kadar Kolesterol dengan Metode Liebermann-Burchard ...19
4.1. Penentuan Kadar Kolesterol Total ...20
4.2. Penentuan Kadar Kolesterol HDL ...22
5. Tinjauan tentang Metode Spektrofotometri .. 23
6. Tinjauan tentang Uji Validasi ...24
6.1. Kelurusan dan Trayek Kelurusan ... .25
6.2. Sensitivitas ...25
6.3. Presisi ...25
5.4. Akurasi ...26
BAB III. BAHAN, ALAT DAN METODE PENELITIAN ...27
1. Bahan-bahan yang Digunakan ...27
2. Alat-alat yang Digunakan ...27
3. Cara Kerja ... .27
3.1. Analisis Kualitatif terhadap Vitamin C 27 3.1.1. Pemeriksaan Organoleptis ... .27
3.1.2. Reaksi Warna ... .28
3.1.3. Pemeriksaan Titik Lebur ... .28
3.2. Hewan Percobaan ... .29
3.2.1. Rancangan Percobaan ... .29
4.1. Kelurusan ... .32
4.2. Sensitivitas ... .33
4.3. Presisi ... .33
4.4. Akurasi ... .34
5. Pembuatan Kurva Baku ...34
5.1. Pemilihan Panjang Gelombang Maksimum . 35 5.2. Pembuatan Kurva B a k u ... .35
6. Pengambilan Sampel Darah ... .36
7. Penentuan Kadar ... .36
7.1. Penentuan Kadar Kolesterol Total Serum 36 ' 7.2. Penentuan Kadar Kolesterol HDL serum . 36 8. Analisis Data ...39
BAB IV. HASIL PERCOBAAN ...45
1. Analisis sifat fisika kimia vitamin C .... .44
2. Penentuan panjang gelombang maksimum ... .46
3. Uji validasi ...47
3.1. Kelurusan ... 47
3.2. Sensitivitas ...49
3.3. Presisi ...50
3.4. Akurasi ...52
4. Hasil pemeriksaan kadar kolesterol total .. 53
5. Hasil pemeriksaan kolesterol HDL serum .... 58
BAB V. PEMBAHASAN ...64
BAB VI. KESIMPULAN ...72
BAB VII. SARAN ...73
DAFTAR GAMBAR
1. Penentuan panjang gelombang maksimum larutan
kolesterol ... 46
2. Kurva linier nilai serapan terhadap kadar -
larutan kolesterol pada panjang gelombang
maksimum... 48
Tabel
Serapan larutan kolesterol pada panjang
gelombang 620,5 nm dengan 10 macam kadar .... 47
Hasil pengamatan serapan blanko ... 50
Penentuan presisi ... 51
Penentuan akurasi . . . ... 52
Hasil pemeriksaan kadar kolesterol total
serum marmot ... 53
Hasil uji HSD pemeriksaan kadar kolesterol
total serum marmot kelompok I, II.1, II.2 dan
11. 3 ... 55
Hasil uji HSD pemeriksaan kadar kolesterol
total serum marmot kelompok III, IV.1, IV.2
dan IV. 3 ... 57
Hasil pemeriksaan kadar kolesterol HDL serum
marmot ... 59
Hasil uji HSD pemeriksaan kadar kolesterol
HDL serum marmot kelompok III, IV.1, IV.2 dan
DAFTAR LAMPIRAN
1. Hasil perhitungan koefisien korelasi ... 79
2. Hasil penentuan LOD dan LOQ ... 81
3. Analisa data uji Anakova untuk pemeriksaan kadar
kolesterol total serum marmot... 83
4. Analisa data uji Anakova untuk pemeriksaan kadar
kolesterol HDL serum marmot ... 87
5. Tabel harga koefisien korelasi pada derajat ke-
percayaan 5% dan 1% ... 91
6. Tabel distribusi F pada derajat kepercayaan 0,05 92
R I N G K A S A N
Untuk mengetahui apakah terdapat perbedaan efek dari
dosis vitamin C dilakukan penelitian tentang pengaruh
beberapa macam dosis vitamin terhadap kadar kolesterol
total dan kolesterol HDL serum marmot.
Pada penelitian ini digunakan 40 ekor marmot yang
dibagi menjadi 2 grup, masing-masing grup terdiri dari
4 kelompok, di mana masing-masing kelompok terdiri dari 5
ekor marmot. Kelompok-kelompok tersebut adalah sebagai
berikut :
Grup pertama :
Kelompok I : makanan dasar
Kelompok II.1 : makanan dasar + vitamin C dosis 1
Kelompok 11,2 : makanan dasar + vitamin C dosis 2
Kelompok II.3 : makanan dasar + vitamin C dosis 3
Grup kedua:
Kelompok III : makanan dasar + kolesterol 3% 1 ml
Kelompok IV.'l : makanan dasar + kolesterol 3% 1 ml
+ vitamin C dosis 1
Kelompok IV.1 : makanan dasar + kolesterol 3% 1 ml
+ vitamin C dosis 2
Kelompok IV.1 : makanan dasar + kolesterol 3% 1 ml
+ vitamin C dosis 3
vitamin C diberikan dalam bentuk larutan. Dosis vitamin C
yang diberikan merupakan dosis konversi dari dosis untuk
manusia. Pemberian kolesterol dan vitamin C dilakukan
secara per oral selama satu bulan. Sebelum perlakuan
dilakukan pemeriksaan kadar kolesterol total dan koleste
rol HDL serum. Setelah satu bulan kadar kolesterol total
dan kolesterol HDL serum diperiksa lagi. Sebelum satnpel
darah diambil hewan coba dipuasakan selama 12-14 jam. Pengambilan sampel darah dilakukan secara intra kardial.
Darah ditampung tanpa antikoagulan. Serum yang diperoleh
diperiksa kadar kolesterol total dan kolesterol HDL-nya
dengan metode Huang dan kawan-kawan, menggunakan pereaksi
warna Liebermann-Burchard. Untuk penentuan kadar koleste
rol HDL serum sebelum direaksikan dengan pereaksi warna
Liebermann-Burchard terlebih dahulu dilakukan teknik
pengendapan selektif secara kimiawi untuk lipoprotein-
lipoprotein lain selain HDL dengan menggunakan pereaksi
Heparin dan Mangan Klorida.
Hasil penelitian menunjukkan bahwa pemberian vitamin
C dapat menurunkan kadar kolesterol total secara bermakna,
baik pada keadaan normal maupun hiperkolesterolemia,
Selain itu juga dapat meningkatkan kadar kolesterol HDL
serum pada keadaan hiperkolesterolemia, sedang pada kea
BAB I
PENDAHULUAN
1. Latar Belakang Permasalahan .
Penyakit jantung atau penyakit kardiovaskuler,
juga dikenal sebagai penyakit arteri koronaria, arte-
riosklerosis atau pengerasan ai'teri. Ciri penyakit ini
adalah terjadinya perubahan degeneratif dalam arteri.
Jenis yang umum dari penyakit ini adalah aterosklerosis
[1]. Aterosklerosis merupakan penyebab kematian utama
di Amerika Serikat dan negara-negara Eropa [2]. Di
Indonesia jumlah angka kematian akibat penyakit ini
cenderung meningkat dari tahun ke tahun [3]. Penyakit
ini tidak hanya mempengaruhi orang-orang usia lanjut,
tetapi juga merupakan penyebab kematian dan cacat pada
usia setengah tua [4]. Faktor penyebab utama dari
penyakit ini adalah kadar kolesterol serum, tekanan
darah, dan kebiasaan merokok. Faktor lainnya adalah
umur, jenis kelamin dan keturunan [1]. Kadar kolesterol
total serum telah lama diketahui sebagai faktor penye
bab penyakit aterosklerosis yang paling besar [4].
Individu dengan kadar kolesterol total serum antara
200-239 mg/dl dianggap berada pada batas ambang atero
resiko yang tinggi [5j.
Di dalam darah, kolesterol, trigliserida, dan
fosfolipida terikat pada protein tertentu membentuk
lipoprotein. Lipoprotein dapat digolongkan menjadi
kilomikron, lipoprotein densitas sangat rendah (VLDL),
lipoprotein densitas rendah (LDL), lipoprotein densitas
sedang (IDL), dan lipoprotein densitas tinggi (HDL).
Ada hubungan berkebalikan antara konsentrasi HDL dan penyakit jantung koroner, dan beberapa ahli menganggap
bahwa hubungan yang paling dapat diramalkan adalah
perbandingan kolesterol LDL/HDL [6]. Penelitian para
ahli menunjukkan bahwa wanita jarang menderita penyakit
ini karena pada wanita kadar kolesterol HDL lebih
tinggi dibanding laki-laki, sehingga disimpulkan bahwa
kolesterol HDL merupakan faktor anti resiko terjadinya
penyakit aterosklerosis [7]. Kadar kolesterol LDL
antara 130-159 mg/dl dianggap sebagai batas dan di atas
160 mg/dl dianggap mempunyai resiko tinggi terhadap
timbulnya penyakit aterosklerosis [5]. Kadar kolesterol
HDL cukup 35-65 mg/dl agar tidak terjadi penyakit ini C8].
Jumlah kolesterol dalam darah ditentukan oleh
interaksi 4 faktor, yaitu [9]:
- Laju pembuatan kolesterol oleh hati dari asetat.
- Laju kolesterol yang diubah menjadi asam empedu dan
dibuang melalui usus halus.
- Laju asam empedu yang diserap kembali dan diubah
menjadi kolesterol.
Dalam perkembangan penyakit jantung, banyak pene
litian yang menaruh perhatian pada faktor-faktor dalam
makanan yang dapat mempengaruhi kadar kolesterol plas
ma. Hubungan antara makanan, kolesterol serum dan
penyakit aterosklerosis telah ditunjukkan selama Perang
Dunia Kedua, pada saat pendistribusian makanan di Eropa
Utara cenderung mengarah pada penurunan pemasukan
kalori total, peningkatan karbohidrat, dan penurunan
semua lemak makanan termasuk kolesterol. Data yang
didapat menunjukkan bahwa kematian akibat penyakit
aterosklerosis menurun dengan tiba-tiba pada tahun-
tahun pertama perang [4]. Pemasukan kolesterol per hari
harus kurang dari 300 mg [5]. Tetapi yang penting
adalah biokimia dan proses metabolisme kolesterol dalam
tubuh. Biokimia dan fungsi kedua lipoprotein LDL dan
HDL sangat penting dalam memahami siklus kolesterol.
LDL membawa kolesterol dalam darah, mendorong kole
sterol. sehingga menempel pada sel pembuluh. Se-
baliknya HDL membawa kolesterol kembali ke kandung
empedu, di mana kolesterol diubah menjadi asam empedu
Di Indonesia vitamin C banyak diperdagangkan se
bagai sediaan farmasi, baik sebagai suplemen maupun
obat. Kandungan vitamin C dalam sediaan-sediaan terse-
but bervariasi antara 20 mg sampai 1 g [10]. Vitamin C
dapat digunakan untuk terapi alkoholisme, alergi,
penyakit-penyakit defisiensi dan darah, infeksi dan
lain-lain [11]. •
Pada defisiensi vitamin C dijumpai adanya pening- katan kolesterol dalam serum darah dan penimbunan
kolesterol dalam hati. Hal ini disebabkan oleh keter-
lambatan pengubahan kolesterol dalam hati menjadi asam
empedu. Diduga vitamin C berfungsi mempengaruhi pengu
bahan kolesterol menjadi asam empedu di dalam hati
[12].
Obat-obat hipolipidemik, antara lain klofibrat,
asam nikotinat, dan resin dapat digunakan untuk menu-
runkan kadar kolesterol karena dapat mengganggu sinte-
sis kolesterol dalam tubuh. Tetapi banyak di antara
obat-obat ini yang mempunyai efek samping yang cukup
besar, sehingga sekarang sedang dipertimbangkan untuk
dihindari pengobatan dengan cara mengganggu sintesis
kolesterol [6]. Penggunaan obat-obat ini harus di- dasarkan pada kondisi fisiologis penderita dan tidak
boleh diberikan pada wanita hamil atau yang sedang
2. Permasalahan
Dari latar belakang di atas, maka timbul permasa
lahan bagaimanakah pengaruh pemberian vitamin C terha-
dap kadar kolesterol total dan kolesterol HDL serum
marmot ( Cavia porcellus) ?
3. Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui
pengaruh vitamin C terhadap kadar kolesterol total dan
kolesterol HDL serum marmot (Cavia porcellus).
4. Hipotesis
Vitamin C dapat menurunkan kadar kolesterol total
serum dan meningkatkan kadar kolesterol HDL serum.
5. Manfaat Penelitian
Dari hasil penelitian diharapkan dapat memberi
informasi tentang pentingnya vitamin C sebagai salah
BAB II
TINJAUAN PUSTAKA
1. Tinjauan tentang Vitamin C
1.1. Sumber Vitamin C
Vitamin C tersebar luas dalam hewan dan tumbuh-
an. Dalam jaringan hewan kadar tertinggi ditemukan
dalam korteks adrenal, lensa mata dan hati. Dalam
tumbuhan vitamin C dibentuk secara sinambung dalam
semua organ hijau dan berlimpah dalam daerah yang
paling aktif tumbuh. Kandungan terbesar ditemukan
dalam kulit buah dan dalam beberapa daun lebih banyak
daripada dalam batang [11]. Kadar vitamin C bervaria-
si dalam jaringan tumbuhan [13].
Dalam makanan kadar vitamin C ditemukan sangat
sedikit. dalam ikan, daging, susu yang dipasteurisasi
dan telur, sama sekali tidak ada dalam butir padi
kering dan juga butir padi kecuali mereka telah
bertunas. Kadar vitamin dalam makanan tergantung
kondisi pertumbuhan tanaman, maturasi tanaman dan
perlakuan terhadap bahan-bahan tanaman setelah sele-
sai panen [13].
Beberapa sumber vitamin C yang cukup penting
Tabel I. Kadar vitamin C dalam mg/100 g bahan
No Nama Bahan Kadar dalam mg
1. Jambu biji (guava) 300
2. Daun singkong 275
3. Buah jeruk (citrus fruit) 220
4. Black current 200
5. Jambu monyet . 197
6
.
Paterseli/daun sup 1907. Daun melinjo 182
8. Cabe (green pepper) 120
9. Brokoli 113
10. Daun lobak 109
11. Sawi 102
12. Tomat 100
13. Squash (semacam labu) 90
14. Mangga muda 89
15. Bayam 80
24. Daun kecipir 29
25. Nanas 24
26- Pala 22
27. Sirsak 22
28. Sawo 21
29. Kacang buncis 19
30. ASI 5
31. Pisang ambon 3
1.2. Sifat Fisika Kimia Vitamin C
Vitamin C adalah sinonim dari asam askorbat. Asam askorbat merupakan serbuk kristal, tidak berwar-
na atau putih atau kuning pucat, tidak berbau atau
hampir tidak berbau, rasa asam [14].
Asam askorbat mempunyai dua bentuk isomer, yaitu
isomer L dan isomer D. Bentuk alamiah dari vitamin
ini adalah isomer L. Isomer D aktivitasnya 10%
isomer L [15].
Asam askorbat merupakan bentuk enol dari
3-okso-L-gulofuranolakton [14]. Struktur molekul asam
askorbat atau vitamin C adalah sebagai berikut [13]:
O
Nama kimia :
Kelarutan : larut dalam 3-3,5 bagian air, dalam
25 bagian alkohol dan dalam 10
bagian metanol; Larut dalam aseton;
Praktis tidak larut dalam eter,
kloroform dan petroleum eter [14].
pH : 2,0 padgi kadar 50 mg/ml [13]
Nilai pK pada 25°C [15] : pK1 =4,04
pK2 =11,4
1.3. Stabilitas Vitamin C
Kristal asam askorbat stabil dalam lingkungan
kering dan temperatur kamar [13]. Walaupun stabil
dalam bentuk padat, dalam bentuk larutan relatif
cepat teroksidasi menjadi asam dehidroaskorbat [16].
Larutan asam askorbat dalam air pH S 7,6 tidak di-
oksidasi oleh udara asal tidak ada tembaga dan bahan
lain yang dapat mengkatalisa reaksi [13].
Reaksi yang penting untuk asam askorbat adalah
Q = C
---Asam askorbat sangat peka terhadap berbagai cara
degradasi. Faktor-faktor yang dapat mempengaruhi
degradasi antara lain temperatur, enzim, pH, katalis
logam, kadar awal asam askorbat dan rasio asam askor
bat menjadi asam dehidroaskorbat [15].
1.4. Vitamin C dalam Tubuh
Peran vitamin C dalam nutrisi telah dikarak-
terisasi dengan baik. Vitamin C penting dalam nutrisi
manusia karena ia menjaga bahan-bahan semen yang
terletak antara sel-sel jaringan tubuh dalam kondisi
baik. Sebagai hasil dari aksi ini, vitamin C mencegah
perdarahan dan sakit gusi, hemorrhage jaringan dan
beberapa bentuk anemia. Vitamin C membantu perkem-
Setelah pemberian oral, vitamin C diabsorbsi
dengan cepat. Bagian dosis terabsorbsi cenderung
menurun dengan meningkatnya dosis. Didistribusi
secara luas dalam jaringan tubuh. Kadar dalam lekosit
dan platelet lebih tinggi daripada dalam eritrosit
dan plasma. Asam askorbat dimetabolisme menjadi asam.
dehidroaskorbat, asam 2,3-diketogulonat, oksalat dan karbon dioksida. Terjadi sedikit konjugasi dengan
sulfat membentuk askorbat-3-sulfat. Asam askorbat
melebihi kebutuhan tubuh dieliminasi dengan cepat
dalam urin. Kurang lebih 85% dosis intravena diberi
kan pada subyek yang belum tersaturasi dengan vitamin ini diekskresi dalam urin dalam 24 jam, dengan kurang
lebih 70% dari dosis diekskresi dalam bentuk tidak
berubah dan 15% sebagai asam dehidroaskorbat dan asam
diketogulonat. Jumlah normal yang ada dalam tubuh
melebihi 1,5 g. Kadar dalam plasma dan lekosit secara normal kurang lebih 5-12 ug/ml dan 25-30 ug/10® sel. Berikatan dengan protein plasma kurang lebih 25%
[17 3.
2. Tinjauan tentang Kolesterol
2.1. Sifat Fisika Kimia Kolesterol
Kolesterol merupakan sterol penting yang telah
dipelajari selama bertahun-tahun. Kolesterol merupa-
kan serbuk atau granul halus, warna putih atau
dalam air, perlahan-lahan larut dalam 100 bagian
alkohol dan dalam 50 bagian dehidrat alkohol, larut
dalam aseton, kloroform, dioksan, eter, etil asetat,
petroleum eter, dan minyak tumbuhan (14).
Rumus bangun kolesterol adalah sebagai berikut:
BM = 386,7
Kolesterol memberikan sejumlah reaksi warna yang
karakteristik, antara lain dengan reaksi Liebermann-
Burchard, di mana larutan kolesterol dalam kloroform
dengan penambahan asetat anhidrida dan asam sulfat
pekat akan memberikan warna hijau kebiruan sampai
hijau. Intensitas warna yang diperoleh bervariasi sesuai dengan jumlah kolesterol yang ada, oleh karena
itu reaksi ini merupakan dasar perhitungan kuanti-
tatif. Reaksi warna yang lain dikembangkan oleh
Salkowski, yaitu larutan kolesterol dalam kloroform
dengan penambahan asam sulfat pekat akan memberikan
warna merah kebiruan sampai violet [18].
2.2. Kolesterol dalam Tubuh
Bagian terbesar kolesterol dalam tubuh berasal
dari biosintesis yaitu sekitar 1 gram/hari, dan hanya
sekitar 0,3 gram/hari yang berasal dari makanan
(diet) biasa. Sebenarnya semua jaringan yang mengan-
dung sel berinti mampu mensintesis kolesterol, ter-
utama hepar, korteks adrenalis, Jrulit, usus, testis,
dan aorta. Fraksi mikrosom dan sitosol sel bertang-
gungjawab untuk biosintesis kolesterol [6].
Kolesterol plasma manusia terutama diangkut
dalam LDL dan sedikit dalam HDL dan VLDL. Dalam
populasi orang Amerika terdapat kenaikan kolesterol
yang terus-menerus sampai tercapai maksimum, kira-
kira pada usia 55-60 tahun. Pada usia 21 tahun,
kadar kolesterol plasma rata-rata kurang lebih
180 mg/dl. Setelah usia 25 tahun, kadar akan me-
ningkat sampai 200-250 mg/dl [4].
2.3. Absorbsi dan Transport Kolesterol
Kolesterol dalam makanan diserap dari usus dan
bersama dengan lipid lain, termasuk kolesterol yang
disintesa dalam usus, digabungkan dalam kilomikron
dalam getah bening diesterifikasi dengan asam lemak
rantai panjang. Esterifikasi dapat terjadi dalam
mukosa usus. Sterol tanaman (sitosterol) diabsorbsi
kurang baik. Pada saat sisa kilomikron bereaksi
dengan hepar, sebagian besar ester kolesteril
terhidrolisa dan kolesterol diambil oleh hepar.
VLDL yang dibentuk dalam hepar mentransport
kolesterol ke dalam plasma [6].
Sebagian besar kolesterol ditemukan dalam
bentuk ester dan diangkut sebagai lipoprotein
dalam plasma. Lipoprotein ini merupakan partikel
kompleks yang mengandung apoprotein, protein yang dapat mengikat lipida, dan membantu pengaturannya
dari hepar ke dalam plasma [6].
Berdasarkan densitasnya dapat dibagi lima
fraksi lipoprotein dan di antara kelima fraksi
lipoprotein tersebut, fraksi lipoprotein dengan
. densitas tinggi (HDL) adalah faktor pelindung
(anti resiko) terhadap terjadinya aterosklerosis.
2.4. Faktor-faktor yang Mempengaruhi Kadar Kolesterol
dalam Darah
Adanya kolesterol sebagai salah satu faktor
resiko terjadinya penyakit jantung koroner telah
menyebabkan usaha-usaha untuk menurunkan kadar
- Peningkatan jumlah kolestero-l yang dimakan sedikit
meningkatkan konsentrasi kolesterol dalam plasma.
Biasanya, konsentrasi kolesterol plasma tidak dapat
berubah lebih dari ± 15% dengan mengubah diet,
walaupun kolesterol yang ekstrem dalam diet mungkin
dapat mengubah kadar sampai sebanyak ± 30% [19].
Peningkatan kolesterol dalam makanan sebanyak
100 mg menyebabkan peningkatan kadar kolesterol
sebesar 5 mg per 100 ml serum [6].
- diet yang jenuh lemak meningkatkan konsentrasi
kolesterol darah sebanyak 15-25% [19].
- makan lemak yang mengandung banyak asam lemak
tidak jenuh biasanya menekan konsentrasi koleste
rol darah dalam jumlah ringan sampai moderat [19].
- kekurangan hormon tiroid meningkatkan kolesterol
darah dan sebaliknya [19].
- pada diabetes melitus kolesterol darah sangat me-
ningkat, hal ini diduga akibat peningkatan umum
mobilisasi lipid pada keadaan ini [19].
- hormon seks wanita, estrogen, menurunkan kolesterol
darah, sedangkan hormon seks pria, androgen,
meningkatkan kolesterol darah. Efek ini penting
sekali karena makin tinggi kadar kolesterol pada
laki-laki erat hubungannya dengan peningkatan
kemungkinan terjadinya aterosklerosis [19].
sangat meningkat.
- sterol tanaman (sitosterol) berkompetisi dengan
kolesterol pada proses absorbs! dalam usus. Jika
dikonsumsi dalam jumlah besar, akan dapat menurun-
kan kadar kolesterol plasma [4].
Sebelum 1952 kandungan lemak total dalam
makanan dianggap sebagai faktor yang menentukan
kadar kolesterol plasma. Pada waktu itu Kinsell
melaporkan bahwa lemak hewani meningkatkan kole
sterol plasma, sedangkan lemak tumbuhan menurun-
kannya. Kemudian Keys menemukan bahwa lemak jenuh
meningkatkan kolesterol darah, lemak tak jenuh
banyak menurunkannya, sedangkan lemak tak jenuh
tunggal tidak berpengaruh [4].
2.5. Kolesterol HDL
Lemak bertanggung jawab atas penyediaan energi
bagi tubuh, tetapi terdapat permasalahan dalam
pengangkutan lemak yang bersifat hidrofobik dalam
sirkulasi darah. Hal ini diatasi dengan pembentukan
ikatan antara lemak tidak larut dengan golongan yang
lebih polar seperti fosfolipida, kemudian menggabung- kannya dengan kolesterol dan protein membentuk kom-
pleks lipoprotein yang hidrofilik [6].
Fraksi protein dalam lipoprotein dikenal sebagai
apoprotein. Ada beberapa macam apoprotein, yaitu :
- Apoprotein B.
- Apoprotein C-I, Apoprotein C-II, Apoprotein C-III.
- Apoprotein E
Ada lima golongan lipoprotein yaitu kilomikron,
VLDL, LDL, IDL, dan HDL. Di antara kelima golongan
tersebut yang merupakan faktor anti resiko terhadap
terjadinya aterosklerosis adalah HDL.
HDL disintesa dan disekresi dari hepar dan
usus. HDL yang baru terbentuk (nascent) dari usus
tidak mengandung apoprotein C, tapi hanya apopro
tein A. Oleh sebab itu, tampaknya apoprotein C hanya
disintesa dalam hepar dan dipindahkan pada HDL
intestinal pada saat HDL intestinal memasuki plasma.
HDL yang dibentuk dalam hepar terdiri dari dua
lapisan fosfolipida diskoid yang mengandung apopro
tein dan kolesterol bebas. Lipoprotein-lipoprotein
ini mirip dengan partikel-partikel yang ditemukan
dalam plasma penderita defisiensi enzim lesitin-
kolesterol-asil-transferase (LCAT) [6],
Katalisis oleh enzim LCAT akan mengubah fosfoli
pida dan kolesterol bebas menjadi ester kolesterol
dan lisolesitin. Ester kolesterol akan bergerak
menuju bagian dalam lapisan fosfolipida, sedangkan
lisolesitin dipindahkan ke albumin plasma. Reaksi
berlanjut menghasilkan suatu inti nonpolar yang
dilapisi oleh suatu film dari lemak-lemak polar dan
apoprotein. Hepar dan mungkin juga usus merupakan
tempat €erakhir degradasi apoprotein HDL [6].
Faktor-faktor yang mempengaruhi kadar HDL dalam
darah antara lain :
1. Jenis kelamin
Kadar HDL pada wanita lebih tinggi daripada pria
[6].
2. Aktivitas atau latihan fisik
Latihan dapat menurunkan VLDL dan LDL, meningkat
kan HDL [1].
3. Kafein dan kebiasaan merokok
Dapat meningkatkan LDL dan menurunkan HDL [1].
4. Alkohol
Konsumsi alkohol yang tidak berlebihan dapat
meningkatkan kadar HDL [1].
5. Mineral
Defisiensi tembaga menyebabkan peningkatan kadar
LDL plasma dan penurunan kadar HDL [1].
6. Vitamin C
Terapi vitamin C dosis tinggi menyebabkan penu
runan LDL dan kolesterol total, dan peningkatan HDL Cl].
2.6. Ekskresi Kolesterol
Kira-kira separuh dari' kolesterol yang dielimi-
■ menjadi garam empedu. Sisanya diekskresikan sebagai
steroid netral. Sebagian besar kolesterol yang dieks
kresi dalam empedu direabsorbsi, dan dipercaya bahwa
kolesterol yang berfungsi sebagai prekursor sterol
feces berasal dari mukosa usus. Koprostanol adalah
sterol utama dalam feces, dibentuk dari kolesterol
dalam usus bagian bawah oleh bakteri-bakteri usus.
Sebagian besar garam-garam empedu dari
ekskresi bilier direabsorbsi ke dalam sirkulasi
portal, diambil oleh hepar, dan diekskresi kembali
di dalam empedu. Ini dikenal sebagai sirkulasi
enterohepatik. Garam-garam empedu yang tidak direab
sorbsi atau turunannya diekskresi dalam feces [6].
3. Tinjauan tentang Hewan Percobaan
Pada penelitian, hewan coba yang dapat digunakan
antara lain marmot, tikus, babi, ayam, kelinci dan
kera. Marmot dipilih sebagai hewan coba dengan alasan
sebagai berikut [20]:
- biayanya relatih murah.
- pemeliharaan relatif mudah.
- pertimbangan volume darah yang akan diambil.
- tidak memerlukan tempat pemeliharaan yang luas.
4. Tinjauan tentang Penentuan Kadar Kolesterol dengan
4.1. Penentuan Kadar Kolesterol Total
Penentuan kadar kolesterol total dengan menggu
nakan metode Liebermann-Burchard pertama kali dite
mukan oleh Liebermann pada tahun 1885, dan digunakan
untuk analisis kolesterol oleh Burchard tidak lama
kemudian. Pada penelitian-penelitian awal digunakan
kloroform sebagai pelarut, tetapi reaksi Liebermann-
Burchard sekarang ini menggunakan medium asam asetat-
asam sulfat-asetat anhidrida [21].
Metode lain yang banyak digunakan adalah reaksi
Zak, yang untuk pertama kali digunakan dalam analisis
kolesterol oleh Zlatkis, Zak dan Boyle pada tahun
1953, pembawanya adalah asam asetat-asam sulfat,
tanpa asetat anhidrida. Untuk mendapatkan warna yang
diinginkan harus ditambahkan Fe^+ [21].
Metode menurut Huang dan kawan-kawan yang meng
gunakan pereaksi Liebermann-Burchard mempunyai banyak
keuntungan jika dibandingkan dengan metode lainnya.
Keuntungan metode Huang dan kawan-kawan ini antara
lain [22]:
- prosedur pelaksanaannya relatif mudah.
- hanya menggunakan satu pereaksi warna dan dengan
pemeriksaan secara langsung.
- pereaksi yang digunakan stabil selama 2 minggu pada
suhu kamar dan 4 minggu di dalam almari es.
menit dan warna yang terjadi tetap stabil selama 20
menit.
- faktor suhu tidak begitu mempengaruhi reaksi warna.
Pada pemeriksaan antara suhu 21-25°C tidak memberi-
kan hasil yang berbeda.
Metode lain yang dianggap sebagai metode
rujukan adalah metode Abel dan kawan-kawan. Metode
ini tnemerlukan beberapa tahap reaksi, antara lain
penyabunan dari ester kolesterol dan ekstraksi dari
kolesterol bebas. Dengan demikian diperlukan pera-
latan yang banyak dan perlu ketrampilan khusus serta
memakan waktu yang lebih lama dan memungkinkan ter
jadinya kesalahan yang lebih besar, disamping itu
pereaksi warna yang digunakan hanya stabil selama
satu jam sehingga harus selalu dibuat baru [22].
Prinsip reaksi Liebermann-Burchard menurut
metode Huang dan kawan-kawan yaitu berdasarkan sifat
kolesterol yang dapat bereaksi dengan suatu asam
kuat membentuk suatu senyawa kolestapoliena yang
berwarna hijau kebiruan. Kadar senyawa kolestapo
liena ini dapat diukur secara kolorimetri atau
spektrofotometri. Pada metode menurut Huang dan
kawan-kawan ini digunakan pereaksi Liebermann-
Burchard yang mengandung 30% asam asetat glasial, 60%
asetat anhidrida, dan 10% asam sulfat pekat [23].
Kolesterol ion. karbanium
dari 3 ,5-Dien
Asetat anhidrida SO.
Kation Pentenil max 620 nm
4.2 Penentuan Kadar Kolesterol HDL
Kolesterol HDL ditentukan dengan menggunakan
metode pengendapan selektif yaitu dengan menggunakan
heparin dan Mangan klorida. Prinsip dari metode ini
adalah : lipoprotein-lipoprotein di dalam serum
kecuali HDL diendapkan. Dua tahapan yang harus dila
kukan pada penentuan kadar kolesterol HDL yaitu tahap
Oleh karena itu faktor yang mempengaruhi metode ini
adalah tergantung pada kesempurnaan dari pengendapan
lipoprotein-lipoprotein selain HDL [24].
Metode pengendapan selektif ini berdasarkan pada
sifat lipoprotein dalam darah [selain HDL], yaitu
kemampuannya bereaksi dengan kation bervalensi dua n *
(Mn^ ) dan polianion (heparin), membentuk partikel kompleks yang tidak larut. Semakin besar molekul
polianion atau molekul lipoproteinnya, akan semakin
besar pula kecenderungan molekul-molekul tersebut
untuk bergabung menjadi partikel kompleks. Maka
, dengan jalan memilih pereaksi yang sesuai, dapat dilakukan pengendapan selektif terhadap fraksi-fraksi lipoprotein selain HDL. Untuk selanjutnya fraksi HDL
yang terlarut ditentukan kadar kolesterolnya seperti
pada penentuan kadar kolesterol total.
5. Tinjauan tentang Metode Spektrofotometri
Metode spektrofotometri adalah salah satu metode
instrumental yang didasarkan atas pengukuran serapan dari molekul terhadap sinar. Metode spektrofotometri
dapat digunakan untuk analisis kualitatif dan kuantita- tif. Jika pada panjang gelombang tertentu suatu zat
mempunyai serapan yang spesifik, maka metode ini dapat
digunakan untuk penentuan identifikasi zat tersebut. Untuk analisis kuantitatif didasarkan pada nilai sera
Pengukuran serapan biasanya dilakukan pada panjang
gelombang maksimum. Pada pengukuran serapan suatu
larutan hampir selalu digunakan blanko untuk mengatur
spekrofotometer, sehingga pada panjang gelombang pengu
kuran mempunyai serapan nol. Maksud dari blanko terse
but adalah untuk koreksi serapan yang disebabkan oleh
pelarut. pereaksi, sel ataupun pengaturan alat.
Analisis kuantitatif dengan spektrofotometer
didasarkan pada hukum Lambert-Beer, yaitu [26]:
A = a.b.c
dimana : A = serapan
a = daya serap
b = tebal medium
c = kadar senyawa yang menyerap
6. Tinjauan tentang Uji Validasi
Validasi dari suatu metode analisis adalah suatu
proses untuk meyakinkan bahwa karakteristik dari metode
memenuhi persyaratan untuk diterapkan pada analisis
yang dimaksud. Parameter validasi dari metode analisis
yang dipakai sebagai pedoman untuk pengujian mutu
adalah presisi, akurasi, sensitivitas, selektivitas,
kelurusan dan ketidakrataan [27].
Yang akan dilakukan pada penelitian ini adalah
6.1. Kelurusan dan Trayek Kelurusan
Kelurusan suatu metode analisis adalah kemam-
puan memberikan hasil uji yang secara langsung atau
melalui transformasi matematik, sebanding dengan
konsentrasi analit dalam sampel dengan rentang yang
diberikan. Linieritas suatu metode analisis diper-
oleh dengan melakukan penyelesaian matematik ter
hadap hasil-hasil analisis terhadap sampel dengan
berbagai kadar analit. Trayek kelurusan adalah jarak
dari yang terendah sampai yang tertinggi yang
masih sesuai dengan hukum yang berlaku [27].
6.2. Sensitivitas
Sensitivitas dinyatakan dengan LQD (Limit of
Detection) untuk analisis kualitatif dan LOQ (Limit
of Quantitation) untuk analisisx kuantitatif. LOD
adalah batas kadar terkecil dari arvalit (zat yang
dianalisis) dalam sampel yang masih blsa dideteksi.
LOQ adalah batas kadar terkecil dari analit dalam
sampel yang ditetapkan secara kuantitatif dengan
presisi dan akurasi yang dapat diterima [27].
6.3. Presisi
Presisi adalah suatu derajat keterulangan dari
metode analisis pada kondisi pelaksanaan yang
normal. Biasanya dinyatakan dengan simpangan baku
kecil harga prosen koefisien v&riasi maka makin
baik presisi suatu metode analisis [27].
6.4. Akurasi
Akurasi adalah kedekatan hasil yang diperoleh
dari suatu metode analisis dengan kadar yang sebe-
narnya. Biasanya dinyatakan dengan prosen perolehan
ALAT, BAHAN DAN METODE PENELITIAN BAB III
1. Bahan-bahan yang Digunakan .
- Asam askorbat/vitamin C p.a. (E. Merck)
- Kolesterol p.a. (E. Merck)
- Asam asetat glasial p.a. (E. Merck)
- Asetat anhidrida p.a. (E. Merck)
- Asam sulfat pekat p.a. (Riedel de Haen)
- Natrium sulfat anhidrat p.a. (Ferak)
- Heparin (Leo)
- Mangan klorida tetrahidrat p.a. (E. Merck)
2. Alat-alat yang Digunakan
- Spectrofotometer Hitachi dual wavelength double beam
type 557
- Fisher melting point apparatus
- Tabung pemusing
- Labu ukur
- Pipet volume
- Mikropipet
- Timbangan analitik Sartorius-Werke GMBH Type 2472
3.Cara Kerja
3.1. Analisis Kualitatif terhadap Vitamin C
3.1.1. Pemeriksaan Organoleptis
3.1.2. Reaksi Warna
- Larutan dalam air mereduksi perak nitrat dengan segera dalam keadaan dingin, menghasilkan endapan
hitam [28].
- 2 ml dari suatu larutan 2,0% ditambah 2 ml air,
0,1 g natrium bikarbonat dan kurang lebih 0,02 g
ferro sulfat, kocok dan biarkan, dihasilkan warna
deep-violet (lembayung tua), yang hilang pada
penambahan 5 ml asam sulfat encer [28].
- Larutan dalam air diberi 1 tetes larutan natrium
nitroprussid dan 3 tetes natrium hidroksida
encer, maka pada penambahan hidrogen klorida encer tetes demi tetes terjadi warna biru [293
- Dalam keadaan dingin, mereduksi larutan Fehling
dengan terbentuk endapan merah coklat sampai
jingga kuning [29],
- Larutan dalam air diberi 1 tetes larutan biru
metilen, maka lama-lama warna akan menjadi pucat bila diletakkan di tempat yang terang [29].
3.1.3. Pemeriksaan Titik Lebur
Kurang lebih 1 mg serbuk vitamin C dimasukkan dalam pipa kapiler berdinding gelas tipis dengan panjang 8 cm dan diameter 1 mm, yang salah satu
ujungnya tertutup. Bahan didorong masuk melalui
ujung pipa kapiler yang terbuka, kemudian ujung
mencapai ujungnya. Pipa kapiler ini dipasang pada
tempatnya, kemudian penangas air, dipanaskan perla- han-lahan. Ketika temperatur sekitar 15°C di bawah
titik leburnya, atur nyala api sehingga temperatur
meningkat dengan kecepatan 1-2°C per menit.
Temperatur saat bahan mulai melebur sampai melebur
sempurna disebut jarak titik lebur.
Titik lebur vitamin C adalah 190°C, diikuti dekomposisi [13, 14].
3.2. Hewan Percobaan
3.2.1. Rancangan Percobaan
heirirt percobun
( tin o U
dipuasikia s e lm
I2-H jii •
(files kolesterol to tii
din kolesterol H#L
Grnp pertata Grup kedua
Keloipok I Keloipok 11 (elotpok I I I Keloipok IV
Keterangan :
Kelompok I : makanan dasar
Kelompok II.l : makanan dasar + vitamin C dosis 1
Kelompok II.2 : makanan dasar + vitamin C dosis 2
Kelompok II.3 : makanan dasar + vitamin C dosis 3
Kelompok III : makanan dasar + kolesterol 3% 1 ml
Kelompok IV.1 : makanan dasar + kolesterol 3% 1 ml
+ vitamin C dosis 1
Kelompok IV.2 : makanan dasar + kolesterol 3% 1 ml
+ vitamin C dosis 2
Kelompok IV.3 : makanan dasar + kolesterol 3% 1 ml
+ vitamin C dosis 3
Dalam penelitian ini digunakan 40 ekor marmot
( Cavia porcellus) yang diperoleh dari Peternakan,
Jl. Raya Selecta No. 37, Batu, dengan kriteria
sebagai berikut :
- berjenis kelamin jantan
- berumur 2-3 bulan
- bobot badan 250-400 gram
- berada dalam keadaan normal dan sehat
Pada awal percobaan, 40 ekor marmot tersebut
dibagi menjadi 8 kelompok (masing-masing kelompok
5 ekor marmot) sebagai berikut :
I. Kontrol normal : hewan pecobaan diberi
makanan dasar (kangkung, ubi dan jagung).
vita-min C, yang dikelompokkan atas :
11.1. Diberi makanan dasar dan vitamin C
dosis 1.
11.2. Diberi makanan dasar dan vitamin C
dosis 2.
11.3. Diberi makanan dasar dan vitamin C
dosis 3.
III. Dengan pemberian makanan dasar dan kole
sterol 3% 1 ml.
IV. Dengan pemberian makanan dasar, koleste
rol 3% dan vitamin C, yang dikelompokkan
atas :
IV.1. Diberi makanan dasar, kolesterol 3%
1 ml dan vitamin C dosis 1.
IV.2. Diberi makanan dasar, kolesterol 3%
1 ml dan vitamin C dosis 2.
IV.3. Diberi makanan dasar, kolesterol 3%
1 ml dan vitamin C dosis 3.
Kolesterol diberikan dalam bentuk suspensi
dengan 0.5% akasia sebagai bahan pensuspensi.
Vitamin C diberikan dalam bentuk larutan yang
selalu dibuat baru.
Masing-masing marmot diperlakukan selama se-
bulan sesuai dengan kelompok dengan pemberian
secara per oral. Pada awal sebelum penelitian
terle-bih dahulu marmot dipuasakan selama 12-14 jam.
Pada akhir penelitian juga diambil sampel darah.
3.2.2. Pemilihan Dosis
Dosis bahan penelitian yang digunakan merupakan
dosis untuk manusia yang dikonversikan pada bina-
tang percobaan. Nilai konversi dosis manusia terha dap marmot 400 g adalah 0,031 [31]. Pada penelitian
ini digunakan dosis 500 mg, 1 g dan 1,5 g.
Dosis setara 500 mg = (500 mg x 0,031) : 400 g
= 0,039 mg/g BB marmot
Dengan cara yang sama, untuk dosis yang setara
dengan 1 g dan 1,5 g diperoleh 0,078 mg/g BB marmot dan 0,116 mg/g BB marmot.
4. Uji Validasi
4.1. Kelurusan
Kelurusan didapatkan dari perhitungan persamaan garis regresi.
n. Zxy - (2x) (Zy)
r = ---^n.Zx2 - (Zx)a ) (n.2y2~ (SyT2 )'
di mana : r = koefisien korelasi
x = kadar zat dalam larutan y = serapan yang terbaca
Persamaan garis : Y = bX + a
n.Sxy - Zx.Zy b =
---n.Zx2 - (Zx)2
4.2. Sensitivitas [27]
Untuk analisis instrumental harga LOD ditentukan
dengan cara menganalisa sejumlah sampel blanko dan
menghitung simpangan baku dari hasil yang didapatkan.
Simpangan baku ini dikalikan dengan suatu faktor,
biasanya 2 atau 3, menghasilkan perkiraan dari LOD.
Untuk penentuan harga LOQ, simpangan baku ini
dikalikan dengan 10.
4.3. Presisi
Harga presisi didapatkan berdasarkan perban-
dingan s dengan x atau dengan prosen koefisien
variasi.
s
% KV = — — . 100
x
s = /Z(x-x )2
n-1
Keterangan : x = kadar sampel
x = kadar sampel rata-rata
n = jumlah sampel
4.4. Akurasi
Akurasi metode ini dinyatakan dalam prosen
perolehan kembali (% Recovery) dengan persamaan :
% Recovery = --- . 100
CA + CB
dimana : = kadar sampel mula-mula
Cg = kadar larutan baku yang ditambahkan
Cjr = kadar sampel setelah penambahan larutan
baku
5. Pembuatan Kurva Baku
Pada penelitian ini diperlukan larutan baku induk
dan beberapa larutan baku kerja. Larutan baku induk
dibuat dengan kadar 5000,0 ppm dengan pembuatan sebagai
berikut :
- Ditimbang dengan seksama 250,0 mg kolesterol dimasuk-
k.an ke dalam labu ukur 50 ml, kemudian ditambah
dengan asam asetat glasial sampai garis tanda dan
dikocok sampai homogen.
- Larutan baku kerja dibuat dari pengenceran larutan
baku induk, sehingga didapatkan beberapa maeam kadar
yaitu 200,0 ppm; 400,0 ppm; 500,0 ppm: 1000,0 ppm;
5.1. Pemilihan Panjang Gelombang Maksimum
Pada pemilihan panjang gelombang maksimum meng
gunakan dua macam larutan baku kerja. Pelaksanaannya
sebagai berikut :
- Dipipet 0,2 ml larutan baku kerja dimasukkan ke
dalam tabung reaksi yang berisi pereaksi warna
Liebermann-Burchard yang sebelumnya tabung direndam
dalam air es, kemudian dikocok sampai homogen dan dibiarkan 30 menit pada suhu kamar, dimasukkan ke
dalam kuvet dan dibaca serapannya, dicari panjang
gelombang maksimum dengan alat spektrofotometer.
Sebagai titik nol -digunakan blanko aquadest ditam- bah pereaksi warna Liebermann-Burchard yang selan-
jutnya diperlakukan sama dengan larutan baku kerja
kolesterol.
5.2. Pembuatan Kurva Baku
Kurva baku dibuat dari larutan baku kerja
kolesterol dalam asam asetat glasial dengan kadar
200,0 ppm; 400.0 ppm; 500,0 ppm; 1000,0 ppm; 1500,0
ppm; 2500,0 ppm; 3000,0 ppm; 4000,0 ppm dan 5000,0 ppm. Masing-masing larutan baku kerja tersebut dire- aksikan seperti pada (5.1) dan dibaca serapannya pada
panjang gelombang maksimum yang didapat dari perco-
baaan (5.1). Dari data akan diperoleh persamaan garis
Liebermann Burchard, yang selanjutnya diperlakukan
sama dengan larutan baku kerja kolesterol.
6. Pengambilan Sampel Darah
Sebelum dilakukan pengambilan sampel darah, marmot
yang akan diambil darahnya dipuasakan selama 12-14 jam
sebelumnya. Masing-masing marmot yang akan diambil
darahnya secara intrakardial dianestesi dengan inhalasi
eter (Aether anaestheticus) dengan diperkirakan terca-
painya irama pernapasan yang teratur. Setelah marmot
ditelentangkan dengan posisi dada di depan, kemudian
diraba bagian jantung yang memberikan denyut terkuat.
Dengan menggunakan spuit disposable darah diambil
sebanyak 3 m l , kemudian darah dipindahkan ke dalam
tabung pemusing tanpa antikoagulan. Darah yang terkum-
pul dibiarkan selama 30 menit pada suhu kamar dan
kemudian dipusingkan selama 20 menit, sehingga serumnya
terpisah. Serum yang telah terpisah ini dimasukkan ke
daiam botol yang tertutup rapat, selanjutnya dilakukan
penentuan kadar [33].
7. Penentuan Kadar
7-1. Penentuan Kadar Kolesterol Total Serum
Kadar kolesterol total serum ditentukan menurut
metode Huang dan kawan-kawan dengan menggunakan
satu pereaksi warna yang dibuat dengan cara sebagai
berikut :
Ke dalam bejana yang direndam dalam air es, di
masukkan asam asetat glasial p.a., asetat anhi
drida p.a., asam sulfat pekat p.a. dengan per-
bandingan 3:6:1, dicampur sampai homogen. Kemu
dian ditambahkan ke dalamnya 2% Natrium sulfat
anhidrat p.a., kemudian dikocok sampai
homogen.
Penentuan kadar kolesterol total serum dilakukan
dengan cara sebagai berikut :
Ke dalam tabung-tabung reaksi yang berisi 5 ml
pereaksi Liebermann-Burchard (sebelumnya tabung
direndam dalam air es), dimasukkan dengan hati-
hati masing-masing 0,2 ml serum. Untuk larutan
blanko digunakan aquadest ditambah pereaksi
Liebermann-Burchard. Campuran dikocok sampai
tercampur merata, kemudian dibiarkan 30 menit
pada suhu kamar. Serapan dari masing-masing
larutan tersebut dibaca dalam waktu tidak lebih
10 menit pada panjang gelombang maksimum yang
terpilih, dengan menggunakan alat spektrofotome-
ter [23].
Perhitungan :
Untuk menghitung kadar kolesterol total, diguna
percobaan (5.2).
Catatan :
Sebelum hewan percobaan mengalami perlakuan,
maka dilakukan dulu penentuan kadar kolesterol
total dan kolesterol HDL serum sebagai pem-
banding,
7.2. Penentuan Kadar Kolesterol HDL Serum
Untuk penentuan kadar kolesterol HDL serum,
terlebih dahulu dilakukan teknik pengendapan selektif menggunakan pereaksi heparin dan Mangan klorida.
Pengendapan selektif ini berdasarkan sifat lipopro
tein, yaitu kemampuannya untuk bereaksi dengan kation
bervalensi dua (Mn^+ ) dan polianion (heparin). Pada
proses ini lipoprotein-lipoprotein yang terdapat
dalam serum akan diendapkan, kecuali HDL, kemudian
serum yang mengandung HDL ini ditentukan kadar
kolesterol HDL-nya .
Pada penentuan kadar kolesterol HDL ini, serum
yang digunakan adalah serum yang diambil dari hewan percobaan yang telah dipuasakan sebelumnya selama 12 14 jam. Pelaksanaan penentuan kadar kolesterol HDL
serum adalah sebagai berikut :
Sebanyak 1 ml serum dimasukkan ke dalam tabung
pemusing, kemudian ditambahkan berturut-turut larutan heparin 5000 unit/ml sebanyak 40 nl, dan
50 nl. Campuran dikocok sampai homogen dan di-
diamkan 30 menit pada suhu kamar. Setelah 30 menit, larutan disentrifugasi selama 20 menit,
kemudian supernatannya dipisahkan. Bila superna-
tan masih kelihatan keruh berarti pengendapan
kurang sempurna, maka harus direaksikan lagi
sampai pengendapan sempurna. Supernatan dipipet 0,2 ml dimasukkan ke dalam tabung reaksi yang
berisi 5 ml pereaksi warna Liebermann-Burchard,
yang sebelumnya tabung direndam dulu dalam air
es. Selanjutnya kadar kolesterol HDL ditentukan
sama seperti pada penentuan kadar kolesterol total serum [23].
8. Analisis data
I II III IV
X Y X Y X Y X Y
X 11 Y 11 X 12 Y 12 X 13 Y 13 X 14 Y 14
X21 Y21 X22 Y22 X23 Y23 X24 Y24
X31 Y31 X32 Y32 X33 Y33 X34 Y 34
X41 Y41 X42 Y42 X43 Y43 X44 Y 44
X 51 Y51 X52 Y52 X53 Y53 X54 Y54
Total 2X ZY ZX 2Y 2X ZY SX 2Y
Rata^ X Y X Y X Y X Y
I, II, III, IV = kelompok
X = kadar kolesterol total atau kolesterol
sebelum perlakuan
Y = kadar kolesterol total atau kolesterol
* setelah perlakuan
i = kolom 1, 2, ..., t
j = baris 1. 2, ..., n
HDL
Tabel Anakova Pro CRD
kelompok t-1 Txx Txy Tyy
Dalam
kelompok N-t Exx Exy Eyy SE N-t-1
SE
db = derajat bebas
JK = Jumlah kuadrat
JKS = Jumlah kuadrat sisa
Sxx = koreksi jumlah total kuadrat dari X
Sxy = koreksi jumlah total hasil dari X dan Y
t n t n
Syy = koreksi jumlah total kuadrat dari Y
t n
Txx = perlakuan jumlah kuadrat dari X
Txy = perlakuan jumlah hasil dari X dan Y
Tyy = perlakuan jumlah kuadrat dari Y
t n t n
mengetahui apakah perbedaan yang terjadi itu bermakna
atau tidak. dilakukan uji HSD (Honestly Significant
Difference).
HSD “ q a,k,N - k.\ /RJiT
Jika beda mean > HSD, berarti ada beda yang ber-
makna dan jika beda mean < HSD, berarti tidak ada beda
BAB IV
HASIL PERCOBAAN
1. Analisis sifat fisika kimia vitamin C
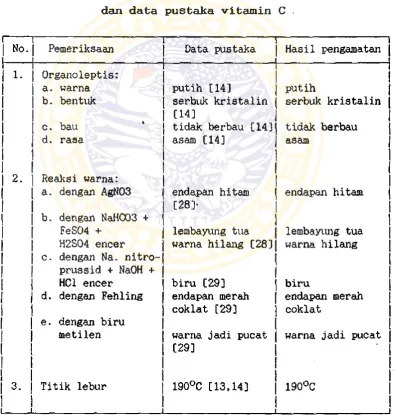
Hasil pemeriksaan sifat fisika kimia dan data
pustaka vitamin C dapat dilihat pada tabel II.
Tabel II. Hasil pemeriksaan sifat fisika kimia
dan data pustaka vitamin C
T T
T No. j
1 Pemeriksaan ij Data pustaka j Hasil pengamatan j
t
1. jOrganoleptis: t1
1 a. warna putih [14] j putih j
I b. bentuk serbuk kristalin j serbuk kristalin j
1 . | [14] j
1 c. ban tidak berbau [14]j tidak berbau j
1
t H2S04 encer | warna hilang [28]j warna hilang j
t c. dengan Na. nitro-j 1
1
prussid + NaOH + |
HC1 encer j biru [29] j biru
1 d. dengan Fehling | endapan merah endapan merah 1
1
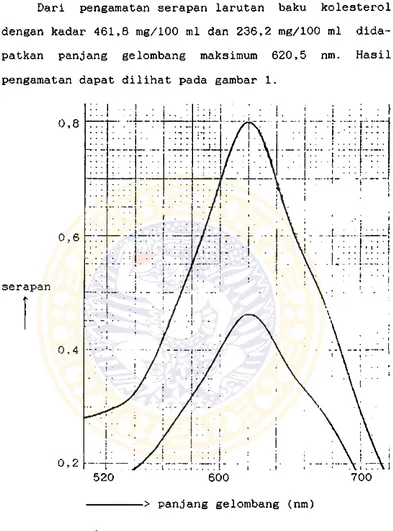
2. Penentuan panjang gelombang maksimum
Dari pengamatan serapan larutan baku kolesterol
dengan kadar 461,8 mg/100 ml dan 236,2 mg/100 ml dida-
patkan panjang gelombang maksimum 620,5 nm. Hasil
pengamatan dapat dilihat pada gambar 1.
> panjang gelombang (nm)
Gambar 1. Penentuan panjang gelombang maksimum
larutan baku kolesterol dengan kadar
3. UJI VALIDASI
3.1. Kelurusan
Kelurusan ditentukan untuk mengetahui adanya
korelasi linier antara kadar zat yang dianalisis
dengan serapan yang diberikan.
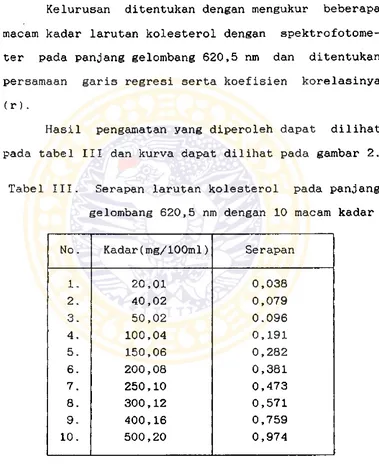
Kelurusan ditentukan dengan mengukur beberapa
macam kadar larutan kolesterol dengan spektrofotome- ter pada panjang gelombang 620,5 nm dan ditentukan
persamaan garis regresi serta koefisien korelasinya
(r).
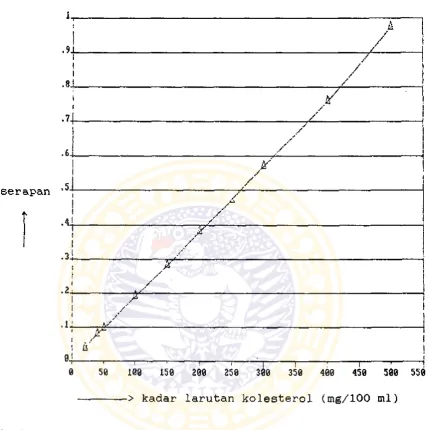
Hasil pengamatan yang diperoleh dapat dilihat
pada tabel III dan kurva dapat dilihat pada gambar 2.
Tabel III. Serapan larutan kolesterol pada panjang gelombang 620,5 nm dengan 10 macam kadar
No. Kadar(mg/lOOml) Serapan
1- 20,01 0,038
2. 40,02 0,079
3. 50,02 0.096
4. 100,04 0,191
5. 150,06 0,282
6. 200,08 0,381
7. 250,10 0,473
8. 300,12 0,571
9. 400,16 0,759
,9J
/
t/
serapan .6-J
.5.
.4j
1
•
■'+-.2^
X /
.1
---,---,--- ,--- ,--- ---!---- 1---- ;---- 1---- 1---- f
0 50 100 150 230 250 300 350 400 450 500 550
--- > kadar larutan kolesterol (mg/100 ml)
Gambar 2. Kurva serapan terhadap kadar larutan kolesterol
Dari hasil perhitungan didapatkan persamaan
garis y = 1,9264.10~^x - 2,9612.10“^, dengan harga
koefisien korelasi (r) = 0,9998. Dari tabel koefisien
korelasi diketahui bahwa pada derajat kebebasan (f)
10 dengan derajat kepercayaan 0,05, diperoleh harga r
tabel = 0,632 berarti harga r hitung lebih besar dari
harga r tabel yang menunjukkan adanya korelasi linier
antara' kadar dengan serapan yang diberikan. Hasil
perhitungan dapat dilihat pada lampiran 1.
3.2. Sensitivitas
Harga LOD dan LOQ ditentukan dengan cara mengu-
kur serapan blanko sebanyak 10 kali, kemudian diukur
simpangan bakunya. Untuk penentuan LOD simpangan baku
ini dikalikan dengan 3 , kemudian hasilnya dimasukkan
pada persamaan kurva baku, sehingga didapatkan kadar
terkecil yang dapat terdeteksi. Untuk penentuan LOQ,
simpangan baku dikalikan dengan 10. Cara perhi-
tungannya sama dengan penentuan LOD.
Hasil pengamatan serapan blanko dapat dilihat
Tabel IV
Hasil pengamatan serapan blanko
No Serapan
1. 0,007
2. 0,010
3. 0,006
4. 0,008
5. 0,006
6. 0,009
7. 0,011
8. 0,010
9. 0,018
10. 0,006
Dari hasil perhitungan didapatkan harga LOD
adalah 2,44 mg/100 ml, dan harga LOQ adalah
4,55 mg/100 ml.
3.3. Presisi
Presisi ditentukan untuk mengetahui derajat
kinerulangan dari metode analisis pada kondisi pelak- sanaan yang normal. Harga presisi didapatkan berda-
sarkan perbandingan s dan x atau dengan prosen koefi-
sien variasi. Harga presisi ini didapatkan dengan
inengamati serapan larutan kolesterol pada kadar
358,08 mg/lOOml sebanyak 10 kali. Hasil pengamatan
-Tabel V. Penentuan presisi
No. Kadar(mg/lOOml) ( x - x ) ( x - x ) 2
1 . 354,53 -2,80 7,8400
2. 356,60 -0,73 0,5329
3. 358,68 1,35 1,8225
4. 360,24 2,91 8,4681
5. 358,68 1,35 1,8225
6. 355,57 -1,76 3,0976
7. 358,68 1,35 1,8225
8. 357,64 0,31 0,0961
9. 357,64 0,31 0,0961
10. 355,05 -2,28 5,1984
M II O x = 357,33 2=30,7967
Perhitungan :
= 1,8498
s
% KV = --- x 100% x
1,8498
= --- x 100% 357,33
3.4. Akurasi
Akurasi diperoleh berdasarkan perbandingan
antara kadar sampel terhitung dengan kadar sampel
yang sebenarnya atau dinyatakan dengan prosen perole-
han kembali (% Recovery) dengan persamaan :
Cx
% Recovery = --- x 100% Ca + Cb
di mana : Cx = kadar terukur
Ca = kadar sampel mula-mula
Cb = kadar larutan baku yang ditambahkan
Hasil pengamatan dapat dilihat pada tabel VI
Tabel VI. Penentuan akurasi
Ca Cb Ca+Cb Cx % Recovery
62.27
Rata-rata = 99,88%
Dari hasil pengamatan didapatkan prosen recovery
rata-rata 99,88%. Prosen recovery yang memenuhi
syarat adalah 90-110% [37]. Berarti metode yang
4. Hasil pemeriksaan kadar kolesterol total serum
Pemeriksaan kadar kolesterol total serum marmot
dibagi menjadi 8 kelompok, yaitu : .
Kelompok I : makanan dasar rkontrol normal)
Kelompok II. 1 : makanan dasar + vitamin C dosis■ 1
Kelompok II. 2 : makanan dasar + vitamin C dosis 2
Kelompok II. 3 : makanan dasar + vitamin C dosis. 3
Kelompok Ill : makanan dasar + kolesterol 3% 1 ml
Kelompok IV. 1 : makanan dasar + kolesterol 3% 1 ml
Hasil pemeriksaan kadar kolesterol total serum
marmot dapat dilihat pada tabel VII.
Tabel VII
Hasil pemeriksaan kadar kolesterol total serum marmot
Keterangan :
X = kadar kolesterol total serum marmot sebelum
perlakuan (mg/lOOml)
Y = . kadar kolesterol total serum marmot setelah
perlakuan (mg/lOOml)
Hasil pengamatan tersebut diolah secara statistik
dengan uji analisis kovarians (Anakova) yang tertera
pada lampiran 3, dengan a = 0,05.
* Uji Anakova untuk mengetahui apakah ada perbedaan di
antara kelompok I, II.1, II.2, II.3, dalam hal kole
sterol total [34, 38].
Dari hasil perhitungan dengan Anakova didapatkan :
Fhitung = 4,56 ; derajat bebas v-^ = 3
v2 = 15
Ftabel (a = 05) = 3,29
Fhitung > Ftabel’ Pada a = °'05
4.56 > 3,29
Maka H^ diterima dan Hq ditolak, hal ini berarti
bahwa ada perbedaan efek di antara kelompok-kelompok
tersebut dalam hal kadar kolesterol total. Untuk
mengetahui apakah perbedaan tersebut bermakna atau
tidak, maka dilakukan uji HSD. Hasil uji HSD dapat
Tabel VIII
Hasil uji HSD pemeriksaan kadar kolesterol total
serum marmot kelompok I, II.l, II.2 dan II.3
XI XII. 1 XI1.2 XII .3
XI - 4,36 6,02 7,27
xII.l - - 1,66 2,91
XII .2 - - - 1,25
XI1.3 - - -
-Keterangan :
X = selisih kadar kolesterol rata-rata setelah
dan sebelum perlakuan (mg/lOOml)
q = harga tabel pada a = 0,05, dengan derajat
bebas k dan N-k
RJK = rata-rata jumlah kuadrat (dalam perlakuan)
Harga HSD yang didapat 2,28 ; hal ini berarti :
- terdapat perbedaan bermakna antara kelompok II.l, II.2 dan II.3 bila dibandingkan dengan kelompok I (kontrol)
- tidak ada perbedaan bermakna antara kelompok
11.2 bila dibandingkan dengan kelompok II. 1, juga
antara kelompok II.3 bila dibandingkan dengan
kelompok II.2
* Uji Anakova untuk mengetahui apakah efek yang terjadi
setelah perlakuan dipengaruhi oleh kadar kolesterol
total sebelum perlakuan [34, 38].
Dari hasil perhitungan dengan anakova didapatkan :
^hitung = 2866,40; deraj at bebas = 1
v2 = 15
Ftabel = ° ’05 ) = 4 >54
^hitung ^ Ftabel’ Pa(^a a - 0,05 2866,40 > 4,54
Maka diterima dan Hq ditolak, hal ini berarti ada
pengaruh kadar kolesterol total sebelum perlakuan
dengan efek yang ditimbulkan setelah perlakuan.
* LJj i Anakova untuk mengetahui apakah ada perbedaan di
antara kelompok III, IV.1, IV.2, IV.3, dalam hal
kolesterol total [34, 38].
Dari hasil perhitungan dengan Anakova didapatkan :
Fhitung = 8 >92 ; deraj at bebas = 3
v2 = 15
Ftabel (a = °?05) = 3>29
Maka diterima dan Hq ditolak, hal ini berarti ada
perbedaan efek di antara kelompok-kelompok tersebut
dalam hal kadar kolesterol total.
Untuk mengetahui apakah perbedaan tersebut bermakna
atau tidak, maka dilakukan uji HSD. Hasil uji HSD
dapat dilihat pada tabel IX.
j RJK '
HSD = q a,k,N-k\ /----V n
= 7 , 1 4
Tabel IX
Hasil uji HSD pemeriksaan kadar kolesterol total
serum marmot kelompok III, IV.1, IV.2 dan IV.3
X I 1 1 i—i > i—1
X
X I V . 2 X I V . 3
X I 1 1 - 7,88 9 , 5 5 12,04
XIV.l - - 1,67 4,16
X IV.2 - - - 2 , 4 9
X I V . 3 - - -
-Keterangan :
X = selisih kadar kolesterol rata-rata setelah
<3 = harga tabel pada a = 0,05, dengan derajat
bebas k dan N-k
RJK = rata-rata jumlah kuadrat (dalam perlakuan)
Harga HSD yang didapat 7,14 ; hal ini berarti :
- terdapat perbedaan bermakna antara kelompok IV.1,
IV.2 dan IV.3 bila dibandingkan dengan kelompok
III (kontrol).
- tidak ada perbedaan bermakna antara kelompok IV.1,
IV.2 dan IV.3 bila saling dibandingkan.
* Uji Anakova untuk mengetahui apakah efek yang terjadi
setelah perlakuan dipengaruhi oleh kadar kolesterol
total sebelum perlakuan [34, 38]
Dari hasil perhitungan dengan anakova didapatkan :
FhitUng = 621,18 ; derajat bebas v^ = 1
' v2 = 15
F t a bel “ 0,05 ) = 4,54
^hitung Ftabel’ Pac^a a = 0,05
621,18 >4,54
Maka diterima dan Hq ditolak, hal ini berarti ada
pengaruh kadar kolesterol total sebelum perlakuan
dengan efek yang ditimbulkan setelah perlakuan.
5. Hasil pemeriksaan kolesterol HDL serum
Pemeriksaan kadar kolesterol HDL serum marmot
Hasil pemeriksaan kadar kolesterol HDL serum
marmot dapat dilihat pada tabel X.
Tabel X
Hasil pemeriksaan kadar kolesterol HDL serum marmot
i I I . 1 I I . 2 I I . 3 I l l I V . l I V . 2 I V .3
X T K Y K r X r >! r X r X r X f
5 7 ,6 0 58,12 52,41 54 ,4 ? ( 4 , 4 3 70,58 50 ,3 3 5 5 ,0 0 9 7 ,5 7 9 3 ,9 4 ? ? ,6 5 101,72 9 1 ,8 6 9 9 ,6 5 7 5 ,2 5 8 9 , 7B B l , 4 8 8 0 ,4 4 73,4? 70,06 2 3 ,3 4 25,94 25 ,4 2 3 1 ,1 3 9 2 ,9 0 87 ,7 1 22 ,3 0 27 ,4 9 8 0 ,9 6 ? 1 ,3 4 74,21 85,63 58 ,1 2 41,75 51,37 50,33 59,68 43,83 4 7 ,9 8 80,96 21,26 29 ,0 5 19,71 23 ,8 6 86,67 ? 3 ,4 2 45,66 51,37 3 3 ,7 2 29 ,0 5 2 7 ,4 ? 3 1 ,4 5 38 , ?1 41,51 67 ,4 4 7 1 ,1 0 3 0 ,0 ? 2B,53 72 ,4 5 7 9 ,9 2 69 ,5 4 7 5 ,7 7 7 9 ,4 0 9 3 ,4 2 2 1 ,2 4 23 ,3 4 8 1 ,4 8 85,11 52, ?3 57 ,0 8 3 3 ,2 0 3 5 ,2 8 5 ? ,1 6 40 ,7 1 96 ,5 3 10 6,40 2 7 ,4 9 3 4 ,2 4 8 1 ,4 8 8 9 ,2 7
1= 2 5 2 ,1 8 252,70 286,44 291,44 2 4 1,2? 2 5 8 ,?4 244,3? 273,47 3 0 0,98 299,94 310,84 33? ,39 3 5 6,52 394,42 354,00 409,47
r = 5 0 ,4 4 50,54 57,29 58 ,3 3 4 8 ,2 4 51 ,7 ? 4 8 ,8 8 5 4 ,4 ? 4 0 ,2 0 5 9 ,9 ? 42 ,1 7 4 7 ,8 8 7 1 ,3 0 7 8 ,8 8 7 1 ,2 0 8 1 ,8 9
Keterangan :
X = kadar kolesterol HDL serum marmot sebelum
perlakuan (mg/lOOml)
Y = kadar kolesterol HDL serum marmot setelah
perlakuan (mg/lOOml)
Hasil pengamatan tersebut diolah secara statistik
dengan uji analisis kovarians (Anakova) yang tertera
pada lampiran 4, dengan a = 0,05.
* Uji Anakova untuk mengetahui apakah ada perbedaan di
antara kelompok I, II.1, II.2, II.3, dalam hal kole
Dari hasil perhitungan dengan Anakova didapatkan :
Fhitung “ 3,26 ; derajat bebas v^ = 3
v2 = 15
F tabel = - 3,29
Fhitung < Ftabel’ Pada a = ° ’05
3,26 < 3,29
Maka Hq diterima dan ditolak, hal ini berarti
bahwa ada perbedaan efek di antara kelompok-kelompok
tersebut dalam hal kadar kolesterol HDL. Oleh karena
itu tidak perlu dilakukan uji HSD.
* Uji Anakova untuk mengetahui apakah efek yang terjadi
setelah perlakuan dipengaruhi oleh kadar kolesterol
HDL sebelum perlakuan [34, 38]
Dari hasil perhitungan dengan anakova didapatkan :
Fhitung = 674,47 ; derajat bebas v^ = 1 v2 = 15
Ftabel (a = ° ’05 } = 4 ’54
Fhitung > Ftabel’ Pada a = ° ’05 674,47 > 4,54
Maka H ^ diterima dan Hq ditolak, hal ini berarti ada
pengaruh kadar kolesterol HDL sebelum perlakuan
dengan efek yang ditimbulkan setelah perlakuan.
* Uji Anakova untuk mengetahui apakah ada perbedaan di
antara kelompok III, IV.1, IV.2, IV.3, dalam hal