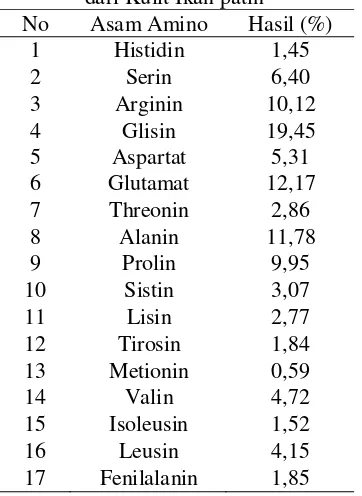
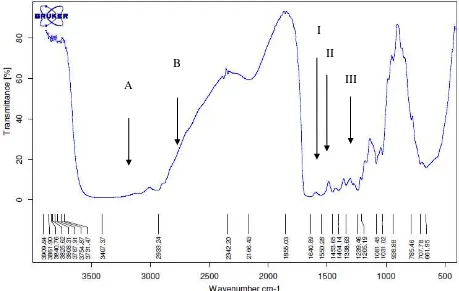
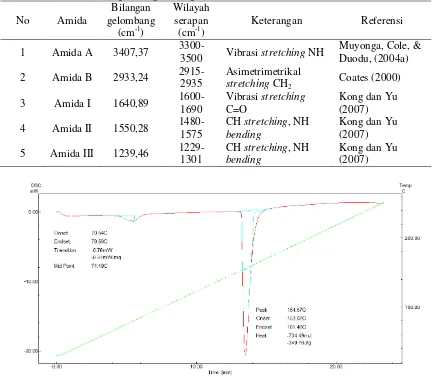
ISOLASI DAN KARAKTERISASI KOLAGEN DARI KULIT IKAN PATIN (Pangasius sp.)
Teks penuh
Gambar
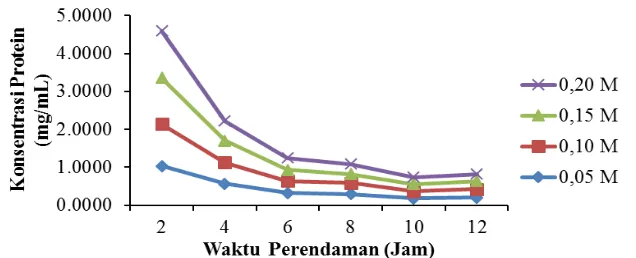
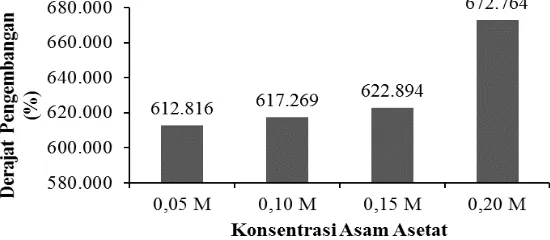
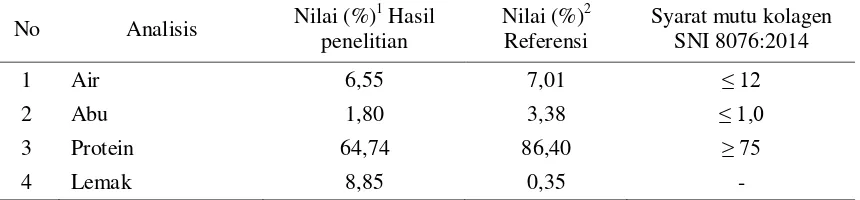
Dokumen terkait
Pekerja tetap adalah orang yang bekerja pada perusahaan/usaha dengan menerima upah/gaji secara tetap, tidak tergantung pada absensi/kehadiran pekerja tersebut dan biasanya
Publikasi ini merupakan publikasi rutin yang diterbitkan tiap tahun oleh Koordinator Statistik Kecamatan (KSK) Wanasalam.. Publikasi ini berisi gambaran umum
Dari pernyataan tersebut dapat dilihat bahwa manusia menciptakan interaksi baru tanpa harus bertemu fisik yang salah satunya melalui internet ( social networking
adiknya, Sidang Menanti, memperlihatkan ciri kepemimpinan yang adil dan damai dalam menjalankan roda pemerintahan. Model kepemimpinan mereka mengutamakan harmoni
Jenis penelitian ini adalah penelitian eksperimen yang bertujuan untuk mengetahui pengaruh jenis pelarut terhadap perubahan warna dan lama penyimpanan kertas
Sampai saat ini, belum banyak penelitian yang dilakukan untuk mengkaji efektifitas tanaman naungan dalam hubungannya dengan besarnya sumbangan bahan organik dari
Dari proses penelitian konsolidasi tanah organik melalui variasi pemadatan tanah dengan sampel kadar air optimum, kering dan basah maka nilai yang didapat dari perilaku