UJI AKTIVITAS ANTIOKSIDAN MENGGUNAKAN RADIKAL 1,1-DIFENIL-2-PIKRILHIDRAZIL (DPPH) DAN PENETAPAN KANDUNGAN FENOLIK TOTAL FRAKSI ETIL ASETAT EKSTRAK
ETANOL DAUN TRENGGULI (Cassia fistula L.)
SKRIPSI
Diajukan Sebagai Salah Satu Syarat Mendapat Gelar Sarjana Farmasi (S.Farm.)
Diajukan oleh :
Anthony Felix
NIM: 098114021
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
UJI AKTIVITAS ANTIOKSIDAN MENGGUNAKAN RADIKAL 1,1-DIFENIL-2-PIKRILHIDRAZIL (DPPH) DAN PENETAPAN KANDUNGAN FENOLIK TOTAL FRAKSI ETIL ASETAT EKSTRAK
ETANOL DAUN TRENGGULI (Cassia fistula L.)
SKRIPSI
Diajukan Sebagai Salah Satu Syarat Mendapat Gelar Sarjana Farmasi (S.Farm.)
Diajukan oleh :
Anthony Felix
NIM: 098114021
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
DENGAN SYUKUR SEBESAR-BESARNYA KEPADA
TUHAN YANG MAHA ESA. KARYA INI SAYA
vii
PRAKATA
Puji syukur kami panjatkan ke hadirat Allah yang telah memberikan rahmat
serta karunia-nya kepada penulis sehingga penulis berhasil menyelesaikan skripsi
yang berjudul ”Uji Aktivitas Antioksidan Menggunakan Radikal 1,1-Difenil-2-Pikrilhidrazil (DPPH) dan Penetapan Kandungan Fenolik Total Fraksi Etil Asetat Ekstrak Etanol Daun Trengguli (Cassia Fistula L.)
Skripsiini dibuat sebagai tugas akhir yang menjadi syarat kelulusan wajib
untuk mendapatkan gelar Sarjana Farmasi (S,Farm). Penulis menyusun skripsi ini
dalam jangka waktu yang cukup panjang melalui penelitian dan pengamatan yang
dilakukan sendiri bersama teman-tema satu tim dan juga di bawah bimbingan dosen
pembimbing skripsi,
Penulis ingin menyampaikan terima kasih kepada:
1. Ipang Djunarko, M.Sc., Apt., selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma
2. Prof. Dr.C.J. Soegihardjo, Apt.,selaku Dosen Pembimbing yang telah
memberikan bimbingan selama pengusulan skripsi, saat penelitian dan
selama penulisan skripsi dengan kesabaran dan penuh perhatian.
3. Yohanes Dwiatmaka, M.Si.,selaku Dosen Penguji yang memberikan
viii
4. Dra. M.M.Yetty Tjandrawati, M.Si., selaku Dosen Penguji yang
memberikan banyak masukkan demi terselesaikannya karya tulis skripsi
ini.
5. Segenap laboran Laboratorium Farmakognosi-Fitokimia (Mas Wagiran)
dan Laboratorium Farmasi Fisika (Mas Agung) atas segala bantuan
selama penulis melakukan penelitian di laboratorium Laboratorium
Farmakognosi-Fitokimia dan Farmasi Fisika.
6. Teman-teman satu kelompok antioksidan Aldo Christian, Mikhael
Gustandy, Willigis Danu Patria yang mendukung selama penelitian dan
penulisan skripsi ini.
7. Teman- teman satu kos yang sering memberikan kritik dan saran (Is
Sumitro, Oei Johanes, Fendy).
8. Teman-teman kelas 2009 A bantuannya yang tidak dapat penulis sebutkan
satu persatu.
Penulis menyadari,masih banyak kesalahan dan kekurangan dalam penulisan
skripsi ini,Oleh sebab itu penulis sangat mengharapkan bantuan dan masukkan untuk
membuat laporan skripsi ini menjadi bermanfaat.
Yogyakarta,12 Maret 2013
ix
DAFTAR ISI
JUDUL ... i
LEMBAR PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERSETUJUAN PUBLIKASI KARYA ... vi
KATA PENGANTAR ... vii
BAB II. PENELAAHAN PUSTAKA ... 5
x
B. Kandungan Fenolik Total ... 6
C. Antioksidan…………. ... 7
D. Metode 1,1-difenil-2-pikrilhidrazil (DPPH) ... 8
E. Metode Folin Ciocalteu ... 10
F. Spektrofotometri Visibel ... 11
G. Pembuatan Simplisia dan Ekstraksi ... 11
H. Validasi Metode Analisis ... 12
1. Linearitas ... 13
2. Presisi ... 14
3. Spesifisitas ... 15
I. Analisis Statistika.. ... 15
J. Landasan Teori………. ... 16
K. Hipotesis……….. ... 18
BAB III. METODE PENELITIAN ... 19
A. Jenis dan Rancangan Penelitian ... 19
B. Variabel Penelitian ... 19
C. Definisi Operasional ... 19
D. Bahan dan Alat Penelitian ... 20
1. Bahan ... 20
2. Alat ... 20
E. Tata Cara Penelitian ... 21
1. Determinasi tanaman ... 21
xi
3. Preparasi sampel ... 21
4. Pembuatan fraksi etil asetat ... 22
5. Pembuatan Larutan DPPH, baku pembanding, larutan uji ... 22
6. Uji pendahuluan ... 23
7. Optimasi uji daya antioksidan ... 23
8. Penentuan aktivitas antioksidan ... 24
9. Optimasi penentuan fenolik total ... 25
10. Penetapan kadar fenolik total... 25
11. Analisis hasil ... 26
BAB IV. PEMBAHASAN ... 28
A. Determinasi Tanaman Trengguli ... 28
B. Pengumpulan Bahan ... 28
C. Hasil Ekstraksi ... 30
D. Hasil Fraksinasi …. ... 33
E. Uji Pendahuluan……… ... 34
1. Hasil uji kualitatif antioksidan ... 34
2. Hasil uji kualitatif fenolik ... 35
F. Optimasi Metode Pengukuran Aktivitas Antioksidan ... 36
G. Validasi Metode Pengukuran Aktivitas Antioksidan ... 39
1. Linearitas ... 40
2. Presisi ... 41
3. Spesifisitas ... 43
xii
I. Optimasi Pengukuran Fenolik Total ... 50
1. Hasil pengukuran Operating Time ... 50
2. Hasil pengukuran panjang gelombang maksimum ... 51
J. Validasi Metode Penetapan Fenolik Total ... 52
1. Linearitas ... 52
2. Presisi ... 53
3. Spesifisitas ... 54
K. Hasil Pengukuran Fenolik Total ... 54
BAB V.KESIMPULAN DAN SARAN ... 57
A. Kesimpulan………. ... 57
xiii
DAFTAR TABEL
Tabel I. Nilai CV yang dapat diterima menurut Kingston (2004) ... 15
Tabel II. Hasil pengukuran λ max DPPH ... 37
Tabel III. Hasil CV dari sampel bahan baku pembanding ... 42
Tabel IV. Hasil CV dari sampel fraksi etil asetat ekstrak etanol ... 42
Tabel V. Hasil perolehan IC dan persamaan regresi linier baku pembanding ... 46
Tabel VI. Pengukuran IC50 kuersetin ... 46
Tabel VII. Hasil pengukuran seri fraksi etil asetat ekstrak etanol ... 47
Tabel VIII. Hasil Pengukuran IC50 fraksi uj ... 47
Tabel XI. Hasil CV kurva asam galat ... 53
Tabel XII. Hasil pengukuran larutan seri asam galat ... 55
xiv
DAFTAR GAMBAR
Gambar 1.a. Kuersetin, b. Struktur inti flavonoid. ... 7
Gambar 2. Asam Galat ... 10
Gambar 3. Diagram alur uji hipotesis variabel numerik (Dahlan, 2012) ... 16
Gambar 4. Uji kualitatif antioksidan B= blanko +DPPH, A=kuersetin+ DPPH, C= fraksi etil asetat ekstrak etanol+DPPH ... 35
Gambar 5. Uji kualitatif fenolik. A= blanko +Folin Ciocalteu, B= asam galat+Folin Ciocalteu, C= fraksi asetat ekstrak etanol +Folin Ciocalteu ... 36
Gambar 6. Operating time dari baku kuersetin ... 38
Gambar 7. Plot operating time fraksi etil asetat ekstrak etanol ... 39
Gambar 8. Kurva seri baku ... 40
Gambar 9. Kurva seri fraksi etil asetat ekstrak etanol ... 41
Gambar 11. Perbandingan IC50 kuersetin dan fraksi etil asetat ekstrak etanol ... 49
Gambar 12. Plot operating time asam galat ... 51
xv
DAFTAR LAMPIRAN
Lampiran 1. Pengesahan determinasi tanaman trengguli……… 61
Lampiran 2. Gambar dan Foto………. 62
Lampiran 3. Penimbangan DPPH dan pembuatan larutan induk……… 64
Lampiran 4. Data penimbangan kuersetin dan pembuatan larutan induk…………... 65
Lampiran 5. Data penimbangan bahan baku dan rendemen……… 66
Lampiran6. Data penimbangan fraksi etil asetat ekstrak etanol………. 67
Lampiran 7. Scanning pengkoreksi………. 69
Lampiran8. Optimasi Pengukuran aktivitas antioksidan menggunakan DPPH……. 72
Lampiran 9. Uji aktivitas antioksidan menggunakan radikal DPPH………... 80
Lampiran 10. Optimasi Pengukuran fenolik……….. 83
Lampiran 11. Pengukuran fenolik total……….. 91
xvi
ABSTRACT
The purpose of this study was to determine the antioxidant activity of ethyl acetate fraction of ethanol extract from trengguli leaves. Trengguli leaves determined before the experiment to ensure the validity of the sample. Fresh dried Trengguli leaves be used because it can be used for the long term. Results drying macerated with ethanol for the ethanol extract. The ethyl acetate fraction from ethanolic extract used for preliminary test tubes to detect with standard antioxidant quercetin. Ethyl acetate fraction was made by liquid liquid extraction with washbenzene and water. Aqueous phase was taken and used to liquid-liquid extraction with ethyl acetate. Phase ethyl acetate is then taken. Fraction dried by rotary evaporator. .
Preliminary test carried out using DPPH reagent for the antioxidant activity of ethyl acetate fraction and diluted Folin Ciocalteu reagent for the phenolic content. Measurement then performed on samples with visible spectrophotometry and obtained IC50 values to determine the antioxidant activity and the value gallic acid
equivalent (GAE) to determine the content of phenolic total. Result of research shows. the average IC50 value of quercetin was 11,42 ± 0,053 µg/mL, and the average
of mean IC50 fraction of ethyl acetate ethanolic extract was 83,98 ± 2,239 µg/mL.
Ethyl acetate fraction trengguli leaf ethanolic extract (Cassia fistula L,) has average value of gallic acid equivalent of 15,323 ± 0,075 GAE mg/g.
xvii
INTISARI
Tujuan dari penelitian ini adalah untuk mengetahui aktivitas antioksidan dari fraksi etil asetat ekstrak etanol dari daun trengguli. Daun trengguli dideterminasi terlebih dahulu untuk menjamin keabsahan sampel. Daun trengguli yang segar dikeringkan sehingga dapat digunakan untuk jangka panjang. Hasil pengeringan dimaserasi dengan etanol untuk mendapatkan ekstrak etanol. Ekstrak etanol digunakan untuk uji tabung pendahuluan untuk mengetahui adanya antioksidan dengan standar kuersetin. Fraksi etil asetat dibuat dengan terlebih dahulu dilakukan ekstraksi cair cair dengan washbensin dan air. Fase air diambil dan diekstraksi cair-cair dengan etil asetat. Fase etil asetat kemudian diambil dan dikeringkan dengan
vacuum rotary evaporator.
Uji pendahuluan dilakukan dengan menggunakan reagen DPPH untuk aktivitas antioksidan pada fraksi etil asetat yang diencerkan dan reagen Folin Ciocalteu untuk adanya kandungan fenolik. Pengukuran kemudian dilakukan terhadap sampeldengan spektrofotometri visible dan didapat nilai IC50 untuk
menentukan aktivitas antioksidan dan nilai ekuivalen asam galat untuk menentukan kandungan fenolik total. Hasil dari penelitian menunjukkan,nilai IC50 rata-rata
1 BAB I PENGANTAR A.Latar Belakang
Pada masa modern semakin banyak berkembang penyakit-penyakit
degeneratif seperti diabetes dan kanker pada manusia. Adanya penyakit ini sering
dipengaruhi oleh terbentuknya radikal bebas dari hasil metabolisme, polusi, dan
radiasi ultraviolet. Radikal bebas pada tubuh menjadi salah satu penyebab utama
penyakit degeneratif seperti kanker. Radikal bebas akan bereaksi dengan lipid,
protein bahkan DNA di dalam tubuh dan akan merusak jaringan tubuh, sehingga
menimbulkan berbagai penyakit degeneratif.
Radikal bebas dapat diatasi dengan adanya antioksidan. Antioksidan
digunakan untuk menangkap radikal-radikal bebas tersebut agar tidak merusak sel-sel
tubuh. Manusia telah membuat bahan sintetis yang dapat berfungsi sebagai
antoksidan contoh butylated hydroxyanisole (BHA), butylated hydroxytoluene
(BHT). Namun, antioksidan sintesis toksik jika digunakan sebagai obat pada
manusia, penggunaan secara umum hanya sebagai pengawet pada bahan minyak atau
lemak agar tidak teroksidasi selama penyimpanan. Oleh karena itu, penelitian perlu
dilakukan untuk mengeksplorasi antioksidan alami dari tanaman (Isfahlan, 2010)
Kandungan kimia tanaman seperti fenolik, dan flavonoid diketahui sebagai
senyawa bioaktif yang bermanfaat sebagai pencegah penyakit (Isfahlan, 2010).
menghentikan reaksi propagasi dari radikal bebas yang menjadi penyebab kanker.
Pada review bioefikasi oleh Moshahid, Irshad, Gamal (2009) ekstrak dari daun, kulit
batang dan akar diketahui memilki kemampuan menghambat radikal bebas sehingga
berpotensi untuk antioksidan. Ekstrak daun juga memilki kemampuan peroksidasi
lipid. Ekstrak etanol dari daun diketahui membantu penyembuhan luka dan regenerasi
jaringan.
Antioksidan tanaman trengguli di Indonesia terutama pada daun belum
banyak diteliti. Penelitian yang telah dilakukan kebanyakan dilakukan oleh peneliti
di luar negeri dan hanya sebatas ekstrak murni. Penggunaan fraksi dengan pelarut
tertentu akan mampu untuk mempersempit ruang lingkup penelitian dan dapat
digunakan sebagai dasar dalam penelitian isolasi fitokimia. Seanyawa fenolik dalam
tanaman merupakan salah satu senyawa dalam tanaman yang memiliki aktivitas
antioksidan. Oleh karena itu, penulis merasa perlu untuk melakukan pengamatan
aktivitas antioksidan dan pengukuran fenolik total dari fraksi etil asetat ekstrak etanol
dari daun trengguli.
1. Permasalahan
Dari latar belakang tersebut maka dirumuskan masalah dalam penelitian ini
adalah:
a. Berapakah nilai IC50 dari fraksi etil asetat ekstrak etanol daun trengguli
b. Berapakah nilai kadar fenolik total berdasarkan nilai g ekuivalen asam galat
dari fraksi etil asetat ekstrak etanol daun trengguli (Cassia fistula L.) ?
2. Keaslian penelitian
Penelitian mengenai tanaman trengguli telah beberapa kali ditemukan
diantaranya:
“Antioxidant Activities of Phenolic, Proanthocyanidin, and Flavonoid
Components in Extracts of Cassia fistula” (Luximon-Ramma A, Bahorun, Soobrattee, Aruoma), 2002 antioksidan dalam penelitian ini diukur dengan Trolox
Equivalent Capacity (TEAC) dan ferric-reducing antioxidant power (FRAP) assays.
“Antifungal activity from leaf extracts of Cassia alata L., Cassia fistula L.
and Cassia tora L. (Phongpaichit, Souwalak, Nongyao, Vatcharin dan Metta, 2004)
Penelitian ini dilakukan terhadap aktivitas antifungal dari ekstrak daun trengguli.
“Bioefficacy of Cassia fistula Linn. (Leguminosae) leaf extract against
chikungunya vector, Aedes aegypti (Diptera: Culicidae)” (Govindarajan, 2009) mengenai efektifitas ekstrak daun trengguli sebagai antilarva nyamuk
Penelitian ini berbeda karena menggunakan uji antioksidan metode radikal
scavenger DPPH dan sampel yang digunakan dari ekstrak etanol fraksi etil asetat
daun trengguli yang diambil dari taman Universitas Sanata Dharma. Berdasarkan
penelusuran yang telah dilakukan penelitian berjudul: “Uji Aktivitas Antioksidan
Kandungan Fenolik Total Ekstrak Etanol Fraksi Etil Asetat Ekstrak Etanol Daun
Trengguli (Cassia fistula. L)” belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat metodologis Memperoleh metode pengukuran aktivitas antioksidan
dan kadar fenolik total dari fraksi asetat ekstrak etanol yang murah dan praktis.
b. Manfaat teoretis Mendapatkan nilai IC50 atau aktivitas antioksidan dari daun
trengguli serta kadar fenolik totalnya.
c. Manfaat praktis Memperoleh data yang dapat digunakan untuk
pengembangan manfaat daun trengguli lebih lanjut.
B. Tujuan Penelitian
Tujuan dari penelitian ini adalah:
a. Mengetahui nilai IC50 dari fraksi etil asetat ekstrak etanol daun trengguli
(Cassia fistula L).
b. Mengetahui nilai kadar fenolik total fraksi etil asetat ekstrak etanol daun
5
BAB II
PENELAAHAN PUSTAKA A. Trengguli
Klasifikasi berdasarkan plant.usda.gov diakses tanggal 2 Mei 2013.
Kingdom : Plantae – Plants
Subkingdom : Tracheobionta – Vascular plants
Superdivision : Spermatophyta – Seed plants
Division : Magnoliophyta – Flowering plants
Class : Magnoliopsida – Dicotyledons
Subclass : Rosidae
Order : Fabales
Family : Fabaceae – Pea family
Genus : Cassia L. – cassia
Species : Cassia fistula L. – golden shower
( USDA, 1996)
Tanaman Cassia fistula L. diketahui memiliki khasiat antipiretik dan
analgesik. Selain itu, ditemukan bahwa bermanfaat juga dalam penyakit kulit,
menyembuhkan luka. Ekstrak daun diketahui dapat menghambat peroksidase lipid
yang berkaitan dengan karakter antioksidan oleh (Moshahid et al., 2009). Kandungan
kimia dari Cassia fistula L. mengandung epifzelechin, epiafzelezin-3-O glucoside,
epicatechin, procyanidin B2, biflavonoid, triflavonoid, rhein, rhein glucoside,
sennoside A (Bahorun, 2005).
B.Kandungan Fenolik Total
Istilah komponen fenolik menunjukkan kumpulan dari zat zat dalam
tanaman yang pada umumnya memiliki cincin aromatik yang berikatan dengan satu
atau lebih subtituen hidroksil. Zat fenolik cenderung untuk larut air, karena biasanya
bergabung dengan glukosa sebagai glikosida dan biasanya terletak di vakuola sel
(Harborne 1998).
Senyawa fenolik merupakan bagian dari tanaman yang sangat penting.
Fenolik memiliki kemampuan menangkap radikal bebas karena keberadaan gugus
hidroksil. Total fenolik dapat diukur dengan menggunakan metode Folin Ciocalteu
(Yusoff dan Ade, 2011).
Flavonoid adalah kelas yang beraneka ragam dari senyawa
metabolitsekunder fenolik tanaman, dengan berat molekul rendah yang
dikarakterisasi dengan inti flavan. Lebih dari 4000 flavonoid telah teridentifikasi dan
tersebar pada daun, biji, batang, dan bunga dari tanaman. Pada tanaman, komponen
Manfaat kesehatan flavonoid yang paling penting adalah sifat sebagai antioksidan dan
kemampuan untuk mengkelat (Heim, Anthony, dan Dennis, 2002).
Flavonoid adalah turunan benzo-γ-pyrone yang terdiri dari fenolik dan cincin piran dan diklasifikasikan berdasarkan subtitusi. Flavonoid makanan dibedakan
berdasarkan pola hidroksilasi, konjugasi antara cincin aromatik, gugus glikosidik, dan
gugus metoksi. Polimerasi dari struktur inti menghasilkan tannin dan spesies komplek
lainnya seperti pada anggur merah, anggur dan teh hitam (Heim et al, 2002).
Gambar 1.a. Kuersetin, b. Struktur inti flavonoid
Flavonoid tersebar secara luas pada tanaman, sebagai bagian pigmen dari
antosianin pada kelopak bunga dan bagian daun dalam tanaman tingkat tinggi.
Flavonoid biasa bergabung dalam kombinasi glikosida. Flavonol aglikon yang biasa
ada pada tanaman, kamperol, quercetin, dan myrcetin (Harbone, 1998).
C.Antioksidan
Pentingnya oksidasi pada tubuh dan pada bahan makanan telah dikenali.
timbul tergantung dari produksi dari radikal bebas dan spesies reaktif oksigen yang
menyebabkan perubahan oksidatif (Antolovich, Prenzler, Patsalides, 2001).
Radikal bebas adalah atom atau molekul yang memiliki sebuah elektron tak
berpasangan pada jari jari terluar dari atom. Sifatnya tidak stabil dan pada struktur
biologis dapat menyebabkan kerusakan oksidatif. Untuk mencegahnya digunakan
herbal sebagai sumber antioksidan (Chaisawvong dan Supapor, 2009).
Spesies oksigen reaktif adalah molekul yang mengandung oksigen yang
sangat reaktif, temasuk radikal bebas. Semua jenis oksigen reaktif dapat bereaksi
dengan membran, asam nukleat, protein, enzim dan molekul lain yang menyebabkan
kerusakan sel (Savakal, 2008).
Kerusakan oksidatif pada DNA, protein, dan makromolekul lain akan
menyebabkan munculnya berbagai penyakit. Penyakit-penyakit tersebut antara lain
penyakit jantung dan kanker. Reaksi kimia oleh antioksidan terhadap spesies oksigen
reaktif, yaitu dengan mendonorkan elektron ke spesies oksigen reaktif membuat
kereaktifannya berkurang (Savakal, 2008).
D.Metode 1,1-difenil-2-pikrilhidrazil (DPPH)
Aktivitas antioksidan tidak dapat diukur secara langsung tetapi oleh efek dari
antioksidan dengan mengontrol banyaknya oksidasi. Metode yang digunakan sangat
dari hasil, sebagai contoh, oksidasi dari asam linoleat diikuti konjugasi dien
(Antholovich et al, 2001).
DPPH digunakan secara luas untuk mengukur kemampuan dari zat yang
bekerja sebagai penangkap radikal bebas atau hidrogen donor, dan untuk
mengevaluasi aktivitas antioksidandalam makanan. Metode DPPH dapat digunakan
pada sampel berupa zat padat maupun cair dan tidak spesifik pada satu komponen
antioksidan tetapi berlaku pada keseluruhan kapasitas antioksidan dari sampel
(Prakash, 2001).
Parameter yang diperkenalkan sebagai interpretasi dari hasil pengukuran
dengan metode DPPH disebut efficient concentration atau nilai IC50 sering juga
disebut IC50. IC50 didefinisikan sebagai konsentrasi dari substrat yang menyebabkan
50% hilangnya aktivitas DPPH yang ditunjukkan berupa warna (Molyneux, 2004).
DPPH radikal menyerap pada panjang gelombang 517 nm dan pada sebuah
sistem bebas substrat, aktivitas antioksidan dapat ditetapkan dengan memonitoring
penurunan absorbansi. Hasil dilaporkan sebagai EC50, yang merupakan jumlah
antioksidan yang dibutuhkan untuk menurunkan 50% dari konsentrasi DPPH awal.
Waktu yang dibutuhkan untuk mencapai steady state juga ikut dihitung (Antolovich
et al, 2001).
Pada metode radikal bebas DPPH, kemampuan antioksidan diukur pada suhu
pengaruh suhu. Mekanisme reaksi antara antioksidan dengan DPPH tergantung dari
konformasi dari molekul senyawa antioksidan (Lamaison, 1990).
E.Metode Folin Ciocalteu
Prinsip dari metode Folin Ciocalteu adalah menggunakan kemampuan gugus
fenol mereduksi. Reaksi terhadap redoks tersebut akan terjadi pada suasana basa.
Reduksi fosfotungstanat fosfomolibdenum (reagen Folin Ciocalteu) oleh ion fenol
merubah warna larutan yang diuji berwarna biru tua. Semakin tua warna yang
diperoleh semakin besar absorbansinya menunjukkan semakin besar jumlah
kandungan fenol (Yusoff dan Ade, 2011).
Asam galat adalah sebuah asam organic yang dikenal sebagai
3,4,5-trihydroxybenzoicacid (C6H2(OH)3COOH)/. Asam galat ditemukan secara luas pada
kerajaan tanaman. Asam galat dengan kadar yang tinggi ditemukan pada gallnuts,
anggur, sumac, daun teh, hops, dan kulit kayu oak ( Massoud, Hagad, Ali, dan Nazir,
2012).
F. Spektrofotometri Visibel
Spektrofotometer adalah instrumen yang dapat memisahkan radiasi
polikromatik menjadi beberapa panjang gelombang. Spektrofotometer terdiri
darisumber radiasi pada panjang gelombang tertentu, monokromator untuk memilih
panjang gelombang dari sumber radiasi, tempat sampel, detektor, dan alat untuk
membaca hasil yang dikeluarkan detektor (Christian, 2004)
Radiasi ultraviolet dan radiasi visible merupakan bagian dari spektrum
elektromagnetik, yang termasuk bentuk lain dari radiasi seperti radio, infrared (IR),
kosmik, dan Xrays. Ketika radiasi berinteraksi dengan material, sejumlah proses
dapat terjadi, termasuk refleksi, sebaran, penyerapan, fluoresen. Fosforesen
(absorpsida reemisi) dan reaksi fotokimia. Secara umum pada pengukuran spektra
UV visible, yang diinginkan adalah penyerapan (absorbansi) (Owen, 2000).
Pada umumnya semakin panjang dari conjugated system pada molekul,
semakin dekat λ max sampai pada wilayah visible. Karakteristik transisi energi dan penyerapan panjang gelombang adalah lebih merupakan sifat dari gugus atom
tertentu dibandingkan elektron. Ketika terjadinya absorpsi tersebut, dua tipe gugus
yang mempengaruhi dihasilkannya spektrum dari molekul yaitu kromofor dan
auksokrom (Thermospectronic, 2011).
G.Pembuatan Simplisia dan Ekstraksi
Untuk melakukan analisis fitokimia tumbuhan dapat dikeringkan sebelum
yang baik untuk mencegah perubahan kimia. Setelah kering, tanaman dapat disimpan
untuk jangka waktu lama (Harbone, 1998).
Umumnya material tanaman seharusnya dikeringkan pada temperatur di
bawah 30° C untuk menghindari dekomposisi dari komponen termolabil. Material
tersebut harus dilindungi dari cahaya sebab memiliki potensial dari transformasi
kimia dari pemaparan radiasi ultraviolet (Sarker, Zahid, dan Alexander, 2006).
Ketika material segar tanaman diperlukan untuk suatu penelitian, disarankan
untuk dilakukan ekstraksi secepat mungkin menggunakan pelarut organik seperti
metanol atau etanol, yang akan mendeaktivasi enzim yang ada pada tanaman (Sarker
et al, 2006).
H.Validasi Metode Analisis
Validasi metode analisis merupakan penilaian terhadap parameteryang ada
dalam percobaan laboratorium, yang digunakan untuk membuktikan bahwa
parameter tersebut memenuhi persyaratan sebagai metode yang layak digunakan atau
valid (Harmita, 2004). Parameter yang diuji dalam suatu analisis antara lain:
kecermatan, keseksamaan, selektifitas, linearitas, batas deteksi dan kuantitasi,
ketangguhan metode, dan ketahanan metode. Parameter yang diperlukan untuk
divalidasi dapat diseleksi tergantung metode yang digunakan (Harmita, 2004).
Dalam penelitian, dapat terjadi error yang menurunkan validitas data. Tipe
1. Gross error
Gross error tidak dapat diatasi sehingga ketika terjadi kesalahan tersebut
pengujian harus diulang (Prichard, 2001).
2. Sistematis
Systematic error merupakan perbedaan anatara rata-rata data yang teramati,
diperoleh dari seri dengan jumlah besar ( n≥ 8) dan true value (Burgess, 2000).
3. Random error
Random errormerupakan perbedaan antara nilai tunggal yang teramati
dengan rata-rata dari nilai yang teramati dalam lebih besar (paling tidak delapan),
diperoleh dari menerapkan prosedur analisis yang sama dalam sampel homogennya
(Burgess, 2000).
Parameter untuk validasi adalah sebagai berikut,
1. Linearitas
Linearitas di definisikan sebagai kemampuan dari suatu prosedur analisis
dalam suatu range untuk mendapatkan hasil tes yang yang proporsional secara
langsung terhadap konsentrasi analit dari sampel. Linearitas dapat ditunjukkan secara
langung dari pengujian dengan pengenceran larutan stok standar atau dengan
mengukur campuran sintetis dari komponen produk uji (Huber, 2010).
Linearitas ditentukan dengan lima sampai enam konsentrasi standar yang
memiliki rentang konsentrasi 80-120% dari konsentrasi yang diperkirakan. Respon
proporsional dengan pengukuran matematis. Suatu persamaan regresi linear berlaku
sebagai hasil seharusnya memiliki intersep yang tidak berbeda signifikan dari nol
(Huber, 2010).
Laporan yang dihasilkan harus termasuk kemiringan dari garis, intercept,
dan koefisien korelasi data yang menunjukkan korelasi yang jelas antara respon dan
analit. Hasil tidak boleh menunjukkan deviasi yang signifikan dari linearitas, yang
berarti koefisien korelasi harus r>0,99, pada area kerja (80%-120%) (Kingston, 2004)
2. Presisi
Presisi dari metode analisis menunjukkan kedekatan dari suatu data (derajat
persebaran) antara suatu seri pengukuran yang diperoleh dari sampling yang
dilakukan berkali-kali dari sampel homogen yang sama dalam kondisi yang telah
ditetapkan (Ermer dan Miller, 2005). Presisi dapat dibagi tiga tingkatan yaitu
keterulangan (repeatability), intermediate precision, dan reproducibility (Ermer dan
Miller, 2005).
Sebagai parameter presisi, standar deviasi, standar deviasi relatif (coefficient
of variation), dan confidence interval harus dihitung untuk tiap tingkatan presisi
(Ermer dan Miller, 2005). Standar deviasi adalah suatu pengukuran dari nilai yang
teramati sebagai hasil dari random error (Burgess, 2000). Standar deviasi adalah
parameter yang penting dalam mendeskripsikan jarak dari distribusi normal sebagai
Rumus Standar Deviasi (s) dan ragam (s2):
Tabel I. Nilai CV yang dapat diterima menurut Kingston (2004) Kadar zat aktif
(%)
Nilai KVyang masih dapat diterima (%)
Spesifisitas merupakan sifat dari prosedur analisis untuk mengukur hanya
kandungan yang memang ingin diukur. Metode yang digunakan tidak boleh
merespon terhadap kandungan lain dari analit atau material lain yang ada (Burgess,
2000). Metode preparasi sampel tidak boleh hanya membawa jumlah yang terukur
dari sampel tetapi komponen yang bersama-sama dengan analit tidak boleh
mengganggu dalam analisis (Ohanesian, Streeter, 2002).
I. Analisis Statistika
Metode Shapiro-Wilk mengolah data dasar dalam tabel distribusi frekuensi.
Data tersebut kemudian diurut, kemudian data dibagi dalam dua kelompok untuk
dikonversi dalam Shapiro-Wilk. Analisis statistik dapat juga dilanjutkan transformasi
Diagram dari alur metode statistika ditunjukkan dalam Gambar di bawah ini
(Gambar 2).
Gambar 3. Diagram alur uji hipotesis variabel numerik (Dahlan, 2012) J. Landasan Teori
Antioksidan adalah senyawa yang mempunyai kemampuan menangkap
spesies oksigen reaktif atau radikal bebas lainnya. Radikal bebas dapat menyebabkan
kerusakan pada struktur sel manusia sehingga dapat menyebabkan gangguan seperti
kanker. Antioksidan digunakan untuk mencegah kerusakan akibat radikal bebas. Hipotesis komparatif
Variabel numerik
Sebaran Normal ?
Ya Tidak
Berpasangan Tidak Berpasangan
2 kelompok >2 kelompok
Pemanfaatan antioksidan dari bahan alam dilakukan karena lebih aman dibandingkan
antioksidan sintesis yang biasa sebagai pengawet.
Penelitian sebelumnya menujukkan daun dari tanaman Cassia fistula L.
mengandung senyawa flavonoid dan kaya akan fenolik. Tanaman ini juga digunakan
sebagai obat tradisional di India. Ekstrak etanol dari daun Cassia fistula L. diketahui
memiliki kemampuan menyembuhkan luka da regenerasi organ tubuh. Ekstrak dari
daun diketahui memiliki daya hambat terhadap peroksidasi lipid yang disebabkan
spesies oksigen reaktif.
Metode pengukuran aktivitas antioksidan DPPH sering digunakan sebagai
metode untuk mengukur aktivitas antioksidan yang cepat dan mudah. DPPH bekerja
sebagai radikal scavenging yang menangkap unpaired electron dari senyawa yang
mengandung antioksidan. Pengukuran dilakukan dengan spektrofotometri visible
untuk melihat penurunan absorbansi DPPH karena adanya antioksidan.
Metode Folin Ciocalteu dapat digunakan untuk mengukur kandungan fenolik
total dari sampel ekstrak. Reagen fosfotungstanat fosfomolibdat akan tereduksi oleh
adanya gugus fungsional fenolat sehingga membentuk warna biru. Warna ini dapat
K.Hipotesis
Fraksi etil asetat ekstrak etanol daun trengguli (Cassia fistula L.) memiliki
aktivitas antioksidan dinyatakan sebagai IC50 dan memiliki kandungan fenolik yang
19
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan termasuk penelitian eskploratif.
B.Variabel Penelitian
1. Variabel bebas berupa konsentrasi fraksi etil asetat ekstrak etanol daun trengguli.
2. Variabel tergantung berupa aktivitas antioksidan dan kandungan fenolik total
fraksi etil asetat ekstrak etanol daun trengguli, tergantung dari jenis, perawatan dan
tempat tumbuh tanaman
3. Variabel pengacau terkendali berupa tempat tumbuh tanaman, waktu pemanenan,
umur tanaman, dan cara panen.
4. Variabel pengacau tidak terkendali berupa cahaya matahari dan cuaca.
C.Definisi Operasional
1. Ekstrak etanol daun trengguli adalah sari hasil proses maserasi daun trengguli
dengan penyari menggunakan etanol.
2. Fraksi etil asetat adalah hasil fraksinasi ekstrak etanol daun trengguli dengan
3. Persen inhibition concentration (%IC) adalah persen yang menyatakan
kemampuan fraksi etil asetat ekstrak etanol daun trengguli untuk menangkap
radikal DPPH.
4. Inhibition concentration 50% (IC50) adalah nilai konsentrasi fraksi etil asetat
ekstrak etanol daun trengguli yang menghasilkan penangkapan 50% radikal
DPPH.
D.Bahan dan Alat Penelitian 1. Bahan
Daun trengguli diperoleh dari tanaman trengguli koleksi Universitas Sanata
Dharma, akuades (Laboratorium Kimia Analisis Instrumental Fakultas Farmasi
Universitas Sanata Dharma); bahan kualitas p.a. E. Merck yaitu:metanol, asam galat;
bahan kualitas p.a. Sigma Chem. Co., USA, yaitu: DPPH (1,1-difenil-2
pikrilhidrazil), reagen Folin-Ciocalteu dan kuersetin; bahan kualitas teknis Brataco
Chemica, yaitu: washbensin dan etil asetat; bahan kualitas teknis CV. General
Labora, yaitu:etanol dan metanol pa. ; dan aluminium foil.
2. Alat
Grinder, neraca analitik (Scaltec SBC 22, BP 160P), vacuum rotary
evaporator (Janke & Kunkel), waterbath (labo-tech, Heraeus), vortek (Janke
&Kunkel), spektrofotometer UV-Vis (Perkin Elmer Lamda 20), corong Buchner,
oven, mikropipet 10-1000 µL; 1-10 mL (Acura 825, Socorex), tabung reaksi bertutup,
E.Tata Cara Penelitian 1. Determinasi tanaman
Determinasi tanaman trengguli dilakukan di Laboratorium Biologi Farmasi,
Fakultas Farmasi USD menurut Van Steenis (1981).
2. Pengumpulan tanaman
Tanaman trengguli (Cassia fistula L.) diperoleh dari tanaman milik
Universitas Sanata Dharma. Pengambilan daun dengan kriteria berwarna hijau tua
segar dengan warna yang tua dan pada saat tanaman menjelang berbunga.
Pengambilan pada pagi hari atau sebelum tengah hari.
3. Preparasi sampel
Sebanyak 90 g daun trengguli segar, dibersihkan, lalu dikeringkan dengan
dikering anginkan ditempat teduh sampai terbentuk simplisia kering dengan kadar air
kurang dari 10 %. Simplisia daun trengguli kemudian dihaluskan dengan grinder.
Simplisia yang telah dihaluskan dituang ke dalam bejana maserasi, ditambah etanol
sampai terendam sempurna, dan dicampur homogen.
Campuran dimaserasi pada suhu ruangan selama dua hari. Filtrat diperoleh
melalui penyaringan menggunakan kertas saring kasar dengan bantuan corong
Buchner dan pompa vakum. Ampas penyaringan diremaserasi dengan etanol
secukupnya selama dua hari. Filtrat kemudian dicampurkan dengan filtrat terdahulu.
Keseluruhan filtrat yang diperoleh diuapkan pelarutnya hingga diperoleh ekstrak
4. Pembuatan fraksi etil asetat
Ekstrak etanol daun trengguli ditambah 300 mL air hangat dan dilakukan
ekstraksi cair-cair menggunakan washbensin dengan perbandingan larutan ekstrak :
washbensin (2:1, v/v), kemudian didiamkan sampai terpisah sempurna. Fase air akan
berada pada bagian bawah, sedangkan fase washbensin berada pada bagian atas.
Dari hasil ekstraksi cair-cair tersebut diperoleh dua fraksi, yaitu fraksi
washbensin dan fraksi air. Selanjutnya fraksi air diekstraksi lagi menggunakan etil
asetat dengan perbandingan larutan fraksi air-etil asetat (1:1, v/v) sehingga
didapatkan fraksi air dan etil asetat. Setelah dipisahkan fraksi etil asetat diuapkan
dengan vacuum rotary evaporator. Fraksi yang telah kering digunakan untuk
dianalisis lebih lanjut.
5. Pembuatan Larutan DPPH, baku pembanding, larutan uji
a. Pembuatan larutan DPPH. 15,8 mg DPPH dilarutkan ke dalam metanol.
Diperoleh larutan DPPH dengan konsentrasi 0,4 mM. Larutan tersebut ditutup dengan
alumunium foil dan dibuat selalu baru.
b. Pembuatan larutan stok kuersetin. 2,5 mg stok kuersetin ditimbang dan
ditambahkan metanol hingga 10 mL.
c. Pembuatan larutan seri kuersetin. Diambil 0,2; 0,3; 0,4; 0,5; dan 0,6 larutan
stok kuersetin dan diencerkan dengan metanol hingga 10 mL pada labu ukur, dan
d. Pembuatan larutan uji dari ekstrak etanol fraksi etil asetat. Sebanyak 25 mg
ekstrak ditimbang dan dilarutkan dengan metanol sampai 25 mL dan didapat
konsentrasi 1 mg/mL. Larutan tersebut diambil 5 mL lalu diencerkan ke 50 ml. Dari
larutan intermediet diambil sebanyak 3; 4,75; 6; 8,25, dan 10 mL lalu diadd dengan
metanol hingga 10 mL, sehingga didapat konsentrasi 30; 47,5; 60; 82,5, dan 100
g/mL.
6. Uji pendahuluan
a. Uji fenolik. Sejumlah larutan asam galat dan larutan uji dimasukkan
masing-masing dalam tabung reaksi dan ditambahkan reagen Folin Ciocalteu (1/10 v/v),
Larutan tersebut ditambahkan dengan 4,0 mL natrium karbonat 1 M. Setelah 10 menit
warna larutan diamati.
b. Uji aktvitas antioksidan. Sebanyak 2 mL larutan DPPH, dimasukkan dalam
masing-masing tiga labu takar berukuran 10 mL. Metanol sebagai kontrol, larutan
kuersetin konsentrasi 15 µg/mL, dan larutan uji konsentrasi 100 µg/mL dibuat pada
labu takar 10 mL. Selanjutnya diencerkan dengan metanol hingga tanda batas.
Larutan tersebut divortek 30 detik. Selama 30 menit diamati perubahan warna yang
terjadi.
7. Optimasi uji daya antioksidan
a. Penentuan OT (Operating Time). 2 mL larutan DPPH 0,4 mM dimasukkan ke
dalam labu takar sebanyak tiga buah, masing-masing berukuran 10 mL, kemudian
10; dan 15 µg/mL kemudian ditambahkan metanol hingga tanda batas. Larutan
tersebut divortek selama 30 detik. Setelah itu dibaca absorbansinya dengan
spektrofotometri visible pada panjang gelombang 517 selama 1 jam. Perlakuan ini
juga dilakukan untuk mencari OT dari larutan uji fraksi etil asetat pada konsentrasi
30, 65, dan 100 µg/mL.
b. Penentuan panjang gelombang maksimum. Pada tiga labu takar berukuran 10
mL, dimasukkan masing- masing 0,2; 0,6; dan 1,0 mL larutan DPPH 0,4 mM. Tiap
labu takar tersebut ditambahkan metanol hingga tanda batas sehingga konsentrasi
DPPH menjadi 0,02; 0,06; dan 0,08 mM Larutan tersebut divortek 3 detik. Larutan
kemudian didiamkan selama OT. Lalu dilakukan pengukuran absorbansinya dengan
spektrofotometri visible pada panjang gelombang antara 400-600 nm.
8. Penentuan aktivitas antioksidan
a. Pengukuran absorbansi larutan kontrol. Pada labu takar 10,0 mL,
dimasukkan sebanyak 2,0 mL larutan DPPH 0,4 mM kemudian ditambahkan metanol
p.a hingga tanda batas. Larutan tersebut dibaca absorbansinya pada saat OT dan
panjang gelombang serapan maksimum. Pengerjaan dilakukan sebanyak tiga kali.
Larutan ini digunakan sebagai larutan kontrol untuk menguji larutan pembanding dan
larutan uji.
b. Pengukuran absorbansi larutan pembanding dan uji. Sebanyak 2,0 mL
larutan DPPH 0,4 mM dimasukkan ke dalam masing masing labu takar 10,0 mL
konsentrasi larutan yang telah dibuat. Selanjutnya ditambahkan metanol p.a. hingga
tanda batas. Larutan tersebut kemudian divortek selama 30 detik dan diamkan selama
OT. Larutan dibaca absorbansinya dengan spektrofotometer visibel pada panjang
gelombang maksimum. Pengerjaan dilakukan sebanyak tiga kali.
c. Validasi metode uji aktivitas antioksidan. Hasil dari prosedur 7a dan b
divalidasi berdasarkan presisi (%CV), linearitas (nilai r) serta spesifisitas (spektra
kontrol).
9. Optimasi penentuan fenolik total
a. Penentuan OT (Operating Time). Dibuat larutan baku asam galat konsentrasi
50; 100; dan 150 µg/mL dalam metanol. Masing-masing larutan diambil 0,5 mL dan
ditambahkan dengan reagen Folin Ciocalteu serta 4 mL larutan natrium karbonat 1
M. Absorbansinya diukur pada panjang gelombang 750 nm selama 30-60 menit.
Operating time ditentukan ketika absorbansi larutan telah stabil.
b. Penentuan panjang gelombang maksimum. Dibuat larutan baku asamgalat
dengan konsentrasi 50; 100; dan 150 µg/mL dalam metanol. Masing-masing diambil
sebanyak 5 mL dan ditambahkan dengan reagen Folin Ciocalteu yang telah
diencerkan dengan air serta 4 mL larutan natrium karbonat 1 M. Sampel didiamkan
selama OT kemudian diukur absorbansinya pada panjang gelombang 600-800 nm.
10. Penetapan kadar fenolik total
a. Pembuatan kurva baku asam galat. Sebanyak 0,5 mL larutan asam galat 50;
telah diencerkan dengan air (1:10; v/v). Larutan selanjutnya ditambah dengan 4,0 mL
natirum karbonat 1 M. Setelah 10 menit, absorbansinya dibaca pada panjang
gelombang 750 nm terhadap blanko yang terdiri atas akuades : metanol p.a. (1:1;
v/v), reagen Folin-Ciocalteu, dan larutan natrium karbonat 1 M.
b. Validasi metode penetapan kandungan fenolik total. Hasil dari prosedur 9a
divalidasi berdasarkan, presisi (%CV), linearitas (nilai r) serta spesifisitas (spektra
kontrol).
c. Estimasi kandungan fenolik total larutan uji. Diambil 0,5 mL larutan uji 400
µg/mL, lalu dimasukkan ke dalam tabung reaksi, dan dilanjutkan sebagaimana
perlakuan pada pembuatan kurva baku asam galat. Kandungan fenolik total
dinyatakan sebagai g ekuivalen asam galat (g ekuivalen asam galat per g fraksi etil
asetat).
11. Analisis hasil
Aktivitas penangkapan radikal DPPH (%) dihitung dengan rumus :
Aktivitas penangkapan radikal=
Keterangan:
A = absorbansi
Data aktivitas (%) dianalisis dan dihitung nilai IC50 melalui analisis probit.
IC50 merupakan konsentrasi yang mampu menghambat 50% aktivitas DPPH.
Kandungan fenolik total dalam fraksi etil asetat ekstrak etanol daun trengguli
ke dalam persamaan kurva baku asam galat sehingga diperoleh nilai g ekuivalensi
larutan uji terhadap asam galat. Nilai tersebut kemudian dihitung:
F=Kandungan fenolik total=
28
BAB IV
PEMBAHASAN
A. Determinasi Tanaman Trengguli
Determinasi tanaman diperlukan untuk memastikan bahan yang digunakan
telah sesuai dengan jenis tanaman yang akan digunakan sebagai bahan penelitian.
Tanaman yang digunakan harus diidentifikasi spesies tanamannya sehingga penelitian
yang dilakukan sesuai tujuan yang telah ditetapkan. Determinasi tanaman dilakukan
di Laboratorium Farmakognosi Fitokimia, Fakultas Farmasi, Universitas Sanata
Dharma, Yogyakarta, pada tanggal 29 Januari 2013. Proses determinasi dilakukan
dengan acuan menurut van Stenis (1981). Hasil determinasi telah menunjukkan
bahwa tanaman yang digunakan adalah Cassia fistula L (Lampiran 1).
B.Pengumpulan Bahan
Bahan daun tanaman trengguli diperoleh pada tanggal 21 September 2012
dari tanaman inventaris milik Universitas Sanata Dharma, Kampus III, Paingan,
Yogyakarta. Tanaman yang digunakan merupakan tumbuhan yang sengaja ditanam di
lingkungan Kampus III, Universitas Sanata Dharma, Paingan, Yogyakarta. Pemilihan
kampus Universitas Sanata Dharma karena minim cemaran yang berasal dari
kendaraan dan juga cemaran penyakit dan jamur karena dirawat secara khusus
sebagai tanaman taman. Selain itu, spesies tanaman lebih mudah dipastikan karena
telah terdaftar pada bagian rumah tangga.
Pemanenan daun trengguli dipilih sesuai kriteria berikut, yaitu pada musim
kemarau, tanaman belum berbunga, pemanenan dilakukan pada pagi hari. Pemanenan
dilakukan pada musim kemarau supaya kelembaban udara kecil sehingga
meminimalisir jamur dan mempermudah proses pengeringan. Tanaman yang belum
berbunga dipilih dengan harapan metabolit sekunder yang diduga mengandung
aktivitas antioksidan berada dalam jumlah yang maksimal. Waktu pagi hari
digunakan untuk memanen agar tanaman tidak terlalu banyak menerima sinar UV.
Sinar UV akan mendegradasi senyawa metabolit. Hal ini tidak diinginkan karena
dalam senyawa metabolit sekunder diduga mengandung aktivitas antioksidan.
Daun yang digunakan dipilih mulai dari daun urutan ketiga dari pucuk
batang, karena daun setelah urutan ketiga dari pucuk merupkan daun yang telah tua
sehingga diharapkan kadar metabolit sekunder dan kandungan kimia lainnya
memiliki jumlah yang besar dan seragam dengan daun daun lainnya. Daun dipucuk
termasuk daun yang baru saja tumbuh dan kemungkinan besar kandungan metabolit
dan kandungan kimia lainnya belum sebesar daun yang tua. Daun yang dipilih untuk
karena umur daun masih dianggap terlalu muda dan bukan daun kuning karena
kandungan kimia di dalamnya telah hilang atau rusak.
Kriteria lain dari daun yang diperhatikan antara lain, tidak berjamur dan
tidak berulat dan tidak busuk. Kriteria tersebut menjadi pertimbangan agar daun yang
digunakan dalam ekstraksi tidak mengalami perubahan kandungan kimiaatau
biotransformasi karena adanya cemaran-cemaran tersebut. Daun-daun yang sesuai
dengan kriteria tersebut dikumpulkan lalu dicuci untuk membersihkan debu atau
kotoran yang menempel pada permukaan daun.
Daun kemudian dikering-anginkan sehingga kandungan airnya berkurang.
Tujuan dari pengeringan adalah untuk mengawetkan daun sehingga dapat disimpan
selama beberapa waktu. Setelah daun dikeringkan, simplisia kering dapat disimpan
untuk jangka panjang (Raaman, 2006). Pelaksanaan pengeringan harus dalam kondisi
terkontrol agar tidak terjadi kerusakan kandungan kimia (Raaman, 2006).
Pengeringan tidak dilakukan dengan suhu tinggi melainkan dengan suhu ruang.
Pengeringan dalam suhu ruang dipilih untuk mengurangi kemungkinan kerusakan zat
kimia akibat suhu tinggi. Hasil pengeringan dijadikan serbuk supaya dapat
dimaserasi.
C.Hasil Ekstraksi
Ekstraksi dilakukan untuk menyari zat kimia termasuk metabolit sekunder
dari dalam daun. Ekstraksi organik merupakan suatu proses untuk memisahkan zat
diekstraksi dihancurkan atau digiling menjadi serbuk lalu dicampur dengan suatu
pelarut (Raaman, 2006). Daun yang telah dipilih tadi digiling dengan grinder hingga
halus. Serbuk hasil penggilingan kemudian diayak, untuk memperoleh ukuran
partikel yang kecil. Daun diubah menjadi serbuk agar luas permukaan efektifnya
meningkat dan kontak dengan pelarut meningkat.
Ekstraksi dilakukan dengan menggunakan metode maserasi. Metode
maserasi adalah metode ekstraksi yang melibatkan perendaman dan pengadukan
bahan tanaman dengan pelarut (Raaman, 2006). Metode ini dipilih karena maserasi
sederhana sehingga mudah dilakukan. Prosedur ekstraksi ini tidak membutuhkan
panas sehingga dapat mencegah degradasi senyawa yang terkandung dalam tanaman.
(Sarker, Zahid, dan Alexander, 2006). Proses ekstraksi berhenti sepenuhnya setelah
mencapai kesetimbangan antara zat dalam ekstrak dengan zat dalam tanaman (Sarker
et al, 2006). Metode ini memiliki kelemahan waktu yang dibutuhkan dalam proses
ektraksi cukup panjang (Sarker et al, 2006).
Pelarut yang digunakan adalah etanol 76 % karena senyawa fenolik seperti
flavonoid yang diduga memiliki aktivitas antioksidan dapat terekstrak. Pemilihan
etanol sebagai pelarut dibandingkan dengan metanol, yaitu metanol memiliki
ketoksikan yang lebih tinggi dibandingkan etanol. Penggunaan metanol yang toksik
untuk ekstrak dirasakan kurang aman apabila digunakan dengan tujuan konsumsi.
Pelarut etanol dapat masuk ke sel tumbuhan dengan baik dan menarik zat-zat di
Proses maserasi menggunakan serbuk daun yang telah diayak lalu
dimaserasi dengan etanol. Proses maserasi dilakukan selama dua hari, setelah dua
hari cairan ekstrak diambil, kemudian dilakukan maserasi ulang terhadap sisa serbuk,
maserasi ulang dilakukan dua kali. Tujuan maserasi ulang adalah untuk menarik
sebanyak mungkin komponen yang terkandung di dalam serbuk daun sehingga hasil
esktraksi yang diperoleh dapat lebih maksimal. Dari hasil maserasi, diperoleh cairan
yang berwarna hitam kecoklatan.
Hasil ekstraksi kemudian diuapkan sehingga diperoleh ekstrak kental yang
kemudian akan digunakan untuk proses selanjutnya. Proses penguapan dilakukan
dengan alat bantu vacuum rotary evaporator. Tujuan penguapan ini adalah untuk
memisahkan antara zat yang terekstrak dengan pelarut yang digunakan, sehingga
dapat diperoleh ekstrak kering atau kental. Vacuum rotary evaporator digunakan
karena dapat memisahkan pelarut dengan lebih sempurna dan lebih cepat
dibandingkan dengan dipanaskan di waterbath. Vacuum rotary evaporator juga tidak
membutuhkan suhu tinggi sehingga mengurangi kemungkinan degradasi akibat
pengaruh suhu tinggi.
Ekstrak kental yang diperoleh ditimbang dengan cawan sehingga dapat
diketahui bobot ekstrak yang dihasilkan. Bobot ekstrak dibandingkan dengan bobot
bahan serbuk yang digunakan untuk perhitungan rendemendari proses ekstraksi yang
dilakukan. Bobot ekstrak yang diperoleh adalah g dari 90 g bahan serbuk yang
D.Hasil Fraksinasi
Bahan ekstrak yang diperoleh memiliki berbagai jenis zat yang terlarut
didalamnya. Fraksinasi dilakukan untuk membagi ekstrak yang telah diperoleh
menjadi jumlah senyawa yang lebih kecil. Dalam penelitian ini, fraksi yang diteliti
adalah fraksi etil asetat. Sebelum fraksinasi, ekstrak etanol kental dilarutkan dengan
air hangat agar mudah difraksi. Fraksinasi diawali dengan pencucian ekstrak dengan
washbensin untuk membersihkan pengotor nonpolar yang mungkin terbawa seperti
lapisan lilin dan juga klorofil.
Pencucian washbensin terhadap ekstrak menggunakan prinsip ekstraksi
cair-cair. Ektraksi cair-cair prinsip like dissolve like sehingga zat yang nonpolar akan
terbawa dalam pelarut nonpolar dan begitu juga sebaliknya. Pencucian dilakukan
dalam corong pisah. Prinsip pemisahan larutan dalam corong pisah menggunakan
perbedaan berat jenis antar cairan. Washbensin memiliki berat jenis yang lebih kecil
dibandingkan air, sehingga akan berada diatas permukaan air. Fase air kemudian
diambil dan fase washbensin dibuang, dan fase air siap difraksi dengan etil asetat.
Fraksi etil asetat diperoleh dengan menggunakan proses yang sama seperti
pada proses pencucian dengan washbensin. Etil asetat dicampur dengan hasil
pencucian dengan corong pisah. Etil asetat berada diatas permukaan air karena berat
jenis yang lebih kecil. Senyawa polar yang larut air seperti vitamin akan terbawa
asetat dan identifikasinya dari batang tanaman menyatakan dari fraksi etil asetat dapat
mengambil golongan flavonoid.
Etil asetat akan terpisah diatas permukaan air. Fraksi etil asetat yang
dihasilkan berupa cairan encer yang memilki warna orange cerah. Fraksi yang
diperoleh diuapkan dengan vacuum rotary evaporator. Fraksi kental yang diperoleh
ditimbang dan diperoleh 0,31 g, dan dihitung rendemen proses fraksi 0,34 %.
E.Uji Pendahuluan
Uji pendahuluan bertujuan untuk melihat secara kualitatif adanya aktivitas
antioksidan dan juga adanya senyawa fenolik dalam fraksi etil asetat. Uji
pendahuluan ini penting karena sebagai orientasi keberadaan dari kandungan yang
akan diteliti yaitu senyawa fenolik dan adanya aktivitas antioksidan dari fraksi etil
asetat ekstrak etanol daun trengguli.
1. Hasil uji kualitatif antioksidan
Uji kualitatif antioksidan bertujuan untuk melihat adanya aktivitas
antioksidan dari fraksi etil asetat ekstrak etanol daun trengguli. Uji kualitatif
dilakukan dengan menambahkan DPPH (1,1-diphenil-2-picrylhidrazil) dalam tabung
berisi fraksi cair. Pada keadaan tidak terdapat antioksidan, DPPH akan berwarna
ungu terang. Reaksi antara DPPH dengan senyawa antioksidan akan menyebabkan
terjadi penurunan intensitas warna DPPH. Pelaksanaan uji kualitatif aktivitas
antioksidan menggunakan metanol sebagai kontrol negatif dan kuersetin sebagai
Gambar 4. Uji kualitatif antioksidan B= blanko +DPPH, A=kuersetin+ DPPH, C= fraksi etil asetat ekstrak etanol+DPPH
Hasil uji kualitatif menunjukkan terjadi perubahan warna fraksi + DPPH
menjadi kekuningan. Hasil yang sama terjadi juga pada kontol positif sedangkan
kontrol negatif tetap berwarna ungu terang. Perubahan warna yang terjadi
menunjukkan adanya reaksi antara senyawa dalam fraksi dengan DPPH. Dari hasil
tersebut dapat disimpulkan bahwa fraksi etil asetat ekstrak etanol daun trengguli
memilki aktivitas antioksidan.
2. Hasil uji kualitatif fenolik
Uji kualitatif fenolik bertujuan untuk melihat apakah dalam fraksi etil asetat
ekstrak etanol memilki kandungan senyawa fenolik. Pengujian kualitatif dilakukan
dengan menggunakan reagen Folin Ciocalteu yang ditambahkan ke dalam fraksi cair.
Keberadaan senyawa fenolik akan ditunjukkan dari perubahan warna fraksi dari yang
sebelumnya orange cerah menjadi biru, akibat dari reaksi gugus fenolik dengan
senyawa Folin Ciocalteu.
Pengujian yang dilakukan menggunakan pembanding berupa kontrol
kuersetin, dan metanol. Kontrol kuersetin sebagai kontrol positif sedangkan metanol
sebagai kontrol negatif. Hasil uji kualitatif menunjukkan terjadi pada fraksi etil asetat
terjadi perubahan warna menjadi biru tua, setelah ditambahkan reagen Folin
Ciocalteu, perubahan yang sama juga terjadi pada kontrol positif kuersetin, dan pada
metanol tidak terjadi perubahan warna. Dari uji kualitatif yang telah dilakukan
disimpulkan bahwa fraksi etil asetat ekstrak etanol daun trengguli memiliki
kandungan senyawa fenolik.
Gambar 5. Uji kualitatif fenolik. A= blanko +Folin Ciocalteu, B= asam galat+Folin Ciocalteu, C= fraksi asetat ekstrak etanol +Folin Ciocalteu
F. Optimasi Metode Pengukuran Aktivitas Antioksidan 1. Hasil pengukuran panjang gelombang maksimum
Pengukuran panjang gelombang maksimum bertujuan untuk mengukur pada
panjang gelombang berapa yang dapat memberikan serapan atau absorbansi
maksimum. Penentuan panjang gelombang maksimum dilakukan terhadap DPPH,
karena yang akan diukur adalah penurunan kadar absorbansi yang terjadi saat DPPH
C
berinteraksi dengan senyawa antioksidan. Panjang gelombang untuk absorbansi
maksimum, panjang gelombang yang digunakan bervariasi pada 515 nm, 518, dan
520 nm. Akan tetapi, nilai dari absorbansi absolut tidaklah penting, panjang
gelombang dapat diatur sesuai dengan panjang gelombang yang memberikan
absorbansi maksimum pada instrumen yang digunakan ( Molyneux, 2004).
Pengukuran panjang gelombang maksimum menggunakan kontrol DPPH
dengan tiga tingkat konsentrasi. DPPH kontrol tersebut discan absorbansinya pada
range panjang gelombang 400-600 nm.
Tabel II. Hasil pengukuran λ max DPPH
Dari hasil pengukuran diperoleh λ max dari DPPH adalah 515,5. Panjang gelombang yang diperoleh ini dianggap mampu memberikan absorbansi maksimal
sesuai dengan instrumen yang digunakan. Panjang gelombang ini digunakan untuk
mengukur operating time dan kurva seri baku dan sampel fraksi.
2. Hasil pengukuran Operating Time
Operating time adalah waktu yang diperlukan oleh dua senyawa untuk
mencapai reaksi optimal. Reaksi yang optimal ditunjukkan dari perubahan absorbansi
menjadi stabil pada pengukuran dengan spektrofotometer. Reaksi yang terjadi antara
senyawa antioksidan dengan DPPH akan menyebabkan penurunan absorbansi DPPH Konsentrasi DPPH λ max terukur (nm) Rata-rata
0,02 Mm 515,5
515,5 0,06 Mm 515,5
dan warna ungu DPPH akan memudar. Pengukuran operating time bertujuan
mengurangi kesalahan pengukuran.
Pengukuran operating time dilakukan dengan mengukur absobansi dari
sampel setiap 5 menit selama 60 menit atau 1 jam. Pengambilan absorbansi tiap 5
menit bertujuan untuk mempermudah pelaksanaan percobaan. Waktu yang
disarankan untuk reaksi DPPH menurut Molyneux (2004) adalah 30 menit. Tetapi
karena adanya perbedaan jenis dan kekuatan antioksidan disarankan untuk menguji
dulu hingga reaksi optimal.
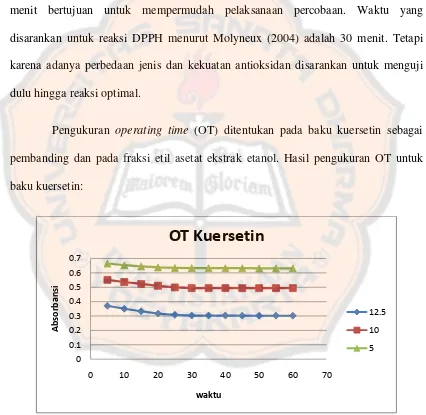
Pengukuran operating time (OT) ditentukan pada baku kuersetin sebagai
pembanding dan pada fraksi etil asetat ekstrak etanol. Hasil pengukuran OT untuk
baku kuersetin:
Gambar 6. Operating time dari baku kuersetin
Gambar 7. Operating time fraksi etil asetat ekstrak etanol
Dari data yang diperoleh (Gambar 6 dan 7) diketahui telah terjadi kestabilan
penurunan konsentrasi mulai dari menit ke-30. Setelah mencapai 30 menit, terjadi
perubahan yang walaupun tidak besar tetapi dapat dikatakan mulai stabil. Kesimpulan
yang diperoleh OT untuk percobaan ini dicapai pada menit ke-30. Untuk seterusnya
pengujian dilakukan dengan OT yang telah berhasil disimpulkan.
G.Validasi Metode Pengukuran Aktivitas Antioksidan
Validasi metode analisis merupakan suatu penilaian dari suatu metode
apakah telah memenuhi persyaratan yang ditentukan atau tidak. Kaidah-kaidah
metode analisis yang perlu diperhatikan adalah linearitas, presisi, akurasi dan
spesifisitas pengukuran dari suatu metode analisis. Linearitas digunakan untuk
melihat apakah kurva seri telah memiliki pengukuran yang linier.
1. Linearitas
Linearitas dari data dilihat dari koefisien relatif dari persamaan regeresi
linier dari data kurva seri baku maupun kurva seri fraksi etil asetat ekstrak etanol.
Menurut Kingston (2004) syarat linearitas apabila R (coefficient relative) persamaan
kurva baku mencapai 0,99 atau mendekati nilai 1.
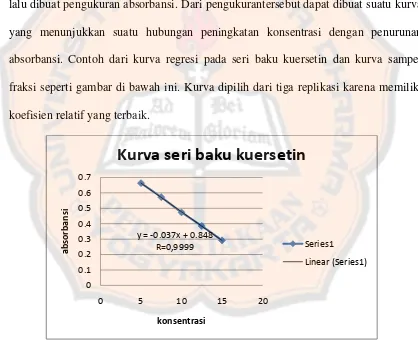
Regresi linier diperoleh dari membuat seri larutan dengan range 80-120%
lalu dibuat pengukuran absorbansi. Dari pengukurantersebut dapat dibuat suatu kurva
yang menunjukkan suatu hubungan peningkatan konsentrasi dengan penurunan
absorbansi. Contoh dari kurva regresi pada seri baku kuersetin dan kurva sampel
fraksi seperti gambar di bawah ini. Kurva dipilih dari tiga replikasi karena memiliki
koefisien relatif yang terbaik.
Gambar 8. Kurva seri baku
Gambar 9. Kurva seri fraksi etil asetat ekstrak etanol
Kurva seri baku menunjukkan nilai koefisien relasi (R) menunjukkan 0,999.
Nilai R tersebut telah mencapai nilai 0,99 atau mendekati 1 sehingga dapat dikatakan
linear. Dari kurva seri fraksi asetat ekstrak etanol, koefisien relasi (R) dari persamaan
kurva tersebut adalah 0,999. Nilai R terebut dianggap memenuhi syarat linearitas,
karena R mencapai 0,99 atau mendekati nilai 1. Kesimpulan yang dapat diambil,
metode yang digunakan memiliki koefisien relasi yang baik dan menghasilkan data
yang linier
2. Presisi
Presisi dari metode dilihat dari Coefficient Variable (CV), presisi
menunjukkan bahwa dalam beberapa kali pengukuran variasi antara hasil pengukuran
konsentrasi yang sama tidak terlalu jauh. Semakin tinggi rentangnya, menunjukkan
bahwa metode menghasilkan data yang kurang konsisten, atau bervariasi.
Tabel III. Hasil CV dari sampel bahan baku pembanding
memiliki rentang 0,76%-4,14%. Berdasarkan Kingston (2004) menunjukkan rentang
konsentrasi di bawah 0,1% sebaiknya memiliki rentang CV<20%., sehingga CV
terukur dapat dinyatakan menunjukkan metode DPPH memiliki presisi yang baik
dalam pengukuran baku. Data dari CV sampel fraksi etil asetat ekstrak etanol,
ditunjukkan dalam Tabel IV di bawah ini. Data CV dari sampel menggunakan data
yang diperoleh dari larutan seri fraksi etil asetat ekstrak etanol.
Tabel IV. Hasil CV dari sampel fraksi etil asetat ekstrak etanol
Berdasarkan nilai CV yang diperoleh dari bahan baku pembanding memiliki
rentang 0,79%-3,35%. Menurut Kingston (2004) menunjukkan rentang konsentrasi di
bawah 0,1% sebaiknya memiliki rentang CV<20%. Sehingga CV terukur dapat
dinyatakan menunjukkan metode DPPH memiliki presisi yang baik dalam
pengukuran fraksi etil asetat ekstrak etanol daun trengguli.
3. Spesifisitas
Spesifisitas melihat apakah metode yang digunakan dapat secara spesifik
mengukur zat uji yang akan diukur. Untuk melihat spesifisitas pada alat yang
digunakan adalah dengan melihat spektra dari pelarut, larutan baku, dan larutan
fraksi. Pengamatan pada spektra menunjukkan tidak terdapat puncak atau peak pada
range pengukuran panjang gelombang yang digunakan untuk mengukur DPPH
sehingga tidak terdapat gangguan dari fraksi etil asetat ekstrak etanol, baku maupun
dari pelarut. Kesimpulan yang dapat diperoleh, metode pengukuran aktivitas
antioksidan dikatakan spesifik dalam mengukur absorbansi DPPH.
H.Hasil Pengukuran Aktivitas Antioksidan.
Setelah data optimasi diperoleh pengukuran aktivitas antioksian dapat
dilakukan. Uji aktivitas antioksidan yang dilakukan menggunakan
1,1-diphenyl-2-pycrilhidrazil untuk mengukur kemampuan suatsu bahan menghambat radikal.
Pengukuran aktivitas antioksidan dalam penelitian ini akan mengukur besarnya IC50
dari baku kuersetin sebagai pembanding dan IC50 dari fraksi etil asetat ekstrak etanol
dalam menghambat 50% aktivitas DPPH (Molyneux, 2004). Untuk memperoleh IC50
masing- masing sampel diperlukan membuat larutan seri dari baku dan juga fraksi.
Metode DPPH memiliki prinsip dari penurunan larutan radikal DPPH ketika
terdapat keberadaan antioksidan pendonor hidrogen (Wangcharoen dan Wallaya,
2007). DPPH memiliki sifat sebagai radikal bebas stabil dengan adanya delokalisasi
elektron bebas diseluruh molekul, sehingga molekul tidak berubah seperti halnya
radikal bebas lainnya (Molyneux, 2004). Ketika DPPH dicampur dengan zat yang
memiliki donor hidrogen, DPPH akan berubah menjadi bentuk tereduksinya yang
memilki warna kuning pucat karena masih adanya gugus pycryl.
Gambar 10. Perubahan DPPH akibat adanya antioksidan, Ket: AH= antioksidan
IC50 diperoleh dengan mengukur absorbansi seri larutan dari sampel yang
diukur sehingga akan diperoleh persamaan regresi dari hubungan persentase daya
hambat absorbansi sampel dengan konsentrasi dari sampel yang diukur. Persamaan
yang dapat menghambat DPPH sebesar 50%. Semakin kecil konsentrasi yang
dibutuhkan aktivitas antioksidan dari sampel yang diukur semakin kuat.
Baku yang digunakan sebagai pembanding adalah kuersetin. Kuersetin
digunakan karena merupakan salah satu konstituen flavonoid dari tanaman yang
diketahui memiliki aktivitas antioksidan. Baku pembanding ini digunakan sebagai
pembanding dari kekuatan aktivitas antioksidan fraksi etil asetat ekstrak etanol daun
trengguli. Kuersetin mampu menurunkan intensitas warna dari DPPH yang
membuktikan kalau kuersetin merupakan antioksidan yang cukup poten.
Data dari perolehan IC (Inhibition Concentration) disajikan dalam Tabel di
bawah ini. Tabel V menunjukkan perolehan IC yang dihitung dalam kurva kalibrasi
dari baku pembanding. Dari Tabel tersebut terlihat semakin tinggi kandungan
kuersetin daya penghambatannya terhadap DPPH akan lebih besar sehingga
absorbansi yang dihasilkan akan semakin kecil. Hal yang sama juga berlaku untuk
Tabel VII yang menunjukkan IC dari sampel fraksi etil asetat ekstrak etanol daun
trengguli. IC50 dari kuersetin ditampilkan pada Tabel VI dan IC50 sampel fraksi etil
Tabel V. Hasil perolehan IC dan persamaan regresi linier baku pembanding