SKRIPSI
FORMULASI DAN APLIKASI EDIBLE COATING BERBASIS PATI SAGU DENGAN PENAMBAHAN VITAMIN C PADA PAPRIKA
(Capsicum annuum varietas Athena)
Oleh :
VERONICA GUNAWAN F24051191
2009
FAKULTAS TEKNOLOGI PERTANIAN INSTITUT PERTANIAN BOGOR
FORMULASI DAN APLIKASI EDIBLE COATING BERBASIS PATI SAGU DENGAN PENAMBAHAN VITAMIN C PADA PAPRIKA
(Capsicum annuum varietas Athena)
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN Pada Departemen Ilmu dan Teknologi Pa ngan,
Fakultas Teknologi Pertanian, Institut Pertanian Bogor
Oleh :
VERONICA GUNAWAN F24051191
2009
DEPARTEMEN ILMU DAN TEKNOLOGI PANGAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
INSTITUT PERTANIAN BOGOR FAKULTAS TEKNOLOGI PE RTANIAN
FORMULASI DAN APLIKASI EDIBLE COATING BERBASIS PATI SAGU DENGAN PENAMBAHAN VITAMIN C PADA PAPRIKA
(Capsicum annuum varietas Athena) SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar SARJANA TEKNOLOGI PERTANIAN pada Departemen Ilmu dan Tek nologi Pangan
Fakultas Teknologi Pertanian Institut Pertanian Bogor
Oleh :
VERONICA GUNAWAN F24051191
Dilahirkan pada tanggal 21 Februari 1987 Di Medan
Tanggal lulus: 1 September 2009
Menyetujui, Bogor, 7 September 2009
Prof. Dr. Ir. Rizal Syarief, DESS. Miskiyah, SPt., MP.
Dosen Pembimbing Akademik 1 Dosen Pembimbing Akademik 2
Mengetahui,
Dr. Ir. Nurheni Sri Palupi, M.Si
Sekretaris Departemen Ilmu dan Teknologi Pangan a.n. Ketua Departemen Ilmu dan Teknologi Pangan
Veronica Gunawan. F24051191. Formulasi dan Aplikasi Edible Coating Berbasis Pati Sagu dengan Penambahan Vitamin C pada Paprika ( Capsicum
annuum varietas Athena). Dibawah bimbingan Rizal Syarief dan Miskiyah
(2009)
RINGKASAN
Sayuran menjadi penting untuk memenuhi kebutuha n pangan penduduk karena menjadi salah satu penyedia gizi berupa serat, vitamin, protein, dan mineral yang dibutuhkan oleh tubuh manusia. Seiring perkembangan zaman, kesadaran masyarakat akan kesehatan serta pentingnya nilai gizi dalam sayuran juga semakin meningkat. Permintaan produk buah -buahan dan sayuran baik di dalam maupun di luar negeri cenderung terus meningkat. Salah satu kendala utama ekspor hortikultura adalah produktivitas tanaman dan kualitas yang rendah.
Paprika merupakan salah satu jenis say uran yang memiliki prospek pasar yang terbuka dan cukup luas baik pasar lokal maupun ekspo r. Namun, paprika merupakan jenis sayuran yang tidak awet ( perishable commodity ) karena umur simpannya 1 sampai 2 minggu sehingga diperlukan teknologi penanganan pasc a panen yang baik (Kader, 1992). Salah satu teknologi penanganan pasca panen yang dapat diterapkan pada paprika adalah edible coating berbasis pati sagu. Penelitian dilakukan untuk memperoleh formulasi edible coating yang terbaik sehingga dapat memperpanja ng umur simpan paprika.
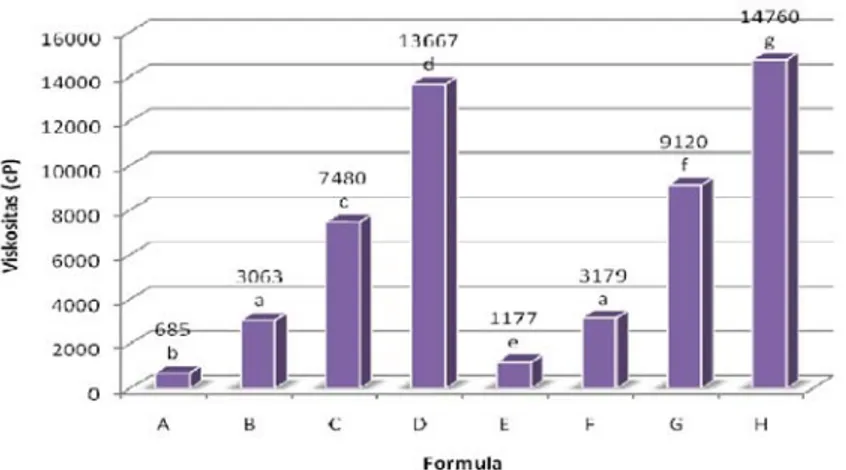
Penelitian ini diawali dengan karakterisasi pati sagu sebelum digunakan. Setelah itu dicari formulasi yang terbaik dengan perlakuan konsentrasi CMC (0,5%; 1,0%; 1,5%; dan 2,0%) dan konsentrasi gliserol (10% dan 20%). Formula edible film yang terpilih adalah gliserol 10% dan CMC 1%. Edible film tersebut memiliki viskositas larutan film sebesar 3.063 cP; Aw 0,51; nilai L sebesar 34,95; O2TR sebesar 1,16 cc/m2/24 jam; WVTR sebesar 225, 48 g/m2/24 jam; ketebalan 0,19 mm; dan kuat tarik se besar 69,79 kgf/cm2.
Penelitian utama meliputi aplikasi edible coating pada paprika dengan metode pencelupan dan mengamati perubahan mutu paprika selama penyimpanan. Perlakuan yang diberikan pada penelitian ini adalah konsentrasi vitamin C (0%; 0,5%; dan 1,0%), lama pencelupan (3 dan 5 menit), dan s uhu penyimpanan paprika (8oC dan 20oC). Parameter mutu yang digunakan adalah mutu fisik (susut bobot, warna, dan kekerasan), mutu kimia (kadar air dan vitamin C) , mutu mikrobiologi paprika (a ngka lempeng total), dan mutu organoleptik (tekstur, warna, aroma, rasa, dan penerimaan umum). Pengamatan dilakukan sampai sampel yang diamati mengalami kerusakan.
Aplikasi coating pada paprika menunjukkan bahwa pada suhu 20oC perlakuan coating (baik tanpa vitamin C maupun dengan penambahan vitamin C) mampu memperpanjang umur simpan paprika selama 3 hari (untuk paprika yang dicoating tanpa penambahan vitamin C dan dengan penambahan vitamin C 1,0%) dan 5 hari (untuk paprika yang dicoating dengan penambahan vitamin C 0,5%). Penambahan vitamin C 0,5% lebih efektif dibandingkan vitamin C 1,0%.
Pada suhu 8oC perlakuan coating tanpa penambahan vitamin C tidak mampu memperpanjang masa simpan paprika. Namun, adanya penambahan vitamin C pada coating efektif memperpanjang umur simpan papr ika selama 3 hari (untuk paprika yang dicoating dengan penambahan vitamin C 0,5% selama 3 menit ), 6 hari (untuk paprika yang dicoating dengan penambahan vitamin C 0,5% selama 5 menit) dan 7 hari (untuk paprika yang dicoating dengan penambahan vitamin C 1,0% selama 3 dan 5 menit ). Penambahan vitamin C 1,0% lebih efektif dibandingkan vitamin C 0,5%.
Penyimpanan pada suhu rendah lebih efektif menurunkan laju kerusakan dari segi kimia, yaitu kadar air dan segi fisik, yaitu susut bobot, warna, dan kekerasan dibandingkan perlakuan coating. Penambahan vitamin C ke dalam larutan coating efektif dalam menurunkan laju degradasi vitamin C serta meningkatkan kandungan awal vitamin C paprika. Kombinasi perlakuan coating dan suhu penyimpanan yang rendah efektif dalam memp erpanjang umur simpan paprika.
RIWAYAT HIDUP
Penulis dilahirkan di Medan, Sumatera Utara pada tanggal 21 Februari 1987. Penulis merupakan anak pertama dari tiga bersaudara anak dari pasangan Lim Benny Gunawan dan Nun Maliah Nginda.
Penulis menempuh pendidikan di TK W.R. Supratman (1990 -1993), SD W.R. Supratman (1993-1996), SD Karya Iman (1996 -1999), SMP Karya Iman (1999-2002), dan SMA Dian Harapan (2002 -2005). Pada tahun 2005, penulis diterima sebagai mahasiswa di Institut Pertanian Bogor melalui jalur SPMB (Seleksi Penerimaan Mahasiswa Baru) untuk mengikuti Tahap Persiapan Bersama (TPB) selama 1 tahun dan pada tahun 2006 diterima sebagai mahasiswa di Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Selama masa perkuliahan, penulis terlibat dalam organisasi -organisasi kemahasiswaan seperti Unit Kegiatan Mahasiswa Keluarga Mahasiswa Buddhis IPB (UKM KMB-IPB), Himpunan Mahasiswa Teknologi Pangan (HIMITEPA), serta serta aktif di berbagai kepan itiaan. Penulis juga berkesempatan untuk mengikuti berbagai kegiatan non akademis seperti Pela tihan Sistem Management ISO 9001:2000 dan ISO 22000:2005, dan beberapa seminar. Pada tahun 2007, penulis menjadi salah satu wakil dari Institut Pertanian Bogor da lam Pekan Ilmiah Mahasiswa Nasional sebagai salah satu peserta Debat Bahasa Mandarin yang diadakan oleh Departemen Pendidikan Tinggi (DIKTI) dan National Student Conference on Food Science and Technology yang diadakan oleh Universitas Soegijapranata di Semarang. Pada tahun 2009, penulis melakukan penelitian di Balai Besar Pengembangan dan Penelitian Pascapanen Pertanian mengenai “Formulasi dan Aplikasi Edible Coating Berbasis Pati Sagu dengan Penambahan Vitamin C pada Paprika ( Capsicum annuum varietas Athena)” di bawah bimbingan Prof. Dr. Ir. Rizal Syarief, DESS dan Miskiyah, SPt., MP. Penelitian ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian pada Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuha n Yang Maha Esa atas berkat dan anugerah-Nya sehingga penulis selalu diberikan kemudahan dalam menyelesaikan skripsi ini. Dalam kesempatan ini pula, penulis ingin mengucapkan terima kasih yang sangat besar kepada semua pihak yang turut membantu penulis selama menjalani masa perkuliahan, penelitian, hingga penyele saian skripsi ini sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian IPB.
Penulis mengucapkan terima kasih kepada:
1. My Family : papa, mama, dan adik -adikku, Fransisca dan Freddy yang selalu mendoakan dan memotivasi penulis untuk memberi yang terbaik dalam menyelesaikan penelitian dan skripsi.
2. Prof. Dr. Ir. Rizal Syarief, DESS dan Miskiyah, SPt., MP. selaku dosen pembimbing yang telah memberikan bimbingan, arahan, dan saran selama penelitian dan penyelesaian skripsi ini.
3. Widaningrum, STP. dan Ir. Christina Winarti, MA selaku tim koodinator proyek penelitian ‘Formulasi Dan Aplikasi Edible Coating Pada Paprika (Capsicum annuum) Untuk Meningkatkan Masa Simpan Minimal 10 Hari ’ atas kesempatan yang diberikan pada penulis untuk terlibat dalam proyek ini, untuk arahan, bimbingan, dan kesaba rannya selama masa penelitian .
4. Dr. Ir. Yadi Haryadi, M. Sc. selaku dosen penguji yang telah memberikan banyak masukan bagi perbaikan skripsi ini.
5. Sahabat terbaik dan teman sekamarku : Mervina, Teresia, Vidya, Stella, dan Catherine yang selalu memberi semangat, dukungan, dan bantuannya selama penulis melaksanakan penelitian, seminar, skripsi, dan sidang. I won’t forget what we’ve been through …
6. My Partner, eping (Eveline) atas kerja sama, bantuan, dukungan, dan motivasi kepada penulis selama melaksanakan penelitian, seminar, skripsi, mengurus sidang, dan memperbaiki skripsi ini bersama.
7. Sahabat-sahabat di Bogor: Ci Bhe -bhe, Bobo, Beli, Tata, Cha -cha, Iso, Siska, Lissa, Marcel, Angki, Mike, Waggy, Wiwi, Kak Wing atas dukungan dan
bantuan yang diberikan selama penulis melaksanakan penelitian, seminar, skripsi, dan sidang.
8. Teman-teman UKM KMB-IPB 42: Angie, Andi, Deni, Fransisca, Glenn, Goto, Kenchi, Lisa, Puteri, Suhendri, Stefhani, dan Vera atas dukungan dan motivasi yang diberikan.
9. Pihak-pihak Balai Besar Pengembangan dan Penelitian Pascapanen Pertan ian, Cimanggu-Bogor : Pak Tri, Pa Yudi, Pa Ato, Pa Sis, Mbak Ika, Mbak Citra, dan Bu Tisna atas bantuan dan masukannya selama melakukan penelitian di Balai.
10.Teman-teman ITP’42 yang tidak dapat disebutkan satu persatu atas pengalaman yang menyenangkan da n waktu yang telah dilewatkan bersama penulis selama 3 tahun ini selama kuliah.
11.Dosen, Staf Administrasi di UPT, Staf Perpustakaan PITP, LSI, dan PAU atas bantuannya bagi kelancaran selama penulis kuliah di IPB.
12.Pihak-pihak lain yang tidak dapat dise butkan satu persatu yang telah membantu penulis baik secara langsung maupun tidak langsung dalam penyusunan skripsi ini.
Penulis juga mohon maaf apabila selama ini banyak kesalahan dan sikap yang tidak berkenan kepada semua pihak.
Akhir kata penulis menyad ari bahwa skripsi ini masih jauh dari sempurna dan tidak lepas dari berbagai kekurangan. Penulis berharap semoga skripsi ini dapat bermanfaat bagi seluruh pihak yang membutuhkan dan terhadap perkembangan Ilmu dan Teknologi, khususnya bidang Ilmu dan Teknologi Pangan.
Bogor, 5 September 2009 Penulis
DAFTAR ISI
Halaman
KATA PENGANTAR ... ...i
DAFTAR ISI ... .iii
DAFTAR TABEL ... ..v
DAFTAR GAMBAR ... .vi
DAFTAR LAMPIRAN ... .viii
I. PENDAHULUAN A. LATAR BELAKANG... 1
B. PERUMUSAN MASALAH ... 2
C. TUJUAN DAN MANFAAT ... 3
1. Tujuan Penelitian ... 3
2. Manfaat Penelitian ... 3
II. TINJAUAN PUSTAKA A. PAPRIKA (Capsicum annuum) ... .4
B. SIFAT FISIOLOGIS PAPRIKA SELAMA PENYIMPANAN ... 6
C. EDIBLE COATING ... 7
D. EDIBLE COATING BERBASIS POLISAKARIDA ... 9
E. PATI SAGU ... .9
F. GLISEROL SEBAGAI PLASTICIZER ... 10
G. CARBOXYMETHYL CELLULOSE (CMC) ... 11
H. MINYAK BIJI BUNGA MATAHARI ... 12
I. ANTIOKSIDAN ... 14
J. VITAMIN C ... 16
III. METODOLOGI PENELITIAN A. BAHAN DAN ALAT ... 18
B. METODE PENELITIAN ... 18
1. Penelitian Pendahuluan ... 21
2. Penelitian Utama ... 24
3. Pengamatan dan Pengujian ... 27
3.2 Karakteristik Edible Film ... 31
3.3 Metode Analisis Aplikasi Edible Coating pada Paprika ... 36
IV. HASIL DAN PEMBAHASAN A. PENELITIAN PENDAHULUAN ... 39
1. Karakteristik Pati Sagu... 39
2. Karakteristik Edible Film ... 39
3. Penentuan Formulasi Edible Coating... 52
B. PENELITIAN UTAMA ... 53
1. Aplikasi Edible Coating dan Umur Simpan... 53
2. Karakteristik Organoleptik ... 57
3. Sifat Fisik ... 61
4. Sifat Kimia ... 70
5. Analisis Mikrobiologi (Total Plate Count) ... 75
V. KESIMPULAN DAN SARAN A. KESIMPULAN ... 77
B. SARAN ... 78
DAFTAR PUSTAKA ... 79
DAFTAR TABEL
Halaman Tabel 1. Kandungan gizi paprika ( Capsicum annum)
tiap 100 gram buah segar ... 5
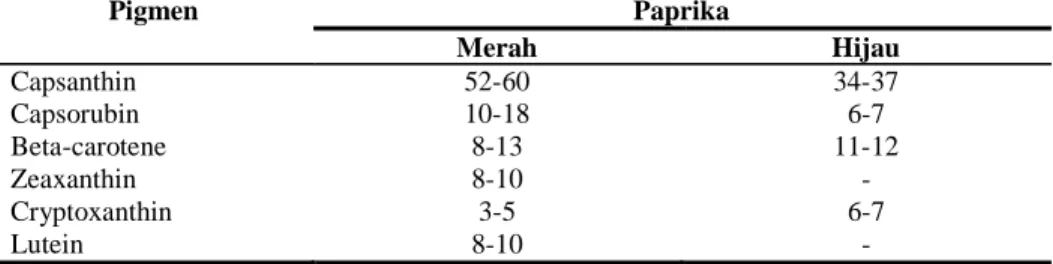
Tabel 2. Komponen pigmen paprika (berdasarkan persen total karotenoid) ... 6
Tabel 3. Komposisi kimia pati sagu setiap 100 g ... 10
Tabel 4. Komposisi dan karakt eristik fisik minyak biji bunga matahari ... 13
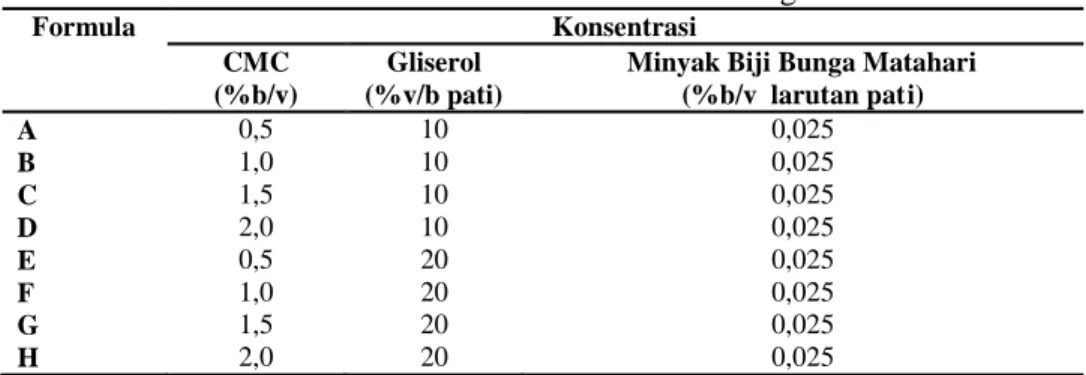
Tabel 5. Formulasi konsentrasi CMC dan gliserol ... 21
Tabel 6. Perlakuan yang digunakan dalam penelitian u tama ... 24
Tabel 7. Ambang Batas Toleransi Aktivitas Air (aw) untuk Pertumbuhan dan Perkembangan Mikroorganism e ... 42
Tabel 8. Hasil Karakterisasi Film... 52
Tabel 9. Hasil Karakterisasi Paprika ... 53
DAFTAR GAMBAR
Halaman
Gambar 1. Buah Paprika (Capcisum annuum)... ..5
Gambar 2. Paprika Merah ... ..6
Gambar 3. Reaksi Fenton dan Haber-Weiss ... 15
Gambar 4. Reaksi ion logam yang terlibat dalam proses oksidasi. ... 16
Gambar 5. Tahapan penelitian aplikasi edible film pada paprika ... 20
Gambar 6. Proses pembuatan edible film (kontrol)... 23
Gambar 7. Tahapan aplikasi edible coating pada paprika ... 26
Gambar 8. Micro-cal Messmer ... 32
Gambar 9. Tensile Strength and Elongation TesterStograph-MI Toyoseiki... ...33
Gambar 10. Gas Transmission Rate Tester Speedivac 2………...35
Gambar 11. Water Vapor Transmission Rate Tester Bergerlahr ... 36
Gambar 12. Nilai rata-rata hasil pengukuran viskositas l arutan edible film ... 40
Gambar 13. Nilai rata-rata hasil pengukuran warna edible film ... 41
Gambar 14. Nilai rata-rata hasil pengukuran Aw edible film rata-rata ... 43
Gambar 15. Nilai rata-rata skor kesukaan panelis terhadap warna film... 44
Gambar 16. Nilai rata-rata skor kesukaan panelis terhadap kejernihan film... 45
Gambar 17. Nilai rata-rata skor kesukaan panelis terhadap tekstur film... 46
Gambar 18. Nilai rata-rata skor kesukaan panelis terhadap keregangan film ... 47
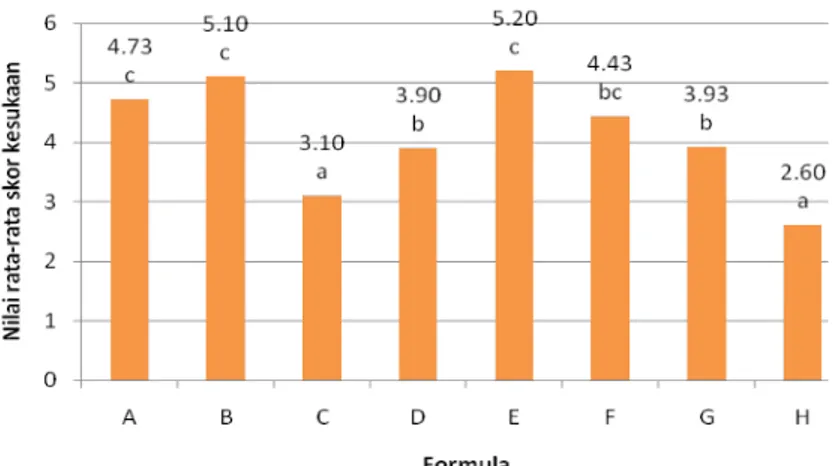
Gambar 19. Nilai rata-rata skor kesukaan panelis terhadap keseluruhan film ... 48
Gambar 20. Hasil pengukuran ketebalan film ... 49
Gambar 21. Hasil pengukuran kuat tarik film………... ...50
Gambar 22. Hasil pengukuran laju transmisi oksigen film ... 51
Gambar 23. Hasil pengukuran laju transmisi uap air film... 52
Gambar 24. Posisi warna paprika berdasarkan nilai a dan b. ... 53
Gambar 26. Kerusakan paprika akibat kapang ... 56
Gambar 27. Nilai rata-rata skor kesukaan terhadap warna paprika ... 57
Gambar 28. Nilai rata-rata skor kesukaan terhadap aroma paprika ... 58
Gambar 29. Nilai rata-rata skor kesukaan terhadap tekstur paprika ... 59
Gambar 30. Nilai rata-rata skor kesukaan terhadap rasa paprika ... 60
Gambar 31. Nilai rata-rata skor kesukaan terhadap keseluruhan paprika ... 61
Gambar 32. Susut bobot paprika penyimpanan pada suhu 20oC ... 63
Gambar 33. Susut bobot paprika penyimpanan pada suhu 8oC ... 64
Gambar 34. Kekerasan paprika penyimpanan pada suhu 20oC ... 67
Gambar 35. Kekerasan paprika penyimpanan pada suhu 8oC ... 67
Gambar 36. Skala hue ... 69
Gambar 37. Nilai hue paprika penyimpanan pada suhu 20oC ... 69
Gambar 38. Nilai hue paprika penyimpanan pada suhu 8oC ... 70
Gambar 39. Kadar air paprika penyimpanan pada suhu 20oC ... 71
Gambar 40. Kadar air paprika penyimpanan pada suhu 8oC ... 71
Gambar 41. Kadar vitamin C paprika penyimpanan pada suhu 20oC... 73
Gambar 42. Kadar vitamin C paprika penyimpanan pada suhu 8oC... 74
Gambar 43. Angka lempeng total paprika penyimpanan pada suhu 20oC... 76
DAFTAR LAMPIRAN
Halaman Lampiran 1. Kandungan gizi paprika ( Capsicum annuum)
tiap 100 g buah segar ---85
Lampiran 2. Komposisi dan karakteristik fisik minyak biji bunga matahari ---86
Lampiran 3. Data proksimat pati sagu ---87
Lampiran 4. Hasil pengukuran viskositas larutan film --- 88
Lampiran 5. Hasil pengukuran warna film ---89
Lampiran 6. Hasil pengukuran Aw ---89
Lampiran 7. Analisis statistik nilai viskositas larutan film ---90
Lampiran 8. Analisis statistik nilai warna film ---93
Lampiran 9. Analisis statistik nilai Aw film---96
Lampiran 10. Form uji organoleptik edible film---99
Lampiran 11. Hasil uji organoleptik warna edible film--- 100
Lampiran 12. Hasil uji organoleptik kejernihan edible film ---102
Lampiran 13. Hasil uji organoleptik tekstur edible film --- 104
Lampiran 14. Hasil uji organoleptik keregangan edible film ---106
Lampiran 15. Hasil uji organoleptik keseluruhan edible film ---108
Lampiran 16. Karakteristik paprika awal ---110
Lampiran 17. Form uji organoleptik paprika ---110
Lampiran 18. Hasil uji organoleptik warna paprika ---111
Lampiran 19. Hasil uji organoleptik aroma paprika ---113
Lampiran 20. Hasil uji organoleptik tekstur paprika ---115
Lampiran 21. Hasil uji organoleptik rasa paprika ---117
Lampiran 22. Hasil uji organoleptik keseluruhan paprika ---119
Lampiran 23. Hasil pengukuran susut bobot ---121
Lampiran 24. Hasil pengukuran kekerasan ---123
Lampiran 25. Hasil pengukuran warna ---125
Lampiran 26. Hasil pengukuran kadar air ---127
Lampiran 27. Hasil pengukuran vitamin C ---128
I. PENDAHULUAN
A. LATAR BELAKANG
Jumlah penduduk yang semakin bertambah menuntut tersedianya bahan pangan yang dapat memenuhi kebutuhan penduduk untuk kelangsungan hidupnya. Salah satu bahan pangan yang menjadi kebutuhan penduduk adalah sayuran. Sayuran menjadi penting untuk memenuhi kebutuhan pangan penduduk karena menjadi salah satu penyedia gizi berupa serat, vitamin, protein, dan mineral yang dibutuhkan oleh tubuh manusia. Hal ini seiring dengan perkembangan zaman, kesadaran masyarakat akan kesehatan, serta pentingnya nilai gizi dalam sayuran.
Permintaan produk buah -buahan dan sayuran baik di dalam maupun di luar negeri cenderung terus meningkat. Salah satu kendala utama ekspor hortikultura adalah produktivitas tanaman dan kualitas yang rendah. Negara pengimpor menuntut adanya sayuran segar yang bermutu tinggi baik untuk konsumsi segar maupun industri pengolahan, antara lain penampakan yang baik, relatif tahan lama, dan tidak cepat layu selama penyimpanan. Masalah mutu dan kualitas sayuran perlu menjadi perhatian mengingat sifat komoditas sayuran yang mudah rusak dan mudah busuk. Penanganan pasca panen yang baik termasuk salah satu usaha untuk dapat memperpanjang tingkat kesegaran sayuran.
Beberapa metode yang dapat dilakukan untuk memperpanjang masa simpan komoditas hortikultura, salah satunya dengan mengaplikasikan edible coating. Edible coating adalah suatu lapisan tipis yang rata, dib uat dari bahan yang dapat dikonsumsi, dan dapat berfungsi sebagai barrier agar tidak kehilangan kelembaban, bersifat permeabel terhadap gas -gas tertentu, serta mampu mengontrol migrasi komponen -komponen larut air yang dapat menyebabkan perubahan pigmen dan komposisi nutrisi sayuran (Kro chta, et al., 1994). Metode edible coating dapat memperpanjang umur simpan dan mempertahankan mutu produk yang di coating.
Penelitian edible film yang akan dilakukan pada penelitian ini adalah pembuatan edible film yang berasal dari pati sagu. Pati sagu mudah didapat dan
harganya lebih murah. Untuk meningkatkan stabilitas, menjaga nutrisi dan warna sayuran yang di coating, maka akan ditambahkan antioksidan. Antioksidan berfungsi untuk melindungi produk yang di coating agar terhindar dari ketengikan oksidatif, degradasi, dan penurunan mutu warna. Penelitian ini menggunakan vitamin C sebagai antioksidan. Vitamin C memiliki kemampuan untuk menangkap O2sehingga laju respirasi produk yang di coating berkurang. Selain itu, penambahan vi tamin C pada edible coating diharapkan dapat menurunkan laju degradasi vitamin C yang dimiliki oleh bahan yang di coating. Sayuran yang dijadikan sebagai objek penelitian ini adalah paprika.
Paprika merupakan salah satu sayuran yang memiliki prospek cerah. Walaupun bukan merupakan tanaman asli Indonesia, perubahan gaya hidup dan pola konsumsi penduduk khususnya di perkotaan menyebabkan permintaan terhadap paprika semakin meningkat. Paprika digolongkan sebagai jenis sayuran yang tidak awet ( perishable commodity), daya simpannya antara 1 sampai 2 minggu (Kader, 1992) sehingga aplikasi edible coating dari pati sagu dengan penambahan vitamin C diharapkan mampu mempertahankan mutu dan memperpanjang umur simpan paprika.
B. PERUMUSAN MASALAH
Paprika merupakan salah satu jenis komoditas sayuran yang konsumennya sebagian besar orang asing serta masyarakat Indonesia kalangan menengah dan atas. Jenis pasar yang banyak menyerap komoditas ini adalah pasar khusus seperti hotel, restoran, katering, dan pasar swalayan. Paprika mempunyai harga jual lebih tinggi daripada cabai biasa, yaitu kira -kira 3 hingga 5 kali harga cabai biasa.
Paprika memiliki prospek pa sar yang terbuka dan cukup luas baik pasar lokal maupun ekspor. Namun , paprika merupakan jenis sayuran yang tidak awet (perishable commodity) karena umur simpannya 1 sampai 2 minggu, sehingga diperlukan teknologi penanganan pasca panen yang baik. Salah satu teknologi penanganan pasca panen yang dapat diterapkan pada paprika adalah edible coating.
Dalam penelitian ini beberap a masalah dirumuskan untuk dicari pemecahannya, antara lain:
1. Menentukan formulasi edible film dari pati sagu 2. Mengetahui karakterisik edible film yang dihasilkan
3. Mengetahui pengaruh penambahan antioksidan , yaitu vitamin C ke dalam formula edible coating terhadap umur simpan produk dan mutu paprika setelah dicoating
C. TUJUAN DAN MANFAAT 1. Tujuan Penelitian
Penelitian ini bertujuan mempelajari pembuatan edible film dari pati sagu dengan penambahan Vitamin C, mempelajari karakteristik edible film dari pati sagu yang dihasilkan, dan pengaruh edible coating dengan penambahan vitamin C terhadap paprika untuk mempertahankan mutu dan memperpanjang umur simpan paprika tersebut.
2. Manfaat Penelitian
Dengan dilakukannya penelitian ini, diharapkan dap at diperolehnya teknologi penanganan pasca panen sayuran yang dapat mempertahankan mutu dan memperpanjang umur simpan paprika sehingga dapat meningkatkan daya saing produk sayuran Indonesia di pasar global.
II. TINJAUAN PUSTAKA
A. PAPRIKA (Capsicum annuum)
Tanaman Paprika berasal dari Amerika Tengah dan Amerika Selatan dimana banyak spesies yang telah dibudidayakan beratus tahun sebelum Colombus mendarat di benua tersebut (Alberta 2004; Wien 1997). Penanaman paprika menyebar ke Eropa dan Asia setel ah tahun 1500. (Van Winden, 1988). Walaupun termasuk tanaman tahunan, paprika dibudidayakan sebagai tanaman setahun di daerah beriklim subtropis, tetapi di daerah tropis kemungkinan akan tumbuh dan memberikan hasil selama lebih dari beberapa tahun (Wien, 1997).
Menurut klasifikasi tumbuhan, paprika ( Capsicum annuum) termasuk dalam (Prihmantoro dan Indriani, 2003) :
Divisio : Spermatophyta Subdivisio : Angiospemae Kelas : Dicotyledonae Ordo : Solanales Famili : Solanacea Genus : Capsicum
Spesies : Capsicum annuum
Paprika membutuhkan kondisi tertentu untuk pertumbuhannya, yaitu suhu 24 -30oC pada siang hari dan 9 -12oC pada malam hari. Meskipun demikian, tanaman paprika masih dapat bertahan pada suhu 38oC (Hartz, 2002). Di Indonesia, tanaman paprika co cok ditanam di dataran tinggi yang bersuhu 16 -25oC (Prihmantoro dan Indriani, 2003). Tanaman paprika baru mulai dibudidayakan di Indonesia pada tahun 1990. Propinsi Jawa Barat merupakan salah satu pusat penanaman paprika di Indonesia (Prabaningrum et al., 2002).
Bentuk buah paprika mirip lonceng, sehingga dinamakan bell pepper. Meskipun aroma buah paprika pedas menusuk, namun rasanya tidak pedas, bahkan cenderung manis sehingga disebut sweet pepper. Paprika pada umumnya dibedakan menurut bentuk, wa rna, dan ukuran. Pada umumnya bentuk paprika dibedakan menjadi dua bentuk, yaitu yang berbentuk blok
(blocky) atau lonceng (bell) dan yang berbentuk lonjong ( lamujo). Paprika dikelompokkan berdasarkan 4 warna utama, yaitu merah, hijau, kuning dan oranye (Gunadi et al., 2006). Berdasarkan ukuran buah dibedakan menjadi empat kategori, yaitu kecil (diameter buah 6,5-8 cm, bobot buah 120-160 g); sedang (diameter buah 7, 5-9,5 cm, bobot buah 160 -200 g); besar (diameter buah 9-11 cm, bobot buah 200-250 g); dan sangat besar (diameter buah > 11 cm, bobot buah > 250 g) (Hadinata, 2004).
Gambar 1. Buah paprika (Capsicum annuum)
Paprika (Capsicum annuum) mengandung sedikit protein, lemak, dan gula, tetapi banyak mengandung karoten dan se bagai sumber vitamin C dapat dilihat pada Tabel 1. Kandungan vitamin C pada paprika jauh lebih tinggi daripada buah jeruk (Morgan dan Lennard, 2000). Kandungan gizi paprika secara lengkap dapat dilihat pada Lampiran 1.
Tabel 1. Kandungan gizi paprika ( capsicum annuum) dalam 100 gram buah segar
Kandungan Gizi Paprika Merah Paprika Hijau Paprika Kuning Protein (g) Lemak total (g) Karbohidrat (g) Vitamin C (mg) Vitamin A (IU) 0,99 0,3 6,03 190 3.131 0,86 0,17 4,64 0,06 0,37 1 0,21 6,32 183,5 200 Sumber: anonim (2008)
Pada umumnya paprika dig unakan sebagai bumbu penyedap atau bahan masakan. Selain itu juga, paprika dapat digunakan sebagai zat pewarna makanan. Antosianin yang terkandung dalam paprika merupakan zat pewarna
makanan yang memiliki keunggulan dibandingkan dengan pewarna makanan yang berasal dari sumber makanan lain, yaitu lebih tahan suhu tinggi dan stabil pada kisaran pH lebar, yaitu 1 sampai 9 (Hartuti, 2004).
Tabel 2. Komponen pigmen paprika berdasarkan persen total karotenoid
Pigmen Paprika Merah Hijau Capsanthin Capsorubin Beta-carotene Zeaxanthin Cryptoxanthin Lutein 52-60 10-18 8-13 8-10 3-5 8-10 34-37 6-7 11-12 -6-7 -Sumber : Curl (1962) dalam Purseglove et al. (1981)
Gambar 2. Paprika merah
B. SIFAT FISIOLOGI PAPRIKA SELAMA PENYIMPANAN
Paprika termasuk kategori sayuran buah yang mudah rusak (perishable food). Paprika seperti buah-buahan dan sayuran pada umumnya, setelah dipanen akan mengalami perubahan kimia, fisik, serta organoleptik. Hal ini disebabkan aktivitas fisiologisnya masih tetap aktif, antara lain respirasi, sehingga akhirnya mengalami senesence dan pembusukan (Apandi, 1984).
Menurut Pantastico (1986), paprika merupakan komoditi ho rtikuktura yang cukup aman disimpan selama 3 -5 minggu pada suhu sekitar 7oC dan kelembaban relatif (RH) 85 -90%, tanpa adanya perlakuan tambahan. Pada
suhu yang lebih rendah yakni 0oC dan RH yang sama, paprika mampu bertahan sampai 4-6 minggu (Ditjen Pert. Tan. Pangan Deptan. RI, 1992).
Paprika memiliki laju etilen yang relatif rendah, sehingga pengaruhnya cukup kecil terhadap pembusukan selama kemasannya berventilasi baik (Ryall dan Lipton, 1972) dimana pada suhu 5oC paprika akan memproduksi gas e tilen sekitar 0,1-1,0 ml/kg/jam sehingga termasuk dalam kategori tingkat rendah (Hardenberg et al., 1986). Pola respirasi paprika digolongkan ke dalam resp irasi non-klimaterik (Kader, 1992 ). Paprika menghasilkan gas CO2yang sedikit/rendah, yakni 8 mg/kg/jam pada suhu 0oC. Menurut Robinson (1975), diacu dalam Kays (1991), p roduksi CO2 ini akan meningkat dengan naiknya suhu selama penyimpanan paprika. Laju produksi CO2 paprika dipengaruhi oleh ketersed iaan oksigen selama penyimpanan.
C. EDIBLE COATING
Menurut Gennadios dan Weller (1990), edible coating merupakan lapisan tipis yang dibuat dari bahan yang dapat dimakan. Metode untuk aplikasi coating pada buah dan sayuran terdiri dari beberapa cara, yakni metode pencelupan ( dipping), pembusaan, penyemprotan (spraying), penuangan (casting), dan aplikasi penetesan terkontrol. Metode pencelupan (dipping) merupakan metode yang paling banyak digunakan terutama pada sayuran, buah, daging, dan ikan, dimana produk dicelupkan ke dalam larutan yang digunakan sebagai bahan coating.
Edible coating dapat membentuk suatu pelindung pada bahan pangan karena berperan sebagai barrier yang menjaga kelembaban, bersifat permeabel terhadap gas -gas tertentu, dan dapat mengontrol migrasi komponen-komponen larut air yang dapat menyebabkan perubahan k omposisi nutrisi. Edible coating digunakan pada buah-buahan dan sayuran untuk mengurangi terjadinya kehilangan kelembaban, memperbaiki penampilan, sebagai barrier untuk pertukaran gas dari produk ke lingkungan atau sebaliknya, serta sebagai antifungal dan antimikroba (Krotcha et al., 1994).
Komponen utama penyusun edible coating dapat dikelompokkan menjadi tiga kategori, yaitu hidrokoloid, lipid, dan komposit (campuran). Hidrokoloid yang dapat digunakan untuk membuat edible coating adalah protein (gelatin, kasein, protein kedelai, protein jagung, dan gluten gandum) dan polisakarida (pati, alginat, pektin, gum arab, dan modifikasi karbohidrat lainnya). Lipida yang dapat digunakan adalah lilin, bees wax, gliserol, dan asam lemak (Donhowe dan Fennema, 1994 , diacu dalam Krochta et al., 1994). Bahan baku yang dapat ditambahkan dalam pembuatan coating adalah antimikroba, antioksidan, flavor, pewarna, dan plasticizer (Krochta et al., 1994).
Edible coating yang dibuat dari hidrokoloid memiliki beberapa kelebihan diantaranya baik untuk melindungi produk te rhadap oksigen, karbondioksida, lipida, serta memiliki sifat mekanis yang diinginkan dan meningkatkan kesatuan struktural produk. Kekurangannya adalah coating dari polisakarida kurang baik digunakan untuk mengatur migrasi uap air, sedangkan coating dari protein biasanya sangat dipengaruhi oleh perubahan pH. Edible coating yang dibuat dari lipid memiliki beberapa kelebihan , diantaranya baik digunakan untuk melindungi produk dari penguapan air atau sebagai bahan pelapis untuk mengoles produk konfeksionari. Kekurangannya adalah kegunaannya dalam bentuk murni sebagai coating terbatas, karena cukup banyak kekurangan integritas dan ketahanannya (Donhowe dan Fennema, 1994, diacu dalam Krochta et al., 1994)
Beberapa keuntungan yang diperoleh apabila produk dikemas dengan edible coating yaitu: (1). menurunkan Aw permukaan bahan sehingga kerusakan oleh mikroorganisme dapat dihindari ; (2). memperbaiki struktur permukaan bahan sehingga permukaan menjadi mengkilat ; (3). mengurangi terjadinya dehidrasi sehingga susut bobot dapat dicegah ; (4). mengurangi kontak oksigen dengan bahan sehingga oksidasi dapat dihindari (ketengikan dapat dihambat); (5). sifat asli produk seperti flavor tidak me ngalami perubahan; dan (6). memperbaiki penampilan produk (Santoso et al., 2004).
D. EDIBLE COATING BERBASIS POLISAKARIDA
Polisakarida larut air merupakan senyawa polimer berantai panjang yang dilarutkan ke dalam air, dengan tujuan mendapatkan viskositas larutan yang cukup kental (Glicksman, 1984). Kompo nen-komponen inilah yang akan berperan untuk mendapatkan kekerasan, kerenyahan, kepadatan, kualitas ketebalan, viskositas, adhesivitas, kemampuan pembentukan gel, serta mouthfeel yang baik. Selain itu, senyawa ini sangat ekonomis bila digunakan untuk industri karena mudah didapat dan non toxic (Krochta et al., 1994).
Edible coating menggunakan bahan dasar polisakarida banyak digunakan terutama pada buah dan sayuran , karena memiliki kemampuan bertindak sebagai membran permeabel yang selektif terhadap pertuka ran gas CO2 dan O2. Sifat inilah yang dapat memperpanjang umur simpan karena respirasi buah dan sayuran menjadi berkurang (Krochta et al., 1994). Selain itu, polisakarida menghasilkan film dengan sifat mekanik yang baik. Pati sagu merupakan salah satu cont oh polisakarida. Oleh karena itu, pati sagu berpotensi diaplikasikan dalam teknologi edible coating.
Jenis polisakarida yang dapat digunakan sebagai bahan untuk pembuatan edible film adalah selulosa, pati dan turunannya, seaweed extract, exudates gums, dan seed gums. Film polisakarida yang rendah kalori dan bersifat nongreasy dapat digunakan untuk memperpanjang umur simpan buah dan sayuran dengan cara mencegah dehidrasi, oksidasi, serta terjadinya browning pada permukaan, mengontrol komposisi gas CO2 dan O2 dalam atmosfer internal sehingga mampu mengurangi laju respirasi (Krochta et al., 1994).
E. PATI SAGU
Pati sagu merupakan hasil ekstraksi empulur pohon sagu ( Metroxylon sp) dengan cara mengekstrak tepung/pati dengan bantuan air sebagai perantara (Flach, 1983). Komponen terbesar yang terkandung dalam sagu adalah pati. Pati sagu tersusun atas dua fraksi penting yaitu amilosa yang merupakan fraksi linier dan amilopektin yang merupakan fraksi cabang. Kandungan amilosa pati sagu adalah 27% dan kandungan amilopektin pati
sagu adalah 73%. Rasio amilosa dan amilopektin akan mempengaruhi sifat -sifat pati. Apabila kadar amilosa tinggi maka pati ber-sifat kering, kurang lekat, dan menyerap air lebih banyak (Wirakartakusumah et al., 1986).
Pati sagu dalam bentuk aslinya merupakan butiran atau granula yang berwarna putih mengkilat, tidak berbau, dan tidak berasa . Pati sagu berbentuk ellips (prolate ellipsoidal), mirip pati kentang dengan ukuran 5 -80 mm dan relatif lebih besar dibandingkan pati serelia (Wirakartakusumah et al., 1986). Menurut Wilton dan Wilton (1947), hilum pati sagu tidak terpusat, berada pada ujung yang bulat dan terdapat cincin yang tidak seragam pada granula pati tersebut. Granula pati sagu berbentuk ellips agak terpotong dengan ukuran granula sebesar 2 0 – 60 μm dan suhu gelatinisasinya berkisar 60 – 72oC (Knight, 1989).
Tabel 3. Komposisi kimia pati sagu setiap 100 g
Komponen Jumlah Kalori (Kal) Protein (g) Lemak (g) Karbohidrat (g) Air (g) Fosfor (mg) Kalsium (mg) Besi (mg) 353 0,7 0,2 84,7 15 13 11 15 Sumber : Direktorat Gizi, Dep. Kes. RI (1979)
F. GLISEROL SEBAGAI PLASTICIZER
Aplikasi edible coating polisakarida biasanya dikombinasikan dengan beberapa pangan fungsional seperti resin, plasticizer, surfaktan, minyak, lilin (waxes), dan emulsifier yang memiliki fungsi memberikan permukaan yang halus dan mencegah kehilangan uap air (Krochta et al., 1994). Menurut Banker (1966), plasticizer merupakan substansi non volatil, memiliki titik didih yang tinggi, dan jika ditambahkan ke dalam suatu materi dapat mengubah sifat fisik atau sifat mekanik materi tersebut. Plasticizer dapat mengurangi gaya intermolekul sepanjang rantai polimer, sehingga mengakibatkan fleksibilitas edible film meningkat. Namun juga mengakibatkan turunnya permeabilitas film tersebut. Plasticizer ditambahkan
pada pembuatan edible coating untuk mengurangi kerapuhan, meningkatkan fleksibilitas, dan ketahanan film terutama jika disimpan pada suhu rendah (Ketser dan Fennema, 1989).
Salah satu plasticizer yang dapat digunakan dalam pembuatan edible coating adalah gliserol. Gliserol efektif sebagai plasticizer karena kemampuannya mengurangi ikatan hidrogen internal pada ikatan intermolekular sehingga dapat melunakkan struktur film, meningkatkan mobilitas rantai biopolimer, dan memperbaiki sifat mekanik film. Gliserol bersifat humektan, dimana bagian dari aksi plasticizing berasal dari kemampuannya untuk menahan air pada edible coating tersebut (Lieberman dan Gilbert, 1973).
Gliserol merupakan senyawa poliol yang memiliki tiga gugus hidroksil dalam satu molekul (alkohol trivalen). Rumus kimianya adalah C3H8O3, dengan berat molekul 92,10; massa jenisnya 1,23 g/cm3; dan titik didihnya 204oC. Gliserol memiliki sifat mudah larut air, meningkatkan viskositas larutan, mengikat air, bersifat hidrofilik , mempunyai titik didihnya yang tinggi, bersifat polar, dan non volatil (Winarno, 1997).
G. CARBOXYMETHYL CELLULOSE (CMC)
Carboxymethyl cellulose (CMC) banyak digunakan sebagai bahan penstabil pada makanan. CMC yang banyak dipakai pada industri makanan adalah garam Na carboxy methyl cellulose , atau disingkat CMC, yang dalam bentuk murninya disebut gum selulosa. Pembuatan CMC dilakukan dengan cara mereaksikan NaOH dengan selulosa murni, kemudian ditambahkan Na kloroasetat (Winarno, 1997).
ROH + NaOH R-ONa + HOH
R-ONa + ClCH2COONa R-CH2COONa + NaCl
CMC bersifat larut dalam air panas maupun air dingin , tetapi tidak larut dalam pelarut organik. CMC masih dapat larut dalam campuran air dan pelarut yang larut air seperti etanol dan aseton (Nisperos -Carriedo, 1994, diacu dalam Krochta et al., 1994). CMC memiliki gugus karboksil sehingga
kekentalan larutan CMC dipengaruhi oleh pH larutan. Adapun pH optimum CMC adalah 5 dan pada pH<3 CMC akan mengendap (Winarno, 1997).
CMC dapat bereaksi dengan gula, pati, dan h idrokoloid lainnya. Selain itu, CMC membantu melarutkan protein dalam bahan pangan seperti kasein, gelatin, dan protein kedelai. CMC jarang digunakan sebagai bahan dasar tunggal dalam pembuatan edible film. Akan tetapi kemampuannya untuk membentuk film yang kuat dan tahan minyak sangat baik untuk diaplikasikan (Nisperos-Carriedo, 1994, diacu dalam Krochta et al., 1994).
CMC banyak digunakan dalam formulasi coating untuk melapisi produk-produk segar maupun olahan. Beberapa fungsinya adalah untuk menjaga tekstur alami, kerenyahan dan kekerasan produk, menghambat pertumbuhan kapang pada keju dan sosis, dan mengurangi penyerapan oksigen tanpa menyebabkan peningkatan kadar karbondioksida pada jaringan buah-buahan (Nisperos-Carriedo, 1994, diacu dalam Krochta et al., 1994).
Penambahan CMC ke dalam pembentukan film dari pati bertujuan untuk memperbaiki penampakan, kekuatan, kekompakan, laju transmisi zat, serta mempercepat pembentukan matrik film. Tanpa penambahan CMC, pembentukan film dari pati memerlukan energi ya ng cukup besar dan waktu yang cukup lama, serta film yang dihasilkan kurang cerah, rapuh, dan kurang kompak. CMC akan berinteraksi den gan pati dan air melalui ikatan elektrostatik dan ikatan hidrogen membentuk kompleks elektrostatik yan g lebih stabil (Hikmat, 1997).
H. MINYAK BIJI BUNGA MATAHARI
Bunga matahari (Helianthus annuus L.) merupakan tumbuhan semusim dari suku kenikir-kenikiran (Asteraceae). Bunga matahari populer baik sebagai tanaman hias maupun tanaman penghasil minyak. Bunga tumbuhan ini sangat khas, yaitu besar dan berwarna kuning terang, dengan kepala bunga yang besar (diameter bisa mencapai 30 cm). Bunga ini sebetulnya adalah bunga majemuk, tersusun dari ratusan hingga ribuan bunga kecil pada satu bonggol. Bunga matahari juga memiliki perilaku khas, yaitu
bunganya selalu menghadap ke arah matahari atau heliotropisme (Anonim, 2009b).
Bunga matahari diketahui telah tumbuh di Arizona, New Mexico pada tahun 3000 SM dan di lembah Miss isipi-Missouri pada tahun 900 SM (Tambun, 2006). Semenjak abad ke-17 bijinya digunakan dalam campuran roti atau diolah sebagai pengganti kopi serta cokelat. Penggunaannya sebagai sumber minyak mulai dirintis pada abad ke -19. Sebagai bahan pangan, minyak bunga matahari cocok dipakai untuk meng goreng, mengentalkan, serta campuran salad. Minyak bunga matahari kaya akan asam linoleat (C18:2), suatu asam lemak tak jenuh yang baik bagi kesehatan manusia (Anonim, 2009b).
Tabel 4. Komposisi dan karakteristik fisik minyak biji bunga m atahari
Karakteristik Umumnya Kisaran
Bilangan Iodin Bilangan Penyabunan Unsaponifiable number Titik leleh (oC) Komposisi Trigliserida : Trisaturated (GS3) Disaturated (GS2U) Monosaturated (GSU2) Triunsaturated (GU3) 133,0 -0,3 3,1 26,6 70,2 125,0 – 136,0 188 – 194 0,3 – 1,3 -18 – (-20)
-Catatan : G = gliserida; S = saturated; U = unsaturated; AOM = Active Oxygen Method
Sumber : O’Brien (2004)
Minyak biji bunga matahari diekstrak dari biji matahari dengan kandungan minyak dalam biji bunga mat ahari sebesar 25-30 % (% berat). Proses pengolahan minyak biji bunga matahari di awali dengan proses ekstraksi. Namun minyak mentah yang dihasilkan masih mengandung materi-materi pengotor yang kemudian disingkirkan melalui proses refining (Degumming, Neutralizing, Washing, Drying, Bleaching , dan Deoderizing). Minyak biji bunga mataha ri (refined oil) digunakan sebagai minyak salad, minyak goreng, dan sebagai sumber pembuatan margarin (Tambun, 2006).
Menurut O’Brien (2004), komposisi kimia minyak biji bunga matahari dipengaruhi oleh cuaca, suhu, faktor genetik, dan posisi biji di dalam bunga. Komposisi asam lemak bervariasi dari tahun ke tahun dan wilayah ke wilayah
lainnya. Edible film yang terbuat dari polisakarida bersifat lengket. Untuk memperbaiki sifat ini maka ditambahkan minyak. Minyak biji bunga matahari ini ditambahkan ke dalam formula edible film berfungsi sebagai pelumas agar edible film yang dihasilkan tidak lengket.
I. ANTIOKSIDAN
Antioksidan adalah semua bahan yang dapat menghambat oksidasi tanpa memperhatikan mekanismenya (Lindsay, 1985, diacu dalam Fennema, 1996). Penambahan antioksidan pada bahan pangan dimaksudkan agar bahan pangan tersebut tetap dapat dikonsumsi untuk periode penyimpanan yang lebih panjang (Coppen, 1989). Menurut Ketaren (198 5), antioksidan yang digunakan dalam bahan pangan seharusnya mempunyai sifat -sifat, yaitu aman dalam penggunaanya, tidak menimbulkan perubahan bau dan warna, efektif dalam konsentrasi rendah, dapat bertahan dalam proses pemasakan, dan harganya murah. Efektifitas antioksidan terhadap kecepatan atau tingkat oksidasi dipengaruhi oleh struktur antioksidan, kondisi oksidasi, dan jenis sampel yang teroksidasi.
Menurut Winarno (1997), antioksidan dibagi menjadi dua kategori, yaitu antioksidan primer dan sekunder. Antioksidan primer berperan dalam menghentikan reaksi pembentukan radikal dengan cara melepaskan atom hidrogen, seperti tokoferol, sesamol, asam askorbat, butylated hydroxyanisole (BHA), butylated hydroxytoluene (BHT), dan propyl galate (PG). Antioksidan ini dapat bereaksi dan menstabilkan radikal lipid.
Antoksidan sekunder (pelindung) berperan dalam mereduksi kecepatan rantai inisiasi melalui berbagai mekanisme. Mekanisme antioksidannya dapat terjadi melalui pengikatan ion -ion logam, penangkapan (scavenger) oksigen, dan dekomposisi hi droperoksida menjadi produk non radikal. Beberapa contoh senyawa antioksidan sekunder adalah turunan asam fosfat, asam askorbat, senyawa karoten, sterol, fosfolipid, dan produk reaksi Maillard. Fungsi utama antioksidan sekunder adalah mencegah terbentuknya radikal yang paling berbahaya, yaitu radikal hidroksil (Taher, 2003).
Radikal hidroksil terbentuk melalui reaksi Fenton dan reaksi Haber -Weiss. Reaksi pembentukan radikal hidroksil melalui reaksi Fenton dan reaksi Haber-Weiss terlihat pada Gambar 3.
Fe2+(Cu+) + H2O2 Fe3+(Cu2+) + OH-+˙OH A. Reaksi Fenton
Fe3+(Cu2+) + O2˙- Fe2+(Cu+) + O2 (tahap 1) Fe2+(Cu+) + H2O2 Fe3+(Cu2+) + OH-+˙OH (tahap 2)
B. Reaksi Haber-Weiss
Gambar 3. Reaksi Fenton dan Haber -Weiss (Taher, 2003)
Menurut Ranney (1979), antioksidan diklasifikasik an menjadi tiga golongan berdasarkan prinsip kerjanya dalam mencegah terjadinya proses oksidasi. Pertama adalah antioksidan yang mempunyai gugus fenol dan amina aromatik seperti BHA, BHT, dan fenilamin. Antioksidan tersebut bekerja dengan cara bereaksi den gan radikal bebas yang terdapat di dalam sistem dan membentuk produk non radikal dan suatu radikal antioksidan . Jika radikal antioksidan yang dihasilkan cukup stabil, maka radikal antioksidan tersebut tidak akan berperan sebagai suatu inisiator dari reaksi berikutnya.
Kedua, antioksidan yang berfungsi dengan cara yang sama untuk menghilangkan molekul-molekul hidroperoksida dari sistem, tetapi tanpa melibatkan radikal-radikal bebas. Contoh antioksidan ini adalah dilauril tiodipropionat (DLTP). Molekul ini m engandung atom sulfur teroksidasi yang mampu bereaksi dengan molekul hidroperoksida berikutnya.
Ketiga, antioksidan yang dapat menginaktifkan logam yang bisa mempercepat terjadinya oksidasi. Inisiasi oksidasi bisa dihasilkan melalui reaksi pertukaran elektron antara substrat dan ion logam bervalensi banyak. Ion logam akan direduksi dan dihasilkan suatu radikal bebas, kemudian ion logam dapat dioksidasi kembali oleh oksigen dari udara untuk menghasilkan
katalis oksidasi. Reaksi ion logam yang terlibat dalam proses oksidasi dapat dilihat pada Gambar 4.
R + Mn+ R + M(n-1)+
M(n-1) + Mn+
Antioksidan juga dapat digolongkan berdasarkan sumber yang diperolehnya, yakni antioksidan sintetik dan alami. Antioksidan sintetik sangat efektif dalam menghambat re aksi oksidasi lemak. Akan tetapi penggunaannya banyak menimbulkan kekhawatiran yang disebabkan efek sampingnya (efek patologis). Antioksidan alami diperoleh dengan cara diekstrak pelarut dengan pe larut yang sesuai.
Penambahan antioksidan dalam edible coating berfungsi untuk meningkatkan stabilitas dan menjaga nilai gizi dan warna produk makanan dari ketengikan oksidatif, degrad asi, dan penurunan mutu warna. Adapun jenis antioksidan tersebut adalah asam (baik dalam bentuk garam maupun ester) dan komponen fen olik (Sherwin, 1990). Asam yang dapat digunakan berupa asam sitrat, asam askorbat dan esternya, yang berfungsi untuk mengkelat logam atau bersifat sinergis ketika digunakan sendiri maupun kombinasi keduanya. Komponen fenolik yang dapat digunakan antara lai n: butil hidroksi toluena (BHT), butil hidroksi anisol (BHA), tetra butirat hidroksi kuinon (TBHQ), propil galat, dan tokoferol, yang berfungsi untuk menghambat oksidasi yang berhubungan dengan lemak dan minyak makanan (Krochta et al., 1994).
J. ASAM ASKORBAT (VITAMIN C)
Asam askorbat (vitamin C) merupakan vitamin larut air. Vitamin ini dapat berbentuk sebagai asam L -askorbat dan asam L-dehidroaskorbat, dimana keduanya mempunyai keaktifan sebagai vitamin C. Asam askorbat bersifat sangat mudah teroksidasi seca ra reversibel menjadi asam L -dehidroaskorbat. Asam L-dehidroaskorbat secara kimia sangat labil dan dapat mengalami
oksidasi
perubahan lebih lanjut menjadi asam L -diketogulonat yang tidak memiliki keaktifan vitamin C lagi (Winarno, 1997).
Vitamin C mempunyai rumus empiris C6H8O6, yang bentuk murni merupakan kristal putih, tidak berwarna, tidak berbau, dan mencair pada suhu 190-192oC. Senyawa ini bersifat reduktor kuat dan mempunyai rasa asam. Vitamin C sangat mudah larut dalam air, sedikit larut dalam alkohol, dan tidak larut dalam benzena, eter, kloroform, minyak, dan sejen isnya (Andarwulan dan Sutrisno, 1992).
Vitamin C mudah teroksidasi dan proses oksidasi tersebut dipercepat oleh panas, sinar, alkali, enzim, oksidator, serta oleh katalis logam, seperti tembaga, dan besi. Vitamin C mempunyai sifat umum yang penting sebagai antioksidan yang mempengaruhi reaksi redoks potensial (reduksi zat -zat yang larut dalam air di dalam dan di luar sel) dalam sistem biologis. Vitamin C merupakan komponen alami yang mempunyai sifa t pereduksi dan dapat menangkap radikal bebas yang merupakan hasil samping proses oksidasi sehingga kerusakan jaringan dapat dicegah (Linder, 1992).
Vitamin C bekerja di dalam dan di luar sel dalam mereduksi radikal bebas. Vitamin C sebagai donor elektron akan memberikan elektronnya kepada radikal bebas yang memiliki elektron tak berpasangan kemudian melemahkan kereaktifannya ( Nabet, 1996). Asam askorbat dan garamnya sering digunakan sebagai antioksidan pada berbagai macam pangan olahan, antara lain produk pangan dalam kaleng, minuman ringan, dan beverages.
Fungsi asam askorbat dalam bahan pangan adalah sebagai penangkap oksigen sehingga mencegah proses oksidasi, mendegenerasi fenolik atau antioksidan larut lemak, menjaga kelompok sulfihidril dalam bentuk –SH, bersinergis dengan zat pengkelat, dan atau untuk mengurangi produk o ksidasi yang tidak diinginkan. Dalam edible coating, asam askorbat dan dehidroaskorbat berperan dalam menangkap O2sehingga laju respirasi produk yang dicoating berkurang (Fennema, 199 6).
III. METODOLOGI PENELITIAN
A. BAHAN DAN ALAT
Bahan-bahan yang digunakan adalah paprika, pati sagu, gliserol, CMC, minyak biji bunga matahari, asam askorbat standar, HCl, kristal K2SO4, kristal HgO, H2SO4,NaOH-Na2S2O3,indikator campuran merah metil dan metil biru, heksana, larutan Luff Schrool, KI, H2SO4, Na2S2O3, amilosa murni, etanol 95%, NaOH, larutan iod (iod + KI), akuades, KIO3, amilum, media Plate Count Agar (PCA), dan larutan pengencer.
Alat-alat yang digunakan adalah pisau, panci, kain ka sa, penangas, plastic wrap, box styrofoam, oven vakum, desikator, tanur, neraca analitik, Aw meter, labu Kjehdhal, alat destilasi, buret, labu lemak, kertas saring, soxhlet, spektofotometer, hand mixer, kain saring, gelas piala 1000 ml, hot plate, pelat kaca pencetak film, kantong plastik berkelim, kondensor pendingin balik, Brokefield Model DV III+ Base Unit Rev. A, Micro -cal Messmer, Shibaura WA 260, Tensile Strength and Elongation TesterStograph -MI Toyoseiki, Gas Transmission Rate Tester Speedivac 2, Wat er Vapor Transmission Tester Bergerlahr, Rheometer Precision, Minolta Chromameter 300, cold storage, cawan porselin, cawan aluminium, cawan petri, erlenmeyer, gelas piala, labu takar, pipet volumetrik, pipet tetes, tabung reaksi, dan inkubator.
B. METODOLOGI
Penelitian dilakukan dalam dua tahapan, yaitu penelitian pendahuluan dan penelitian utama. Penelitian pendahuluan dilakukan untuk mengetahui karakteristik bahan baku dan penentuan formulasi edible film yang terbaik. Bahan baku yang dikarakterisasi adalah pati sagu (kadar air, abu, protein, lemak, amilosa) dan paprika (warna, kekerasan, vitamin C, dan total mikroba). Penelitian utama meliputi aplikasi edible coating berdasarkan formulasi yang terbaik pada paprika dan pengamatan mutu paprika selama peny impanan.
Formulasi edible film terdiri dari campuran pati sagu dengan penambahan CMC, gliserol, dan minyak biji bunga matahari. Film yang dihasilkan diuji karakteristiknya, meliputi pengukuran viskositas larutan edible
film, warna film (Jowitt et al., 1987), Aw, uji organoleptik penampakan edible film (Meilgaard et al., 1999), ketebalan film (ISO 4591, 1979), kuat tarik (ASTM D882, 2002), laju transmisi O2 (ASTM D1434-1982, reapproved 1998), dan laju transmisi uap air (ASTM, 1983) . Selanjutnya ditentukan film terbaik berdasarkan hasil analisis tersebut. Formula yang terbaik kemudian ditambahkan vitamin C dan diaplikasikan pada paprika dengan cara di coating.
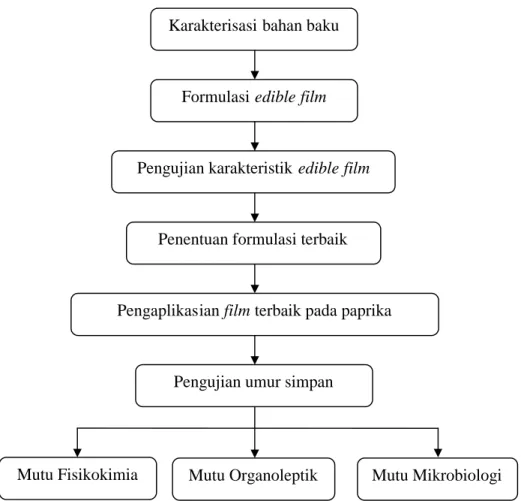
Paprika yang telah diaplikasikan dengan edible coating akan diuji sifat organoleptik (tekstur, warna, aroma, rasa, dan penerimaan umum) dengan uji rating hedonik. Uji organoleptik dilakukan 1 hari setelah proses coating. Selanjutnya, dilakukan pengujian umur simpan yang terdiri dari analisis fisik (warna, kekerasan, dan susut bobot), analisis kimia (kadar air dan vitamin C), dan analisis mikrobiologi ( Total Plate Count). Analisis fisik dilakukan setiap 3 hari sekali, sedangkan analisis kimia dan mikrobiologi dilakukan setiap minggu. Pengujian ini dilakukan sampai sampel mengalami kerusakan. Parameter kerusakan yang dimaksud adalah kisut, adanya kapang, dan lepasnya bagian batang. Jika ditemukan salah satu dari parameter tersebut, sampel dinyatakan rusak. Secara keseluruhan, tahapan penelitian dapa t dilihat pada Gambar 5.
Gambar 5. Tahapan penelitian aplikasi edible film pada paprika Karakterisasi bahan baku
Formulasi edible film
Pengujian karakteristik edible film
Penentuan formulasi terbaik
Pengaplikasian film terbaik pada paprika
Pengujian umur simpan
1. Penelitian Pendahuluan
Penelitian pendahuluan diawali dengan persiapan bahan baku pati sagu. Bahan baku edible film yang digunakan adalah pati sagu. Pati sagu diayak dengan saringan 100 mesh. Selanjutnya dikemas dalam kantong plastik dan disimpan dalam lemari pendingin. Jika akan digunakan, maka pati sagu dikeluarkan dari lemari pendingin dalam keadaan tertutup dan dibiarkan di suhu ruang sampai suhunya konstan. Kemudian sampel di keluarkan dari kantong plastik dan siap digunakan untuk penelitian.
Sebelum digunakan, pati sagu dikarakterisasi terlebih dahulu. Edible film dibuat dari bahan-bahan pembentuk film yang terdiri dari pati sagu, Carboxymethyl Cellulose (CMC), akuades sebagai pelarut, gliserol sebagai plastisizer, dan minyak biji bunga matahari. Perlakuan yang diberikan pada penelitian ini adalah: (a). Konsentrasi gliserol (% volume/bobot pati), yaitu 10% dan 20%; (b). Konsentrasi CMC (% bobot/volume larutan pati) , yaitu 0,5%, 1,0%, 1,5%, dan 2,0%.
Formulasi yang digunakan dalam penelitian pendahuluan dapat dilihat pada Tabel 5.
Tabel 5. Formulasi konsentrasi CMC dan gliserol
Formula Konsentrasi
CMC (%b/v)
Gliserol (%v/b pati)
Minyak Biji Bunga Matahari (%b/v larutan pati) A B C D E F G H 0,5 1,0 1,5 2,0 0,5 1,0 1,5 2,0 10 10 10 10 20 20 20 20 0,025 0,025 0,025 0,025 0,025 0,025 0,025 0,025
Cara pembuatan edible film adalah sebagai berikut: 1 bagian pati sagu dari persiapan pati sagu dicampur dengan 10 bagian akuades d an diaduk dengan mixer skala 1 sampai homogen selama 10 menit, lalu disaring dengan kain saring. Suspensi pati dimasukkan ke dalam gelas piala 1000 ml dan dipanaskan di atas hot plate sambil diaduk dengan mixer skala 1 sampai mencapai suhu 55C. Kemudian ditambahkan gliserol sedikit demi sedikit sambil terus dipanaskan dan diaduk dengan mixer skala 1 sampai homogen. Setelah itu,
ditambahkan minyak biji bunga matahari untuk membuat tekstur film tidak terlalu lengket. Larutan edible film dipanaskan hingga mencapai suhu 60oC kemudian ditambahkan Carboxymethyl Cellulose (CMC) sedikit demi sedikit sambil terus dipanaskan dan diaduk dengan mixer skala 2, sampai suspensi pati mengental dan berubah warna menjadi jernih.
Suspensi pati yang sudah mengental tersebu t masih banyak mengandung gas terlarut sehingga perlu dilakukan penghilangan gas menggunakan oven vakum pada tekanan 80 kPa sampai gas terlarutnya hilang ( 20 menit). Setelah semua gas terlarut hilang, suspensi yang telah mengental tersebut kemudian dituang ke pelat kaca pencetak film berukuran 20 x 20 cm secara merata sampai membentuk lembaran film yang tipis dan rata. Kemudian dibiarkan kering dan dimasukkan ke dalam oven pada suhu 75C selama 4-5 jam.
Edible film yang telah terbentuk dilepas dari ceta kan dengan cara memotong di sekeliling film pada cetakan dengan pisau, lalu menarik salah satu ujungnya dengan hati-hati. Edible film yang sudah lepas dilapisi dengan alufo dan dikemas dalam kantong plastik. Edible film yang diperoleh ini digunakan sebagai kontrol.
Film yang dihasilkan akan diuji karakteristiknya untuk menilai film yang terbaik, yaitu viskositas larutan film, aw, dan uji rating hedonik (warna, tekstur, kejernihan, keregangan, dan keseluruhan). Data-data yang diperoleh akan dianalisis secara statistik dengan menggunakan ANOVA yang dibantu dengan media pengolahan SPSS. Berdasarkan hasil analisis statistik, dipilih dua formulasi terbaik yang selanjutnya dianalisis ketebalan, laju transmisi uap air, laju transimisi oksigen, dan kuat tarik. Kemudian, dipilih satu formulasi terbaik yang selanjutnya diaplikasikan pada paprika. Tahapan pembuatan edible film seperti terlihat pada Gambar 6 .
Gambar 6. Proses pembuatan edible film (kontrol)
Gliserol (10% dan 20%) Minyak Biji Bunga Matahari (0,025%) Pati sagu : akuades
(1:10)
CMC (0,5%; 1,0%; 1,5%; 2,0%) sedikit demi sedikit
Adonan Film Disaring (kain saring)
Diaduk dengan mixer (skala 110 menit)
Dipanaskan sambil diaduk dengan mixer (skala 1,55oC)
Dipanaskan sambil diaduk dengan mixer (skala 2,60oC)
Dihilangan gas (oven vakum P=80kPa, 20
menit)
Dicetak dan diratakan
Dikeringkan (oven T=50oC, 18-24 jam atau T=75oC, 4-5 jam)
Film
Dipanaskan hingga larutan mengental dan berubah menjadi jernih
2. Penelitian Utama
Penelitian utama dilakukan setelah diperoleh formula yang terbaik dari penelitian pendahuluan. Formula yang terbaik kemudian diaplikasikan pada buah paprika. Pembuatan larutan coating dilakukan sama seperti pada penelitian pendahuluan namun diberi perlakuan pena mbahan vitamin C, yaitu setelah larutan edible coating didinginkan hingga suhu 30oC sebelum diaplikasikan pada paprika.
Paprika segar dengan ketuaan panen yang seragam (ketuaan komersial petani) dan berwarna merah setelah dicuci bersih ditiriskan kemudian diberi perlakuan edible film dengan cara pencelupan. Perlakuan yang diberikan pada penelitian ini adalah sebagai berikut : (a). Konsentrasi vitamin C (% volume/volume larutan pati), y aitu 0% (sebagai kontrol); 0.5%; dan 1,0 %; (b). Suhu penyimpanan, yaitu s uhu 20oC dan 8oC; (c). Lama pencelupan, yaitu 3 dan 5 menit. Tabel 6 menunjukkan perlakuan yang digunakan dalam penelitian ini.
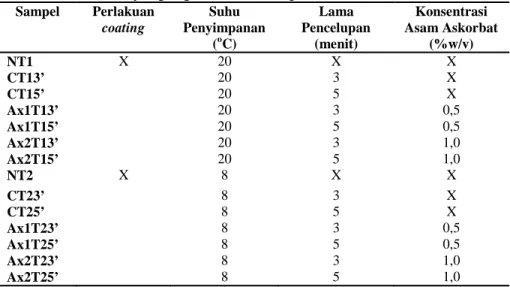
Tabel 6. Perlakuan yang digunakan dalam penelitian utama
Sampel Perlakuan coating Suhu Penyimpanan (oC) Lama Pencelupan (menit) Konsentrasi Asam Askorbat (%w/v) NT1 X 20 X X CT13’ √ 20 3 X CT15’ √ 20 5 X Ax1T13’ √ 20 3 0,5 Ax1T15’ √ 20 5 0,5 Ax2T13’ √ 20 3 1,0 Ax2T15’ √ 20 5 1,0 NT2 X 8 X X CT23’ √ 8 3 X CT25’ √ 8 5 X Ax1T23’ √ 8 3 0,5 Ax1T25’ √ 8 5 0,5 Ax2T23’ √ 8 3 1,0 Ax2T25’ √ 8 5 1,0 Keterangan: X = tidak dilakukan √ = dilakukan
Paprika dicelupkan pada formula edible film selama 3 dan 5 menit. Selanjutnya paprika tersebut dikeringanginkan. Pengemasan dilakukan dengan meletakkan paprika ke dalam box styrofoam dan ditutup plastic wrap. Selanjutnya paprika disimpan pada suhu penyimpanan yaitu suhu cold room (8C) dan suhu AC (20C) sampai paprika menjadi rusak. Perlakuan dilakukan sebanyak 2 (dua) ulangan. Tahapan aplikasi edible coating pada paprika terlihat pada Gambar 7.
Setelah coating, paprika akan diuji mutu organoleptiknya untuk mengetahui pengaruh coating terhadap kesukaan panelis. Hasil uji organoleptik akan dianalisis secara statistik dengan menggunakan menggunakan ANOVA yang dibantu dengan media pengolahan SPSS . Selama penyimpanan, paprika akan dianalisis mutu fisik dan mutu kimianya. Analisis fisik paprika dilakukan setiap tiga hari sekali sedangkan analisis kimia dilakukan seminggu sekali. Pengujian dilakukan hingga paprika mengalami kerusakan.
Gliserol (konsentrasi terpilih)
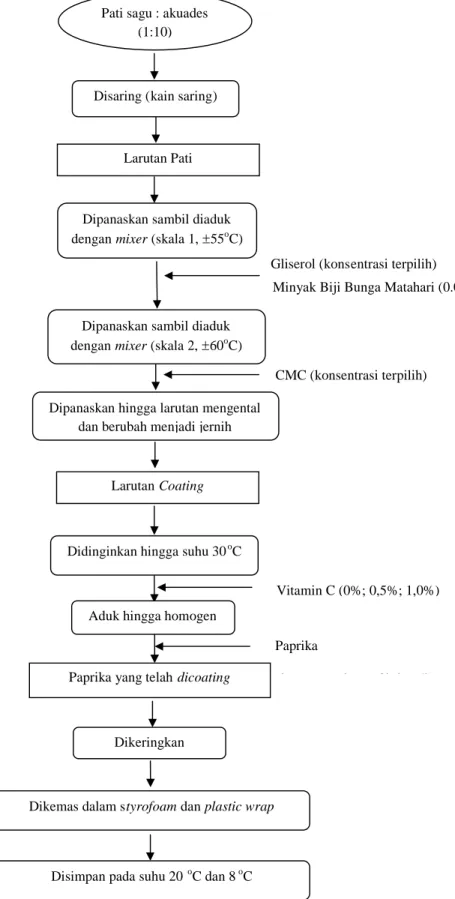
Gambar 7. Tahapan aplikasi edible coating pada paprika
Minyak Biji Bunga Matahari (0.025%)
CMC (konsentrasi terpilih) Pati sagu : akuades
(1:10)
Disaring (kain saring)
Dipanaskan sambil diaduk dengan mixer (skala 1,55oC)
Larutan Pati
Dipanaskan hingga larutan mengental dan berubah menjadi jernih
Larutan Coating Dipanaskan sambil diaduk dengan mixer (skala 2,60oC)
Paprika
(lama pencelupan 3’ dan 5’) Paprika yang telah dicoating
Dikeringkan
Dikemas dalam styrofoam dan plastic wrap
Disimpan pada suhu 20oC dan 8oC Didinginkan hingga suhu 30oC
Aduk hingga homogen
3. Pengujian dan Pengamatan 3.1. Uji Proksimat Pati Sagu
a. Kadar Abu (Apriyantono et al., 1989)
Cawan pengabuan dibakar dalam tanur, kemudian didinginkan dalam desikator, dan ditimbang. Sampel sebanyak 3 -5 gram ditimbang dalam cawan tersebut, kemudian cawan yang berisi sampel dibakar sampai didapatkan abu berwarna abu -abu atau sampai bobotnya konstan. Pengabuan dilakukan dalam dua tahap, yaitu pertama pada suhu sekitar 400oC dan kedua pada suhu 5500C. Cawan yang berisi sampel didinginkan dalam desikator, kemudian ditimbang dengan neraca analitik.
Catatan : sebelum masuk tanur, sampel yang ada dalam ca wan dibakar dulu pada pembakar sampai asapnya habis.
Perhitungan :
b. Kadar Air Metode Oven Biasa (Apriyantono et al., 1989)
Cawan alumunium dikeringkan dalam oven pada suhu 105oC selama 15 menit, lalu didinginkan dalam desikator selama 10 menit. Cawan ditimbang menggunakan neraca analitik. Sampel sebanyak 5 gram dimasukkan ke dalam cawan, kemudian cawan serta sampel ditimbang dengan neraca analitik. Cawan berisi sampel dikeringkan dalam oven pada suhu 105oC selama 6 jam. Selanjutnya cawan berisi sampel didinginkan dalam desikator, kemudian ditimbang. Setelah itu, cawan berisi sampel dikeringkan kembali dalam oven selama 15 -30 menit, lalu ditimbang kembali. Pengeringan diulangi hingga diperoleh bobot konstan (selisih bobot0,0005 gram).
c. Kadar Protein Metode Kjeldahl Mikro (Apriyantono et al., 1989) Sejumlah kecil sampel (kira -kira akan dibutuhkan 3-10 ml HCl 0,01 N atau 0,02) ditimbang, dipindahkan ke dalam labu Kjedahl 30 ml. Setelah itu, ditambahkan 1,9 ± 0,1 gram K2SO4, 40 ± 10 mg HgO, dan 2,0 ± 0,1 ml H2SO4 ke dalam labu Kjedahl yang berisi sampel. Jika sampel lebih dari 150 mg, ditambahkan 0, 1 ml H2SO4untuk setiap 10 mg bahan organik di atas 15 mg. Setelah itu, beberapa butir batu didih dimasukkan labu Kjedahl yang berisi sampel kemudian labu Kjedahl yang berisi sampel dan telah dimasukkan batu didih didihkan selama 1 -1,5 jam sampai cairan menjadi jernih. Setelah cairan jernih, labu Kjedahl yang berisi sampel didinginkan dan ditambahkan sejumlah kecil air secara perlahan-lahan ke dalamnya, kemudian didinginkan kembali. Isi labu dipindahkan ke dalam alat destilasi. Labu Kjedahl yang isinya sudah dipindahkan ke dalam alat destilasi dicuci dan bilas 5 -6 kali dengan 1-2 ml air, air cucian dipindahkan ke dalam alat destilasi.
Erlenmeyer 125 ml yang berisi 5 ml larutan H3BO3 dan 2-4 tetes indikator (campuran dua bagian metil merah 0, 2% dalam alkohol dan satu bagian metilen blue 0,2% dalam alkohol) diletakan di bawah kondensor. Ujung tabung kondensor harus te rendam di bawah larutan H3BO3 kemudian di tambahkan 8 -10 ml larutan NaOH-Na2S2O3 dan dilakukan destilasi sampai tertampung kira -kira 15 ml destilat dalam erlenmeyer. Setelah itu, tabung kondensor dibilas dengan air dan bilasannya ditampung dalam erlenmeyer yang sama. Selanjutnya isi erlenmeyer diencerkan sampai kira-kira 50 ml dan kemudian ditritasi dengan HCl 0,02 N sampai terjadi perubahan warna menjadi abu -abu. Penentuan protein pun dilakukan untuk blanko.
Cara perhitungan kadar protein :
Nilai 5.70 = faktor konversi untuk tepung
contoh blanko contoh mg x HClx xN HCl ml HCl ml N 14.007 100 % Kadar Protein = 5,70 x %Nd. Kadar Lemak Metode Soxhlet (AOAC, 1984)
Labu lemak yang akan digunakan dalam alat ekstraksi Soxhlet dikeringkan di dalam oven, lalu didinginkan di dalam desikator kemudian ditimbang. Ditimbang 2 g sampel di dalam gela s piala, ditambahkan 30 ml HCl 25% dan 20 ml air serta beberapa batu didih. Ditutup gelas piala yang dengan gelas arloji dan dididihkan selama 15 menit (larutan sampel). Larutan sampel disaring dengan kertas saring dalam keadaan panas dan dicuci dengan air panas hingga tidak bereaksi asam lagi.
Kertas saring yang digunakan untuk menyaring larutan sampel dikeringkan berikut isinya pada suhu 100 -105oC (kertas saring sampel). Kertas saring dimasukan sampel ke dalam kertas pembungkus sampel yang telah dilengkapi kapas dibagian ujungnya kemudian dibentuk menjadi bentuk tabung (timbel). Timbel tersebut diekstrak dengan heksana selama 2-3 jam pada suhu kurang lebih 80oC. Selanjutnya, labu lemak yang berisi lemak hasil ekstraksi dipanaskan di dalam oven pada suhu 10 0-105°C. Setelah itu didinginkan di dalam desikator, kemudian ditimbang.
e. Total Gula (Metode Luff Schoorl, SNI -01-2892-1992)
Timbang bahan 0,1215 gram sampel, dipindahkan ke dalamlabu takar 100 ml. Tambahkan HCl 30% dan akuades. Setelah itu dipanaskan di dalam water bath pada suhu 99,9oC selama 2,5 jam. Setelah itu, ditambahkan NaOH 45% untuk menetralkan pH larutan yang ditandai dengan menggunakan indikator fenolftalein dimana larutan berubah warna menjadi semburat warna merah mud a kemudian diencerkan dengan akuades hingga tanda tera dan disaring.
Sebanyak 5 ml larutan dimasukkan ke dalam erlenmey er dan ditambahkan 5 ml larutan Luff Schrool dan 5 ml akuades. Blanko dibuat dari 5 ml larutan Luff Schrool ditambah 5 ml akuades. Kemudian erlenmeyer dihubungkan dengan pendingin balik lalu dididihkan (usahakan 2 menit sudah mendidih). Pendidihan dipertahankan selama 10
menit lalu didinginkan dan ditambahkan 3 ml KI 20% dan 5 ml H2SO4 26.5%.
Iodium yang dibebaskan dititrasi d engan larutan Na-thiosulfat 0,1N menggunakan indikator pati 2 -3 ml. Penetapan berat glukosa dilakukan dengan membandingkan volume Na -thiosulfat yang diperlukan dengan tabel Luff Schrool.
Kadar Gula (%) = bobot glukosa x FP x 100% bobot sampel
Kadar Pati (%) = 0,9 x Kadar gula (%)
f. Kadar Amilosa dan Amilopektin (AOAC, 1984)
Pengukuran amilosa didasarkan pada metode spektrofotometri. Kurva standar dibuat dengan menggunakan amilosa murni sebagai standar. Timbang 40 mg amilosa murni, tambah 1 ml etanol 95%, da n 9 ml NaOH 1 N. Panaskan dalam air mendidih selama 10 menit sampai tergelatinisasi. Pindahkan seluruh gel dalam labu takar 100 ml, tepatkan dengan air. Pipet masing-masing 1, 2, 3, 4, dan 5 ml larutan diatas, masukkan ke dalam labu takar 100 ml. Tambahkan masing-masing ke dalam labu takar tersebut 0,2 ; 0,4; 0,6; 0,8; dan 1 ml, lalu tambahkan masing -masing 2 ml larutan iod. Tepatkan dengan akuades. Biarkan selama 20 menit. Ukur absorbansi pada 625 nm.
Timbang 100 mg sampel dalam bentuk tepung, tambahkan 1 ml etanol 95% dan 9 ml NaOH 1 N. Panaskan dalam air mendidih selama 10 menit sampai terbentuk gel. Pindahkan seluruh gel dalam labu takar 100 ml, tepatkan dengan air. Pipet 5 ml larutan tersebut, tambahkan 1 ml asam asetat 1 N, dan 2 ml larutan iod, lalu encerkan sampai 100 ml dengan akuades. Biarkan selama 20 menit. Ukur absorbansi pada 625 nm. Hitung kadar amilosa dan amilopektin dalam sampel dengan rumus :
Kadar amilosa (%) =
dimana : C = Konsentrasi amilosa contoh (mg/ml) V = Volume akhir contoh (ml)