26
III. METODOLOGI PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Maret 2019 sampai Juli 2019, di Laboratorium Ilmu dan Teknologi Pangan Universitas Muhammadiyah Malang. 3.2 Alat dan Bahan
3.2.1 Alat
Alat-alat yang digunakan untuk proses pembuatan water kefir buah sirsak meliputi: panci, kompor gas, pengaduk, saringan, pipet ukur, gelas ukur, botol ukuran 350 ml, plastik, karet, termometer dan inkubator, tabung rekasi, erlenmeyer 100 ml, laminar airflow. Alat yang digunakan untuk analisa water kefir buah sirsak meliputi: timbangan analitik, inkubator, plate count, petridisk, jarum ose, labu ukur erlenmeyer 100 ml, pipet tetes, karet penghisap, tabung reaksi, rak tabung reaksi, lemari es, penyaring, kertas saring, labu ukur, buret, beaker glass 100 ml, gelas ukur 10 ml dan 250 ml, spektrofotometer merek Genesys 20, Color reader CR 10 merk Conica Minotta, pH meter merk WTW tipe pH 315i, dan alat bantu lainnya.
3.2.2 Bahan
Bahan sari sirsak adalah sirsak (Annona muricata L.) varietas lokal yang diperoleh dari pasar Besar Malang, gula pasir, susu skim, kefir grains dari BPPT Batu dan aquades. Bahan-bahan lain berupa MRS Agar, PDA, aquades, pereaksi anthrone, larutan 0.1 N NaOH, indikator phenolphtalein (PP), CaCO3, H2SO4
bahan kimia serta bahan-bahan pendukung lainnya yang diperoleh dari Laboratorium Ilmu dan Teknologi Pangan Universitas Muhammadiyah Malang.
27 3.3 Metode Penelitian
Penelitian ini dibagi dalam 2 bagian, bagian ke-1 yaitu pembuatan sari sirsak dengan menggunakan varietas sirsak jenis (Annona muricata L.) dan bagian ke-2 yaitu pengaplikasian kefir grains dengan berbagai konsentrasi yang berbeda pada sari sirsak yang telah dibuat sebelumnya dan telah diberi penambahan konsentrasi sukrosa dengan berbagai jumlah konsentrasi yang berbeda. Penelitian dilaksanakan dengan menggunakan rancangan acak kelompok (RAK) faktorial yang terdiri dari dua faktor, yaitu konsentrasi sukrosa (S), dan konsentrasi starter (B) dengan pola faktorial 4x2 setiap perlakuan diulang sebanyak tiga kali sehingga diperoleh 24 satuan percobaan:
Faktor I: konsentrasi sukrosa (S), dengan 4 level: S1= konsentrasi sukrosa 2% (w/v)
S2= konsentrasi sukrosa 4% (w/v) S3= konsentrasi sukrosa 6% (w/v) S4= konsentrasi sukrosa 8% (w/v)
Faktor II: konsentrasi starter (B), dengan 2 level: B1= konsentrasi starter 4% (w/v)
B2= konsentrasi starter 8% (w/v)
Sehingga diperoleh matriks delapan (8) kombinasi perlakuan yang dapat diihat pada tabel 5. sebagai berikut :
Tabel 5. Matriks Kombinasi Perlakuan Konsentrasi Starter dan Sukrosa Konsentrasi
Starter Konsentrasi Sukrosa
S1 S2 S3 S4
B1 B1S1 B1S2 B1S3 B1S4
28 Keterangan :
B1S1 : konsentrasi starter 4% (w/v) + konsentrasi sukrosa 2% (w/v) B1S2 : konsentrasi starter 4% (w/v) + konsentrasi sukrosa 4% (w/v) B1S3 : konsentrasi starter 4% (w/v) + konsentrasi sukrosa 6% (w/v) B1S4 : konsentrasi starter 4% (w/v) + konsentrasi sukrosa 8% (w/v) B2S1 : konsentrasi starter 8% (w/v) + konsentrasi sukrosa 2% (w/v) B2S2 : konsentrasi starter 8% (w/v) + konsentrasi sukrosa 4% (w/v) B2S3 : konsentrasi starter 8% (w/v) + konsentrasi sukrosa 6% (w/v) B2S4 : konsentrasi starter 8% (w/v) + konsentrasi sukrosa 8% (w/v) *semua perlakuan ditambahkan susu skim sebanyak 5 % (w/v) 3.4 Prosedur Pelaksanaan Penelitian
3.4.1 Pembuatan Sari Sirsak
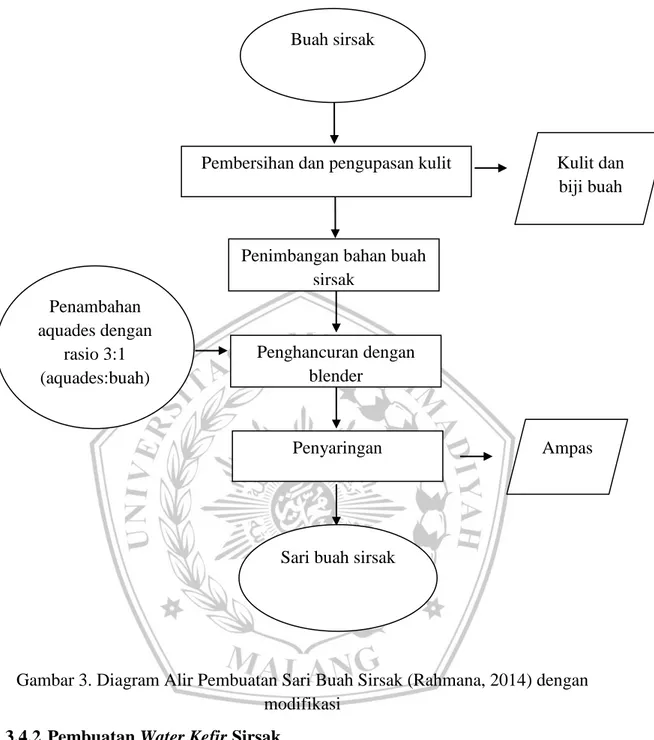
Water kefir sirsak dibuat dari bahan baku sirsak varietas (Annona muricata L.). Tahapan pembuatan water kefir sirsak diawali dengan melakukan penyortiran buah, buah yang telah busuk, terlalu matang atau yang terlihat sifat tidak normal dipisahkan agar tidak mempengaruhi mutu akhir produk. Kemudian buah yang telah disortir kemudian dihilangkan kulit buah, biji dan bagian buah yang tidak dapat dimakan dibuang. Daging buah kemudian ditimbang. Buah kemudian dihancurkan dengan blender, kemudian ditambah dengan air perbandingan 1:3 (buah:aquades). Setelah diblender disaring dan didapatkan sari buah sirsak (Rahmana, 2014).
29
Gambar 3. Diagram Alir Pembuatan Sari Buah Sirsak (Rahmana, 2014) dengan modifikasi
3.4.2 Pembuatan Water Kefir Sirsak
Sari sirsak yang telah diperoleh kemudian ditambahkan sukrosa dengan konsentrasi yang berbeda diantaranya 2%, 4%, 6% dan 8%. Sari buah sirsak kemudian dipasteurisasi pada suhu 80oC selama 15 menit. Dalam keadaan panas sari buah sirsak dimasukkan kedalam botol 250 ml yang sudah disterilkan, kemudian didinginkan hingga suhu mencapai 37oC. Setelah sari buah sirsak sudah jadi, dilakukan tahap selanjutnya yaitu untuk mendapatkan water kefir sirsak, sari
Pembersihan dan pengupasan kulit
Penimbangan bahan buah sirsak Penghancuran dengan blender Penambahan aquades dengan rasio 3:1 (aquades:buah) Penyaringan
Sari buah sirsak Buah sirsak
Kulit dan biji buah
30
sirsak diinokulasi starter kefir dengan penambahan jumlah konsentrasi starter yang bervariasi 4% dan 8% (w/v). Kemudian diaduk hingga tercampur rata, dimasukkan ke dalam botol dan menutupnya rapat kemudian menginkubasi pada suhu 37oC dengan perlakuan lamanya fermentasi selama 24 jam. Setelah proses fermentasi Water kefir sirsak dengan berbagai macam perlakuan tersebut kemudian dilakukan analisa fisik, kimia, mikrobiologi dan organoleptik.
Gambar 4 . Diagram alir proses pembuatan water kefir sirsak (Diniyah, 2013) yang dimodifikasi
3.5 Parameter Pengamatan
Parameter pengamatan yang diuji yaitu kualitas kimia meliputi pengujian total asam teritrasi (TAT), pH, gula reduksi, dan kadar alkohol. Kualitas fisik
Pasteurisasi
(pada suhu 80oC ,15 menit) Sari buah sirsak
250 ml
Pendinginkan sampai 37oC
Water kefir sirsak Inokulasi starter : 4% dan 8% (w/v) Inkubasi T= 37oC, t = 24 jam Penambahan Perlakuan Sukrosa 2%, 4%, 6% dan 8% (w/v) serta susu skim 5 (w/v)% Parameter Pengujian Total Asam Tertitrasi
pH
Intensitas Warna Uji Total BAL Uji Yeast
Uji Kadar Alkohol Uji Gula Reduksi Uji Organoleptik
31
meliputi intensitas warna (L, a, b). Kualitas mikrobiologi meliputi pengujian total bakteri asam laktat (BAL), dan total yeast, serta parameter organoleptik (kenampakan, aroma, dan rasa).
3.5.1 Uji Total Asam Tertitrasi (AOAC,1995)
2,5 ml sampel dimasukkan ke dalam labu ukur 25 ml, kemudian ditambahkan aquades sampai tanda batas, selanjutnya dihomogenkan dan disaring. Filtrat di ambil 10 ml dan dimasukkan ke dalam erlenmeyer. Ditambahkan 3 tetes indikator PP. Dititrasi dengan larutan 0.1 N NaOH hingga warna larutan berubah menjadi merah muda dan warna tersebut tidak berubah kembali selama 30 detik. Pada akhir titrasi dihitung jumlah NaOH yang digunakan.
N = Normalitas larutan NaOH 0,1 N ml eq = 0,0901
BM asam laktat (CH3CHOHCOOH) = 90 ml sampel = 1 ml
fp = 10
3.5.2 Uji pH (Badan Standarisasi Nasional, 2004) 1. Menyalakan pH meter;
2. Membilas elektroda dan temperature prob menggunakan akuades dan mengeringkannya;
3. Melakukan kalibrasi dengan mencelupkan elektroda pada larutan penyangga (pH 7) serta asam (pH 4) dan membersihkannya;
4. Membilas kembali elektroda menggunakan akuades dan mengeringkan; % asam laktat = ml NaOH x N NaOH x (berat ml eq asam) x fp x 100 %
32
5. Mencelupkan elektroda pada sampel, dengan menekan tombol Ar (hold) dan Enter kemudian mengunggu pembacaan pada layer stabil serta muncul indicator autolock pada layar;
6. Mencatat nilai yang tertera pada layar digital.
3.5.3 Penentuan Intensitas Warna Metode L, a, b Hunter (Yuwono dan Susanto, 1998)
1. Siapkan sampel dalam plastik PP (transparan) 2. Nyalakan colour reader
3. Tentukan target L, a, b. Dimana; L, adalah kecerahan ; axis a, nilai positif (+) berarti merah, nilai (-) berarti hijau; axis b, nilai positif (+) berarti kuning, dan nilai negatif (-) berarti biru
4. Tekan tombol target dan kemudian mencatat nilai warna pada tertera. 3.5.4 Perhitungan Total Bakteri Asam Laktat (Fardiaz, 1993)
1 Diambil 1 ml sampel kemudian memasukkan ke dalam tabung reaksi 2 Tambahkan 9 ml aquades kemudian menutup dan mengocoknya
3 Lakukan pengenceran bertingkat sampai pengenceran ke enam (10-6) dengan cara mengambil 1 ml suspensi dan menaruhnya dalam tabung reaksi ke dua kemudian menambahkannya 9 ml aquades. Melakukan hal yang sama pada tabung ke tiga sampai enam
4 Diambil 1 ml suspensi pada tabung ke enam kemudian memasukkan ke dalam cawan petri
5 Masukkan medium de Man Ragosa and Sharpe Agar (MRSA) steril yang telah didinginkan sampai suhu 45 OC sebanyak 15 ml
6 Gerakkan cawan petri untuk penyebaran sel-sel bakteri asam laktat secara merata dan memadat
33
7 Menginkubasi di dalam inkubator pada suhu 37OC dengan posisi cawan terbalik selama 24 jam
8 Menghitung koloni yang tumbuh menggunakan colony counter. Total koloni yang terhitung harus memenuhi Standar Internasional Commition of Food (ICMF), yaitu antara 30 sampai 300 koloni per cawan petri.
3.5.5 Uji Yeast (Asyikeen, dkk., 2012)
Pencawanan dilakukan dengan menggunakan media biakan MEA sebanyak 48 g ke dalam 1000 ml aquades, kemudian larutan MEA tersebut dipanaskan hingga mendidih dilanjutkan sterilisasai. Pencawanan dilakukan dengan memipet 1 ml sampel hasil pengenceran ke dalam cawan petri, pencawanan dilakukan secara duplo dari pengenceran 10-4 -10-6 . Kemudian dilakukan penghitungan yeast menggunakan colony counter (Fardiaz, 1993) setelah inkubasi.
3.5.6 Uji Kadar Alkohol Spektrofotometri (Day, 1992)
1. Penentuan Kuva standar : digunakan ethanol dengan berbagai konsentrasi 0%, 0,3%, 0,6%, 0,12%, 0,25%, 0,5%, 1%. Masing-masing larutan standar diukur absorbansinya pada panjang gelombang 600 nm;
2. Sebanyak 0,5 sampel cair, diencerkan dengan akuades 15 ml;
3. Menambahkan K2CrO4 sebanyak 12,5 ml. Terjadi perubahan saat
ditambahkan kalium dikromat, dimana warna menjadi jingga;
4. Memanaskan campuran sampel, hal ini bertujuan agar reaksi berlangsung cepat. Setelah pemanasan, sampel berwarna hijau kehitaman;
5. Mendinginkan campuran yang telah diencerkan dan homogenkan dengan vortex, kemudian ukur absorbansi pada panjang gelombang 600 nm.
Koloni per gram = jumlah koloni x 1
34 6. Menghitung kadar alkohol dalam sampel.
3.5.7 Uji Gula Reduksi Metode Luff Schoorl (AOAC, 1997 yang disitasi oleh Sudarmadji dkk. (1997))
1. Menimbang bahan 2 gram dengan timbangan analitik;
2. Menambahkan akuades sebanyak 25 ml pada labu takar 25 ml sampai batas tera dan menghomogenkan;
3. Menyaring sampel dengan kertas saring;
4. Mengambil filtrat 12,5 ml dan dimasukkan ke dalam erlenmenyer 100 ml, menambahkan 12,5 ml Luff Schoorl. Membuat blanko yaitu 12,5 ml larutan Luff Schoorl dan 12,5 ml akuades;
5. Mendidihkan pada hot plate dan pendingin balik, pertahankan 10 menit setelah mendidih;
6. Mendinginkan dengan cepat pada air mengalir; 7. Menambahkan 7,5 ml larutan KI dan homogenkan;
8. Menambahkan 12,5 ml H2SO4 dan menambahkan 5 tetes amilum dan
homogenkan;
9. Mentitrasi dengan Na2S2O3 0,1 N sampai berwarna putih keruh dan catat
volume titrasi;
10. Menghitung Kadar Gula Reduksi dengan rumus: Δ ml Sampel= ml Balnko - ml Sampel
Mg Glukosa= Kadar Glukosa pada Tabel + Δ (Sisa. Δ)
( )
35
3.5.8 Analisa Organoleptik Hedonic Scale (Rahayu, 2001)
Uji organoleptik yang dilakukan meliputi kenampakan, warna, kekentalan dan rasa. Pengujian menggunakan uji skala hedonic yang terdiri dari 5 nilai dengan 5 pernyataan dapat dilihat pada Tabel 6.
Tabel 6 . Skor Organoleptik
Nilai Aroma Rasa Mouthfeel Kesukaan
1 Sangat Tidak Menyengat Sangat Tidak Asam Sangat Tidak Berkarbonasi Sangat Tidak Suka 2 Tidak Menyengat Tidak Asam Tidak
Berkarbonasi
Tidak Suka 3 Cukup Menyengat Cukup Asam Cukup
Berkarbonasi
Cukup Suka
4 Menyengat Asam Berkarbonasi Suka
5 Sangat
Menyengat
Sangat Asam Sangat Berkarbonasi
Sangat Suka
Pengujian dilakukan dengan memberikan sampel secara acak 9 macam sampel yang masing – masing telah diberi kode yang berbeda kepada 20 panelis. Selanjutnya panelis diminta memberi penilaian terhadap sampel sesuai skala hedonic yang ada.
3.5.9 Analisa Data
Data dari hasil pengamatan tiap parameter pada penelitian ini dianalisis menggunakan analisa data ANOVA (Analysis of Variant) untuk mengetahui interaksi dan pengaruh dari setiap perlakuan. Jika terdapat Interaksi dan pengaruh pada data hasil pengamatan maka akan diuji lanjut menggunakan uji DMRT 5% (Duncan’s Multiple Range Test). Dan untuk memilih kombinasi perlakuan terbaik pada penelitian ini menggunakan nilai efektivitas uji De Garmo.