OPTIMASI VOLUME ETANOL DAN AKUADES DALAM PROSES PERKOLASI DAUN STEVIA (Stevia rebaudiana Bertonii M.) DENGAN
APLIKASI DESAIN FAKTORIAL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Far.)
Program Studi Ilmu Farmasi
Oleh :
Totok Lasmono Hadi Purwanto NIM : 058114167
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA 2009
OPTIMASI VOLUME ETANOL DAN AKUADES DALAM PROSES PERKOLASI DAUN STEVIA (Stevia rebaudiana Bertonii M.) DENGAN
APLIKASI DESAIN FAKTORIAL
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Far.)
Program Studi Ilmu Farmasi
Oleh :
Totok Lasmono Hadi Purwanto NIM : 058114167
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA 2009
Untuk Tuhan Yesus yang selalu menjagaku
Untuk Mama & Papa yang selalu memberi dukungan
Untuk Kakak dan Adikku yang selalu memberi semangat
Dan untuk Alamamaterku
Kebersamaan adalah....
Berbagi rasa, memberi kedamaian, saling memperhatikan,
saling mengasihi, mengerti artinya dicintai dan mencintai,
menerima apa adanya.
Sukses adalah suatu hal yang tidak dapat kita bayar
dengan tunai. Kita harus membayarnya dengan cara
mencicil dan melakukan pembayaran setiap hari
-Zig ziglar-
PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa atas berkat dan karunia-Nya penulis dapat menyelesaikan skripsi yang berjudul “Optimasi Volume Etanol dan Akuades dalam Proses Perkolasi Daun Stevia (Stevia rebaudiana Bertonii M.) dengan Aplikasi Desain Faktorial ” sebagai salah satu syarat untuk mencapai gelar sarjana pada Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Skripsi ini merupakan bagian dari penelitian payung ”Optimasi Proses Isolasi Steviosida Sebagai Pemanis Pengganti Gula” yang dibiayai Hibah PHK A3 Dikti tahun 2008. Dalam penulisan skripsi ini, penulis mendapatkan bantuan dari banyak pihak. Pada kesempatan ini penulis ingin menyampaikan penghargaan dan ucapan terima kasih kepada:
1. Yohanes Dwiatmaka, M.Si. selaku dosen pembimbing I atas bimbingan dan pengarahannya baik selama penelitian maupun penyusunan skripsi ini. 2. Sri Hartati Yuliani, M.Si., Apt. selaku dosen pembimbing II atas bimbingan
dan pengarahannya baik selama penelitian maupun penyusunan skripsi ini. 3. Romo Drs. Petrus Sunu Hardiyanta, S.J., S.Si. selaku penguji atas segala
masukan, kritik, dan sarannya.
4. Yustina Sri Hartini M.Si., Apt selaku penguji atas segala masukan, kritik, dan sarannya.
5. Mas Wagiran, Mas Sigit, Mas Andri, dan Mas Sarwanto atas bantuannya selama peneliti bekerja di laboratorium Farmakognosi Fitokimia.
ix
INTISARI
Pada penelitian ini dilakukan optimasi volume etanol dan akuades sebagai cairan penyari dalam proses perkolasi daun S. rebaudiana. Desain faktorial diaplikasikan dalam penelitian ini. Penelitian ini bertujuan untuk mengetahui faktor dominan dan pengaruh interaksi antara etanol dan akuades, serta volume cairan penyari yang optimum untuk mendapatkan ekstrak dengan kadar steviosida tertinggi.
Penelitian ini termasuk penelitian eksperimental murni menggunakan desain faktorial dengan dua faktor yaitu volume etanol dan akuades. Penelitian diawali dengan determinasi tanaman, pembuatan serbuk, defatisasi dan penyarian secara perkolasi. Analisis kualitatif perkolat dengan KLT silika gel F254 dan fase
gerak kloroform:metanol:akuabides (10:15:2) serta deteksi bercak dengan pereaksi KI dan vanilin-asam sulfat. Penetapan kadar steviosida dengan mengukur luas area di bawah kurva (AUC) menggunakan software Image-J. Data hasil penelitian dianalisis secara statistik menggunakan Yate’s Treatment dengan tingkat kepercayaan 95 % untuk mengetahui tingkat signifikansi tiap faktor dan interaksi keduanyadalam menentukan respon kadar steviosida.
Hasil analisis data menunjukkan bahwa etanol merupakan faktor dominan yang signifikan berpengaruh dengan nilai F hitung 47,2498 lebih besar dari F tabel 10,128 sedangkan interaksi tidak berpengaruh terhadap respon kadar steviosida. Berdasarkan hasil penelitian dapat ditemukan area optimum volume cairan penyari untuk mendapatkan ekstrak dengan kadar steviosida tertinggi (> 7% b/b).
Kata kunci : steviosida, perkolasi, desain faktorial, Image-J, Yate’s Treatment
ABSTRACT
The optimation of ethanol and aquadest volumes as solvent were performed in percolation process of S. rebaudiana leaves. Factorial design was applied in this research. This research has the objectives to know the dominant factor and interaction effect between ethanol and aquadest, also the optimum volumes of solvent to get the highest concentration of stevioside within the extract.
This research was included to be a pure experimental research using application factorial design of two factors, ethanol and aquadest. This research was preceded by determination of plant, powderisation, defatitation, and extraction by percolation. Qualitative analysis of percolate by TLC silica gel F254
and mobile phase chloroform:methanol:aquabidest (10:15:2) also detection of spot with KI and vanilin-sulphuric acid reagents. Assay the concentration of stevioside by measure area under curve using software image-J. Data of this research are analysed statistically using Yate’s Treatment with confidence level 95% to know the significance level of each factor and interaction between them to determine the respon stevioside concentration.
The results of data analyse show that ethanol is the significance dominant factor with F value 47,2498 higher than F tabel 10,128 and interaction have no effect to the respon stevioside concentration. Based on the results of research , it was found optimum area volume of solvent to get the highest concentration of stevioside within the extract (> 7% w/w).
Keywords : stevioside, percolation, factorial design , Image-J, Yate’s Treatment
DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PEENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI ... vi
PRAKATA... vii
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI... x
ABSTRAK ... xi
DAFTAR ISI ... xii
DAFTAR TABEL... xvi
DAFTAR GAMBAR ... xvii
DAFTAR LAMPIRAN... xviii
BAB I PENDAHULUAN ... 1
A. Latar Belakang... 1
1. Perumusan Masalah ... 4
2. Keaslian Penelitian... 5
3. Manfaat Penelitian ... 5
B. Tujuan Penelitian... 5
BAB II TINJAUAN PUSTAKA... 6
A.Stevia rebaudiana Bertonii M. ... 6
1. Uraian Tanaman ... 6
H.Desain Faktorial... 18
I. KLT .. ... 20
J. Image J ...24
K.Landasan Teori ... 24
L.Hipotesis ... 25
BAB III METODE PENELITIAN ... 26
A.Jenis dan Rancangan Penelitian... 26
B.Variabel dan Definisi Operasional ... 26
1. Klasifikasi Variabel ... 26
2. Definisi Operasional ... 26
C.Bahan Penelitian ... 27
D.Alat Penelitian ... 28
E.Tata Cara Penelitian... 28
1. Determinasi Tanaman S.rebaudiana 2. Pembuatan serbuk simplisia S.rebaudiana a. Pengumpulan Bahan ... 28
b. Sortasi Kering ... 28
c. Pembuatan serbuk... 29
3. Pembuatan Ekstrak Tanaman S.rebaudiana ...29
a. Defatisasi serbuk simplisia ... 29
b. Ekstraksi serbuk simplisia secara erkolasi dengan adanya variasi volume etanol dan akuades... 29
4. Analisis Kualitatif Steviosida... 30
5. Analisis Kuantitatif Steviosida... 30
a. Pembuatan larutan standar steviosida 2 mg/ml. ... 30
b. Pembuatan kurva baku... 31
c. Penetapan kadar steviosida dalam ekstrak S. rebaudiana dengan program ImageJ....31
6. Analisis Hasil.. ... 32
a. Analisis hasil kadar steviosida dengan desain faktorial ... 32
b. Yate’s Treatment... 32
BAB IV HASIL DAN PEMBAHASAN A.Determinasi Tanaman... 34
B.Pembuatan Serbuk Simplisia Stevia rebaudiana...34
1. Pengumpulan Bahan ... 34
2. Sortasi Kering ... 35
3. Pembuatan serbuk... 35
C.Pembuatan Ekstrak Cair Dari Daun Stevia rebaudiana ...36
1. Defatisasi serbuk simplisia ... 36
2. Perkolasi dengan aplikasi Desai Faktorial... 37
D.Analisis Kualitatif Ekstrak Tanaman S. rebaudiana (Bert.)... 39
E.Analisis Kuantitatif Ekstrak Tanaman S. rebaudiana (Bert.)... 42
1. Pembuatan Kurva baku ... 42
2. Penentuan kadar sampel dengan softwareImage J...44
F. Analisis Hasil Kadar Steviosida ... 44
BAB V KESIMPULAN DAN SARAN... 49
A.Kesimpulan ... 49
B.Saran ... 49
DAFTAR PUSTAKA ... 50 Lampiran ... 53 Biografi Penulis... 67
DAFTAR TABEL
Tabel I. Gugus gula glikosida steviol... 9
Tabel II. Rancangan percobaan desain faktorial dengan dua faktor dan dua level19 Tabel III. Perbandingan volume etanol dan akuades yang digunakan pada perkolasi ... 30
Tabel IV. Harga Rf baku dan sampel ekstrak steviosida ... 42
Tabel V. Data jumlah steviosida (µg) dengan AUC ... 43
Tabel VI. Data Kadar steviosida (% b/b) untuk masing-masing percobaan ... 44
Tabel VII. Hasil Analisis Satistik Yate’s Treatment... 46
DAFTAR GAMBAR
Gambar 1. Stevia rebaudiana Bert... 7 Gambar 2. Struktur glikosida steviol ... 9 Gambar 3. Struktur kimia steviosida... 11 Gambar 4. Kromatogram baku steviosida dan ekstrak steviosida deteksi vanilin
asam sulfat... 41 Gambar 5. Kurva baku hubungan jumlah steviosida (µg) dengan AUC ... 43 Gambar 6. Pengaruh akuades terhadap kadar steviosida yang terekstrak pada
etanol level rendah dan tinggi ... 45 Gambar 7. Pengaruh etanol terhadap kadar steviosida yang terekstrak pada
akuades level rendah dan tinggi ... 45 Gambar 8. Contour Plot Kadar Steviosida ... 48
DAFTAR LAMPIRAN
Lampiran 1. Surat Keterangan Determinasi... 54
Lampiran 2. Data Penimbangan Baku Steviosida... 56
Lampiran 3. Data Kurva Baku Steviosida... 56
Lampiran 4. Data kadar steviosida pada sampel... 57
Lampiran 5. Data Desain Faktorial dan Efek masing-masing Faktor...57
Lampiran 6. Perhitungan Persamaan Desain Faktorial ... ...58
Lampiran 7. Perhitungan Yate’s Treatment... 60
Lampiran 8. Foto simplisia kering dan serbuk daun Stevia rebaudiana ... 63
Lampiran 9. Foto Alat ... 64
Lampiran 10. Foto Larutan Pereaksi Semprot ... 64
Lampiran 11. Foto Perkolat...65
BAB I
PENDAHULUAN A. Latar belakang
Sekarang ini, perhatian masyarakat di Indonesia akan pentingnya pencegahan penyakit dan perbaikan kesehatan semakin besar. Salah satu penyakit yang banyak diderita dan bersifat kronis adalah diabetes. Upaya peningkatan kesehatan berkaitan dengan penyakit ini adalah mengurangi konsumsi gula atau menggunakan pemanis dengan nilai kalori yang rendah seperti pada pemanis buatan (Widodo, 2008).
Pemanis buatan adalah adalah bahan tambahan pangan yang dapat menyebabkan rasa manis pada produk pangan yang tidak atau sedikit mempunyai nilai gizi atau kalori, hanya boleh ditambahkan ke dalam produk pangan dalam jumlah tertentu (Anonim,2004). Pada mulanya pemanis buatan ini ditujukan untuk penderita penyakit diabetes dan pencegahan terjadinya caries pada gigi. Namun dikarenakan kemudahan untuk mendapatkan dan harganya yang relatif murah, penggunaan pemanis buatan ini meluas pada masyarakat umum termasuk yang tidak mengidap diabetes ( Wati, 2004).
Zat pemanis sintetis yang sering digunakan adalah Ca atau Na sakarin dan siklamat. Penggunaan sakarin pada konsentrasi tinggi menimbulkan rasa pahit getir dan pada jangka panjang dikhawatirkan memicu terjadinya kanker (Achyar, 2005). Penggunaan siklamat berbahaya bagi kesehatan karena senyawa hasil metabolismenya yaitu sikloheksamina bersifat karsinogenik yang dapat merangsang pertumbuhan tumor pada kandung kemih tikus (Mudjajanto, 2005).
2
Oleh karena itu, banyak dilakukan penelitian mengenai pemanis pengganti gula yang sedikit atau hampir tidak mengandung kalori tetapi lebih baik untuk kesehatan. Salah satu yang potensial untuk dikembangkan adalah pemanis alami dari tanaman Stevia rebaudiana Bertonii atau yang lebih dikenal dengan nama stevia (Midmore and Rank, 2002).
Stevia rebaudiana Bertonii, spesies yang paling manis, mengandung seluruh glikosida di daunnya, dan steviosida merupakan komponen yang paling banyak terkandung di dalamnya (3% - 8% dari berat kering daunnya) (Melis, 1992). Steviosida memiliki tingkat kemanisan 110-270 kali dibandingkan gula (Midmore and Rank, 2002). Keuntungan menggunakan steviosida adalah karena stabil, rendah kalori, menjaga kesehatan gigi dengan menurunkan intake gula, dan baik untuk penderita diabetes, stabil dipanaskan sampai 2000C, stabil dalam asam, dan tidak terfermentasi (Geuns, 2003).
Hasil penelitian toksisitas steviosida, menunjukkan tidak adanya efek toksik yang muncul pada tikus dengan pemberian steviosida sampai 7% dari makanan selama tiga bulan. Hasil penelitian jangka pendek juga menunjukkan tidak adanya efek mutagenik ataupun genotoksik dari steviosida (Bakal and Nabors, 1986).
melalui ekstraksi dengan etanol panas (Martono, Kristopo, Sihasale, 2007) ataupun dengan ekstraksi dengan air panas (Matsushita, 1979). Perolehan kristal yang dihasilkan pada penelitian Matsushita sebesar 7,5% sedangkan penelitian Martono dkk hanya sebesar 0,97%. Perbedaan perolehan kristal yang jauh ini belum menunjukkan bahwa air berperan lebih besar dalam penyarian steviosida. Hal ini dapat dikarenakan perbedaan daun S. rebaudiana yang digunakan dalam masing-masing penelitian. Menurut Lutony (1993) kandungan steviosida pada daun S. rebaudiana di Jepang dapat mencapai 20% sedangkan di Indonesia kurang dari 20 %. Selain itu juga dimungkinkan adanya perbedaan dalam proses deklorofilasi dan kristalisasi yang dapat mempengaruhi perolehan kristal steviosida sesudah proses ekstraksi.
Berdasarkan hasil recovery kristal kedua penelitian di atas dibandingkan dengan kandungan steviosida yang terdapat dalam daun, dirasa perlu ditingkatkan recovery kristal yang diperoleh. Proses awal dalam peningkatan recovery kristal ini dengan cara meningkatkan jumlah steviosida yang tersari.
Langkah yang dapat dilakukan guna meningkatkan penyarian biasanya digunakan campuran penyari antara etanol dan air. Perbandingan jumlah etanol dan air tergantung pada bahan yang akan disari. Dari pustaka dapat ditelusuri kandungannya baik zat aktif maupun zat lainnya sehingga dapat dilakukan beberapa percobaan untuk mencari perbandingan pelarut yang tepat (Anonim,1986).
4
digunakan dalam penelitian ini sehingga dapat diketahui pengaruh dari masing-masing penyari dan interaksinya serta volume cairan penyari yang optimum untuk mendapatkan ekstrak dengan kadar steviosida tertinggi. Melalui metode ini dapat dikurangi trial and error dalam percobaan jika dibandingkan dengan meneliti efek faktor secara terpisah (Bolton,1997). Proses ekstraksi yang dilakukan pada penelitian ini menggunakan perkolasi pada suhu 300C sehingga akan meningkatkan efisiensi dari proses ekstraksi dengan mengurangi biaya operasional bahan bakar yang dibutuhkan dibandingkan dengan kedua penelitian
sebelumnya yang menggunakan etanol ataupun air panas. Diharapkan dengan ditemukannya area optimum cairan penyari akan
diperoleh batasan level dari faktor yang diteliti untuk mendapatkan ekstrak dengan kandungan steviosida terbesar. Pemanfaatan teknologi pengolahan, khususnya proses ekstraksi ini nantinya diharapkan dapat meningkatkan perolehan kristal yang diperoleh sehingga juga dapat meningkatkan nilai ekonomis daun S. rebaudiana serta pengembangannya sebagai bahan alternatif pemanis pengganti gula yang alami.
1. Perumusan Masalah
Dari latar belakang di atas, masalah yang muncul dapat dirumuskan sebagai berikut :
a. Manakah yang paling dominan antara etanol 96%, akuades, atau interaksi keduanya dalam menentukan kadar steviosida yang tersari?
2. Keaslian Penelitian
Sejauh penelusuran pustaka penulis, penelitian tentang optimasi volume cairan penyari etanol dan akuades pada proses perkolasi daun S.rebaudiana terhadap perbedaan kadar steviosida yang tersari dengan aplikasi desain faktorial belum pernah dilakukan oleh peneliti lain.
3. Manfaat Penelitian a. Manfaat Teoritis
Penelitian ini diharapkan dapat menambah khasanah ilmu pengetahuan, khususnya dalam bidang kefarmasian sains teknologi mengenai aplikasi desain faktorial pada proses perkolasi steviosida dari daun S. rebaudiana.
b. Manfaat Praktis
Hasil penelitian ini diharapkan dapat memberikan data mengenai pengaruh volume etanol dan akuades ataupun interaksinya dalam proses perkolasi daun S. rebaudiana serta volume cairan penyari paling optimal untuk mendapatkan ekstrak dengan kadar steviosida terbesar.
B. Tujuan Penelitian
1. Mengetahui pengaruh yang dominan antara etanol, akuades, ataupun interaksi keduanya dalam menentukan kadar steviosida yang tersari.
BAB II
TINJAUAN PUSTAKA A. Stevia rebaudiana Bertonii M. 1. Uraian Tanaman
Stevia rebaudiana Bertonii M. merupakan salah satu anggota dari 154 jumlah spesies stevia dan salah satu dari hanya dua yang menghasilkan glikosida steviol (Soejarto, Douglas, Farnsworth 1982). S. rebaudiana merupakan anggota dari famili Compositae. Tanaman ini merupakan tanaman perenial bersemak kecil, yang dapat tumbuh hingga ketinggian 65 cm. Percepatan pembungaan dari tanaman ini setelah tumbuh minimal empat daun sejati telah dapat dilakukan. Reproduksi dari gamet jantan dan betinanya mirip dengan angiospermae angiosperms. Stevia adalah diploid dan mempunyai 11 pasang kromosom, yang sebagian besar karakteristiknya dari anggota genus yang berasal dari Amerika Selatan (Brandle and Rosa, 1992).
Tanaman ini merupakan tanaman asli dari daerah Rio Monday, dataran tinggi di Paraguay. Tanaman ini dapat mencapai tinggi 80 cm saat semua bagian matang. Stevia pertama kali dibawa ke daerah eropa pada tahun 1887 ketika M.S Bertonii mempelajari karakteristik unik dari Indian dan Mestizos Paraguay (Lewis, 1992). Daun dari S. rebaudiana ini digunakan sebagai agen pemanis yang biasa digunakan. Sebuah usaha besar untuk membuat stevia sebagai hasil pertanian di Jepang dimulai oleh Sumida (1968). Sejak saat itu, stevia mulai dikenal sebagai hasil pertanian di beberapa negara diantaranya: Brazil, Korea,
Meksiko, Amerika Serikat, Indonesia, Tanzania, dan sejak tahun 1990 di Kanada (Brandle and Rosa, 1992).
Gambar 1. Stevia rebaudiana Bertonii M. 2. Kegunaan
8
3. Kandungan Kimia
Gambar 2. Struktur glikosida steviol
Tabel I. Gugus gula glikosida steviol
Glikosida Diterpen R1 R2 Tingkat
10
B. Glikosida 1. Umum
Glikosida adalah senyawa yang bila terhidrolisis menghasilkan molekul gula (glikon) dan senyawa bukan gula (a-glikon). Ikatan antara gikon dan aglikon dapat berupa atom O, S, N, dan C, sehingga terdapat empat macam ikatan antara glikon dan aglikon dalam glikosida, yaitu ikatan O-heterosid, ikatan S-heterosid, ikatan N-heterosid, ikatan C-heterosid (Mursyidi, 1990). Pembagian glikosida berdasarkan aglikonnya : golongan antrakinon, golongan saponin, golongan sianofor, golongan tiosianat, golongan flavonol, golongan alkohol, golongan aldehid, golongan lakton, golongan fenol, golongan lain dan senyawa nitrat, golongan kardioaktif (Mursyidi, 1990).
Glikosida pada umumnya adalah larut baik dalam air dan etanol, dalam bahan pelarut seperti eter, kloroform, benzen, tidak larut. Asam encer dan basa encer, dan seringkali pemanasan suatu larutan dalam air menyebabkan pemisahan glikosida (Voigt, 1994).
2. Diterpen
dan diketahui bahwa biosintetik terpenoid merupakan polimerisasi senyawa isopren. Terpenoid bisa digolongkan menjadi :
a. Monoterpenoid dengan jumlah atom C = 10 b. Seskuiterpenoid dengan jumlah atom C =15 c. Diterpenoid dengan jumlah atom C = 20 d. Sesterpenoid dengan jumlah atom C = 25 e. Triterpenoid dengan jumlah atom C = 30
f. Tetraterpenoid dengan jumlah atom C = 40 (Mursyidi, 1990). C. Steviosida
Steviosida merupakan pemanis utama (60-70%) dari pemanis total dalam Stevia sp, dan diketahui mempunyai tingkat kemanisan 110-270 kali kemanisan gula. Steviosida inilah yang bertanggung jawab terhadap after taste yang seringkali dilaporkan (licorice after taste) (Midmore and Rank, 2002). Ekstrak stevia mengandung persentase besar glikosida diterpen steviol, steviosida dan rebaudiosida A (Kuznesof, 2007).
12
Larutan steviosida pada rentang pH 3-9 dengan suhu 1000C selama 1 jam tidak menunjukkan penurunan kadar yang signifikan. Steviosida dipertimbangkan mengalami dekomposisi pada pH 10. Penelitian lain menunjukkan steviosida sangat stabil dalam larutan asam dan dengan adanya garam. Steviosida tidak berinteraksi dengan bahan makanan dan tidak menyebabkan browning. Selain itu steviosida juga tidak terfermentasi sehingga tidak kariogenik (Bakal and Nabors, 1986).
D. Penyarian
Penyarian adalah kegiatan penarikan zat yang dapat larut dari bahan yang tidak dapat larut dengan pelarut cair. Simplisia yang disari mengandung zat aktif yang dapat larut dan zat yang tidak dapat larut seperti serat, karbohidrat, protein, dan lain-lain (Anonim,1986). Proses penyarian dapat dipisahkan menjadi : pembuatan serbuk, pembasahan, penyarian dan pemekatan (Anonim,1986).
Pada umumnya penyarian akan bertambah baik bila permukaan serbuk simplisia yang bersentuhan dengan cairan penyari makin luas. Tetapi dalam pelaksanaannya tidak selalu demikian, karena penyarian masih tergantung juga pada sifat fisik dan kimia simplisia yang bersangkutan (Anonim,1986).
Pada dasarnya proses ekstraksi dibedakan menjadi dua fase:
Fase pencucian. Pada penyatuan cairan ekstraksi dengan material simplisia maka sel-sel yang dirusak atau terusakkan dengan operasi penghalusan langsung kontak dengan bahan pelarut. Komponen sel yang terdapat di sini dengan lebih mudah dapat diambil atau dicuci. Dalam fase pertama ekstraksi ini, sebagian bahan aktif akan tiba-tiba berpindah ke dalam bahan pelarut. Semakin halus serbuk simplisia, maka semakin optimal jalannya proses pencucian simplisia (Voigt, 1994).
Fase ekstraksi. Yang lebih kompleks adalah peristiwa selanjutnya, yaitu fase ekstraksi karena untuk melarutkan komponen dalam sel yang tidak terluka bahan pelarut harus mendesak masuk ke dalamnya. Membran sel yang mengering dan menciut yang terdapat dalam simplisia mula-mula harus dirubah dalam suatu keadaan, yang memungkinkan suatu pelintasan bahan pelarut ke dalam bagian sel. Hal itu terjadi melalui pembengkakan, dengan demikian membran mengalami suatu pembengkakan volume melalui pengambilan molekul bahan pelarut. Kemampuan mengikat dari zat perancah terhadap molekul cairan, menyebabkan struktur perancak tersebut menjadi longgar, sehingga terbentuk ruang antarmiselar, yang memungkinkan bahan ekstraksi mencapai ke dalam ruang dalam sel. Peristiwa pembengkakan ini dalam skala tinggi disebabkan oleh air (Voigt, 1994).
14
mengikuti difusi melalui ruang antarmiselar. Gaya yang bekerja adalah gaya difusi melalui adanya perbedaan konsentrasi antara larutan di dalam sel dengan cairan ekstraksi yang mula-mula masih tanpa bahan aktif. Bahan kandungan sel akan mencapai ke dalam cairan di sebelah luar selama difusi melintasi melintasi membran sampai terbentuknya suatu keseimbangan konsentrasi antara larutan di sebelah dalam dan di sebelah luar sel (Voigt, 1994).
Penyarian dipengaruhi oleh : a. Derajat kehalusan serbuk
b. Perbedaan konsentrasi yang terdapat mulai dari pusat serbuk simplisia sampai ke permukaannya, maupun pada perbedaan konsentrasi yang terdapat pada lapisan batas, sehingga suatu titik akan dicapai, oleh zat-zat yang tersari jika ada daya dorong yang cukup untuk melanjutkan perpindahan massa (Anonim,1986).
Jenis ekstraksi mana dan bahan ekstraksi mana (cairan ekstraksi, menstruum) yang digunakan, terutama tergantung dari kelarutan bahan kandungan serta stabilitasnya. Oleh karena banyak bahan tumbuhan larut alkohol, maka air atau etanol lebih disukai penggunaannya sebagai cairan pengekstraksi (Voigt, 1994).
Ekstrak adalah sediaaan kering, kental, atau cair dibuat dengan menyari simplisia atau nabati menurut cara yang cocok, diluar pengaruh cahaya matahari secara langsung (Anonim, 1979).
E. Perkolasi
ditempatkan dalam suatu bejana silinder yang bagian bawahnya diberi sekat berpori. Cairan penyari dialirkan dari atas ke bawah melalui serbuk tersebut, cairan penyari akan melarutkan zat aktif sel-sel yang dilalui sampai keadaaan jenuh (Anonim, 1986).
Prinsip perkolasi adalah sebagai berikut : serbuk simplisia ditempatkan dalam suatu bejana silinder yang bagian bawahnya diberi sekat berpori. Cairan penyari dialirkan dari atas ke bawah melalui serbuk tersebut, cairan penyari akan melarutkan zat aktif sel-sel yang dilalui sampai mencapai keadaan jenuh. Gerak ke bawah disebabkan oleh kekuatan gaya beratnya sendiri dan cairan di atasnya dikurangi dengan daya kapiler yang cenderung untuk menahan. Kekuatan yang berperan pada perkolasi antara lain : gaya berat, kekentalan, daya larut, tegangan permukaan, difusi osmosa, adhesi, daya kapiler, dan daya geseran (friksi) (Anonim, 1986).
Alat yang digunakan untuk perkolasi disebut perkolator, cairan yang digunakan untuk perkolasi disebut cairan menstrum, larutan yang keluar dari perkolator disebut sari atau perkolat sedangkan sisa setelah dilakukannya penyarian disebut ampas atau sisa perkolasi (Anonim, 1986).
Serbuk simplisia yang akan diperkolasi tidak langsung dimasukkan ke dalam bejana perkolator, tetapi dibasahi atau dimaserasi terlebih dahulu dengan cairan penyari. Maserasi dilakukan dalam bejana tertutup (Anonim, 1986).
16
zat aktif tidak tersari sempurna maka penekanan dapat dilakukan dengan agak kuat. Sebaiknya bila perkolat tidak menetes, berarti massa terlalu padat atau serbuk simplisia terlalu halus. Bila hal ini terjadi, isi perkolator harus dibongkar, dan kemudian dimasukkan kembali dengan penekanan yang agak longgar (Anonim, 1986).
Cairan penyari dituangkan perlahan-lahan hingga di atas permukaan massa masih tergenang dengan cairan penyari. Cairan penyari harus selalu ditambahkan sehingga terjaga adanya lapisan cairan penyari di atas permukaan massa (Anonim, 1986).
Keran diatur sehingga kecepatan menetes 1ml tiap menit. Jika penetesan terlalu cepat, penyarian tidak sempurna, sebaliknya penetesan terlalu lambat akan membuang waktu dan kemungkinan menguap lebih besar (Anonim, 1986).
Untuk menentukan akhir perkolasi dapat dilakukan pemeriksaan zat aktif secara kualitatif pada perkolat terakhir (Anonim, 1986).
F. Sokhletasi
Bahan yang akan diekstraksi berada dalam sebuah kantung ekstraksi (kertas, karton dan sebagainya) di dalam sebuah alat ekstraksi dari gelas yang bekerja kontinu (perkolator). Wadah gelas yang mengandung kantung diletakkan di antara labu suling dan suatu pendingin aliran balik dan dihubungkan dengan melalui pipa pipet (Voigt, 1994).
Uap cairan penyari naik ke atas melalui pipa samping, kemudian diembunkan kembali oleh pendingin tegak. Cairan turun ke labu melalui tabung yang berisi serbuk simplisia. Cairan penyari sambil turun melarutkan zat aktif serbuk simplisia. Karena adanya sifon maka setelah cairan mencapai permukaan sifon, seluruh cairan akan kembali ke labu. Cara ini lebih menguntungkan karena uap panas tidak melalui serbuk simplisia, tetapi melalui pipa samping (Anonim, 1986).
G. Pengeringan
Tujuan pengeringan adalah mendapatkan simplisia yang tidak mudah rusak, sehingga dapat disimpan dalam waktu yang lama. Caranya dengan mengurangi kadar air. Air yang masih tersisa dalam simplisia pada kadar tertentu dapat merupakan media pertumbuhan kapang dan jasad renik lainnya. Enzim tertentu dalam sel masih dapat bekerja, menguraikan senyawa aktif sesaat setelah sel mati dan selama bahan simplisia tersebut masih mengandung air tertentu (Anonim, 1985).
18
pengeringan sudah dapat menghentikan proses enzimatik dalam sel bila kadar airnya mencapai kurang dari 10%. Penghentian reaksi peruraian enzimatik akan mencegah penurunan mutu atau perusakan simplisia (Anonim, 1985).
Hal-hal yang perlu diperhatikan dalam proses pengeringan adalah suhu pengeringan, kelembaban udara, waktu pengeringan, dan luas permukaan bahan. Suhu pengeringan tergantung dari bahan simplisia dan cara pengeringannya. Bahan simplisia yang dikeringkan pada suhu 30-900C, tetapi suhu yang terbaik adalah tidak melebihi 600C (Anonim, 1985).
Berbagai cara pengeringan telah dikenal dan digunakan orang. Pada dasarnya dikenal dua macam pengeringan, yaitu pengeringan alamiah dengan menggunakan sinar matahari secara langsung, dan yang satu dengan diangin-anginkan. Selain pengeringan alamiah ada juga pengeringan buatan yaitu dengan merancang suatu alat pengering sederhana, praktis, dan murah dengan hasil yang cukup baik. Proses pengeringan diharapkan terkontrol untuk mencegah dan menghindari perubahan kimia karena panas sinar matahari yang mengandung sinar ultraviolet ( Anonim, 1985).
H. Desain Faktorial
Factorial design sederhana salah satunya adalah dengan dua faktor pada dua level (rendah dan tinggi). Hal ini berarti ada dua faktor yang masing-masing faktor diuji pada dua level yang berbeda, yaitu pada level rendah dan tinggi (Bolton, 1990).
Optimasi campuran dua bahan (berarti ada dua faktor) dengan desain faktorial (two level factorial design) dilakukan berdasarkan:
Y = bo + b1X1 + b2X2 + b12X1X2
Dengan: Y = respon hasil atau sifat yang diamati X1, X2 = level bagian A, level bagian B
bo, b1, b2, b12 = koefisien dapat dihitung dari hasil percobaaan
bo = rata-rata hasil semua percobaan
b1, b2, b12 = koefisien yang dihitung dari hasil percobaan
Pada desain faktorial dua level dan dua faktor diperlukan empat percobaan (2n=4, dengan 2 menunjukkan level dan n menunjukkan jumlah faktor). Penamaan formula untuk 4 percobaan adalah formula (1) untuk percobaan I, formula a untuk percobaan II, formula b untuk percobaan III, dan formula ab untuk percobaan IV (Bolton, 1990)
Rancangan percobaan desain faktorial sebagai berikut:
Tabel II. Rancangan percobaan desain faktorial dengan dua faktor dan dua level
Percobaan Faktor A Faktor B Interaksi
1 - - +
20
Percobaan b = faktor A level rendah, faktor B tinggi
Percobaan ab = faktor A level tinggi, faktor B tinggi (Bolton, 1997). Efek masing-masing faktor dan interaksinya dapat dihitung sebagai rata-rata selisih antara respon pada level rendah dengan respon pada level tinggi. Efek dan interaksi faktor yang diteliti dapat dirumuskan menjadi persamaan berikut:
Efek faktor A= ((a-(1)) + (ab-b)) / 2 Efek faktor B = ((b-(1)) + (ab-a)) / 2
Interaksi = ((ab-b)) + ((1)-a) / 2 (Bolton, 1997).
Desain faktorial memiliki beberapa keuntungan. Metode ini memiliki efisiensi yang maksimum untuk memperkirakan efek yang dominan dalam menentukan respon. Keuntungan utama desain faktorial adalah bahwa metode ini memungkinkan untuk mengidentifikasi efek masing-masing faktor, maupun efek interaksi antar faktor. Metode ini ekonomis, dapat mengurangi jumlah penelitian jika dibandingkan dengan meneliti dua efek faktor secara terpisah (Bolton, 1997).
I. KLT
Fase diam dibuat dari salah satu penjerap yang khusus digunakan untuk KLT yang dihasilkan oleh berbagai perusahaan. Panjang lapisan tersebut 200 mm dengan lebar 200 atau 100 mm. Untuk analisis, tebalnya 0,1-0,3 mm, biasanya 0,2 mm. Sebelum digunakan, lapisan disimpan dalam lingkungan yang tidak lembab atau bebas dari uap laboratorium (Stahl, 1985).
Fase gerak ialah medium angkut dan terdiri atas satu atau beberapa pelarut. Pelarut bergerak di dalam fase diam, yaitu suatu lapisan berpori, karena ada gaya kapiler. Pelarut yang digunakan hanyalah bertingkat mutu analitik dan bila diperlukan, sistem pelarut multikomponen ini harus berupa suatu campuran sesederhana mungkin yang terdiri atas maksimum tiga komponen. Pada kromatografi jerap, pelarut pengembang dapat dikelompokkan ke dalam deret eluotropik berdasarkan sifat elusinya. Misalnya, heksana nonpolar mempunyai efek elusi lemah, kloroform cukup kuat, dan metanol yang polar efek elusinya kuat. Tetapan dielektrik memberi informasi mengenai kepolaran suatu senyawa. Laju rambat tergantung kepada viskositas pelarut dan tentu juga kepada struktur lapisan (misalnya butiran penjerap) (Stahl, 1985).
Fase gerak dapat berupa hampir segala macam pelarut atau campuran pelarut. Silika gel merupakan fase diam yang paling banyak digunakan dalam KLT. Material ini dapat langsung digunakan atau dicampur dengan pengikat misalnya kalsium sulfat untuk membuat lapisan yang lebih kohesif. Bila digunakan pengikat CaSO4 maka pada namanya diberi tanda G, misalnya silika
22
Sistem pelarut untuk KLT dapat dipilih dari pustaka, tapi lebih sering kita mencoba-coba saja karena waktu yang diperlukan sebentar. Sistem yang paling sederhana adalah campuran pelarut organik yang dipakai untuk memisahkan molekul yang mempunyai satu dan atau dua gugus fungsi. Pelarut diotak – atik terutama dengan mengubah – ubahnya dan mencampurnya agar diperoleh kepolaran yang tepat untuk pemisahan tertentu, biasanya dengan menggunakan deret eluotropi sebagai pedoman. Tiga faktor yang harus kita ingat ketika mencampur pelarut untuk membuat pengembang campuran. Faktor pertama ialah bahwa hanya pelarut yang mempunyai kepolaran yang serupa yang dapat dicampur. Faktor kedua ialah bahwa kepolaran campuran tidak merupakan fungsi linier dari susunan campuran tetapi merupakan fungsi logaritma. Akhirnya, harus diingat bahwa kita dapat memakai landaian antara dua pelarut pada beberapa metode (Gritter, 1991).
Penotolan dimulai 1,5 cm dari tepi pelat bagian bawah, jarak antara 2 totolan 1cm dan diameter totolan 2-5mm. Sampel ditotolkan pada pelat yang sudah dilapisi dengan menggunakan mikropipet atau syringe dengan volume penotolan 1-5µl (Gritter, 1991).
KLT merupakan metode fisikokimia, artinya pada saat pendeteksian lokasi bercak dari komponen yang terpisah yang tidak berwarna umumnya dilakukan dengan cara fisika dan kimia. Cara fisika yaitu dengan melihat senyawa berfluoresensi di bawah lampu UV atau melihat senyawa tidak berfluoresensi dengan latar belakang berfluoresensi. Adapun cara kimia yaitu dilakukan penyemprotan dengan substansi kimia yang akan memberikan noda atau bercak baik yang terlihat pada cahaya tampak ataupun sebagai noda yang tampak pada lampu ultraviolet (Hardjono, 1983).
Deteksi paling sederhana adalah jika senyawa menunjukkan penyerapan di daerah UV gelombang pendek ( radiasi utama kira-kira 254 nm) atau jika senyawa ini dapat dieksitasi ke fluoresensi radiasi UV gelombang pendek dan atau gelombang panjang (365 nm). Jika dengan kedua cara ini senyawa tidak dapat dideteksi maka harus dicoba dengan reaksi kimia. Pertama tanpa pemanasan lalu bila perlu dengan pemanasan (Stahl, 1985).
Jarak pengembangan pada senyawa pada kromatogram biasanya dinyatakan dengan angka Rf atau hRf
Rf = Jarak titik pusat bercak dari penotolan Jarak rambat fase gerak
24
J. Image-J
Image J adalah suatu software Java yang digunakan untuk memproses suatu gambar yang dirancang untuk memproses dan menganalisis suatu gambar, seperti gambar sel secara 3 dimensi, gambar radiological, atau sistem multi gambar perbandingan sistem hemologi. Image J dirancang dan dibuat menjadi program yang lebih mudah dipahami dan digunakan untuk proses mempelajari suatu gambar. Image J dapat digunakan untuk menghitung area, statistik, nilai pixel dan intensitas dari suatu objek gambar, seperti penggunaan KLT densitometer (Anonim, 2008). Lempeng KLT yang telah dielusi kemudian dihitung intensitas bercaknya menggunakan program Image J (Zeligs and Bradlow, 2006).
K. Landasan Teori
Sebagian besar literatur mengekstrak tanaman S. rebaudiana dengan air atau alkohol (etanol atau metanol) panas. Penyarian dengan campuran air dan etanol ini biasanya digunakan untuk meningkatkan penyarian. Perbandingan antara jumlah etanol dan air yang digunakan untuk penyarian tergantung pada bahan yang akan disari.
konsentrasi. Pada maserasi, penyarian yang terjadi tidak maksimal dikarenakan adanya keseimbangan konsentrasi antara cairan penyari dengan sel simplisia.
Steviosida merupakan senyawa glikosida diterpen steviol yang merupakan kandungan utama dalam daun S. rebaudiana. Glikosida steviol merupakan golongan senyawa yang larut dalam air maupun etanol.
Proses penyarian steviosida secara perkolasi menggunakan campuran etanol dan air ini diharapkan dapat meningkatkan kadar steviosida yang tersari. Digunakan variasi volume etanol dan air dalam proses penyarian sehingga melalui desain faktorial dapat diketahui faktor mana yang paling berpengaruh dalam menentukan kadar steviosida, serta volume cairan penyari optimum untuk mendapatkan ekstrak dengan kadar steviosida terbesar.
L. Hipotesis
Hi(1) : kadar steviosida yang didapatkan melalui perkolasi daun S.rebaudiana
menggunakan volume etanol level rendah berbeda dengan volume etanol level tinggi.
Hi(2) : kadar steviosida yang didapatkan melalui perkolasi daun S.rebaudiana
menggunakan volume akuades level rendah berbeda dengan volume akuades level tinggi.
Hi(3) : ada interaksi antara volume etanol dan volume akuades dalam menentukan
BAB III
METODE PENELITIAN A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk dalam penelitian eksperimental murni karena adanya intervensi atau perlakuan terhadap subyek uji, dengan desain penelitian secara desain faktorial.
B. Variabel dan Definisi Operasional 1. Klasifikasi Variabel
a. Variabel Bebas
Volume etanol dan akuades masing-masing 150 ml dan 375 ml. b. Variabel Tergantung
Kadar steviosida yang tersari dari daun S. rebaudiana. c. Variabel Pengacau Terkendali
1) Suhu sokhlet diatur pada rentang 640C – 650C. 2) Suhu ekstraksi menggunakan 300C
d. Variabel Pengacau Tak Terkendali
Lama dan proses pengeringan simplisia setelah dipanen. 2. Definisi Operasional
a. Perkolasi merupakan suatu metode ekstraksi menggunakan variasi jumlah pelarut etanol dan akuades dengan perkolator yang telah dimodifikasi menggunakan pemanas dengan suhu 300C, kecepatan tetesan 1ml/menit.
b. Ekstrak Steviosida merupakan ekstrak cair yang didapatkan secara perkolasi 300C dengan variasi volume etanol dan akuades yang berasal dari serbuk daun S. rebaudiana.
c. Etanol yang dimaksud dalam penelitian ini adalah etanol 96 % d. Air yang dimaksud dalam penelitian ini adalah akuades
e. Respon adalah besaran yang akan diamati perubahan efeknya, besarnya dapat dikuantitatifkan. Dalam penelitian ini, respon yang dimaksud adalah banyaknya steviosida.
f. Efek adalah perubahan respon yang disebabkan variasi level dan faktor. g. Area optimum adalah area dimana variasi volume etanol dan akuades
menghasilkan ekstrak dengan kadar steviosida >7% b/b dari bobot serbuk kering daun S. rebaudiana.
h. Steviosida yang dimaksud dalam penelitian ini adalah steviosida yang setara dengan baku steviosida (99,2% assay dengan HPLC BM 804,87 Wako Jepang).
i. Penetapan kadar steviosida dengan menghitung luas area di bawah kurva (AUC) bercak pada lempeng KLT dengan program Image J.
C. Bahan Penelitian
28
kloroform p.a., metanol p.a., akuabides, pereaksi semprot KI, pereaksi semprot vanilin-asam sulfat.
D. Alat Penelitian
Alat yang digunakan dalam penelitian ini antara lain: alat-alat gelas, grinder, ayakan mesh 50, oven, lemari es, sokhlet, seperangkat alat perkolasi, perangkat KLT, neraca analitik (Precision Balance, model GB-3002, Melter Todelo), hot plate magnetic stirer merk Cenco Instrument, pipet kapiler 1 µl merk Einmal-Mikropipetten, lampu UV 254 nm, chamber, scanner, program Image J.
E. Tata Cara Penelitian 1. Determinasi Tanaman S. rebaudiana
Determinasi Tanaman S. rebaudiana dilakukan oleh Balai Besar Penelitian dan Pengembangan Tanaman Obat dan Obat Tradisional (B2P2TO2T) menurut Backer (1968).
2. Pembuatan serbuk simplisia S. rebaudiana a. Pengumpulan bahan
Penelitian ini menggunakan simplisia daun S. rebaudiana yang diperoleh dari Balai Besar Penelitian dan Pengembangan Tananaman Obat dan Obat Tradisional (B2P2TO2T).
b. Sortasi Kering
c. Pembuatan serbuk
Daun tanaman S. rebaudiana hasil sortasi yang telah dioven selama satu hari, diserbuk menggunakan grinder (mesin penyerbuk). Kemudian serbuk diayak dengan ayakan nomor mesh 50. Proses pengayakan untuk setiap 500 gram serbuk berlangsung selama 5 menit hingga diperoleh derajat kehalusan serbuk yang dikehendaki.
3. Pembuatan Ekstrak Tanaman S. rebaudiana a. Defatisasi serbuk simplisia
Lima puluh gram daun S. rebaudiana yang telah halus, dipisahkan dari senyawa – senyawa non polar menggunakan pelarut heksan sejumlah volume 2 kali sirkulasi dengan alat soklet. Sokletasi ini dilakukan selama 2 x 8 jam, dengan jumlah sirkulasi 3 – 4 kali per 10 menit pada suhu 640C – 650C. Simpan residu sampel dalam oven suhu 400C. Setelah kering residu sampel kemudian siap untuk diekstraksi.
b. Ekstraksi serbuk simplisia secara perkolasi dengan adanya variasi volume etanol dan akuades
30
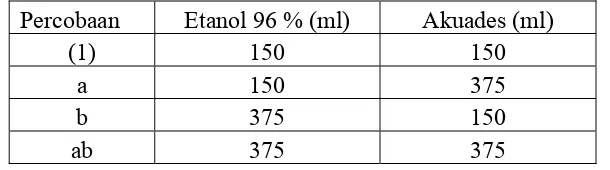
serta ditambahkan berulang–ulang cairan penyari secukupnya sehingga selalu terdapat selapis cairan penyari di atas simplisia dan diatur suhu perkolator sesuai yang diinginkan yaitu 300C. Digunakan variasi volume pelarut etanol dan akuades seperti pada tabel III:
Tabel III. Perbandingan volume etanol dan akuades yang digunakan pada perkolasi
Percobaan Etanol 96 % (ml) Akuades (ml)
(1) 150 150
a 150 375
b 375 150
ab 375 375
Proses perkolasi dihentikan setelah didapatkan ekstrak dengan volume total sesuai desain percobaan. Replikasi dilakukan sebanyak 2 kali.
4. Analisis Kualitatif Steviosida
Analisis kualitatif kandungan steviosida dilakukan dengan KLT menggunakan fase diam Silika Gel F254 dan fase geraknya kloroform:
5. Analisis Kuantitatif Steviosida
a. Pembuatan larutan standar steviosida 2 mg/ml
Larutan standar steviosida 2 mg/ml dibuat dengan menimbang kurang lebih seksama 10 mg baku steviosida dan dilarutkan dengan akuabides sampai 5 ml.
c. Pembuatan kurva baku
Larutan standar steviosida (2 mg/ml) ditotolkan pada lempeng Silika Gel F254 dengan pipa mikro kapiler, dengan jumlah totolan masing-masing
1µl, 2µl, 3µl, 4µl, 5µl, 6µl, dan 7µl dimana masing-masing totolan tersebut mengandung seri jumlah standar steviosida sebanyak 2µg, 4µg, 6µg, 8µg, 10µg, 12µg, dan 14µg. Kemudian dielusi dengan fase gerak kloroform : metanol : akuabides (10:15:2). Selanjutnya dilakukan pengukuran luas area di bawah kurva (AUC) bercak menggunakan program Image J. Kemudian ditentukan persamaan kurva baku y = Bx + A antara seri baku dengan luas area.
d. Penetapan kadar steviosida dalam ekstrak S. rebaudiana dengan program Image J
Pemisahan dilakukan dengan KLT dengan fase diam Silika Gel F254 dan
32
Kadar steviosida diketahui dengan memasukkan luas area di bawah kurva (AUC) bercak yang ditetapkan pada Image J sebagai nilai Y dalam persamaan kurva baku.
6. Analisis Hasil
a. Analisis hasil kadar steviosida dengan desain faktorial
Berdasarkan respon tiap kombinasi dapat diperoleh persamaan desain faktorial :
Y = b0 + b1XA + b2XB + b12XAXB
Keterangan :
Y = respon hasil percobaaan/sifat yang diamati, dalam hal ini kadar steviosida
XA = faktor pertama, dalam hal ini etanol 96%
XB = faktor kedua, dalam hal ini akuades
b0, b1, b2, b12 = koefisien yang dapat dihitung berdasarkan hasil
percobaan
Dari persaamaan desain faktorial dapat dibuat suatu profil kadar steviosida dengan adanya variasi volume etanol dan akuades yang digunakan. Kemudian dapat dihitung besarnya efek etanol, efek akuades maupun interaksi yang dihasilkan.
b. Yate’s Treatment
95% untuk melihat signifikansi dari tiap faktor dan interaksinya dalam mempengaruhi respon kadar steviosida.
Sebelumya ditentukan terlebih dahulu, hipotesis alternatif (Hi) yang menyatakan respon kadar steviosida faktor level rendah berbeda dengan respon kadar steviosida faktor level tinggi dan ada interaksi antara faktor dalam mempengaruhi respon, sedangkan H0 merupakan negasi dari Hi yang menyatakan
respon kadar steviosida faktor level rendah tidak berbeda dengan respon kadar steviosida faktor level tinggi dan tidak ada interaksi antara faktor dalam mempengaruhi respon. Hi diterima dan H0 ditolak bila harga F hitung lebih besar
dari F tabel. F tabel diperoleh dari Fα (numerator, denominator) dengan taraf kepercayaan 95 %. Derajat bebas dan interaksi sebagai numerator yaitu 1, dan derajat bebas experimental error sebagai denomimator yaitu 3, sehingga diperoleh harga F tabel untuk interaksi pada semua respon adalah F0,05(1,3) = 10,128
BAB IV
HASIL DAN PEMBAHASAN A. Determinasi Tanaman
Determinasi tanaman dilakukan untuk mendapatkan kepastian akan kebenaran tanaman yang diselidiki sesuai dengan yang dimaksud dalam penelitian. Determinasi dilakukan dengan mencocokkan tanda serta ciri-ciri yang ada pada tanaman dengan kunci determinasi yang ada dalam buku acuan. Determinasi tanaman stevia ini dilakukan oleh Balai Besar Penelitian dan Pengembangan Tananaman Obat dan Obat Tradisional (B2P2TO2T) menurut Backer (1968).
Berdasarkan hasil determinasi yang dilakukan di Balai Besar Penelitian dan Pengembangan Tananaman Obat dan Obat Tradisional (B2P2TO2T) Tawangmangu, tanaman yang digunakan dalam penelitian ini adalah Stevia rebaudiana Bertonii M. (lampiran 1).
B. Pembuatan Serbuk simplisia S rebaudiana 1. Pengumpulan bahan
Penelitian ini menggunakan simplisia daun S. rebaudiana yang diperoleh dari Balai Besar Penelitian dan Pengembangan Tananaman Obat dan Obat Tradisional (B2P2TO2T). Pihak B2P2TO2T mengumpulkan simplisia S. rebaudiana yang dipanen oleh petani di sekitar daerah Tawangmangu setiap dua bulan sekali. Berdasarkan keterangan B2P2TO2T, simplisia ini merupakan varietas jumbo yang dipanen pada umur daun yang sama oleh para petani.
2. Sortasi Kering
Sortasi kering dilakukan dengan tujuan memisahkan daun S. rebaudiana dari bagian-bagaian yang tidak diinginkan seperti batang, bunga, ranting dan juga pengotor lain yang masih tertinggal seperti adanya tanah atau kerikil. Dalam penelitian ini digunakan daun dari tanaman S. rebaudiana dikarenakan kandungan steviosidanya paling tinggi (3% - 8% dari berat kering daunnya).
3. Pembuatan serbuk
Daun S. rebaudiana hasil sortasi kemudian dikeringkan. Pengeringan ini dilakukan dengan oven pada suhu 400C – 500C selama satu hari. Peletakan daun dalam oven ini haruslah rata dan tidak terlalu tebal untuk menjamin keseragaman dan keefektivan pengeringan. Faktor-faktor yang mempengaruhi pengeringan adalah suhu pengeringan, kelembaban udara, aliran udara, waktu pengeringan dan luas permukaan bahan. Daun yang sudah kering ini nantinya akan mempermudah penyerbukan dengan grinder (mesin penyerbuk).
Proses pengayakan serbuk dilakukan dengan menggunakan ayakan no mesh 50. Menurut Matsushita (1979), range ukuran mesh penyerbukan daun S. rebaudiana antara 50-400. Melalui pengayakan ini akan diperoleh ukuran partikel serbuk yang kecil ( ≤ ukuran mesh 50) sehingga proses ekstraksi bertambah baik. Hal ini dikarenakan luas kontak area antara cairan penyari dengan serbuk makin besar.
36
orientasi jika terlalu cepat, banyak serbuk yang belum terpisah secara maksimal. Sedang jika terlalu lama, maka proses pengayakan tidak akan efisien.
C. Pembuatan Ekstrak Cair Dari Daun Stevia rebaudiana 1. Defatisasi serbuk simplisia
Defatisasi ini bertujuan untuk menghilangkan senyawa-senyawa non polar yang terkandung dalam daun seperti lemak, minyak esensial, dan pigmen tumbuhan. Senyawa non polar ini perlu dihilangkan untuk meminimalkan pengaruhnya terhadap proses ekstraksi steviosida. Senyawa-senyawa yang relatif non polar ini dapat ikut tersari oleh adanya etanol, selain itu air juga dapat melarutkan lemak sehingga akan ikut meningkatkan kejenuhan. Senyawa-senyawa non polar pada S. rebaudiana menurut Kuznesof (2007) meliputi dekanoic acid, pentacosane, octacosane, stigmasterol, lupeol, dan pentacyclic triterpene. Melalui defatisasi ini, diharapkan proses ekstraksi steviosida yang dilakukan pada tahap selanjutnya akan lebih optimal. Pelarut heksan digunakan dalam defatisasi ini, dikarenakan kepolarannya yang sangat rendah sehingga akan lebih efektif dalam menyari senyawa non polar dan tidak mengurangi kadar steviosida yang nantinya tersari yang bersifat relatif polar.
digunakan sejumlah 2 x sirkulasi untuk menjamin agar proses penyarian terus berlangsung (tidak kehabisan atau hangus). Lama defatisasi ini 2 x 8 jam, yang menunjukkan bahwa tiap 8 jam dilakukan penggantian cairan penyari (heksan) agar proses penyarian lebih efektif (cairan penyari yang baik haruslah murni atau azeotrop). Waktu dan jumlah sirkulasi sudah dioptimasi untuk menghasilkan titik akhir defatisasi yang menunjukkan cairan terlihat jernih (indikator visual sudah habisnya senyawa yang terlarut oleh heksan).
2. Perkolasi dengan aplikasi Desain Faktorial
Ekstraksi secara perkolasi ini dilakukan dengan mengalirkan cairan penyari melalui serbuk simplisia yang telah dibasahi. Cairan penyari akan dialirkan dari atas ke bawah melalui serbuk dan akan melarutkan zat aktif dalam sel-sel sampai jenuh. Pembasahan atau maserasi ini penting untuk simplisia yang mengandung bahan yang mudah mengembang jika kontak dengan air. Jika bahan tersebut langsung dialiri cairan penyari tanpa pembasahan, maka cairan penyari tidak dapat menembus ke seluruh bagian sel dengan sempurna (penyarian tidak efektif karena tidak seluruh sel mengembang). Apabila bahan tersebut dibasahi terlebih dahulu, seluruh sel serbuk akan mengembang dan aliran cairan penyari akan merata.
38
10%). Penetesan yang terlalu cepat menyebabkan penyarian tidak sempurna, sedangkan penetesan yang terlalu lambat akan menyebabkan kemungkinan menguapnya cairan penyari lebih besar dan tidak efisien dalam hal waktu penyarian.
Kondisi penyarian harus dijaga agar selalu ada selapis cairan penyari di atas serbuk (tergenangi). Jika serbuk kering terutama pada bagian permukaan dapat menyebabkan adanya gelembung-gelembung udara yang mengganggu penyarian. Cairan penyari tidak dapat menembus sel-sel zat aktif karena terhalang oleh gelembung udara. Selain itu aliran perkolat akan melambat karena gaya aliran ke bawah berkurang jika tidak ada selapis cairan penyari di atas serbuk.
Pada proses perkolasi ini digunakan suhu 300C untuk meningkatkan efisiensi proses ekstraksi dengan mengurangi beban bahan bakar sekaligus mengontrol suhu proses ekstraksi. Suhu dapat meningkatkan kelarutan bahan aktif dalam cairan penyari. Oleh karenanya dengan suhu yang terkontrol ini diharapkan dapat mengurangi variabilitas penelitian sehingga perolehan kadar steviosida yang didapatkan hanya berasal dari pengaruh variasi volume etanol dan akuades.
Pada penelitian ini, pertimbangan yang digunakan untuk menentukan level rendah tiap faktor 150 ml dengan total volume 300 ml adalah perbandingan minimal serbuk dengan cairan penyari untuk mendapatkan hasil ekstrak yang cukup memberikan respon adalah 1 : 10. Serbuk yang digunakan 30 g, sehingga total volume cairan penyari minimal adalah 300 ml. Level tinggi tiap faktor yang digunakan adalah 375 ml. Hal ini didasari pertimbangan total volume cairan penyari yang digunakan yakni 750 ml. Pada saat orientasi, penyarian dengan volume 750 ml didapatkan tetesan perkolat yang mulai terlihat bening, yang dapat diindikasikan penyarian telah mendekati titik maksimalnya. Selain itu, diharapkan dengan penggunaan volume penyari pada rentang level tersebut dapat memberikan hasil yang berbeda secara signifikan terhadap kadar steviosida.
D. Analisis Kualitatif Ekstrak Tanaman S. rebaudiana (Bert.) Analisis kualitatif dilakukan dengan menggunakan prinsip Kromatografi lapis Tipis (KLT). Tahap ini dilakukan untuk memastikan bahwa ekstrak yang dihasilkan benar mengandung senyawa yang dikehendaki, dalam hal ini adalah steviosida.
Penggunaan fase diam Silika Gel F254 adalah karena bersifat polar
sehingga dapat mengikat senyawa yang akan kita pisahkan yaitu steviosida yang bersifat relatif polar. Selain itu, fase diam yang cocok digunakan untuk pemisahan senyawa terpenoid adalah Silika Gel F254. Fase gerak yang digunakan adalah
40
campuran dari tiga komponen ini dikarenakan satu pelarut saja (akuabides) dapat menggerakkan bercak terlalu jauh sedangkan jika kloroform saja tidak dapat menggerakkan bercak cukup jauh. Pencampuran akuabides dan kloroform saja dikhawatirkan dapat menyebabkan terjadinya pemisahan pelarut pada saat dikembangkan, karena perbedaan kepolaran yang cukup jauh (sesuai deret eleutropik). Oleh karena itu, fungsi penambahan metanol disini untuk mengatasi perbedaan kepolaran yang cukup jauh sehingga nantinya fase gerak dapat lebih tercampur, selain juga untuk mengubah kepolaran campuran fase gerak.
Analisis kualitatif steviosida dilakukan dengan menotolkan sampel ekstrak dan baku steviosida pada lempeng Silika Gel F254, kemudian dielusi
Gambar 4. Kromatogram baku steviosida dan ekstrak steviosida deteksi vanilin asam sulfat
Keterangan
Fase Diam : Silika Gel F254
Fase gerak : kloroform: metanol: akuabides (10:15:2) Deteksi : vanilin asam sulfat
42
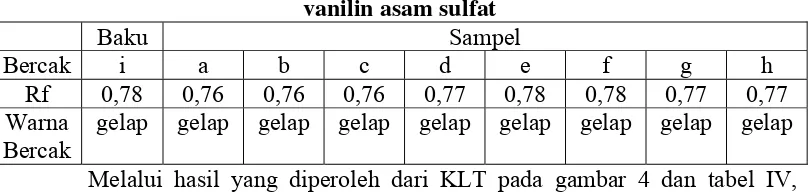
Tabel IV. Harga Rf baku dan sampel ekstrak steviosida dideteksi dengan vanilin asam sulfat
gelap gelap gelap gelap gelap gelap gelap gelap gelap Melalui hasil yang diperoleh dari KLT pada gambar 4 dan tabel IV, diketahui bahwa sampel ekstrak mengandung steviosida. Hal ini ditunjukkan dari kedelapan bercak sampel ekstrak, yang semuanya memiliki harga Rf mirip dengan Rf standar steviosida yaitu 0,78 dan intensitas warna bercak yang menyerupai baku.
E. Analisis Kuantitatif Ekstrak Tanaman Stevia rebaudiana (Bert.). 1. Pembuatan Kurva baku
Kurva baku yang digunakan dalam penelitian ini menggunakan seri jumlah baku steviosida(µg), bukan menggunakan seri kadar baku seperti pada umumnya pembuatan kurva baku. Hal ini dikarenakan minimnya jumlah baku steviosida yang tersedia untuk dibuat seri kadar baku yang sesuai. Pembuatan seri baku berdasarkan massa atau jumlahnya ini dilakukan dengan jumlah penotolan yang berbeda-beda. Semakin banyak totolan menunjukkan semakin besar massa steviosida yang terelusi.
Persamaan kurva baku ini dibuat dengan menggunakan data pada totolan kedua sampai totolan keenam. Hal ini dikarenakan totolan pertama sulit teramati (terlalu tipis), sedangkan pada totolan ketujuh, visualisasi bercaknya menyulitkan Image-J untuk mendapatkan data luas bercak di bawah kurva (AUC) yang sesuai sehingga data bercak ketujuh tidak dimasukkan dalam perhitungan persamaan kurva baku. Data nilai AUC dari totolan baku kedua sampai keenam masih meliputi nilai AUC sampel, sehingga persamaan kurva baku yang diperoleh dapat digunakan untuk mengetahui jumlah steviosida pada sampel.
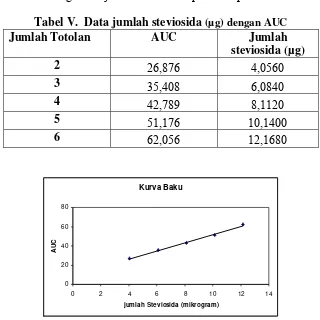
Tabel V. Data jumlah steviosida (µg) dengan AUC
Jumlah Totolan AUC Jumlah
steviosida (µg)
44
2. Penentuan kadar sampel dengan Software Image J
Penentuan kadar sampel dilakukan sama seperti pada pembuatan kurva baku, hanya saja jumlah totolan yang digunakan tetap yaitu 3 µl. Data yang diperoleh adalah :
Tabel VI. Data Kadar steviosida (% b/b) untuk masing-masing percobaan Pengulangan
Uji
1 a b ab
1 3,6227 5,5953 3,6598 8,3992
2 2,7630 5,3066 4,4363 7,1767
Rata-rata 3,1929 5,4509 4,0481 7,7879
SD 0,6079 0,2041 0,5491 0,8644
Berdasarkan tabel VI diketahui bahwa rata-rata kadar steviosida terbesar didapatkan pada percobaaan ab yaitu dengan menggunakan volume etanol 375 ml dan volume akuades 375 ml.
F. Analisis Hasil Kadar Steviosida
Data kadar steviosida yang didapatkan berdasarkan tiap-tiap percobaan diolah lebih lanjut menggunakan aplikasi desain faktorial, sehingga didapatkan efek etanol 96 % = 2,9989; efek akuades = 1,5961; efek interaksi = 0,7409. Berdasarkan data tersebut diketahui bahwa efek etanol 96% paling dominan.
0
100 150 200 250 300 350 400
volume akuades (ml)
100 150 200 250 300 350 400
Volume Etanol (ml)
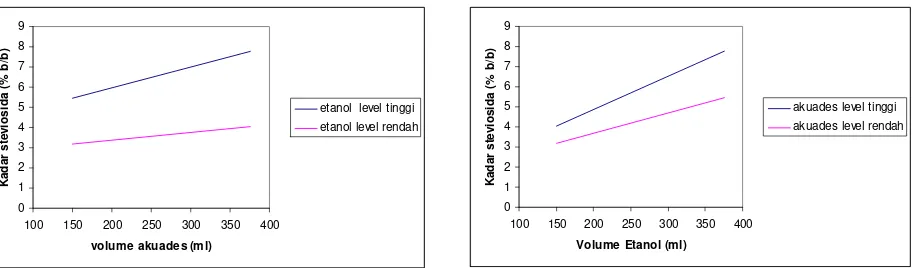
Gambar 6. Pengaruh akuades terhadap kadar steviosida yang
tersari
Gambar 7. Pengaruh etanol terhadap kadar steviosida yang
tersari
Pada etanol 96% level rendah, peningkatan akuades akan meningkatkan
kadar steviosida yang tersari. Pada etanol 96% level tinggi, peningkatan akuades
juga meningkatkan kadar steviosida yang tersari (gambar 6).
Pada akuades level rendah, peningkatan etanol 96% akan meningkatkan
kadar steviosida yang tersari. Pada akuades level tinggi, peningkatan etanol 96%
juga meningkatkan kadar steviosida yang tersari (gambar 7).
Melalui hubungan kedua gambar di atas, diketahui bahwa etanol 96%
maupun akuades memiliki efek meningkatkan kadar steviosida yang tersari. Akan
tetapi, efek dari etanol dalam meningkatan kadar steviosida yang didapatkan lebih
besar. Hal ini dapat terlihat dari jarak antar garis etanol level rendah dan tinggi
yang lebih lebar dengan jarak antar garis akuades level rendah dan tinggi. Hal ini
juga terlihat dari perhitungan desain faktorial pada lampiran 5 dimana nilai efek
etanol 96% paling besar yaitu 2,9989. Adanya interaksi antara etanol 96 % dan
46
Namun untuk menentukan faktor mana yang paling berpengaruh dalam meningkatkan kadar steviosida yang tersari haruslah diuji terlebih dahulu secara statistik apakah pengaruh tersebut signifikan atau tidak. Pengujian secara statistik ini menggunakan Yate’s Treatment. Melalui pengolahan data secara statistik didapatkan hasil ‘:
Tabel VII. Hasil Analisis Satistik Yate’s Treatment Source of
variation
Degrees of
freedom Sum of Squares Mean Squares
F
Replicates 1 28602,3431 28602,3431
Treatment 3 2176268,182 725422,7273
a 1 1618920,183 1618920,183 47,2515
b 1 458546,7641 458546,7641 13,3836
ab 1 98801,2349 98801,2349 2,8837
Experimental error
Nilai Ftabel (1,3) dengan tingkat kepercayaan 95% adalah 10,128. Berdasarkan analisis statistik Yate’s Treatment (Tabel VII) diketahui nilai Fhitung
etanol 96% 47,2515 > 10,128 , sedangkan Fhitung akuades 13,3836 > 10,128,
Nilai Fhitung interaksi lebih kecil dari F tabel sehingga Hi3 ditolak, Ho3
diterima yang menunjukkan tidak ada interaksi antara volume etanol 96% dengan volume akuades dalam menentukan respon kadar steviosida rendah (lampiran 7). Hal ini menunjukkan interaksi tidak berpengaruh secara signifikan, sehingga respon kadar steviosida lebih dipengaruhi oleh faktor yang digunakan, dalam hal ini etanol 96% dan akuades. Namun etanol 96% memberikan efek yang paling dominan, dikarenakan nilai F-nya paling besar.
Efek etanol yang paling dominan ini, dapat dikarenakan kelarutan steviosida yang lebih larut dalam etanol dibandingkan dengan akuades. Hal ini menyebabkan pada saat penyarian dengan komponen etanol lebih besar, lebih banyak pula steviosida yang tersari. Hal ini sesuai dengan penelitian Moussa, Zeitoun dan Hassan (2003) tentang sifat fisikokimia stevia, yang menyatakan bahwa stevia sweetener highly soluble in ethanol and methanol, soluble in water.
Dari hasil penetapan kadar steviosida pada tiap-tiap percobaan, didapatkan persamaan desain faktorial Y = 1,7761+ 5,6449 x 10-3 XA - 5,8978 x
10-4 XB + 2,9270 x 10-5 XAXB. Melalui persamaan tersebut dibuat contour plot
48
yakni >7% b/b, sehingga steviosida yang nantinya didapatkan dapat lebih maksimal.
Gambar 8. Contour Plot kadar steviosida yang didapatkan dari ekstraksi
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Etanol 96% berpengaruh paling dominan dalam menentukan kadar steviosida yang terekstrak.
2. Ditemukan area optimum volume penyari etanol dan akuades untuk menghasilkan ekstrak dengan kadar steviosida terbesar ( >7% b/b).
B. Saran
1. Perlu dilakukan optimasi terhadap penggunaan etanol 96%, akuades, dan suhu sehingga dapat diketahui pengaruh ketiga faktor tersebut dan interaksinya terhadap kadar steviosida yang terekstrak.
2. Perlu dilakukan penelitian lebih lanjut untuk pembentukan kristal steviosida dari ekstrak yang dihasilkan.
50
DAFTAR PUSTAKA
Anonim, 1985, Cara Pembuatan Simplisia, 105-123, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 1986, Sediaan Galenik, 16-17, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 1979, Farmakope Indonesia edisi III, 9, Departemen Kesehatan Republik Indonesia, Jakarta
Anonim, 2004, Keputusan Kepala Badan Pengawasan Obat dan Makanan Republik Indonesia No. hk.00.05.5.1.4547 tentang Persyaratan Penggunaan bahan Tambahan Pangan pemanis Buatan dalam Produk Pangan. Tahun 2004, BPOM, Jakarta
Anonim, 2008, http://www.scientistsolution.com/t11475-image+j.html, diakses tanggal 20 okober 2008
Achyar, 2005, Zat Aditif Pada Makanan,
http://www.pppgtertulis.or.id/index.php?id=16, diakses tanggal 5
November 2008
Amstrong, N.A., James, K.C., 1996, 131 – 165, Pharmaceutical Experimental Design and Interpretation, Taylor and Francis, USA
Backer, C.A., Bakhuizen van den Brink R.C., 1968, flora of Java, Volume I & II, 2, Warta Tumbuhan Obat, Volume I
Bakal, A.I., Nabors, L.O., 1986, Alternative Sweeteners, 295-304, Marcel Dekker, Inc., Ner York
Bolton, S., 1990, Pharmaceutical StatisticPractical and Clinical Application, 2ndI Ed., 308-553, Marcell Dekker Inc., New York
Bolton,S.,1997, Pharmaceutical StatisticPractical and Clinical Application , 3rd Ed., 326, Marcell Dekker Inc., New York
Brandle, J.E., dan Rosa, N., 1992, Heritability for yield, leaf: stem ratio and stevioside content estimated from a landrace cultivar of Stevia rebaudiana. Can. J. Plant Sci. 72: 1263-1266
Gritter, R.J., Bobit, J.M., Schwarting, A.E., 1991, 107-155, Introduction to Chromatography, diterjemahkan oleh Kosasih Padmawinata, Cetakan II, Penerbit ITB, Bandung
Hardjono, S., 1983, Kromatografi, 32-34, Laboratorium Analisa Kimia Pusat, Universitas Gajah Mada, Yogyakarta
Kuznesof, P.M., 2007, 1-8, Steviol Glycosides : Chemical and Technical Assessment
Lewis W.H., 1992, Economic Botanical, 336, Great Britain
Lutony, 1993, Tanaman Sumber Pemanis, Jakarta : Penebar Swadaya.
Mantovanelli, I.C.C., Ferretti, E.C., M. R. Simões, M.R., dan C. Ferreira da Silva. 2004. The effect of temperature and flow rate on the clarification of the aqueous stevia-extract in a fixed-bed column with zeolites. Braz. J. Chem. Eng. São Paulo . vol.21 no.3: 449-458.
Martono, Y., Kristopo, H., Sihasale, L.R.,2007, Recovery produk ekstrak steviosida sebagai bahan alternatif pengganti gula dari Stevia rebaudiana (Bert.), laporan penelitian, Fakultas Sains dan Matematika, Universitas Satya Wacana : Salatiga
Matshushita, 1979, 1-5, Separation of Sweet Component from Natural Sweet Extracts
Megeji, N.W., Kumar, J.K., Singh, V., Ahuja, P.S., Introducing Stevia rebaudiana, a natural zero-calorie sweetener, Institute of Himalayan Bioresource Technology, Palampar 176 061, India, Current Science, Vol.88, No.5, 10 Maret 2005.
Melis, M.S., 1992, 213-217, Stevioside effect on renal function of normal and hypertensive rats, Journal of Ethnopharmacology 36(3), USA
Midmor, D.J., and Rank, A.H., 2002, A New Rural Industry – Stevia- to Replace Imported Chemical Sweeteners, RIRDC Rural Industries Research & Development Corporation
Moussa, M.M; Zeitoun. A.M.; ZeitounA.A. and Hassan I. Mona, 2003, Physicochemical properties of stevia sweeteners as natural low caloric sweetener, Egypt. J. Dairy Sci..31,pp 61-70, 31(??), 61 - 7
52
Mudjajanto, E.S. 2005. Keamanan Jajanan Tradisional. http://www.kompas.com/kompas-cetak/0502/17/ilpeng/1563189.htm, diakses tanggal 5 November 2008
Mursyidi, A.,1990, Analisis Metabolit Sekunder, 192-193, 245, Penerbit: Proyek Pengembangan Pusat Fasilitas Bersama Antar Universitas (Bank Dunia XVII)-PAU Bioteknologi Universitas Gadjah Mada, Yogyakarta
Nanayakkara, N.P., Klocke, J.A., Compadre, C.M., Hussain, R.A., Pezzuto, J.M. & Kinghorn, A.D. (1987) Characterization and feeding deterrent effects on the aphid, Schizaphis graminum, of some derivatives of the sweet compounds, stevioside and rebaudioside A. J. Nat. Prod., 50, 434-441. Sapna, S., Avinash, K., Mukul, T., Pathak, A.K., 2008, Pharmacognosy and
Phytochemical Investigation of Stevia rebaudiana, Pharmacognosy magazine,vol 4, issue 13 (suppl), Jan-Mar 2008
Soejarto DD, Douglas K, dan Farnsworth NR. 1982. Potential sweetening agents of plant origin. III. Organoleptic evaluation of Stevia leaf herbarium samples for sweetness. J Nat;45(5):590-599.
Stahl, E., 1985, Drug Analysis by Chromatography and Microscopy : a practical supplement to to pharmacopias, diterjemahkan oleh Kosasih P. dan Soediro, 205-207, ITB, Bandung
Sumida T (1968). Reports on stevia introduced from Brazil as a new sweetness resource in Japan (English summary). J. Cent. Agric. Exp. Stn. 31: 1-71. Voigt, R., 1994, Buku Pelajaran teknologi Farmasi, edisi ke-5, diterjemahkan
oleh Soendani Noerono, 565-572, Universitas Gadjah Mada, Yogyakarta Wati, H.H., 2004, Kadar Pemanis Buatan Pada Minuman Yang Dijual Di Sekolah
Dasar Di Kecamatan Wonoayu Kabupaten, Sidoarjo,
http://etd.library.ums.ac.id/go.php? id= jiptummpp-gdl-s1-2004 hennyhikma-132, diakses tanggal 8 januari 2009.
Widodo, R., 2008, Mengenal Pemanis Buatan Mutakhir, http://www.untag-sby.ac.id/index.php?mod=berita&id=128, diakses tanggal 8 januari 2009
54
56
Lampiran 2. Data Penimbangan Baku Steviosida Berat Cawan = 13,36065 g
Berat Cawan + Zat = 13,37079 g Berat Zat = 0,01014 g
= 10,14 mg add 5 ml Konsentrasi Baku Steviosida = 2,028 mg/ml
Kadar Steviosida dalam 1µl (1 totolan ) = 2,028 µg
Lampiran 3. Data Kurva Baku Steviosida
Jumlah Totolan AUC Massa (µg)
2 26,876 4,0560
3 35,408 6,0840
4 42,789 8,1120
5 51,176 10,1400
6 62,056 12,1680
A = 9,2098 B = 4,2469 R = 0,9975
Lampiran 4. Data kadar steviosida pada sampel