Kondensasi Senyawa Karbonil dan Reaksi Cannizaro
Maykel Gautama
10512075 ; K-01; Kelompok Vmaykel.gautama@gmail.com
Abstrak
Reaksi Cannizzaro adalah reaksi redoks yang menggunakan dua buah molekul aldehid yang direaksikan sehingga membentuk satu molekul alkohol primer dan satu molekul asam karboksilat dalam suasana basa. Pada percobaan ini telah berhasil dilakukan kondensasi dibenzalaseton dengan dua cara dan juga dilakukan reaksi cannizzaro pada benzaldehid sehingga menghasilkan benzil alkohol dan asam benzoat. Pada percobaan pertama , dilakukan sintesis senyawa dibenzalaseton dengan mereaksikan benzaldehid dengan aseton dan etanol. Pada percobaan kedua dilakukan lagi síntesis dibenzalaseton tapi dengan menggunakan reagen 4-metoksibenzaldehid , aseton dan etanol. Dan pada percobaan ketiga dilakukan reaksi cannizzaro dengan menggunakan benzaldehid.
Kata kunci: Reaksi Cannizzaro, Dibenzalaseton, Benzaldehid, Benzil Alcohol, Asam Benzoat.
Abstract
Cannizzaro reaction is a redox reaction which uses two molecules of an aldehyde and reacted it to produce a primary alcohol molecule and a carboxylic acid molecule in base state. In this experiment, condensation of dibenzalacetone with two method successfully performed and cannizzaro reaction with benzaldehyde performed to produce benzyl alcohol and benzoic acid. In first experiment, dibenzalacetone synthesized from benzaldehyde with acetone and ethanol. In second experiment, dibenzalacetone synthesized again but with different compound, using reagen 4-methoxybenzaldehyde, acetone, and ethanol. In third experiment, cannizaro reaction performed using benzaldehyde.
Keywords: Cannizzaro Reaction, Dibenzalacetone, Benzaldehyde, Benzyl Alcohol, Benzoic Acid.
1. PENDAHULUAN
Reaksi kondensasi aldol dapat terjadi dengan mereaksikan suatu aldehid dengan suatu aldehid lain ataupun keton pada suasana basa. Pertama-tama aldehid direaksikan dengan suatu basa sehingga menghasilkan suatu ion enolat lalu ion enolat ini di reaksikan dengan suatu aldehid atau keton sehingga di dapatkan senyawa aldol(aldehid dan alkohol). Pada percobaan kali ini digunakan 2 reagen berbeda untuk mensintesis dibenzalaseton , yang pertama menggunakan benzaldehid dan aseton sebagai reagennya dan yang kedua menggunakan 4-metoksi benzaldehid dan aseton sebagai reagennya. Selain itu pada percobaan kali ini juga dilakukan reaksi Cannizzaro terhadap benzaldehid. Reaksi Cannizzaro terjadi ketika aldehid di panaskan di dalam larutan hidroksida sehingga sebagian aldehid teroksidasi menjadi asam karboksilat dan sisanya tereduksi menjadi alcohol primer.
Tujuan dari percobaan kali ini adalah mensintesis senyawa aldol yaitu dibenzalaseton
dan juga melakukan reaksi Cannizzaro terhadap benzaldehid sehingga menghasilkan asam benzoat dan alcohol primer lalu menentukan rendemen , galat titik leleh dan Rfnya.
2. METODE PERCOBAAN
Pada percobaan ini , dilakukan tiga percobaan yaitu dua percobaan untuk sintesis dibenzalaseton dengan reagen yang berbeda dan satu percobaan adalah melakukan reaksi Cannizzaro pada benzaldehid. Percobaan pertama adalah sintesis dibenzalaseton dengan menggunakan reagen benzaldehid. Pertama-tama 1mL enzaldehid dicampurkan dengan 0,37 mL asetón & 1 mL etanol. Lalu dibuat juga larutan campuran dari 1 gram NaOH, 10mL air dan 8 mL etanol di dalam labu erlenmeyer 50 mL. Setengah dari campuran benzaldehid yang telah dibuat kemudian dimasukkan ke dalam larutan NaOH dan campuran diaduk selama 20 menit sambil ditambahkan sisa campuran benzaldehid. Jika campuran belum homogen , ditambahkan etanol.
Campuran di aduk sampai terbentuk padatan yang mengendap. Campuran ini kemudian di saring menggunakan corong Buchner dan padatan yang terbentuk dicuci dengan air untuk menghilangkan basa yang masih tersisa. Senyawa dibenzalaseton yang terbentuk ini kemudian direkristalisasi dengan menggunakan etenol. Kristal dibenzalaseton kemudian ditimbang dan ditentukan rendemen dan galat titik lelehnya. Lakukan juga kromatografi lapis tipis terhadap sedikit kristal pada pelat silika dengan eluennya adalah etil asetat : n-heksana dengan perbandingan 2:8 , lalu ditentukan nilai Rfnya.
Pada percobaan kedua , reagen yang digunakan adalah 4-metoksibenzaldehid. Pertama-tama 2,5 mL 4-metoksibenzaldehid dicampurkan dengan 1 mL aseton dan 25 mL etanol dalam labu erlenmeyer 100 mL. Lalu ke dalam campuran ditambahkan 5 mL larutan NaOH 10 % dan 20 mL air lalu labu erlenmeyer ditutup. Campuran ini kemudian diguncangkan selama 10 menit sambil dibuka tutupnya sesekali. Campuran lalu didiamkan selama 5-10 menit sambil sesekali diguncangkan kemudian labu erlenmeyer dimasukkan ke dalam penangas es. Larutan campuran kemudian di saring menggunakan corong Buchner dan cristal yang terbentuk di cuci dengan air dingin. Cristal ini kemudian direkristalisasi dengan menggunakan etanol. Produk akhir ini kemudian ditimbang lalu ditentukan rendemen dan galat titik lelehnya. Lakukan juga kromatografi lapis tipis terhadap sedikit kristal pada pelat silika dengan eluennya adalah etil asetat : n-heksana dengan perbandingan 2:8 , lalu ditentukan nilai Rfnya.
Pada percobaan ketiga ini dilakukan reaksi Cannizzaro dengan menggunakan reagen benzaldehid. Pertama-tama , 3 gram KOH di larutkan dala 6 mL air pada labu bundar 50 mL. Kemudian pada larutan KOH ditambahkan 2 mL benzaldehid. Campuran ini kemudian direfluks selama 30 menit sambil diaduk dengan magnetik stirrer. Campuran kemudian didinginkan pada suhu kamar lalu di masukkan ke dalam corong pisah. Cammpuran ini kemudian diekstraksi dua kali dengan masing-masing ekstraksi menggunakan 25 mL eter. Dari kedua ekstraksi , diambil fasa airnya dan diteteskan HCl pekat sampai pHnya
3 lalu fasa air ini didingiinkan di dalam penangas es sampai terbentuk kristal. Campuran ini kemudian disaring dengan menggunakan corong Buchner. Kristal yang merupakan asam benzoat ini kemudian direkristalisasi dengan menggunakan air. Hasil akhir kristal ini kemudian ditimbang dan ditentukan rendemen dan galat titik lelehnya. Pada fasa eter hasil ekstraksi , ditambahkan NaSO4 anhidrat atau CaCl2 anhidrat dan larutan eterkemudian disaring dengan penyaringan biasa ke labu erlenmeyer 50 mL. Uapkan eter ini pada pemanas listrik sampai didapatkan kristal yang merupakan benzil alkohol. Benzil alkohol ini kemudian ditimbang. Lakukan juga kromatografi lapis tipis terhadap benzaldehid , hasil síntesis kristal asam benzoat dan cristal benzil alkohol dengan mengunakan eluen metanol : kloroform dengan perbandingan 2:8 . Kemudian ditentukan nilai Rf dari masing-masing zat.
3. HASIL DAN PEMBAHASAN
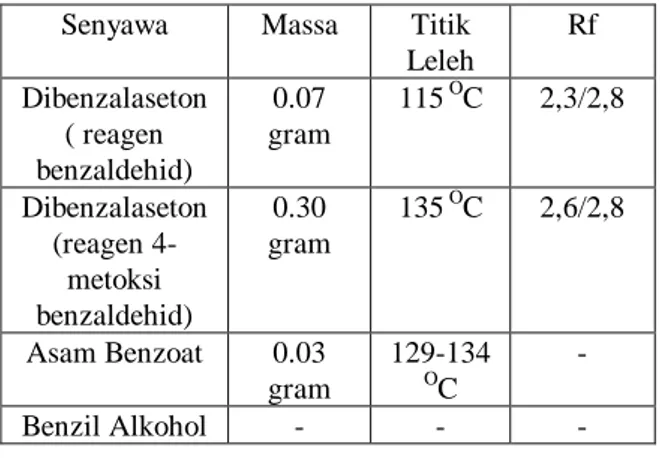
Tabel 1. Data pengamatan hasil percobaan Senyawa Massa Titik
Leleh Rf Dibenzalaseton ( reagen benzaldehid) 0.07 gram 115 OC 2,3/2,8 Dibenzalaseton (reagen 4-metoksi benzaldehid) 0.30 gram 135 OC 2,6/2,8 Asam Benzoat 0.03 gram 129-134 O C - Benzil Alkohol - - -
Pada percobaan pertama , sintesis dibenzalaseton dengan menggunakan reagen benzaldehid diperoleh kristal yang berwarna putih kekuningan dengan massa 0.07 gram sedangkan massa teoritisnya adalah :
Mol benzaldehid awal :
3 1 9 .9 1 0 6 .1 1 .0 5 / 1 0 / 3 x x g ra m m L x g ra m m o l v m L m o l M r
Mol aseton awal (pereaksi pembatas) :
3 0 . 7 9 / 5 8 .0 8 / 1 0 .3 7 5 0. 0 x x g r a m m L v m g r a m m o l x L M r m o l
Massa teoritis dibenzalaseton : 3
1 0 2 3 4 .3 0
5 .0x m o l x g r a m /m o l 1 .1 8 g r a m
sehingga diperoleh rendemen dibenzalaseton dari reagen benzaldehid sebesar :
1 0 0 % 0 .0 7 1 0 0 % 5 .9 3 % 1 . 1 8 m a s sa x m a s sa d ib e n z a la se t d ib e n z a la se to n p e r c o b a a n te o ritis g ra m g ra o x m n
Dan titik leleh dari dibenzalaseton pada percobaan ini adalah 115OC dengan galat sebesar :
1 0 0 % 1 1 5 1 1 1 1 0 0 % 3 . 6 % 1 1 1 0 O O O l e l e h p e r c o b a a n T i t i k l e l e h l i t e r a t u r l e l e T i t i k T i t i k x C C x h l i t e t r C r a u
Pada sintesis 4-metoksidibenzalaseton dengan reagen 4-metoksi benzaldehid , diperoleh massa dibenzalaseton sebesar 0.3 gram sedangkan massa teoritisnya adalah :
Mol awal 4-metoksi benzaldehid :
2.5 1 .119 / 0.023 122.13 / x x gram mL gra v mL mol Mr m m lo
Mol aseton awal (pereaksi pembatas) :
1 0.79 0.014 / 58.08 / x x gram m L gram m ol v m L m ol M r
Massa teoritis 4-metoksidibenzalaseton :
266.30 / 3.7283
0.014m olx gram m ol gram
Sehingga diperoleh rendemen produk sebesar :
4 metoksi 4 metoksi 3. 10 7283 0% 0.3 100% 8.05% massa x massa dib dibenzalaseton percobaan teoritis gram g enzalaseto ram n x
Dan titik leleh dari 4-metoksidibenzalaseton yang diperoleh adalah 135 OC sehingga galatnya sebesar : 1 0 0 % 1 3 5 1 3 0 1 0 0 % 3 . 8 % 1 3 0 5 O O O l e l e h p e r c o b a a n T i t i k l e l e h l i t e r a t u r l e l e T i t i k T i t i k x C C x h l i t e t r C r a u
Pada reaksi Cannizzaro , hanya berhasil didapatkan kristal asam benzoat dengan massa sebesar 0.03 gram namun benzil alkohol tidak berhasil disintesis. Sehingga rendemen dari kristal asam benzoat ini adalah :
Mol benzaldehid awal (pereaksi pembatas) :
2 1 .05 0.0 / / 19 106.13 x x gram m L gram m ol v m L m ol M r
Mol KOH awal : 3 5 6 / 0 .0 54 g ra m g ra m m o l m m o M r l
Massa teoritis Asam Benzoat :
½ x 0.019 mol x 108 gram/mol =1.026 gram Rendemen : 100% 0.03 100 % 3.01 1.026 %
asam benzoat percobaan asam benzoat teoritis gram g massa x massa ramx
Galat yang di peroleh untuk asam benzoat ini adalah : 1 0 0 % 1 3 1 . 5 1 2 2 1 0 0 % 7 . 7 8 % 2 1 2 O O O l e l e h p e r c o b a a n T i t i k l e l e h l i t e r a t u r l e l e h l i t e r a t u r T i t i k T i t i k x C C x C
Pada percobaan sintesis dibenzalaseton , etanol digunakan sebagai pelarut dan penggunaan NaOH sebagai pensuasana basa dan juga sebagai pereaksi dalam pembuatan ion enolat dari aseton. Aseton memiliki atom hidrogen
sehingga dalam suasana basa ia dapat membentuk karbanion dari hasil penyerangan OH- ke atom C karbonil dan menjadikan nya suatu nukleofil. Ion enolat ini sangat reaktif dan bermuatan negatif , sehingga ia dapat menyerang atom C karbonil pada benzaldehid menghasilkan benzalaseton. Benzaldehid tidak bisa menjadi suatu ion enolat karena ia tidak memiliki atom Hidrogen
. Kemudian benzal aseton di serang lagi oleh ion OH- (masih bersuasana basa) pada atom C karbonilnya sehingga pada benzilaseton terjadi tautomerisasi menjadi bentuk enol. Hasil akhir dari reaksi ini adalah dibenzalaseton. Pembagian larutan benzaldehid dan aseton menjadi dua bagian , supaya sebagian aseton pada larutan awal yang di campur larutan KOH bereaksi sempurna semuanya menghasilkan ion enolat lalu kemudian baru ditambahkan sisa larutan benzaldehid dan aseton sehingga ion enolat yang terbentuk di awal bereaksi dengan benzaldehid dan aseton baru dari larutan sisa bereaksi dengan NaOH. Pengadukan ini berfungsi untuk mempercepat berlangsungnya reaksi secara kinetik (supaya ion enolat lebih cepat bertumbukan dengan benzaldehid). Rekristalisasi bertujuan untuk memurnikan kristal dibenzaldehid yang terbentuk , rekristalisasi ini dilakukan dengan menyaring larutan kristal dibenzalaseton dengan etanol secara panas-panas dengan penyaringanbiasa supaya semua analit larut dalam etanol dan disaring sebelum analit mulai membentuk kristal lagi sehingga di harapkan ion pengotor akan tertahan pada kertas saring tersebut saat analit berada dalam fasa larutan. Dari hasil perhitungan , rendemen yang didapat sebesar 5.93 % dengan galat 3.6 %. Jika dilihat dari % galatnya maka senyawa sintesis ini kemungkinan adalah murni dibenzalaseton karen % galatnya kurang dari 5 % namun dilihat dari rendemennya yang kecil , kemungkinan ini disebabkan karena kurang lama dan kurang kuatnya pengadukan larutan sehingga kristal dibenzalaseton yang terbentuk tidak optimal. Selain itu , kemungkinan lainnya adalah saat peroses rekristalisasi , terlalu banyak menggunakan etanol sehingga setelah di saring , sulit untuk membentuk banyak kristal karena jumlah pelarut yang banyak dan juga suhu pelarut yang cukup tinggi.
Pada percobaan kedua , di sintesis 4-metoksidibenzalaseton. yang mekanismenya mirip dengan pembentukan dibenzalaseton. Rendemen yang di peroleh dari percobaan ini sebesar 8.05 % dengan % galat sebesar 3.85 %. Sama seperti percobaan 1 , jika dilihat dari % galatnya , senyawa 4-metoksidibenzaldehid ini murni karena % galatnya kurang dari 5 % namun jika dilihat dari rendemennya , kemungkinan kurangkan kuatnya penguncangan yang dilakukan sehingga antara 4-metoksi benzaldehid dan aseton tidak bereaksi semuanya & saat proses rekristalisasi terlalu banyak digunakan etanol untuk melarutkan senyawa 4-metoksidibenzaldehid.
Pada Percobaan ketiga yaitu reaksi Cannizzaro , air digunakan sebagai pelarut dan benzaladehid dan KOH sebagai reagen. Untuk menghasilkan Asam benzoat dan benzil alkohol di perlukan energi yang besar karena rekasi yang terjadi merupakan reaksi yang eksoterm maka dilakukan refluks. Lalu dilakukan ekstraksi sebanyak 2 kali dengan masing-masing menggunakan 25 mL eter supaya hasil ekstraksi yang di dapatkan lebih baik daripada dengan ekstraksi sekali namun dengan volume yang banyak karena ion-ion yang ingin diekstrak manjadi lebih tersebar pada fasa air & di fasa air bisa didapatkan ion hasil ekstrak lebih banyak. Fasa air mengandung asam benzoat sedangkan fasa eter mengandung benzil alkohol. Di fasa eter di tambahkan Na2SO4 anhidrat supaya mengikat molekul air yang kemungkinan masih tersisa dari proses ekstraksi tadi. Pada percobaan ini tidak berhasil dilakukan penguapan eter karena waktu yang dibutuhkan praktikan tidak mencukupi untuk melakukan penguapan & pengeringan benzil alkohol dari fasa eter. Asam benzoat yang diperoleh dari percobaan ini memiliki rendemen 3.01 % dengan galat 7.78 %. Persentase dari galat yang kecil ini kemungkinan karena kurang
efektifnya ektraksi yang dilakukan sehingga ion-ion benzoat dari fasa eter sedikit yang terekstrak ke fasa air dan saat diuapkan hanya sedikit sekali asam benzoat yang terbentuk. Dilihat dari galatnya senyawa ini masih belum murni asam benzoat karena galatnya lebih besar dari 5 % karena asam benzoat yang didapat terlalu sedikit sehingga tidak dilakukan rekristalisasi dan kemungkinan masih terdapat zat pengotor seperti benzaldehid yang masih belum bereaksi.
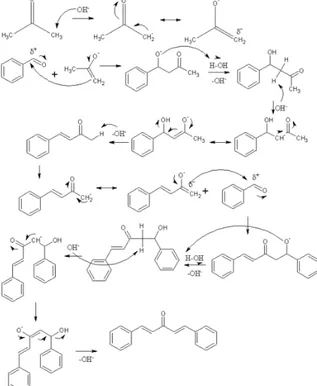
Gambar 1. Mekanisme reaksi pembentukan dibenzalaseton.
4. KESIMPULAN
Pada percobaan kali ini , telah berhasil di sintesis senyawa dibenzalaseton dengan rendemen sebesar 5.93% , galat sebesar 3.6% & Rf 2,3/2,8 . Telah berhasil juga disintesis senyawa 4-metoksi dibenzalaseton dengan rendemen sebesar 8.05% , galat 3.85% & Rf 2,6/2,8. Dan Telah berhasil di sintesis asam benzoat dari reaksi Cannizzaro dengan rendemen sebesar 3.01% & galat sebesar 7.78% namun tidak berhasil diuji KLT dan tidak berhasil di sintesis Benzil Alkohol dari reaksi Cannizzaro.
UCAPAN TERIMAKASIH
Terima kasih saya ucapkan kepada teman-teman praktikum Senyawa Organik Polifungsi kelompok 5 yang selama satu semester ini menemani saya dalam praktikum ini. Terima kasih juga kepada seluruh teman-teman K-01 Kimia ITB 2012 yang telah membantu saya juga baik dalam
hal moral maupun dalam materi pelajaran sehingga saya bisa menyelesaikan laporan akhir praktikum ini. Saya juga berterima kasih kepada seluruh asisten praktikum Senyawa Organik Polifungsi shift Selasa yang telah membimbing saya selama praktikum dan terima kasih juga saya ucapkan kepada Ibu Dr.Deana Wahyuningrum, S.Si., M.Si. yang menjadi Pemimpin Praktikum selama satu semester ini dan juga selalu mengingatkan pentingnya peralatan keselamatan selama praktikum. Tak lupa saya ucapkan juga terima kasih kepada kedua orang tua saya , Tuhan Yang Maha Esa serta pihak-pihak lain yang tidak bisa di sebutkan satu-persatu , karena berkat mereka semua saya bisa menyelesaikan tugas ini.
DAFTAR PUSTAKA
[1] Fessenden, Ralph, J dan Johan, S. Fessenden, 1999, Kimia Organik, Jilid I, Edisi 3, Erlangga : Jakarta.
[2] Juntak, Devi, Reaksi Kondensasi Senyawa Karbonil : Pembuatan Dibenzalaseton.
http://www.for-chem-is-try.wordpress.com, 2014.
[3] Hull, L.A, 2001 , The Dibenzalacetone Reaction Revisited, Journal of Chemical Education, 78(2) , p.226.
[4] Mayo, D.W. , Pike , R.M., Forbes, D.C. , 2011, Microscale Organic Laboratory : with Multistep and Multiscale Synthesis, 5th edition, John Wiley & Sons, New York, p.174-184;310-317.
[5] Pasto, D.J. ,Johnson, C.R., Miler,M.J., 1992 , Experimental Organic Chemistry, Prentice-Hall, Englewood Cliffs, New Jersey, p.509. [6] Wilcox, C.F. and Wilcox, M.F., 1998,
Experimental Organic Chemistry. A Small Scale Approach, Prentice-Hall, Ebglewood Cliffws, New Jersey, p.397.