Interaksi AtMEK1-EXGT pada Arabidopsis thaliana pada Saat Terjadi Pelukaan
Teks penuh
Gambar
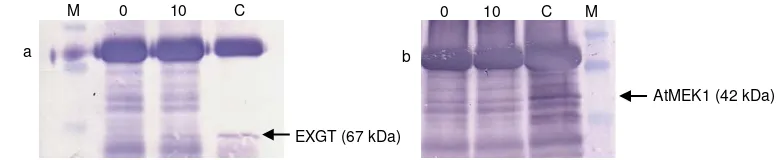
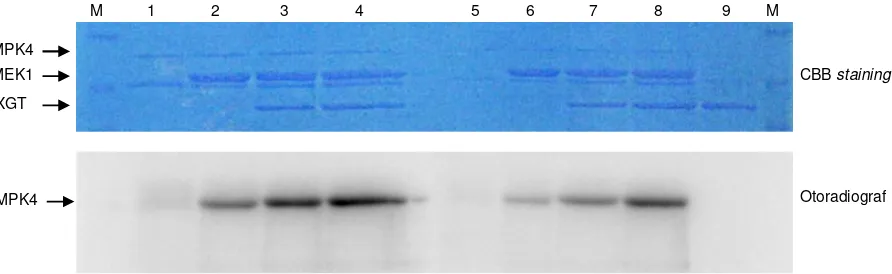
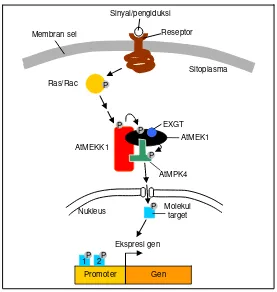
Dokumen terkait
Keluaran dari rangkaian ini akan diproses melalui mikrokontroler ATMega2560, sehingga dapat menampilkan hasil data setiap pasien yang di monitoring pada user interface
perubahan keempat ini adalah Undang-Undang dasar Negara Republik Indonesia Tahun 1945 yang ditetapkan pada tanggal 18 Agustus 1945 dan diberlakukan kembali dengan Dekrit Presiden
International Business & Marketing Management – Victoria University of Wellington. Marketing Management
An online resource bank and community forum where teachers can access thousands of Cambridge support resources, exchange lesson ideas and materials, and join subject-specific
Dan semoga setelah apa yang kita dapat atau kita ketahui dari pembelajaran ini dapat membantu kita dan menjadikan kita seorang yang dapat berfikir dan bertindak dengan benar
Oleh karena itu informasi tentang kesehatan gigi merupakan bagian dari kesehatan secara keseluruhan yang tidak bisa dipisahkan dan penting dalam menunjang kualitas
1) Keanekaragaman jenis burung diurnal di Hutan Sebadal Taman Nasional Gunung Palung ditemukan 40 jenis yang masuk ke dalam 17 family dan 4 ordo dengan total
Perkembangan masyarakat Indonesia pada saat ini dalam menghadapi era globalisasi yang penuh dengan tantangan dan kemungkinan yang bisa terjadi seakan-akan masyarakat Indonesia