172
KAJIAN KOMPATIBILITAS SEDIAAN REKONSTITUSI PARENTERAL DAN PENCAMPURAN SEDIAAN INTRAVENA PADA TIGA RUMAH SAKIT
PEMERINTAH DI SUMATERA BARAT
(Compatibility Study on Reconstituted Parenteral Dosage Form and Intravenous Admixture at Public Hospitals in West Sumatra)
Henny Lucida1, Khairil Armal2, Harefa3, Muslim Suardi1, Puspa Pameswari1, Miranda Yuneidi1, Allan Bara Yufi1 , Lahvem Alginda1, Lisa Bella Aprianda1
1 Bagian Farmasetika, Fakultas Farmasi Universitas Andalas Padang
2 Rumah Sakit Stroke Nasional Bukittinggi
3 Rumah Sakit Umum Daerah Dr. M. Zein Painan
email: hennylucida@gmail.com
ABSTRACT
This paper reports observational prospective studies on the reconstitution and admixture of the intravenous/parenteral dosage forms by nurses at three public hospitals in West Sumatra namely DR. M. Djamil Hospital Padang, The National Stroke Hospital (RSSN) Bukittinggi and Dr. M Zein Hospital Painan from October 2011 – January 2013. Procedures observed were the reconstitution of antibiotic dried injections (meropenem, ceftriaxon and cefotaxim) and the admixture of phenytoin sodium parenteral solution, regarding aseptic technique, the type and volume of solvent or intravenous solution used in the admixtures. These were then confirmed by laboratory experiments of the same procedures to assess dosage form compatibility and concentration of drug dissolved.
Results showed that aseptic techniques had not been applied during the reconstitution and admixture procedure of parenteral solution at all hospitals observed. Dried injection of antibiotics were reconstituted with sterile aqueous solution on the trolley in The Internal Medicine Ward of Dr. M Djamil and Dr. M. Zein Hospital respectively, while at the RSSN (ICU) it was done in the nurse station. At two hospitals, the dried powdered antibiotics were reconstituted with half recommended volume of solvent. Phenytoin sodium injection solution was mixed with inappropriate solvent (Ringer Lactate). The use of inappropriate solvent type and volume would potentially result in drug’s physical incompatibility such as precipitation and concentration reduction. Laboratory data showed that reconstitution of Meropenem with sterile aqueous solution at recommended volume obtained concentrations of 100.55%, 98.95% and 91.05% at time=0; 24 and 48 hours respectively at room temperature. If it was reconstituted with half of that volume, the concentrations were 78.56%, 78.50% and 73.32% at time=0; 24 and 48 hours respectively at room temperature. Dried injection of cefotaxim reconstituted with recommended volume of solvent obtained the solute concentrations of 102.07%; 96.31% and 93.43% at time=0; 24 and 48 hours, followed by discoloration at room temperature. If it was reconstituted with half of that volume, the concentration of drug in solution was 88.35% at time=0; visually no precipitation but discoloration occurred during storage at room temperature.
In conclusion, the reconstitution and admixture of the intravenous/parenteral dosage forms at the hospitals have not fulfilled Good Preparation Practice (GPP) criteria and required pharmacist’s supervision. Nurses should be trained about GPP and equipped with the Standard Operation Procedure (SOP).
Keywords: antibiotics dried injection, reconstitution of parenteral dosage forms, intravenous admixtures.
173
PENDAHULUAN
Pencampuran intravena (intravenous
admixtures) merupakan suatu proses
pencampuran obat steril dengan larutan intravena steril untuk menghasilkan suatu sediaan steril yang bertujuan untuk penggunaan intravena. Ruang lingkup dari
intravenous admixtures adalah pelarutan atau
rekonstitusi serbuk steril, penyiapan suntikan intravena sederhana, dan penyiapan suntikan intravena kompleks (Kastango, 2004). Sesuai Standar Kompetensi Apoteker Indonesia, apoteker bertanggung jawab untuk memastikan bahwa pencampuran sediaan steril di rumah sakit sesuai dengan Praktek Penyiapan Obat yang Baik (Good
Preparation Practices, GPP) sehingga
terjamin sterilitas, kelarutan dan kestabilannya. Bila terjadi ketidaktepatan dalam pencampuran intravena, baik dari segi prosedur aseptis, teknik pencampuran, pelarutan, dan penyimpanannya dapat menyebabkan pengendapan obat yang beresiko menimbulkan penyumbatan pada alat injeksi dan membahayakan pasien. Tempat dan lama penyimpanan juga berpengaruh pada stabilitas obat. Obat yang sudah direkonstitusi memiliki batas waktu kestabilannya sehingga perlu diperhatikan lama penyimpanannya.
Faktor ketidakstabilan di dalam air menyebabkan sediaan injeksi antibiotika turunan -laktam seperti golongan sefalosporin dan meropenem tersedia dalam bentuk serbuk yang harus direkonstitusi dengan pelarut yang sesuai segera sebelum digunakan. Proses rekonstitusi sediaan antibiotika yang tidak sesuai GPP dapat
memicu ketidak efektifan terapi, bila berlangsung terus menerus dan masiv dapat menjadi salah satu pemicu terjadinya resistensi bakteri terhadap antibiotika tertentu. Resistensi bakteri penyebab infeksi nosokomial telah menjadi masalah serius di rumah sakit Indonesia dan perlu dikendalikan (KEMENKES, 2011). Selain rekonstitusi antibiotika, hal lain yang berpotensi menimbulkan masalah adalah pencampuran larutan injeksi obat dengan cairan intravena steril sebelum diberikan kepada pasien. Salah satunya adalah larutan injeksi fenitoin natrium yang mengandung propilen glikol untuk meningkatkan kelarutannya. Proses pencampuran yang tidak tepat berpotensi menyebabkan pengendapan sehingga kadar obat terlarut berkurang dan menyebabkan tidak optimalnya terapi sehingga dapat menyebabkan penurunan kualitas hidup pasien maupun mengancam jiwa.
Proses rekonstitusi dan pencampuran sediaan intravena biasanya dilakukan oleh perawat segera sebelum disuntikkan kepada pasien. Proses ini perlu diawasi oleh farmasis untuk menjamin bahwa prosedur yang dilakukan telah sesuai GPP. Oleh karena itu, kami tertarik untuk mengevaluasi cara penyiapan larutan injeksi antibiotika dan fenitoin natrium pada 3 rumah sakit pemerintah yang berbeda. Tujuan penelitian ini adalah untuk mengetahui apakah prosedur rekonstitusi dan pencampuran intravena telah mengikuti GPP. Proses yang sama dilakukan di laboratorium untuk membuktikan apakah proses tersebut menghasilkan sediaan injeksi yang memenuhi syarat.
METODE PENELITIAN
Penelitian ini merupakan gabungan antara metoda observasi prospektif di rumah sakit dan pembuktian di laboratorium. Alat dan bahan yang digunakan di laboratorium adalah: shaking incubator (Memmert), Spektrofotometer UV-Vis (SHIMADZU 1700), sediaan steril meropenem generik (Dexa Medica), sefotaksim generik (Dexa
Medica), fenitoin generik (PT. Ikapharmindo Putramas), aqua pro injection, Ringer Laktat dan NaCl 0,9% (PT. Widatra Bhakti).
Penelitian di rumah sakit dilaksanakan selama masing-masing 3 bulan mulai bulan Oktober 2011 sampai Januari 2013 bertempat di Bangsal Penyakit Dalam dan Bangsal Syaraf Rumah Sakit DR. M.
174 Djamil Padang, Ruang ICU RSSN Bukittinggi dan Bangsal Penyakit Dalam Rumah Sakit Dr. M. Zein Painan. Pengamatan dilakukan terhadap prosedur rekonstitusi injeksi kering meropenem, seftriakson dan sefotaksim serta pencampuran larutan injeksi fenitoin natrium meliputi:
a. Lokasi rekonstitusi dan pencampuran sediaan intravena
b. Prosedur aseptis
c. Jenis dan volume pelarut yang digunakan masing-masing oleh 3 orang perawat yang berbeda. Hasil pengamatan dicatat dan dibandingkan dengan persyaratan di literature. Prosedur yang dilakukan perawat diulangi di laboratorium untuk menganalisis apakah terjadi pengendapan dan penetapan kadar zat aktif terlarut.
Metoda analisis kuantitatif yang dilakukan meliputi:
a. Penetapan metoda analisis dan validasi metoda analisis meropenem, fenitoin natrium dan sefotaksim (Patel, 2012; Walash, 2011 dan Kumar, 2011)
Sejumlah tertentu zat aktif dilarutkan di dalam sejumlah volume
aqua pro injection kemudian dikocok
hingga homogen. Larutan induk kemudian diencerkan sehingga konsentrasi menjadi 15 µg/mL lalu diukur absorban dengan panjang gelombang 200 – 400 nm untuk penetapan panjang gelombang maksimum Untuk validasi metoda analisis, dilakukan pengenceran bertingkat larutan induk zat aktif sehingga menghasilkan suatu seri larutan zat aktif. Absorban masing-masing larutan ditentukan pada panjang gelombang maksimum masing-masing zat aktif. Linearitas respon alat terhadap konsentrasi zat aktif ditentukan melalui persamaan regresi kurva kalibrasi. Nilai limit deteksi dan limit kuantitasi dihitung berdasarkan persamaan:
Limit deteksi (LOD) = 3,3 × SD/S
Limit quantitasi (LOQ) = 10 × SD/S
Dimana SD adalah simpangan baku residual dan S adalah kemiringan kurva.
b. Penetapan Kelarutan Masing-Masing Obat dalam Pelarut yang sesuai menurut literature (Trissel, 2009)
Masing-masing zat aktif dilarutkan atau dicampurkan dengan pelarut yang sesuai (meropenem dosis 1 g dilarutkan dengan 25 mL aqua pro injection, fenitoin ampul dosis 100 mg dicampurkan dengan 50 mL NaCl 0,9%, sefotaksim dosis 1 g dilarutkan dengan 12 mL aqua pro
injection) kemudian diletakkan dalam
shaking incubator dengan perputaran
100 rpm pada suhu 250C selama 2 jam untuk mencapai kesetimbangan sistem. Larutan diukur absorbannya dengan spektrofotometer UV. Penetapan kadar juga dilakukan pada selang waktu 24 jam untuk melihat stabilitas larutan.
c. Penetapan Kelarutan Masing-Masing Obat dengan Jenis dan Volume Pelarut yang Ditemukan di Rumah Sakit.
Meropenem dosis 1 g dilarutkan dengan 10 mL aqua pro
injection kemudian dikocok sampai
homogen. Larutan disaring dengan kertas saring kemudian filtrat diambil dan diukur absorbannya dengan spektrofotometer UV. Penetapan kadar juga dilakukan pada selang waktu 24 jam untuk melihat stabilitas larutan.
Fenitoin ampul dosis 100 mg dicampurkan dengan 50 mL Ringer Laktat. Larutan dikocok sampai homogen dan diukur absorbannya dengan spektrofotometer UV. Penetapan kadar juga dilakukan pada
175 selang waktu 24 jam untuk melihat stabilitas larutan.
Sefotaksim dosis 1 g dilarutkan dengan 2,5 mL aqua pro
injection kemudian dikocok sampai
homogen. Larutan disaring dengan
kertas saring kemudian filtrat diambil dan diukur absorbannya dengan spektrofotometer UV. Penetapan kadar juga dilakukan pada selang waktu 24 jam untuk melihat stabilitas larutan.
HASIL DAN DISKUSI Hasil
Jumlah pasien yang menggunakan antibiotik meropenem di bangsal penyakit dalam RSUP DR. M. Djamil Padang dari bulan Mei hingga Juli 2012 adalah 44 orang (laki-laki 21 orang; perempuan 23 orang). Meropenem merupakan antibiotika pilihan terakhir apabila terapi dengan antibiotika lainnya tidak efektif. Ketiga perawat yang diamati melakukan prosedur yang sama dalam proses pencampuran sediaan intravena. Proses pencampuran dilakukan diatas trolli pada ruangan perawatan pasien tanpa mempertimbangkan kondisi aseptis. Jenis dan volume pelarut yang digunakan dapat dilihat pada Tabel I.
Dari penelitian yang dilakukan selama kurang lebih tiga bulan (November 2012 - Januari 2013) di bangsal penyakit dalam RSUD Dr. M. Zein Painan, jumlah pasien yang menggunakan seftriakson adalah 44 orang (laki-laki 25 orang; perempuan 19 orang). Sedangkan jumlah pasien yang menggunakan sefotaksim adalah 13 orang (laki-laki 9 orang; perempuan 4 orang). Antibiotik injeksi yang paling banyak digunakan di bangsal penyakit dalam RSUD Dr. M. Zein Painan adalah seftriakson (77,19%) dan sefotaksim (29,82%) disamping antibiotik injeksi lain seperti levofloksasin (3,5%), ciprofloksasin (1,75%)
dan gentamisin (1,75%). Proses pencampuran dilakukan diatas troli pada ruang perawatan tanpa mempertimbangkan teknik aseptis. Jenis dan volume pelarut yang digunakan dapat dilihat pada Tabel I.
Hasil observasi yang dilakukan di Ruang ICU RSSN Bukittinggi dari bulan Juli – September 2012, jumlah pasien yang menerima sediaan parenteral berupa injeksi kering seftriakson dan sefitaksim yang direkonstitusi adalah 21 orang. Sediaan direkonstitusi di ruangan perawat tanpa memperhatikan teknik aseptis; jenis dan volume pelarut seperti pada Tabel I.
Dari pengamatan pencampuran larutan injeksi fenitoin natrium di Bangsal Syaraf Rumah Sakit DR. M. Djamil Padang terdapat ketidak tepatan jenis cairan intravena pada beberapa kasus yaitu penggunaan Ringer Laktat meskipun sebagian besar telah menggunakan NaCl 0,9% sesuai persyaratan literature (Tabel I).
Untuk mengkonfirmasi apakah prosedur pelarutan di rumah sakit telah menghasilkan sediaan obat yang stabil dengan dosis yang sesuai, maka perlu dilakukan analisis kuantitatif zat aktif terlarut. Hasil validasi metoda analisis secara spektrofotometri UV-Visibel dapat dilihat pada Tabel II.
176
Tabel I. Data ketepatan volume pelarut untuk rekonstitusi meropenem sefotaksim dan seftriakson di 3 rumah sakit yang diamati
Sediaan (dosis)
Jenis & volume pelarut
yang ditambahkan Tempat pencampuran Teknik aseptis Rumah Sakit Seharusnya (Trissel, 2009)) Injeksi kering meropenem (1 gram)a Aqua pi;10 mL Aqua pi; 20 mL Ruang perawatan pasien - Injeksi kering meropenem (0,5 gram)a Aqua pi; 5 mL Aqua pi;10 mL Ruang perawatan pasien - Injeksi kering seftriakson (1 gram)b Aqua pi; 10 mL Aqua pi; 10 mL Ruang perawatan pasien - Injeksi kering sefotaksim (1 gram)b Aqua pi; 5 mL Aqua pi; 5 mL Ruang perawatan pasien - Injeksi kering seftriakson (1 gram)c Aqua pi; 5 mL Aqua pi; 10 mL Ruang perawat - Injeksi kering sefotaksim (1 gram)c Aqua pi; 5 mL Aqua pi; 5 mL Ruang perawat - Larutan injeksi fenitoin
natrium (100mg/2mL)d Ringer Laktat NaCl 0,9%, kadar <5mg/mL Ruang perawatan pasien -
a : Bangsal Penyakit Dalam Rumah Sakit DR. M Djamil Padang
b : Bangsal Penyakit Dalam RSUD Dr M Zein Painan c : Ruang ICU RSSN Bukittinggi
d : Bangsal Syaraf Rumah Sakit DR. M Djamil Padang
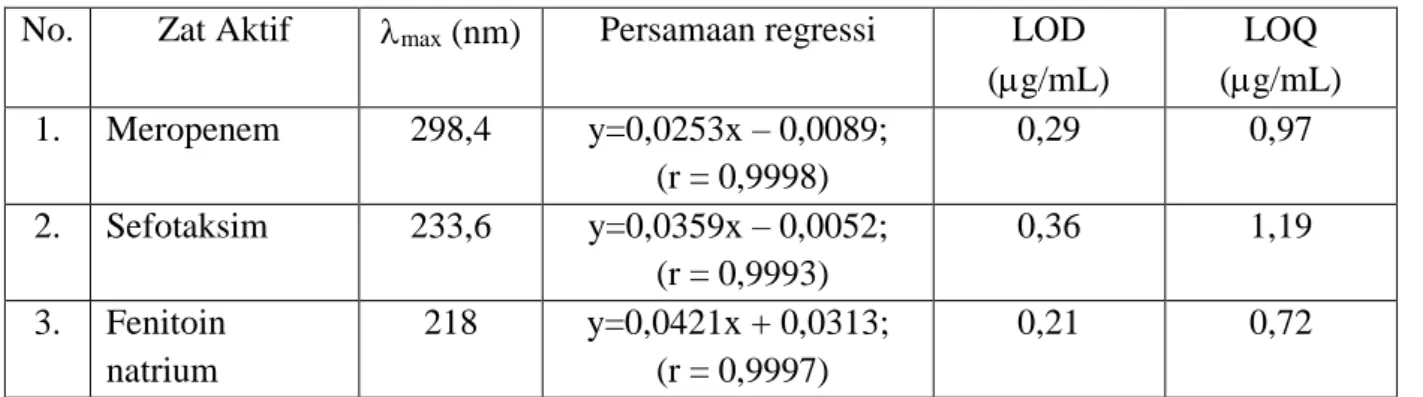
Tabel II. Hasil Validasi Metoda Analisis
No. Zat Aktif max (nm) Persamaan regressi LOD
(g/mL) LOQ (g/mL) 1. Meropenem 298,4 y=0,0253x – 0,0089; (r = 0,9998) 0,29 0,97 2. Sefotaksim 233,6 y=0,0359x – 0,0052; (r = 0,9993) 0,36 1,19 3. Fenitoin natrium 218 y=0,0421x + 0,0313; (r = 0,9997) 0,21 0,72
Hasil penetapan kadar meropenem, sefotaksim dan fenitoin natrium bila dilarutkan sesuai literature dan bila
dilarutkan menurut prosedur di rumah sakit dapat dilihat pada Tabel III.
177
Tabel III. Kadar zat aktif di dalam sediaan parenteral setelah direkonstitusi atau dicampur No. Nama zat aktif Kadar zat aktif setelah rekonstitusi/pencampuran
(%)
Keterangan Prosedur sesuai
literature
Prosedur di rumah sakit
1. Meropenem 100,55% (t=0) 98,95% (t=24 jam) 91,05% (t=48 jam) 78,56% (t=0) 78,50% (t=24 jam) 73,32% (t=48 jam) 2. Sefotaksim 102,07% (t=0) 96,31% (t=24 jam) 93,43% (t=48 jam) 88,35% (t=0) Terjadi perubahan warna setelah disimpan 3. Fenitoin natrium 91,76% (t=0) 80,72% (t=24 jam) 76,00% (t=48 jam) 89,44% (t=0) 82,96% (t=24 jam) 76,72% (t=48 jam) Terjadi pengendapan
Reaksi inkompatibilitas yang terjadi diantaranya adalah perubahan warna larutan sefotaksim setelah direkonstitusi dan
terjadinya pengendapan fenitoin setelah dicampur baik dengan NaCl 0,9% maupun dengan Ringer laktat (Gambar 1) .
Gambar 1. Pengendapan fenitoin setelah pencampuran dengan NaCl 0,9% (kiri) dan Ringer laktat (kanan)
Diskusi
Hasil pengamatan pada semua rumah sakit menunjukkan bahwa proses rekonstitusi dan pencampuran sediaan parenteral belum memperhatikan teknik aseptis untuk mencegah kontaminasi mikroba selama proses pelarutan/pencampuran berlangsung. Terdapat 4 faktor yang menentukan apakah sterilitas sediaan parenteral dapat dijaga selama proses pencampuran yaitu ruangan yang memiliki tingkat kontaminasi mikroba minimal, bahan dan alat steril, perawat terlatih dan penerapan teknik aseptis. Oleh sebab itu melarutkan sediaan injeksi di atas troli pada ruang perawatan bukan merupakan pilihan yang tepat, karena di ruangan tersebut
lalu lintas manusia tidak terkontrol. Idealnya, proses rekonstitusi dan pencampuran sediaan injeksi antibiotika dilakukan di dalam ruangan bersih dengan kontaminasi mikroba minimal, sebaiknya di dalam ruang khusus yang memiliki penyaring udara. Dalam kondisi ruangan yang terbatas di rumah sakit, bila pencampuran dilakukan di ruang perawatan, sebaiknya perawat menggunakan sarung tangan steril dan kapas yang dibasahi etanol 70% untuk mengurangi kontaminasi mikroba pada sediaan injeksi. Jarum dan karet penutup vial diaseptiskan dengan kapas yang dibasahi etanol 70% sebelum karet vial ditusuk, karena kontaminan dari udara tempat merekonstitusi sediaan dapat
178 menempel pada penutup vial dan jarum suntik (IV Reconstitution Video, 2010).
Jika dilihat dari cara merekonstitusi sediaan ada beberapa perawat yang mengocok vial dengan posisi jarum tetap berada di dalam vial dan ada sebagian dengan jarum dikeluarkan dari dalam vial. Dan pada saat mengocok vial/botol ada yang mengocok dengan kencang dan tidak pada posisi 90o sehingga ditemukan serbuk pada tutup vial, dan pada beberapa kasus ditemukan serbuk yang tidak larut pada bagian bawah vial. Tetapi sebagian besar kasus serbuk terlarut dengan sempurna. Seharusnya pada saat pengocokan vial, jarum dibiarkan di dalam vial, hal ini bertujuan untuk mencegah menempelnya kontaminan pada jarum suntik. Pengocokan sebaiknya dilakukan pada posisi 900 karena pada posisi ini kontak antara zat dengan pelarut lebih besar dan zat dapat terlarut dengan baik. Pengocokan tidak boleh dilakukan terlalu kencang, karena dapat menyebabkan serbuk tertinggal dibagian bawah tutup vial.
Proses rekonstitusi meropenem dengan aqua pro injection dengan volume
separuh dari yang seharusnya
memperlihatkan konsentrasi meropenem yang berbeda serta akan mempengaruhi kesempurnaan kelarutannya di dalam sediaan akhir. Meropenem agak sukar larut dalam air dengan kelarutan 1:30-100 sehingga meropenem belum dapat larut dengan sempurna apabila 1 g dilarutkan dalam 10 mL air steril, begitu juga dengan 500 mg yang dilarutkan dengan 5 mL air steril seperti yang dilakukan di rumah sakit. Kelarutan yang tidak sempurna akan mempengaruhi kadar obat di dalam darah sehingga akan mempengaruhi keefektifan obat dalam menyembuhkan infeksi yang diderita oleh pasien. Pada studi lain dinyatakan bahwa, konsentrasi yang optimal meropenem adalah 50 mg/mL sehingga meropenem dapat disimpan selama 8 jam pada suhu 25°C dan 48 jam pada suhu 4°C (Sweetman, 2009; Astrazeneca, 2007). Jadi, volume pelarut yang digunakan di rumah sakit tidak sesuai dengan volume minimal yang disarankan oleh literatur untuk menjamin obat dapat
terlarut dengan sempurna sebelum diinjeksikan kepada pasien.
Sediaan injeksi seftriakson di RSUD Dr. M. Zein Painan disiapkan dengan cara melarutkan 1 g serbuk kering dalam vial dengan 10 ml aqua pro injeksi (sesuai dengan literatur dan instruksi pabrik). Untuk pemberian 2 g tetap di larutkan masing-masing 1 gram dan untuk pemberian 500 mg tetap dilarutkan 1 gram dalam vial 10 ml kemudian diambil 5 ml, dan sisanya hanya dibuang saja. Untuk kasus seperti ini, sebaiknya jika pasien yang mendapat dosis 500 mg lebih dari satu orang maka penyiapannya dapat dilakukan secara bergantian. Maksud secara bergantian adalah 10 ml diambil 5 ml untuk pasien A dan 5 ml lagi untuk pasien B, begitu seterusnya untuk pasien dengan regimen yang sama.
Cara rekonstitusi di atas sudah benar, seftriakson 250 mg, 500 mg, 1 g, atau 2 g masing-masing dapat direkonstitusi dengan 2,4; 4,8; 9,6; atau 19,2 ml larutan IV kompatibel untuk mendapatkan larutan dengan konsentrasi sekitar 100 mg/ml (AHFS, 2011; Trissel, 2009). Seftriakson yang direkonstitusi dengan aqua pro injeksi yang menghasilkan konsentrasi 100 mg/ml hanya boleh disimpan maksimum 6 jam pada suhu < 250 C atau 24 jam dalam lemari es (instruksi pabrik). Seftriakson yang direkonstitusi dengan dekstrosa 5%, SWFI, atau NaCl 0,9% dengan konsentrasi 100 mg/ml stabil selama 2 hari bila disimpan pada suhu kamar (250 C) (Association Pharmacist American, 2010).
Sediaan injeksi sefotaksim disiapkan dengan melarutkan 1 g serbuk kering sefotaksim dalam vial dengan 5 ml aqua pro injeksi (sesuai dengan literatur dan instruksi pabrik), dan untuk pemberian 2 g tetap dilarutkan 1 gram dalam 5 ml aqua pro injection sebanyak dua kali. Sefotaksim 500 mg, 1 g, 2 g masing-masing dapat direkonstitusi dengan 10 ml aqua pro injeksi untuk mendapatkan larutan dengan konsentrasi sekitar 50, 95, dan 180 mg/ml (AHFS, 2011; Trissel, 2009).
Pemberian injeksi antibiotika hasil rekonstitusi sudah tepat pasien karena pada
179 saat penyiapan semua sediaan dilabel terlebih dahulu dengan menuliskan nama pasien, nama obat dan ruangan tempat pasien dirawat. Sediaan disiapkan kurang lebih satu jam sebelum jam pemberian, setelah sediaan direkonstitusi langsung diberikan kepada pasien, dan waktu pemberian nya sudah sama setiap hari nya yaitu setiap jam 12 siang untuk pemberian satu kali sehari, setiap jam 12 siang dan 12 malam untuk pemberian dua kali sehari.
Pencampuran larutan injeksi fenitoin (ampul) dengan NaCl 0,9% ataupun Ringer Laktat menghasilkan larutan yang tidak stabil dan tidak kompatibel sehingga menimbulkan endapan berupa kristal fenitoin. Dari pengamatan di rumah sakit tidak dapat diketahui dengan pasti apakah terjadi endapan kristal fenitoin saat pencampuran larutan fenitoin, baik dengan NaCl 0,9% ataupun dengan Ringer Laktat. Namun diketahui dari pengalaman dan pengamatan sebelumnya bahwa setiap sediaan fenitoin yang diproduksi dari pabrik yang berbeda dan NaCl 0,9% atau Ringer Laktat yang diproduksi dari pabrik yang berbeda akan menghasilkan stabilitas dan kompatibilitas larutan yang berbeda pula. Sediaan fenitoin yang dipakai di RSUP. DR. M. Djamil Padang sendiri merupakan produksi MersiFarma dan Ikapharmindo sedangkan NaCl 0,9% dan Ringer Laktat diproduksi Widatra dan Bibrown.
Tobias dan Kellick mengamati secara mikroskopis larutan 10 mg natrium fenitoin dalam 1–50 mL NaCl 0,9% dan mereka menemukan bentuk kristal fenitoin dalam semua konsentrasi larutan yang mereka buat. Namun mereka tidak menemukan kristal saat pemberian infus intravena. Frank mengulang kembali penelitian yang mereka lakukan dan memperoleh hasil yang sama. Lain halnya dengan hasil penelitian yang diperoleh oleh Chan, yang mencatat bahwa campuran dari 100 mg fenitoin dalam 25 – 50 mL NaCl 0,9% menghasilkan bentuk mikrokristal dengan segera, terjadi dalam rentang waktu 10–15 menit (Lawrence, 2007).
Baumann et al. meneliti pencampuran natrium fenitoin dengan konsentrasi 1 g/L dalam dekstrosa 5%; NaCl 0,9%; campuran dekstrosa 5% dan NaCl 0,9%; dan dalam Ringer Laktat. Pada waktu yang berbeda sampel disaring dengan saringan 0,22 µm. Pada filtrat yang dihasilkan oleh larutan NaCl 0,9% dan Ringer Laktat tidak terjadi pengkristalan dalam waktu 4 jam dan terjadi pengkristalan 0,8% dalam waktu 8 jam. Bentuk kristal tidak terlihat hingga 6–9 jam setelah pencampuran. Sebaliknya, pada larutan dekstrosa 5% dan campuran dekstrosa 5% dan NaCl 0,9%, terlihat pengkristalan 1– 8 jam. Bentuk kristal terlihat dalam hitungan menit (Lawrence, 2007).
Data analisis kadar zat terlarut dalam sediaan antibiotika hasil rekonstitusi menunjukkan hasil yang memenuhi syarat bila jenis dan volume pelarut sesuai yang tertera di etiket atau literature. Namun bila dilarutkan dengan volume pelarut separuhnya menghasilkan kadar obat yang tidak memenuhi syarat (< 90%), sehingga tidak sesuai dengan dosis yang seharusnya diinjeksikan kepada pasien. Fenomena ini dapat menyebabkan tidak efektifnya terapi atau memperpanjang lama rawatan pasien.
Analisa kompatibilitas menunjukkan terjadi pengendapan fenitoin setelah pencampuran dengan NaCl 0,9% atau Ringer Laktat. Pelarut yang disarankan untuk pencampuran injeksi fenitoin natrium adalah NaCl 0,9% (Trissel, 2009). Pengendapan terjadi diduga disebabkan berkurangnya kelarutan fenitoin natrium di dalam pelarut campur. Pengalaman farmasis di rumah sakit menunjukkan bahwa pencampuran dengan larutan NaCl 0,9% dengan merk tertentu dapat menghasilkan injeksi fenitoin natrium tanpa pengendapan. Disamping itu, inkompatibilitas lainnya adalah berkurangnya kadar obat terlarut selama penyimpanan pada suhu kamar. Oleh sebab itu sangat disarankan larutan injeksi antibiotika segera diberikan kepada pasien setelah direkonstitusi. Bila harus disimpan, disarankan di dalam lemari pendingin.
180
KESIMPULAN
Dapat disimpulkan bahwa prosedur rekonstitusi dan pencampuran sediaan parenteral di rumah sakit belum memenuhi kriteria Good Preparation Practice (GPP)
dan perlu diawasi oleh farmasis. Perawat perlu dibekali dengan pelatihan dan prosedur operasi standar rekonstitusi dan pencampuran sediaan parenteral.
UCAPAN TERIMA KASIH
Ucapan terima kasih disampaikan kepada pimpinan dan perawat terkait di RSUP DR. M. Djamil Padang, Rumah Sakit Stroke Nasional (RSSN) Bukittinggi dan
RSUD Dr. M Zein Painan yang telah
memberikan izin dan membantu
terlaksananya penelitian ini.
DAFTAR PUSTAKA
Association Pharmacist American. 2009-2010. Drug Information Handbook 18th
edition. USA: Lexi-Comp.
Astrazeneca. 2007. Product monograph of
Merrem. Ontario: Astrazeneca Canada
Inc.
American Society of Health-System Pharmacists Customer Service Department. 2011. AHFS Drug
Information Essentials. American
Society of Health-System Pharmacists Customer Service Department, inc. 7272 Wisconsin Avenue Bethesda. Kastango, E.S., Bradshaw, B.D. 2004. USP
chapter 79: Establishing a practice standard for compounding sterile preparations in pharmacy. Am J
Health-Syst Pharm, 6, 1928-1938.
KEMENKES RI. 2011. Pedoman Pelayanan
Kefarmasian Untuk Terapi
Antibiotik.Jakarta: KEMENKES RI.
Kumar, C.H.A., Kumar, T.A., Gurupadayya, B.M., Sloka, S.N., M.B Rahul Reddy. 2010. Novel spectrophotometric determination of Valacyclovir and Cefotaxime using 1, 2 napthaquinone-4-sulfonic acid sodium in bulk and
pharmaceutical dosage form. Scholars
Research Library, 4, 278-287.
Lawrence. 2007. United states pharmacopoeia thirtieth edition. USA: The United States Pharmacopeial Convention
Patel, N. 2012. Method development and validation for the simultaneous estimation of meropenem and sulbactam sodium. Current Pharma
Research, 2, 480-486.
Sweetman, C Sean. 2009. Martindale The
Complete Drug Reference 36th Edition.
London: Chicago Pharmaceutical Press.
Trissel, Lawrence A. 2009. Handbook on
Injectable Drugs ed 15th. American
Society of Health System Pharmacists. Sweetman, S.C. 2009. Martindale. (36th
edition). London: Pharmaceutical Press.
Walash, M.I., Rizk, M.S, Sheribah, Z.A, Salim, M.M. 2011. Derivative spectrophotometric analysis of benzophenone (as an impurity) in phenytoin. Chemical Central journal, 5, 85.