Lampiran 1. Prosedur analisis sifat fisik (Muchtadi & Sugiono 1989) 1. Densitas Kamba
Masukkan bahan ke dalam gelas ukur sampai volumenya mencapai 100 ml. Usahakan pengisian sampai benar-benar padat. Keluarkan semua bahan dari gelas ukur dan timbang beratnya. Nyatakan densitas kamba bahan dalam gr/ml. Densitas kamba = Berat Contoh
Volume contoh 2. Derajat Putih
Alat Whiteness meter ditera. contoh dimasukkan ke dalam plat-plat tersedia. sampai padat dan rata. pembacaan derajat putih contoh dapat langsung dilakukan sesuai jarum penunjuk alat.
3. Analisis pH Tepung
Alat pH meter dikalibrasi dahulu dengan menggunakan larutan standar ber pH netral (pH 7). Elektoda kemudian dimasukkan ke dalam sampel tepung yang akan diukur pH nya sehingga dapat terbaca nilai pH tepung.
Lampiran 2. Prosedur analisis sifat fungsional (Fardiaz et al 1992)
1. Daya Serap Air (Sathe dan Salunka. 1981 dalam Fardiaz et al 1992)
Sebanyak 1 gram contoh ditimbang. kemudian dimasukkan ke dalam tabung reaksi (tabung sentrifuse). Selanjutnya ditambahkan 10 gr air dan dikocok dengan vortex mixer. Kemudian disentrifuse dengan kecepatan 3500 rpm selama 30 menit. Selanjutnya diukur volume supernatant dengan menggunakan gelas ukur 10 ml.
Daya serap air = Volume air awal - Volume supernatant Berat kering contoh
2. Daya Serap Minyak
Contoh ditimbang sebanyak 1 gram. kemudian dicampur dan dikocok dengan 10 gr minyak menggunakan pengaduk magnetic. Kemudian disentrifuse dengan kecepatan 3500 rpm selama 30 menit. Selanjutnya diukur volume supernatant.
Daya serap minyak = Volume minyak awal – Volume supernatant
Lampiran 3. Prosedur analisis kimia
1. Penetapan kadar air dengan metode Oven (Apriyantono et al 1989)
Cawan kosong dan tutupnya dikeringkan dalam oven selama 15 menit dan didinginkan dalam desikator. kemudian ditimbang (untuk cawan alumunium didinginkan selama 10 menit dan cawan porselen didinginkan selama 20 menit). Kemudian timbang dengan cepat kurang lebih 5 gram sampel yang sudah dihomogenkan dalam cawan. Angkat tutup cawan dan tempatkan cawan beserta isi dan tutupnya di dalam oven selama 6 jam. Hindari kontak antara cawan dengan dinding oven. Untuk produk yang tidak mengalami dekomposisi dengan pengeringan yang lama. dapat dikeringkan selama 1 malam (16 jam).
Selanjutnya pindahkan cawan ke desikator. tutup dengan penutup cawan. lalu didinginkan. Setelah dingin timbang kembali. Keringkan kembali ke dalam oven sampai di peroleh berat yang tetap.
Berat sampel (gram) = W1
Berat sampel setelah dikeringkan (gram) = W2 Kehilangan berat (gram) =W3
Persen kadar air (dry basis) = W3 X 100 W2
Persen kadar air (wet basis) = W3 X 100 W1
Total Padatan (%) = W2 X 100 W1
2. Penetapan total abu (Apriyantono et al 1989)
Siapkan cawan pengabuan. kemudian bakar dalam tanur. didinginkan dalam desikator. dan ditimbang. Timbang sebanyak 3–5 gram sampel dalam cawan tersebut. kemudian letakkan dalam tanur pengabuan. bakar sampai didapat abu berwarna abu-abu atau sampai beratnya tetap. Pengabuan dilakukan dalam dua tahap : pertama pada suhu sekitar 400oC dan kedua pada suhu 550oC. Didinginkan kemudian ditimbang.
% Abu = Berat abu (g) X 100 Berat sampel (g)
3. Penetapan kadar protein dengan metode Mikro Kjeldahl (Apriyantono et al 1989)
Timbang sampel kira-kira akan membutuhkan 3-10 ml HCl 0.01 N atau 0.02 N ). pindahkan ke dalam labu kjeldahl 30 ml. Tambahkan 1.9 ± 0.1 g K2SO4. 40 ± 10 mg HgO. dan 2.0 ± 0.1 ml H2SO4 untuk setiap 10 mg bahan organik diatas 15 mg. Kemudian tambahkan beberapa butir batu didih. Didihkan sampel selama 1-1.5 jam sampai cairan jernih. Dinginkan. tambahkan sejumlah kecil air secara perlahan-lahan (hati-hati tabung menjadi panas). kemudian dinginkan. Pindahkan isi labu ke dalam alat destilasi. Cuci dan bilas labu 5-6 kali dengan 1-2 ml air. pindahkan air cucian ini ke dalam alat destilasi.
Letakkan erlenmeyer 125 ml yang berisi 5 ml larutan H2BO3 dan 2-4 tetes indikator (campuran 2 bagian metil merah 0.2% dalam alkohol dan 1 bagian metilen blue 0.2% dalam alkohol) dibawah kondensor. Ujung tabung kondensor harus terendam di bawah larutan H3BO3. Lalu. tambahkan 8-10 ml larutan NaOH-Na2S2O3. kemudian lakukan destilasi sampai tertampung kira-kira 15 ml destilat dalam erlenmeyer. Bilas tabung kondenser dengan air. dan tampung bilasannya dalam erlenmeyer yang sama. Encerkan isi erlenmeyer sampai kira-kira 50 ml kemudian titrasi dengan HCl 0.02 N sampai terjadi perubahan warna menjadi abu-abu. Lakukan juga penetapan blanko.
% N = (ml HCl-ml blanko) X normalitas X 14.007 X 100 mg sampel
% Protein = % N X faktor konversi atau
Protein (%) = (Vol titrasi x 0.014 x N HCl x 6.25 x 100)/Berat sampel
3. Penetapan kadar lemak dengan metode Ekstraksi Soxhlet (Apriyantono et al 1989)
Ambil labu lemak yang ukurannya sesuai dengan alat ekstrasi Soxhlet yang akan digunakan. dikeringkan dalam oven. didinginkan dalam desikator dan ditimbang. Kemudian timbang 5 gram sampel dalam bentuk tepung langsung dalam saringan tibel. yang sesuai ukurannya. kemudian tutup dengan kapas-wool yang bebas lemak. Sebagai alternatif sampel dapat dibungkus dengan kertas
saring. Letakkan timbel atau kertas saring yang berisi sampel tersebut dalam alat ekstrasi Soxhlet. kemudian pasang alat kondenser diatasnya dan labu lemak di bawahnya.
Tuangkan pelarut dietil eter atau petroleum eter ke dalam labu lemak secukupnya. sesuai dengan ukuran soxhlet yang digunakan. Lakukan refluks selam minimum 5 jam sampai pelarut yang turun kembali ke labu lemak berwarna jernih. Distilasi pelarut yang ada di dalam labu lemak. tampung pelarutnya. Selanjutnya labu lemak yang berisi lemak hasil ekstraksi dipananskan dalam oven pada suhu 105oC. Setelah dikeringkan sampai berat tetap dan didinginkan dalam desikator. timbang labu beserta lemaknya tersebut. Kemudian berat lemak dapat dihitung.
% Lemak = Berat lemak (g) X 100 Berat sampel
4. Penetapan kadar karbohidrat dengan metode Karbohidrat by difference (Winarno 1995)
% Karbohidrat = 100% - % (protein + lemak + abu + air)
5. Penetapan serat pangan dengan metode Enzimatis ( Asp et al 1983)
Sebanyak 1 gram sampel dimasukkan ke dalam erlenmeyer. ditambahkan 25 ml larutan buffer Na-fosfat 0.1 M pH 6 dan dibuat menjadi suspensi kemudian diaduk. Selanjutnya ditambahkan 0.1 ml enzim termamyl. erlenmeyer kemudian ditutup dengan alumunium foil. dan diinkubasi dalam penangas air bersuhu 100oC selama 15 menit sambil sesekali diaduk.
Sampel diangkat dan didinginkan ditambahkan 20 ml air destilata. pH diatur 1.5 dengan menggunakan HCl. Selanjutnya ditambahkan 100 mg enzim pepsin. erlenmeyer ditutup dan diingkubasikan dalam penangas air bergoyang bersuhu 40oC selama 60 menit. Kemudian ditambahakan 20 ml air destilata. pH diatur menjadi 6.8 dengan NaOh lalu tambahkan 20 ml air destilata. pH diatur menjadi 6.8 dengan NaOH lalu tambahkan 100 mg pankreatin. tutup Erlenmeyer dan diingkubasikan dalam penangas air bergoyang pada suhu 40oC selama 60 menit. Kemudian pH diatur menjadi 4.5 menggunakan HCl. Larutan sampel disaraing
melalui crucible kering yang telah ditimbang beratnya (porositas 1) dan ditambahkan 0.5 gram celite kering (berat tepat diketahui). Pada penyaringan dilakukan pencucian dengan 2x10 ml air destilata.
1) Residu (serat tidak larut)
Cuci dengan 2x10 ml etanol 95% dan 2x10 ml aseton. Kemudian dikeringkan pada suhu 105oC sampai mencapai berat konstan (semalam). Setelah didinginkan dalam desikator kemudian ditimbang (D1). Diabukan pada suhu 550oC selama 5 jam. Setelah didinginkan dalam desikator. ditimabang (I1). 2) Filtrar (serat larut)
Volume filtrate diatur menjadi 100 ml. Kemudian ditambahkan 400 ml etanol 95% hangat (60oC). Biarkan mengendap selama 1 jam. Disaring dengan crucible kerin yang telah ditimbang beratnya (porositas 2) dan ditambahkan 0.5 gram celite kering (berat tepat diketahui). Dicuci dengan 2x10 ml etanol 78%. 2x10 ml etanol 95%. dan 2x10 ml aseton. Dikeringkan pada suhu 105oC sampai mencapai berat konstan (semalam). Setelah didinginkan dalam desikator kemudian ditimbang (D2). Diabukan pada suhu 550oC selama 5 jam. Setelah didinginkan dalam desikator. ditimbang (I2)
3) Blanko
Blanko diperoleh dengan cara seperti prosedur untuk sampel tetapi tanpa sampel (B1 dan B2). Perhitungan :
% Serat tidak larut (IDF) = (D1-I1-B1) x 100%
Berat sampel
% Serat larut (SDF) = (D2-I2-B2) x 100%
Berat sampel
% Serat pangan (TDF) = %IDF + % SDF
Keterangan :
D = berat setelah pengeringan I = berat setelah pengabuan B = berat blanko bebas abu
7. Bioavailability zat besi dengan metode in vitro (Roig et al 1999) a. Bahan dan alat
Semua peralatan gelas dicuci. direndam dalam larutan HNO3 10% (v/v) selama 24 jam dan dibilas dengan air bebas ion sebelum digunakan. Bahan dan alat yang digunakan meliputi :
1. HCl 37%
2. Suspensi Pepsin :
1.6 pepsin didispersikan ke dalam 0.1 M HCl dan ditepatkan volumenya menjadi 10 ml. suspense ini dibuat sewaktu akan digunakan.
3. Campurkan pankreatin : Sebanyak 1 g pankreatin dan 6.25 g ekstrak bile didispersikan dalam 0.1 M NaHCO dan tepatkan volumenya menjadi 250 ml. Campuran ini dibuat sewaktu akan digunakan.
4. Kantung Dialisis :
Kantung dialisis dipotong dengan panjang 20 cm dan kemudian direndam dalam air bebas ion sampai akan digunakan.
5. Botol-botol gelas :
Botol-botol gelas dengan ukuran yang sesuai dan mencukupi. digunakan untuk tempat sampel dan kantung dialisis.
b. Persiapan sampel (Gambar )
Formula snack bar diblender kering sampai menyerupai bubuk
Ditimbang setara 2 gram protein
Analisis ketersediaan zat besi
Gambar. Tahap-tahap persiapan sampel c. Prinsip analisis
Zat besi (Fe) pada sampel dihidrolisis dari ikatannya dengan protein menggunakan enzim-enzim penernaan yang terdapat di lambung dan usus halus. Fe bebas yang terdapat dalam larutan sampel akan berdifusi melalui membran semipermeabel ke dalam kantung dialysis yang berisi buffer NaHCO3. Fe dalam dialisat menunjukkan jumlah Fe yang diserap tubuh. dalam alat pencuci gelas. dibilas dengan air destilata dan direndam dalam HCL 1 N selama 4 jam.
b. Persiapan sampel
Timbang sampel sedemikian rupa sehingga kandungan proteinnya sekitar 2 gr. Selanjutnya tambahkan air bebas ion hingga volumenya mencapi 75 ml. kemudian blender sampai halus. Siapkan sampel tersebut duplo.
Suspensi pepsin. Masukkan 1 gr pepsin ( sigma P7000) ke dalam labu takar 25 ml. Kemudian tepatkan volumenya dengan HCL 0.1 N. Digunakan dalam bentuk segar atau siapkan segera sebelum digunakan.
Pankreatin bile. Campurkan 2 gr pankreatin (Sigma P1750) dan 12.5 gr ekstrak bile (Sigma B8631). kemudian larutkan dalam NaHCO3 0.1 M dan buat volumenya menjadi 1 liter dengan NaHCO3 0.1 M.
Larutan protein presipitan. Larutkan 100 gr asam triklor asetat (TCA. Sigma T4885) dan 50 gram hidroksil amonium klorida (Sigma H9876) dalam air. Kemudian tambahkan 100 ml HCL pekat dan tepatkan volume larutan menjadi 1 liter menggunakan air bebas ion.
Larutan standar Fe. Buat larutan dengan konsentrasi 0. 0.25. 0.5. 1.0. 2.0. dan 4.0 ug/ml Fe sebagai FeCl3 dalam HCl 0.1 N.
Katong dialisis. Potong kantong dialisis (Spectrapor 1. 6000-8000 MWCO. Fisher 3 8700) sepanjang 15 cm dan rendam dalam air bebas ion. sekurang-kurangnya 1 jam.
Vial. Siapkan vial (tabung dialisis) (Fisher 3-335-10D) lengkap dengan penutupnya. Buat lubang kecil pada tutup untuk mengeluarkan gas.
Lampiran 4. Lembar uji organoleptik snack bar sorghum
Lembar Uji Hedonik (Kesukaan)
Nama Panelis : Tanggal Pengujian:
Jenis Kelamin : L/P
Nama Produk : Snack bar Sorghum
Uji Kesukaan (Hedonic Test)
Dihadapan saudara disajikan 4 macam snack bar sorghum dengan kode tertentu. Saudara diminta untuk memberikan penilaian terhadap keempat sampel sesuai dengan tingkat kesukaan saudara. dengan ketentuan di bawah ini.
Pengisian dilakukan dengan cara membuat garis vertikal pada setiap mistar sesuai dengan ketentuan dan kode produk. Cantumkan kode sesuai dengan label pada setiap garis vertikal yang diberikan. Diharapkan Saudara berkumur terlebih dahulu dengan air mineral sebelum mencoba ke formula lainnya.
Warna : I---I---I---I---I---I---I---I---I
Amat Sangat Biasa Amat Sangat suka tidak suka
Tekstur : I---I---I---I---I---I---I---I---I
Amat Sangat Biasa Amat Sangat suka tidak suka
Aroma : I---I---I---I---I---I---I---I---I
Amat Sangat Biasa Amat Sangat suka tidak suka
Rasa : I---I---I---I---I---I---I---I---I
Amat Sangat Biasa Amat Sangat suka tidak suka
Keseluruhan : I---I---I---I---I---I---I---I---I Amat Sangat Biasa Amat Sangat suka tidak suka
Komentar:... ... ...
Lembar Uji Mutu Hedonik (Kesukaan)
Nama Panelis : Tanggal Pengujian:
Jenis Kelamin : L/P
Nama Produk : Snack bar sorghum
Uji Mutu Hedonik (Kesukaan)
Dihadapan saudara disajikan 4 macam snack bar sorghum dengan kode tertentu. Saudara diminta untuk memberikan penilaian terhadap keempat sampel dengan ketentuan di bawah ini.
Pengisian dilakukan dengan cara membuat garis vertikal pada setiap mistar sesuai dengan ketentuan dan kode produk. Cantumkan kode sesuai dengan label pada setiap garis vertikal yang diberikan. Diharapkan Saudara berkumur terlebih dahulu dengan air mineral sebelum mencoba ke formula lainnya.
Warna : I---I---I---I---I---I---I---I---I Coklat Coklat Putih Kehitaman Kekuningan Gading
Tekstur : I---I---I---I---I---I---I---I---I Sangat padat keras Padat Renyah
1 2 3 4 5 6 7 8 9 Coklat kehitam an Coklat tua Cokl at Cokl at mud a Coklat Kekunin gan Kuning kecoklat an Kuni ng ema s Kuning keputihan Putih gadi ng 1 2 3 4 5 6 7 8 9 Sangat padat sangat keras Padat sangat keras Padat keras Padat agak keras Padat Agak padat empuk Empuk Empuk renyah Renyah
Aroma : I---I---I---I---I---I---I---I---I Amat Netral Amat Sangat Sangat Apek Harum 1 2 3 4 5 6 7 8 9 Amat sangat apek Sangat apek Apek Agak apek Netral (tidak berbau) Agak harum Harum Sangat harum Amat sangat harum Rasa : I---I---I---I---I---I---I---I---I
Pahit Hambar Asam Manis
Komentar:... ... ... ... 1 2 3 4 5 6 7 8 9 Pahit Pahit asam Pahit manis Agak pahit Hambar Agak manis Manis Agak manis Asam manis
Lampiran 5. Gambar bahan dan analisis snack bar
Adonan snack bar sebelum dipanggang Pemanggangan produk snack bar
Analisis zat besi
Alat analisis serat pangan
Lampiran 6. Hasil Analisis Sifat Fisik dan Fungsional Tepung Sorghum
Sifat fisik
1. Densitas kamba
Sampel Berat Volume (ml) densitas kamba rata-rata Sorghum 1 19.3577
25 0.7743 0.79 Sorghum 2 20.1212 0.8048
Contoh perhitungan :
Densitas kamba = Berat Contoh /Volume contoh
2. Derajat putih
Sampel Derajat putih Kadar % rata-rata Sorghum 1 55.3 50.27 50.33 Sorghum 2 55.6 50.18 Sorghum 3 55.2 50.54 3. pH Sampel pH rata-rata Sorghum 1 6.100 6.142 Sorghum 2 6.152 Sorghum 3 6.174 Sifat Fungsional 1. Daya serap air
Sampel B.sampel B.Tabung B.air B.total Berat kering Daya serap air rata-rata Sorghum 1 1.0084 13.4754 10.0133 14.4838 16.006 1.5095 1.51 Sorghum 2 1.0036 9.1925 10.2480 10.1961 11.721 1.5192 Contoh perhitungan :
Daya serap air = (berat kering - berat tabung) – berat sampel Berat sampel
= (16.006-13.4754) – 1.0084 = 1.5095 1.0084
2. Daya serap minyak
Sampel B.sampel B.Tabung B.minyak B.total Berat kering Daya serap minyak rata-rata Sorghum 1 1.0081 13.3963 10.0523 24.4567 15.4725 1.06 0.98 Sorghum 2 1.0094 13.3104 10.0278 24.3476 15.2347 0.91 Contoh perhitungan :
Daya serap minyak = (berat kering - berat tabung) – berat sampel Berat sampel
Lampiran 7. Hasil Analisis Sifat Kimia Snack Bar Sorghum 1. Hasil analisis kadar air
Kode
Sampel Protein Lemak
Kadar
abu KH
kadar air dry
kadar
air wet SMTL SML SMTOT Fe F 1 9,19 3,98 1,50 89,09 19,03 15,99 11,55 1,50 13,05 4,22 9,75 4,22 1,53 88,17 18,01 15,26 11,74 1,44 13,18 3,88 9,54 4,26 1,53 88,60 19,44 16,28 11,41 1,54 12,95 3,75 9,30 3,99 1,60 88,81 18,88 15,88 11,44 1,78 13,22 3,79 F 2 7,18 3,58 1,43 91,45 18,73 15,77 8,29 2,22 10,51 4,15 7,82 3,91 1,46 90,28 18,30 15,47 8,00 2,11 10,11 3,52 6,29 3,81 1,54 91,61 17,74 15,06 8,12 2,50 10,61 3,74 6,84 3,80 1,45 91,07 17,49 14,89 8,09 2,34 10,43 3,44 F 3 13,38 11,56 1,90 76,18 17,13 14,62 10,18 3,43 13,61 4,93 12,76 11,46 2,10 76,73 17,22 14,69 10,39 3,61 13,99 5,52 13,13 11,45 2,21 76,25 17,17 14,65 10,10 3,77 13,87 4,36 12,64 11,40 2,45 76,53 17,11 14,61 9,96 3,83 13,79 4,68 F 4 14,00 14,74 2,11 70,78 12,65 11,23 9,56 4,29 13,85 4,80 14,34 14,84 1,89 70,57 12,69 11,26 9,83 3,97 13,80 3,83 14,67 14,65 1,84 70,60 13,16 11,63 9,60 4,14 13,73 3,63 13,38 14,30 2,15 71,73 12,43 11,05 10,31 3,98 14,29 4,24
2. Hasil analisis kadar bioavailabilitas zat besi
Kurva Standard Fe Konsentrasi (ppm) Puncak (mm) 0 0 0.5 3.7 1 8 2 14.5 3 21 4 28
Sampel protein kadar
(%) Berat setara 2 % protein (g) Berat sampel Bio (g) Kadar Fe sampel (ppm) Total Fe sampel (mg) Berat Dialisat (g) Peak (mm) Aliquot ml a b kadar Fe dialisat (ppm) Fe Dialisat (mg) Bioavai labilitas (%) Tp.Sorg hum 10.15 19.690 3.947 1043.84 4.120 29.94 1.8 50 6.926 0.412 0.347 0.0100 2.1508 Tp.Sorg hum 10.15 19.690 3.946 1021.63 4.031 37.61 1.9 50 0.286 0.0107 2.3568 Formula 4 12.23 16.162 3.238 320.56 1.038 33.52 2.0 50 0.342 0.0115 8.2074 Formula 4 12.52 16.162 3.232 308.72 0.998 32.53 2.0 50 0.352 0.0115 9.0141
Contoh perhitungan :
Berat setara 2 gram protein = (2 g/kadar protein sampel g) X 100g = (2 g/10.15g) X 100 g = 19.70 g
Perkiraan berat sampel bio per 20 g suspensi
= 19.70 g + 75 ml H2O bebas ion + 3.75 ml HCl = 80.45 g
(asumsi. sampel membutuhkan ± 3.75 ml HCl untuk membuat pH nya menjadi 2). suspense di tera menjadi 100 gr dg H20 bebas ion
= 20 g X 19.70 g = 3.94 g 100 g
Total Fe sampel bio = penimbangan sampel bio x kadar Fe (ppm) = 3.9467 g X 1043.84 mg = 4.1197 mg Fe
1000 g
Berdasarkan kurva standar Fe di atas. maka persamaan linear yang dapat digunakan untuk mencari Fe sampel adalah
Y = aX + b
= 6.926X + 0.412
Dimana : Y = absorbansi
X = konsentrasi Fe (ppm)
a = slope (kemiringan secara statistik) b = intercept ( titik perpotongan terhadap Y)
jika absorbansi sampel dengan berat dialisat 29.94 g dalam 50 ml aliquot adalah 1.8 faktor pengenceran 1 dan absorbansi blanko 0.00 . maka kadar Fe adalah :
Y = (abs sampel dalam aliquot x fp)- abs blanko Y = aX + b
aX + b = (abs sampel dalam aliquot x fp) – abs blanko
X (ppm) = ((abs sampel dalam aliquot x fp) – abs blanko) – b a
X (ppm) = ((1.8 x 1) – 0.00) – 0.412 = 0.200 ppm 6.926
Karena X (ppm) merupakan konsentrasi Fe sampel dalam volume aliquot. maka kadar Fe sampel (mg/100g) dengan berat 1.0085 g adalah :
Kadar Fe dialisat = x mg X ml aliquot
1000 ml
X 1000
Berat sampel = 0.200 mg x 50 ml 1000 mlX 1000
29.9355 g = 0.334 mg/1000 g = 0.334 ppmJika dalam 1000 g terdapat 0.3340 ppm. maka dalam 29.94 g dialisat terdapat mg Fe dialisat = (berat dialisat/1000) x kadar Fe dialisat (ppm)
= (29.9355 g/1000) x 0.334ppm = 0.0099 mg =0.010 Bioavailabilitas Fe (%) = Fe dialisat / total Fe sampel bio x 100%
= 0.010 mg x 100% = 2.146 % =2.15 % 0.4659 mg
Lampiran 8. Sidik Ragam (ANOVA) Sifat Kimia Snack Bar Sorghum ANOVA JK db KT F Sig. Protein Formula 126.456 3 42.152 189.042 .000 Error 2.676 12 .223 Total 129.132 15 Lemak Formula 351.957 3 117.319 4647.453 .000 Error .303 12 .025 Total 352.260 15
Kadar Abu Formula 1.394 3 .465 23.008 .000
Error .242 12 .020
Total 1.637 15
Karbohidrat Formula 1123.956 3 374.652 1727.818 .000
Error 2.602 12 .217
Total 1126.558 15
Kadar Air Wet Formula
50.257 3 16.752 166.071 .000 Error 1.211 12 .101 Total 51.468 15 SMTL Formula 23.581 3 7.860 167.251 .000 Error .564 12 .047 Total 24.145 15 SML Formula 16.627 3 5.542 210.558 .000 Error .316 12 .026 Total 16.943 15 SMTOT Formula 32.227 3 10.742 283.515 .000 Error .455 12 .038 Total 32.681 15 Fe Formula 3.086 3 1.029 6.287 .008 Error 1.964 12 .164 Total 5.050 15
Lampiran 9. Sidik Ragam (ANOVA) Organoleptik Snack Bar Sorghum ANOVA JK db KT F Sig. Warna Formula 16.795 3 5.598 3.585 .016 Error 181.117 116 1.561 Total 197.912 119 Tekstur Formula 9.972 3 3.324 1.953 .125 Error 197.388 116 1.702 Total 207.360 119 Aroma Formula 19.699 3 6.566 4.710 .004 Error 161.735 116 1.394 Total 181.435 119 Rasa Formula 13.530 3 4.510 2.601 .055 Error 201.102 116 1.734 Total 214.632 119 Keseluruhan Formula 8.720 3 2.907 3.955 .010 Error 85.258 116 .735 Total 93.978 119 Mutu warna Formula 42.136 3 14.045 6.924 .000 Error 235.314 116 2.029 Total 277.450 119 Mutu tekstur Formula 40.951 3 13.650 6.816 .000 Error 232.302 116 2.003 Total 273.253 119 Mutu aroma Formula 2.273 3 .758 .516 .672 Error 170.420 116 1.469 Total 172.693 119 Mutu rasa Formula 7.775 3 2.592 1.493 .220 Error 201.422 116 1.736 Total 209.197 119
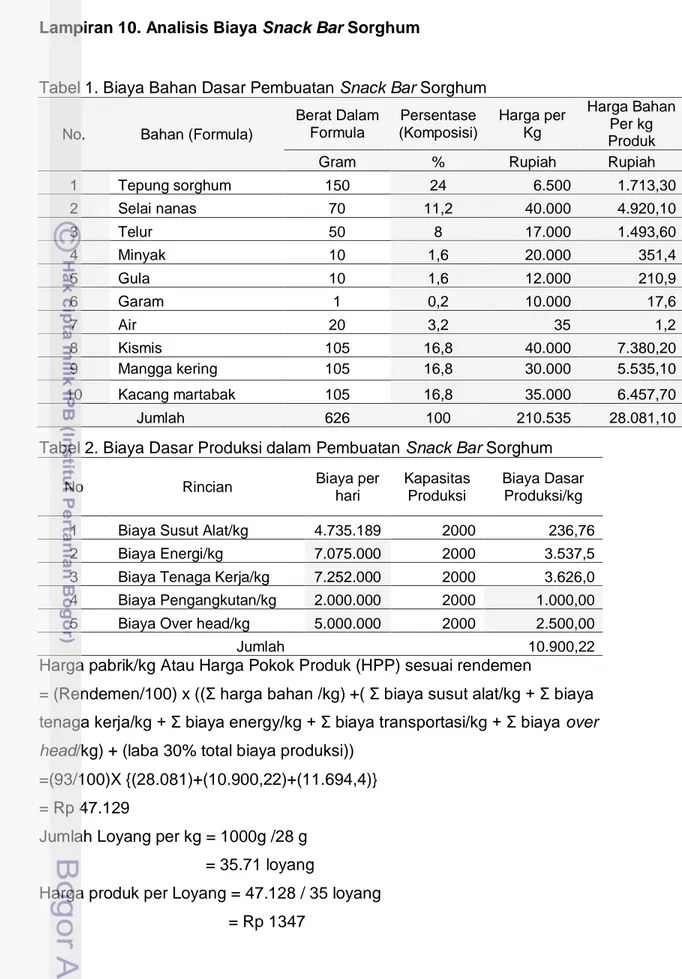
Lampiran 10. Analisis Biaya Snack Bar Sorghum
Tabel 1. Biaya Bahan Dasar Pembuatan Snack Bar Sorghum
No. Bahan (Formula)
Berat Dalam Formula Persentase (Komposisi) Harga per Kg Harga Bahan Per kg Produk Gram % Rupiah Rupiah 1 Tepung sorghum 150 24 6.500 1.713,30 2 Selai nanas 70 11,2 40.000 4.920,10 3 Telur 50 8 17.000 1.493,60 4 Minyak 10 1,6 20.000 351,4 5 Gula 10 1,6 12.000 210,9 6 Garam 1 0,2 10.000 17,6 7 Air 20 3,2 35 1,2 8 Kismis 105 16,8 40.000 7.380,20 9 Mangga kering 105 16,8 30.000 5.535,10 10 Kacang martabak 105 16,8 35.000 6.457,70 Jumlah 626 100 210.535 28.081,10
Tabel 2. Biaya Dasar Produksi dalam Pembuatan Snack Bar Sorghum
No Rincian Biaya per hari
Kapasitas Produksi
Biaya Dasar Produksi/kg 1 Biaya Susut Alat/kg 4.735.189 2000 236,76 2 Biaya Energi/kg 7.075.000 2000 3.537,5 3 Biaya Tenaga Kerja/kg 7.252.000 2000 3.626,0 4 Biaya Pengangkutan/kg 2.000.000 2000 1.000,00 5 Biaya Over head/kg 5.000.000 2000 2.500,00
Jumlah 10.900,22
Harga pabrik/kg Atau Harga Pokok Produk (HPP) sesuai rendemen
= (Rendemen/100) x ((Σ harga bahan /kg) +( Σ biaya susut alat/kg + Σ biaya tenaga kerja/kg + Σ biaya energy/kg + Σ biaya transportasi/kg + Σ biaya over head/kg) + (laba 30% total biaya produksi))
=(93/100)X {(28.081)+(10.900,22)+(11.694,4)} = Rp 47.129
Jumlah Loyang per kg = 1000g /28 g = 35.71 loyang
Harga produk per Loyang = 47.128 / 35 loyang = Rp 1347