UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL DAUN PETAI (Parkia speciosa Hassk.) TERHADAP Staphylococcus aureus ATCC 25923 DAN
Escherichia coli ATCC 25922 Sabrina Handayani Tambun
118114130
INTISARI
Penyakit infeksi dapat disebabkan oleh bakteri di antaranya Staphylococcus aureus dan Escherichia coli. Penyakit infeksi merupakan salah satu penyebab kematian terbesar di dunia sehingga diperlukan alternatif untuk mengatasi yaitu dengan memanfaatkan bahan alam. Daun petai mengandung terpenoid, fenolik, flavonoid, saponin dan alkaloid. Senyawa - senyawa tersebut diketahui memiliki aktivitas antibakteri.
Penelitian ini bertujuan untuk mengetahui aktivitas antibakteri ekstrak etanol daun petai (Parkia speciosa Hassk.) terhadap S. aureus dan E. coli. Penelitian termasuk eksperimental murni, dengan rancangan acak lengkap pola satu arah. Tahapan penelitian meliputi persiapan, ekstraksi, identifikasi kandungan senyawa, uji aktivitas antibakteri dengan metode difusi sumuran, dilanjutkan dengan metode dilusi cair untuk mengetahui Kadar Hambat Minimal (KHM) dan Kadar Bunuh Minimum (KBM). Hasil uji aktivitas antibakteri dianalisis statitistik menggunakan Shapiro Wilk untuk uji distribusi normal data, Kruskal Wallis untuk mengetahui perbedaan secara keseluruhan dan Mann – Whitney untuk mengetahui perbedaan antar konsentrasi dan kontrol negatif.
Hasil penelitian menunjukkan bahwa ekstrak etanol daun petai memiliki aktivitas antibakteri terhadap S. aureus, tetapi tidak memberikan aktivitas antibakteri terhadap E. coli. Nilai KHM ekstrak etanol daun petai terhadap S. aureus adalah pada konsentrasi 25%, sedangkan nilai KBM belum dicapai.
ABSTRACT
Infectious diseases can be caused by bacteria such as Staphylococcus aureus and Escherichia coli. Infectious diseases are one of the biggest causes of death in the world so that necessary alternative to solve it, by exploit natural materials. Petai leaves containing terpenoids, phenolic, flavonoid, saponin and alkaloid. Those compounds known have antibacterial activity.
This study was purposed to determine antibacterial activity ethanol extract of petai leaves (Parkia speciosa Hassk.) against S. aureus and E. coli. This study is purely experimental, completely randomized and one way design. Steps of this study include the preparation, extraction, identification of compounds, antibacterial activity test used difussion method, followed by liquid dilution method to determine the Minimal Inhibitory concentration (MIC) and Minimum Bactericidal Concentration (MBC). Antibacterial activity test results were analyzed using the Shapiro Wilk statitistik to normal data distribution, Kruskal Wallis test to determine significant differences in whole group and Mann - Whitney to determine the differences between concentration and negative control.
The results of this study showed that the ethanol extract of petai leaves have antibacterial activity against S. aureus, but it did not have antibacterial activity against E. coli. MIC of ethanol extract of petai leaves against S. aureus at concentration 25%, while the MBC has not obtained.
UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL DAUN PETAI (Parkia speciosa Hassk.) TERHADAP Staphylococcus aureus ATCC 25923 DAN
Escherichia coli ATCC 25922 SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Diajukan oleh :
Sabrina Handayani Tambun NIM : 118114130
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
UJI AKTIVITAS ANTIBAKTERI EKSTRAK ETANOL DAUN PETAI (Parkia speciosaHassk.) TERHADAP StaphylococcusaureusATCC 25923DAN
EscherichiacoliATCC 25922
SKRIPSI
Diajukan untuk MemenuhiSalah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Diajukan oleh : Sabrina Handayani Tambun
NIM :118114130
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
i v
Halaman Persembahan
Sebab Aku inimengetahui rancanganrancangan apa yang ada padaKu
mengenai kamu, demikianlah Firman TUHAN, yaitu rancangan damai sejahte dan buka rancangan kecelakaan, untuk memberikan kepadamu hari depan yan penuh harapan (Yeremia 29 : 11)
Kupersembahkan karyakecilku ini untuk :
Yesus Kristus, sumber hidup dan semangatku
Keluargaku tercinta 5R untuk semua cinta, doa dan semangat
Chandra Christian Sinaga
Semua orang yang membutuhkan karya ini
v i i PRAKATA
Segala puji syukur dan terimakasih penulispanjatkan ke hadirat Tuhan Yang Maha
Esa, karena cinta dan berkatNya yang tiada batas sehingga penulis dapa menyelesaikan skripsi yang berjudul UJI AKTIVITAS ANTIBAKTERI
EKSTRAK ETANOL DAUN PETAI (Parkia speciosaHassk.) TERHADAP StaphylococcusaureusATCC 25923DAN EscherichiacoliATCC 25922dengan baik.
Skripsi ini disusun untuk memenuhi salah satu syarat untuk memper Sarjana Farmasi di Fakultas Farmasi Universitas Sanata Dharma Yogyaka menyadari penulisan skripsi ini tidak lepas dari bimbingan, saran, bantuan dan dukungan berbagai pihak baik secara langsungmaupuntidaklangsung, sehingga dalam
kesempatan ini penulis ingin berterimakasih kepada :
1. Orangtuaku tercinta,Bapak Ramses Tambun danIbu Nenteria Manurung atas
segalakasih sayang tiada batas,doa tulus yang selalu menemani langkah dan menjadi sumber semangatku.
2. Ibu Aris Widyastuti,M.Si., Ph.D., Apt.selaku dekan Fakultas Farmasi UniveristasSanata Dharma.
3. Bapak Yohanes Dwiatmaka, M.Si., selaku Dosen Pembimbing Skripsidan
Dosen Penguji Skripsi yang telah meluangkan waktu untuk mendam membimbingdan memberikan masukan hingga penulisan skripsi ini sele.
4. IbuDr. Yustina Sri Hartini, M. Si., Apt.selakuDosen Penguji Skripsi yang telah meluangkan waktu,memberikan kritik danmasukan yang membangun
v i i i
5. IbuDamiana Sapta Candrasari, S. Si., M. Sc., selaku Dosen Penguji Skripsi yang telah meluangkan waktu, memberikan kritik dan masukan membangun dalam penyelesaianskripsi ini.
6. Ibu Agustina Setiawati, M.Sc., Apt selaku Kepala Penanggung Laboratorium Fakultas Farmasi yang telah memberikan izin dalam pe semua fasilitas laboratoriumselama proses penelitian.
7. Bapak Ipang Djunarko, M.Sc,Apt., selaku Dosen Pendamping Akademik yang telah membantu selama prosesstudi.
8. Ibu Maria Dwi Budi Jumpowati, S.Si, atas kesediaannya untukberdiskusi,dan masukanmengenai Mikrobiologi sertamotivasi yang diberikan.
9. BapakWagiran, Bapak Mukminin,Bapak Kunto, Bapak Parlan dan MasSigit
serta seluruh Laboran Fakulatas Farmasi Universitas Sanata Dha bantuan selama penelitian.
10.Ibu Evi, Mas Andi, Bapak Havid serta seluruh karyawan Balai Ke Yogyakartayang telah membantu selama penelitian Mikrobiologi.
11.Teman seperjuanganku Petai geng,Metta,Sari, Aloyatas kerjasama, kebersamaan,pengetahuan,ide, kesabaran, danmotivasiselama penelitian.
12.Abang dan adikku tersayang Rocky Jaya Tambun dan Rani Leonita T yang telah memberikan kasih sayang, semangat dan keceriaan
13.Chandra Christian Sinaga atas segala doa, kasih sayang,tawa dandukungan semangat yang tiada hentibagi penulis.
i x
15.Sahabat sahabatku terkasih Ellen, JeindanKaidahuntuk segala nasehat, keceriaandan semangat yang tiada henti dari jauh.
16.KosmatesSariayuersJohannadanVirlis untukkeceriaan dan kebersamaannya.
17.Ibu, babeh, Sevtin dan Sekolah Pingit, atas semuaperhatian danpelajaran hidup yang berhargaselama penulis menjadivolunteerpengajarSekolah Pingit.
18.Teman temanFSM C, FKKB,angkatan 2011 Fakultas Farmasi Sanata Dharma,atas kebersamaanya selama proses perkuliahan.
19.Semua pihak yang tidak dapat penulis sebutkansatu persatu yang juga berperan dalam penulisan skripsi ini.
Penulis menyadari masih banyak kekurangan dalam penulisan skri Oleh karena itu penulis mengharapkan kritik dan saran yang memban berbagai pihak. Semoga naskah skripsi ini dapat bermanfaat.
Yogyakarta,30 April2015
x DAFTAR ISI
HALAMAN JUDUL ...i
HALAMAN PERSETUJUAN PEMBIMBING ...ii
HALAMAN PENGESAHAN ...iii
HALAMAN PERSEMBAHAN ...iv
PERNYATAAN KEASLIAN KARYA ...v
PERNYATAAN PERSETUJUAN PUBLIKASI ...vi
PRAKATA ...vii
2.Keaslian penilitian...4
3.Manfaat penelitian...5
B. TUJUANPENELITIAN...6
BAB II. PENELAAHAN PUSTAKA... 7
A.Tanaman Petai...7
x i
C.Bakteri uji... 11
D.Ekstraksi...17
E.Uji Aktivitas Antibakteri...20
F.Landasan Teori...21
G .Hipotesis...23
BAB III. METODOLOGI PENELITIAN...24
A.Jenis dan Rancangan Penelitian...24
B.Variabel dan Definisi Operasional...24
C.AlatPenelitian...25
D.BahanPenelitian...26
E.Tata Cara Penelitian...26
1.Pengumpulan Bahan Daun Petai...26
2.Pengeringandan pembuatan serbuk daun petai...27
3.Penetapan susut pengeringan serbuk daun petai... 27
4.Pembuatan ekstrak etanol daun petai...27
5. Skrining fitokimia daun petai...28
6.Uji aktivitas antibakteri ekstrak etanol daun petai terhadapS.aureus danE.coli...30
7.Analisis Hasil...33
BAB IV PEMBAHASAN ...35
A.Penyiapan Bahan...35
1. Pengumpulan daun dan determinasi...35
x i i
3.Penetapan susut pengeringan serbuk daun petai... 36
4. Pembuatan ekstrak etanol daun petai...37
B.Skrining fitokimia...39
C.Identifikasi bakteri...44
D .Uji aktivitas antibakteri ekstrak etanol daun petai terhadapS.aureus ATCC 25923danE. coli ATCC25922difusi sumuran...46
E.Penetapan KHM dan KBM ekstrak etanol daun petai terhadapS.aureus ATCC 25923...53
BAB V KESIMPULAN DAN SARAN ...56
A.Kesimpulan...56
B.Saran...56
DAFTAR PUSTAKA ...57
LAMPIRAN ...63
x i i i DAFTAR TABEL
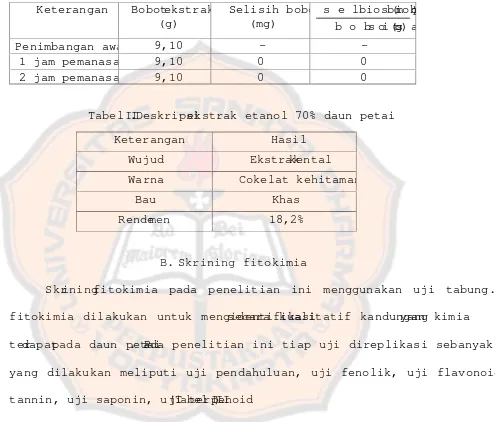
Tabel I. Bobot Tetap ekstrak etanol daun petai...39
Tabel II.Deskripsi ekstrak etanol 70% daun petai...39
Tabel III. Hasil ujitabungskrining fitokimia...40
Tabel IV . Diameter zona hambat ekstrak etanol daun petaiterhadap bakteri
E. Coli ATCC 25922danS. aureus ATCC 25923...49
Tabel V. Kategori daya hambat...49
Tabel VI. HasilMann WithneyWilcoxondiameter zona hambat seri
konsentrasi ekstrak etanol daun petai terhadapS.aureus...52
Tabel VII. Hasil uji dilusi cair ekstrak etanol daun petai terhadap bakt
S.aureus...54
x i v DAFTAR LAMPIRAN
Lampiran 1.Surat Keterangan Simplisia Daun Petai...64
Lampiran 2.Surat Izin Penelitian di Laboratorium Balai Kesehatan Yogyakarta...65
Lampiran 3.Sertifikat hasil ujiStaphlococcus aureusATCC 25923...66
Lampiran 4. Sertifikat hasil ujiEscherichia coliATCC 25922...67
Lampiran 5.Fotopengeringan daun petai...68
Lampiran 6.Hasil penenetapan susut pengeringan...68
Lampiran 7.Fotopenguapanmenggunakanrotary evaporator...69
Lampiran 8. Hasil ekstrak etanol daun petai...69
Lampiran 9. Hasilujitabungpendahuluan...70
Lampiran10.Hasil ujitabungfenolik...71
Lampiran11.Hasil ujitabungflavonoid...72
Lampiran 12.Hasil ujitabungalkaloid...73
Lampiran 13.Hasil ujitabungtanin...74
Lampiran 14.Hasilujitabungsaponin...75
Lampiran 15.Hasil ujitabungterpenoid...76
Lampiran 16.Variasi konsentrasi ekstraketanol daun petai...77
Lampiran17.Identifikasi bakteri...78
Lampiran 18.Hasiluji aktivitas antibakteri terhadapS.aureusdengan difusi sumuran...83
x v
Lampiran 20.Hasil pengukuran diameter zona hambat ekstrak etanol daun petai...85
Lampiran 21.Uji KHM dan KBM EkstrakEtanol Daun Petai denganm etode
dilusicair...86
Lampiran 22. Ujipenegasan denganstreak plate...87
Lampiran 23. Hasil uji dilusi cair...88
x v i Intisari
Penyakit infeksi dapat disebabkan oleh bakteri diantaranyaStaphylococcus aureusdanEscherichiacoli.Penyakit infeksi merupakansalah satu penyebab kematian terbesar di dunia sehinggadiperlukan alternatifuntuk mengatasiyaitudengan
memanfaatkanbahan alam. Daun petai mengandung terpenoid, fenolik, flavonoi, saponin dan alkaloid. Senyawa- senyawa tersebut diketahuimemiliki aktivitas
antibakteri.
Penelitian ini bertujuanuntuk mengetahuiaktivitas antibakteri ekstrak etanol daun petai(Parkia speciosaHassk.)terhadapS.aureusdanE.coli.Penelitiantermasuk
eksperimental murni, dengan rancangan acak lengkap polasatu arah. Tahapan penelitianmeliputipersiapan,ekstraksi,identifikasi kandungan senyawa,uji aktivitas antibakteri dengan metodedifusisumuran, dilanjutkan dengan metode dilusicairuntuk mengetahui Kadar Hambat Minimal (KHM)dan Kadar Bunuh Minimum (KBM). Hasil uji aktivitas antibakteri dianalisisstatitistik menggunakanShapiro Wilkuntukuji
distribusinormaldata,Kruskal Wallisuntuk mengetahui perbedaan secara keseluruhan danMann Whitneyuntuk mengetahuiperbedaanantar konsentrasidan kontrol
negatif.
Hasil penelitian menunjukkan bahwa ekstrak etanol daun petai memili antibakteri terhadapS.aureus, tetapi tidak memberikan aktivitas antibakteri t
E. coli. Nilai KHM ekstrak etanol daun petaiterhadapS.aureusadalahpada konsentrasi25%, sedangkan nilai KBMbelum dicapai.
x v i i
ABSTRACT
Infectious diseasescan be causedbybacteriasuchasStaphylococcusaureusand
Escherichiacoli.Infectious diseasesareone of thebiggest causes of deathin theworld so that necessaryalternativetosolve it,by exploitnaturalmaterials. Petaileaves containingterpenoids,phenolic,flavonoid, saponin and alkaloid.Thosecompounds knownhaveantibacterial activity.
Thisstudy waspurposedtodetermineantibacterial activityethanol extractof petai leaves(Parkia speciosaHassk.)againstS.aureusandE.coli.This studyispurely experimental,completely randomizedand one way design.Steps of this studyinclude the preparation,extraction,identification ofcompounds,antibacterialactivity testused difussionmethod, followedby liquiddilution methodto determine theMinimal Inhibitoryconcentration(MIC) and Minimum Bactericidal Concentration(MBC ). Antibacterialactivity testresultswere analyzedusing theShapiro Wilkstatitistikto
normaldata distribution,Kruskal Wallistestto determinesignificant differences in wholegroupandMann -Whitneytodeterminethedifferencesbetweenconcentration
andnegative control.
The results ofthis studyshowedthat theethanolextract ofpetaileaveshave
antibacterial activityagainstS.aureus,butitdidnothaveantibacterialactivity against
E.coli.MIC ofethanol extractof petai leavesagainstS.aureusat concentration25% , while the MBC has not obtained.
1 BAB I PENGANTAR
A. Latar Belakang
Penyakit infeksi merupakan masalah di bidang kesehatandan menjadisalah satu
penyebab kematianterbesar di dunia.Infeksi selaindisebabkan oleh virus dapat juga
disebabkan oleh bakteri, fungi, protozoa (Jawetz, Melnickdan Adelberg, 2005).
Penyakit infeksi saluranpernapasandan penyakitdiare merupakan penyakit yang
seringdialamimasyarakat(Adila, Nurmiati dan Agustien, 2013).Menurut hasilSistem
Informasi Rumah Sakitcit.Anonim (2012), diare dan infeksi saluran pernapas
m asuk dalamperingkat 10 besar penyakit penyebab rawat inap di Rumah
Indonesia padatahun 2009 dan tahun 2010Berdasarkan data yang diperoleh. W orld
H ealthO rganisation(2012), penyakit diaredan infeksi saluran pernapasanmenjadi
penyebab kematian tingkat ketiga di negaranegara berkembang. Selain itu, penyakit
penyakit tersebut juga masuk dalam 10 peringkat besar penyebab kemat
Pada tahun 2012,diare menyebabkan kematian 1,5 juta jiwa, sedangkan infeksi
pernafasan menyebabkan kematian 1,6 juta jiwa di dunia.
Penyakitdiarebiasanyadisebabkan oleh bakteriEscherichia coli(World
Gastroenterology Organisation, 2012).Sedangkan, infeksi saluran pernapasan dapa
disebabkan oleh bakteriStaphylococcusaureus(Brooks, Butel dan Morse, 2007).
PemilihanS.aureusdanE.colisebagai bakteriujiyangdigunakan dalam penelitian
Berdasarkan data kesehatan,kematian yang disebabkan oleh infeksibakteri
cukuptinggi,sehinggaperlu diimbangi dengan penemuan obat baru yanglebih efektif
untuk pengatasaninfeksi. Salahsatu alternatifyang dapat dilakukanyaitu dengan
memanfaatkanbahan alam yang memiliki aktivitas antibakteri. Banyak baha
sekitar yang dapat digunakan sebagai obat tradisional namun masyar
mengetahui dan memanfaatkannya. Pemanfaatan bahan alam disekitar seba
antibakteri karena efek samping yang dihasilkan tidaklebihmerugikan dibanding obat
sintesis,selain itu lebih mudah diperolehdan tersedia terus menerus(Kardinan dan
Kusuma, 2004).Hal ini mendorong penelitiuntuk melakukan eksplorasi bahan alam
yang berpotensi antibakteri.
Petai (Parkia speciosaHassk.) merupakan salah satu bahan alam yang sering
dikonsumsi oleh masyarakatsebagai lalapan atau diolahmenjadicampuranmasakan
lainnya,namun ada jugayang tidak menyukai petai karena aromanya yang kha
Menurut penelitianKamisah, Othman, Qodriyah dan Jaarin (2013),hasilsubstansi
fitokimia petaimenggunakantanaman petai yang berasal dari Malaysiayaitubiji petai
mengandung alkaloid, terpenoid, flavonoid, fenolik.Sedangkan daun petai
mengandung terpenoid, flavonoid dan fenolik.Pada penelitian ini juga dikatakan
masyarakat setempatmenggunakan petaisebagai obat tradisional untuk mengobati
berbagai penyakit dan gejala seperti diabetes, ginjal dan sakit kepal
diketahui memilikipotensiaktivitasantimikroba,antioksidan, hipoglikemik dan
antitumor.Penelitian yang dilakukan Kurniawati (2014),ekstrak etanolkulit buah petai
tanin. Ekstrak kulit petai yang dihasilkan pada penelitiantersebuttidak memiliki
aktivitas antibakteri terhadapS. aureusdanE. coli.Padapenelitian Pratama (2015),
kulit batang pohon petaim engandung senyawa flavonoid, alkaloid, fenolik
terpenoidsertamemiliki aktivitas antibakteri terhadapS. aureusdanE. coli. Menurut
Kumalasari dan Sulistyani (2011), senyawaalkaloid, terpenoid, saponin, tanin, fenol
dan flavonoiddiketahui memiliki aktivitas sebagai antibakteri.Oleh karena itu, peneliti
tertarik melakukanpencarian kandungansenyawa pada daun petai,namundari berasal
dari tempat berbedayaitu tanaman petai yang diambildari Kabupaten Sleman,
Yogyakarta.Kandungan senyawa kimia yang terdapat pada tanaman dapat dipenga
oleh faktor lingkungan. Menurut Artini, Astuti dan Warditiani (201
lingkungan seperti iklim, suhu udara, sinar matahari, kelembaban udara, angin dan
keadaan tanah sangat berpengaruh terhadap proses pertumbuhan tanama
metabolit sekunder yang dihasilkan.Penelitianterkaitpencariansenyawa perlu
dilakukan untuk mengetahui kandungan senyawa aktif pada daun petai dan ya
sebagai antibakteri, sehingga diharapkan diperolehantibakteri baru dengan aktivitas
yang lebih baik.
1.Rumusan masalah
a. Senyawakimia apa saja yang terdapat pada ekstrak etanol daun petai
b. Apakah ekstrak etanol daun petai memiliki aktivitas antibakteterhadap
S.aureusdanE.coli?
c. Berapa Kadar Hambat Minimal (KHM)dan Kadar Bunuh Minimum (KBM)
2. Keaslian penelitian
Sejauh penelusuranpustaka oleh penulis, penelitian mengenai akti
antibakteri ekstrak etanol daun petai terhadap bakteriS.aureusdanE.colibelum
pernah dilakukan.Penelitian mengenaitanamanpetaiyangpernah dilakukanyaitu :
a. Penelitian ekstrak metanol bijipetaiterhadapbakteriHelicobacter pylori;ekstrak
etil asetat bijipetaiterhadapbakteriEscherichia coli; suspensi air bijipetai
terhadappertumbuhanbakteriAeromonas hydrophila,Staphylococcus aureus,
Streptococcus agalactiae,Streptococcus anginosusdan Vibrio parahaemolyticu
(Kamisah,dkk, 2013).
b. Fraksinasi ekstrak kulit petaimemilikipotensi antioksidan. Hasil uji identifika
pada penelitian tersebut adalah kulit petai mengandung alkaloid,
saponin, dan tanin (Mahardika, 2013).
c. Ekstraksi dan identifikasi senyawa pada bijiParkia speciosadengan karbon
dioksida superkritis (Azizi, Salman, Nik, dan Mohd, 2006).
d. Uji aktivitas antibakteri ekstrak biji petai terhadap pertumbuha
Helicobacter pyloridanEscherichia coli(Sakunpak dan Panichayupakaranant,
2012).
e. Aktivitas antibakteri ekstrak kulit petai (Parkia speciosaHassk.) terhadap bakteri
Perbedaanpenelitian yang dilakukan penulisdengan penelitiandiatasadalah
asal tanaman, bagian tanaman,penyari danjenisbakteriuji yang digunakan dalam
penelitian.Pada penelitian yang dilakukan olehKamisah,dkk(2013) menggunakanbiji
petai yang berasal dari Malaysia denganpenyari metanol, etil asetat dan airdengan
mikroba ujiH. pylori,E. coli, A. hidrophila, S. agalactiae, S. anginosusdanV.
parahaemolyticu; sedangkan penelitian yang dilakukan penulis menggunakandaun
petai dari Kabupaten Sleman denganpenyarietanolserta bakteri ujiE. ColidanS.
aureus.Pada penelitianSakunpak dan Panichayupakaranant (2012) menggunakan bi
petai yang diekstraksi dengan etil asetatterhadap bakteriH. pyloridanE. coli;
sedangkan penelitian yang dilakukan penulis menggunakandaun petaiyang diekstraksi
dengan etanol 70%terhadap bakteriS. aureusdanE. coli.Penelitianyang dilakukan
olehKurnawati (2014), serbuk simplisia kulit petai diekstraksi dengan
secara bertingkat dengan pelarut n-heksana, etil asetat, dan etanol 70%; sedang
penelitian yang dilakukan penulismenggunakanserbuk daun petai yang diekstraksi
denganmetode maserasimekanikmenggunakanetanol 70%.
3. Manfaat penelitian
a.Manfaat Teoritis
Penelitian ini diharapkan dapat memberikan informasi dalam ilmu pe
khususnya di bidangkesehatan dalam bidang obat tradisional mengenai penggun
b.Manfaat Praktis
Penelitian ini diharapkan dapat mem berikan informasi mengenai manfaat daun
petai sebagai obat tradisional bagi masyarakat terutama untuk mengobatipenyakit yang
disebabkan oleh infeksi bakteriS.aureusdanE.colidan juga dapat dikembangkan
menjadi sediaan farmasi agar mempermudah dalam penggunaan.
B. Tujuan Penelitian
1. Mengetahuisenyawakimia dalam ekstrak etanol daun petai
2. Mengetahui aktivitasantibakteri ekstrak etanol daun petaiterhadapS.aureusdan
E.coli
3. Mengetahui Kadar Hambat Minimum (KHM)dan Kadar Bunuh Minimum (KBM)
7 BAB II
PENELAAHAN PUSTAKA
A.Tanaman Petai
1.Klasifikasi tanaman petai
Menurut Plantamor (2008), tanaman petai diklasifikasikan sebagai b
Kingdom : Plantae
Species :Parkia speciosaHassk.
Tanaman petai memiliki beberapa nama daerah, diantaranya Pateh (
Parira ( Batak Karo), Pelila (Batak Toba), Petang (Lampung) dan Pete h
dan Jawa Timur ) (Adi, 2008).
2.Deskripsi tanaman petai
Tanaman petai berbentuk pohon dengan tinggi 5- 14 meter. Batang berkayu,
bulat bercabang, berwarna cokelat kemerahan. Daun menyirip ganda, uju
pangkal membulat, dengan panjang 4- 20 cm,lebar 2- 3 cm,warna hijau. Bunga
warna hijau. Biji berbentuk pipih, tebal, warna hijau. Akar tunggang
(Sunanta, 1992).
3.Kandungan kimia daun petai
Tanaman petai mengandung alkaloid, saponin, terpenoid, fenolik, fl
tanin.Kandungan kimia yang terdapat pada daun petai yaitu terpenoid,
flavonoid(Kamisah,dkk, 2013).
4.Khasiat daun petai
Daun petai berkhasiat sebagai peluruh air seni, obat cacing, menu
gula darah dan melancarkan peredaran darah (Adi, 2008).Daun petai juga digunakan
untuk mengatasi borok (Utami dan Asmaliyah, 2010).
B.Skrining Fitokimia
Skrining fitokimia dilakukan untuk mengetahui kandungan senyawa aktif pada
tanaman yang memiliki aktivitas tertentu.Fenolikmerupakan senyawa yang sangat
luas terjadi secara alami, mempunyai struktur yang bervariasi serta mem
satu gugus fenolik pada strukturnya (SarkerdanNahar, 2007). Fenolik pada tanaman
sebagian besar disintesis dari fenilalanin melalui aksi fenilalanin am
Senyawa ini berperan penting untuk tanamandan memiliki beberapa fungsi.Salah satu
peran penting yaitusebagai pertahananterhadap patogen dan herbivora (Rao, 2012).
Flavonoid merupakan golongan fenolik yang terdistribusi secara
tanaman. Pada struktur flavonoidterdapat lebih dari satu benzena(berbagai C15
lazim ditemukan dan beberapa jenisnya merupakan pigmen pada tumbuhan tingkat
tinggi (Rao, 2012).Beberapa flavonoid mempunyai sifatantibakteri,antioksidan,
antiinflamasi, antihepatotoksik(SarkerdanNahar, 2007).
Fenolik dan flavonoidmemberikan aktivitas antibakteri dengan merusa
membran sel sehingga terjadi perubahan permeabilitas sel yang dapat m
terhambatnya pertumbuhan sel atau matinya sel. Selain itu, Senyawa f
gugus hidroksi yang akan berikatandengan protein sehingga mengubah konformasi
protein membran sel target, mendenaturasi protein sel dan mengerutka
sehingga dapat melisiskan dinding sel(Pelczar dan Chan, 1988,cit.Kumalasaridan
Sulistyani, 2011).
Alkaloidmerupakan kelompok metabolit sekunder yang mengandung nitroge
yang aktif secara farmakologis. Dalam kebanyakan alkaloid, atom nitrog
bagiandari cincinheterosiklik. Alkaloid secara biosintesis diturunkan dari asam amino.
Alkaloid umumnyadikelompokkan sesuai dengan asam amino, baik yang
menyediakan nitrogen ataupun kerangka asam amino (Sarkerdan Nahar, 2007).
Alkaloid berasal dari alkali (basa) karena alkaloid memiliki sifat bas
garam yang larut air dengan asamasam mineral(Soegihardjo, 2013).Mekanisme
alkaloid sebagai antibakteri denganmengganggu komponen penyusun peptidoglikan
pada sel bakteri, sehingga lapisan dinding sel tidak terbentuk se
Taninmerupakan senyawapolifenol alami yang heterogentersebarsecara luas
pada tanaman,senyawa amorf, yang menghasilkan larutan koloidal asidik. Tanin
dengan pemberian garam besi (FeCl3) membentuk senyawa larut air berwarna
kehijauan atau biru gelap (SarkerdanNahar, 2007).Tanin yang larut air dan alkohol
biasanya ditemukan pada bagian akar, kulit kayu, batang dan lapisan an
tanaman. Tanin dapat membentuk kompleks dengan protein, karbohidrat, gel
alkaloid (Rao, 2012).Tanin bekerja sebagaiantibakteri dengan merusak membran sel
bakteri, sehingga sel bakteri lisis (Adila, NurmiatidanAgustien, 2013).Selain itu, tanin
memberikan aktivitas antibakterimelaluireaksi dengan membran sel, inaktivasi enzim
dan destruksi atau inaktivasi fungsimateri genetik.(Masduki , 1996,cit.Juliantina,
Citra, Nirwani, Nurmasitoh dan Bowo, 2009).
Saponinmerupakan glikosida yang tersebar luas pada tanaman, memili
seperti sabun (soaplike) dan menghasilkan busa. Saponin memiliki berat mol
tinggidimana molekul gula dikombinasikan dengan triterpen atau steroi
Senyawa ini sebagian besar amorf di alam, larut dalam air, alkohol dan
pelarut non polar seperti benzena, n-hexan(Rao, 2012).Saponin memberikan aktivitas
antibakteri dengan mengganggu permeabilitas membran sel bakteri,
mengakibatkan kerusakan membran sel dan menyebabkan keluarnya be
komponen penting dari dalam sel bakteri yaitu protein, asam nukleat da
Terpenoidditemukan pada hampir semua tanaman tingkat tinggi. Senya
diturunkan dari kombinasi dua atau lebih satuan isopren. Isopren merup5
karbon, yang secara kimiawidikenal sebagai 2-metil-1,3-butadiena. Terpenoid
dikelompokkan berdasarkan banyaknya unit atau satuan isoprenyang terlibat pada
pembentukan senyawa (SarkerdanNahar, 2007).Terpenoid memberikan aktivitas
antibakteri dengan mengganggu proses terbentuknya dinding sel, sehingg
tidak terbentukatau terbentuk tidak sempurna (Darsana, BesungdanMahatmi, 2012).
Selain itu,terpenoid bereaksi dengan porin (protein transmembran) pada mem
dinding sel bakteri membentuk ikatan polimer yang kuat sehingga meng
rusaknya porin. Kerusakanporin merupakan pintu keluar masuknya substans
sehingga mengurangi permeabilitas dinding sel bakteri yang akan menga
bakteri akan kekurangan nutrisi maka pertumbuhan bakteri terhambat atau mati (Salni,
Hanifa dan Ratna,2011).
C.Bakteri uji
1.Staphylococcus aureus
Staphylococcus aureustermasuk dalam famili Micrococcaceae. Bakteri
termasukGram positif, berdiameter sekitar0,8 1,0 m, disebutStaphylococcus
karena berbentuk bulat dantersusun dalam kelompok seperti anggur yang tidak teratur
dan biasanya membentuk koloni berwarna abuabu hingga kuning tua kecokelatan
sehingga dinamakanaureus(Pandji, 2010).S.aureusmerupakan anaerob fakultatif,
tidakbergerak dan membentuk spora,berkembang biak dengan cepat pada suhu 37C,
tahanpada panas (tahan pada suhu 50C selama 30 menit) dan NaCl 9%.Bakteri ini
memproduksikatalase yang mengubah hidrogen peroksida menjadi air dan hi,
bakteri ini memfermentasikankarbohidrat secara lambat, menghasilkan asam lakt
dan tidak menghasilkan gas (Brooks,dkk,2007).
S. aureusmerupakan flora normal rongga hidung, saluran cerna atau kulit.
Namun juga merupakan bakteri patogen yangmenyebabkan berbagai infeksi
diantaranyainfeksi pada kulit, seperti impetigo, furunkulosis, sindrom kul
infeksi yang lebih serius seperti pneumonia, mastitis, flebitis dan m
kronis yaitu osteomielitis, endokarditis.Bakteri inijuga dapat menyebabkan keracunan
makanan karenaenterotoksin yang dihasilkan dan menyebabkantoxic shock syndrome
akibat pelepasan superantigen ke dalam aliran darah (Radji, 2010).
Bakteriini dapat menyebabkan penyakitmelalui kemampuannya untuk
berkembang biak dan menyebar luas dijaringan serta dengan cara menghasilkan
berbagai substansi ekstraselular (Brooks,dkk, 2007). Mekanisme infeksiS.aureus
perlawanan terhadap sistem pertahanan inang dan melakukanpelepasan beberapa jenis
toksin (Radji, 2010).Enzim dan toksin yang berperan yaitu:
a.Katalase, mengubah hidrogen menjadi peroksida
b.Koagulase, protein mirip enzim yang menggumpalkan plasma oksalat ata
Koagulase berikatan dapat dengan protombin inang kemudian keduanya
aktif secara enzimatik yang menginisiasi polimerasi fibrin.
c.Eksotoksin, padaS.aureusterdiri dari alfatoksinyang merupakan hemolisin kuat;
beta toksin dapat merusak membran terutama sel darah merah.
d.Leukosidin,merupakan dua kompleks protein toksin yang bekerja secara
pada membran sel darah putih membentuk pori dan meningkatkan perme
sehingga dapat membunuh sel darah putih.
e.Toksin eksoliatif,toksin ini merupakan superantigen yaitu tipe A dan tipe
ini menyerang protein spesifik menyebabkan deskuamasi generalis
staphylococcal scaled skin syndrome.
f. Toksin SyndromSyok-Toksik,superantigen protropikal yang berikatan denga
MHC, merangsang sel T sehingga menimbulkan manifestasi demam, syok,
kulit pada sindrom syok toksin
g. Enterotoksin,merupakan superantigen penyebab keracunan makanan terut
yang mengandung karbohidrat danprotein. Toksin ini tahan terhap panas dan ke
enzim usus
2.Escherichia coli
Gambar 2.Escherichia coli(Carr, 2014).
Escherichia colimerupakanbakteri Gram negatif, termasuk dalam famili
Enterobacteriaceae, berbentukbatang pendek, tidak berspora,kadang berderet seperti
rantai, memiliki flagel, ukuran kecil-sedang, konsistensinyahalus, tepi rata. Bakteri
inimempunyai morfologiyang khas pada media pembeda,tes indol positif dan
menghasilkan gas dari glukosa.E.colimerupakan flora normal pada usus,menjadi
patogen jika jumlah bakteri ini dalam saluran pencernaanmeningkat atau berada di luar
usus(Jawetz,dkk,2005).
Serotipe antigenikE.colitelah dikenal berdasarkan peerbedaanstruktur antigen
somatik O ( liposakarida), antigen H ( flagel), antigen K (kapsul). PenyakiE.
colisangat bergantungpada ekspresi faktor virulensi masingmasing serotipe bekteri
ini, termasuk adanya adhesin, invasin, jenis toksin yang diproduksi d
mengatasi pertahanan tubuh. Beberapa galurE.colimenjadi penyebab infeksi pada
manusia, seperti infeksi saluran kemih, infeksi meningitis pada neona
Penularan penyakit oleh infeksiE.coliterjadi melalui kontak langsung, biasanya
terjadi di tempat yang memiliki sanitasi dan lingkungan yang kurang
makanan yang tidak dimasak dan daging yang terkontaminasi (Radji, 2010
Berdasarkan sifat virulensi, bakteri ini dikelompokkanmenjadiE.coliyang
menyebabkan infeksi intesin dan infeksi ekstraintestin.
a.E.coliyangmenyebabkan infeksi ekstraintestin :
1. Sepsis, terjadi bila pertahananhostnormal tidak kuat, sehinggaE.colibisa
masuk ke peredaran darah dan menyebabkan sepsis. Neonatus rentan
sepsis karena antibodi IGM yang masih sedikit. Sepsis dapat ter
infeksi saluran kemih (Brooks,dkk, 2007).
2.E.colimeningitis neonatus (NMEC), infeksi biasa terjadi setelah
masuk ke dalam pembuluh darah melalaui nasofaring atau san
gastrointestinal kemudian masuk kedalam selsel otak, dengan antigen kapsul
K1 sebagai faktor virulensi utama penyebab meningitis padabayi. Antigen
kapsul K1 bekerjamenghambat fagositosis, reaksi komplemen dan reaks
imunitashospes(Radji, 2010).
3.E. coliuropatogenik (UPEC), patogenesis UPEC dengan bantuan protn
penting pada adhesin yaitu P-fimbria atau PAP(pyelenophritis-associated pili)
sehingga terjadi kolonisasi pada kanung kemih penderita. UPEC
bakteri ini juga menghasilkan hemolisis yang bersifat sitotoks
membran selhost(Radji, 2010).
b.E.coliyangmenyebabkan infeksiintestin :
1.E.colienterotoksigenik(ETEC),merupakan bakteri penyebab diare pada anak
dan wisatawan yang berpergian ke daerahbersanitasi buruk.ETEC
menginfeksi mukosa usus halus melalui beberapa faktor kolonisas
yang berbeda. Setelah membentuk kolonisasi, salah satu ata
enderotoksin dilepaskan yaituheat labile toxin(LT) atauheat stabile toxin
(ST). Toksin ini akan menarik cairan dan elektrolit dari mukosa us
bersifat lebih virulen.
2.E.colienteropatogenik(EPEC),merupakan penyebab utama diare pada bayi.
Ciri infeksi EPEC dari lesi hispatologi yaitu tidak terlihatnya mikrovili
adanya pelekatan antar bakteri dengan membran sel epitel di se
EPEC menyebabkan terikatnya lesi, pelekatan lesi mengganggu ker
usus, yang menyebabkan diare.
3.E.colienteroagregatif(EAEC) ,merupakan penyebab utama diare akut dan
kronis pada masyarakat didaerah berkembang. MelekatnyaEAEC pada sel
mukosa usus disebabkan karena produksi lendir dan deposisi bakt
biofilm lendir bakteri. Kolonisasi persisten EAEC menghasilkan enterotoksin
dan sitotoksin yangberpotensi menyebabkaninfeksipada sel-sel usus,
4.E.colienteroinvasif (EIEC),mekanisme patogenenesi infeksimirip dengan
infeksi olehspesiesShigelladan menembus mukosa usus, terutama pada
lapisan usus besar. EIEC akan menyerang sel-sel epitel usus besar,
memproduksi enderotoksin dan menyebabkan kematian sel epitel
Kerusakan histologis yang dihasilkan yaitu peradangan dan ulser
yang merupakan karakteristikdisentri bacillary.
5.E. colienterohemoragik (EHEC),Patogenesis EHEC berhubungan dengan
produksi racun shigalike, racun ini mirip dengan toksin shiga Shigella
dysenteriae. Efek sitotoksik racun shigalike mengganggu kerja mukosusus
besar dan menyebabkan diare. Selain itu, racun ini mampu melewati
untuk mencapai sel-sel endotel yang melapisi pembuluh darah kecil y
melewati usus, ginjal, dan organ lainnya, menyebabkan gangguan me
yang akhirnya menyebabkan HUS (hemolytic-uremic syndrome)
(Dipiro, 2008).
D.Ekstraksi
Ekstraksi adalah pemisahan senyawa aktif dari jaringan tanaman me
pelarut selektif dengan prosedur standar. Metode ekstraksi ini memisa
tanaman yang larut dan meninggalkan metabolit yang tidak larut. Tujuan
ekstraksi standar untuk simplisia yaitu untuk memperoleh bagian yang diing
Ekstrak adalah sediaan yang dapat berupa kering, cair atau kent
dengan menyari simplisia nabati atau hewani menurut cara yang sesu
pengaruh cahaya matahari langsung (BPOM RI, 2010). Sedian ekstrak dibua
agar zat berkhasiatyang terdapat pada simplisia dalam bentuk yang mempunyai ka
tinggi (Anief, 1997).
Metode metode ekstraksi diantaranya :
1. Ekstraksi menggunakan pelarut
a.Cara dingin
1) Maserasi merupakan cara penyarian untuk simplisia yang zat aktifnya
mudah larut dalamlarutan penyari dan tidak mengandung zat yang muda
mengembang dalam cairan penyari. Maserasi dilakukan dengan merendam
serbuksimplisia dalam cairan penyari. Prinsip maserasi yaitu c
menembus dinding sel dan masuk kedalam ronggasel yang mengandung
zat aktif.Zat aktif akan terlarut karena adanya perbedaan konsentra
larutan zat aktif didalam dan diluar sel, sehingga larutan yang
ke luar. Keuntungan ekstraksi dengan maserasi yaituperalatan dan cara
pengerjaan sederhana danmudah diusahakan (Departemen Kesehatan
Republik Indonesia, 1986).
2) Perkolasimerupakan metodeekstraksimenggunakanpelarut yang selalu
baru sampai sempurna, umumnya dilakukan pada temperaturruangan.
dan perkolasi sebenarnya (penetesan / penampungan ekstrak).Ekstraksi ini
membutuhkan pelarut yang lebih banyak.
b.Cara panas
1) Soxhletmerupakan ekstraksi dengan pelarut yang selalu b
menggunakan alat khusus sehingga ekstraksi berjalan kontinyu dengan
jumlah pelarut konstan dan adanya pendingin balik.
2) Refluks merupakan ekstraksidengan pelarut pada temperaturtitik didihnya,
selama waktu tertentu dan jumlah pelarut yang relatif konst
adanya pendingin balik.
3) Digesti merupakanmaserasi kinetik (dengan pengadukan kontinu) pa
temperatur yang lebih tinggi dari suhu kamar, biasanya dilakuka
40 50 C.
4) Infus merupakanekstraksisimplisiamenggunakanair pada suhu 90 C
selama 15 menitpada penangas air (bejana infus tercelup dalam penangas
air mendidih).
5) Dekok merupakaninfusadenganwaktu yang lebih lama (lebih dari 30
menit) dan titik didihnya sampai titik didih air.
2.Destilasi uap
Destilasi uap merupakan ekstraksi senyawa dengan kandungan yang
menguap (minyak atsiri) dari bahan (segar atau simplisia) dengan ua
secara kontinu sampai sempurna dan diakhiri dengan kondensasi fase ua
menjadi destilat air bersama senyawa yang memisah sempurna atau sebagian.
(Depkes RI, 2000).
E.Uji Aktivitas Antibakteri
Pengujian aktivitas antibakteri bertujuan untuk mengetahui kemampua
senyawa dalam menghambat maupun membunuh bakteri. Uji aktivitas antibakteri
dapat dilakukan dengan 2 metode yaitu :
1.Metode difusi
Pada metode difusi, bakteri ditanam pada media yang sesuai dan
diletakkan kertas cakram yang berisi senyawa uji atau dibuat sumuran de
tertentu yang diisi senyawa uji.Prinsip metode ini yaitu aktivitas antibakt
berdasarkan luas daerah hambat pertumbuhan bakteri karena berdifusinya
dari titik awal pemberian ke daerah difusi (HugodanRussel, 2004). Pada metode difusi
untuk menentukan kekuatan aktivitas antibakteri dilakukan dengan cara meng
diameter zona jernih disekitar cakram atau sumuran (Brooks, dkk,2007).
2.Metode dilusi
Prinsip metode dilusi yaitu membuat seri pengenceran konsentras
antibakteri. Metode dilusi dibagi menjadi dua yaitu dilusi cair dan dilusi pada
perbedaan pada kedua metode ini hanya pada media yang digunakan.Cara pada metode
dilusi, yaitumemasukkan senyawa antibakteri ke dalam medium biakan bakteri
ini digunakan untuk menentukan KHM (kadar hambat minimum) dan KBM(kadar
bunuh minimum). Hasil diamati dari konsentrasi terendah yang dapat meng
atau membunuh bakteri (Jawetz,dkk,2005).
Pada dilusi padat, KHM ditentukan dengan mengamati kadar terkecil
antibakteri yang terlihat jernih tanpa adanya pertumbuhan antibakteri
Sedangkan menurutLennete,pada dilusi cair KHM ditentukan dengan mengukurOD
(Optical Density) setelahinkubasi dikurangi absorbansi sebelum inkuba
menggunakan spektrofotometer. Apabila terdapatkonsentrasi terendah yang
menghambat pertumbuhan bakteri, ditunjukkan dengan tidak adanya keker
bakteri 0), maka didapatkan Konsentrasi HambatMinimum (KHM) (Fatisa, 2013).
Konsentrasi senyawa antibakteri yang dimungkinkan sebagai KHM atau KBM
ulang pada media baru tanpa adanya penambahan bakteri uji dan diinkubasi selama
18 24 jam. Media baru yang tetap terlihat jernih setelah inkubasiditetapkan sebagai
KBM. Sedangkan, jika media menunjukkan adanya pertumbuhan bakteri di
sebagai KHM (Pratiwi, 2008).
F.Landasan Teori
Penyakit infeksiterus berkembangdan menjadisalah satu penyebab utama
kematiandi dunia.Selain disebabkan oleh virus dan jamur, penyakit infeksi
disebabkan oleh bakteri. Bakteri yang berperan diantaranyaS. aureusdanE. coli.Oleh
karena itu,perlu dilakukan penelitian untuk memperoleh alternatifpengatasan infeksi
diperoleh, serta efek samping yang lebih kecil. Salah satu bahan al
dimanfaatkanyaitu daun petai (Parkia speciosaHassk.).Menurut penelitianKamisah,
Othman, Qodriyah dan Jaarin (2013),tanaman petaimengandung alkaloid, terpenoid,
flavonoid, fenolikdan saponin.Biji petai mengandung alkaloid, terpenoid, flavonoi
fenolik.Sedangkan daun petai mengandung terpenoid, flavonoid dan fenol
Penelitian yang dilakukan Kurniawati (2014),ekstrak etanolkulit buah petai memiliki
senyawa alkaloid, terpenoid, saponin, dan tanin. Padapenelitian Pratama (2015),
ekstrakkulit batang pohon petaim engandung senyawa flavonoid, alkaloid, fenolik
terpenoid sertamemiliki aktivitas antibakteri terhadapS. aureusdanE. coli.Menurut
Kumalasari dan Sulistyani (2011), senyawa alkaloid, terpenoid, saponin,
dan flavonoid diketahui memiliki aktivitas sebagai antibakteri.
Senyawa kimia pada daun petaidiperoleh dengan melakukan ektraksi
menggunakan metode maserasi.Etanol digunakan sebagai penyari serbuk daun petai
karena menurutPadmasari, Astuti dan warditiani(2013) etanol dapat menarik
senyawa senyawa yang larut pada pelarut non polar hingga polar, sehingga
diharapkan senyawa yangterkandungdapat tersari dengan optimal.
Aktivitas antibakteriekstrak etanol daun petaiterhadap bakteriS. aureusdanE.
coliditunjukkan dengan metode difusi sumuran berdasarkan terbentuknyaer
zona hambat disekitar sumuran dan metode dilusi untuk menentukan niladan
G. Hipotesis
Senyawa kimia esktrak etanol daun petai yang diduga memiliki
antibakteri adalah fenolik, flavonoid, alkaloid, tanin, saponin dan tEkstrak
etanol daun petai (Parkia speciosaHassk.) memiliki aktivitas antibakteri terhadapS.
aureusdanE. coli,memiliki kadar hambat minimum (KHM)sertakadar bunuh
24 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian rancangan eksperimental
rancangan penelitian acak lengkap pola satu arah. Penelitian ini
Laboratorium Farmakognosi-Fitokimiadan Laboratorium Mikrobiologi, Fakultas
Farmasi Universitas Sanata Dharma,Laboratorium Mikrobiologi Balai Kesehatan
Yogyakarta.
B. Variabel dan Defenisi Operasional
1. Variable Penelitian
a. Variabel bebas: konsentrasi ekstrak etanol daun petai (Parkia speciosa).
b. Variabel tergantung: diameter zona hambat(mm).
c. Variabelpengacauterkendali: asal tanaman, cara ekstraksi, waktuinkubasi
(24 jam), suhu inkubasi (37 C), jenis mikroba uji,kepadatan bakteri,volume
larutan uji yang diinokulasikan.
d. Variabelpengacautak terkendali : umur tanaman.
2. Defenisi Operasional
a. Aktivitasantibakteri adalah kemampuan ekstrak etanol daun pe
menghambatatau membunuhbakteriujiS.aureusdanE.colidiamati dengan
terbentuknya zona hambat disekitar sumuranyang menggambarkan
b. Ekstrak etanol daun petai adalahsediaan berupa ekstrak kental yang diperol
dengan cara maserasiserbuk daunmenggunakan penyari etanol, kemudian
diuapkan menggunakanrotary evaporatordanwaterbathhingga diperoleh
ekstrak kentaldenganbobot tetapdantidak tumpah pada penuangan.
c. Zona hambat adalah zona jernih di sekitar sumuran yang menunjukka
penghambatan pertumbuhan bakteriS. aureusdanE. colioleh aktivitas
ekstrak etanol daun petai, dinyatakan dalam milimeterdan dibandingkan
dengan kontrol negatif (DMSO 5%) sebagai pelarut.
d. Kontrol negatif adalah DMSO 5% yang digunakan sebagai pelarut eks
pembanding ekstrak pada uji aktivitas antibakteri.
e. Kadar Hambat Minimum (KHM) adalah konsentrasi terendah dari eks
etanol daun petai yang mampu menghambat pertumbuhan bakteriS.aureus
danE.coli,penentuan KHM menggunakan metode dilusi cair.
f. Kadar Bunuh Minimum (KBM) adalahkonsentrasi terendah dari ekstrak
etanol daun petai yang mampu membunuh pertumbuhan bakteriS.aureusdan
E.coli.
C. Alat Penelitian
Alat-alat yang digunakanpada penelitianspektrofotometerUV (UV mini-1240
UV VisSpechtrophotometerShimadzu),Microbiological safety Cabinet(MSC),alat
-alat gelas (Pyrex), cawan petri, pengayak,cotton budsteril, jarum ose, pipet volume,
vortex,platform shaker(Innova2100 New Brunswick Scientific), mikropipet
(Memmert),moisture balance (HG53 Halogen Moistur Analyzer),autoklaf, inkubator
(Haraeus),bunzen,vacuum rotary evaporator(Buchi Labortechnik AG CH-9230),
kuvet,kertas saring, bunsen, penggaris (butterfly).
D. Bahan Penelitian
Daun petai; aquadest steril;dimetilsulfoksida(DMSO) 5% (Merck)sebagai
pelarutekstrak dan kontrol negatif,amoksisilin sebagai kontrol positif, mikroba uji
kultur murniSthapylococcus aureusATCC 25922danEscherichia coliATCC 25923
(Laboratorium Mikrobiologi Balai Kesehatan Yogyakarta),media pertumbuhan
mikroba ujiMueller HintonAgar(MHA) (Merck),Mueller Hinton Broth(MHB)
(Merck),etanol 70%(Brataco), larutan Mc.Farland 0,5(1,5.108CFU).
E. Tata Cara Penelitian
1.Pengumpulan daun petai
Bahan berupa daun petaidiambil dari Kabupaten Sleman. Kriteria bagian daun
yang diambilyaitu daun yang diambil berwarna hijau, dan belum terlalu tua
2.Pengeringan dan pembuatan serbuk simplisia daun petai
Daun petai yang telah dikumpulkan dicuci bersih dari kotoran da
tanaman lain. Daun dikeringkan pada ruangan khusus, atapfiber glassdengan suhu
48 C. Pengeringan dihentikan jika daun mudah remuk saat diremas,
menggunakan pengayak hingga diperoleh serbuk dengan ukuran halus.
disimpan dalamwadah kering dan tertutup rapat.
3.Penetapan susut pengeringan serbuk daun petai
Lima gram serbuk simplisia daun petaiditimbang, serbuk yang ditimbang
selanjutnyadimasukkan kedalammoisture balancesecara merata,dipanaskan pada
suhu 105 C selama 15 menit. Kemudian dihitung selisih bobot serbuk simplisi
petai sebelum pemanasan dan setelah pemanasan.
s u s u tp e n g e r i n g a n= b o b o ts e b e l u mp e m a n a s a n" b o b o ts e t e l a hp e m a n a s a n s e b e l u mp e m a n a s a n x 1 0 0 % 4.Pembuatan ekstak etanol daun petai
Ektrak etanol daun petai dibuat dengan metode maserasi perbandinga(50
gram serbuk daun dalam 500 ml pelarut etanol 70%). Maserasi dilakukan dengan cara
50 gram serbuk daun petai dimasukkan dalam erlenmeyer, kemudian ditambahi 375
mL etanol 70% digojog selama 2x 24 jam menggunakanshakerdengan kecepatan
160rpm. Ekstrak yang diperoleh kemudiandisaring dengan kertas saring dengan
bantuanvacuumdan corongBuchner,filtratdisebut sebagai maserat I. Selanjutnya
ampas hasil saringan ditambahkan lagidengan 125 mL etanol 75%di remaserasi
selama 1x 24 jam, hasil ekstrak yang diperoleh sebagai maserat II.
Maserat II digabungkan kemudian dipekatkan menggunakanrotary vacuum
evaporatorpada suhu 65 C. Hasil disimpan dalam cawan porselin yangsudah ditara
sebelumnya, dilanjutkan penguapan menggunakan penangas air pada suhu
5.Skrining fitokimiadaun petai dengan uji tabung
a. Pembuatan larutan uji fitokimia
Pembuatan larutan uji untukuji fitokimia dilakukan dengan cara melarutka
sebanyak 500 mg ekstrak etanol daun petai dalam 50 mL etanol 70%.
b.Uji pendahuluan
Dua gram serbuk daun petai ditambahkan dengan 20 mL aquadest dipa
di ataswaterbathselama – 15 menit, selanjutnya disaring. Jika larutan menjadi berwarna merah hingga kuning dan saat penambahan KOH LP, warna l
menjadi lebih intensif menunjukkan adanya senyawa yang mengandung kr
dengan gugus hidrofilik.
c.Uji fenolik
Sebanyak 3mL larutan uji ditambahkan5 - 7 tetes larutan FeCl3 1%. Bila
berwarna hijau, merah, ungu atau hitam menunjukkan hasil positif dan
Kinghorn, 2006).
d.Uji flavonoid
Tiga mililiter larutan uji ditambah dengan1-2 tetesNaOH LP, terjadi
pembentukan intensitas warna kuning. Denganpenambahan HCl intensitas warna
kuning berubah menunjukkan adanya flavonoid(JonesdanKinghorn, 2006).
e.Uji alkaloid
Dua mililiter larutan uji diuapkan di dalam porselin pada pena
menit, sisanya dilarutkan dengan 5 mL HCl 2 N. Kemudian, larutanyang diperoleh
HCL 2N; tabung reaksi B larutan ditambah 3 tetes pereaksi Dragendorf
reaksi C larutan ditambah dengan 3 tetes peraksi Mayer. Terbentuknya endapat
jingga pada penambahan Dragendorff dan endapan kuning pada penam
pereaksiMayer menunjukkan adanya alkaloid(Jones danKinghorn, 2006).
f.Uji tanin
Sebanyak 1mL larutan uji ditambahkan2-3 tetes larutan FeCl310% . Adanya
tanin ditunjukkan denganterbentuknya warna biru tuaatau hitam kehijauan (Jones
danKinghorn, 2006).
g.Uji saponin
Seratus miligram serbuk daun petai ditambah 10 mL akuades dalam
reaksi, ditutup dan dikocok kuat-kuat selama 30 detik. Tabung dibiarkan dala
posisi tegak selama 30 menit.Apabila terbentuk buih dari permukaan cairandan
setelah–30 menitpenambahan 1 tetes HCl 2Nbusa tidak hilang maka menunjukkan
adanya saponin(Depkes RI, 1995).
h.Uji terpenoid
Sebanyak 2,5 mL larutan uji dicampur dengan 1 mL kloroform danditambah
1,5 mL H2SO4 pekat secara hati-hati (lewat dinding). Jikaberwarna coklat
kemerahan pada permukaan dalam larutan menunjukkan hasil positif(Edeoga,
6.Uji aktivitas antibakteri ekstak etanol daun petaiterhadapS.aureusdanE.coli
a.Identifikasi bakteri uji
1)Staphylococcus aureus
Bakteri ditanam ke media geolitik kemudian diinkubasi selama
pada suhu 37 C, setelah diinkubasi dan terdapat endapan hitam pa
tempat diinokulasikan bakteri maka menunjukkan bahwa bakteri yang
diidentifikasi adalahS.aureus. Setelah 24 jam diinkubasi, bakteri diisolas
media geolitik ke media Enrich, selanjutnya diinkubasi kembali s
24 jam pada suhu 37C, jika terdapat endapan hitam dengan kabut putih s
diinkubasi menunjukkan bahwabakteri yang diidentifikasikanadalahS.
aureus.Kemudian, diambil 1-2 ose bakteri, diinokulasi ke dalam media gul
-gula (glukosa, laktosa, manitol, maltosa, sakarosa), media NA mi
Simons Citrate(SC), mediaSulfureIndole Motil(SIM) dan diinkubasi selama
24 jam. Setelah diinkubasi selama 24 jam, dilakukan pengecatan gr
2)Escherichia coli
Bakteri ditanam ke media BGLB (Brilliant Green Lactose Bile) kemudian
diinkubasi selama 24 jam pada suhu 44 C. Jika setelah inkubasi terdapat
gelembung gas dari tabung Durham yang ada di dalam tabung reaks
menunjukkan bahwa bakteri yang diidentifikasi adalahE. coli. Setelah
diinkubasi, bakteri diisolasi dan ditanam ke media TBX (Tryptone Bile X
-Glucuronide) dan diinkubasi selama 24 jam pada suhu 37 C. Jika setelah
bakteri yang diuji adalahEscherichia coli.Kemudian, diambil 1-2 ose bakteri,
diinokulasi ke dalam media gula-gula (glukosa, laktosa, manitol, maltosa,
sakarosa), media NAmiring,Simons Citrate(SC),Sulfure Indole Motil(SIM)
dan diinkubasi selama 24 jam. Setelah diinkubasi, dilakukan penge
b.Pembuatan suspensi bakteri uji
Pembuatan suspensi bakteri dilakukan dengan mengambil 1-2 ose bakteri dari
stok yang telah dibuat sebelumnya, diinokulasikan pada 5 mL mediaMHB (Mueller
Hinton Broth), suspensi kemudian divortex.SuspensibakteriS.aureusdanE.coli
tersebutdisetarakankekeruhannya dengan larutan standar Mc. Farland0,5 (1,5 x 108
CFU) menggunakan alatDensicheck.
c.Pembuatan variasi konsentrasi larutan uji
Pembuatan variasi konsentrasi larutan uji dilakukan dengan cara melarutkan
ekstrak kental daun petai dengan DMSO 5%. Kemudian dilakukan penge
sehingga diperoleh konsentrasi 50%; 25%; 12,5%; 6,25%; 3,125%. DM
digunakan sebagai kontrol negatif dan amoksisilin 125mg/ 5mL digunakbagai
kontrol positif.
d.Uji aktivitas anti bakteri dengan metode difusi sumuran
Uji aktivitasantibakteri dengan metode difusi sumuran dilaku
menggunakan metodeKirby Bauer.MediaMueller Hinton Agar(MHA) yang telah
memadat pada petri di dioleskanbakteri uji pada permukaan secara merata
menggunakancotton budsteril. Kemudian, dibuat sumuran dengan menggunakan
50 L ekstrak etanoldaun petaidengan berbagai variasikonsentrasi(50%; 25%;
12,5%; 6,25% dan 3,125%). Amoksisilin 125 mg/ 5ml sebagai kontrol positidan
DMSO 5% sebagai kontrol negatif dari ekstrak etanol. Petri-petritersebutselanjutnya
diinkubasi selama 24 jam pada suhu 37C kemudian diamati ada tidaknya zona
hambat disekitar sumuran. Zona hambat yang terbentuk diukur dengan pearis. Uji
aktivitas antibakteridireplikasi sebanyak 3 kali.
e.Pengukuran KHM dengan metode dilusi cair
PengukuranKonsentrasi Hambat Minimum (KHM ) danKonsentrasi Bunuh
Minimimum (KBM ) dilakukan dengan metode dilusi/pengenceran. Media yang
digunakan adalah MediaMueller HintonBroth(MHB ).Ekstrak etanol daun petai
(ParkiaspeciosaHassk.) dibuat variasi konsentrasi(50%; 25%;21,875%; 18,75%;
15,625%;12,5%; 6,25%; 3,125%; 1,563% dan 0,782%). Mula-mula pengujian
dilakukan dengan membuat suspensi bakteri yang disetarakan kekeruhann
larutan standarMc. Farland0,5 (1,5 x 108 CFU) menggunakan alatDensicheck.
Penentuan KHM dan KBMmenggunakanspektrofotometer ( 480nm) dengan
mengukurOptical Density(OD ). Tahap penentuan KHM dan KBM yaitu7 tabung
reaksiyang masing-masing berisi 5 mL media MHBsteril,ditambah 200 L ekstrak
etanoldaunpetaidengan berbagai variasi konsentrasidan200 L suspensibakteri.
Tujuhtabung reaksi yang telah berisi media MHB, ekstrakdengan berbagai variasi
konsentrasidan suspensi bakterikemudian diukurOptical Density(OD)sebelum dan
setelahinkubasi selama 12-18 jam pada suhu 37 C dalam inkubator.NilaiKHM
K onsentrasi terendah yang menghambat pertumbuhan bakteri, ditunjukka
tidak adanya kekeruhan (OD bakteri adalah0).Sedangkanuntuk penentuanKBM,
dilakukan uji lanjutan dengan cara mengambil 1-2 ose dari konsentrasi yang
menunjukkan KHM,distreakke media MHA steril.Selanjutnyadiinkubasi selama
24 jam pada suhu 37C. Setelah diinkubasi, dilihatapakah terdapatpertumbuhan
bakteripada media yangdistreak.Jika tidak terdapat pertumbuhan bakteri, ma
diperoleh Kadar Bunuh Minimum (KBM). Tetapi, jika terdapat pertumbuha
media yang streak, makakonsetrasiyang diperoleh adalah Kadar Hambat Minimum
(KHM).
F. Analisis hasil
Uji aktivitas antibakteriditunjukkan dengan data zona hambat yang diperoleh
dengan menggunakanmetode pengujian difusi sumuran pada berbagai var
konsentrasi dibandingkan dengankontrol negatif dan direplikasi sebanyak 3 ka
Pengukuran zona hambat dilakukan dengan menggunakanpenggaris dalam satuan
milimeter, kemudian dianalisis secara statistik.
Data zona hambat aktivitas antibakteri ekstrak etanol daun petai
diuji menggunakanShapiroWilkuntuk mengetahui apakah data tiap kelompok
terdistribusi normal. Jika data terdistribusi normal dilanjutkan de
variansi searah (ANA VA), untuk mengetahui perbedaan bermakna zona hambat ant
kelompok, baik antar konsentrasi maupun dengan kontrol.Sedangkan,jikadata tidak
secara keseluruhan,dilanjutkan denganMann Whitneyuntuk mengetahui perbedaan
antar konsentrasi dan kontrol.
Nilai KHM dan KBM yang diperoleh dengan menggunakan metode dilusi
dianalisis secara deskriptif. Nilai KHM dan KBMdidapatdengancaramengukur
kekeruhan dengan melihat absorbansi menggunakan spektrofotometervisiblesehingga
didapatkan nilaioptical density(OD). Nilai KHM dan KBM diperoleh jika nilai OD
= 0. Semudian ditegaskan pada media MHAsteriluntuk mengetahuikonsentrasi
35 BAB IV
HASIL DAN PEMBAHASAN
Penelitian ini dilakukan untuk mengetahuikandungan senyawapada daun petai
(Parkia speciosaHassk.),aktivitas antibakteri daun petai terhadap bakteriS.aureusdan
E.colisertakonsentrasi hambat minimum (KHM)dan Konsentrasi bunuh minimum
(KBM).
A. Penyiapan Bahan
1.Pengumpulan daun petaidan determinasi
Tanaman petai yang digunakan pada penelitian ini diperoleh dari
Sleman, Yogyakarta pada Bulan Mei2014. Daun yang diambil adalah daun yang tida
terlalu mudajuga tidak terlalu tua, karenadiharapkan dalam kondisi tersebut
kandungan senyawa berada dalam jumlah optimum.Bila daun yang diambil terlalu
muda dikhawatirkan senyawa yang terbentuk belum maksimal, sedangkan j
yang diambil terlalu tua maka dikhawatirkan ada senyawa yang suda
Pembuktian kebenaran tanaman yangdigunakan dilakukandeterminasidengan
mencocokkan ciriciri tanaman. Hasilsurat keteranganCV Merapi Farma Herbal
(lampiran 1)menunjukkan bahwa tanaman yang digunakan dalam penelitian ada
benar petai(Parkia speciosaHassk.).
2.Pembuatan serbuk simplisia
Daun petai yang telahterkumpulkemudiandilakukanpemisahanuntuk
bagian yang diinginkan. Selanjutnyadicuci bersih menggunakan air untuk
menghilangkan pengotor yang menempel. Daunyang sudah bersih kemudian
dikeringkan pada ruangan khusus, atapfiber glassdengan suhu 48 C. Pengeringan
dihentikan jika daun mudah remuk saat diremas. Pengeringan bertujuan
mengurangi kadar air, dimana air merupakan media yang baik untuk pean
mikroba dan juga untuk mempermudah penghancuran. Kemudian dilakukan
penyerbukandengan menggunakan penyerbuk hingga halus, serbuk yang dipe
diayakhingga diperoleh serbuk dengan ukuran halus.Ukuran partikel yang kecil akan
meningkatkan luaspermukaan kontak serbuk dengan penyari sehingga rendemen yang
diperoleh lebih banyak.Serbuk yang sudah diayak disimpan dalam wadah tertut
rapat, di tempat kering dan terlindung dari sinar matahari langsung a
rusak.
3.Penetapan susutpengeringan serbukdaun petai
Penetapan susut pengeringan serbuk simplisia daun petai bertuj
mengetahui kandunganairdanjumlah semua jenis bahan yang mudah menguap dan
hilang padakondisi tertentu.MenurutMenteri Kesehatan Republik Indonesia (2009),
susut pengeringan dinyatakan sebagai nilai persen terhadap bobot awal,
tidak melebihi 10%.Pada penelitian ini penetapan susut pengeringan mengguna
moisture balance,pemanasan dilakukanpada suhu 105 C selama 15 menit. Suhu yang
digunakan 105 C yaitusuhudiatas titik didih air,agardapatmenguapkan air yang
terkandung dalam serbukdaun petai. Ratarata susut pengeringan serbuk daun petai
dari 10%,sehingga dapat disimpulkan serbuk daun petai yang digunakan da
penelitiantelah memenuhi kriteria yang ditetapkan.
4.Pembuatan ekstak etanol daun petai
Serbuk simplisia daun petai kemudian dibuat ekstrak dengan metode
Ektrak etanol daun petai dibuat dengan metode maserasi, 50 gram daun petai dire
dalam 500ml etanol 70% (perbandingan 1 : 10) selama 2 x 24 jam.Pemilihan metode
maserasi dikarenakan pengerjaan dan alat yang sederhana. Selain itu menurut Rusdi,
cit.,Dewi (2010), maserasi merupakan ekstraksi dingin sehingga diharapakan sem
metabolit sekunder dalam daunpetaidapat diperoleh, tanpa adanya kerusakan ata
perubahan kimia akibat pemanasan dan juga dapat menghasilkan ekstrak da
banyak, maserasi juga digunakan karena kandungan kimia yang diharapkan mudah
larut dalam penyari.
Prinsip maserasi yaitu penyari akan menembus dinding sel menuju
yang mengandung zat aktif, adanya perbedaan konsentrasi antara zat akt
di dalam dan di luar sel mengakibatkan zataktif menjadi larut dan terdesak kelua
(Departemen Kesehatan Republik Indonesia, 1986).Maserasi menggunakan bantuan
shakeruntuk penggojogan atau dikenal dengan maserasi mekanik bertujua
kontak cairan penyari dengan serbuk simplisia akan meningkat,sehingga waktu yang
diperlukanuntuk senyawa terlarut dalam larutan penyari lebih cepat. Et
digunakan sebagai cairan penyari karena etanol 70% sangat efektif dalam mela
senyawa yang terkandung dalam serbuk simplisia daunpetaidapat terlarut dengan
optimal (Kumalasari danSulistyani, 2011).
Ekstrak yang diperoleh kemudiandisaringmenggunakankertas saring dengan
bantuanvacuumdan corongBuchner.Ampas kemudian diremaserasiselama 1 x 24
jammenggunakan penyari etanol.Remaserasi dilakukan untuk menarik senyawa yang
mungkin masih adasehingga hasil ekstrak yang diperoleh maksimal.Filtrat kemudian
diupakan menggunakanrotary vacuum evaporatorpada suhu 65 C bertujuan
menguapkan cairan penyari. Kemudian filtrat dimasukkan dalam cawan ,
penguapan dilanjutkan menggunakan penangasair pada suhu 60 C untuk memastikan
semua cairan penyari sudah teruapkan. Penguapan dilakukan sampai diper
kental dengan bobot tetap(Tabel I). Menurut Depkes RI (1986) bobot tetap adalah
selisih 2 kali penimbangan berturut-turut tidak lebihdari 0,5mg tiap gram sisa yang
ditimbang. Ekstrak kental yang diperoleh yaitu 9,10g. Ekstrak yang diperoleh
kemudian dihitung rendemennya. Penetapan rendemen bertujuan mengukurefektivitas
pelarutyang digunakan dalammengestrak senyawa kimia yang terkandung dalam daun
petai. Semakin besarrendemen yang diperoleh semakin efektif pelarut yang dig
Tabel I. Bobot Tetap ekstrak etanol daun petai
1 jam pemanasan 9,10 0 0
2 jam pemanasan 9,10 0 0
Tabel II.Deskripsiekstrak etanol 70% daun petai
Keterangan Hasil
Skriningfitokimia pada penelitian ini menggunakan uji tabung. S
fitokimia dilakukan untuk mengidentifikasisecara kualitatif kandungan kimiayang
terdapatpada daun petai. Pada penelitian ini tiap uji direplikasi sebanyak 3
yang dilakukan meliputi uji pendahuluan, uji fenolik, uji flavonoid,
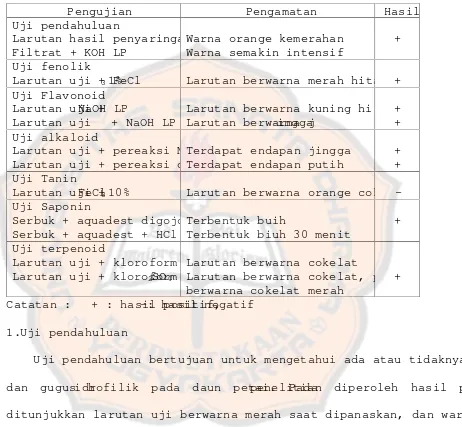
Tabel III. Hasil uji skriningfitokimia uji tabung
Larutan uji + FeCl31% Larutan berwarna merah hita + Uji Flavonoid
Larutan uji +FeCl310% Larutan berwarna orange coke -Uji Saponin Larutan uji + kloroform +2SO4
Larutan berwarna cokelat
Uji pendahuluan bertujuan untuk mengetahui ada atau tidaknya gugus
dan gugus hidrofilik pada daun petai. Padapenelitian diperoleh hasil positif
ditunjukkan larutan uji berwarna merah saat dipanaskan, dan warna menj
intensif saat penambahan KOH LP. Hal ini menunjukkan bahwa daun petai
gugus kromofor dan gugus hidrofilik.
2.Uji fenolik
Uji fenolik pada penelitian ini dilakukan dengan cara larutan uji di
mengindikasikan adanya fenolik. Hasil uji fenolik memberikan hasil
ditunjukkan dengan terbentuknya larutan berwarna merah hitam. Hal ini menunjukkan
bahwa pada ekstrak etanol daun petai terdapat fenolik.
3.Uji flavonoid
Pada uji flavonoid larutan uji daun petai ditetesi dengan NaOH LP.
intensitas warna kuning menunjukkan adanya senyawa flavonoid.Intensitas warna
kuning yang terbentuk pada penambahan natrium hidroksida dikarenakan
memiliki gugus orto dihidroksi. NaOH mengionisasi gugus hidroksi pada i
sehingga menyebabkan terjadinya pergeseran batokromik. Sedangkan pena
larutan HCl pada uji berfungsi menghentikan reaksi dan mengembalikan
semula (Markham,1988).
Hasil uji flavonoid menunjukan warna larutan menjadi kuning hi
penambahan NaOH LP dan larutan menjadi berwarna jingga setelah penamba
Hal ini menunjukkan terdapat senyawa flavonoid pada ektrak etanol daun
4.Uji alkaloid
Pada uji alkaloid larutan uji dilarutkan dengan HCl 2N. penamba
bertujuan untuk membentuk garam. Karena alkaloid bersifat basa sehi
membentuk garampada pelarut yang bersifat asam.Pemanasan pada penangas air
bertujuan untukmempercepat pembentukan garam.Larutan uji yang sudah
ditambahkan HClkemudian dibagi menjadi beberapa tabung.Tabung pertama
ditambah pereaksi Mayer yang berisimerkurium klorida dan kalium iodida. Larutan
tetraiodomerkurat(II). Alkaloid mengandung atom nitrogen yang mempuny
pasangan elektron bebas sehingga dapat digunakan untuk membentuk ikatan kovalen
koordinat dengan ion logam . Nitrogen pada alkaloid akan bereaksi denga
K+ dari kalium tetraiodomerkurat(II) membentuk komplekskalium alkaloid, yang
hasilpositifditunjukkan denganterbentuknya endapan putih(Marliana, Suryanti dan
Suyono, 2005) .
Tabung kedua ditambah pereaksi Dragendorff (bismuth (III) klorida dan kalium
iodida). Nitrogen pada alkaloid akan berikatanmembentukikatan kovalen koordinat
dengan ion K+ yang logam berat dari pereaksi Dragendorff yang men
terbentuknya endapan berwarna jingga (Marliana,dkk., 2005). Hasil uji alkaloid pada
tabung pertama dengan penambahan pereaksi Mayerterdapat endapan berwarna putih,
pada tabung kedua dengan penambahan pereaksi Dragendorff terbentuk
berwarna jingga. Hal ini menunjukkan ekstrak etanol daun petai dimungki
mengandung senyawa alkaloid.
5.Ujitanin
Pada penelitian ini,uji tanin menggunakan pereaksi FeCl3, hasil postif
ditunjukkan dengan perubahan warna menjadi biru tua atau hitam
PenambahanFeCl3pada larutan uji menyebabkan gugus hidroksil pada senyawa
yang merupakan senyawa fenolik akan bereaksi dengan larutan sehingga me
terbentuknya warna biru tua atau hijau (Sangi, MomuatdanKumaunang 2012). Hasil
uji tanin tidak menunjukan perubahan warna, sehingga diperkirakan tidak ter
6.Uji saponin
Uji saponin pada penelitian ini dilakukan dengan penambahan akua
serbuk kemudian digojog. Hasil positif ditunjukkan dengan terbentuknya buih yang
stabil dan buih tidak hilang setelah penambahan HCl. Saponin memigugus
hidrofilik dan hidrofobik. Saatdigojog gugus hidrofil akan berikatandengan air
sedangkan gugus hidrofobakanberikatan dengan udara sehinggamembentuk buih
(KumalasaridanSulistyani, 2011). PenambahanHCl yang bersifatasamberguna untuk
menambah kepolaransehingga gugus hidrofil akan berikatan dan buih yang terbe
menjadi stabil. Hasil uji saponin menunjukkan adanya buih pada tabung
penggojogan, setelahpendiaman 30 menit dan penambahan HCl buih tidak hilang.
ini menunjukkan dimungkinkan terdapat senyawa saponin pada daun petai.
7.Uji terpenoid
Uji terpenoid dilakukan dengan cara penambahan kloroform pada la
kemudian ditambahi H2SO4 pekat. Penambahan pereaksi kloroform dan H2SO4
berikatan dengan molekul senyawaterpenoidsehingga menghasilkanreaksi yang
tampak pada perubahan warnamenjadi merah atau cokelat. Hasil uji terpenoi
menunjukkan adanya perubahan warna larutan menjadi cokelatdengan cincin
berwarna merah pada permukaan, sehingga diduga ekstrak etanol da