UJI SITOTOKSISITAS EKSTRAK KLOROFORM DAUN PACAR AIR (Impatiens balsaminaL.) TERHADAP KULTUR SEL HeLa
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Lise Natalia NIM : 058114079
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
UJI SITOTOKSISITAS EKSTRAK KLOROFORM DAUN PACAR AIR (Impatiens balsaminaL.) TERHADAP KULTUR SEL HeLa
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Lise Natalia NIM : 058114079
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
v
HALAMAN PERSEMBAHAN
“If you can imagine it, you can achieve it. If you can dream it,
you can become it."
William Arthur Ward
-Kupersembahkan karya ini untuk
Papa dan mamaku tercinta, atas kasih sayang, doa dan dukungan
yang terus menyertaiku.
Adik-adikku terkasih, Victor dan Vera
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
Yang bertanda tangan di bawah ini, saya mahasiswa Universitas Sanata Dharma :
Nama : Lise Natalia
Nomor Mahasiswa : 058114079
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul :
“Uji Sitotoksisitas Ekstrak Kloroform Daun Pacar Air (Impatiens balsamina L.) terhadap Kultur Sel HeLa”
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, me-ngalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikan secara terbatas, dan mempublikasikannya di Internet atau media lain untuk kepentingan akademis tanpa perlu meminta ijin dari saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini yang saya buat dengan sebenarnya.
Dibuat di Yogyakarta
Pada tanggal : 1 Juni 2009
Yang menyatakan,
vi
PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa atas segala anugerah-Nya sehingga penulis dapat menyelesaikan skripsi dengan judul “Uji Sitotoksisitas
Ekstrak Kloroform Daun Pacar Air (Impatiens balsaminaL.) terhadap Kultur Sel HeLa”. Skripsi ini dibuat untuk memenuhi salah satu syarat memperoleh gelar
Sarjana Farmasi (S.Farm.) pada Program Studi Farmasi di Universitas Sanata
Dharma.
Penulisan skripsi ini tidak mungkin terselesaikan tanpa adanya bimbingan,
bantuan dan dukungan dari berbagai pihak, maka pada kesempatan ini, penulis mengucapkan terima kasih kepada:
1. Rita Suhadi, M.Si., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata
Dharma yang telah banyak meluangkan waktu, tenaga dan atas segala masukan serta sarannya dalam penyusunan skripsi ini.
2. Drs. A. Yuswanto S.U., Ph.D., Apt., selaku dosen pembimbing yang telah banyak meluangkan waktu, tenaga dan atas segala masukan serta sarannya
dalam penyusunan skripsi ini.
3. Drs. Mulyono, Apt., selaku dosen penguji yang telah berkenan menguji dan memberikan banyak masukan dan saran.
vii
5. Ign. Y Kristyo B, M.Si., yang telah memberikan banyak masukan dalam identifikasi dan determinasi tumbuhan.
6. Drs. P. Sunu Hardiyanta, S.G., M.Sc., yang telah memberikan masukan dan saran dalam pengolahan statistik.
7. Segenap dosen dan karyawan di Fakultas Farmasi Universitas Sanata Dharma,
terima kasih atas bantuannya selama ini.
8. Kepala Laboratorium Penelitian dan Pengujian Terpadu UGM atas ijin yang
diberikan untuk melakukan penelitian skripsi ini.
9. Mbak Yuli dan segenap karyawan Laboratorium Penelitian dan Pengujian
Terpadu UGM yang telah banyak membantu dalam penelitian skripsi ini.
10. Orang tua dan adik-adikku tercinta, atas segala dukungan dan doa yang selalu menyertaiku.
11. Suharso, atas segala dukungan dan kasih sayang yang diberikan selama penyusunan skripsi ini.
12. Anni dan Dhita, atas kerjasama, canda tawa dan keluh kesah selama
penyusunan skripsi ini.
13. Limdrawati dan Meri, terima kasih atas segala semangat dan bantuan yang
diberikan selama penyusunan skripsi ini.
14. Semua pihak yang telah banyak membantu penyusunan skripsi ini.
Atas segala bantuan yang telah diberikan selama ini, penulis mengucapkan
viii
kritik dan saran yang bersifat konstruktif demi penyempurnaan skripsi ini. Skripsi ini diharapkan dapat bermanfaat bagi perkembangan ilmu pengetahuan.
ix
PERNYATAAN KEASLIAN KARYA
Saya menyatakan bahwa sesungguhnya skripsi yang saya tulis ini tidak memuat
karya atau bagian karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagai layaknya karya ilmiah.
Yogyakarta, 13 Mei 2009 Penulis,
x INTISARI
Pengobatan tradisional menggunakan tanaman obat di masyarakat sudah cukup luas. Tanaman Pacar air (Impatiens balsamina) secara empiris dapat digunakan untuk mengobati berbagai penyakit, antara lain kanker. Penelitian ini bertujuan untuk mengetahui apakah ekstrak kloroform daun pacar air memiliki efek sitotoksik terhadap sel HeLa.
Penelitian ini adalah penelitian eksperimental murni dengan rancangan acak pola satu arah. Uji sitotoksisitas dilakukan pada kultur sel HeLa dan sel Vero menggunakan metode direct counting dengan perwarna trypan blue. Data yang diperoleh berupa persen kematian kultur sel HeLa dan sel Vero. Efek sitotoksisitas ekstrak kloroform daun pacar air terhadap kultur sel HeLa dan Vero dianalisis secara statistik dengan uji z dan harga LC50 akan dihitung dengan analisis probit.
Hasil penelitian menunjukkan bahwa ekstrak kloroform daun pacar air memiliki efek sitotoksik terhadap kultur sel HeLa dan sel Vero. Harga LC50 ekstrak klroform daun pacar air terhadap kultur sel HeLa sebesar 53,7 µg/ml dan sel Vero sebesar 275,4 µg/ml.
xi ABSTRACT
Traditional medication using herbs is widely spreaded in society.
Impatiens balsamina herbs can be used to cure many kinds of diseases, one of them is cancer. This research is aimed to determine whether the chloroform extract ofImpatiens balsaminaleaves have cytotoxic effect to HeLa cell cultures. The study is a pure experimental research with random complete and one way design. The cytotoxicity assay is tested to HeLa and Vero cell cultures using direct counting method with trypan blue stained. The data obtained were death percentage of HeLa and Vero cell cultures. The cytotoxicity effect of the chloroform extract of Impatiens balsamina leaves to HeLa cell cultures are analyzed using z-test and the LC50values are analyzed using probit.
The result shows that chloroform extract of Impatiens balsamina leaves have a cytotoxic effect to HeLa and Vero cell cultures. The LC50 value of chloroform extract of Impatiens balsamina leaves to HeLa cell cultures is 53,7 µg/ml and Vero cell culture is 275,4 µg/ml.
xii DAFTAR ISI
Halaman
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PRAKATA ... vi
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI ... x
ABSTRACT ... xi
DAFTAR ISI ... xii
DAFTAR TABEL ... xvi
DAFTAR GAMBAR ... xviii
DAFTAR LAMPIRAN ... xx
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Rumusan masalah ... 2
2. Keaslian penelitian ... 3
3. Manfaat penelitian ... 3
B. Tujuan ... 3
1. Tujuan umum ... ... 3
2. Tujuan khusus ... ... 3
xiii
A. Tanaman pacar air (Impatiens balsaminaL.)... 4
1. Keterangan botani ... 4
2. Kandungan kimia ... 4
3. Khasiat dan penggunaan ... 5
B. Kanker ... 5
1. Karsinogenesis ... 5
2. Kanker seviks ... 6
3. Sel HeLa ... 6
4. Sel vero ... 6
C. Ekstraksi ………... 7
1. Definisi ekstrak ... 7
2. Cairan pelarut ... 7
3. Ekstraksi ... 7
4. Maserasi ... 8
D. Uji Sitotoksisitas ... 8
E. Landasan teori ... 9
F. Hipotesis ... 10
BAB III METODOLOGI PENELITIAN ... 11
A. Jenis dan Rancangan Penelitian ... 11
B. Variabel Penelitian dan Definisi Operasional ... 11
1. Variabel utama ... 11
2. Variabel pengacau terkendali ... 11
xiv
C. Alat dan Bahan ... 12
1. Alat .... ... 12
2. Bahan ... 12
D. Tata Cara Penelitian ... 13
1. Determinasi tanaman ... 13
2. Pengumpulan bahan ... 13
3. Ekstraksi ... 13
4. Pembuatan medium pencuci dan penumbuh ... 14
5. Propagasi dan panen sel HeLa ... 15
6. Propagasi dan panen sel normal ... 16
7. Uji sitotoksisitas ekstrak kloroform daun pacar air ... 16
E. Analisis Hasil... 17
BAB IV HASIL DAN PEMBAHASAN ... 18
A. Determinasi tanaman... 18
B. Pengumpulan daun pacar air ... 18
C. Ekstraksi ... 19
D. Pembuatan medium pencuci dan medium penumbuh ... 19
E. Propagasi dan panen sel HeLa ... 20
F. Propagasi dan panen sel vero ... 20
G. Uji sitotoksisitas ekstrak kloroform daun pacar air ... 21
BAB V. KESIMPULAN DAN SARAN... 31
A. Kesimpulan ... 31
xv
DAFTAR PUSTAKA ... 32 LAMPIRAN ... 35
xvi
DAFTAR TABEL
Halaman
Tabel I. Jumlah Sel yang Hidup dari Tiap Sumuran pada Berbagai Tingkat Konsentrasi Ekstrak klroform daun pacar air dengan
metode direct counting ... 23
Tabel II. % kematian sel HeLa pada berbagai konsentrasi ekstrak kloroform daun pacar air ... 23
Tabel III. Jumlah Sel Vero yang Hidup dari Tiap Sumuran pada Berbagai Tingkat Konsentrasi ekstrak kloroform daun pacar
air dengan MetodeDirect Counting ... 27
Tabel IV. % kematian sel vero pada berbagai konsentrasi ekstrak kloroform daun pacar air ... 28
Tabel V. Data perhitungan jumlah sel HeLa dengan perhitungan Langsung ... 36
Tabel VI. Data perhitungan jumlah sel Vero dengan perhitungan
Langsung ... 37 Tabel VII. Data log konsentrasi, % kematian dan harga probit sel HeLa
pada replikasi I... 46 Tabel VIII. Data log konsentrasi, % kematian dan harga probit sel HeLa
pada replikasi II ... 47
xvii
Tabel X. Data log konsentrasi, % kematian dan harga probit sel vero pada replikasi I... 49
Tabel XI. Data log konsentrasi, % kematian dan harga probit sel vero pada replikasi II... 50
Tabel XII. Data log konsentrasi, % kematian dan harga probit sel vero
pada replikasi III ... 51 Tabel XIII. Nilai r (koefisien korelasi) pada level signifikansi 5% dan
xviii
DAFTAR GAMBAR
Halaman
Gambar 1. Foto kultur sel HeLa di haemocytometer setelah diberi
trypan blue... 22
Gambar 2. Kultur sel HeLa di sumuran ... 22
Gambar 3. Kultur sel Vero di sumuran ... 22 Gambar 4. Grafik konsentrasi ekstrak kloroform daun pacar air (µg/ml)
terhadap % kematian sel HeLa... 24 Gambar 5. Grafik log konsentrasi terhadap harga probit pada
replikasi I ... 25
Gambar 6. Grafik log konsentrasi terhadap harga probit pada
replikasi II ... 25
Gambar 7. Grafik log konsentrasi terhadap harga probit pada
replikasi III ... 26
Gambar 8. Grafik konsentrasi ekstrak kloroform daun pacar air (µg/ml)
terhadap % kematian sel vero ... 28 Gambar 9. Kurva log konsentrasi terhadap harga probit sel vero pada
replikasi I... 29 Gambar 10. Kurva log konsentrasi terhadap harga probit sel vero pada
replikasi II ... 29
Gambar 11. Kurva log konsentrasi terhadap harga probit sel vero pada replikasi III ... 30
xix
xx
DAFTAR LAMPIRAN
Halaman Lampiran 1. Foto tanaman dan daun pacar air (Impatiens balsaminaL.) .... 35
Lampiran 2. Perhitungan jumlah sel yang hidup ... 36
Lampiran 3. Perhitungan persentase kematian sel HeLa dan sel Vero ... 42 Lampiran 4. Perhitungan LC50dengan analisis probit dan
uji linearistas ... 46 Lampiran 5. Analisis statistik uji z pada kelompok kontrol dan
perlakuan ... 54
1 BAB I PENGANTAR A. Latar belakang
Kanker dapat menyerang siapa saja tanpa mengenal umur dan jenis
kelamin. Kanker merupakan salah satu penyebab kematian di dunia dan sebagian
besar terjadi di negara berkembang. Menurut data WHO yang diterbitkan pada tahun 2008, pada tahun 2005 sebanyak 7,6 juta kematian di dunia terjadi akibat
kanker (Anonim, 2008a). Di Indonesia sekitar 800.000 orang terserang kanker tiap tahunnya (Anonim, 2007).
Kanker serviks adalah kanker yang menyerang bagian ujung bawah rahim
yang menonjol ke vagina (liang senggama). Menurut data dari WHO, setiap tahun di seluruh dunia sebanyak 490 ribu perempuan didiagnosa menderita kanker
serviks (Anonim, 2008b). Hingga saat ini kanker serviks masih menduduki urutan pertama penyakit yang paling banyak menyerang wanita di Indonesia. Sementara
di dunia, penyakit kanker serviks ini terbanyak kedua setelah kanker payudara
(Mardiana, 2008).
Berbagai cara pengobatan telah dilakukan untuk mengobati penyakit
kanker, antara lain dengan menggunakan radiasi, kemoterapi, dan pembedahan (Diananda, 2008). Akan tetapi, pengobatan-pengobatan tersebut memiliki banyak
efek yang tidak menyenangkan dan biaya juga relatif mahal. Oleh karena itu,
2
Pengobatan tradisional menggunakan tanaman obat di masyarakat sudah cukup luas, salah satunya yaitu menggunakan tanaman pacar air. Tanaman pacar
air memiliki beberapa khasiat, antara lain untuk kanker pencernaan, bengkak, rematik, bisul, radang kulit, antiinflamasi (Arisandi dan Andriani, 2006).
Penelitian di Cina menunjukkan bahwa ekstrak kloroform daun pacar air
memiliki aktivitas antitumor terhadaphepatocelluler carcinoma cell line HepG2. Senyawa yang aktif telah diidentifikasi sebagai 2-methoxy-1,4-naphthoquinone
(Zhi-Shan, 2008). Sel HeLa memiliki persamaan dengan sel Hep G2 dimana kedua sel ini berasal dari suatu carcinoma dan penyebabnya adalah virus
(Anonim, 2008c dan Anonim, 2008d).
Untuk mengetahui apakah tanaman pacar air mempunyai khasiat sebagai antikanker terhadap sel HeLa, perlu dilakukan penelitian. Penelitian dilakukan
dengan menggunakan ekstrak kloroform dari daun pacar air dan diuji efek sitotoksiknya terhadap kultur sel HeLa dengan metode direct counting
menggunakan alat haemocytometer. Hasil penelitian diharapkan dapat menjadi
dasar untuk mengembangkan tanaman pacar air sebagai senyawa antikanker terutama terhadap sel HeLa.
1. Rumusan masalah
Berdasarkan latar belakang yang telah dipaparkan, maka dapat
dirumuskan permasalahan sebagai berikut:
3
b. seberapa besar harga LC50 dari ekstrak daun pacar air terhadap kultur sel HeLa dan sel Vero?
2. Keaslian penelitian
Belum pernah dilakukan penelitian mengenai sitotoksisitas ekstrak
kloroform daun pacar air terhadap kultur sel HeLa.
3. Manfaat penelitian a. manfaat teoritis
Penelitian ini dapat memberikan informasi tentang efek sitotoksisitas ekstrak kloroform daun pacar air terhadap sel HeLa dan melengkapi serta
memperkaya teori yang telah ada mengenai khasiat dari tanaman pacar air.
b. manfaat praktis
Penelitian ini diharapkan dapat membuktikan efek daun pacar air sebagai
antikanker.
B. Tujuan 1. Tujuan umum
Untuk mengetahui apakah ekstrak kloroform daun pacar air bersifat sitotoksik.
2. Tujuan khusus
a. untuk mengetahui apakah ekstrak kloroform daun pacar air memiliki efek
sitotoksik terhadap kultur sel HeLa dan sel Vero.
4 BAB II
PENELAAHAN PUSTAKA A. Tanaman Pacar Air 1. Keterangan Botani
Tanaman pacar air (Impatiens balsamina) termasuk dalam familia
Balsaminaceae (Backer dan Brink, 1965). Tanaman ini merupakan terna berbatang basah, bercabang, dengan daun tunggal, bentuk lanset memanjang
pinggir bergerigi warna hijau muda tanpa daun penumpu. Bunga berwarna cerah, ada beberapa macam warna, seperti merah, orange, ungu, putih. Ada yang
“engkel” dan yang “dobel”. Buahnya buah kendaga, bila masak akan membuka
menjadi 5 bagian yang terpilin. Biasanya ditanam sebagai tanaman hias dengan tinggi 30-80 cm (Arisandi dan Andriani, 2006).
2. Kandungan Kimia
Kandungan kimia pada tanaman pacar air , bunga:Anthocyanins,cyanidin,
delphinidin,pelargonidin, malvidin,kaempherol, quercetin; akar:cyanidin mono
-glycoside (Arisandi dan Andriani, 2006); Daun: 2-methoxy-1,4-naphthoquinone
yang diisolasi dalam suatu penelitian di Thailand (Thongnopnua et al, 1991).
Beberapa derivat dari naphthoquinone memiliki efek sitotoksik terhadap sel kanker, salah satunya yaitu plumbagin. Menurut penelitian yang dilakukan,
plumbaginmemiliki efek anti tumor terhadap sel kanker payudara (Ahmad et al,
5
3. Khasiat dan Penggunaan
Tanaman pacar air memiliki beberapa khasiat, antara lain untuk peluruh
haid, kanker pencernaan, bengkak, rematik, bisul, radang kulit, keputihan, tulang patah atau retak, antiinflamasi dan keputihan (Arisandi dan Andriani, 2006).
B. Kanker
Kanker adalah sekelompok penyakit yang ditandai dengan pertumbuhan sel yang tidak terkendali, invasi jaringan lokal dan migrasi sel ke tempat yang
jauh (metastasis). Tumor dapat berupa benign dan malignant. Tumor benign
bukan merupakan kanker, biasanya berkapsul dan terlokalisasi. Tumor ini jarang
mengalami metastasis dan ketika dihilangkan, jarang muncul lagi. Sebaliknya,
tumor malignant menginvasi dan merusak jaringan sekitarnya. Pada tumor
malignant cenderung terjadi metastasis sehingga kekambuhan biasanya terjadi
setelah penghilangan atau pengrusakan tumor primer (Balmer, Valley dan Iannucci, 2005).
1. Karsinogenesis
Karsinogenesis, proses terjadinya kanker, merupakan serangkaian mekanisme yang dihasilkan dari akumulasi kesalahan pada jalur pengaturan vital.
Hal ini dimulai ketika sel tunggal kemudian membelah dan mengalami perubahan sehingga dapat lebih bertahan daripada sel-sel sekitarnya. Sel yang telah berubah
ini menghasilkan jutaan sel yang pada akhirnya menimbulkan kanker (King,
6
2. Kanker serviks
Kanker serviks terjadi ketika sel pada serviks mengalami pertumbuhan
yang tidak terkontrol dan kemudian dapat menginvasi jaringan sekitarnya atau menyebar ke seluruh tubuh (Dolinsky dan Christine, 2008).
Kanker serviks kebanyakan terjadi sebagai suatu squamous carcinoma
sebanyak 95 % dan sedikit terjadi pada selendocervical columnal sebagai suatu
adenocarcinoma (5%). Faktor resiko terjadinya kanker serviks antara lain
berhubungan seks pada usia dini, pasangan seks berganti-ganti, perokok dan terpapar olehHuman Papilloma Virus(HPV) (King, 2000).
3. Sel HeLa
Sel HeLa adalah sel yang ditemukan pada kanker serviks yang menyebabkan kematian yang tinggi pada wanita. Sel ini diisolasi pertama kali
pada Februari 1951 dari seorang wanita yang bernama Henrietta Lacks di Baltimore. Sel HeLa merupakan sel epithelial dari carcinoma cervix yang
ditransformasi olehHuman Papilloma Virus (HPV)18 (Anonim, 2008c).
4. Sel Vero
Sel Vero diinisiasikan pada tahun 1962 terdapat dalam ginjal kera dewasa
7
C. Ekstraksi 1. Definisi ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang
sesuai, kemudian semua atau hampir semua pelarut diuapkan dari massa atau
serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang telah ditetapkan (Anonim, 1995).
2. Cairan pelarut
Cairan pelarut dalam proses pembuatan ekstrak adalah pelarut yang baik
(optimal) untuk senyawa kandungan yang berkhasiat atau yang aktif, dengan
demikian senyawa tersebut dapat terpisahkan dari bahan dan dari senyawa kandungan lainnya, serta ekstrak hanya mengandung sebagian besar senyawa
kandungan yang diinginkan. Faktor utama untuk pertimbangan pada pemilihan cairan penyari adalah sebagai berikut : selektivitas, kemudahan bekerja dan proses
dengan cairan tersebut, ekonomis, ramah lingkungan, dan keamanan (Anonim, 2000).
3. Ekstraksi
Ekstraksi merupakan kegiatan penarikan kandungan kimia yang dapat
larut sehingga terpisah dari bahan yang tidak larut dengan pelarut cair. Simplisia yang diekstrak mengandung senyawa aktif yang dapat larut dan senyawa tidak
dapat larut seperti serat, karbohidrat, protein dan lain-lain. Senyawa aktif yang
8
4. Maserasi
Maserasi adalah proses pengekstraksian simplisia dengan menggunakan
pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar) (Anonim, 2000). Cairan penyari akan menembus dinding sel dan
masuk ke dalam rongga sel yang mengandung zat aktif., zat aktif akan larut dan
karena adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan yang ada di luar sel, maka larutan yang terpekat didesak ke luar. Peristiwa tersebut
berulang sehingga terjadi keseimbangan konsentrasi antara larutan di luar sel dan di dalam sel. Keuntungan maserasi adalah cara pengerjaan dan peralatan yang
digunakan sederhana dan mudah diusahakan, kerugiannya adalah pengerjaannya
lama dan penyariannya kurang sempurna (Anonim, 1986).
D. Uji Sitotoksisitas
Sitotoksisitas adalah sifat toksik atau beracun suatu senyawa terhadap sel yang hidup. Uji sitotoksisitas adalah uji in vitro dengan menggunakan kultur sel
yang digunakan dalam evaluasi keamanan obat, kosmetika, zat tambahan
makanan, pestisida, dan digunakan juga untuk mendeteksi adanya aktivitas sitotoksik dari suatu senyawa. Sistem ini merupakan uji kualitatif dan kuantitatif
dengan cara menetapkan kematian sel (Freshney, 2000).
Metodedirect counting
Metode yang umum dan sering dipakai dalam penghitungan sel adalah
menggunakanhaemocytometerkarena keefisienan dan keakuratannya. Digunakan suatu chamber hitung yang kaku berbentuk kotak dan memiliki kedalaman 0,1
9
mikroskop dan sel dihitung pada sejumlah bilik yang dipilih. Dari perhitungan yang dilakukan, dapat ditentukan jumlah sel per ml dari suspensi. Untuk
mengetahui sel yang hidup dan yang mati dapat digunakan zat penanda seperti
trypan blue. Trypan blue hanya masuk ke membran sel mati sehingga sel yang
mati akan berwarna biru gelap (Doyle and Griffiths, 2000).
Suatu uji sitotoksisitas menggunakan metode BST menyatakan jika suatu uji sitotoksisitas menghasilkan harga LC50kurang dari 1000μg/ml maka senyawa
tersebut dinyatakan bersifat toksik dan bila lebih besar dari 1000 μg/ml maka senyawa tersebut dinyatakan tidak toksik terhadap senyawa uji Suatu senyawa
berpotensi sebagai antikanker bila memiliki harga LC50 ≤30 μg/ml (Meyer et al,
1982). National Cancer Institute (NCI) menyatakan jika uji sitotoksik suatu senyawa menghasilkan nilai LC50≤ 20 μg/ml, maka senyawa tersebut memiliki
potensi untuk dikembangkan sebagai senyawa antikanker (Suffness and Pezzuto, 1991 cit., Rahmawati, Katno dan Triyono, 2008).
E. Landasan Teori
Saat ini banyak tanaman yang dapat digunakan untuk mengobati kanker, salah satunya adalah daun pacar air. Berdasarkan penelitian di Thailand, suatu
senyawa yang diisolasi dari ekstrak daun pacar air mengandung 2-methoxy
-1,4-naphthoquinone (Thongnopnua et al, 1991). Senyawa ini merupakan derivat dari
naphthoquinone. Beberapa derivat dari naphthoquinone memiliki berbagai
aktivitas, antara lain adalah sebagai anti tumor.
Penelitian di Cina juga menunjukkan bahwa ekstrak kloroform daun pacar
10
HepG2. Senyawa yang aktif diisolasi dan diidentifikasi sebagai 2-methoxy
-1,4-napthoquinone(Zhi-Shan, 2008).
Berdasarkan penelitian tersebut, maka dilakukan penelitian dengan mengekstraksi daun pacar air menggunakan kloroform untuk melihat apakah
ekstrak tersebut memiliki efek sitotoksisitas terhadap sel HeLa, dimana sel HeLa
merupakan selepithelialdaricarcinoma cervix.
F. Hipotesis
11 BAB III
METODOLOGI PENELITIAN A. Jenis dan Rancangan Penelitian
Penelitian uji sitotoksisitas ekstrak kloroform daun pacar air terhadap
kultur sel HeLa ini termasuk penelitian eksperimental murni dengan rancangan
acak lengkap pola satu arah. Penelitian ini dilakukan di Laboratorium Penelitian dan Pengujian Terpadu UGM.
B. Variabel penelitian dan Definisi operasional 1. Variabel utama
a. Variabel Bebas
Kadar ekstrak kloroform daun pacar air yaitu 800 g/ml, 700 g/ml, 600
g/ml, 500 g/ml, 400 g/ml, 300 g/ml, 200 g/ml, 175 g/ml, 150 g/ml,
125g/ml, 100g/ml, 75g/ml, 50g/ml dan 25g/ml.
b. Variabel Tergantung
Persentase kematian kultur sel HeLa dan sel Vero.
2. Variabel pengacau terkendali
a. Medium tumbuh sel HeLa dikendalikan dengan menggunakan medium RPMI-1640 serum dan medium sel normal dengan medium M199 serum.
b. Tempat tumbuh dan waktu pemanenan daun pacar air dikendalikan dengan memanen daun pada tempat dan waktu yang sama.
3. Definisi operasional
12
b. Ekstrak kloroform daun pacar air adalah ektrak yang diperoleh dengan mengekstraksi secara maserasi serbuk kering daun pacar air dengan
menggunakan pelarut kloroform.
C. Alat dan Bahan 1. Alat
Peralatan yang digunakan dalam penelitian ini terdiri atas : alat-alat gelas, oven, mesin serbuk, filter, timbangan analitik (Mettler Toledo), alumunium
foil, autoklaf, tissue culture flask, tabung conical (Nunc), swing rotor sentrifuge
(PLC), inkubator (Memmert), mikropipet, lemari pendingin (Sharp), 96-well plate
(NunclonTM), laminar air flow (LabconcoR), mikroskop (Olympus),
haemocytometer (Neubauer Improved), yellowtip, bluetip, tabung effendorf, tissue, sarung tangan dan masker.
2. Bahan
Bahan-bahan yang digunakan dalam penelitian ini ialah :
a. Daun pacar air segar
b. Kultur sel HeLa yang diambil dari stok di LPPT Universitas Gadjah Mada, Yogyakarta.
c. Kultur sel Vero yang diambil dari stok LPPT Universitas Gadjah Mada, Yogyakarta
d. Larutan penyari yang digunakan dalam preparasi ekstrak kloroform daun
pacar air (Impatiens balsamina)
13
f. Medium penumbuh : RPMI-1640, Natrium Bikarbonat, HEPES, FBS (Foetal Bovine Serum) 10%, Penisilin-Streptomisin 1%, dan Fungison 0,5%.
g. Tripsin 0,25%
h. Reagen Pewarna :Trypan Blue
i. Aquabidest
j. Dimethyl Sulfoxide (DMSO) 0,25%
D. Tata Cara Penelitian 1. Determinasi tanaman
Determinasi daun pacar air dilakukan di Laboratorium Farmakognosi
Fitokimia, Fakultas Sanata Dharma, Yogyakarta menggunakan acuan baku
(Backer dan Brink, 1965).
2. Pengumpulan bahan
Daun pacar air yang digunakan untuk penelitian diambil pada daerah Tajem, Sleman. Daun segar pacar air diseleksi, dicuci dengan air mengalir untuk
menghilangkan kotoran-kotoran yang melekat, kemudian ditiriskan hingga
kandungan air hilang. Daun dijemur di bawah sinar matahari yang ditutupi oleh kain berwarna gelap kemudian dimasukkan ke dalam oven pada suhu 45oC selama
12 jam. Setelah benar-benar kering, daun kemudian diserbuk menggunakan mesin hingga diperoleh serbuk dengan ukuran 65 mesh.
3. Ekstraksi
Serbuk kering daun pacar air ditimbang, dibungkus dalam kertas dan dimasukkan ke dalam tabung erlenmeyer dan ditambahkan dengan penyari ke
14
digunakan yaitu kloroform dan proses ekstraksi yang digunakan pada penelitian ini adalah maserasi. Ekstrak yang didapat selanjutnya dilakukan penguapan
dengan vacum rotary evaporator hingga didapat ekstrak kental. Ekstrak kental yang didapat dilanjutkan dengan penguapan di atas oven hingga kloroform
menguap semua.
4. Pembuatan medium pencuci dan medium penumbuh a. Pembuatan medium pencuci
RPMI 1640 dilarutkan dalam aquabidest kurang lebih 80 ml, ditambah 2,3 g natrium bikarbonat, 2 g HEPES [4-(2-Hidroxyethyl)-1-piperazine ethane
sulphonic acid], diencerkan sampai 100 ml, pH dibuat 7,2, lalu disterilkan dengan
filter berdiameter 0,22 μm. Medium disimpan dalam almari es pada suhu 4oC (Freshney, 1986; Jacoby dan Pastan, 1979).
b. Pembuatan medium kultur (RPMI 1640-serum)
Untuk medium RPMI 1640-serum, RPMI 1640 dilarutkan dalam
aquabidest kurang lebih 80 ml, ditambah 2,3 g natrium bikarbonat, 2 g HEPES
[4-(2-Hidroxyethyl)-1-piperazine ethane sulphonic acid], diencerkan sampai 100 ml, pH dibuat 7,2, ditambahkan FBS (Foetal Bovine Serum) 10%,
penisilin-streptomisin 1% dan fungison 0,5% dalam medium RPMI 1640 dan disterilkan dengan filter berdiameter 0,22 μm. Media disimpan dalam almari es pada suhu
15
5. Propagasi dan panen sel HeLa a. Propagasi sel HeLa
Sel diambil dari tangki nitrogen cair, kemudian segera dicairkan dalam penangas air 37oC, kemudian ampul disemprot dengan etanol 70%. Ampul dibuka
dan sel HeLa dipindahkan dalam tabung conical steril yang berisi medium RPMI
1640. Suspensi sel disentrifugasi selama 5 menit, supernatan dibuang, diganti dengan medium RPMI yang baru, kemudian disuspensikan perlahan. Suspensi sel
lalu disentrifugasi kembali selama 5 menit kemudian dicuci ulang sekali lagi. Supernatan dibuang, pelet ditambahkan 1 ml medium penumbuh yang
mengandung 10% FBS. Resuspensikan secara perlahan sampai homogen,
kemudian sel ditumbuhkan dalam tissue culture flask kecil dan diinkubasikan dalam inkubator dengan suhu 37oC dengan aliran 5% CO2. Setelah 24 jam,
medium penumbuh diganti dan sel ditumbuhkan hingga konfluen dan jumlahnya cukup untuk penelitian (Freshney, 1986; Jacoby dan Pastan, 1979).
b. Panen sel HeLa
Setelah jumlah sel cukup (kurang lebih setelah berumur 7 hari), medium diganti dengan RPMI-1640 baru sebanyak 5 ml kemudian sel dilepaskan dari
dinding flask dengan cara diberi tripsin. Sel dipindahkan dalam tabung conical
steril dan ditambahkan medium RPMI-1640 sampai volume 10 ml dan
disentrifugasi dengan kecepatan 3000 rpm selama 5 menit. Supernatan dibuang
16
sehingga memperoleh konsentrasi sel sebesar 2 x104/100 μl dan siap dipakai untuk penelitian (Freshney, 1986; Jacoby dan Pastan, 1979).
6. Propagasi dan panen sel normal
Sel normal yang digunakan dalam penelitian ini adalah sel Vero.
Propagasi dan panen sel Vero menggunakan langkah yang sama dengan propagasi
dan panen sel HeLa. Perbedaannya hanya terletak pada medium yang digunakan. Sel Vero menggunakan medium M199.
7. Uji sitotoksisitas ekstrak kloroform daun pacar air
Pada uji sitotoksisitas, sebanyak 100 µl suspensi sel HeLa dengan
kepadatan 2x104 sel/100 µl dimasukkan dalam sumuran-sumuran 96-well plate
yang telah berisi 100 µl ekstrak kloroform daun pacar air dengan kadar 200
g/ml, 175g/ml, 150 g/ml, 125 g/ml, 100g/ml, 75g/ml, 50g/ml dan 25
g/ml dan untuk sel vero, kadar ekstrak kloroform daun pacar air yang digunakan
yaitu 800 g/ml, 700 g/ml, 600 g/ml, 500 g/ml, 400 g/ml, 300 g/ml, 200
g/ml dan 100 g/ml. Untuk kontrol, digunakan 100 μl suspensi sel dan
ditambahkan medium. Selanjutnya plate diinkubasikan selama 24 jam pada suhu 37oC, dalam incubator dengan aliran 5% CO2(Freshney, 1986; Jacoby dan Pastan,
1979). Pada akhir masa inkubasi, tiap sumuran sel diresuspensi, kemudian
ditambahkan 100 l trypan blue. Pipet 10 μl tiap sumuran dan masukkan dalam
haemocytometer. Hitung jumlah sel hidup dan mati pada tiap konsentrasi dan
kontrol di bawah mikroskop. Sel yang hidup akan tampak relatif bulat transparan. Sedangkan sel yang mati akan tampak gelap dan tidak cemerlang (Doyle and
17
E. Analisis Hasil
Analisis hasil dilakukan dengan perhitungan persentase kematian sel
dengan rumus :
% kematian =
A B
A )
(
x 100%
Keterangan:
A : jumlah sel yang hidup pada sumuran kontrol media
B : jumlah sel yang hidup pada sumuran yang telah diberi perlakuan ekstrak
kloroform daun pacar air
Untuk menghitung harga LC50 dilakukan perhitungan menggunakan analisis probit sedangkan untuk menganalisis signifikansi antara perlakuan dan
kontrol dilakukan pengolahan data statistik uji z. Untuk menganalisis signifikansi antara LC50 sel HeLa dan sel Vero digunakan analisis statistik uji t sampel
18 BAB IV
HASIL DAN PEMBAHASAN A. Determinasi Tanaman
Bahan utama yang digunakan dalam penelitian adalah daun pacar air.
Untuk memastikan identitas tanaman uji dan menghindari terjadinya kesalahan
dalam pengambilan tanaman uji maka dilakukan determinasi tanaman. Determinasi dilakukan dengan mencocokkan tanaman dengan kunci determinasi
(Backer dan Brink, 1965).
Determinasi dilakukan di Laboratorium Farmakognosi Fitokimia, Fakultas
Farmasi, Universitas Sanata Dharma, Yogyakarta. Hasil determinasi menyatakan
bahwa tanaman yang digunakan dalam penelitian ini adalah benar Impatiens balsamina(Lampiran 7).
B. Pengumpulan Daun Pacar Air
Daun pacar air yang digunakan diambil dari tanaman pacar air yang
tumbuh di daerah Tajem, Sleman pada bulan Agustus 2008. Daun pacar air yang
akan digunakan perlu dicuci dengan air mengalir untuk membersihkan kotoran dan debu yang menempel pada permukaan daun.
Pembuatan simplisia daun pacar air dilakukan dengan pengeringan menggunakan oven pada suhu 450C selama 12 jam. Pengeringan dilakukan untuk
mencegah kerusakan simplisia karena air merupakan media pertumbuhan kapang
19
ini bertujuan untuk memperkecil ukuran partikel sehingga memperluas area kontak daun terhadap pelarut pada proses ekstraksi.
C. Ekstraksi
Bahan uji yang digunakan dalam penelitian ini adalah ekstrak kloroform
daun pacar air. Ekstraksi dilakukan secara maserasi dengan larutan penyari
klorofom. Pada metode ini sampel direndam dalam larutan penyari pada suhu ruangan. Perendaman menyebabkan cairan penyari menembus dinding sel
sehingga dapat melarutkan zat aktif. Adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan yang ada di luar sel menyebabkan zat aktif yang ada
di dalam sel akan terdesak ke luar sel. Peristiwa ini akan terjadi terus menerus
hingga terjadi keseimbangan antara konsentrasi larutan di dalam sel dan luar sel. Pemilihan larutan penyari dilakukan berdasarkan kelarutan dari senyawa
aktif yang diinginkan. Dalam penelitian ini, senyawa yang akan diuji adalah naftokuinon dimana senyawa tersebut larut dalam kloroform, sehingga larutan
penyari yang digunakan adalah kloroform. Metode maserasi tidak menggunakan
panas sehingga zat aktif yang termolabil tidak rusak.
D. Pembuatan Medium Pencuci dan Medium Penumbuh
Dalam penelitian digunakan 2 macam medium yaitu : medium pencuci dan medium penumbuh. Medium pencuci untuk sel HeLa adalah RPMI-1640
ditambah HEPES dan natrium bikarbonat.
Medium penumbuh mengandung RPMI-1640, natrium bikarbonat, HEPES, FBS (Foetal Bovine Serum) 10%, penisilin-streptomisin 0,5%, dan
20
karena mampu mendukung nutrisi pertumbuhan pada kultur sel HeLa. Medium pencuci dan penumbuh untuk sel Vero juga sama, namun yang berbeda adalah
mediumnya yaitu M199.
Dalam medium, kombinasi antibiotik penisilin-streptomisin digunakan
untuk menghindari kontaminan bakteri, baik gram positif maupun negatif. Selain
itu, fungison dalam medium digunakan untuk menjaga agar medium bebas dari kontaminan jamur. Medium kultur yang digunakan harus bebas dari kontaminan
agar pertumbuhan kultur sel tidak terhambat akibat adanya persaingan mendapatkan nutrisi.
E. Propagasi dan Panen Sel HeLa
Sel HeLa yang akan digunakan disimpan dan dibekukan dalam tangki nitrogen cair agar kondisi sel tetap normal. Medium sel juga harus diganti secara
rutin. Medium diganti pada saat medium yang berwarna merah berubah menjadi oranye hingga kuning.
Sel HeLa dipanen pada saat konfluen dan jumlahnya telah mencukupi
untuk digunakan dalam penelitian. Sel HeLa diresuspensikan dengan medium dan medium dibuang. Setelah itu, sel diberi tripsin agar terlepas dari dinding flask dan
disentrifugasi, supernatan dibuang. Sel yang diperoleh, dihitung jumlahnya menggunakanhaemocytometer.
F. Propagasi dan Panen Sel Vero
21
menggunakan langkah yang sama dengan sel HeLa, namun yang berbeda adalah mediumnya. Medium untuk sel Vero adalah M199.
G. Uji Sitotoksisitas Ekstrak Kloroform Daun Pacar Air
Uji sitotoksisitas dilakukan untuk mengetahui potensi ketoksikan ekstrak
kloroform daun pacar air terhadap kultur sel HeLa. Hasil dari uji sitotoksisitas
dapat digunakan untuk menentukan LC50, yaitu konsentrasi ekstrak kloroform daun pacar air yang mampu mematikan 50% populasi kultur sel HeLa.
Uji sitotoksisitas dilakukan menggunakan metode perhitungan langsung dengan haemocytometer. Dalam metode ini pengamatan dilakukan langsung di
bawah mikroskop. Untuk membedakan sel mati dan hidup maka sel akan diberi
pewarna trypan blue dimana trypan blue masuk ke membran sel yang mati sehingga sel yang mati akan tampak lebih gelap sedangkan sel yang hidup relatif
bulat dan transparan (gambar 1).
Sebelum sel diberi trypan blue, terlebih dahulu dilakukan pengamatan
morfologi sel di bawah mikroskop. Sel yang hidup akan tampak bulat, bening,
22
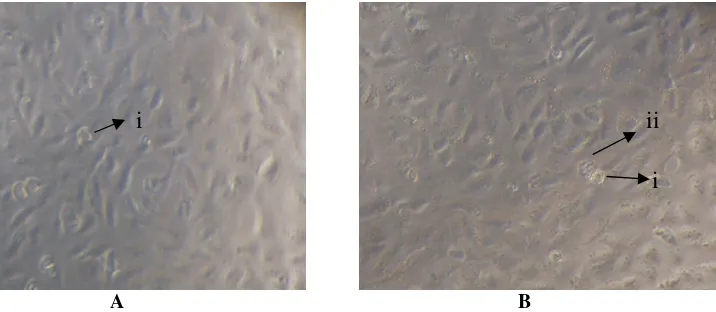
i
ii
Gambar 1. Kultur sel HeLa dihaemocytometer setelah diberitrypan blueKet. : i = sel HeLa hidup dan ii = sel HeLa mati
i
i
ii
A B
Gambar 2. Kultur sel HeLa di sumuran (perbesaran 100x). A : sel HeLa tanpa perlakuan (kontrol), B : sel HeLa diberi ekstrak kloroform daun pacar air konsentrasi 100 µg/ml
Ket. i = sel hidup dan ii = sel mati
i ii
i
A B
Gambar 3. Kultur sel Vero di sumuran (perbesaran 100x). A : sel Vero tanpa perlakuan (kontrol), B : sel Vero diberi ekstrak kloroform daun pacar air konsentrasi 100 µg/ml
23
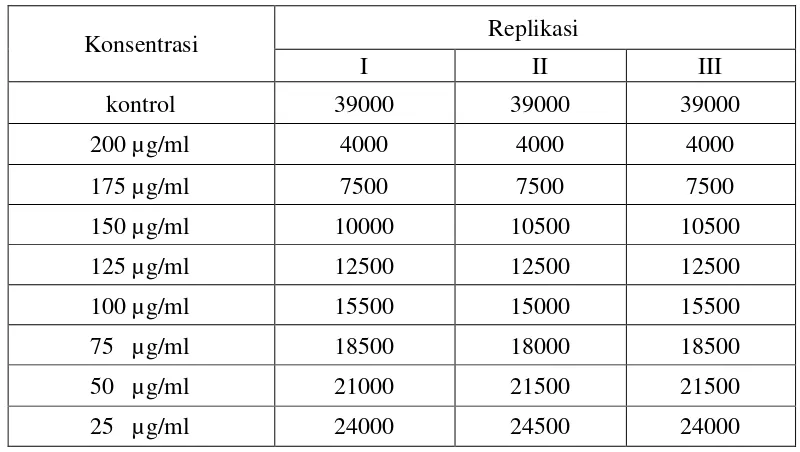
Tabel I. Jumlah Sel yang Hidup dari Tiap Sumuran pada Berbagai Tingkat Konsentrasi Ekstrak klroform daun pacar air dengan Metode Direct Counting
Konsentrasi Replikasi
I II III
kontrol 39000 39000 39000
200 µg/ml 4000 4000 4000
175 µg/ml 7500 7500 7500
150 µg/ml 10000 10500 10500
125 µg/ml 12500 12500 12500
100 µg/ml 15500 15000 15500
75 µg/ml 18500 18000 18500
50 µg/ml 21000 21500 21500
25 µg/ml 24000 24500 24000
Dari hasil yang diperoleh (tabel I), maka dapat dihitung persentase kematian sel
HeLa dengan pengurangan jumlah sel HeLa hidup pada kelompok kontrol dengan jumlah sel HeLa hidup pada kelompok perlakuan dibagi jumlah sel HeLa hidup
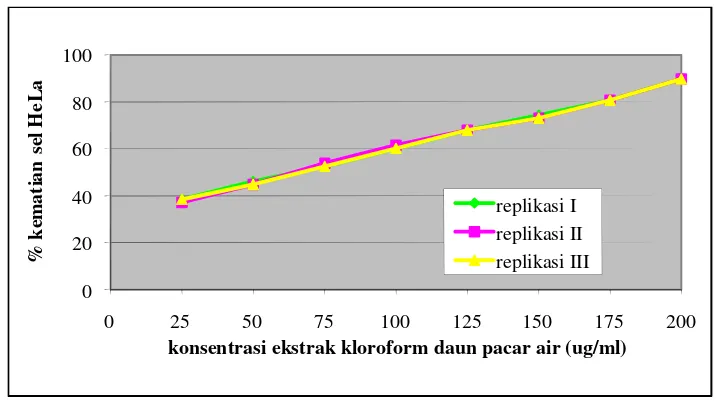
pada kelompok kontrol. Persentase kematian sel HeLa semakin meningkat dengan
meningkatnya konsentrasi ekstrak kloroform daun pacar air (gambar 4).
Tabel II. % kematian sel HeLa pada berbagai konsentrasi ekstrak kloroform daun pacar air
Konsentrasi % kematian sel HeLa
Replikasi I Replikasi II Replikasi III
25 µg/ml 38,46 37,18 38,46
50 µg/ml 46,15 44,87 44,87
75 µg/ml 52,56 53,85 52,56
100 µg/ml 60,26 61,54 60,26
125 µg/ml 67,95 67,95 67,95
150 µg/ml 74,36 73,08 73,08
175 µg/ml 80,77 80,77 80,77
24
Gambar 4. Grafik konsentrasi ekstrak kloroform daun pacar air (µg/ml) terhadap % kematian sel HeLa
Dalam penelitian ini digunakan kontrol normal yaitu sel HeLa ditumbuhkan dalam medium tanpa diberi perlakuan. Kontrol normal digunakan
dengan tujuan untuk mengetahui efek sitotoksik ekstrak kloroform daun pacar air
terhadap sel HeLa. Analisis dilakukan dengan membandingkan jumlah sel hidup dan mati pada kelompok kontrol terhadap kelompok perlakuan, apakah terdapat
perbedaan yang signifikan atau tidak. Hasil penelitian dianalisis secara statistik dengan uji z yang dihitung secara manual.
Analisis menggunakan uji z dengan α = 0,05 memperoleh hasil
perhitungan yang menunjukkan z hitung > z tabel sehingga H0 ditolak. Jadi, hasil perhitungan menunjukkan terdapat perbedaan yang signifikan antara jumlah sel
hidup kelompok kontrol dan perlakuan (Lampiran 5). Dengan demikian dapat dikatakan bahwa sel yang mati merupakan akibat dari perlakuan yang diberikan
dalam penelitian ini yaitu pemberian ekstrak kloroform daun pacar air ke sel.
0
konsentrasi ekstrak kloroform daun pacar air (ug/ml)
25
Untuk memperoleh LC50 ekstrak kloroform daun pacar air terhadap sel HeLa, maka dilakukan analisis probit. Analisis probit merupakan analisis regresi
antara log konsentrasi dengan harga probit. Pada analisis regresi perlu dilakukan uji linearitas (Lampiran 4). Hasil uji linearitas menunjukkan r hitung > r tabel
yaitu grafik replikasi I linier terhadap persamaan garis y = 1,61x + 2,22 (gambar
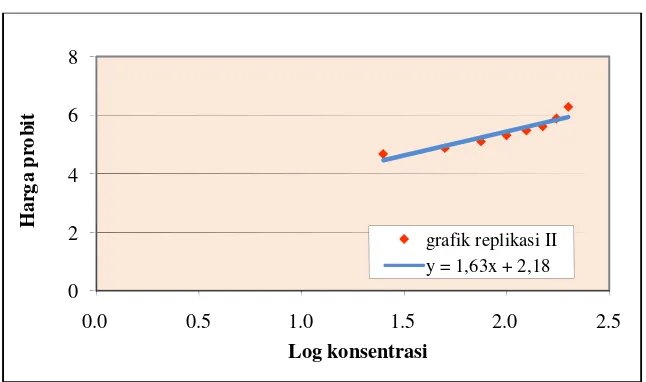
5) yaitu grafik replikasi II linier terhadap persamaan garis y = 1,63x + 2,18 (gambar 6) dan grafik replikasi III linier terhadap persamaan y = 1,61x + 2,21
(gambar 7)
Gambar 5. Grafik log konsentrasi terhadap harga probit pada replikasi I
Gambar 6. Grafik log konsentrasi terhadap harga probit pada replikasi II
0
grafik replikasi I y = 1,61x + 2,22
26
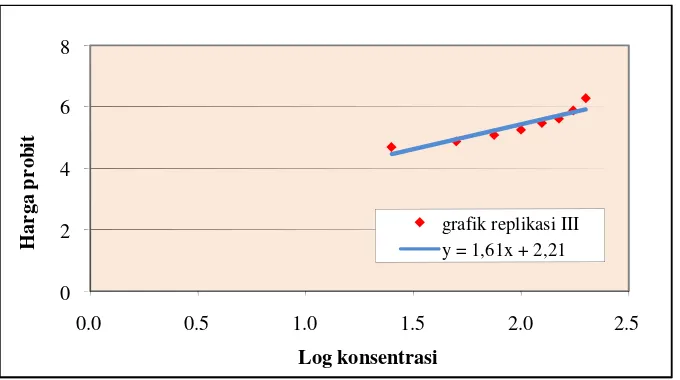
Gambar 7. Grafik log konsentrasi terhadap harga probit pada replikasi III
Perhitungan dengan analisis probit memperoleh LC50 ekstrak kloroform
daun pacar air terhadap sel HeLa sebesar 53,7 µg/ml dimana nilai LC50 tersebut > 20 µg/ml. Semakin kecil LC50 suatu senyawa maka semakin toksik senyawa
tersebut. Penelitian sitotoksisitas ekstrak kloroform daun pacar air juga dilakukan
terhadap kultur sel lain dengan nilai LC50 sebesar 52,5 µg/ml pada sel SiHa (Adhitama, 2009) dan 33,9 µg/ml pada sel T47D (Anni, 2009).
Untuk mengetahui apakah ekstrak kloroform daun pacar air juga bersifat sitotoksik terhadap sel normal, maka ekstrak tersebut juga diujikan pada sel Vero
sebagai sel normal. 0 2 4 6 8
0.0 0.5 1.0 1.5 2.0 2.5
H
a
r
g
a
p
r
o
b
it
Log konsentrasi
27
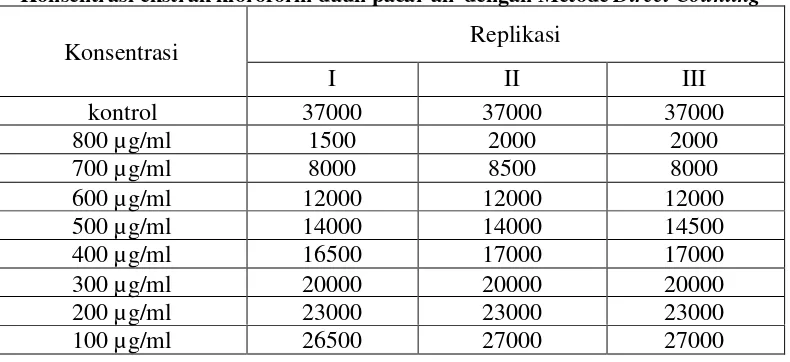
Tabel III. Jumlah Sel Vero yang Hidup dari Tiap Sumuran pada Berbagai Tingkat Konsentrasi ekstrak kloroform daun pacar air dengan MetodeDirect Counting
Konsentrasi Replikasi
I II III
kontrol 37000 37000 37000
800 µg/ml 1500 2000 2000
700 µg/ml 8000 8500 8000
600 µg/ml 12000 12000 12000
500 µg/ml 14000 14000 14500
400 µg/ml 16500 17000 17000
300 µg/ml 20000 20000 20000
200 µg/ml 23000 23000 23000
100 µg/ml 26500 27000 27000
Dari data di atas (tabel III), dapat dihitung persentase kematian sel Vero dengan
persentase kematian sel Vero dengan pengurangan jumlah sel Vero hidup pada kelompok kontrol dengan jumlah sel Vero hidup pada kelompok perlakuan dibagi
jumlah sel Vero hidup pada kelompok kontrol. Persentase kematian sel Vero semakin meningkat dengan meningkatnya konsentrasi ekstrak kloroform daun
28
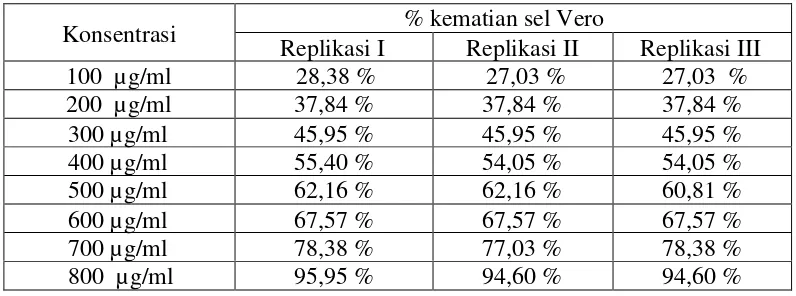
Tabel IV. % kematian sel Vero pada berbagai konsentrasi ekstrak kloroform daun pacar air
Konsentrasi % kematian sel Vero
Replikasi I Replikasi II Replikasi III
100 µg/ml 28,38 % 27,03 % 27,03 %
Gambar 8. Grafik konsentrasi ekstrak kloroform daun pacar air (µg/ml) terhadap % kematian sel Vero
Potensi ketoksikan (LC50) sel Vero dapat diperoleh dengan menggunakan analisis probit sehingga dapat dibandingkan dengan LC50 pada sel HeLa. Hasil
pengujian linearitas pada analisis probit sel Vero menunjukkan bahwa grafik
replikasi I linier terhadap persamaan garis y = 2,05x + 0,02 (gambar 9), grafik replikasi II linier terhadap persamaan garis y = 2,01x + 0,10 (gambar 10) dan
0
konsentrasi ekstrak kloroform daun pacar air (ug/ml)
29
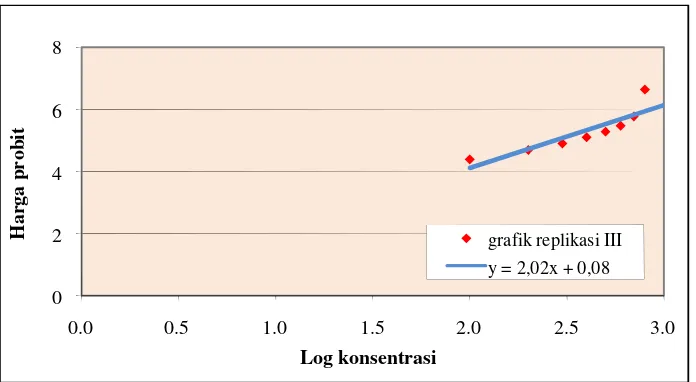
grafik replikasi III linier terhadap persamaan garis y = 2,02x + 0,08 (gambar 11). Harga LC50 ekstrak kloroform daun pacar air terhadap kultur sel Vero adalah
275,4 µg/ml.
Gambar 9. Kurva log konsentrasi terhadap harga probit sel Vero pada replikasi I
Gambar 10. Kurva log konsentrasi terhadap harga probit sel Vero pada replikasi II
0
grafik replikasi I y = 2,05x + 0,02
30
Gambar 11. Kurva log konsentrasi terhadap harga probit sel Vero pada replikasi III
Untuk mengetahui apakah terdapat perbedaan antara LC50 sel Vero dan LC50 sel HeLa digunakan analisis statistik uji t sampel independen pada taraf
kepercayaan 95%. Hasil yang diperoleh dari uji t sampel independen menunjukkan bahwa terdapat perbedaan bermakna antara LC50 sel Vero dan LC50
sel HeLa (lampiran 6). Oleh karena itu, ekstrak kloroform daun pacar air
memiliki potensi untuk dikembangkan sebagai agen antikanker.
0 2 4 6 8
0.0 0.5 1.0 1.5 2.0 2.5 3.0
H
a
rg
a
p
r
o
b
it
Log konsentrasi
31 BAB V
KESIMPULAN DAN SARAN A. Kesimpulan
Dari data yang diperoleh dan analisis yang dilakukan, maka dapat disimpulkan bahwa :
1. Ekstrak kloroform daun pacar air memiliki efek sitotoksik terhadap kultur sel
HeLa dan Vero.
2. Harga LC50 ekstrak kloroform daun pacar air terhadap kultur sel HeLa adalah
53,7 µg/ml dan 275,4 µg/ml terhadap kultur sel Vero sehingga esktrak ini memiliki potensi untuk dikembangkan sebagai agen anti kanker.
B. Saran
Dari hasil penelitian tersebut, maka disarankan :
1. Penelitian lebih lanjut mengenai efek sitotoksisitas fraksi dari ekstrak
kloroform daun pacar air terhadap sel HeLa.
2. Penelitian lebih lanjut mengenai mekanisme kematian sel HeLa oleh ekstrak
32
DAFTAR PUSTAKA
Adhitama, W., 2009, Uji Sitotoksisitas Ekstrak Kloroform Daun Pacar Air (Impatiens balsamina L.) terhadap Kultur Sel SiHa, Skripsi, Fakultas Farmasi USD, Yogyakarta
Anni, 2009, Uji Sitotoksisitas Ekstrak Kloroform Daun Pacar Air (Impatiens balsamina L.) terhadap Kultur Sel T47D, Skripsi,Fakultas Farmasi USD, Yogyakarta
Anonim, 1986, Sediaan Galenik, 10-16, Departemen Kesehatan Repubilik Indonesia, Jakarta
Anonim, 1995, Farmakope Indonesia, edisi V, 7, Departemen Kesehatan Indonesia, Jakarta
Anonim, 2000,Parameter Standart Umum Ekstrak Tumbuhan Obat, cetakan 1,1-61 departemen kesehatan repubilik Indonesia, Jakarta
Anonim, 2007, 800.000 Orang Indonesia Terserang Kanker Tiap Tahun, http://www.suarapembaruan.com/News/2007/05/14/Utama/ut01.htm, diakses tanggal 1 Agustus 2008
Anonim, 2008a, Cancer, http://www.who.int/cancer/en/, diakses tanggal 1 Agustus 2008
Anonim, 2008b, Angka Kematian Kanker Leher Rahim Masih Tinggi,
http://www.indofamilyhealth.com/index2.php?option=com_content&do_p df=1&id=518,diakses tanggal 20 Maret 2009
Anonim, 2008c, Cell Biology, http://www.atcc.org/ATCCAdvancedCatalog Search/ProductDetails/tabid/452/Default.aspx?ATCCNum=CCL2&Templ ate=cellBiology, diakses tanggal 28 Maret 2009
Anonim, 2008d, Cell Biology, http://www.atcc.org/ATCCAdvancedCatalog Search/ProductDetails/tabid/452/Default.aspx?ATCCNum=CRL-10741& Template=cellBiology,diakses tanggal 10 Mei 2009
Arisandi, Y., dan Andriani, Y., 2006, Khasiat Berbagai Tanaman untuk Pengobatan,Eska media, Jakarta
33
Balmer, C.M., Valley, A.W., Iannucci, A., 2005, Pharmacotherapy : A Pathophysiologic Approach, sixth edition, 2280, 2285-2286, McGraw-Hill, USA
Diananda, R, 2008, Mengenal Seluk-Beluk Kanker, 28-31, 43-46, Katahati, Yogyakarta
Dolinsky, C., and Christine Hill-Kayser , 2008, Cervical Cancer: The Basics, http://www.oncolink.org/types/article.cfm?c=6&s=17&ss=129&id=8226, diakses tanggal 7 April 2009
Doyle, A., and Griffiths, J.B., 2000, Cell and Tissue Culture For Medical Researh, 49, 155, John Willey and Sons Ltd, New York
Freshney, R.I., 1986,Animal Cell Culture A Practical Approach, second edition, 71-73, IRL Press Ltd, Washington DC.
Freshney, R. I., 2000,Culture f Animal Cells : A Manual of Basic Technique, 14th Edition, 336-338, John Wiley and Sons Inc., New York
Jacoby, W.B., and Pastan, I.H., 1979, Methods in Enzymology Cell Culture, Volume VIII, Academia Press Inc, New York
King, R.J.B., 2000, Cancer Biology, 2ndedition, School of Biological Sciences, University of Surrey, England
Mardiana, L., 2008, Kanker pada Wanita: Seri Agrisehat, 18, Penebar Swadaya, Jakarta
Meyer, B.N., Ferrigni, N.R., Putnam, J.E., Jacobsen, L.B., Nochols, D.E., Mc Laughlin, J.L., 1982, Brine Shrimp: A Convenient General Bioassay for Active Plant Concenient,Planta Medica, 45; 32-34
Rahmawati, N., Katno dan Triyono, A., 2008, Uji Efek Sitotoksik Ekstrak Etanolik Daun Bandotan (Ageratum conzoides L.) terhadap Sel HeLa,
Jurnal Tumbuhan Obat Indonesia, Vol.1, No.1, 51
34
35
Lampiran 1. Foto tanaman dan daun pacar air (Impatiens balsaminaL.)
Gambar 12. Foto tanaman pacar air
36
Lampiran 2. Perhitungan Jumlah kultur sel yang hidup
Tabel V. Data perhitungan jumlah kultur sel HeLa dengan perhitungan langsung
Konsentrasi
Replikasi
I II III
Hidup Mati Hidup Mati Hidup Mati
kontrol 78 0 78 0 78 0
200 µg/ml 8 31 8 33 8 33
175 µg/ml 15 29 15 29 15 29
150 µg/ml 20 27 21 27 21 27
125 µg/ml 25 25 25 25 25 25
100 µg/ml 31 22 30 22 31 22
75 µg/ml 37 19 36 19 37 19
50 µg/ml 42 16 43 15 43 15
37
Tabel VI . Data perhitungan jumlah kultur sel Vero dengan perhitungan langsung
Jumlah kultur sel yang hidup dan mati dari tiap sumuran dapat dihitung dengan
rumus :
Jumlah sel/sumuran = 4
x
x 10 x 200
Keterangan :
x = jumlah sel hasil perhitungan langsung padahaemocytometer
4 = jumlah bilik dalamhaemocytometer
10 = jumlah volume yang masuk dalam bilikhaemocytometer(10 µl)
200 = jumlah volume total (200 µl) Konsentrasi
Replikasi
I II III
Hidup Mati Hidup Mati Hidup Mati
kontrol 74 0 74 0 74 0
800 µg/ml 3 38 4 37 4 37
700 µg/ml 16 31 17 30 16 29
600 µg/ml 24 24 24 24 24 24
500 µg/ml 28 21 28 21 29 20
400 µg/ml 33 18 34 18 34 18
300 µg/ml 40 16 40 16 40 16
200 µg/ml 46 13 46 12 46 13
38
Perhitungan jumlah sel HeLa yang hidup pada tiap sumuran 1. Kontrol
Replikasi I = 784 x 10 x 200 = 39000
Replikasi II = 784 x 10 x 200 = 39000
Replikasi III =78
4 x 10 x 200 = 39000
2. Konsentrasi 200 µg/ml
Replikasi I = 84x 10 x 200 = 4000
Replikasi II = 8
4x 10 x 200 = 4000
Replikasi III =84x 10 x 200 = 4000
3. Konsentrasi 175 µg/ml Replikasi I = 15
4 x 10 x 200 = 7500
Replikasi II = 154 x 10 x 200 = 7500
Replikasi III =154 x 10 x 200 = 7500
4. Konsentrasi 150 µg/ml
Replikasi I = 204 x 10 x 200 = 10000
Replikasi II = 214 x 10 x 200 = 10500
Replikasi III =214 x 10 x 200 = 10500
5. Konsentrasi 125 µg/ml
Replikasi I = 254 x 10 x 200 = 12500
39
Replikasi III =254 x 10 x 200 = 12500
6. Konsentrasi 100 µg/ml
Replikasi I = 314 x 10 x 200 = 15500
Replikasi II = 304 x 10 x 200 = 15000
Replikasi III =314 x 10 x 200 = 15500
7. Konsentrasi 75 µg/ml Replikasi I = 37
4 x 10 x 200 = 18500
Replikasi II = 364 x 10 x 200 = 18000
Replikasi III =374 x 10 x 200 = 18500
8. Konsentrasi 50 µg/ml
Replikasi I = 424 x 10 x 200 = 21000
Replikasi II = 43
4 x 10 x 200 = 21500
Replikasi III =434 x 10 x 200 = 21500
9. Konsentrasi 25 µg/ml Replikasi I = 48
4 x 10 x 200 = 24000
Replikasi II = 494 x 10 x 200 = 24500
40
Perhitungan jumlah sel Vero yang hidup pada tiap sumuran 1. Kontrol
Replikasi I = 744 x 10 x 200 = 37000
Replikasi II =744 x 10 x 200 = 37000
Replikasi III = 74
4 x 10 x 200 = 37000
2. Konsentrasi 800 µg/ml
Replikasi I = 34x 10 x 200 = 1500
Replikasi II = 44x 10 x 200 = 2000
Replikasi III =44x 10 x 200 = 2000
3. Konsentrasi 700 µg/ml
Replikasi I = 164 x 10 x 200 = 8000
Replikasi II = 174 x 10 x 200 = 8500
Replikasi III =164 x 10 x 200 = 8000
4. Konsentrasi 600 µg/ml
Replikasi I = 244 x 10 x 200 = 12000
Replikasi II = 244 x 10 x 200 = 12000
Replikasi III =244 x 10 x 200 = 12000
5. Konsentrasi 500 µg/ml
Replikasi I = 284 x 10 x 200 = 14000
41
Replikasi III =29
4 x 10 x 200 = 14500
6. Konsentrasi 400 µg/ml
Replikasi I = 334 x 10 x 200 = 16500
Replikasi II = 34
4 x 10 x 200 = 17000
Replikasi III =344 x 10 x 200 = 17000
7. Konsentrasi 300 µg/ml Replikasi I = 40
4 x 10 x 200 = 20000
Replikasi II = 404 x 10 x 200 = 20000
Replikasi III =40
4 x 10 x 200 = 20000
8. Konsentrasi 200 µg/ml
Replikasi I = 464 x 10 x 200 = 23000
Replikasi II = 46
4 x 10 x 200 = 23000
Replikasi III =464 x 10 x 200 = 23000
9. Konsentrasi 100 µg/ml Replikasi I = 53
4 x 10 x 200 = 26500
Replikasi II = 544 x 10 x 200 = 27000
42
Lampiran 3. Perhitungan persentase kematian kultur sel HeLa dan sel Vero Perhitungan % kematian pada sel HeLa dapat dihitung dengan rumus :
% kematian =
A : jumlah sel HeLa yang hidup pada sumuran kontrol media
B : jumlah sel HeLa yang hidup pada sumuran yang telah diberi perlakuan ekstrak kloroform daun pacar air
44
46
Lampiran 4. Perhitungan LC50dengan analisis probit dan uji linearitas Perhitungan LC50dengan analisis probit pada sel HeLa
Replikasi I
Tabel VII. Data log konsentrasi, % kematian dan harga probit sel HeLa pada replikasi I
Dengan Regresi linear log konsentrasi ekstrak kloroform daun pacar air terhadap
harga probit didapatkan nilai : a = 2,22; b = 1,61; r = 0,93 Sehingga persamaannya : y = bx + a
y = 1,61 x + 2,22 5 = 1,61 x + 2,22 x = 1,73
No Konsentrasi % kematian Harga probit Log kadar
1 200 µg/ml 89,74 6,28 2,30
2 175 µg/ml 80,77 5,88 2,24
3 150 µg/ml 74,36 5,64 2,18
4 125 µg/ml 67,95 5,47 2,10
5 100 µg/ml 60,26 5,25 2,00
6 75 µg/ml 52,56 5,08 1,88
7 50 µg/ml 46,15 4,90 1,70
47
Replikasi II
Tabel VIII. Data log konsentrasi, % kematian dan harga probit sel HeLa pada replikasi II
No Konsentrasi % kematian Harga probit Log kadar
1 200 µg/ml 89,74 6,28 2,30
2 175 µg/ml 80,77 5,88 2,24
3 150 µg/ml 73,08 5,61 2,18
4 125 µg/ml 67,95 5,47 2,10
5 100 µg/ml 61,54 5,31 2,00
6 75 µg/ml 53,85 5,10 1,88
7 50 µg/ml 44,87 4,87 1,70
8 25 µg/ml 37,18 4,67 1,40
Dengan Regresi linear log konsentrasi ekstrak kloroform daun pacar air terhadap
harga probit didapatkan nilai : a = 2,18; b = 1,63; r = 0,94 Sehingga persamaannya : y = bx + a
48
Replikasi III
Tabel IX. Data log konsentrasi, % kematian dan harga probit sel HeLa pada replikasi III
No Konsentrasi % kematian Harga probit Log kadar
1 200 µg/ml 89,74 6,28 2,30
2 175 µg/ml 80,77 5,88 2,24
3 150 µg/ml 73,08 5,61 2,18
4 125 µg/ml 67,95 5,47 2,10
5 100 µg/ml 60,26 5,25 2,00
6 75 µg/ml 52,56 5,08 1,88
7 50 µg/ml 44,87 4,87 1,70
8 25 µg/ml 38,46 4,69 1,40
Dengan Regresi linear log konsentrasi ekstrak kloroform daun pacar air terhadap
harga probit didapatkan nilai : a = 2,21; b = 1,61; r = 0,93 Sehingga persamaannya : y = bx + a
y = 1,61 x + 2,21 5 = 1,61 x + 2,21 x = 1,73
Rata-rata x =
3
73 , 1 73 , 1 73 ,
1
= 1,73
49
Perhitungan LC50dengan analisis probit pada sel Vero Replikasi I
Tabel X. Data log konsentrasi, % kematian dan harga probit sel Vero pada replikasi I
Dengan Regresi linear log konsentrasi ekstrak kloroform daun pacar air terhadap harga probit didapatkan nilai : a = 0,02; b = 2,05 ; r = 0,86
Sehingga persamaannya : y = bx + a
y = 2,05x + 0,02 5 = 2,05x + 0,02
x = 2,43
No Konsentrasi % kematian Harga probit Log kadar
1 800 µg/ml 95,95 % 6,75 2,90
2 700 µg/ml 78,38 % 5,77 2,85
3 600 µg/ml 67,57 % 5,47 2,78
4 500 µg/ml 62,16 % 5,31 2,70
5 400 µg/ml 55,41 % 5,13 2,60
6 300 µg/ml 45,95 % 4,90 2,48
7 200 µg/ml 37,84 % 4,69 2,30
50
Replikasi II
Tabel XI Data log konsentrasi, % kematian dan harga probit sel Vero pada replikasi II
Dengan Regresi linear log konsentrasi ekstrak kloroform daun pacar air terhadap harga probit didapatkan nilai : a = 0,10; b = 2,01; r = 0,88
Sehingga persamaannya : y = bx + a y = 2,01x + 0,10
5 = 2,01x + 0,10
x = 2,44
No Konsentrasi % kematian Harga probit Log kadar
1 800 µg/ml 94,60 % 6,64 2,90
2 700 µg/ml 77,03 % 5,74 2,85
3 600 µg/ml 67,57 % 5,47 2,78
4 500 µg/ml 62,16 % 5,31 2,70
5 400 µg/ml 54,05 % 5,10 2,60
6 300 µg/ml 45,95 % 4,90 2,48
7 200 µg/ml 37,84 % 4,69 2,30
51
Replikasi III
Tabel XII. Data log konsentrasi, % kematian dan harga probit sel Vero pada replikasi III
Dengan Regresi linear log konsentrasi ekstrak kloroform daun pacar air terhadap
harga probit didapatkan nilai : a = 0,08; b = 2,02; r = 0,88 Sehingga persamaannya : y = bx + a
y = 2,02x + 0,08
5 = 2,02x + 0,08 x = 2,44
Rata-rata x =
3
44 , 2 44 , 2 43 ,
2
=
2,44LC50= antilog 2,44
= 275,4 µg/ml
No Konsentrasi % kematian Harga probit Log kadar
1 800 µg/ml 94,60 % 6,64 2,90
2 700 µg/ml 78,38 % 5,77 2,85
3 600 µg/ml 67,57 % 5,47 2,78
4 500 µg/ml 60,81 % 5,28 2,70
5 400 µg/ml 54,05 % 5,10 2,60
6 300 µg/ml 45,95 % 4,90 2,48
7 200 µg/ml 37,84 % 4,69 2,30
52
Uji linearitas untuk analisis regresi
Tabel XIII. Nilai r (koefisien korelasi) pada level signifikansi 5% dan 1%
Degrees of
(De Muth, 1999)
n = 8
df = n-2 = 8-2 = 6
r tabel (df = 6,α= 0,05) = 0,707
Apabila : r hitung > r tabel, maka linear r hitung < r tabel, maka tidak linear
Uji linearitas pada sel HeLa - Replikasi I
r hitung = 0,93r hitung > r tabel (linear) - Replikasi II
r hitung = 0,94 r hitung > r tabel (linear) - Replikasi III
53
Uji linearitas pada sel Vero - Replikasi I
r hitung = 0,86r hitung > r tabel (linear) - Replikasi II
r hitung = 0,88r hitung > r tabel (linear) - Replikasi III
54
Lampiran 5. Analisis statistik uji z pada kelompok kontrol dan perlakuan
1
Kontrol dan konsentrasi 200 µg/µl
1
Kontrol dan konsentrasi 175 µg/µl
55
Kontrol dan konsentrasi 150 µg/µl
1
Kontrol dan konsentrasi 125 µg/µl
1
Kontrol dan konsentrasi 100 µg/µl
56
Kontrol dan konsentrasi 75µg/µl
1
Kontrol dan konsentrasi 50µg/µl
1
Kontrol dan konsentrasi 25µg/µl
57
Lampiran 6. Analisis statistik uji t sampel independen
H0 = tidak terdapat perbedaan antara LC50 sel Vero dan sel HeLa
H1 = terdapat perbedaan antara LC50 sel Vero dan sel HeLa
58
59
BIOGRAFI PENULIS