SKRINING DAN UJI AKTIVITAS LIPOLITIK MIKROBA HIDROKARBONOKLASTIK
Elga Renjana, Dr. Ni’matuzahroh, dan Dr Sri Sumarsih, M.Si. Prodi S-1 Biologi, Departemen Biologi, Fakultas Sains dan Teknologi,
Universitas Airlangga, Surabaya
ABSTRACT
This study aimed to screen and test the lipolytic activity of hydrocarbonoclastic microbial from collection of Microbiology Laboratory of FST Airlangga University. Screening of hydrocarbonoclastic microbial was performed using rhodamine-B agar which contained cooking oil 1%. Microbes which had lipolytic activity were marked with orange flourescent zone around the colony. Hydrocarbonoclastic microbial which had the highest lipolytic activity index was Actinobacillus sp. The lipase enzyme of Actinobacillus sp. was produced in Bushnell Haas liquid medium which added cooking oil 1%. Lipolytic activity of Actinobacillus sp. was measured using a spectrophotometer UV –vis (λ = 410 nm) with p-nitrophenyl palmitat as substrat on phosphat buffer pH 7.0, 37 ºC. Lipolytic activity from crude lipase enzyme extract of Actinobacillus sp. was 1,36 U/ml at 24 hours incubation time. Characterization of the enzyme was done by determining the optimum pH and temperature at optimum incubation time. Maximum lipolytic activity of Actinobacillus sp. was 1,55 U/ml at pH 7.0, 60 ºC. Keywords: lipolytic activity, Actinobacillus sp., rhodamine-B agar
PENDAHULUAN
Enzim merupakan molekul biopolimer protein yang tersusun dari serangkaian asam amino dalam komposisi dan susunan rantai yang teratur dan tetap. Enzim berfungsi sebagai aktivator dalam reaksi biokimia dan bersifat spesifik terhadap substrat, sehingga mempermudah proses pemutusan
suatu rantai kompleks tertentu (Syamsudin dkk., 2008). Lipase merupakan enzim yang dapat larut dalam air dan secara alami mengkatalis hidrolisis ikatan ester dalam substrat lipid yang tidak larut air (Miller et al., 2010).
Saat ini aktivitas pengeboran minyak bumi di Indonesia dan penggunaan derivat-derivatnya mulai
mengalami peningkatan. Peningkatan aktivitas tersebut mengakibatkan kenaikan tingkat pencemaran tanah oleh hidrokarbon karena kandungan senyawa hidrokarbon dalam minyak bumi sangatlah besar. Menurut Via (2009), kandungan senyawa hidrokarbon murni dalam minyak bumi sebesar 90-99%. Salah satu upaya pemulihan lahan tercemar minyak yang saat ini sudah mulai dikembangkan di Indonesia adalah bioremediasi (Ni’matuzahroh dkk., 2009). Bioremediasi merupakan upaya untuk menghilangkan pengaruh kontaminan (zat pencemar)
dengan menggunakan
mikroorganisme, sehingga substansi kontaminan tersebut berkurang (Arsyad dan Rustiadi, 2008).
Mikroba hidrokarbonoklastik merupakan mikroba yang mampu mendegradasi hidrokarbon untuk keperluan metabolisme dan perkembangbiakannya. Senyawa hidrokarbon dalam minyak bumi merupakan sumber karbon bagi mikroba hidrokarbonoklastik (Nugroho, 2006). Pada mekanisme degadrasi tersebut, mikroba hidrokarbonoklastik menghasilkan
suatu senyawa berupa enzim lipase. Aktivitas mikroba dalam mendegradasi hidrokarbon menggunakan lipase disebut aktivitas lipolitik.
Laboratorium Mikrobiologi Departemen Biologi FST Universitas Airlangga memiliki koleksi 11 isolat mikroba hidrokarbonoklastik potensial yang berhasil diisolasi oleh Ni’matuzahroh dkk. (2009). Namun selama ini belum dilakukan skrining kemampuan lipolitik dari mikroba hidrokarbonoklastik tersebut. Oleh karena itu, perlu dilakukan skrining dan uji aktivitas lipolitik mikroba hidrokarbonoklastik, sehingga dapat menjadi sumber alternatif dalam perolehan enzim lipase yang dapat digunakan untuk mendegradasi hidrokarbon pada lahan tercemar minyak.
METODE PENELITIAN a. Bahan penelitian
Bahan yang digunakan sebagai sumber mikroba merupakan koleksi mikroba hidrokarbonoklastik Laboratorium Mikrobiologi Departemen Biologi FST Universitas Airlangga yang diisolasi oleh
Ni’matuzahroh dkk. (2009), yaitu Candida famata, Pseudomonas aeruginosa, P. putida hasil isolasi dari Depo PERTAMINA Surabaya, Acinetobacter faecalis tipe II, Actinobacillus sp., C. parapsilopsis, P. cepacea, P. flourescens-25, P. pseudomallei, Rhodotorulla mucilaginosa hasil isolasi dari pengeboran minyak Desa Wonocolo, Bojonegoro, dan Bacillus subtilis 3Kp hasil isolasi dari perairan Kali Donan Cilacap, Jawa Tengah. Bahan-bahan yang digunakan untuk pembuatan media dan uji adalah Nutrient Agar (NA), Sabouraud Dextrose Agar (SDA), Nutrient Broth (NB), minyak goreng, powder agar, K2HPO4, KH2PO4, NH4NO3,
MgSO4.7H2O, CaCl2.2H2O, FeCl3,
NaCl, p-nitrofenil palmitat (p-NPP), rhodamin-B, buffer fosfat pH 5.0, 6.0, 7.0, 8.0, alkohol 70%, air fisiologis, spiritus, dan akuades.
b. Prosedur penelitian
1. Skrining mikroba
hidrokarbonoklastik penghasil lipase
Skrining mikroba dilakukan dengan pembuatan medium uji (rhodamin-B agar) dengan komposisi
20 ml medium Bushnell Haas cair, 0,6 ml (3%) minyak goreng dan 0,04 ml rhodamin-B 0,1% dalam H2O.
Selanjutnya mikroba hidrokarbonoklastik diinokulasi sebagai spot kecil ke medium uji dan diinkubasi pada suhu 37 ºC selama 48 jam. Aktivitas lipolitik ditandai dengan munculnya zona pendaran berwarna oranye kemerahan di sekitar koloni mikroba di bawah sinar UV pada λ = 312 nm.
2. Uji aktivitas enzim terhadap p -nitrofenil palmitat
Penentuan aktivitas enzim lipase dilakukan dengan metode Pereira-Meirelles et al. (1997) dalam Sumarsih (2005) yang dimodifikasi. Aktivitas enzim ditentukan dengan metode spektrofotometrik dengan substrat p-nitrofenil palmitat (p-NPP). Pada tabung Eppendorf yang diisi 700 µl larutan p-NPP 0,503 mM dalam buffer fosfat pH 7.0. Kemudian ditambahkan 300 µl supernatan yang mengandung enzim lipase ekstraseluler. Campuran diinkubasi dalam waterbath pada suhu 37º C selama 30 menit. Setelah diinkubasi, campuran ditambahkan 100 µl larutan Na2CO3 0,2 M.
p-nitrofenol yang terbentuk ditandai dengan warna kuning, kemudian diukur dengan spektrofotometer UV-Vis pada λ = 410 nm.
c. Karakterisasi enzim lipase Karakterisasi enzim lipase dilakukan dengan memproduksi enzim lipase pada inkubasi optimal yang selanjutnya dilakukan penentuan aktivitas lipolitik pada suhu dan pH optimal enzim lipase tersebut. Penentuan pH optimal aktivitas enzim lipase dilakukan dengan melarutkan substrat p-NPP pada buffer fosfat dengan variasi pH 5.0, 6.0, 7.0, dan 8.0. Sedangkan penentuan suhu optimal aktivitas enzim lipase dilakukan pada pH optimal dengan variasi suhu inkubasi ,yakni 30, 40, 50, 60, dan 70 ºC.
HASIL DAN PEMBAHASAN a. Aktivitas Lipolitik Mikroba
Hidrokarbonoklastik Koleksi Laboratorium Mikrobiologi FST Universitas Airlangga Hasil skrining aktivitas lipolitik pada 11 spesies mikroba hidrokarbonoklastik koleksi Laboratorium Mikrobiologi FST Universitas Airlangga menunjukkan
bahwa semua spesies memiliki aktivitas lipolitik dimana ditandai dengan pendaran berwarna oranye di sekitar koloni mikroba. Kesebelas spesies tersebut adalah Acinetobacter faecalis tipe II, Actinobacillus sp., Bacillus subtilis 3Kp, Candida famata, C. parapsilopsis, Pseudomonas aeruginosa, P. cepacea, P. flourescens-25, P. pseudomallei, P. putida, dan Rhodotorulla mucilaginosa. Adanya aktivitas lipolitik dikarenakan mikroba menghasilkan enzim lipase yang digunakan untuk menghidrolisis trigliserida dalam minyak goreng menjadi gliserol dan asam lemak. Pendaran berwarna oranye yang ada di sekitar koloni mikroba hidrokarbonoklastik terbentuk karena terjadi pembentukan dimer kompleks antara rhodamin-B dengan asam lemak dan monogliserida atau digliserida (Wirawan, 2009).
b. Indeks Aktivitas Lipolitik Mikroba Hidrokarbonoklatik Koleksi Laboratorium Mikrobiologi FST Universitas Airlangga
Hasil penelitian menunjukkan bahwa bakteri Actinobacillus sp.
memiliki indeks aktivitas lipolitik tertinggi di antara spesies mikroba hidrokarbonoklastik lainnya dengan nilai 3,50 (Gambar 1). Tingginya indeks aktivitas lipolitik bakteri Actinobacillus sp. dikarenakan diameter zona pendarannya paling besar. Hal ini sesuai dengan pernyataan Hou and Johnston (1992) bahwa bakteri penghasil lipase yang baik dapat dilihat dari kekuatan pendaran dan diameter zona
pendaran yang dihasilkan. Hasil analisis statistik juga menunjukkan bahwa indeks aktivitas lipolitik bakteri Actinobacillus sp. mayoritas berbeda nyata dengan mikroba lainnya (Tabel 1). Dengan demikian, Actinobacillus sp. dipilih sebagai isolat uji yang akan diukur kemampuan aktivitas lipolitiknya dan dikarakterisasi enzim lipase yang dihasilkan.
Gambar 1. Indeks aktivitas lipolitik mikroba hidrokarbonoklastik koleksi Laboratorium Mikrobiologi FST Universitas Airlangga
Tabel 1. Indeks aktivitas lipolitik mikroba hidrokarbonoklastik dan uji statistiknya
No Spesies Mikroba
Indeks Aktivitas Lipolitik
pada Ulangan ke- Rata-rata
1 2 3
1 Acinetobacter faecalis tipe II 0,08 0,18 0,18 0,15a ± 0,06 2 Actinobacillus sp. 3,31 3,67 3,51 3,50b ± 0,18 3 Bacillus subtilis 3Kp 0,25 0,22 0,23 0,23ac ± 0,02 4 Candida famata 0,51 0,24 0,25 0,33a ± 0,15 5 C. parapsilopsis 0,22 0,07 0,16 0,08a ± 0,08 0,15 3,50 0,23 0,33 0,16 0,22 1,39 0,88 1,29 1,62 1,75
6 Pseudomonas aeruginosa 0,31 0,22 0,14 0,22a ± 0,09 7 P. cepacea 1,51 1,22 1,43 1,39d ± 0,15 8 P. flourescens-25 1,15 0,83 0,67 0,88ad ± 0,24 9 P. pseudomallei 1,47 1,10 1,30 1,29cd ± 0,19 10 P. putida 1,28 1,86 1,71 0,62ad ± 0,30 11 Rhodotorulla mucilaginosa 2,56 0,56 2,13 1,73ad ± 1,50 c. Kemampuan Bakteri Actinobacillus sp. dalam Menghasilkan Lipase
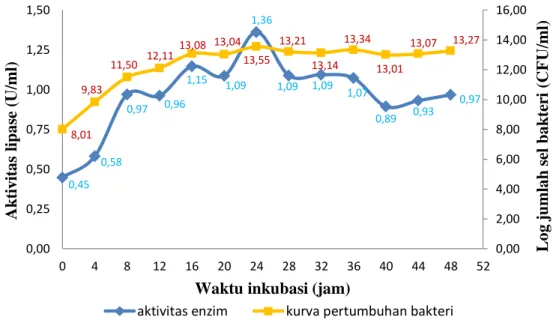
Berdasarkan hasil penelitian (Gambar 2) bahwa aktivitas lipolitik mulai mengalami peningkatan pada jam ke-4 sampai jam ke-24 dimana bakteri berada pada fase log (eksponensial). Namun pada jam ke-28 sampai jam ke-40 aktivitas lipolitik mengalami penurunan, sehingga mengakibatkan pertumbuhan bakteri melambat atau memasuki fase stasioner. Naiknya aktivitas enzim antara jam ke-4 sampai jam ke-24 dan menurunnya aktivitas enzim antara jam ke-28 sampai jam ke-48 disebabkan adanya perbedaan waktu yang dibutuhkan enzim dan peningkatan jumlah enzim yang bereaksi dengan substrat.
Selain itu, menurunnya aktivitas enzim juga disebabkan berkurangnya jumlah substrat atau jumlah produk enzim menghambat pembentukan kompleks enzim substrat (Hasnunidah dan Sumardi, 2009). Menurut Wirawan (2009), penurunan aktivitas lipolitik diduga karena adanya hambatan dari metabolit yang dikeluarkan bersamaan dengan lipase oleh bakteri pada media produksinya. Berdasarkan hasil penelitian dapat diketahui bahwa waktu inkubasi optimal yang diperlukan bakteri Actinobacillus sp. dalam memproduksi enzim lipase adalah pada jam ke-24. Aktivitas lipolitik pada waktu inkubasi optimal adalah sebesar 1,36 U/ml.
Gambar 2. Pertumbuhan dan aktivitas lipolitik bakteri Actinobacillus sp. pada media Busnell Haas + minyak goreng 1%
d. Karakterisasi Enzim Lipase Bakteri Actnobacillus sp. Berdasarkan Gambar 3 diketahui bahwa pada pH 5.0 hingga 7.0 aktivitas lipolitik mengalami peningkatan. Akan tetapi, aktivitas lipolitik mengalami penurunan pada pH 8.0. Penurunan aktivitas lipolitik ini dikarenakan enzim mengalami denaturasi atau struktur sekunder dan tersiernya berubah. Perubahan nilai pH akan menyebabkan struktur dan aktivitas enzim berubah dan mengakibatkan perubahan muatan
residu asam amino (Sofia, 2000 dalam Hasnunidah dan Sumardi, 2009). Di samping itu, tiap enzim memiliki struktur molekul yang berbeda-beda, dimana ada yang memiliki rantai samping basa, netral, atau asam. Hal tersebut mengakibatkan suatu enzim secara keseluruhan dapat bermuatan positif atau negatif pada pH tertentu (Dewi, 2009). Dengan demikian diketahui bahwa pH optimal aktivitas lipolitik dari bakteri Actinobacillus sp. adalah pada pH 7.0. 0,45 0,58 0,97 0,96 1,15 1,09 1,36 1,09 1,09 1,07 0,89 0,93 0,97 8,01 9,83 11,50 12,11 13,08 13,04 13,55 13,21 13,14 13,34 13,01 13,07 13,27 0,00 2,00 4,00 6,00 8,00 10,00 12,00 14,00 16,00 0,00 0,25 0,50 0,75 1,00 1,25 1,50 0 4 8 12 16 20 24 28 32 36 40 44 48 52 L o g j u m la h s el b a k te ri ( C F U /m l) A k ti v it a s li p a se ( U /m l)
Waktu inkubasi (jam)
Gambar 3. Aktivitas lipolitik bakteri Actinobacillus sp. pada berbagai pH dengan suhu 37º C
Gambar 4. Aktivitas lipolitik bakteri Actinobacillus sp. pada berbagai suhu dalam kondisi pH optimal (pH 7.0)
Berdasarkan Gambar 4 diketahui pada suhu 30º hingga 60º C terjadi peningkatkan aktivitas lipolitik. Namun pada suhu 70º C terjadi penurunan aktivitas lipolitik karena enzim mengalami denaturasi protein. Dengan demikian diketahui bahwa suhu optimal aktivitas lipolitik dari bakteri Actinobacillus sp. adalah pada suhu 60º C. Hasil ini didukung oleh Reetz et al. (2006) yang menyatakan bahwa kisaran suhu
optimal lipase untuk mengkatalisis reaksi adalah antara 20º – 60º C. Dari hasil penelitian aktivitas lipolitik bakteri Actinobacillus sp. pada pH dan suhu optimal adalah sebesar 1,55 U/ml.
Aktivitas lipolitik bakteri Actinobacillus sp. ini lebih besar bila dibandingkan dengan hasil penelitian Liu et al. (2006) yang menggunakan isolat uji Aeromonas sp. dengan aktivitas lipolitik sebesar 0,70 U/ml.
0,91 0,99 1,19 1,09 0,75 1,00 1,25 1,50 4 5 6 7 8 9 A kt iv it as lipa se ( U /m l) pH 1,06 1,12 1,16 1,55 1,46 0,75 1,00 1,25 1,50 1,75 2,00 20 30 40 50 60 70 80 A kt iv it as lip ase (U /m l) Suhu (ºC)
Selain itu, nilai aktivitas lipolitik bakteri Actinobacillus sp. juga lebih besar bila dibandingkan dengan hasil penelitian Guzman et al. (2008) yang menggunakan isolat uji Bacillus pumilus dengan aktivitas lipolitik sebesar 0,079 U/ml. Tingginya aktivitas lipolitik bakteri Actinobacillus sp. menunjukkan bahwa bakteri ini berpotensi dalam menghasilkan enzim lipase. Di samping itu, enzim lipase bakteri Actinobacillus sp. optimal pada suhu 60º C. Oleh karena itu, enzim lipase ini dapat diaplikasikan untuk industri yang melakukan proses produksi pada suhu tinggi, seperti industri makanan dan kosmetik.
KESIMPULAN
Berdasarkan hasil dan pembahasan dapat disimpulkan
bahwa spesies mikroba hidrokarbonoklastik koleksi Laboratorium Mikrobiologi FST Universitas Airlangga yang memiliki aktivitas lipolitik adalah Acinetobacter faecalis tipe II, Actinobacillus sp., Bacillus subtilis 3Kp, Candida famata, C. parapsilopsis, Pseudomonas aeruginosa, P. putida, P. cepacea, P. flourescens-25, P. pseudomallei, Rhodotorulla mucilaginosa dimana mikroba yang memiliki indeks aktivitas lipolitik tertinggi adalah Actinobacillus sp. Actinobacillus sp. memiliki kemampuan menghasilkan enzim lipase sebesar 1,36 U/ml pada waktu inkubasi optimal 24 jam. Karakteristik enzim lipase dari Actinobacillus sp. adalah memiliki optimal pada suhu 60 ºC dan pH 7.0 dengan aktivitas lipolitik sebesar 1,55 U/ml.
DAFTAR PUSTAKA
Arsyad, S. dan Rustiadi, E. 2008. Penyelamatan Tanah, Air, dan Lingkungan. Edisi Pertama. Crestpent Press dan Yayasan Obor Indonesia. Dewi, G.D.F. 2009. Isolasi dan
Karakterisasi Ekstrak Kasar Enzim Laktase dari
Fungi Pelapuk. Skripsi. Departemen Kimia, FSAINTEK, Universitas Airlangga.
Guzman, M.N., Vargas, V.A., Antezana, H., and Svoboda, M. 2008. Lipolytic Enzyme
Production by
Halophilic/Halotolerant Microorganisms Isolated
from Laguna Verde, Bolivia. J. Revista Boliviana De Quimica, 25.
Hasnunidah, N. dan Sumardi. 2009. Isolasi Bacillus sp.
Penghasil Lipase dari Saluran Pencernaan Ayam Kampung. Jurusan Biologi. FMIPA. Unila.
Hou, C.T. and Johnston, T.M. 1992. Screening of Lipase Activities with Culture from The Agricultural
Research Culture
Collection. J. Am. Oil. Chem. Soc., 69, 1088-1097.
Liu, C.H., Chen, W.M., and Chang, J.S. 2006. Methods for Rapid Screening and Isolation of Bacteria Producing Acidic Lipase: Feasibility Studies and Novel Activity Assay Protocols. J. Microb Biotechnol., 23, 633-640.
Miller, F.P., Vandome, A.F., and McBrewster, J. 2010. Lipase. Alphascript Publishing. USA. Ni’matuzahroh, Supriyanto, A., Affandi, M. dan Fatimah. 2009. Bioremediasi Tanah
Tercemar Minyak
Menggunakan Konsorsium Mikroba. Laporan Hibah Penelitian Strategis Nasional Tahun Anggaran 2009. Universitas Airlangga.
Nugroho, A. 2006. Bioremediasi Hidrokarbon Minyak Bumi. Yogyakarta: Graha Ilmu. Reetz, M.T., Carballeira, J.D., Vogel,
A. 2006. Iterative Saturation Mutagenesis on the Basis of B Factors as a Strategy for Increasing Protein Thermostability. Angew. Chem. Int. Ed., 45, 7745-7751.
Sumarsih, S. 2005. Skrining Bakteri
Penghasil Lipase
Termostabil dari Reaktor pada Pabrik Minyak Goreng. Laporan Penelitian Dipa Penerimaan Bukan Pajak Tahun Anggaran 2005. FMIPA. Universitas Airlangga.
Syamsudin, Sri Purwanti, dan Andri Taufick R. 2008. Efektivitas Enzim dalam Sistem Lumpur Aktif pada Pengolahan Air Limbah Pulp dan Kertas. Berita Selulosa Vol. 43 (2), hal 83-92.
Via. 2009. Minyak Bumi. http://kimiakoloid.com/blog/? cat=13. Diakses tanggal 18 Januari 2011.
Wirawan, B. 2009. Potensi Bakteri Endofit Tanaman Obat sebagai Penghasil Senyawa Antihiperlipidemia melalui Aktivitas Lipase. Skripsi. Departemen Biologi. FMIPA. IPB. Bogor.