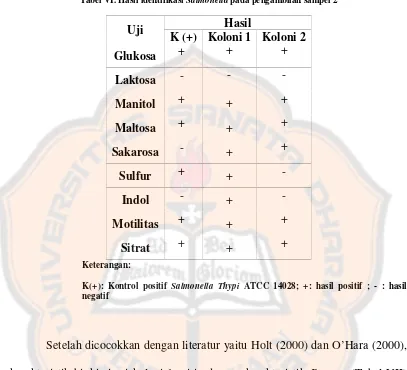
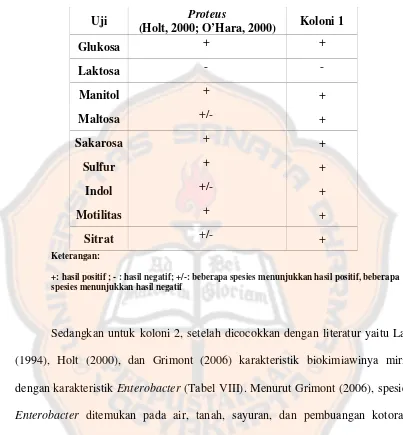
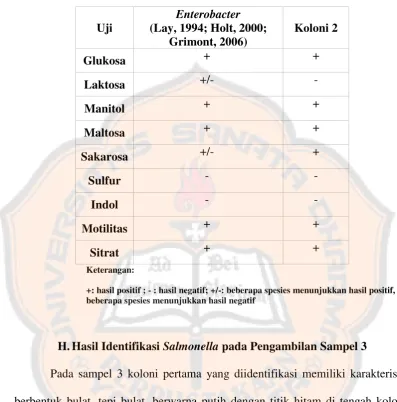
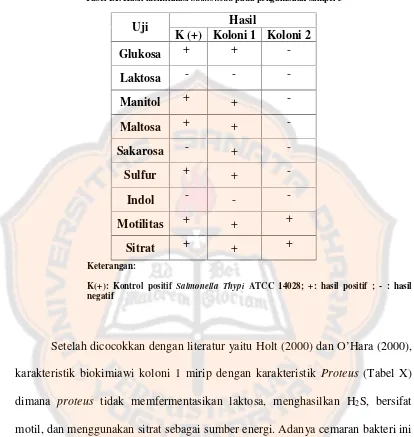
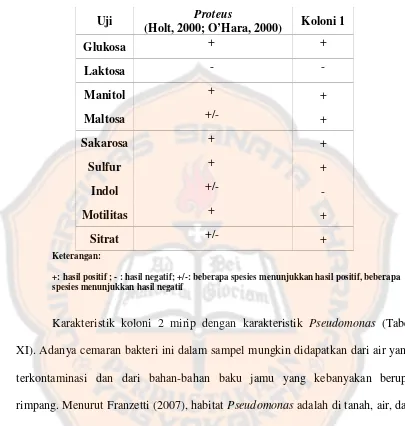
Uji Angka Kapang/Khamir (AKK), Angka Lempeng Total (ALT), dan identifikasi salmonella pada jamu cekok yang diproduksi penjual jamu racik ``x`` di Yogyakarta - USD Repository
Teks penuh
Gambar


Dokumen terkait
Menurut saya pengertian dari segitiga sama sisi adalah suatu bidang datar yang dibatasi pleh tiga buah garis lurus” [Lalu mengambil segitiga sama sisi warna pink] “Tiga
Hitunglah arus dari sumber tegangan v = 311 sin 314 t yang dihubungkan dengan tahanan 100 ohm serta tentukan beda fase antara arus dan tegangan3. Sebuah kumparan mempunyai
Rancangan sistem pendukung keputusan pemilihan guru favorit di MA AZ-ZAIN Lengkong menggunakan metode Analytical Hierarchy Process, yang dibuat dengan menggunakan 3
Penggunaan PLTMH sebagai energi alternatif yang cost friendly, user friendly, environment friendly, and material friendly diharapkan dengan peran Puslitbang
Dalam melakukan penelitian perlu adanya desain penelitian terlebih dahulu. 6) desain penelitian merupakan rencana untuk memilih sumber-sumber data dan data yang akan dipakai untuk
Teman-teman KLAbers angkatan 2011 ada Kak Nila Anggreiny yang sudah memberikan waktu untuk memperhatikan kami, mengontrol, memberi semangat dan nasihat untuk kebaikan penulis
Jika database dalam mode ARCHIVELOG, maka hot (on line) backup dapat dilakukan. Persiapan sebelum menaikkan database Setting ORACLE_SID, di shell csh setenv
[r]