BAB V PEMBAHASAN - Pemanfaatan limbah selulosa dalam kulit durian (durio zibethinus) sebagai bahan baku pembuatan bioetanol melalui proses fermentasi saccharomyces cerevisiae - Digital Library IAIN Palangka Raya
Teks penuh
Gambar
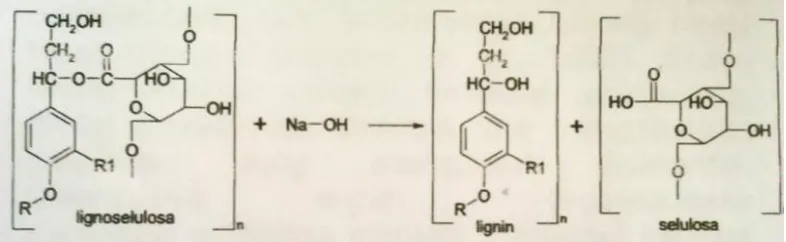
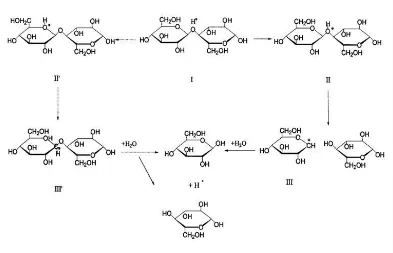
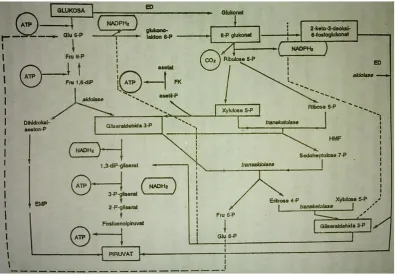
Dokumen terkait
Laporan K euangan Program Imbalan Pasti, meliputi Laporan A set neto tersedia untuk manfaat purnakarya, Nilai kini aktuarial dari manfaat purnakarya terjanji, dan
recency effect took place. 2) There is no different judgment between the overconfidence participant who receives good news followed by bad news (++--) and the
Definisi ini sudah mencakup semua hak yang dimaksud oleh para ahli diatas, seperti hak Allah SWT terhadap hambanya (al-haq al-diniy), hak kepemilikan (haq
THE EFFECTIVENESS OF HANGAROO GAME FOR TEACHING VOCABULARY (An Experimental Research at Seventh Grade Students of SMP Negeri 3 Purwokerto in.. Academic
Evaluasi proses dari pelaksanaan PDK dari banyak aspek yang diukur seperti dalam penelitian ini meliputi proses persiapan PDK (proses pendaftaran PDK, proses
Bogor, Bandung Jumlah KAK 1 buku Terfasilitasinya 75 ijin - - 131,500,000 131,500,000 144,650,000 sedang BPT Pengaduan Dalam Pelayanan Peluang
storage (temperatur masuk rak pengering) dengan temperatur lingkungan, meskipun intensitas radiasi matahari mengalami penurunan pada malam
Penggunaan lampu Light Emmitting Diode (LED) hijau untuk mengurangi bycatch penyu pada perikanan jaring insang ( gillnet ) dilakukan di perairan Paloh, Kalimantan