i
UJI AKTIVITAS ANTIOKSIDAN MENGGUNAKAN METODE DPPH DAN PENETAPAN KANDUNGAN FENOLIK TOTAL FRAKSI ETIL
ASETAT EKSTRAK ETANOLIK DAUN DADAP SEREP (Erythrina subumbrans (Hassk.)Merr.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat
Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Aldo Kristian
NIM : 098114038
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Skripsi ini kupersembahkan untuk :
Tuhanku Yesus Kristus atas segala berkat dan penyertaan-Nya
Bapak, Ibu dan Kakak-kakakku atas kasih sayang
dan segala hal yang diberikan
vii
KATA PENGANTAR
Puji dan syukur penulis kepada Tuhan atas segala rahmat, berkat, anugrah
dan penyertaan-Nya kepada penulis sehingga penulis dapat menyelesaikan skripsi
yang berjudul “UJI AKTIVITAS ANTIOKSIDAN MENGGUNAKAN METODE DPPH DAN PENETAPAN KANDUNGAN FENOLIK TOTAL FRAKSI ETIL ASETAT EKSTRAK ETANOLIK DAUN DADAP SEREP (Erythrina subumbrans (Hassk.) Merr.)” ini dengan baik. Skripsi ini disusun
untuk memenuhi salah satu persyaratan untuk memperoleh gelar Sarjana Farmasi
(S.Farm) pada Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Penulis ingin berterima kasih kepada segala pihak yang telah memberikan
bantuan baik dukungan, bimbingan, sarana, materil maupun moril dalam
penyusunan skripsi ini. Oleh karena itu, dalam kesempatan ini penulis
mengucapkan terima kasih atas segala bantuan yang telah diberikan kepada:
1. Ipang Djunarko,M.Sc.,Apt., selaku Dekan Fakultas Farmasi Universitas Sanata
Dharma.
2. Prof.Dr.C.J. Soegihardjo,Apt., selaku Dosen Pembimbing yang telah
memberikan perhatian, bimbingan dan arahan dari awal pengusulan skripsi
sampai penulisan skripsi ini selesai.
3. Lucia Wiwid Wijayanti,M.Si., selaku Dosen Penguji atas ketersediaannya
untuk menguji dan juga memberikan masukan dan saran dalam skripsi ini.
4. Yohanes Dwiatmaka,M.Si., selaku Dosen Penguji atas ketersediaannya untuk
viii
5. Rini Dwiastuti S.Far.,Apt, M.Sc., selaku Dosen Pembimbing Akademik yang
telah membimbing dan memberi nasihat kepada penulis.
6. Sahabat seperjuangan skripsi DPPH, Anthony Felix, Mikhael Gustandy,
Willigis Danu Patria yang selalu membantu dan bekerjasama dengan luar biasa.
7. Teman-teman FSM dan FST A 2009, atas kerjasama, dukungan dan bantuan
yang diberikan.
8. Segenap laboran Laboratorium Fakultas Farmasi Universitas Sanata Dharma
atas segala bantuan selama penulis melakukan penelitian di laboratorium.
9. Pemerintah Kabupaten Bengkayang, Kal-Bar, atas bantuan dana yang
diberikan.
10.Semua pihak yang telah memberikan bantuan dan dukungan yang tidak dapat
disebut satu per satu.
Penulis menyadari bahwa masih terdapat ketidaksempurnaan dalam
penulisan skripsi ini. Dengan segala kerendahan hati penulis akan menerima
segala kritik dan saran yang membangun dari semua pihak. Akhir kata, semoga
skripsi ini dapat bermanfaat bagi ilmu pengetahuan dan banyak pihak.
Yogyakarta, 10 Maret 2013
ix
x
2. Nama tumbuhan………. 6
3. Klasifikasi dadap serep…..……… 6
4. Gambaran umum……… 7
5. Kandungan kimia dadap serep……… 7
B. Senyawa Fenolik………. 8
C. Radikal Bebas……… 9
D. Antioksidan……… 11
E. Penyarian……… 13
F. Metode DPPH dan Folin-Ciocalteu……….... 14
G. Validasi Metode………...…… 16
H. Landasan Teori………. 18
I. Hipotesis……….. 19
BAB III METODOLOGI PENELITIAN……… 20
A. Jenis dan Rancangan Penelitian……….. 20
B. Variabel……… 20
C. Definisi Operasional………..……….… 20
D. Bahan dan Alat Penelitian……… 21
1. Bahan penelitian……….. 21
2. Alat penelitian……….…… 21
E. Tatacara Penelitian……… 22
1. Determinasi tumbuhan……… 22
2. Pengumpulan bahan……….…… 22
xi
4. Pembuatan larutan pembanding dan uji……….… 23
5. Uji pendahuluan………..… 24
6. Optimasi metode uji aktivitas antioksidan………..…… 25
7. Uji aktivitas antioksidan……….…… 26
8. Optimasi metode penetapan kandungan fenolik total…………. 27
9. Penetapan kandungan fenolik total………. 27
F. Analisis Hasil……… 28
BAB IV HASIL DAN PEMBAHASAN……….… 31
A. Determinasi……….. 31
B. Hasil Pengumpulan Bahan……… 31
C. Hasil Preparasi Sampel……….…… 34
1. Ekstraksi sampel………..… 34
2. Fraksinasi ekstrak……….… 35
D. Hasil Uji Pendahuluan………... 37
1. Uji pendahuluan aktivitas antioksidan……….… 37
2. Uji pendahuluan senyawa fenolik……… 39
E. Hasil Optimasi Metode Uji Aktivitas Antioksidan………. 40
1. Penentuan panjang gelombang maksimun (λ maks)……… 40
2. Penentuan Operating Time(OT)………... 41
F. Hasil Validasi Metode Uji Aktivitas Antioksidan………. 43
1. Presisi metode uji aktivitas antioksidan ……… 45
2. Linearitas metode uji antioksidan……….. 46
xii
G. Hasil Uji Aktivitas Antioksidan dengan Radikal DPPH……… 48
H. Hasil Optimasi Metode Penetapan Kandungan Fenolik Total……….. 55
1. Penentuan operating time(OT)……….. 55
2. Penentuan panjang gelombang maksimum……… 56
I. Hasil Validasi Metode Penetapan Kandungan Fenolik Total………… 57
1. Presisi metode penetapan kadar kandungan fenolik total……….. 57
2. Linieritas metode penetapan kandungan fenolik total……… 58
3. Spesifisitas metode penetapan kandungan fenolik total………. 59
J. Hasil Penetapan Kandungan Fenolik Total………. 59
BAB V KESIMPULAN DAN SARAN………. 62
A. Kesimpulan……….……. 62
B. Saran………... 62
DAFTAR PUSTAKA……….. 63
LAMPIRAN……….… 66
xiii
DAFTAR TABEL
Halaman
Tabel I. Berbagai Reactive Oxygen Species (ROS) dan
antioksidan sebagai penetral………. 13
Tabel II. Kisaran recoveryhasil analisis yang diterima………….. 17
Tabel III. Kriteria nilai presisi yang masih dapat diterima………... 17
Tabel IV. Hasil Scanningpanjang gelombang maksimum DPPH… 40
Tabel V. Hasil pengukuran absorbansi seri baku kuersetin
yang direaksikan dengan radikal DPPH……… 43
Tabel VI. Hasil pengukuran absorbansi seri fraksi etil asetat
ekstrak etanol daun dadap serep yang direaksikan
dengan DPPH……… 44
Tabel VII. Hasil presisi aktivitas antioksidan standar kuersetin……. 45
Tabel VIII. Hasil presisi aktivitas antioksidan fraksi etil asetat……… 45
Tabel IX. Hasil aktivitas antioksidan kuersetin dengan metode
DPPH………. 51
Tabel X. Hasil aktivitas antioksidan fraksi etil asetat ekstrak
etanol daun dadap serep dengan metode DPPH…………. 52
Tabel XI. Hasil perhitungan IC50 kuersetin dan Fraksi etil asetat
ekstrak etanol daun dadap serep………. 53
Tabel XII. Penggolongan tingkat kekuatan antioksidan kuersetin
xiv
Tabel XIII. Hasil scanning panjang gelombang maksimum………….. 57
Tabel XIV. Hasil presisi asam galat dari beberapa parameter……… 58
Tabel XV. Hasil pengukuran absorbansi asam galat yang
direaksikan dengan Folin-Ciocalteu……… 58
Tabel XVI. Hasil penentuan jumlah fenolik total fraksi etil asetat
xv
DAFTAR GAMBAR
Halaman
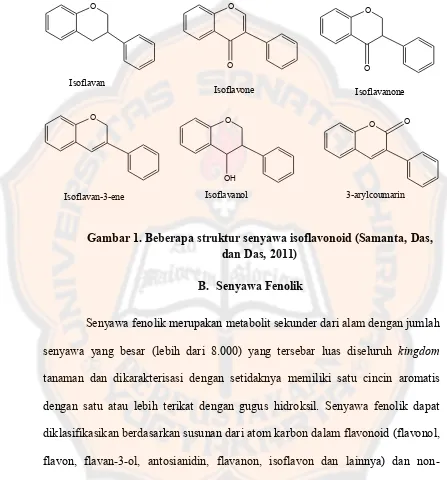
Gambar 1. Beberapa struktur senyawa isoflavonoid……… 8
Gambar 2. Klasifikasi flavonoid produk alam………. 9
Gambar 3. Usulan mekanisme reaksi antara BHT dan DPPH……….. 12
Gambar 4. Reaksi antara radikal DPPH dengan senyawa antioksidan.. 15
Gambar 5. Skema jalannya penelitian……….. 30
Gambar 6. Blanko DPPH , Fraksi etil asetat, Kuersetin…………..…. 38
Gambar 7. Blanko reagen Folin-ciocalteau , Fraksi+reagen
Folin-ciocalteau, Asam galat+ragen Folin-ciocalteatu…… 39
Gambar 8. Grafik penentuan OT kuersetin (Replikasi 2)……….. 42
Gambar 9. Grafik Penetuan OT Fraksi Etil Asetat (Replikasi 1)……... 42
Gambar 10. Reaksi antara radikal DPPH dengan senyawa……….. 48
Gambar 11. Struktur senyawa kuersetin……….. 49
Gambar 12. Usulan mekanisme reaksi kuersetin dan radikal DPPH…… 49
Gambar 13. Kurva persamaan regresi linier aktivitas antioksidan
kuersetin……….. 51
Gambar 14. Kurva persamaan regresi linier aktivitas antioksidan
fraksi etil asetat……… 52
Gambar 15. Grafik penentuan OT asam galat (Replikasi 1)……… 56
Gambar 16. Reaksi pembentukan kompleks molybdenum-blue……….. 60
xvi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Surat determinasi tanaman dadap serep………. 66
Lampiran 2. Gambar tanaman dadap serep……… 67
Lampiran 3. Perhitungan rendemen………...… 68
Lampiran 4. Data penimbangan untuk pengujian
aktivitas antioksidan……….. ... 69
Lampiran 5. Data perhitungan konsentrasi pengujian
aktivitas antioksidan………. 70
Lampiran 6. Scanning pengkoreksi………... 72
Lampiran 7. Optimasi metode uji aktivitas antioksidan………. 73
Lampiran 8. Uji aktivitas antioksidan menggunakan radikal DPPH.. 74
Lampiran 9. Perhitungan nilai IC50 kuersetin dan fraksi air
ekstrak metanol daun dadap serep………... 84
Lampiran 10. Penimbangan bahan pengujian kandungan fenolik total... 85
Lampiran 11. Perhitungan konsentrasi pengujian fenolik total………… 85
Lampiran 12. Scanning kontrol asam galat………. 88
Lampiran 13. Optimasi penentuan kandungan fenolik total……… 88
Lampiran 14. Perhitungan kandungan fenolik total……… 93
xvii INTISARI
Dalam pengobatan tradisional di Indonesia, daun dari tanaman dadap serep berkhasiat untuk mengobati sakit kepala, batuk serta untuk minuman bagi wanita sehabis melahirkan. Senyawa fenolik merupakan salah satu kandungan bioaktif dari daun dadap serep. Penelitian ini dilakukan untuk mengetahui aktivitas antioksidan fraksi etil asetat ekstrak etanol daun dadap serep secara in vitro yang didasarkan pada efek peredaman radikal bebas larutan 1,1-difenil-pikrilhidrazil (DPPH) yang dinyatakan dengan inhibition concentration 50 (IC50). Kandungan fenolik total juga ditentukan menggunakan pereaksi Folin-Ciocalteu dengan baku standar asam galat yang dinyatakan dengan massa ekivalen asam galat. Prinsip metode ini adalah senyawa fenolik teroksidasi dalam suasana basa dan pereaksi Folin-Ciocalteu tereduksi menjadi larutan berwarna biru yang dapat diukur dengan spektrofotometer visibel pada panjang gelombang 750 nm. Hasil penelitian menunjukkan bahwa fraksi etil asetat ekstrak etanol daun dadap serep mempunyai aktivitas antioksidan dengan nilai IC50 sebesar 245,15 ± 4,26 µg/mL dan kandungan fenolik total sebesar 8,51 ± 0,18 ekivalen asam galat per g fraksi etil asetat ekstrak etanol daun dadap serep dan metode yang digunakan belum tervalidasi.
xviii
ABSTRACT
In Indonesian traditional medicine, the leaves of dadaps (Erythrina subumbrans (Hassk.) Merr.) are efficacious to cure headaches, cough and can also be used as a drink for women after childbirth. Phenolic compound is one of the bioactive contents in dadaps leaves. This research was conducted to determine the antioxidant activities of ethyl acetate fraction of ethanol extract of dadaps leaves in vitro based on the reducing effect of free radical of 1,1-diphenyl-pikrilhidrazil (DPPH) solution expressed by inhibition concentration 50 (IC50). The total phenolic contents was also determined by using the Folin-Ciocalteu reagent with gallic acid standard expressed by the mass of gallic acid equivalents. The principle of this method is oxidized phenolic compounds in alkaline medium and Folin-Ciocalteu reagent is reduced to a blue solution that can be measured by the visible spectrophotometer at a wavelength of 750 nm. The results showed that the ethyl acetate fraction of ethanol extract of dadaps leaves had antioxidant activities with IC50 valued in the amount of 245.15 ± 4.26 µg/mL and the total phenolic content of 8.51 ± 0.18 gallic acid equivalent per g of ethyl acetate fraction of ethanol extract of dadaps leaves and the method has not been validated.
1 BAB I PENGANTAR A. Latar Belakang
Paparan sistem biologis dari xenobiotik, polusi, radiasi pengion atau
cahaya UV dan perkembangan kondisi patologis tertentu menyebabkan tekanan
oksidatif, akibatnya meningkatkan produksi oksigen radikal. (Sapakal et al.,
2008). Pembentukan radikal bebas dan reaksi oksidasi pada biomolekul akan
berlangsung sepanjang hidup. Inilah penyebab utama dari proses penuaan dan
berbagai penyakit degeneratif (Silalahi, 2006). Radikal oksigen terus dibentuk
pada semua organisme hidup, dengan efek merusak yang menyebabkan cedera
dan kematian sel (Sapakal et al., 2008). Jenis Reaktif Oksigen Spesies (ROS)
termasuk radikal hidroksil, radikal anion superoksida, hidrogen peroksida, radikal
nitrat oksida, radikal hipoklorit, dan berbagai lipid peroksida mampu bereaksi
dengan membran lipid, asam nukleat, protein, enzim dan molekul kecil lainnya,
yang mengakibatkan kerusakan sel (Sapakal et al., 2008).
Antioksidan adalah zat yang berperan penting dalam menunda atau
mencegah penyakit degeneratif oleh kerusakan oksidatif dari komponen sel hidup
yang disebabkan oleh radikal bebas. Didalam tubuh secara alami telah
mengandung enzim-enzim yang berperan sebagai antioksidan dalam tubuh seperti
enzim glutation reduktase (GSH), superoksida dismutase (SOD), katalase (CAT),
glutation peroksidase (GPX), diketahui dapat melemahkan spesies oksigen reaktif
dengan menghilangkan potensi oksidan atau dengan mengubah spesies oksigen
tekanan oksidatif berlebih didalam tubuh, menyebabkan produksi radikal bebas
menjadi meningkat didalam tubuh yang berakibat dibutuhkannya tambahan
antioksidan yang cukup untuk menanggulangi tekanan oksidatif yang tinggi
tersebut sehingga dapat mengurangi dampak kerusakan sel sebagai akibat dari
reaksi radikal bebas.
Antioksidan sintetik seperti butylated hidroksitoluen (BHT), butylated
hydroxyanisole (BHA), tert-butylhydroquinone (TBHQ) dan propil gallate (PG)
telah digunakan selama bertahun-tahun, namun senyawa tersebut sedang diperiksa
untuk kemungkinannya dalam menimbulkan toksisitas. Oleh karena itu, sekarang
ini dilakukan penelitian intensif tentang antioksidan polifenol alami yang berasal
dari tumbuhan untuk menggantikan antioksidan sintetis (Qader et al.,2011).
Dadap serep (Erythrina subumbrans) adalah salah satu tanaman yang
secara tradisional digunakan untuk minuman bagi wanita sehabis melahirkan dan
untuk mengobati sakit kepala. Rebusan daunnya juga digunakan untuk mengobati
batuk (Anonim, 2007). Dalam tanaman dadap serep memiliki kandungan senyawa
bioaktif seperti alkaloid, flavonoid, isoflavonoid, saponin dan lektin. Senyawa
fenolik tersebut memiliki peranan penting dalam kaitan penggunaan tanaman
terhadap manfaatnya bagi kesehatan. Salah satu manfaat dari kandungan senyawa
fenolik pada tanaman dadap serep telah dibuktikan dalam penelitian
Rukachaisirikul et al.,(2007) yang menunjukan tanaman dadap serep (Erythrina
subumbrans) mengandung senyawa fenolik yang beraktivitas antibakteri lebih
kuat dibanding standar antibiotik vancomycin dan oxacillin terhadap beberapa
Senyawa fenolik merupakan senyawa bioaktif dari tumbuhan yang
merupakan sumber antioksidan alami yang aman. Untuk melihat potensi
antioksidan dari tanaman dadap serep, dalam penelitian ini dilakukan pemeriksaan
aktivitas antioksidan fraksi etil asetat ekstrak etanolik daun dadap serep yang
dilakukan dengan metode 1,1-difenil-2-pikrilhidrazil (DPPH) secara
spektrofotometri. Metode DPPH dipilih karena sederhana, mudah, cepat dan peka
serta hanya memerlukan sedikit sampel. Aktivitas diukur dengan menghitung
jumlah pengurangan intensitas warna ungu DPPH yang sebanding dengan
pengurangan konsentrasi larutan DPPH. Peredaman tersebut dihasilkan oleh
bereaksinya molekul Difenil Pikril Hidrazil dengan atom hidrogen yang
dilepaskan satu molekul komponen sampel sehingga terbentuk senyawa Difenil
Pikril Hidrazin dan menyebabkan terjadinya peluruhan warna DPPH dari ungu ke
kuning (Zuhra, Tarigan dan Sihotang, 2008). Penentuan kandungan fenolik total
dari fraksi etil asetat ekstrak etanolik daun dadap serep dilakukan menggunakan
metode Folin-Ciocalteu dimana merupakan salah satu metode yang cepat dan
sederhana dalam menentukan kandungan fenolik total (Fu et al., 2011).
B. Permasalahan
1. Berapakah nilai aktivitas antioksidan fraksi etil asetat ekstrak etanolik daun
dadap serep dengan menggunakan metode DPPH yang dinyatakan dengan IC50 ?
2. Berapakah kandungan fenolik total fraksi etil asetat ekstrak etanolik daun dadap
C. Keaslian Penelitian
Sejauh pengamatan penulis, penelitian tentang uji aktivitas antioksidan
daun dadap pernah dilakukan oleh :
Estrada, E.I., 2010, dengan judul “Actividad Antioxidante De Alcaloides De
Erythrina Americana Miller”. Penelitian ini menggunakan daun dadap spesies
Erythrina Americana Miller yang diperoleh di universitas nacional autonoma
de Mexico (Mexico) dan uji aktivitas antioksidan dengan metode DPPH (2,2
-diphenyl-1-picrylhydrazyl).
Perbedaan antara penelitian ini dengan penelitian sebelumnya adalah
bahwa dalam penelitian ini daun dadap serep spesies Erythrina subumbrans
(Hassk.) Merr. yang digunakan dipanen dari dari kebun tanaman obat Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta.
D. Manfaat Penelitian 1. Manfaat teoritis
Penelitian ini diharapkan dapat memberikan pengetahuan tentang aktivitas
antioksidan fraksi etil asetat ekstrak etanolik daun dadap serep dengan
menggunakan metode DPPH yang dinyatakan dengan IC50. 2. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi tentang aktivitas
antioksidan daun dadap serep sehingga bisa dimanfaatkan sebagai alternatif untuk
E. Tujuan Penelitian
1. Mengetahui aktivitas antioksidan menggunakan metode DPPH fraksi etil asetat
ekstrak etanolik daun dadap serep.
2. Mengetahui nilai aktivitas antioksidan fraksi etil asetat ekstrak etanolik daun
dadap serep dengan menggunakan metode DPPH yang dinyatakan dengan IC50 dan mengetahui nilai kandungan fenolik total fraksi etil asetat ekstrak etanolik
6
BAB II
PENELAAHAN PUSTAKA A. Dadap Serep 1. Keterangan botani
Dadap serep termasuk tanaman legum pohon, berasal dari Asia Tenggara
dan tersebar di seluruh kepulauan nusantara. Varietas tanaman ini dibedakan
berdasarkan ada tidaknya duri pada kulitnya (Purwanto, 2007).
2. Nama tumbuhan
Nama latin : Erythrina subumbrans Hassk. (Anonim, 2007).
Nama sinonim : Erythrina hypaphorus Boerl., Erythrina lithosperma
Miquel (Anonim, 2007).
Nama daerah : dadap minyak, dadap limit (sunda); dadap lengan,
dadap lisah (jawa); dadap lenga, thetheuk oleng
(Madura) (Purwanto, 2007).
3. Klasifikasi dadap serep menurut USDA (2011)
Kingdom : Plantae
Subkingdom : Tracheobionta
Superdivisi : Spermatophyta
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Sub Kelas : Rosidae
Ordo : Fabales
Famili : Fabaceae
Genus : Erythrina
4. Gambaran umum
Dadap serep merupakan tanaman legum pohon, tumbuh tinggi agak
bengkok, ketinggian mencapai 15-22 m dengan diameter batang 40-100 cm,
sistem perakaran dalam. Kulit batang berwarna hijau, batang yang tua bercampur
garis-garis kecoklatan, cabang tumbuh lurus ke atas membentuk sudut 45o. Daunnya beranak tiga helai, berbentuk delta atau gemuk bundar ujung agak
meruncing, bagian bawah daun membundar, bila diremas terasa lunak ditangan.
Ukuran panjang tangkai daun 10-20,5 cm; panjang daun 9-19 cm; dan lebar daun
6-17 cm. Daun atas berukuran lebih besar daripada kedua daun penumpu.
Bunganya tumbuh diantara ketiak daun, daun mahkota bunyanya berwarna merah
kekuningan, berbentuk terompet. Polongnya berukuran kecil, berbentuk sabit,
berisi 4-8 biji per polong (Purwanto, 2007).
Dalam penggunaannya, bagian kulit kayu dan daun dadap serep secara
empiris digunakan untuk pengobatan tradisional sebagai campuran dengan
tanaman obat lainnya. Di Indonesia ditemukan daun mudanya digunakan untuk
minuman bagi wanita sehabis melahirkan dan untuk mengobati sakit kepala.
Rebusan daunnya digunakan untuk mengobati batuk (Anonim, 2007).
5. Kandungan kimia dadap serep
Tanaman dadap serep memiliki kandungan senyawa bioaktif seperti
alkaloid, flavonoid, isoflavonoid, saponin dan lektin. Flavonoid dan isoflavonoid
yang terkandung dalam tanaman dadap merupakan senyawa bioaktif yang
baru, senyawa bioktif tersebut juga menunjukan potensi sebagai senyawa
Gambar 1. Beberapa struktur senyawa isoflavonoid (Samanta, Das, dan Das, 2011)
B. Senyawa Fenolik
Senyawa fenolik merupakan metabolit sekunder dari alam dengan jumlah
senyawa yang besar (lebih dari 8.000) yang tersebar luas diseluruh kingdom
tanaman dan dikarakterisasi dengan setidaknya memiliki satu cincin aromatis
dengan satu atau lebih terikat dengan gugus hidroksil. Senyawa fenolik dapat
diklasifikasikan berdasarkan susunan dari atom karbon dalam flavonoid (flavonol,
flavon, flavan-3-ol, antosianidin, flavanon, isoflavon dan lainnya) dan
non-flavonoid (asam fenolat, hidroksinamat, stilben dan lainnya) dan
senyawa-senyawa tersebut umumnya berada terkonjugasi dengan gula dan asam organik
Flavonoid merupakan salah satu kelompok metabolit sekunder terbesar
sebagai senyawa fenolik. Flavonoid melindungi tanaman terhadap berbagai
ancaman biotik dan abiotik yang menunjukkan spektrum dengan beragam fungsi
biologis dan memainkan peran penting dalam interaksi antara tanaman dan
lingkungannya (Samanta et al., 2011). Senyawa fenolik mayoritas yang ada di
alam berada sebagai glikosida. Adanya gula dan gugus hidroksil membuat
senyawa fenolik larut dalam air sedangkan adanya gugus metil dan unit isopentil
membuat flavonoid menjadi lipofilik (Samanta et al., 2011).
Sebagian besar koleksi metabolit dari produk alam disebut dengan istilah
flavonoid yang mencakup senyawa dengan karbon berstruktur C6-C3-C6.
Tergantung pada posisi keterkaitan dari cincin aromatik ke bagian benzopiren,
kelompok produk alam ini dibagi menjadi tiga kelas: Flavonoid (2 -
fenilbenzopiren), isoflavonoid (3-benzopiren) dan Neoflavonoid (Samata et al.,
2011).
O
O
Flavonoids Isoflavonoids
(3-benzopyrans)
O
Neoflavonoids
Gambar 2. Klasifikasi flavonoid produk alam (Samata et al., 2011) C. Radikal Bebas
Reaktif oksigen spesies (ROS) adalah istilah yang meliputi semua
golongan radikal bebas. Jenis ROS termasuk radikal hidroksil, radikal anion
superoksida, hidrogen peroksida, singlet oksigen, radikal nitrat oksida, radikal
hipoklorit, dan berbagai lipid peroksida. Semua mampu bereaksi dengan membran
lipid, asam nukleat, protein, enzim dan molekul kecil lainnya, yang
mengakibatkan kerusakan sel (Sapakal et al, 2008).
Banyak bukti yang telah dikumpulkan untuk melihat kerusakan seluler
yang timbul akibat dari spesies oksigen reaktif (ROS), setidaknya sebagian, dalam
etiologi dan patofisiologi penyakit manusia seperti gangguan neurodegeneratif
(misalnya penyakit alzheimer, penyakit parkinson, multipel sklerosis, syndrom
down), peradangan, infeksi virus, autoimun patologi, dan gangguan sistem
pencernaan seperti peradangan pencernaan dan ulkus. Dalam sistem metabolisme
tubuh, radikal bebas dihasilkan sebagai bagian dari proses normal metabolisme
tubuh, dan reaksi berantai radikal bebas biasanya diproduksi di rantai pernapasan
mitokondria, campuran oksidase fungsi hati, dengan leukosit bakteri, melalui
aktivitas xantin oksidase, polusi atmosfer, dan dari transisi logam katalis, obat dan
xenobiotik. Selain itu, mobilisasi kimia dari cadangan lemak di bawah berbagai
kondisi seperti menyusui, olahraga, demam, infeksi dan bahkan puasa, dapat
menghasilkan peningkatan aktivitas radikal dan meningkatkan kerusakan,
khususnya yang berhubungan dengan kekebalan tubuh dan sistem saraf. Hormon
stres (adrenalin dan noradrenalin) yang disekresikan oleh kelenjar adrenal di
bawah kondisi stres emosional yang berkelanjutan dan berlebihan, yang
kemudian dimetabolisme menjadi lebih sederhana seperti molekul radikal bebas,
D. Antioksidan
Antioksidan merupakan suatu senyawa yang mampu menunda,
memperlambat atau menghambat reaksi oksidasi didalam tubuh. Antioksidan
mampu menstabilkan, atau menonaktifkan radikal bebas sebelum menyerang sel
dalam tubuh. Antioksidan merupakan senyawa yang penting untuk menjaga
kesehatan seluler dan kesehatan sistemik tubuh (Sapakal et al., 2008).
Senyawa antioksidan dapat dibedakan berdasarkan komposisi, sifat fisik
dan kimia, mekanisme dan tempat aksi dari senyawa antioksidan tersebut.
Enzim-enzim yang berperan sebagai antioksidan dalam tubuh seperti Enzim-enzim glutation
reduktase (GSH), superoksida dismutase (SOD), katalase (CAT), glutation
peroksidase (GPX), diketahui dapat melemahkan spesies oksigen reaktif dengan
menghilangkan potensi oksidan atau dengan mengubah spesies oksigen reaktif
dan spesies nitrogen reaktif menjadi senyawa yang stabil. Senyawa dengan bobot
molekul tinggi seperti protein : albumin, ceruplasmin, transferin, haptoglobin
mengikat logam aktif redoks dan membatasi produksi radikal bebas katalis logam.
Senyawa dengan berat molekul rendah dibagi menjadi antioksidan larut lemak
(tokoferol, karotenoid, kina dan beberapa polifenol) dan antioksidan yang larut air
(asam askorbat, asam urat dan beberapa polifenol). Senyawa antioksidan jenis
mineral: selenium, mangan, tembaga, dan seng diakui sebagai antioksidan yang
serbaguna. Senyawa antioksidan jenis vitamin: vitamin A, C, dan E ternyata
memiliki peran penting dalam mencegah atau meminimalkan kerusakan
peroksidasi dalam sistem biologis. Tanaman kaya antioksidan merupakan sumber
jeruk, biji sesame, daun teh hijau, biji kakao, anggur, tomat, jeruk, apel,
biji-bijian, zaitun, wortel (Sapakal et al.,2008).
Sumber-sumber antioksidan dapat berupa antioksidan sintetik maupun
antioksidan alami. Tetapi saat ini penggunaan antioksidan sintetik mulai dibatasi
karena ternyata dari hasil penelitian yang telah dilakukan bahwa antioksidan
sintetik seperti BHT (Butylated Hydroxy Toluena) ternyata dapat meracuni
binatang percobaan dan bersifat karsinogenik. Oleh karena itu industri makanan
dan obat-obatan beralih mengembangkan antioksidan alami dan mencari
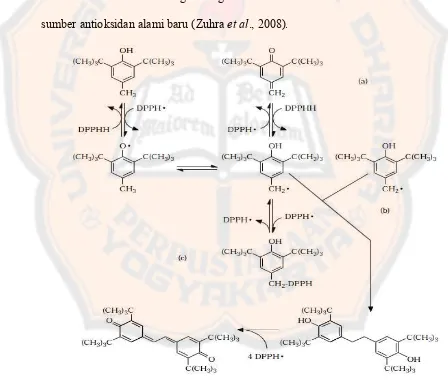
sumber-sumber antioksidan alami baru (Zuhra et al., 2008).
Gambar 3. Usulan mekanisme reaksi antara BHT dan DPPH ((a) donasi kedua atom hidrogen, (b) dimerisasi, (c) kompleksasi) (Bondet,
Tabel I. Berbagai Reactive Oxygen Species (ROS) dan antioksidan sebagai penetral (Sapakal et al., 2008)
Reactive Oxygen Species
(ROS) Senyawa antioksidan
Radikal hidroksil vitamin C, glutation, flavonoid, asam lipoid
Radikal superoksida vitamin C, glutation, flavonoid, SOD
Hidrogen peroksida
vitamin C, glutation, betakaroten, vitamin E, CoQ10, flavonoid, asam
lipoid
Lipid peroksida beta karoten, vitamin E, ubiquinon, flavonoid, glutation peroksidase
E. Penyarian
Penyarian adalah kegiatan penarikan zat atau metabolit aktif yang semula
berada didalam sel yang kemudian ditarik oleh cairan penyari sehingga zat aktif
tersebut larut dalam cairan penyari (Harborne, 1987). Secara umum, penyarian
dapat dibedakan menjadi infudasi, maserasi, perkolasi dan penyarian
berkesinambungan. Sebagai cairan penyari digunakan air, eter, atau campuran
etanol air (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1986).
Maserasi merupakan metode yang melibatkan perendaman dan
penggojogan bahan tanaman didalam pelarut tertentu yang kemudian pelarutnya
diuapkan (Raaman, 2006). Remaserasi merupakan modifikasi cara penyarian
maserasi. Pada proses remaserasi cairan penyari dibagi menjadi dua bagian.
diendap tuangkan dan diperas, ampas dimaserasi lagi dengan cairan penyari yang
kedua (Depkes, 1986). Alkohol didalam banyak penelitian merupakan pelarut
yang cocok untuk berbagai tujuan ekstraksi sebagai pelarut awal yang digunakan
dalam tahapan ekstraksi (Harborne, 1998).
Ekstraksi cair-cair digunakan sebagai cara untuk praperlakukan sampel
untuk memisahkan analit-analit dari komponen-komponen matriks yang mungkin
menganggu pada saat kuantifikasi atau deteksi analit. Ekstraksi cair-cair
ditentukan oleh distribusi Nerst atau hukum partisi yang menyatakan “pada
konsentrasi dan tekanan yang konstan, analit akan terdistribusi dalam proporsi
yang selalu sama diantara dua pelarut yang saling tidak campur”. Perbandingan
konsentrasi pada keadaan setimbang di dalam 2 fase disebut dengan koefisien
distribusi atau koefisien partisi (Kd) dan digambarkan dengan rumus : Kd = 𝑆 𝑜𝑟𝑔 𝑆 𝑎𝑞
Dimana [S]org dan [S]aq masing-masing merupakan konsentrasi analit dalam fase organik dan dalam fase air; Kd merupakan koefisien partisi. Efiseiensi proses ekstraksi tergantung pada nilai distribusinya dan juga tergantung pada
volume relative kedua fase. Adanya ekstaksi berulang (bertingkat) akan
meningkatkan efisiensi ekstraksi (Gandjar dan Rohman, 2007).
F. Metode DPPH dan Folin-Ciocalteu
Metode DPPH merupakan metode yang sering digunakan untuk menguji
aktivitas antioksidan. Metode ini bertujuan untuk mengetahui parameter
ini dapat dicapai dengan cara mengintepretasikan data eksperimental dari metode
tersebut (Molyneux, 2004).
Uji kuantitatif daya antioksidan dilakukan dengan metode DPPH
(1,1-difenil-2-pikrilhidrazil) secara spektrofotometri sinar tampak. Metode ini
didasarkan pada perubahan warna radikal DPPH. Perubahan warna tersebut
disebabkan oleh reaksi antara radikal bebas DPPH dengan satu atom hidrogen
yang dilepaskan senyawa yang terkandung dalam bahan uji untuk membentuk
senyawa 1,1-difenil-2-pikrilhidrazin yang berwarna kuning. Pada metode ini
absorbansi yang diukur adalah absorbansi larutan DPPH sisa yang tidak bereaksi
dengan senyawa antioksidan (Josephy, 1997).
NO2
DPPH Free Radical Phenolic Compounds DPPH Reduced Form
+ A
Gambar 4. Reaksi antara radikal DPPH dengan senyawa antioksidan (Irshad, Zafaryab, Singh, dan Rizvi, 2012)
Dalam metode DPPH, dengan adanya elektron bebas yang tidak
berpasangan pada senyawa radikal DPPH, senyawa tersebut memberikan serapan
maksimum yang kuat pada panjang gelombang 517 nm dan memberikan warna
absorptivitas molar radikal DPPH pada 517 nm dari 9660 ke 1640 ketika elektron
bebas radikal DPPH dipasangkan dengan hidrogen dari senyawa antioksidan
radikal bebas untuk membentuk senyawa DPPH-H. Dengan demikian hasil
dekolorisasi yang terjadi memberikan nilai stoikiometri sehubungan dengan
jumlah elektron yang ditangkap (Prakash, 2001).
Metode Folin-Ciocalteu (F-C) merupakan metode kolorimetri yang
sering digunakan yang berdasarkan reaksi oksidasi yang cepat dari fenol dengan
menggunakan senyawa alkali, umumnya menggunakan sodium karbonat, yang
akan menghasilkan ion fenolat yang cukup besar. Senyawa fenolat yang terbentuk
mereduksi warna kuning F-C menjadi berwarna biru, yang dapat diukur secara
spektrofotometri ( Cicco dan Lattanzio, 2011).
G. Validasi Metode
Validasi metode dilakukan untuk menjamin bahwa metode analisis dapat
memberikan hasil seperti yang diharapakan dengan akurat, spesifik, reprodusibel,
dan tahan pada kisaran analit yang akan dianalisis (Gandjar dan Rohman, 2007).
Akurasi merupakan ketelitian metode analisis atau kedekatan antara nilai
terukur dengan nilai yang diterima baik nilai konvensi, nilai sebenarnya atau nilai
rujukan. Untuk mendokumentasikan akurasi, ICH (International Conference on
Harmanization) merekomendasikan pengumpulan data dari 9 kali penetapan
kadar dengan 3 konsentrasi yang berbeda (misal 3 konsentrasi dengan 3 kali
replikasi). Data harus dilaporkan sebagai persentase perolehan kembali (recovery)
(Gandjar dan Rohman, 2007). Rata-rata persen recovery yang dihasilkan
Tabel II. Kisaran recovery hasil analisis yang diterima (APMVA, 2004)
% Senyawa
impuritis/aktif Rata-rata recovery yang diterima
≥ 10 98-102 %
≥ 1 90-110 %
0,1-1 80-120 %
< 1 75-125 %
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
diekspresikan sebagai simpangan baku relatif dari sejumlah sampel yang berbeda
signifikan secara statistik (Gandjar dan Rohman, 2007).
Tabel III. Kriteria nilai presisi yang masih dapat diterima (APVMA, 2004)
Kadar zat aktif (%)
Nilai KVyang masih dapat diterima (%)
≥ 10 ≤ 2
1-10 ≤ 5
0,1-1 ≤ 10
<0,1 ≤ 20
Spesifisitas adalah kemampuan untuk mengukur analit yang dituju secara
tepat dan spesifik dengan adanya komponen-komponen lain dalam matriks sampel
seperti ketidakmurnian, produk degradasi, dan komponen matriks (Gandjar dan
Rohman, 2007). Jika respon yang dihasilkan dari suatu metode dapat
tersebut dapat dikatakan selektif. Selektifitas suatu metode analisis dapat
ditunjukan dengan menampilkan data yang menggambarkan tidak adanya
interferensi dari hasil produk degradasi dan senyawa yang dapat menyebabkan
interferensi lainnya dalam matriks (APVMA, 2004).
Linearitas merupakan kemampuan suatu metode untuk memperoleh
hasil-hasil uji yang secara langsung proporsional dengan konsentrasi analit pada
kisaran yang diberikan. Linearitas suatu metode merupakan ukuran seberapa baik
kurva kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x)
(Gandjar dan Rohman, 2007).
H. Landasan Teori
Radikal bebas adalah atom atau molekul yang tidak stabil dan sangat
reaktif yang merupakan salah satu faktor penyebab kerusakan sel dalam tubuh.
Untuk mengurangi dampak kerusakan yang diakibatkan dari radikal bebas,
dibutuhkan senyawa antioksidan yang merupakan suatu senyawa yang mampu
menunda, memperlambat atau menghambat reaksi oksidasi didalam tubuh yang
dapat berasal dari radikal bebas. Antioksidan mampu menstabilkan atau
menonaktifkan radikal bebas sebelum menyerang sel dalam tubuh.
Sumber-sumber antioksidan dapat berupa antioksidan sintetik maupun antioksidan alami
yang berasal dari tanaman.
Secara empiris tanaman dadap serep digunakan sebagai bahan obat
tradisional yang digunakan untuk mengobati batuk, sakit kepala, demam dan
minuman bagi wanita sehabis melahirkan. Tanaman dadap serep memiliki
lektin. Adanya berbagai kandungan senyawa fenolik disamping saponin dan lektin
dalam tanaman dadap serep tersebut memberikan kemungkinan besar bahwa
tanaman ini memiliki aktivitas sebagai antioksidan.
Pengujian aktivitas antioksidan dari suatu sampel uji dapat dilakukan
dengan menggunakan metode DPPH. Metode ini didasarkan pada perubahan
warna radikal DPPH yang disebabkan oleh reaksi antara radikal bebas DPPH
dengan senyawa antioksidan yang menyumbangkan satu atom hidrogen yang
dilepaskan senyawa yang terkandung dalam bahan uji untuk membentuk senyawa
1,1-difenil-2-pikrilhidrazin yang berwarna kuning, sisa DPPH yang tidak bereaksi
diukur secara spektrofotometri sinar tampak.
Kandungan senyawa fenolik dari suatu sampel dapat diukur dengan
metode Folin-Ciocalteu (F-C). Metode ini berdasarkan reaksi oksidasi yang cepat
dari fenol dengan menggunakan senyawa alkali, umumnya menggunakan sodium
karbonat, yang akan menghasilkan ion fenolat yang cukup besar. Senyawa fenolat
yang terbentuk mereduksi warna kuning F-C menjadi berwarna biru, yang dapat
diukur secara spektrofotometri.
I.Hipotesis
Fraksi etil asetat ekstrak etanolik daun dadap serep mempunyai aktivitas
antioksidan yang dapat diukur dengan metode DPPH yang dinyatakan dengan
IC50. Kandungan fenolik total fraksi etil asetat ekstrak etanolik daun dadap serep dapat diukur dengan metode Folin-Ciocalteu yang dinyatakan dengan massa
20
BAB III
METODOLOGI PENELITIAN A. Jenis dan Rancangan Penelitian
Penelitian ini merupakan jenis penelitian eksperimental karena subjek uji
diberi perlakuan.
B. Variabel
1. Variabel bebas berupa konsentrasi fraksi etil asetat ekstrak etanolik daun dadap
serep.
2. Variabel tergantung berupa aktivitas antioksidan dan kandungan fenolik total
fraksi etil asetat ekstrak etanolik daun dadap serep.
3. Variabel pengacau terkendali berupa tempat tumbuh tanaman, waktu
pemanenan dan cara panen.
4. Variabel pengacau tidak terkendali berupa cahaya matahari, cuaca, kelembaban,
curah hujan.
C. Definisi Operasional
1. Daun dadap serep adalah daun (folium) segar dari tanaman dadap serep yang
dipanen dari Kebun Tanaman Obat Fakultas Farmasi Universitas Sanata
Dharma (Yogyakarta) dengan bentuk daun belah ketupat, dengan lebar ± 10-17
cm, berwarna hijau.
2. Ekstrak etanolik daun dadap serep adalah sari hasil proses maserasi daun dadap
serep dengan penyari etanol.
3. Fraksi etil asetat adalah hasil fraksinasi ekstrak etanolik daun dadap serep
4. Persen inhibition concentration (%IC) adalah persen yang menyatakan
kemampuan fraksi etil asetat ekstrak etanolik daun dadap serep untuk
menangkap radikal DPPH.
5. Nilai inhibition concentration 50 (IC50) adalah nilai konsentrasi fraksi etil
asetat ekstrak etanolik daun dadap serep yang menghasilkan penangkapan 50%
radikal DPPH.
D. Bahan dan Alat Penelitian 1. Bahan penelitian
Bahan yang digunakan dalam penelitian ini adalah: daun dadap serep
yang diambil dari kebun tanaman obat Fakultas Farmasi Universitas Sanata
Dharma Yogyakarta, akuades (Laboratorium Kimia Analisis Instrumental
Fakultas Farmasi Universitas Sanata Dharma); bahan kualitas p.a. E. Merck,
yaitu: metanol, bahan kualitas p.a. Sigma Chem. Co., USA, yaitu: DPPH, reagen
Folin-Ciocalteu, asam galat, dan kuersetin kualitas Sigma Chem. Co., USA; bahan
kualitas teknis Brataco Chemica, yaitu: wasbensin dan etil asetat; bahan kualitas
teknis CV. General Labora, yaitu: metanol; dan aluminium foil.
2. Alat penelitian
Alat yang digunakan dalam penelitian ini adalah: neraca analitik (Scaltec
SBC 22, BP 160P), vacuum rotary evaporator (Junke & Kunkel), waterbath
(labo-tech, Heraeus), vortex (Janke & Kunkel), spektrofotometer UV-Vis (Perkin
Elmer Lamda 20), blender, corong Buchner, oven, mikropipet 10-1000μL; 1-10
mL (Acura 825, Socorex), tabung reaksi bertutup, dan alat-alat gelas yang lazim
E. Tatacara Penelitian 1. Determinasi tumbuhan
Determinasi tanaman dadap serep dilakukan di Laboratorium
Farmakognosi-Fitokimian, Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta.
2. Pengumpulan bahan
Tanaman dadap serep diperoleh dari kebun tanaman obat Fakultas
Farmasi Universitas Sanata Dharma di Yogyakarta. Pengumpulan pada musim
kemarau bulan Agustus tahun 2012. Pemanenan dilakukan pada tanaman saat pagi
hari.
3. Preparasi sampel
Daun dadap serep segar dicuci dengan air mengalir, dikering-anginkan,
dan ditimbang sebanyak 1 kg, kemudian dihaluskan dengan grinder. Ketika
dihaluskan, daun tersebut ditambahkan sedikit cairan penyari (etanol 76%).
Simplisia yang telah dihaluskan ditimbang 100 g dan dituang kedalam bejana
maserasi, ditambah etanol 76% sampai terendam sempurna, dan dicampur
homogen. Campuran dimaserasi pada suhu ruangan selama dua hari. Filtrat
diperoleh melalui penyaringan dengan corong Buchner. Ampas penyaringan
diremaserasi dengan etanol 76% secukupnya selama dua hari. Kemudian filtratnya
dicampurkan dengan filtrat terdahulu. Campuran filtrat kemudian disaring. Lalu
hasil penyaringan filtrat diuapkan pelarutnya dengan vacuum rotary evaporator
Ekstrak etanol daun dadap serep ditambah 300 mL air hangat dan
diekstraksi cair-cair menggunakan wasbensin dengan perbandingan larutan
ekstrak : wasbensin (1:1 v/v), kemudian didiamkan sampai terpisah sempurna.
Fase air akan berada pada bagian bawah, sedangkan fase wasbensin berada pada
bagian atas.
Dari hasil partisi diperoleh dua fraksi, yaitu fraksi wasbensin dan fraksi
air. Selanjutnya fraksi air diekstraksi cair-cair lagi menggunakan etil asetat dengan
perbandingan larutan fraksi air : etil asetat (1:1 v/v) sehingga didapatkan fraksi air
dan etil asetat. Setelah dipisahkan fraksi etil asetat diuapkan pelarutnya dengan
vacuum rotary evaporator. Hasil fraksi tersebut kemudian ditutup dengan plastik
serta aluminium foil lalu disimpan dalam desikator. Lalu hasil fraksi tersebut
digunakan untuk dianalisis lebih lanjut.
4. Pembuatan larutan pembanding dan uji
a. Pembuatan larutan DPPH
Sejumlah DPPH dilarutkan ke dalam metanol p.a sehingga diperoleh
larutan DPPH dengan konsentrasi 0,4 mM. Larutan tersebut ditutup dengan
alumunium foil dan harus selalu dibuat baru.
b. Pembuatan larutan stok kuersetin
Sebanyak 2,5 mg kuersetin dilarutkan dengan metanol p.a sampai 10,0
mL.
c. Pembuatan larutan pembanding
Diambil sebanyak 0,2; 0,3; 0,4; 0,5; 0,6 mL larutan stok kuersetin,
kemudian ditambahkan metanol p.a sampai 10,0 mL, sehingga diperoleh
d. Pembuatan larutan uji
1. Larutan uji untuk aktivitas antioksidan
Sebanyak 12,5 mg hasil fraksi etil asetat ditimbang, lalu di add
metanol p.a sampai 25,0 mL. Diambil sebanyak 1,5; 3; 4,5; 6; 7,5 mL larutan
tersebut, kemudian ditambahkan metanol p.a sampai 10,0 mL, sehingga
diperoleh konsentrasi larutan uji sebesar 75; 150; 225; 300; 375 μg/mL.
2. Larutan uji untuk penentuan kandungan fenolik total
Sebanyak 5,0 mg hasil fraksi etil asetat ditimbang, lalu ditambahkan
metanol p.a sampai diperoleh konsentrasi larutan uji sebesar 500,0 µg/mL.
e. Pembuatan larutan asam galat
Dibuat larutan asam galat dengan konsetrasi 500 µg/mL dalam
akuades : methanol p.a (1:1). Diambil sebanyak 1,0; 1,5; 2,0; 2,5; dan 3,0 mL
larutan tersebut, kemudian ditambahkan akuades : metanol p.a (1:1) sampai
10,0 mL, sehingga diperoleh konsentrasi larutan baku asam galat sebesar 50;
75; 100; 125; dan 150 µg/mL.
5. Uji pendahuluan
a. Uji fenolik
Sejumlah 0,5 mL larutan uji 500,0 µg/mL dan larutan pembanding
asam galat 150,0 µg/mL dimasukan ke dalam 3 tabung reaksi. Lalu
ditambahkan 5 mL pereaksi fenol Folin-Ciocalteu yang telah diencerkan
dengan akuades (1:10 v/v) kedalam tabung reaksi. Diamkan selama 10 menit.
Tambahkan 4 mL larutan natrium karbonat 1 M. Kemudian amati warna
b. Uji pendahuluan aktivitas antioksidan
Sebanyak 1 mL larutan DPPH dimasukan ke dalam masing-masing
tiga tabung reaksi. Ditambahkan masing-masing dengan 1 mL metanol p.a,
larutan pembanding kuersetin 37,5 μg/mL , dan larutan uji 200,0 μg/mL.
Selanjutnya, larutan tersebut ditambahkan dengan 3 mL metanol p.a. Larutan
tersebut kemudian divortex selama 30 detik. Setelah 30 menit, amati warna
pada larutan tersebut.
6. Optimasi metode uji aktivitas antioksidan
a. Penentuan panjang gelombang serapan maksimum
Pada 3 labu ukur 10 mL, dimasukan masing-masing 0,5; 1,0; 1,5 mL
larutan DPPH. Ditambahkan larutan tersebut dengan metanol p.a hingga tanda
batas sehingga konsentrasi DPPH menjadi 0,020; 0,040; dan 0,080. Larutan
tersebut kemudian divortex selama 30 detik. Diamkan selama OT. Lalu
dilakukan scanning panjang gelombang serapan maksimum dengan
spektrofotometer visibel pada panjang gelombang 400-600 nm.
b. Penentuan operating time (OT)
Sebanyak 2 mL larutan DPPH dimasukan kedalam masing-masing 3
labu ukur 10 mL, ditambahkan masing-masing dengan 2 mL larutan
pembanding kuersetin 5; 10 dan 15 μg/mL. Selanjutnya larutan tersebut
ditambahkan dengan metanol p.a hingga tanda batas. Larutan tersebut
kemudian divortex selama 30 detik. Setelah itu dibaca absorbansinya dengan
spektrofotometer visibel pada panjang gelombang serapan maksimum selama 1
7. Uji aktivitas antioksidan
Uji aktivitas antioksidan ditentukan dengan menggunakan metode
spoktrofotometri sesuai dengan penelitian Rollando (2012).
a. Pengukuran absorbansi larutan DPPH (kontrol)
Pada labu ukur 10 mL, dimasukan sebanyak 2 mL larutan DPPH.
Ditambahan larutan tersebut dengan metanol p.a hingga tanda batas. Kemudian
larutan tersebut dibaca absorbansinya pada saat OT dan panjang gelombang
maksimum. Pengerjaan dilakukan sebanyak 3 kali. Larutan ini digunakan
sebagai kontrol untuk menguji larutan pembanding dan uji.
b. Pengukuran absorbansi larutan pembanding dan uji
Sebanyak 1 mL larutan DPPH dimasukkan ke dalam tabung reaksi
bertutup kemudian ditambah dengan 1 mL larutan pembanding dan uji pada
berbagai seri konsentrasi telah dibuat. Selanjutnya larutan tersebut ditambah
dengan metanol p.a hingga tanda batas. Larutan tersebut kemudian divortex
selama 30 detik dan diamkan selama OT. Larutan dibaca absorbansinya dengan
spektrofotometer visibel pada panjang gelombang maksimum hasil optimasi.
Pengujian dilakukan dengan 3 kali replikasi.
c. Validasi metode uji aktivitas antioksidan
Hasil dari prosedur 7 a dan b, divalidasi presisi (%CV), spesifisitas
(spektra kontrol), dan linearitas (nilai r).
% CV = 𝑆𝑡𝑎𝑛𝑑𝑎𝑟 𝐷𝑒𝑣𝑖𝑎𝑠𝑖 𝑆𝐷 𝑘𝑜𝑛𝑠𝑒𝑡𝑟𝑎𝑠𝑖 𝑡𝑒𝑟𝑢𝑘𝑢𝑟
d. Estimasi aktivitas antioksidan
Hasil dari prosedur 7 a dan b, dihitung nilai % IC dan IC50 untuk kuersetin dan fraksi etil asetat ekstrak etanolik daun dadap serep.
8. Optimasi metode penetapan kandungan fenolik total
Optimasi metode penetapan kandungan fenolik total ditentukan dengan
menggunakan metode spektrofotometri.
a. Penentuan OT
Sebanyak 0,5 mL larutan asam galat 50; 100; dan 150 μg/mL
ditambahkan dengan 5 mL reagen Folin-Ciocalteu yang telah diencerkan dengan
air (1:10 v/v). Larutan selanjutnya ditambahkan dengan 4,0 mL natrium karbonat
1 M. Setelah itu, dibaca absorbansinya dengan spektrofotometer visibel pada
panjang gelombang 750 nm selama 30 menit.
b. Penentuan panjang gelombang maksimum
Sebanyak 0,5 mL larutan asam galat 50; 100; dan 150 μg/mL
ditambahkan dengan 5 mL reagen Folin-Ciocalteu yang telah diencerkan dengan
air (1:1 v/v). Larutan selanjutnya ditambahkan dengan 4,0 mL natrium karbonat 1
M. Diamkan selama OT, absorbansinya dibaca pada λ maksimum dengan
spektrofotometer visibel pada panjang gelombang 600-800 nm.
9. Penetapan kandungan fenolik total
a. Pembuatan kurva baku asam galat
Sebanyak 0,5 mL larutan asam galat 50; 75; 100; 125; dan 150 μg/mL
ditambah dengan 5 mL reagen Folin-Ciocalteu yang telah diencerkan dengan air
Setelah OT, absorbansinya dibaca pada λ maksimum terhadap blanko yang terdiri
atas akuades : metanol p.a (1:1), reagen Folin-Ciocalteu dan larutan natrium
karbonat 1 M. Pengerjaan dilakukan 3 kali.
b. Validasi metode penetapan kandungan fenolik total
Hasil dari prosedur 9 a , divalidasi presisi (%CV), spesifisitas (spektra
kontrol), dan linearitas (nilai r).
% CV = 𝑆𝑡𝑎𝑛𝑑𝑎𝑟 𝐷𝑒𝑣𝑖𝑎𝑠𝑖 𝑆𝐷 𝑘𝑜𝑛𝑠 𝑒𝑡𝑟𝑎𝑠𝑖 𝑡𝑒𝑟𝑢𝑘𝑢𝑟
𝑟𝑎𝑡𝑎 −𝑟𝑎𝑡𝑎𝑘𝑜𝑛𝑠𝑒𝑛𝑡𝑟𝑎𝑠𝑖 𝑡𝑒𝑟𝑢𝑘𝑢𝑟 x 100%
c. Estimasi kandungan fenolik total larutan uji
Diambil 0,5 mL larutan uji 500 μg/mL, lalu masing-masing dimasukan ke
dalam labu takar 10,0 mL dan dilanjutkan sebagaimana perlakuan pada
pembuatan kurva baku asam galat . Kandungan fenolik total dinyatakan sebagai
gram ekivalen asam galat (mg ekivalen asam galat per g fraksi etil asetat).
Lakukan 3 kali replikasi.
F. Analisis Hasil
Aktivitas penangkapan radikal DPPH (%) dihitung dengan rumus :
Absorbansi (larutan kontrol) – Absorbansi sampel (larutan pembanding/uji) X 100%
Absorbansi larutan control
Data aktivitas tersebut dianalisis dan dihitung nilai IC50 mengunakan persamaan regresi linear dengan sumbu x adalah konsentrasi larutan uji maupun
untuk menentukan ada atau tidak adanya perbedaan bermakna antara IC50 larutan pembanding dan larutan uji.
Uji kandungan fenolik total menghasilkan nilai mg ekivalen asam galat
dalam per g fraksi etil asetat. Nilai tersebut didapatkan dari analisis regresi linier
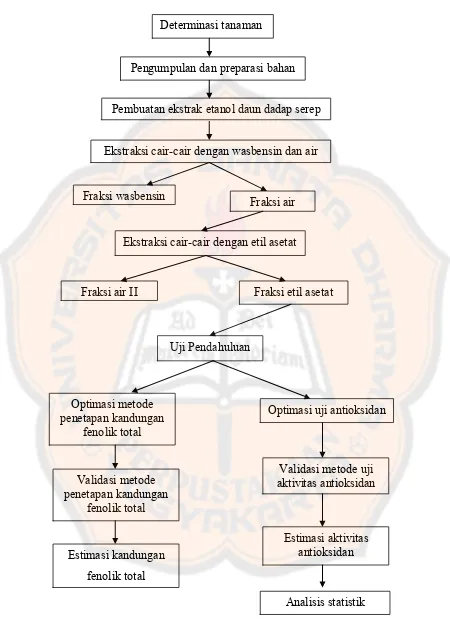
Gambar 5. Skema jalannya penelitian
Determinasi tanaman
Pengumpulan dan preparasi bahan
Pembuatan ekstrak etanol daun dadap serep
Ekstraksi cair-cair dengan wasbensin dan air
Fraksi wasbensin
Fraksi air
Ekstraksi cair-cair dengan etil asetat
31
BAB IV
HASIL DAN PEMBAHASAN A. Determinasi
Dalam penelitian ini langkah pertama yang dilakukan adalah determinasi
tanaman yang akan digunakan sebagai sampel uji. Tujuan dilakukannya
determinasi adalah untuk mengetahui kebenaran identitas tanaman yang
digunakan serta untuk menghindari kesalahan dalam penggunaan tanaman saat
dilakukan penelitian. Determinasi tanaman dadap serep dilakukan di
Laboratorium Farmakognosi-Fitokimia, Fakultas Farmasi Universitas Sanata
Dharma dengan acuan buku Flora of Java (Backer and Bakhuizen van den Brink,
1965). Dari hasil determinasi (lampiran 1) yang dilakukan terbukti bahwa
tanaman yang digunakan dalam penelitian ini adalah dadap serep (Erythrina
subumbrans (Hassk.) Merr.).
B. Hasil Pengumpulan Bahan
Daun dadap serep yang digunakan diperoleh dari kebun tanaman obat
Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta. Daun dipanen tanggal
21 september 2012. Daun dadap serep dipilih yang tidak layu, tidak terdapat bekas
luka daun, masih berwarna hijau dan masih segar. Adanya luka daun pada
tanaman dapat menyebabkan timbulnya respon enzimatik terhadap luka pada daun
tanaman tersebut. Polifenol oksidase merupakan suatu enzim ekstraseluler yang
akan mengoksidasi senyawa fenolik menjadi bentuk radikal dan membentuk
(1987), senyawa fenol pada tanaman sangat peka terhadap adanya proses oksidasi
enzim yang mungkin dapat berakibat hilangnya senyawa fenol. Berkurangnya
senyawa fenolik pada daun maka dapat mengakibatkan pada berkurangnya
aktivitas antioksidan. Seleksi ini dilakukan untuk menjaga kualitas daun yang
akan digunakan sehingga kemungkinan terjadinya pengurangan mutu sampel daun
akibat sudah terjadinya perubahan kandungan kimia daun dari proses perubahan
metabolisme tumbuhan dapat dihindari. Daun kemudian dicuci, dibersihkan
dengan air bersih yang mengalir untuk menghilangkan sisa-sisa partikel debu,
pengotor lain serta kontaminan yang masih tertinggal di daun.
Proses pemanenan dan preparasi simplisia merupakan proses yang dapat
menentukan mutu simplisia daun dadap serep yang akan digunakan sebagai
sampel uji, oleh karena itu diperlukan prosedur baku dalam proses tersebut.
Waktu terbaik untuk pemanenan daun (kualitas pada puncak musim atau waktu
pada hari pemanenan) harus ditentukan sesuai dengan kualitas dan kuantitas
konstituen aktif biologis dari hasil vegetatif total bagian tanaman obat yang
ditargetkan. Dalam pemanenan daun dadap serep dipilih pada saat pagi hari untuk
mendapatkan hasil metabolit sekunder dari tanaman secara maksimal dan tidak
dalam kondisi basah (hujan atau embun) atau dalam kondisi kelembaban tinggi
untuk mengurangi kemungkinan terjadinya kontaminasi oleh mikroba pada
tanaman. Kontaminasi mikroba pada tanaman dapat mengakibatkan berubahnya
metabolisme dari tanaman tersebut. Hal ini dikarenakan adanya senyawa
fitotoksin yang dihasilkan oleh mikroba yang merupakan hasil sintesis mikroba
menginduksi tanaman untuk memproduksi senyawa fitoaleksin yang merupakan
senyawa hasil metabolisme tanaman sebagai pertahanan atas serangan mikroba.
Menurut Harborne (1987), senyawa fitoaleksin pada tanaman dapat berupa
seskuiterpenoid, isoflavonoid, asetilena, atau senyawa fenol. Apabila senyawa
fitoaleksin diproduksi berlebih pada tanaman sebagai tanggapan atas serangan
mikroba, maka jumlah senyawa fenol yang dibutuhkan sebagai sumber fitoaleksin
akan bertambah. Hal ini dapat menimbulkan kandungan senyawa fenol yang
merupakan metabolit sekunder tanaman yang dapat berfungsi sebagai senyawa
antioksidan akan berkurang akibat digunakannya senyawa fenol sebagai sumber
fitoaleksin.
Daun dadap yang telah diperoleh dan dicuci kemudian dikeringkan
sebelum ekstraksi. Menurut World Health Organization (2003), dalam proses
pengeringan, kelembapan udara pada tempat pengeringan diperhatikan dan dijaga
untuk menghindari kelembapan udara berlebih yang dapat menimbulkan
tumbuhnya kontaminan jamur pada daun. Pengeringan dilakukan dalam keadaan
terawasi untuk mencegah terjadinya perubahan kimia yang mungkin terjadi. Daun
dadap serep yang diperoleh dikeringkan segera tanpa menggunakan suhu tinggi
dan dalam aliran udara yang baik. Setelah daun dadap serep benar-benar kering,
C. Hasil Preparasi Sampel
1. Ekstraksi sampel
Serbuk simplisia yang digunakan kemudian diekstraksi dengan cairan
penyari etanol 76%. Menurut Harborne (1998), etanol didalam banyak penelitian
merupakan pelarut yang cocok untuk berbagai tujuan ekstraksi sebagai pelarut
awal yang digunakan dalam tahapan ekstraksi. Metode penyarian yang digunakan
adalah dengan maserasi. Pemilihan metode ini karena dengan metode ini sampel
yang digunakan tidak mengalami perlakuan pemanasan sehingga senyawa yang
tidak cocok dengan pemanasan terjaga stabilitasnya. Maserasi dilakukan selama
dua hari dan dilanjutkan remaserasi selama dua hari. Selama proses maserasi
dilakukan, digunakan juga shaker sebagai alat untuk membantu penggojogan.
Penggojogan dilakukan untuk meningkatkan kontak antara cairan penyari yang
digunakan dengan sampel, sehingga proses ekstraksi metabolit yang terkandung
dalam sampel dapat berjalan lebih efektif dan mendapatkan hasil penyarian yang
maksimal. Remaserasi dalam penelitian ini dilakukan untuk memaksimalkan
hasil perolehan penyarian dari senyawa yang belum tersari akibat sudah jenuhnya
cairan penyari yang digunakan.
Hasil dari proses maserasi dan remaserasi dikumpulkan yang kemudian
disaring dengan corong Buchner yang dilapisi kertas saring dan diintegrasikan
dengan pompa vacuum sehingga proses penyaringan lebih cepat. Filtrat hasil
penyaringan tersebut kemudian diuapkan pelarutnya menggunakan alat vacuum
rotary evaporator. Alat tersebut dapat menguapkan pelarut yang digunakan
vakum, sehingga dapat memperkecil kemungkinan rusaknya senyawa yang
terkandung didalamnya. Perolehan bobot ekstrak daun dadap serep adalah sebesar
14,235 g.
2. Fraksinasi ekstrak
Struktur senyawa aktif dalam tanaman sangat bervariasi. Perbedaaan ini
dipengaruhi golongan dan substituen dari senyawa tersebut. Hal ini dapat
menyebabkan perbedaan polaritas dari tiap-tiap senyawa tersebut sehingga untuk
mengekstraksi senyawa aktifnya diperlukan pelarut dengan polaritas yang
bertingkat. Menurut Snyder (1997), proses fraksinasi akan memisahkan
komponen aktif dari ekstrak daun kedalam fraksi polar, semi polar dan fraksi non
polar. Etanol merupakan salah satu pelarut universal yang dapat menyari banyak
senyawa kimia seperti klorofil, minyak, vitamin dan mineral. Oleh sebab itu
dalam penelitian ini dilakukan fraksinasi yang bertujuan untuk memisahkan
senyawa didalam ekstrak sehingga yang didapat adalah
senyawa-senyawa yang dituju yaitu senyawa-senyawa fenolik. Dalam melakukan fraksinasi dalam
penelitian ini menggunakan prinsip ektraksi cair-cair dimana merupakan teknik
ekstraksi yang menggunakan dua pelarut yang tidak tercampurkan yang
menimbulkan perpindahan senyawa terlarut dari satu pelarut ke pelarut kedua.
Ekstrak yang didapat kemudian dilarutkan dengan air hangat agar lebih
mudah untuk melarutkan ekstrak kental. Fraksinasi dilakukan dengan wasbensin
yang merupakan pelarut non polar. Penggunaan wasbensin yang merupakan
senyawa non polar dimaksudkan untuk mengekstraksi senyawa-senyawa non
menggunakan corong pisah. Dalam corong pisah, fraksi air akan berada dibagian
bawah sedangkan fraksi wasbensin ada di bagian atas. Hal ini dikarenakan adanya
perbedaan bobot jenis antara wasbensin dan air. Fraksi air yang mengandung
senyawa polar seperti fenolik disimpan, sedangkan fraksi wasbensin yang
mengandung klorofil, minyak, lemak dan vitamin tidak digunakan dalam
penelitian ini.
Tahap selanjutnya melakukan fraksinasi kembali dari fraksi air yang
diperoleh menggunakan pelarut etil asetat. Menurut Robinson (1995),
pengekstraksian kembali fraksi air dengan pelarut organik yang tidak bercampur
dengan air tetapi agak polar sering kali bermanfaat untuk memisahkan golongan
fenolik seperti senyawa-senyawa flavonoid dari senyawa yang lebih polar seperti
karbohidrat. Etil asetat merupakan pelarut yang baik untuk ini. Fraksi air akan
berada dibagian bawah dan fraksi etil asetat yang berbobot jenis lebih kecil dari
bobot jenis air akan berada diatas. Fraksi etil asetat akan mengkestraksi senyawa
fenolik aglikon sedangkan senyawa seperti antosianin, glikosida flavonoid akan
berada dalam fraksi air.
Dalam melakukan fraksinasi, dilakukan dengan perbandingan yang sama
antara pelarut etil asetat, wasbensin dan air dengan masing-masing menggunakan
100 mL fraksi. Menurut Gandjar dan Rohman (2007), fraksinasi juga dilakukan
secara berulang sebanyak tiga kali karena ekstraksi berulang dengan volume yang
sama akan lebih efektif dibanding melakukan ekstraksi tunggal dengan volume
aglikonnya bersifat cenderung non polar, sehingga tidak menutup kemungkinan
adanya senyawa tersebut larut dalam air maupun etil asetat.
Setelah didapat fraksi etil asetat, fraksi kemudian diuapkan menggunakan
vaccum rotary evaporator untuk meminimalkan pemaparan pemanasan supaya
stabilitas senyawa fenolik tetap terjaga. Sisa fraksi etil asetat kemudian
dimasukkan kedalam oven dengan suhu 40 oC untuk menguapakan sisa pelarut sehingga didapatkan ekstrak kental. Fraksi kental etil asetat dalam cawan petri
kemudian dibungkus dengan plastik dan ditutup dengan alumunium foil supaya
tidak terkena udara dan tidak terpapar sinar UV yang dapat mendegradasi
senyawa fenolik yang ada didalam fraksi etil asetat. Fraksi etil asetat yang sudah
dibungkus dimasukan didalam desikator agar tidak terpapar lembab dan
ditumbuhi jamur atau mikroba. Bobot fraksi etil asetat yang didapat sebesar 0,424
g dan rendemen fraksi etil asetat yang didapat adalah 0,424 %.
D. Hasil Uji Pendahuluan
1. Uji pendahuluan aktivitas antioksidan
Tujuan uji pendahuluan aktivitas antioksidan adalah untuk mengetahui
secara kualitatif adanya senyawa yang berpotensi memiliki aktivitas antioksidan
di dalam fraksi etil asetat ekstrak etanolik daun dadap serep. Uji ini menggunakan
radikal DPPH dengan kuersetin sebagai pembanding dan fraksi etil asetat ekstrak
etanolik sebagai sampel uji. Uji ini perlu dilakukan sebelum uji kuantitatif dimana
dapat menentukan langkah perlu dilakukannya uji kuantitatif aktivitas antioksidan
Uji ini dilakukan menggunakan tabung reaksi dengan menambahkan
sejumlah larutan kuersetin dan fraksi etil asetat ekstrak etanolik daun dadap serep
ke larutan DPPH. Keberadaan senyawa antioksidan dapat menyebabkan terjadinya
peluruhan warna larutan dari ungu ke kuning.
Gambar 6. Blanko DPPH (B), Fraksi etil asetat (A), Kuersetin (C)
Dalam uji ini digunakan kontrol positif berupa larutan DPPH yang
ditambah kuersetin untuk menunjukan warna larutan jika hasilnya positif (Gambar
5). Kontrol negatif dalam penelitian ini menggunakan larutan DPPH untuk
menunjukan warna larutan apabila hasil uji negatif (Gambar 5). Dari hasil uji yang
dilakukan terlihat adanya penurunan intensitas warna larutan uji fraksi etil asetat
ekstrak etanolik dari warna ungu menjadi kuning (Gambar 5). Ini menunjukan
bahwa hasil pengujian positif dan didalam fraksi etil asetat ekstrak etanolik daun
1. Uji pendahuluan senyawa fenolik
Uji ini bertujuan untuk mengetahui adanya kandungan senyawa fenolik
dalam fraksi etil asetat ekstrak etanolik daun dadap serep. Pengujian dilakukan
dengan metode Folin-Ciocalteau yang didasarkan pada reaksi oksidasi-reduksi
dalam suasana basa. Pengujian dilakukan dengan mencampurkan fraksi etil asetat
ekstrak etanolik daun dadap serep dengan pereaksi Folin-Ciocalteau. Menurut
Cicco dan Lattanzio (2011), reaksi yang terjadi yaitu adanya oksidasi senyawa
fenol dalam suasana basa, yang pada umumnya menggunakan sodium karbonat,
yang mana biasanya akan menghasilkan ion fenolik yang cukup banyak. Ion
fenolat yang terbentuk akan mereduksi warna kuning dari reagen Folin-ciocalteau.
Reaksi positif dari metode ini membentuk kompleks warna biru. Semakin tinggi
kadar fenol pada sampel, semakin banyak produk molekul berwarna biru,
akibatnya intensitas warna biru semakin tinggi.
Uji ini menggunakan kontrol negatif, yaitu pereaksi Folin-Ciocalteu
untuk menunjukan warna larutan jika hasilnya negatif (Gambar 6). Kontrol
positif dalam uji ini menggunakan pereaksi Folin-Ciocalteu yang ditambah asam
galat untuk menunjukan warna larutan jika hasilnya positif (Gambar 6). Dari hasil
penelitian yang dilakukan, fraksi etil asetat yang diberi reagen Folin-Ciocalteu
menunjukan warna biru. Dapat disimpulkan fraksi etil asetat ekstrak etanolik daun
dadap serep mengandung senyawa fenolik.
E. Hasil Optimasi Metode Uji Aktivitas Antioksidan 1. Penentuan panjang gelombang serapan maksimum ( λ maks)
Tujuan penentuan panjang gelombang maksimum adalah untuk
menentukan panjang gelombang dimana larutan DPPH yang digunakan
memberikan absorbansi yang paling optimum. Menurut Gandjar dan Rohman
(2007), pada panjang gelombang maksimum, perubahan yang sedikit dari
konsentrasi akan memberikan perubahan yang paling besar pada absorbansi yang
dihasilkan. Dengan demikian diperoleh sensitivitas yang maksimum.
Panjang gelombang maksimum dilakukan dengan scanning tiga
konsentrasi larutan DPPH. Scanning panjang gelombang dilakukan pada panjang
gelombang 400-600 nm.
Tabel IV. Hasil Scanning panjang gelombang maksimum DPPH