1
Indonesia adalah negara yang terletak di daerah tropis dengan paparan sinar matahari sepanjang tahun. Sinar ultraviolet (uv) yang terdapat dalam sinar matahari merupakan sumber radikal bebas berenergi tinggi (Youngson, 2005). Senyawa radikal bebas ini dapat menimbulkan gangguan fungsi sel, kerusakan struktur sel dan penuaan dini. Salah satu upaya pencegahan yang dapat dilakukan ialah dengan penggunaan antioksidan. Antioksidan adalah senyawa yang dapat menghambat reaksi oksidasi dengan cara mengikat radikal bebas dan molekul yang sangat reaktif (Winarsi, 2007). Antioksidan ini sendiri biasanya diformulasikan menjadi bentuk sediaan peroral dan topikal.
Anggapan bahwa obat dan kosmetik tradisional yang menggunakan bahan alami lebih aman dibandingkan obat sintetik akhirnya memunculkan trend pengobatan back to nature di kalangan masyarakat Indonesia. Salah satu bahan alam yang sering digunakan ialah teh hijau yang berasal dari daun teh (Camellia sinensis L.). Teh hijau dianggap lebih berkhasiat dibandingkan teh oolong dan teh hitam. Hal ini dikarenakan teh hijau memiliki kandungan polifenol sebanyak 30-40%, lebih banyak dibandingkan kandungan polifenol pada teh hitam yang hanya 3-10% (Bruno dkk., 2008). Sebagian besar polifenol yang terkandung di dalam teh hijau adalah senyawa dari golongan katekin, yang diketahui dapat digunakan sebagai antioksidan. Studi menunjukkan bahwa teh hijau memiliki kandungan katekin yang tinggi pada pelarut etanol yaitu berkisar antara 90,33 mg – 124,44 mg
tiap 1000 g sampel (Hu dkk., 2015). Menurut Syah (2006), kemampuan senyawa katekin sebagai antioksidan telah banyak dibuktikan dengan kekuatan 100 kali lebih tinggi daripada vitamin C dan 25 kali lebih efektif daripada vitamin E. Menurut penelitian yang dilakukan Susilo dkk. (2012), ekstrak teh hijau memiliki nilai IC50 4,773 µg/mL. Nilai ini lebih tinggi dibandingkan dengan IC50 kulit buah naga merah yakni 4,603 mg/mL (Widyastuti dkk., 2015), IC50 daun kemangi yakni 21,899 µg/mL (Ikhlas dkk., 2013), IC50 ekstrak kulit buah jeruk nipis yakni 54,458 µg/mL (Khasanah dkk., 2014), dan IC50 ekstrak etanolik buah jambu biji merah yakni 0,30 mg/mL (Nugroho, 2015).
Penggunaan ekstrak teh hijau secara langsung dalam pengobatan topikal dinilai kurang praktis dan efektif, sehingga perlu dibuat dalam bentuk sediaan yang lain. Bentuk sediaan gel dipilih karena mudah diaplikasikan ke kulit. Sediaan gel memiliki keuntungan diantaranya tidak lengket, mudah mengering, dan membentuk lapisan film yang tipis sehingga mudah dicuci.
Umumnya metode yang digunakan dalam suatu formulasi sediaan adalah trial and error. Metode tersebut terkesan kurang jelas dan tidak sistematis dalam pengerjaannya, bersifat coba-coba, dan bersifat tidak efektif dan efisien karena membutuhkan banyak waktu, tenaga, dan biaya (Huisman dkk., 1984). Salah satu metode lain yang dapat dilakukan adalah metode Simplex Lattice Design (SLD), yakni suatu metode yang didasarkan pada perbedaan jumlah komposisi bahan dalam menentukan optimasi formula suatu sediaan (Bolton, 1997).
Penelitian ini bertujuan untuk menentukan perbandingan yang sesuai antara HPMC sebagai gelling agent dan propilen glikol sebagai humektan guna
menghasilkan formula optimum gel ekstrak teh hijau yang memenuhi syarat kualitas, serta menguji pengaruhnya terhadap sifat fisik gel selama masa penyimpanan. Kombinasi dari HPMC dan propilen glikol dioptimasi menggunakan metode SLD dalam software Design Expert®versi 10 Trial.
Tahapan penelitian ini meliputi pengumpulan dan identifikasi simplisia daun teh hijau (Camellia sinensis L.), penyiapan ekstrak teh hijau (pembuatan ekstrak dari simplisia, uji kualitas sifat fisik, dan uji aktivitas antioksidan), formulasi gel ekstrak teh hijau, uji kualitas sifat fisik sediaan gel ekstrak teh hijau (meliputi uji homogenitas, uji penampilan fisik (organoleptis), uji pH, uji viskositas, uji daya sebar, dan uji daya lekat), penentuan formula optimum gel, pembuatan formula optimum gel, dan uji sifat fisik formula optimum gel ekstrak teh hijau selama penyimpanan.
B. Rumusan Masalah
1. Berapakah perbandingan HPMC dan propilen glikol yang dapat menghasilkan formula optimum gel ekstrak teh hijau (Camellia sinensis L.) dengan metode Simplex Lattice Design?
2. Bagaimanakah pengaruh variasi konsentrasi HPMC dan propilen glikol terhadap sifat fisik gel ekstrak teh hijau (Camellia sinensis L.)?
3. Bagaimanakah respon sifat fisik (viskositas, daya sebar, dan daya lekat) formula optimum gel ekstrak teh hijau (Camellia sinensis L.) selama penyimpanan?
C. Manfaat Penelitian
Penelitian ini dapat memberikan informasi penggunaan HPMC dan propilen glikol untuk formula optimum gel ekstrak teh hijau (Camellia sinensis L.) dan sifat fisiknya selama penyimpanan dalam kurun waktu 4 minggu.
D. Tujuan Penelitian
1. Untuk mengetahui perbandingan HPMC dan propilen glikol yang dapat menghasilkan formula optimum gel ekstrak teh hijau (Camellia sinensis L.) dengan metode Simplex Lattice Design.
2. Mengetahui pengaruh variasi konsentrasi HPMC dan propilen glikol terhadap sifat fisik gel ekstrak teh hijau (Camellia sinensis L.).
3. Mengetahui respon sifat fisik (viskositas, daya sebar, dan daya lekat) formula optimum gel ekstrak teh hijau (Camellia sinensis L.) selama penyimpanan.
E. Tinjauan Pustaka 1. Uraian Teh Hijau (Camellia sinensis L.)
Menurut Syamsuhidayat dan Hutapea (2001), tanaman teh diklasifikasikan dalam Tabel I sebagai berikut :
Tabel I. Klasifikasi Tanaman Teh Hijau Divisi Spermathophyta
Sub divisi Angiospermae Kelas Dicotyledoneae Sub kelas Dialypetalae
Ordo Guttiferales (Clusiales) Famili Camelliaceae (Theaceae) Genus Camellia
Teh dihasilkan dari pucuk daun tanaman Camellia sinensis L. Tanaman ini berasal dari Asia tenggara dan Selatan, namun sekarang telah dikembangkan di seluruh dunia, di daerah tropis maupun subtropis. Tanaman teh merupakan semak hijau atau pohon kecil yang biasanya dipanen saat tinggi tanaman belum mencapai dua meter. Daun teh memiliki panjang sekitar 4-15 cm dan lebar 2-5 cm, ujung dan pangkal runcing, serta tepi daun bergerigi. Bunganya berwarna putih kuning, berdiameter 2,5-4 cm dengan 7-8 kelopak.
Berdasarkan proses pengolahannya, teh dapat dikelompokkan menjadi tiga jenis, yaitu : teh hijau (tidak difermentasi), teh oolong (semifermentasi), dan teh hitam (fermentasi penuh). Teh hijau dibuat melalui inaktivasi enzim polifenol oksidasenya di dalam daun teh segar. Metode inaktivasi enzim polifenol oksidase teh hijau dapat dilakukan melalui pemanasan (udara panas) dan penguapan (steam/uap air). Kedua metode tersebut berguna untuk merusak enzim yang dapat merusak pigmen warna di dalam daun teh dan menjadikan teh tetap terjaga warna hijaunya selama proses pengeringan.
Komposisi kandungan daun teh bervariasi tergantung pada beberapa faktor, antara lain : iklim, musim, cara pemanenan, jenis, dan umur tanaman. Daun teh segar mengandung kafein (3,5% dari berat kering), teobromin (0,15-0,2%), teofilin (0,02-0,04%), lignin (6,5%), asam organik (1,5%), klorofil dan pigmen lain (0,5%) (Graham, 1992). Kandungan kimia daun teh lainnya didominasi oleh polifenol flavonoid, selain itu ada pula asam fenolat, asam galat, asam klorogenat, kuersetin, karbohidrat, alkaloid, mineral, vitamin, dan enzim-enzim (Chaturvedula & Prakash, 2011).
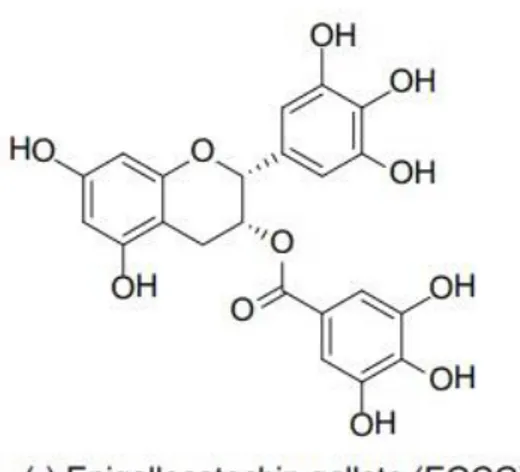
Menurut Bansal dkk., (2012) teh hijau terkenal kaya akan katekin antara lain, epikatekin (EC), epigalokatekin (EGC), epikatekin galat (ECG), dan utamanya epigalokatekin galat (EGCG). Menurut penelitian Ananda (2009), dalam 100 g daun teh terkandung 10,55 g EGCG. Senyawa inilah yang memiliki aktivitas antioksidan kuat untuk mencegah radikal bebas seperti peroksinitrit, superoksida, hidrogen peroksida, dan DPPH (Faramayuda dkk., 2010). Aktivitas antioksidan ini berkaitan dengan kemampuan polifenol teh hijau dlam menyumbang atom H sehingga dapat mengikat radikal bebas. Ikatan antara atom H dan radikal bebas inilah yang membuat radikal bebas yang awalnya reaktif menjadi inaktif dan lebih stabil. Semakin gelap jenis dari teh tersebut maka semakin menurun daya antioksidan dari daun teh tersebut, hal ini dikarenakan kandungan polifenol dari daun tersebut yang berfungsi sebagai antioksidan semakin kecil (Chopra dan David, 2000 cit Tourle, 2004).
Stabilitas katekin teh hijau tergantung pada pH dan suhu. katekin teh hijau menunjukkan sifat yang stabil pada larutan yang bersifat asam (pH < 4), sedangkan pada larutan yang bersifat basa (pH > 4) katekin menjadi sangat tidak stabil. Menurut studi yang dilakukan Zhu dkk., (1997), suhu lingkungan yang tinggi menyebabkan katekin teh hijau menjadi tidak stabil. Hal ini dapat menyebabkan terjadinya epimerisasi, misalnya saja pada EGCG yang berubah menjadi epimer komponen galokatekin galat. Suhu tinggi juga dapat menurunkan aktivitas katekin teh hijau dikarenakan oksidasi, degradasi termal, epimerisasi, dan polimerisasi (Ananingsih dkk., 2013).
Gambar 1. Rumus Bangun EGCG (Bansal dkk., 2012)
2. Monografi Bahan
a. HPMC (Hidroksi Propil Metil Selulosa)
HPMC merupakan polimer hidrofilik berbentuk serat atau serbuk granul berwarna putih kekuningan, tidak berbau, dan tidak berasa. HPMC digunakan sebagai gelling agent dan sebagai peningkat viskositas pada sediaan cair. HPMC larut dalam air panas membentuk larutan koloidal kental, praktis tidak larut dalam kloroform, etanol 95 %, eter, larut dalam campuran etanol dan diklorometan, campuran metanol dan diklorometana, serta campuran alkohol dan air (Rowe dkk., 2009).
HPMC dapat menghasilkan gel yang netral, jernih, tidak berwarna dan tidak berasa, stabil pada pH 3-11 dan punya resistensi yang baik terhadap serangan mikroba serta memberikan kekuatan film yang baik bila mengering pada kulit (Rowe dkk., 2009). Konsentrasi HPMC yang digunakan sebagai pembentuk gel adalah 2-10%. HPMC memiliki stabilitas yang baik walau disimpan dalam jangka waktu lama, tahan terhadap temperatur tinggi,
mempunyai resistensi yang baik terhadap serangan mikroba, dan membentuk koloidal yang kuat (Rowe dkk., 2009).
b. Metil paraben
Metil paraben berbentuk hablur atau serbuk tidak berwarna, atau kristal putih, tidak berbau atau berbau khas lemah, dan mudah larut dalam etanol. Metil paraben berfungsi sebagai preservative atau pengawet yang berguna untuk mencegah kontaminasi, perusakan, dan pembusukan oleh bakteri atau fungi. Konsentrasi metil paraben untuk penggunaan topikal ialah 0,02-0,3% (Rowe dkk., 2009).
c. Propilen glikol
Propilen glikol merupakan larutan jernih atau sedikit berwarna, kental, dengan rasa agak manis. Propilen glikol larut dalam kloroform, etanol, gliserin, dan air, namun inkompatibel dengan reagen oksidasi seperti kalium permanganat. Penyimpanan propilen glikol ialah dalam wadah tertutup baik pada suhu dingin atau rendah dikarenakan sifatnya yang higroskopis. Propilen glikol akan cenderung mengoksidasi dan menimbulkan produk seperti propionaldehida, asam laktat, asam piruvat, dan asam asetat apabila disimpan dalam ruangan terbuka dan pada suhu tinggi. Propilen glikol berfungsi sebagai humektan yang berguna untuk menahan lembab, memungkinkan kelembutan dan daya sebar yang tinggi dari sediaan, dan melindungi gel dari kemungkinan pengeringan (Voigt, 1984).
d. Trietanolamin
Trietanolamin berupa cairan kental, berwarna kuning sampai kuning pucat. Trietanolamin dapat berubah menjadi warna cokelat dengan paparan udara dan cahaya karena sifatnya yang higroskopis (Rowe dkk., 2009). e. Aquadest
Air murni adalah air yang dimurnikan yang diperoleh dengan destilasi, perlakuan menggunakan penukar ion, osmosis balik, atau proses lain yang sesuai. Air murni berupa cairan bening, tidak berwarna, tidak berbau, dan tidak berasa. Dibuat dari air yang memenuhi persyaratan minum dan tidak mengandung zat tambahan lain (Anonim, 1995). Kegunaan air murni ialah sebagai pelarut.
3. Radikal Bebas
Radikal bebas memiliki sifat reaktif dan tidak stabil sehingga untuk mencapai kestabilan atom atau molekul, radikal bebas akan bereaksi dengan molekul sel tubuh dengan cara mengikat suatu elektron (Youngson, 2005). Radikal bebas terbentuk dari reaksi kimia yang berlangsung sangat panjang di dalam tubuh atau hasil pencemaran lingkungan seperti nitrogen, dioksida, ozon, logam berat, asap rokok. Radikal bebas ini akan menyerang pertumbuhan sel, termasuk DNA (Deoxy Nucleic Acid) dan asam lemak tak jenuh (PUFA). Reaksi antara radikal bebas dengan PUFA akan menimbulkan reaksi berantai yang mendorong terbentuknya reaksi radikal bebas dalam jumlah yang banyak. Reaksi berantai ini akan terus menerus berlangsung dalam tubuh apabila tidak segera dicegah dapat merusak sel-sel penting dalam tubuh (Astuti, 1995).
Radikal bebas dapat merusak struktur dan fungsi sel membran dan asam nukleat. Kerusakan akibat serangan radikal bebas menimbulkan berbagai penyakit seperti kanker, jantung, katarak, penuaan dini, dan penyakit degeneratif lainnya. Untuk mengantisipasi kerusakaan akibat radikal bebas tersebut maka tubuh memerlukan suatu substansi penting, yaitu antioksidan (Astuti, 1995).
4. Antioksidan
Antioksidan adalah suatu senyawa yang dapat menghambat terjadinya proses oksidasi. Mekanisme antioksidan dalam menghambat atau memperlambat poses oksidasi terdapat dalam tabel berikut ini :
Tabel II. Mekanisme Aktivitas Antioksidan (Pokorny, 2001)
Kelas Antioksidan Mekanisme
Proper Antioxidant Menginaktivasi radikal bebas lipid Penstabil Hidroperoksida Mencegah dekomposisi dari radikal bebas
Sinergis Meningkatkan aktivitas dari proper antioxidant
Pengkelat logam Mengikat logam berat menjadi komponen yang inaktif
Antioksidan dapat diperoleh secara alami maupun sintesis. Antioksidan alami berpotensi sebagai penangkap, penyetabil radikal, dan peredam oksigen singlet. Mekanisme penangkapan radikal dapat terjadi melalui jalur interaksi antara spesies radikal seperti radikal bebas maupun radikal peroksi. Aktivitas radikal bebas alami bergantung pada struktur kimia senyawa penyusunnya dan kemampuan senyawa tersebut untuk menangkap dan menstabilkannya selama reaksi berlangsung (Yanshlieva-Maslarova, 2001).
5. Pengukuran Aktivitas Antioksidan
Radikal bebas yang umumnya digunakan sebagai model dalam penelitian antioksidan atau peredam radikal bebas adalah DPPH
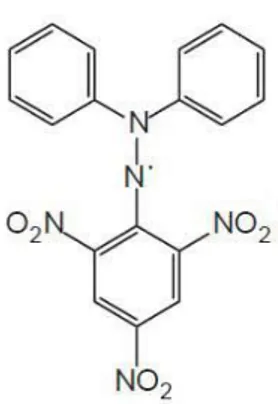
(1,1-Diphenyl-2-Picrylhidrazyl). Metode radikal DPPH secara luas digunakan untuk menguji kemampuan senyawa untuk bertindak sebagai penangkap radikal bebas atau donor hidrogen serta untuk mengevaluasi aktivitas antioksidan. Metode DPPH merupakan metode yang akurat, cepat, dan mudah untuk mendeteksi aktivitas penangkap radikal beberapa senyawa (Prakash dkk., 2001). DPPH adalah radikal bebas yang stabil pada suhu kamar. Radikal DPPH akan membentuk molekul diamagnetik yang stabil ketika menerima elektron atau radikal hidrogen. Interaksi antioksidan dengan DPPH secara transfer elektron maupun transfer radikal hidrogen DPPH akan menetralkan radikal bebas dari DPPH menghasilkan DPPH tereduksi. Jika semua elektron dalam radikal bebas DPPH berpasangan, maka warna larutan berubah dari ungu tua menjadi kuning terang pada λmax 516 nm. Perubahan ini dapat diukur sesuai dengan jumlah elektron atau atom hidrogen yang ditangkap oleh molekul DPPH akibat adanya zat reduktor (Molyneux, 2004).
Parameter yang digunakan untuk menentukan aktitivitas antioksidan adalah Efficient Concentration (EC50) atau Inhibition Concentration (IC50) yaitu konsentrasi senyawa antioksidan yang memberikan % penghambatan sebesar 50%. Semakin rendah nilai EC50 atau IC50 senyawa maka aktivitas antioksidan semakin kuat (Brand-Williams, 1995). Suatu zat dikatakan mempunyai sifat antioksidan bila nilai IC50 kurang dari 200 µg/mL.
Gambar 2. Struktur DPPH (Molyneux, 2004) 6. Ekstraksi
Ekstraksi adalah suatu proses pemisahan satu atau lebih komponen senyawa kimia atau zat aktif dalam suatu campuran menggunakan pelarut tertentu. Tujuannya ialah agar massa zat aktif yang awalnya berada di dalam sel dapat larut secara homogen dalam cairan penyari. Pertimbangan pemilihan metode penyarian yang baik adalah wujud dari bahan uji yang disari (Harborne, 1987). Beberapa macam metode ekstraksi bahan alam antara lain :
a. Ekstraksi secara panas dengan refluks dan penyulingan uap air. b. Ekstraksi secara dingin dengan maserasi, perkolasi, dan soxhlet.
Beberapa pelarut yang dapat digunakan, antara lain : air, etanol, atau pelarut lainnya. Pemilihan pelarut harus mempertimbangkan beberapa faktor, antara lain :
a. Stabil secara fisika dan kimia.
b. Sifat kelarutan senyawa kimia atau zat aktif dalam pelarut tersebut. c. Bereaksi netral atau tidak mempengaruhi zat aktif
d. Tidak mudah menguap dan tidak mudah terbakar
e. Selektif, yakni hanya menarik zat berkhasiat yang dikehendaki f. Diperbolehkan oleh peraturan (Anonim, 1986).
Maserasi adalah metode eksraksi yang paling sederhana. Maserasi merupakan proses penyarian simplisia dengan cara merendam serbuk simplisia menggunakan pelarut dengan sesekali pengadukan pada temperatur kamar. Adanya perbedaan konsentrasi antara larutan zat aktif di dalam sel dengan di luar sel, memungkinkan zat aktif yang terlarut dalam pelarut terdesak ke luar sel. Peristiwa tersebut terjadi secara berulang sehingga terjadi keseimbangan konsentrasi antara larutan di dalam sel dan di luar sel (Anonim, 1986).
Maserasi dilakukan dengan pengulangan penambahan pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya dan disebut remaserasi. Pengadukan dan penggantian cairan penyari perlu dilakukan selama proses maserasi. Maserasi biasanya dilakukan selama beberapa hari pada temperatur kamar (15-20oC) sampai bahan simplisia melarut (Ansel, 1989). Endapan hasil maserasi kemudian dipisahkan dan filtrat yang didapatkan diuapkan hingga didapatkan filtrat yang pekat.
7. Ekstrak
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai kemudian semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian rupa sehingga memenuhi baku yang telah ditetapkan (Anonim, 1995).
Menurut Voigt (1984), berdasarkan sifatnya, ekstrak digolongkan menjadi empat, yaitu :
a. Ekstrak encer (extractum tenue)
b. Ekstrak kental (extractum spissum)
Jenis ekstrak ini liat dalam keadaan dingin dan tidak dapat dituang. Kandungan airnya mencapai 30%.
c. Ekstrak kering (extractum siccum)
Jenis ekstrak ini memiliki konsistensi kering dan dapat digosokkan. Kandungan airnya tidak lebih dari 5%.
d. Ekstrak cair (extractum fluidum)
Jenis ekstrak ini diartikan sebagai ekstrak cair yang dibuat sedemikian rupa sehingga satu bagian simplisia sesuai dengan dua bagian (kadang-kadang satu bagian) ekstrak cair.
8. Gel
Gel ialah suatu sediaan semipadat yang jernih, tembus cahaya, dan mengandung zat aktif, merupakan dispersi koloid yang memiliki kekuatan oleh adanya jaringan yang saling berikatan pada fase terdispersi (Ansel, 1989).
Menurut Voigt (1984), keuntungan sediaan gel diantaranya ialah kemampuan penyebarannya yang baik pada kulit, lambatnya penguapan air dari kulit yang dapat menimbulkan efek dingin, tidak ada penghambatan fungsi rambut secara fisiologis (cocok untuk digunakan pada bagian tubuh yang berambut), tidak menyumbat pori-pori, tidak melapisi kulit secara kedap, mudah dicuci dengan air, dan mampu melepaskan obat dengan baik.
9. Kromatografi Lapis Tipis (KLT)
Kromatografi lapis tipis (KLT) adalah suatu metode analisis yang sangat penting dalam analisis senyawa kimia dalam tumbuhan karena banyaknya
variasi dan kombinasi fase gerak dan fase diam. Kelebihan KLT dalam analisis adalah :
1. Sampel yang dibutuhkan sedikit.
2. KLT dapat memberikan informasi kualitatif dan kuantitatif. 3. KLT dapat memberikan gambaran fingerprint suatu tanaman.
4. KLT dapat digunakan untuk mengidentifikasi obat maupun tanaman. Identifikasi senyawa hasil KLT dapat menggunakan beberapa cara, yaitu:
1. Bercak dilihat langsung menggunakan sinar tampak dan sinar UV. 2. Bercak disemprot atau diuapi terlebih dahulu dengan pereaksi tertentu
baru dilihat pada sinar tampak dan sinar UV.
3. Bercak dikerok terlebih dahulu, kemudian diekstraksi dan ditambah pereaksi tertentu untuk mencari serapan maksimal.
Pada analisis menggunakan metode KLT, identifikasi dapat dilakukan dengan melihat harga Rf senyawa-senyawa yang terdapat pada ekstrak. Harga Rf dapat didefinisikan dalam Persamaan (1) sebagai berikut :
Rf = Jarak yang ditempuh oleh zat terlarut dari titik asal Jarak yang ditempuh oleh fase gerak dari titik asal
(1)
Harga Rf suatu senyawa dapat dibandingkan dengan harga Rf pada literatur jika pelarut, fase diam, serta fase gerak yang digunakan sama (Sastrohamidjojo, 1991). Nilai Rf selalu bernilai pecahan yang terletak antara 0,01 – 0,99. Sedangkan nilai hRf merupakan hasil kali Rf dengan faktor 100. Hal ini hanya untuk mempermudah perhitungan saja.
10.Metode Simplex Lattice Design (SLD)
Optimasi adalah suatu metode atau desain eksperimental yang digunakan guna memudahkan dalam penyusunan dan interpretasi data secara matematis (Armstrong & James, 1986). Salah satu metode yang dapat digunakan adalah SLD. Metode SLD digunakan untuk menentukan optimasi formula pada berbagai perbedaan jumlah komposisi bahan (yang dinyatakan dalam beberapa bagian), dengan jumlah total sama dengan satu bagian. Metode ini dianggap praktis dan cepat karena penentuan formula tidak dilakukan dengan coba-coba (trial and error). Profil respon dapat ditentukan melalui persamaan berdasarkan SLD (Bolton, 1997).
Semua fraksi dari kombinasi dua campuran dapat dinyatakan sebagai garis lurus. Jika ada dua komponen, maka dinyatakan sebagai satu dimensi dan merupakan garis lurus. Titik A menyatakan suatu formula hanya mengandung komponen A. Titik B menyatakan suatu formula hanya mengandung komponen B. Garis AB menyatakan semua kemungkinan campuran A dan B. Titik C menyatakan campuran 0,5 komponen A dan 0,5 komponen B (Armstrong & James, 1986). Persamaan SLD dapat dilihat pada Persamaan (2) :
Persamaan Simplex Lattice Design :
Y = a (A) + b (B) + ab (A)(B) (2)
Keterangan :
Y = respon atau efek yang dihasilkan,
A C
A
B A
A = konsentrasi proporsi komponen A, B = konsentrasi proporsi komponen B,
b, ab = koefisien yang dihitung dari hasil percobaan.
Koefisien diketahui dari perhitungan regresi dan Y adalah respon yang diinginkan. Penentuan formula optimum didapatkan dari respon total yang paling besar. Respon total dihitung dengan rumus pada Persamaan (3) sebagai berikut :
R total = R1 + R2 + R3 + ………… Rn (3)
R1, R2, R3, dan Rn adalah respon masing-masing sifat fisik sediaan. Dari persamaan respon total terebut, akan diperoleh formula yang optimum. Verifikasi dilakukan pada formula yang memiliki respon paling optimum (Armstrong & James, 1986).
11.Kontrol Kualitas Sifat Fisik Gel a. Organoleptis
Pemeriksaan organoleptis biasa dilakukan secara makroskopis dengan mendiskripsikan warna, kejernihan, transparansi, kekeruhan, dan bentuk sediaan (Paye dkk., 2001). Hasil yang didapat dapat digunakan sebagai indikator kualitatif ketidakstabilan fisik suatu sediaan yang bersifat subyektif (Sulaiman dan Kushwahyuning, 2008).
b. Homogenitas
Pemeriksaan homogenitas dapat dilakukan secara visual (Paye dkk., 2001). Homogenitas gel diamati pada object glass di bawah cahaya, dilihat kemungkinan adanya bagian-bagian yang gel yang tidak tercampurkan dengan baik. Homogenitas berpengaruh terhadap efektivitas terapi karena
berhubungan dengan kadar obat yang seragam pada setiap pemakaian. Sediaan yang homogen akan memberikan kadar zat aktif yang sama pada saat pengambilan dan pemakaian. Gel yang stabil harus menunjukkan susunan yang homogen.
c. Viskositas
Viskositas merupakan gambaran suatu benda cair untuk mengalir. Viskositas menentukan sifat sediaan dalam hal campuran dan sifat alirnya pada saat diproduksi, serta sifat-sifat penting pada saat pemakaian, seperti konsistensi, daya sebar, dan kelembaban (Payedkk., 2001). Semakin tinggi viskositas, waktu retensi pada tempat aksi akan naik, sedangkan daya sebarnya akan menurun. Viskositas juga menentukan lama lekatnya sediaan pada kulit, sehingga obat dapat dihantarkan dengan baik.
d. pH
Nilai pH berguna untuk mengetahui pH gel yang telah dihasilkan. Nilai pH sebaiknya sama dengan pH kulit atau tempat pemakaian. Hal ini bertujuan untuk menghindari terjadinya iritasi. Idealnya, pH sediaan topikal adalah sekitar 5-7 (Kaur dkk., 2010).
e. Daya sebar
Daya sebar berkaitan dengan kenyamanan pada pemakaian. Salah satu syarat sediaan gel adalah mudah dioleskan dan mudah merata. Kemudahan dalam pengolesan tersebut dapat diketahui melalui uji daya sebar gel. Meningkatnya daya sebar sediaan, maka luas permukaan kulit yang kontak dengan gelakan semakin luas dan zat aktif dapat terdistribusi dengan baik.
f. Daya lekat
Daya lekat berkaitan dengan kemampuan sediaan untuk menempel pada lapisan epidermis. Semakin besar daya lekat gel, maka semakin baik penghantaran obatnya.
F. Landasan Teori
Komponen gelling agent dan humektan merupakan bagian yang sangat berpengaruh terhadap kualitas fisik sediaan gel. HPMC adalah salah satu gelling agent yang membentuk gel jernih dan memiliki viskositas stabil pada penyimpanan jangka panjang (Rogers, 2009). Hasil penelitian Madan dan Singh (2010) menyebutkan bahwa HPMC memiliki kecepatan pelepasan obat yang baik dan daya sebarnya luas. Konsentrasi HPMC yang cocok untuk sediaan gel berkisar antara 2-10%, namun hasil orientasi konsentrasi HPMC yang lebih kecil dari 3% menghasilkan sediaan yang sangat encer sehingga digunakan konsentrasi HPMC di atas 3% (Suardi dkk., 2008). HPMC umumnya dianggap sebagai bahan dasar yang stabil bahkan setelah paparan panas dan kondisi lembab menunjukkan tidak ada perubahan signifikan dalam uji homogenitas, pH, kejernihan, dan tekstur dari gel HPMC (Dhawan dkk., 2009).
Propilen glikol berfungsi sebagai humektan yang mempertahankan kandungan air dalam sediaan sehingga sifat fisik dan stabilitas sediaan selama penyimpanan dapat dipertahankan. Propilen glikol yang digunakan sebagai penahan lembab adalah dalam konsentrasi dari 10-20% (Haley, 2009). Penambahan propilen glikol pada sediaan topikal dapat meningkatkan laju difusi (Agoes, 1983). Penambahan peningkat penetrasi propilen glikol dapat melarutkan lapisan keratin
pada stratum corneum sehingga meningkatkan jumlah obat yang berpenetrasi lewat kulit dengan cara mengurangi ikatan obat dengan jaringan kulit (Remon, 2007).
Uji sifat fisik selama masa penyimpanan dilakukan untuk menjamin sediaan memiliki sifat yang sama seperti saat sediaan baru dibuat. Ketidakstabilan fisika dari sediaan gel ditandai dengan adanya pemucatan warna atau munculnya warna yang berbeda, timbul bau, perubahan bentuk, atau pemisahan fase, sineresis, perubahan konsistensi, terbentuknya gas, dan perubahan fisik lainnya. Sineresis adalah suatu kondisi dimana gel mengerut secara alamiah saat didiamkan dan mengakibatkan sebagian cairannya terperas keluar. Hal ini terjadi karena struktur matriks/serat gel yang terus mengeras dan akhirnya mengakibatkan terperasnya air ke luar (Martin dkk., 1993).
G. Hipotesis
1. Metode Simplex Lattice Design (SLD) dapat menghasilkan perbandingan HPMC dan propilen glikol yang proporsional sehingga diperoleh formula optimum gel ekstrak teh hijau (Camellia sinensis L.)
2. Variasi konsentrasi HPMC dan propilen glikol tidak mempengaruhi sifat fisik gel ekstrak teh hijau (Camellia sinensis L.) secara signifikan dan sediaan tetap memenuhi syarat kualitas.
3. Sifat fisik gel ekstrak teh hijau (Camellia sinensis L.) tidak mengalami perubahan yang signifikan selama penyimpanan.