LAPORAN AKHIR
HIBAH UNGGULAN PROGRAM STUDI
ANALISIS KOMPOSISI ASAM AMINO DAN POLA PROTEIN
GELATIN HALAL DARI KULIT AYAM BROILER
Oleh:
Dra. Ni Made Puspawati, M.Phil., PhD. NIDN:0019036502
Ida Ayu Gede Widihati, S.Si., M.Si. NIDN:0031126826
Drs. I Nyoman Widana, MSi. NIDN:0008086403
Dibiayai oleh DIPA BLU Universitas Udayana Sesuai dengan Surat Perjanjian Penugasan Pelaksanaan Penelitian Nomor: 1306/UN.14.1.28.1/PP/2015, tanggal 25 Mei 2015
JURUSAN KIMIA
RINGKASAN
Salah satu kelemahan produk gelatin halal yang berasal dari non-mamalia adalah sifat mekaniknya yang kurang bagus sehingga aplikasinya di bidang kedokteran menjadi terbatas. Penelitian ini bertujuan untuk mempelajari pengaruh proses demineralisasi dan perbedaan jenis asam yang digunakan pada proses perendaman terhadap komposisi asam amino dan panjang rantai protein serta kaitannya dengan sifat mekanik gelatin yaitu kekuatan gel. Proses isolasi gelatin terdiri dari tahap deproteinasi menggunakan natrium hidroksida (NaOH 0,15%), demineralisasi dengan asam sulfat (H2SO4), dan dilanjutkan
dengan tahap perendaman menggunakan tiga jenis asam yang berbeda (asetat, laktat, dan sitrat 1%). Pengukuran kekuatan gel dilakukan dengan CT3 Texture Analyzer, analisis komposisi asam amino dilakukan dengan HPLC, dan analisis pola pita protein dilakukan menggunakan metode elektroforesis. Hasil penelitian menunjukkan perbedaan jenis asam yang digunakan berpengaruh terhadap rendemen, kekuatan gel, panjang rantai protein, dan komposisi asam amino dari produk gelatin yang dihasilkan. Rendemen gelatin tertinggi yaitu 21,11% diperoleh melalui proses perendaman asam sitrat (GASH), sedangkan terendah 10,70% diperoleh dengan perendaman asam asetat (GAAH). Sebaliknya kekuatan gel tertinggi 216,63 g bloom diberikan oleh gelatin dengan proses perendaman asam asetat, dan terendah 32.73 g bloom diperlihatkan oleh gelatin dengan proses perendaman asam laktat (GALH). Komposisi utama asam amino dari ketiga produk gelatin yaitu glisin, prolin, glutamate, dan arginin masing-masing dengan persentase berurutan 17,77%, 8,78%, 7,01%, dan 6,79% untuk GASH, 18,58%, 8,93%, 7,08%, dan 7,01% untuk GAAH, dan 20,54%, 9,87%, 7,53%, dan 7,96% untuk GALH. Asam amino histidin dan asam amino essensial triptofan tidak ditemukan pada ketiga produk gelatin hasil perlakuan. Hasil analisis elektroforegram ketiga produk gelatin tidak menunjukkan adanya pita protein dengan berat molekul yang tinggi pada 200kDA untuk rantai protein sheet dan 300kDa
untuk sheet tetapi GAAH dan GASH memperlihatkan pita protein dengan berat molekul yang relatif cukup tinggi yaitu pada 97 kDA dan 85 kDA untuk rantai protein α1 dan αβ. Hal ini menunjukkan bahwa protein gelatin yang diperoleh tidak utuh dan terfragmentasi menjadi protein dengan berat molekul yang lebih rendah. Hal ini ditunjukkan dengan terdapatnya beberapa pita protein pada GAAH dan GASH dengan berat molekul yang lebih rendah yaitu pada 66kDA, 45, kDa, 31 kDA dan 25 kDA. Sedangkan GALH hanya memberikan protein dengan berat molekul yang rendah yaitu 21kDA dan dibawahnya. Pada penelitian ini dapat disimpulkan bahwa sifat mekanik produk gelatin khususnya kekuatan gel tidak dipengaruhi oleh komposisi asam aminonya tetapi dipengaruhi oleh berat molekul dan distribusi berat molekulnya atau pola pita proteinnya. Pada penelitian ini perendaman dengan asam asetat memberikan hasil gelatin dengan sifat mekanik terbaik dan memiliki kualitas mutu yang memenuhi kualitas mutu gelatin Standar Nasional Indonesia (SNI).
PRAKATA
Puji dan syukur penulis panjatkan kehadapan Sang Hyang Widhi Wasa atas rahmat
dan karunia yang dilimpahkan sehingga penelitian dan penulisan laporan akhir penelitian
yang berjudul “ANALISIS KOMPOSISI ASAM AMINO DAN POLA PROTEIN
GELATIN HALAL DARI KULIT AYAM BROILER” ini dapat dilaksanakan dengan baik dan beberapa kendala yang dihadapi dapat diatasi dengan baik. Penulis juga
mengucapkan terima kasih kepada:
1. Rektor Universitas Udayana dan Ketua LPPM
2. Fakultas Matematika Universitas Udayana yang telah memberikan dana PNBP
scheme Hibah Unggulan Program Studi tahun anggaran 2015.
3. Dekan Fakultas MIPA dan Ketua Jurusan Kimia Universitas Udayana yang
telah mengesahkan usulan proposal penelitian ini sehingga dapat dilanjutkan
dan telah memberikan fasilitas penggunaan Laboratorium Penelitian Jurusan
Kimia dan Laboratorium bersama FMIPA Universitas Udayana untuk
penggunaan Instrumen.
4. Kepala Laboratorium Bersama FMIPA Universitas Udayana untuk fasilitas
penggunaaan Instrumen FTIR.
5. Kepala Lanoratorium Balai Penelitian Ternak Bogor untuk Analisis Komposisi
Asam Amino
6. Kepala Laboratorium Center for Development of Advances Sciences and
Technology, Jember Untuk Elektroforesis SDS_PAGE
7. Kepala Laboratorium EHP Fakultas Teknologi Pertanian Universitas Jember
8. Kepala Laboratorium Kimia Organik Jurusan Kimia FMIPA Universitas
Udayana atas bantuannya untuk fasilitas dalan proses pre-treatment dan
pengeringan sampel.
9. Balai Besar Penelitian dan Pengembangan Budi Daya Laut Bali,Gondol
Singaraja atas bantuannya dalam proses pengeringan sampel kulit ayam dengan
10. Tutut Hardikawati dan Anak Agung Rahma Prabawanti , mahasiswa kimia yang
telah membantu dalam pelaksanaan penelitian ini.
Semoga laporan penelitian ini dapat menjadikan acuan untuk penelitian selanjutnya.
Denpasar, 27 Oktober 2015
DAFTAR ISI
2.4 SDS-PAGE (Elektroforesis Gel Poliakrilamida-Sodium Dodesil Sulfat) 5
5
5
11
BAB III METODE PENELITIAN 3.1 Alat dan Bahan
3.2 Tempat Penelitian
13
3.3 Prosedur Kerja 14
BAB IV HASIL DAN PEMBAHASAN 4.1 Penyiapan bahan baku
BAB V. SIMPULAN DAN SARAN
5.1. Simpulan 40
5.2. Saran 41
DAFTAR PUSTAKA 41
DAFTAR GAMBAR
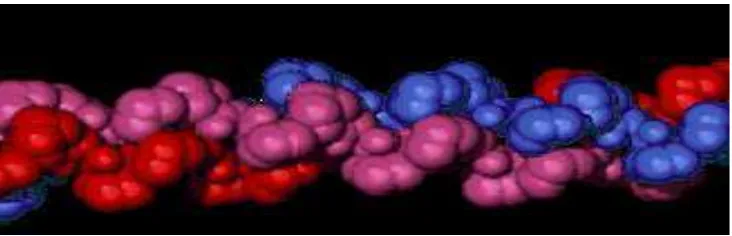
Gambar 2.1. Struktur Tripel Helix Penyusun Gelatin 6
Gambar 2.2. Struktur Kimia Gelatin 8
Gambar 2.3. Contoh elektroforegram gelatin dari Bigeye snapper 13
Gambar 4.1. Foto Kulit ayam kering 19
Gambar 4.2.Foto Serbuk kulit ayam bebas lemak 19
Gambar 4.3.Foto Kulit ayam setelah perendaman NaOH 20
Gambar 4.4.Foto Kulit ayam setelah perendaman 20
Gambar 4.5.Foto Proses ekstraksi Waterbath 21
Gambar 4.6.Foto Gel sebelum dioven 21
Gambar 4.7. Elektroforegram produk gelatin hasil perlakuan 35
Gambar 4.8. Spektra Inframerah gelatin yang diekstraksi dengan asam sitrat 37
Gambar 4.9. Spektra Inframerah gelatin yang diekstraksi dengan asam laktat 38
Gambar 4.10. Spektra Inframerah gelatin yang diekstraksi dengan asam asetat 38
DAFTAR TABEL
Tabel 2.1. Komposisi Asam Amino Gelatin 7
Tabel 2.2. Sifat Gelatin Berdasarkan Jenisnya 9
Tabel 2.3. Standar Mutu Gelatin Menurut SNI No. 06-3735 Tahun 1995 dan British Standard: 757 Tahun 1975
9
Tabel 4.1. Hasil Analisis Proksimat Serbuk Kulit Ayam Broiler 18
Tabel 4.2. Pengaruh Perlakuan Terhadap Nilai Rendemen Gelatin Kulit Ayam 22
Tabel 4.3. Pengaruh Perlakuan Terhadap Nilai pH Gelatin Kulit Ayam 24
Tabel 4.4. Pengaruh Perlakuan Terhadap Nilai Viskositas Gelatin Kulit Ayam 25
Tabel 4.5. Kandungan Proksimat Produk Gelatin Hasil Perlakuan 27
Tabel 4.6. Pengaruh Perlakuan Terhadap Nilai Kekuatan Gel Gelatin Kulit Ayam 29
Tabel 4.7. Komposisi Asam Amino Produk Gelatin Kulit Ayam Hasil perlakuan
Tabel 4.8. Interpretasi gugus fungsi
31
BAB 1. PENDAHULUAN
Gelatin adalah suatu biopolimer yang diperoleh dari hidrolisis parsial kolagen, suatu
protein fibrius penyusun utama jaringan pada kulit, tulang, dan jaringan ikat hewan. Sifat
dari gelatin secara intrinsik dipengaruhi oleh sumber (spesies), umur hewan, dan jenis
kolagen (Johnson, 2009).
1.1. Gelatin dimanfaatkan secara luas dalam industri makanan, kosmetik, farmasi,
tekstil, kertas dan fotografi karena sifatnya yang dapat membentuk gel, busa emulsifier, dan
dapat mempertahankan elastisitas suatu bahan. Manfaat gelatin yang sangat luas
menyebabkan kebutuhan dunia akan gelatin terus meningkat. Di Indonesia kebutuhan akan
gelatin sampai saat ini lebih banyak dipenuhi dengan cara mengimpor dari negara-negara
penghasil gelatin, sehingga harganya menjadi mahal. Selain itu, tingginya harga gelatin
juga disebabkan oleh permintaan konsumen yang tinggi karena pemanfaatan gelatin yang
sangat luas, seperti sebagai bahan kosmetik dan produk farmasi serta bahan baku makanan
(susu dan produknya, es krim, permen karet, pengental, dan mayonnaise), juga sebagai
bahan pembuat film, material medis (hard capsule), dan bahan baku kultur jaringan,
sebagai pelapis kertas, tinta inkjet, korek api, gabus, pelapis kayu untuk interior, karet
plastik, dan lain-lain (Apriyantono, 2003). Sampai sekarang ini gelatin yang beredar di
pasaran, 46 % berasal dari kulit babi, 29,4 % dari kulit sapi, 23,1 % dari tulang sapi, dan
hanya 1,5 % dari sumber lainnya (GME, 2008). Akhir-akhir ini, adanya pertimbangan dan
ketakutan akan BSE dan pengaruh penyakit sapi gila serta adanya prasyarat kehalalan akan
produk gelatin bagi umat muslim, maka bahan baku alternatif dari berbagai jenis ikan
sebagai sumber gelatin selain dari babi dan sapi terus dikembangkan (Jamilah dan
Harvinder, 2002). Beberapa penelitian telah dilakukan, seperti eksplorasi gelatin yang
bersumber dari kulit dan tulang berbagai spesies ikan (Irwandi 2009, Phanat 2010). Namun
sampai saat ini, hanya 1 % dari produksi gelatin dunia berasal dari ikan. Produk gelatin
ikan tidak berhasil menarik perhatian masyarakat karena faktor alergi dan fishy odour
(Rammaya,2012). Sehingga pengembangan gelatin dari sumber selain ikan perlu dikaji
potensinya.
Daging ayam merupakan daging yang paling populer dan murah untuk dikonsumsi
daging ayam meningkat setiap tahunnya. Kulit ayam sebagai hasil samping industri rumah
potong ayam (RPA) belum banyak dimanfaatkan untuk diproses menjadi produk baru yang
bernilai tinggi (Cliche, 2003). Kandungan kolagen yang tinggi pada kulit ayam 38,9%
(Cliche, 2003) sangat potensial untuk dikembangkan menjadi bahan baku alternatif gelatin.
Beberapa penelitian tentang ekstraksi gelatin dari ayam telah dilakukan. Abustam (2008),
telah berhasil mengekstraksi gelatin dari kulit kaki ayam melalui perendaman dengan
menggunakan asam asetat 1% selama 24 jam diperoleh hasil optimum rendemen 12,9 %
dan kekuatan gel 261,44 g bloom.
Miskah (2010) dalam penelitiannya melaporkan ekstraksi gelatin dari tulang dan kulit
kaki ayam melalui variasi konsentrasi asam asetat (CH3COOH) 4%, 5%, 6%, 7%, 8% dan
HCl 4%, 5%, 6%, 7%, 8% serta waktu perendaman 1 hari, 2 hari, 3 hari, 4 hari dan 5 hari,
menghasilkan konsentrasi terbaik pada pembuatan gelatin untuk HCl adalah 4 % yang
menghasilkan rendemen sebesar 11,2 %, sedangkan untuk CH3COOH adalah 7 %
menghasilkan rendemen sebesar 7,956 % dengan waktu perendaman terbaik adalah 1 hari.
Isolasi dan karakterisasi gelatin dari kulit ceker ayam Broiler dengan metode
ekstraksi terkombinasi dengan perendaman basa NaOH dan asam asetat yang
dikombinasikan dengan ekstraksi pelarut menggunakan etanol untuk meghilangkan lemak
telah dilakukan oleh Puspawati dkk, 2011, namun gelatin yang dihasilkan kandungan
lemaknya masih diatas 5% (Puspawati, 2011). Rammaya (2012) dalam penelitiannya
melaporkan ekstraksi gelatin dari residu mechanically deboned chicken meat (MDCM)
yang dilakukan dengan perendaman basa NaOH selama 72 jam dan dengan variasi suhu
ekstraksi pada 60oC,70oC, dan 80oC selama 2 jam yang dilakukan pada pH 4 menghasilkan gelatin dengan kekutan gel rendah (<100 gr bloom), dimana semakin tinggi suhu maka
kekuatan gel gelatin yang diperoleh semakin rendah. Peneliti lainnya, Norizah et.al, 2012,
melaporkan untuk pertama kali ekstraksi gelatin dari kulit ayam kering yang telah diekstrak
lemaknya dengan ekstraksi soxhlet, dengan proses perendaman menggunakan kombinasi
basa NaOH dan asam (asam sulfat dan asam sitrat) masing-masing selama 2 jam, dan
gelatin sapi. Namun Puspawati (2014), melaporkan optimasi proses ekstraksi gelatin dari
kulit ayam broiler yang dilakukan melalui variasi suhu dan lama ekstraksi dengan proses
perendaman campuran basa NaOH 0,15 % dan asam (H2SO40,15% dan asam sitrat0,7%)
menghasilkan gelatin dengan kekuatan gel tertinggi yaitu 145,95 g bloom yang diperoleh
pada suhu ekstraksi 40oC selama 12 jam.
Salah satu kelemahan dari gelatin yang berasal dari non mamalia adalah sifat
mekaniknya yang kurang bagus (rendahnya kekuatan gel gelatin) sehingga pemanfaatannya
terbatas dalam bidang industri non pangan khususnya dalam industri kedokteran. Salah satu
faktor yang berpengaruh terhadap sifat mekanik gelatin adalah komposisi asam amino dan
berat molekulnya (Gudmundson, 2002, Norland, 1990).
Dari uraian diatas, beberapa penelitian tentang ekstraksi dan karakterisasi sifat
fisikokimia gelatin dari kulit ayam telah dilaporkan, namun belum banyak penelitian yang
dilakukan untuk mengkaji pengaruh komposisi asam amino dan pola protein gelatin
(tingkat kemurnian dan berat molekul relatif) terhadap sifat mekanik gelatin khususnya
kekuatan gel. Untuk itu sangatlah penting mempelajari bagaimana pengaruh proses
perendaman dengan jenis asam yang berbeda (sitrat, asetat, dan laktat) terhadap komposisi
dan pola protein produk gelatin yang dihasilkan dan sifat mekaniknya khususnya kekuatan
gel.
1.2. Rumusan Masalah
Dari uraian diatas maka permasalahan yang diangkat adalah:
1. Bagaimana komposisi asam amino dan pola protein dari gelatin halal hasil
ekstraksi kulit ayam Broiler melalui proses perendaman dengan variasi jenis
asam yang digunakan?
2. Bagaimana pengaruh komposisi asam amino dan pola protein gelatin terhadap
1.3. Tujuan Khusus
1. Menganalisis komposisi asam amino dan pola protein dari gelatin halal hasil
ekstraksi kulit ayam Broiler melalui proses perendaman dengan jenis asam yang
berbeda?
2. Mengetahui pengaruh komposisi asam amino dan berat molekul gelatin terhadap
sifat mekanik gelatin khususnya kekuatan gel.
1.4. Urgensi Penelitian
Pemanfaatan gelatin yang sangat luas di bidang industri makanan, kosmetik,
farmasi, obat-obatan, tekstil, kertas, dan fotografi menyebabkan kebutuhan akan gelatin
cenderung meningkat tiap tahunnya. Sampai saat ini, Indonesia masih mengimpor gelatin
untuk memenuhi kebutuhan gelatin dalam negeri. Gelatin yang beredar di pasaran, 46 %
berasal dari kulit babi, 29,4 % dari kulit sapi, 23,1 % dari tulang sapi, dan hanya 1,5 % dari
sumber lainnya (GME, 2008). Akhir-akhir ini, adanya pertimbangan dan ketakutan akan
BSE dan pengaruh penyakit sapi gila, serta adanya prasarat kehalalan akan produk gelatin
bagi umat muslim, maka bahan baku alternatif sebagai sumber gelatin selain dari babi dan
sapi sangat penting untuk dikembangkan.dan diteliti. Penelitian dan pengembangan gelatin
dari tulang dan kulit ikan sudah banyak dilakukan namun produk gelatin ikan kurang
diminati karena baunya dan faktor alergi bagi beberapa orang. Kulit ayam sebagai hasil
samping produksi RPA belum banyak dimanfaatkan untuk diproses menjadi produk baru
yang bernilai tinggi (Cliche, 2003). Kandungan kolagen yang tinggi pada kulit ayam
38,9% (Cliche, 2003) sangat potensial untuk dikembangkan menjadi bahan baku penyedia
gelatin halal. Beberapa penelitian tentang ekstraksi dan karakterisasi sifat fisikokimia
gelatin dari kulit ayam telah dilaporkan, namun belum banyak penelitian yang dilakukan
untuk mengkaji pengaruh komposisi asam amino dan pola protein gelatin (tingkat
kemurnian dan berat molekul relatif) terhadap sifat mekanik gelatin khususnya kekuatan
gel. Untuk itu sangatlah penting mempelajari bagaimana pengaruh proses perendaman
dengan jenis asam yang berbeda (sitrat, asetat, dan laktat) terhadap komposisi dan pola
BAB II. TINJAUAN PUSTAKA
2.1 Ayam Broiler
Ayam pedaging (Broiler) merupakan ayam ras yang memiliki daya produktivitas
tinggi sehingga dapat menghasilkan produksi daging dalam waktu relatif singkat (5-6
minggu).Ayam broiler sering dibudidayakan karena memiliki masa panen yang pendek dan
relatif mudah dalam pemeliharaan, sehingga dalam waktu yang singkat sudah dapat
dipasarkan (Abbas dan Rusmana, 1995).
Kulit ayam merupakan bagian yang berfungsi melindungi permukaan tubuh.Kulit
terdiri dari dua lapis, lapisan luar disebut epidermis dan bagian dalam disebut
dermis.Dermis tersusun dari jaringan pengikat yang mengandung banyak lemak dan serat
kolagen (Nurwantoro dan Mulyani, 2003).Kolagen merupakan sejenis protein yang
mengandung asam amino prolin dan hidroksiprolin. Kandungan kolagen pada kulit ayam
diperkirakan sebesar 38,9% (Cliche, 2003) sehingga kulit ayam berpotensi untuk
dikembangkan menjadi bahan baku pembuatan gelatin.
2.2 Kolagen
Kolagen merupakan komponen struktural utama dari jaringan ikat putih
(whiteconnetive tissue) yang meliputi hampir 30 persen dari total protein pada jaringan dan
organ tubuh vertebrata dan invertebrata. Pada mamalia, kolagen terdapat di kulit, tendon,
tulangrawan, dan jaringan ikat. Demikian juga pada burung dan ikan, sedangkan pada
avertebrata kolagen terdapat pada dinding sel (Bailey dan Light,1989). Molekul kolagen
tersusun dari kira-kira dua puluh asam amino yang memiliki bentuk agak berbeda
bergantung pada sumber bahan bakunya. Asam amino glisin, prolin, dan hidroksiprolin
merupakan asam amino utama kolagen. Asam-asam amino aromatik dan sulfur terdapat
dalam jumlah yang sedikit. Hidroksiprolin merupakan salah satu asam amino pembatas
dalam berbagai protein (Chaplin, 2005). Molekul dasar pembentuk kolagen disebut
tropokolagen yang mempunyai struktur batang dengan BM 300 kDa, dimana di dalamnya
terdapat tiga rantai polipeptida yang sama panjang bersama-sama membentuk struktur
tersendiri, menahan bersama-sama dengan ikatan hidrogen antara group NH dari residu
glisin pada rantai yang satu dengan grup CO pada rantai lainnya. Cincin pirolidin, prolin,
dan hidroksiprolin membantu pembentukan rantai polipeptida dan memperkuat triple heliks
(Wong, 1989).
Gambar 2.1. Struktur Triple Helix Penyusun Gelatin
Tropokolagen akan terdenaturasi oleh pemanasan atau perlakuan dengan zat seperti
asam, basa, urea, dan potassium permanganat, selain itu serabut kolagen dapat
mengalami penyusutan jika dipanaskan di atas suhu penyusutannya (Ts). Suhu penyusutan
(Ts) kolagenikan adalah 45oC. Jika kolagen dipanaskan pada T>Ts (misalnya 65 ± 70oC), serabut triple heliks yang dipecah menjadi lebih panjang. Pemecahan struktur tersebut
menjadi lilitan acak yang larut dalam air inilah yang disebut gelatin. Menurut
Fernandez-Diaz, et. al (2001), kolagen kulit ikan lebih mudah hancur daripada kolagen kulit hewan,
dimana kedua jenis kolagen ini akan hancur oleh proses pemanasan dan aktivitas enzim.
2.3. Gelatin
Gelatin merupakan salah satu produk turunan protein yang diperoleh dari hasil
hidrolisis kolagen hewan yang terkandung dalam tulang dan kulit, dan merupakan senyawa
yang tidak pernah terjadi secara alamiah. Gelatin mempunyai titik leleh 35oC, di bawah suhu tubuh manusia. Titik leleh inilah yang membuat produk gelatin mempunyai
karakteristik yang unik bila dibandingkan dengan bahan pembentuk gel lainnya seperti pati,
alginat, pektin, agar-agar dan karaginan yang merupakan senyawa karbohidrat (Gomez dan
propilen glikol, sorbitol dan manitol tetapi tidak larut dalam aseton, karbon tetraklorida,
benzene, petroleum eter, dan pelarut organik lainnya. Pada kondisi tertentu juga larut dalam
campuran aseton-air dan alkohol-air (Viro, 1992). Gelatin dapat berubah secara reversible
dari bentuk sol ke gel, mengembang dalam air dingin, dapat membentuk film,
mempengaruhi viskositas suatu bahan. Sifat-sifat yang dimiliki gelatin tersebut
menyebabkan gelatin lebih disukai dibandingkan bahan-bahan pembentuk gel lain seperti
karagenan, pektin, dan gum arab (Peranginangin, 2007).
Senyawa gelatin merupakan suatu polimer linier asam-asam amino. Pada umumnya
rantai polimer tersebut merupakan perulangan dari asam amino glisin-prolin-prolin atau
glisin-prolin-hidroksiprolin. Dalam gelatin tidak terdapat asam amino triptofan, sehingga
gelatin tidak dapat digolongkan sebagai protein yang lengkap (Gelatin Food Science,
2007). Gelatin tersusun atas 18 asam amino yang saling terikat dan dihubungkan dengan
ikatan peptida membentuk rantai polimer yang panjang (Eastoe dan Leach, 1977). Secara
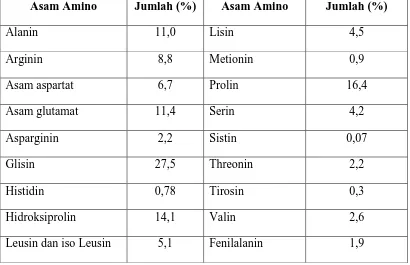
lengkap komposisi asam amino gelatin disajikan pada Tabel 2.1.
Tabel 2.1. Komposisi Asam Amino Gelatin
Asam Amino Jumlah (%) Asam Amino Jumlah (%)
Alanin 11,0 Lisin 4,5
Arginin 8,8 Metionin 0,9
Asam aspartat 6,7 Prolin 16,4
Asam glutamat 11,4 Serin 4,2
Asparginin 2,2 Sistin 0,07
Glisin 27,5 Threonin 2,2
Histidin 0,78 Tirosin 0,3
Hidroksiprolin 14,1 Valin 2,6
Leusin dan iso Leusin 5,1 Fenilalanin 1,9
Komposisi asam amino mempengaruhi sifat mekanik dari produk gelatin. Bila
kandungan asam iminonya (prolin dan hidroksi prolin) rendah maka kekuatan gel dan titik
lelehnyapun akan rendah sehingga sifat mekaniknyapun kurang bagus. Penurunan
komposisi asam amino tergantung pada metode pembuatannya. Pembuatan dengan proses
alkali umumnya lebih banyak mengandung hidroksiprolin dan lebih sedikit tirosin
dibandingkan dengan proses asam (Ward dan Courts, 1977). Struktur kimia gelatin dapat
dilihat pada Gambar 2.2.
Gambar 2.2. Struktur Kimia Gelatin (Poppe, 1992)
Gelatin terbagi menjadi dua tipe berdasarkan perbedaan proses pengolahannya,
yaitu tipe A dan tipe B. Dalam pembuatan gelatin tipe A, bahan baku diberi perlakuan
perendaman dalam larutan asam sehingga proses ini dikenal dengan sebutan proses asam.
Sedangkan dalam pembuatan gelatin tipe B, perlakuan yang diaplikasikan adalah perlakuan
basa. Proses ini disebut proses alkali (Utama, 1997).Bahan baku yang biasanya digunakan
pada proses asam adalah tulang dan kulit babi, sedangkan bahan baku yang biasa digunakan
pada proses basa adalah tulang dan kulit jangat sapi (Viro, 1992). Menurut Wiyono (2001),
gelatin ikan dikatagorikan sebagai gelatin tipe A. Secara ekonomis, proses asam lebih
disukai dibandingkan proses basa. Hal ini karena perendaman yang dilakukan dalam proses
asam relatif lebih singkat dibandingkan proses basa (Wiyono, 2001). Sifat gelatin
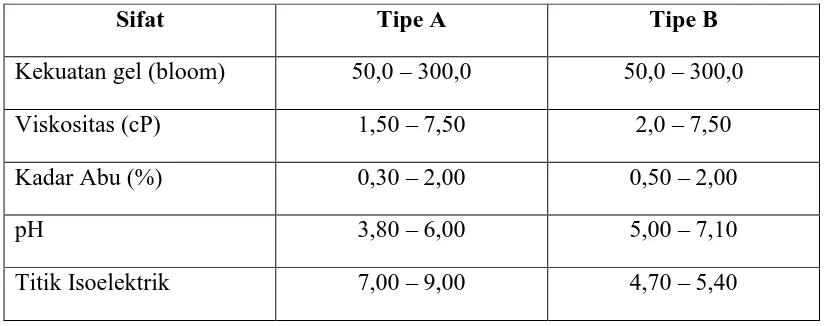
Tabel 2.2. Sifat Gelatin Berdasarkan Jenisnya
Sifat Tipe A Tipe B
Kekuatan gel (bloom) 50,0 – 300,0 50,0 – 300,0
Viskositas (cP) 1,50 – 7,50 2,0 – 7,50
Kadar Abu (%) 0,30 – 2,00 0,50 – 2,00
pH 3,80 – 6,00 5,00 – 7,10
Titik Isoelektrik 7,00 – 9,00 4,70 – 5,40
Sumber: GMIA (2007)
Salah satu sifat fisik gelatin yang menentukan mutu gelatin adalah kemampuannya
untuk membentuk gel yang disebut kekuatan gel. Sifat fisik penting lainnya adalah
viskositas (Poppe (1992). Viskositas terutama dipengaruhi oleh interaksi hidrodinamik
antar molekul gelatin, dipengaruhi suhu, pH dan konsentrasi. Standar mutu gelatin untuk
industri dapat dilihat pada Tabel 2.3.
Tabel 2.3. Standar Mutu Gelatin Menurut SNI No. 06-3735 Tahun 1995 dan British Standard: 757 Tahun 1975
Karakteristik SNI No. 063735a British Standar 757b
Warna Tidak berwarna sampai
kekuningan
Kuning pucat
Bau. rasa Normal -
Kadar air Maksimum 16% -
Kadar abu Maksimum 3,25% -
Kekuatan gel - 50 – 300 bloom
Viskositas - 15 – 70 mps atau 1,5 – 7
cP
Logam berat Maksimum 50 mg/kg -
Arsen Maksimum 2 mg/kg -
Tembaga Maksimum 30 mg/kg -
Seng Maksimum 100 mg/kg -
Sulfit Maksimum 1000 mg/kg -
Sumber: a) Dewan Standarisasi Nasional (SNI 06.3735-1995) (1995)
b) British Standard: 757 (1975)
Proses produksi utama gelatin dapat dibagi menjadi tiga tahapan, yaitu persiapan
bahan baku, konversi kolagen menjadi gelatin, dan yang terakhir perolehan gelatin dalam
bentuk kering. Metode pengkonversian kolagen menjadi gelatin adalah dengan denaturasi
kolagen. Proses denaturasi terjadi dengan pemanasan kolagen pada suhu 40oC atau lebih dengan penambahan senyawa pemecah ikatan hidrogen pada suhu kamar atau lebih rendah,
berupa pemecahan struktur koil kolagen menjadi satu, dua atau tiga rantai polipeptida
secara acak (Gomez dan Montero, 2001).
Konversi kolagen menjadi gelatin terjadi dalam tiga tahap, yaitu hidrolisis lateral,
hidrolisis ikatan polipeptida terutama glisin, dan penghancuran struktur kolagen (Ward dan
Courts, 1977). Menurut Hadiwiyoto (1983) produksi gelatin meliputi tahap-tahap
pengecilan ukuran bahan baku, perendaman, pencucian, pemanasan, pemekatan,
pendinginan, dan pengeringan. Pengecilan ukuran disini menurutnya diperlukan untuk lebih
memperluas permukaan bahan sehingga proses dapat berlangsung lebih cepat dan
sempurna.
Ekstraksi adalah proses denaturasi untuk mengubah kolagen menjadi gelatin dengan
penambahan senyawa pemecah ikatan hidrogen pada suhu kamar atau suhu ang lebih
rendah. Ekstraksi juga dapat dilakukan dengan menggunakan air panas, dimana pada proses
ini terjadi denaturasi, peningkatan hidrolisis dan kelarutan gelatin. Setelah diperoleh ekstrak
dilakukan dengan menggunakan evaporator vakum dengan suhu 43-45oC dan dilanjutkan dengan menggunakan freeze dryer atau oven pada suhu antara 30-60oC (Viro, 1992).
2.3. SDS-PAGE (Elektroforesis Gel Poliakrilamida-Sodium Dodesil Sulfat)
Elektroforesis merupakan proses bergeraknya molekul bermuatan pada suatu medan
listrik. Kecepatan molekul yang bergerak pada medan listrik tergantung pada muatan,
bentuk dan ukuran. Dengan demikian elektroforesis dapat digunakan untuk separasi
makromolekul (seperti protein dan asam nukleat). Posisi molekul yang terseparasi pada gel
dapat dideteksi dengan pewarnaan atau autoradiografi, ataupun dilakukan kuantifikasi
dengan densitometer.
Elektroforesis untuk makromolekul memerlukan matriks penyangga untuk
mencegah terjadinya difusi karena timbulnya panas dari arus listrik yang digunakan.
Elektroforesis biasanya memerlukan media penyangga sebagai tempat bemigrasinya
molekul-mulekul biologi. Media penyangganya bermacam-macam tergantung pada tujuan
dan bahan yang akan dianalisa. Media penyangga yang seringdipakai dalam elektroforesis
antara lain yaitu kertas, selulose, asetat dan gel. Gel poliakrilamid dan agarosa merupakan
matriks penyangga yang banyak dipakai untuk separasi protein dan asam nukleat. Beberapa
faktor mempengaruhi kecepatan migrasi dari molekul protein (Soedarmadji, 1996), yakni:
1. Ukuran molekul protein
Migrasi molekul protein berukuran besar lebih lambat daripada migrasi molekul
berukuran kecil.
2. Konsentrasi gel
Migrasi molekul protein pada gel berkosentrasi rendah lebih cepat daripada
migrasi molekul protein yang sama pada gel berkosentrasi tinggi.
3. Bufer (penyangga)
Dapat berperan sebagai penstabil medium pendukung dan dapat mempengaruhi
kecepatan gerak senyawa karena ion sebagai pembawa protein yang bermuatan.
listrik menjadi maksimal. Hal ini dapat mempercepat gerakan molekul protein.
Kekuatan ion rendah dalam bufer akan menurunkan panas sehingga aliran listrik
akan sangat minimal dan migrasi molekul protein sangat lambat.
4. Medium penyangga
Medium pendukung ideal untuk elektroforesis adalah bahan kimia inert yang
bersifat relatif stabil, mudah ditangani dan mempunyai daya serap yang baik,
sebagai migrasi elektron atau penyaringan berdasarkan ukuran molekul seperti
gel poliakrilamid (Sudarmadji, 1996). Jika ukuran pori dari medium kira-kira
sama dengan molekul, maka molekul yang lebih kecil akan berpindah lebih
bebas di dalam medan listrik, sedangkan molekul yang lebih besar akan dibatasi
dalam migrasinya. Besarnya pori-pori dapat diatur dengan mengubah konsentrasi
penyusun gel poliakrilamidnya yaitu akrilamid dan bisakrilamid.
5. Kekuatan voltase
- Voltase yang dipakai rendah (100-500) V, kecepatan migrasi molekul
sebanding dengan tingginya voltase yang digunakan.
- Voltase yang dipakai tinggi (500-10000) V, mobolitas molekul meningkat
secara lebih tajam dan digunakan untuk memisahkan senyawa dengan BM
rendah serta jenis arus yang dipakai selalu harus searah (bukan bolak balik).
6.Temperatur medium disaat proses elektroforesis berlangsung.
Jika temperatur tinggi akan mempercepat proses bermigrasinya protein dan
sebaliknya jika temperatur rendah akan mengurangi kekuatan bermigrasinya
protein. Pada saat elektroforesis berlangsung, protein akan bergerak dari
elektroda negatif menuju elektroda positif sampai pada jarak tertentu pada gel
poliakrilamid tergantung pada berat molekulnya. Semakin rendah berat
Sebaliknya protein dengan berat molekul lebih besar akan bergerak pada jarak
yang lebih pendek atau mobilitasnya rendah (Sumitro et al., 1996).
Hasil elektroforesis akan didapatkan pita-pita protein yang terpisahkan berdasarkan
berat molekulnya. Tebal tipisnya pita yang terbentuk dari pita protein menunjukkan
kandungan atau banyaknya protein yang mempunyai berat molekul yang sama yang berada
pada posisi pita yang sama. Hal ini sejalan dengan prinsip pergerakan molekul bermuatan,
yakni molekul bermuatan dapat bergerak bebas di bawah pengaruh medan listrik, molekul
dengan muatan dan ukuran yang sama akan terakumulasi pada zona atau pita yang sama
atau berdekatan (Soedarmadji, 1996).
Gambar 2.3. Contohelektroforegram gelatin dari Bigeye snapper (Priacanthus tayenus) (Sukkwai, 2011)
BAB III. METODE PENELITIAN
3.1Alat dan Bahan
Bahan dasar penelitian ini adalah kulit ayam Broileryang dibeli dari RPA UD Eka
Prasetya Nusa Dua, Badung. Bahan-bahan kimia yang digunakan dalam penelitian ini
adalah aquades, aquademineral, asam sulfat (0,15%b/v), asam sitrat (C6H8O7) 1 % (b/v),
asam laktat(C3H6O3) 1% v/v, asam asetat (CH3COOH) 1% (v/v), NaOH (0,15%), pH
indicator,n-heksana, dan gelatin komersial, kertas saring WhatmanNo.4, kertas saring
Alat kimia yang digunakan adalah berupa alat-alat gelas yang biasa digunakan di
Laboratorium kimia dan ditunjang dengan alat lainnya yaitu seperangkat alat soxhlet, hot
plate dan magnetic stirrer, ember, tray, loyang, botol sample, toples plastik, cawan petri,
blender, pisau, waterbath, pH meter, thermometer, oven, teflon, spatula, saringan, corong,
beker gelas, erlenmeyer, timbangan, desikator, cawan petri, oven, TA-XT CT3 Analyser,
viskositas ostwald, FTIR Szimadsu Prestige 21, Elektroforesis.
3.2Tempat Penelitian
Penelitian ini dilaksanakan di Laboratorium Penelitian dan Laboratorium Kimia
Organik Jurusan Kimia, FMIPA, UNUD, Lab. Bersama FMIPA UNUD, Lab. EHP
Teknologi Pertanian, Jember, Lab. Center for Development of Advances Sciences and
Technology CDAST), Jember, dan Lab. Balai Penelitian Ternak Bogor..
3.3 Prosedur Kerja
Proses iolasi gelatin dari kulit ayam Broiler pada penelitian ini mengikuti prosedur
Badii dan Howel (2006), dengan sedikit modifikasi yang terdiri dari tahap persiapan,
perendaman, ekstraksi dan pengeringan, karakterisasi (Figure 3.1).
Penyiapan bahan baku:
15 kg kulit ayam yang segar dibeli dari RPA dicuci bersih dengan air untuk
menghilangkan kotoran-kotoran yang menempel. Lemak yang menempel dipisahkan dari
kulit ayam sebelum dicuci dengan air bersih. Kulit ayam dipotong kecil-kecil ±2-3 cm.
Kulit ayam yang telah dipotong-potong dikeringkan dengan freez drier kemudian kulit
ayam yang telah kering diblender sehingga diperoleh serbuk kulit ayam. Serbuk kulit ayam
selanjutnya diekstrak lemaknya dengan metode soxhletasi menggunakan pelarut n-heksana.
Tahap Perendaman (Pre-Treatment)
Serbuk kulit ayam yang telah bebas lemak kemudian dibagi menjadi 3 bagian yang
nantinya akan dibagi lagi menjadi 3 bagian untuk dilakukan pengulangan. Masing-masing
sebesar ± 15 g serbuk sampel dicampur dengan 200 mL NaOH (0,15% b/v) diaduk dengan
dibuang, residunya kemudian dicuci dengan aquades dan dicampur dengan asam sulfat
(0.15%v/v) diaduk perlahan selama 40 menit dan disentrifugasi. Supernatannya dibuang
dan residunya kemudian direndam dengan 200 mL asam sitrat (1% b/v) diaduk sebentar,
didiamkan selama 40 menit. Setiap 40 menit larutannya dibuang dan diganti dengan larutan
yang baru (dilakukan 3 X). Setelah itu, disaring. Residu yang diperoleh dicuci dengan
aquades sampai pH 4-5 kemudian ditambahkan aquademineral (1:1) dan diekstrak pada
waterbath dengan suhu 45oC selama 24 jam. Prosedur yang sama dilakukan untuk perendaman dengan jenis asam lainnya yaitu asam asetat dan asam laktat. Masing-masing
perlakuan dilakukan pengulangan 3 kali. (Skema Kerja 3.1)
Tahap Pengeringan Gelatin
Ekstrak gelatin yang diperoleh dari masing-masing perlakuan kemudian disaring
menggunakan kertas saring Whatman, diukur volumenya, dimasukkan dalam botol kaca
kedap udara dan diletakkan dalam lemari pendingin bersuhu 4-10oC selama 24 jam. Ekstrak yang telah berubah menjadi gel kemudian diletakkan dalam cawan petri (teflon) dan dioven
selama 24 jam pada suhu 60oC (Cho et. al, 2004), dan didinginkan dalam desikator. Lapisan gelatin yang terbentuk diseluruh permukaan dikerok lalu ditumbuk hingga menjadi
gelatin bubuk dan ditimbang dan disimpan dalam desikator.
Tahap Karakterisasi
Serbuk gelatin yang diperoleh dikarakterisasi gugus fungsinya dengan FTIR di Lab
Bersama FMIPA UNUD. Sedangkan penentuan kekuatan gel akan dilakukan Laboratorium
EHP Fakultas Teknologi Pertanian Universitas Jember, analiis asam amino dilakukan di
ANALISIS ASAM AMINO (Muchtadi, 1992)
Sebanyak 0,2 gram sampel disiapkan dalam tabung reaksi tertutup dan ditambahkan
sebanyak 5 mL HCl 6 N. Sampel dimasukkan dalam oven dengan suhu 100oC selama 18-24 jam. Selanjutnya sampel disaring dengan kertas saring Whatman 40. Hasil hidrolisis
dipipet sebanyak 10µl dan dimasukkan ke dalam tabung reaksi. Kemudian ditambahkan 30
µl larutan pengering, lalu dikeringkan dengan pompa vacuum. Sampel yang telah
dikeringkan ditambahkan larutan derivate sebanyak 30 µl dan dibiarkan kering selama 20
menit. Sampel kemudian diencerkan dengan 200 µl larutan pengencer natrium asetat 1M.
Sampel siap dianalisis dengan HPLC.
Analisis Berat Molekul Gelatin Dengan Metode SDS-PAGE
Sebanyak 50miligram sampel dilarutkan dalam 1,0 mLlarutan buffer(250mM Tris-Cl
pH7,5; 5 mM EDTA; 2% SDS), kemudian dipanaskan pada suhu 85oC selama 1 jam. Setelah itu larutandicampur dengan buffersampel0,5 M tris-HCl, pH 6,8( yang mengandung
4% (b/v) SDS, 20% (v/v) gliserol, dan 10% (v/v) ME) dengan perbandingan 1: 1 (v/v).
Kemudian campuran dipanaskan dengan suhu 100oC selama 3 menit. Sampel dimasukkan ke dalam gel poliakrilamida yang dibuat dengan 7,5% (v/v) running gel dan 4% (v/v)
stacking gel sebanyak :
Elektroforesis dilakukan pada arus konstan 15 mA, kemudian gel diwarnai dengan
buffer staining0,1% (b/v) Coomassie biru R-250 dalam 15% (v/v) metanol dan 5% (v/v)
BAB IV. HASIL DAN PEMBAHASAN 4.1 Penyiapan Bahan Baku
Pembuatan gelatin dari kulit ayam broiler pada penelitian ini dilakukan dengan
menggunakan pelarut kombinasi asam-basa. Serbuk kulit ayam sebelum digunakan pada
tahap awal ekstraksi gelatin, dianalisis kandungan kimianya yang meliputi kadar air, kadar
abu, kadar lemak dan kadar protein. Hasil analisis kandungan kimia dari serbuk kulit ayam
disajikan pada Tabel 4.1.
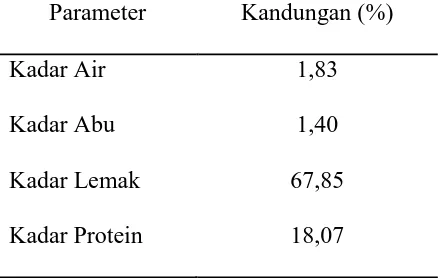
Tabel 4.1. Hasil Analisis Proksimat Serbuk Kulit Ayam Broiler
Parameter Kandungan (%)
Kadar Air 1,83
Kadar Abu 1,40
Kadar Lemak 67,85
Kadar Protein 18,07
Berdasarkan data pada Tabel 4.1., kadar air yang terkandung dalam sampel kulit
ayam sebesar 1,83% yang menunjukkan bahwa sampel yang digunakan tidak dalam
keadaan segar karena telah melalui proses pengeringan menggunakan freeze drier (Gambar
4.1). Proses pengeringan sampel bertujuan agar sampel tidak mudah rusak bila disimpan
dalam jangka waktu yang lama. Kadar abu dalam sampel kulit ayam adalah 1,40% yang
menandakan kandungan mineral dalam kulit ayam cukup rendah. Pada vertebrata, sepertiga
total massa proteinnya disusun oleh kolagen yang terdapat pada jaringan ikat dalam otot,
kulit, tulang, tulang rawan, gigi dan tendon (de Man, 1997). Kandungan protein yang
sebagai bahan baku pembuatan gelatin. Kandungan lemak pada sampel kulit ayam sebesar
67,85%. Lemak yang terkandung pada kulit ayam sangat tinggi, sehingga perlu dilakukan
ekstraksi lemak pada sampel kulit ayam sebelum proses perendaman. Pada penelitian ini,
lemak yang terkandung pada sampel kulit ayam diekstraksi dengan metode soxhletasi
menggunakan pelarut n-heksana sehingga diperoleh serbuk kulit ayam bebas lemak
(Gambar 4.2) .
Gambar 4.1. Kulit ayam kering Gambar 4.2. Serbuk kulit ayam bebas lemak
4.2 Proses Perendaman
Pada proses perendaman digunakan beberapa pelarut yaitu NaOH (0,15% b/v),
H2SO4 (0,15% v/v), dan variasi asam yaitu asam sitrat (C3H5O(COOH)3) (1% b/v), asam
laktat 1%, dan asam asetat 1%, yang bertujuan untuk mempercepat proses perendaman
(3x40 menit untuk masing-masing pelarut) yang mana dengan pelarut tunggal memerlukan
waktu yang relatif lebih lama.
Perendaman dengan basa NaOH bertujuan untuk melarutkan protein non-kolagen
dan penghilangan warna (decolorisation). Hal ini dapat dilihat setelah perendaman dengan
NaOH sampel yang semula berwarna kuning kecoklatan menjadi lebih bersih dan
mengembang (Gambar 4.3). Setelah direndam NaOH kemudian dicuci sampai pH
mendekati netral kemudian direndam kembali dengan H2SO4 (0,15% v/v) selama 3 x 40
menit untuk proses demineralisasi. Setelah disaring kulit ayam direndam kembali dengan
(C3H5O(COOH)3) (1% b/v) selama 3x40 menit. Proses perendaman menyebabkan
karena adanya interaksi antara jaringan kolagen dengan pelarut yang digunakan. Prosedur
yang sama juga dilakukan untuk hidrolisis dengan perendamann asam laktat 1% v/v, dan
asam asetat 1% v/v. Dari rata-rata 15 g serbuk sampel yang digunakan, setelah perendaman
beratnya bertambah rata-rata menjadi 109-258 g (Gambar 4.4).
Gambar 4.3.Kulit ayam setelah perendaman NaOH Gambar 4.4.Kulit ayam setelah perendaman
4.3 Proses Ekstraksi
Kulit ayam yang telah direndam kemudian dicuci dengan aquades mengalir sampai
pH 4-5. Proses ekstraksi dilakukan pada suasana asam karena pada umumnya pH tersebut
merupakan titik isoelektrik dari komponen protein non-kolagen (Fatimah 1996). Sehingga
pada saat proses ekstraksi protein non-kolagen tidak ikut terekstrak. Proses ekstraksi
dilakukan pada sistem waterbath dengan perbandingan sampel kulit ayam dan
quademineral (1:1). Proses ekstraksi berfungsi sebagai lanjutan untuk merusak ikatan
hidrogen antar molekul tropokolagen dan ikatan hidrogen antara rantai-α dalam
tropokolagen yang pada tahap perendaman belum semuanya terurai secara sempurna.
Ikatan hydrogen antara rantai α dalam tropokolagen kali ini didenaturasi oleh molekul H2O.
Tahap ekstraksi ini menyebabkan rantai triple-helix kehilangan stabilitasnya dan akhirnya
terurai menjadi γ rantai α. Denaturasi kolagen menyebabkan rantai tripel-helix secara sempurna bertransformasi menjadin rantai tunggal gelatin. Ekstraksi dilakukan pada
Gambar 4.5 Proses ekstraksi Waterbath Gambar 4.6 Gel sebelum dioven
Hasil ekstraksi kemudian disaring menggunakan kertas saring Whatman No.4.
Kertas saring ini dapat menyaring hasil ekstraksi material organik yang memiliki ukuran
partikel 20-25µm. Filtrat ditampung dan ditempatkan pada toples kemudian disimppan di
lemari pendingin pada suhu 4-10oC selama 24 jam. Perlakuan pada tahap ini adalah untuk membuktikan bahwa ekstrak tersebut adalah gelatin. Hasil ekstrak menunjukkan perubahan
menjadi gel pada suhu 10oC. Pada saat pendinginan, rantai-rantai polipeptida gelatin dapat secara acak kembali membentuk struktur triple-helix. Gel kemudian dioven pada suhu
60oC selama 48 jam untuk proses pengeringan sehingga diperoleh lapisan tipis gelatin (padatan). Suhu dibuat tidak terlalu tinggi untuk menghindari denaturasi rantai polipeptida.
Pada perlakuan ini, gelatin yang semula dalam fase gel mencair akibat pemanasan. Setelah
kering dan didinginkan dalam desikator, gelatin membentuk lapisan tipis pada teflon.
Lapisan ini kemudian dikerok, ditimbang dan dihitung rendemennya.
4.4Karakterisasi Produk Gelatin 4.4.1 Rendemen gelatin
Rendemen merupakan parameter yang penting diketahui untuk menilai efektif
tidaknya proses produksi gelatin. Semakin besar nilai rendemen yang dihasilkan maka
semakin efesien perlakuan yang diberikan. Nilai rendemen gelatin kulit ayam dari berbagai
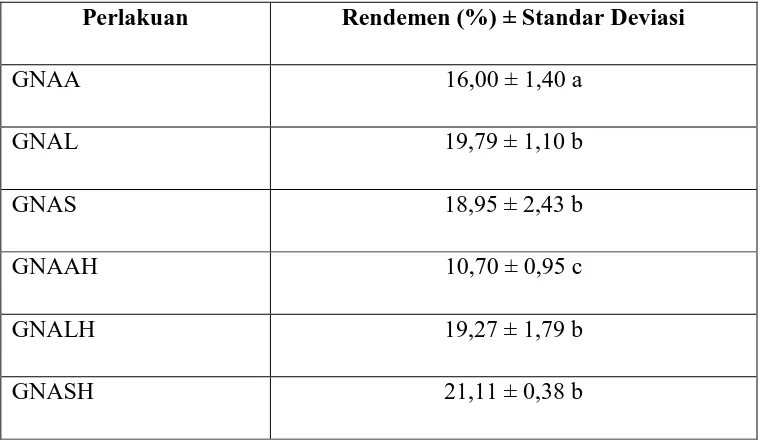
Tabel 4.2. Pengaruh Perlakuan Terhadap Nilai Rendemen Gelatin Kulit Ayam
Perlakuan Rendemen (%) ± Standar Deviasi
GNAA 16,00 ± 1,40 a
GNAL 19,79 ± 1,10 b
GNAS 18,95 ± 2,43 b
GNAAH 10,70 ± 0,95 c
GNALH 19,27 ± 1,79 b
GNASH 21,11 ± 0,38 b
Keterangan: Data yang diikuti huruf berbeda pada kolom menunjukkan perbedaan nyata menurut uji Duncan pada taraf ketelitian 5%
GNAA : gelatin dengan perlakuan asam asetat tanpa demineralisasi dengan asam sulfat GNAL : gelatin dengan perlakuan asam laktat tanpa demineralisasi dengan asam sulfat GNAS : gelatin dengan perlakuan asam sitrat tanpa demineralisasi dengan asam sulfat GNAAH: gelatin dengan perlakuan asam asetat dengan demineralisasi asam sulfat GNALH: gelatin dengan perlakuan asam laktat dengan demineralisasi asam sulfat GNASH: gelatin dengan perlakuan asam sitrat dengan demineralisasi asam sulfat
Nilai rendemen gelatin hasil penelitian berkisar antara 10,70% - 21,11%. Nilai
rendemen tertinggi diperoleh dari perlakuan perendaman sampel kulit ayam dengan NaOH
0,15% dilanjutkan dengan perendaman asam sulfat 0,15%, kemudian perendaman dengan
asam sitrat 1%, yaitu sebesar 21,11%. Sedangkan nilai rendemen terendah diperoleh dari
perendaman sampel dengan NaOH 0,15% dilanjutkan dengan perendaman menggunakan
asam sulfat 0,15%, kemudian perendaman dengan asam asetat 1%, yaitu 10,70%.
Hasil uji Duncan menunjukkan bahwa rendemen gelatin dipengaruhi oleh
perendaman dengan asam sulfat dan tanpa asam sulfat menunjukkan hasil yang berbeda
salah satu larutan perendam. Penggunaan variasi pelarut asam, yaitu asam asetat, asam
laktat dan asam sitrat juga berpengaruh nyata (P<0,05) terhadap hasil rendemen gelatin.
Hasil gelatin dari perlakuan perendaman dengan asam sulfat menghasilkan
rendemen yang relatif lebih rendah dibandingkan gelatin tanpa perendaman asam sulfat.
Hal ini dapat disebabkan penggunaan asam sulfat 0,15% sebelum perendaman dengan
masing-masing asam asetat, asam laktat dan asam sitrat tidak hanya berperan dalam proses
demenineralisasi tetapi juga menyebabkan struktur triple helix pada tropokolagen terurai
menjadi single helix (gelatin) yang larut dalam larutan perendam sehingga saat proses
pencucian ekstrak gelatin ikut terbuang bersama larutan perendam asam sulfat yang
menyebabkan menurunnya rendemen ekstrak gelatin.
Dilihat dari jenis asam yang digunakan, rendemen gelatin juga dapat dipengaruhi
oleh kemampuan interaksi ion H+ dari masing-masing larutan asam dengan kolagen.
Semakin banyak ion H+ maka hidrolisis akan semakin efektif sehingga rendemen yang
dihasilkan juga semakin tinggi. Asam asetat dan asam laktat merupakan asam monoprotik,
dimana hanya dapat melepaskan sebuah proton (H+) di dalam larutannya sedangkan asam
sitrat merupakan asam poliprotik karena memiliki tiga atom hidrogen yang dapat terionisasi
sehingga menyebabkan semakin banyaknya pemecahan ikatan hidrogen yang memudahkan
konversi kolagen menjadi gelatin. Dari keenam jenis perlakuan sampel untuk memperoleh
gelatin, perlakuan perendaman dengan NaOH 0,15% dilanjutkan dengan perendaman asam
sulfat 0,15%, kemudian perendaman dengan asam sitrat 1% merupakan proses perendaman
4.4.2 Derajat keasaman (pH) gelatin
Pengukuran pH larutan gelatin merupakan salah satu parameter yang ditetapkan
dalam penentuan mutu standar gelatin. Nilai pH larutan gelatin berpengaruh terhadap
aplikasi gelatin dalam produk. Nilai pH gelatin berhubungan dengan proses yang digunakan
pada produksi gelatin. Gelatin dengan nilai pH netral lebih disukai karena penggunaannya
yang luas, sehingga proses penetralan memiliki peranan penting untuk menetralkan
sisa-sisa asam maupun basa setelah dilakukan perendaman (Hinterwaldner, 1977). Hasil
pengukuran gelatin dalam penelitian ini terdapat dalam Tabel 4.3.
Tabel 4.3. Pengaruh Perlakuan Terhadap Nilai pH Gelatin Kulit Ayam
Perlakuan pH ± Standar Deviasi
GNAA 5,59 ± 0,00 a
GNAL 4,16 ± 0,00 b
GNAS 4,83 ± 0,00 c
GNAAH 5,12 ± 0,00 d
GNALH 5,48 ± 0,00 e
GNASH 3,79 ± 0,00 f
Keterangan: Data yang diikuti huruf berbeda pada kolom menunjukkan perbedaan nyata menurut uji Duncan pada taraf ketelitian 5%
Berdasarkan hasil pengukuran pH gelatin didapatkan bahwa kisaran nilai pH gelatin
hasil ekstraksi dari kulit ayam pada penelitian ini adalah 3,79 - 5,59. Hasil uji lanjut
Duncan menunjukkan bahwa perbedaan perlakuan perendaman sampel terhadap nilai pH
netral (pH 7) dimiliki oleh perlakuan serbuk kulit ayam dengan perendaman menggunakan
larutan NaOH 0,15% dilanjutkan dengan perendaman dengan larutan asam asetat 1% yaitu
sebesar 5,59 dan nilai pH terendah dimiliki oleh perlakuan sampel kulit ayam dengan
perendaman NaOH 0,15% dilanjutkan dengan perendaman asam sulfat 0,15% dan asam
sitrat 1%, yaitu sebesar 3,79.
Dari nilai pH yang dihasilkan, perlakuan sampel dengan perendaman NaOH
dilanjutkan dengan perendaman asam asetat tanpa perendaman asam sulfat merupakan
perlakuan terbaik untuk menghasilkan gelatin dari kulit ayam, karena paling mendekati
kondisi pH netral, yaitu 5,59. Nilai pH gelatin tersebut juga memenuhi standar gelatin
pangan dan farmasi yang dikeluarkan oleh Norland (2003), yaitu 5,5–7,0.
4.4.3 Viskositas gelatin
Pengukuran viskositas larutan gelatin sangat penting artinya untuk menentukan
mutu dan pengunaan gelatin tersebut. Pengujian viskositas dilakukan untuk mengetahui
tingkat kekentalan gelatin sebagai larutan pada konsentrasi dan suhu tertentu. Hasil
pengukuran viskositas gelatin kulit ayam dengan perbedaan perlakuan terdapat pada Tabel
4.4.
Tabel 4.4. Pengaruh Perlakuan Terhadap Nilai Viskositas Gelatin Kulit Ayam
Perlakuan Viskositas (cP) ± Standar Deviasi
GNAA 1,07 ± 0,09 a
GNAL 0,51 ± 0,01 b
GNAAH 0,82 ± 0,04 c
GNALH 0,10 ± 0,01 d
GNASH 0,30 ± 0,02 e
Keterangan: Data yang diikuti huruf berbeda pada kolom menunjukkan perbedaan nyata menurut uji Duncan pada taraf ketelitian 5%
Berdasarkan uji lanjut Duncan, nilai viskositas gelatin kulit ayam berbeda secara
signifikan (P<0,05). Perbedaan nilai viskositas gelatin dipengaruhi oleh perbedaan
perlakuan terhadap sampel. Kisaran nilai viskositas gelatin yang dihasilkan dari penelitian
ini adalah 0,10 – 1,07 cP. Gelatin hasil ekstraksi dari perlakuan perendaman NaOH 0,15%
dilanjutkan dengan asam asetat 1% tanpa perendaman asam sulfat 0,15% memiliki
viskositas paling tinggi, yaitu 1,07 cP, sedangkan nilai viskositas yang paling rendah
dihasilkan dari gelatin dengan perlakuan perendaman NaOH 0,15% dilanjutkan dengan
perendaman asam sulfat 0,15% dan asam laktat 1%, yaitu 0,10 cP.
Nilai viskositas atau kekentalan larutan gelatin sangat erat kaitannya dengan kadar
air gelatin kering. Semakin rendah kadar air gelatin kering maka kemampuannya untuk
mengikat air (untuk membentuk gel) akan semakin tinggi. Semakin banyak jumlah air yang
terikat oleh gelatin maka gel akan menjadi semakin kental, yang secara langsung
berpengaruh pada semakin tingginya nilai viskositas yang diukur (Kurniadi, 2009).
4.4.4 Analisis kandungan proksimat
Kandungan proksimat produk gelatin hasil perlakuan dengan variasi asam dapat
Tabel 4.5. Kandungan Proksimat Produk Gelatin Hasil Perlakuan
Kode Sampel Kadar air Kadar Abu
Kadar Protein Kadar Lemak
GNAA 12,95 1,45 91,82 1,59
GNAL 15,61 1,91 77,48 1,83
GNAS 13,23 1,63 86,09 1,57
GNAAH 11,53 1,02 80,59 1,85
GNALH 11,84 1,82 78,12 1,63
GNASH 11,50 1,12 78,53 1,33
Kadar air suatu bahan sangat berpengaruh terhadap mutu dan kualitasnya.
Kandungan air dalam bahan menentukan kesegaran, penampakan, tekstur, cita rasa, dan
masa simpan bahan (Winarno, 2002). Peranan air dalam bahan pangan merupakan salah
satu faktor yang mempengaruhi aktivitas metabolisme seperti aktivitas enzim, aktivitas
mikroba, dan aktivitas kimiawi, yaitu terjadinya ketengikan dan reaksi-reaksi non
enzimatis, sehingga menimbulkan perubahan sifat-sifat organoleptik (warna, aroma, rasa)
dan nilai gizinya (de Man, 1997).
Berdasarkan hasil pengukuran kadar air keenam produk gelatin kulit ayam hasil
perlakuan berkisar antara 11,50%-15,60%. Kadar air produk gelatin kulit ayam pada
penelitian ini masih memenuhi standar SNI (1995) No. 3735, yaitu maksimum 16%
sehingga dapat digunakan untuk bahan pangan.
Nilai kadar abu suatu bahan menunjukkan kuantitas mineral yang terkandung dalam
zat organik. Zat anorganik tersebut diantaranya adalah kalsium, kalium, natrium, besi,
magnesium dan mangan (Desrosier, 1988).
Hasil pengukuran terhadap kadar abu keenam produk gelatin hasil perlakuan
berkisar antara 1,02%-1,91%. Berdasarkan Standar Nasional Indonesia (1995), kadar abu
gelatin kulit ayam yang diperoleh dalam penelitian ini memenuhi standar mutu yang
disyaratkan, yaitu maksimum 3,25% dan Norland Product (2003), yaitu maksimum 2,0%,
sehingga gelatin kulit ayam yang diperoleh dapat diaplikasikan kedalam produk pangan.
Gelatin merupakan salah satu jenis protein konversi yang dihasilkan melalui proses
hidrolisis kolagen yang pada dasarnya memiliki kadar protein yang tinggi dan termasuk
protein sederhana dalam kelompok skleroprotein (deMan, 1989). Hasil uji kadar protein
untuk keenam produk gelatin kulit ayam pada penelitian ini berkisar antara
77,48%-91,82%. Berdasarkan hasil pengukuran kadar protein tertinggi diperoleh pada gelatin kulit
hasil perlakuan dengan asam asetat baik dengan proses demineralisasi maupun tanpa
demineralisasi dan terendah diperoleh dengan perlakuan asam laktat yang mana kadar
proteinnya lebih rendah dari protein standar.
Kadar lemak merupakan salah satu parameter yang mempengaruhi perubahan mutu
suatu produk. Gelatin dengan kualitas baik diharapkan tidak mengandung lemak.
Rendahnya kadar lemak gelatin memungkinkan serbuk gelatin dapat disimpan dalam waktu
relatif lama (de Man, 1997).
Hasil penentuan kadar lemak keenam produk gelatin kulit ayam berkisar antara
1,33-1,85%. Nilai kadar lemak pada produk gelatin kulit ayam hasil perlakuan tergolong
gelatin kulit ayam menandakan ekstraksi lemak pada sampel kulit ayam dengan metode
soxhletasi menggunakan pelarut n-heksana sebelum proses perendaman mampu
mengekstrak lemak dengan baik.
4.4.5 Kekuatan gel gelatin
Salah satu sifat fisik yang penting pada gelatin adalah kemampuan untuk
membentuk gel. Kemampuan inilah yang menyebabkan gelatin sangat luas penggunaannya
dalam berbagai bidang industri, sehingga kekuatan gel menjadi pertimbangan dalam
menentukan kelayakan penggunaan gelatin. Kekuatan gel gelatin diukur sebagai besarnya
kekuatan yang diperlukan oleh probe untuk menekan gel sampai kedalaman 4 mm sampai
gel pecah. Satuan untuk menunjukkan kekuatan suatu gel yang dihasilkan dari suatu
konsentrasi tertentu disebut gram bloom (Lachman, 1994). Hasil pengukuran kekuatan gel
gelatin hasil ekstraksi dari kulit ayam terdapat pada Tabel 4.6.
Tabel 4.6. Pengaruh Perlakuan Terhadap Nilai Kekuatan Gel Gelatin Kulit Ayam
Perlakuan Kekuatan Gel (gram bloom) ± Standar Deviasi
GNAA 107,20 ± 1,22 b
GNAL 71,53 ± 1,64 a
GNAS 66,27 ± 0,69 c
GNAAH 216,63 ± 0,11 d
GNALH 32,73 ± 0,14 e
GNASH 109,01 ± 1,18 f
Kekuatan gel yang dihasilkan pada penelitian pembuatan gelatin dari kulit ayam
berkisar antara 32,73 – 216,63 g bloom. Uji lanjut Duncan menunjukkan bahwa perbedaan
perlakuan berpengaruh nyata (P<0,05) terhadap nilai kekuatan gel gelatin kulit ayam.
Kekuatan gel tertinggi dimiliki oleh perlakuan kulit ayam dengan perendaman NaOH
0,15% dilanjutkan dengan perendaman asam sulfat 0,15%, kemudian asam asetat 1%, yaitu
sebesar 216,63 g bloom, sedangkan nilai kekuatan gel terendah dimiliki oleh perlakuan
kulit ayam dengan perendaman NaOH 0,15% dilanjutkan dengan asam sulfat 0,15%,
kemudian asam laktat 1%, yaitu 32,73 g bloom.
Kekutan gel gelatin tergantung dari panjang rantai asam aminonya. Jika proses
hidrolisis kolagen berada pada fase yang tepat, yakni pada rantai polipeptida dimana terjadi
pemutusan ikatan hidrogen, ikatan kovalen silang serta sebagian ikatan peptida, maka akan
dihasilkan struktur gelatin dengan rantai peptida yang panjang sehingga kekuatan gel yang
dihasilkan juga tinggi (Ward dan Courts, 1977).
Gelatin dengan perlakuan terbaik dilihat dari nilai kekuatan gel yang tinggi
diperoleh dari perlakuan dengan perendaman NaOH 0,15% dilanjutkan dengan perendaman
menggunakan asam sulfat 0,15% dan dilanjutkan dengan asam asetat 1%, yaitu 216,63 g
bloom. Nilai kekuatan gel tersebut termasuk dalam gelatin pangan grade B (Norland
Product, 2003), sehingga dapat diaplikasikan dalam produk pangan seperti beer, juice, meat
products dan dairy products (GMIA, 2012). Dalam spesifikasi gelatin farmasi, gelatin
dengan kekuatan gel 216,63 g bloom termasuk ke dalam gelatin farmasi kelas 2 (Norland
4.4.6 Analisis komposisi asam amino
Senyawa gelatin merupakan suatu polimer linier asam-asam amino. Pada umumnya
rantai polimer tersebut merupakan perulangan dari asam amino glisin-prolin-prolin atau
glisin-prolin-hidroksiprolin . Analisis asam amino ini bertujuan untuk mengetahui jenis dan
komposisi asam amino gelatin kulit ayam hasil perlakuan dengan perendaman
menggunakan asam yang berbeda. Hasil analisis komposisi asam amino gelatin kulit ayam
dengan variasi jenis asam yang digunakan pada proses perendaman disarikan pada Tabel
4.7. Secara umum komposisi asam amino gelatin kulit ayam jauh lebih rendah dari
komposisi asam amino gelatin sapi (Eastoe and Leach) namun tidak jauh berbeda dari
komposisi asam amino tulang ayam (Junianto, 2006). Seperti tertera pada Tabel 4.7, secara
deskriptif komposisi asam amino keenam jenis produk gelatin tidak jauh berbeda dengan
kandungan asam amino glisin tertinggi dibandingkan dengan asam amino lainnya yaitu
berkisar antara 15,40%-20,54%.
Tabel 4.7 Komposisi Asam Amino Produk Gelatin Kulit Ayam Hasil perlakuan
Asam Amino (g/100g)
GNAAH GNALH GNASH GNAL GNAA GNAS
ASP 3,83 3,94 3,40 3,89 3,64 3,60
SER 2,08 2,08 1,77 2,25 2,04 2,02
GLU 7,41 7,44 6,33 7,53 7,08 7,01
GLY 18,31 17,88 15,40 20,54 18,08 17,77
HIS * * * * * *
THR 1,65 1,66 1,37 1,86 1,61 1,58
ALA 7,07 6,82 5,84 7,51 7,01 6,79
Prolin 8,85 9,18 7,46 9,87 8,93 8,78
CYS 0,02 0,02 0,02 0,03 0,02 0,02
TYR 0,51 0,54 0,48 0,61 0,51 0,51
VAL 1,67 1,63 1,39 1,84 1,66 1,64
MET 0,77 0,80 0,64 0,92 0,79 0,79
LYS 2,44 2,42 2,07 2,35 2,37 2,29
ILE 1,12 1,11 0,95 1,23 1,12 1,10
LEU 2,36 2,32 1,98 2,61 2,36 2,33
PHE 1,97 1,94 1,67 2,36 1,93 1,92
Hal ini karena gelatin merupakan hasil hidrolisis kolagen yang penyusun utamanya adalah
asam amino glisin. Kandungan glisin tertinggi 20,54% diperoleh melalui perendaman asam
laktat tanpa proses demineralisasi menggunakan asam sulfat dan kandungan glisin terendah
15,40 % diperoleh dari proses perendaman menggunakan asam sitrat setelah proses
demineralisasi menggunakan asam sulfat. Kandungan glisin pada gelatin pada penelitian
ini, tidak berbeda jauh dengan kandungan glisin gelatin tulang ayam yang dilaporkan oleh
Junianto, 2006 yaitu 15,02%. Kandungan glisin yang tinggi pada gelatin diduga dapat
menyebabkan gelatin mudah larut dalam air dan mampu membentuk emulsi. Hal ini
disebabkan karena glisisn merupakan asam amino yang bersifat hidrofilik. (Lehninger,
1982). Asam glutamat dan alanin juga terdapat dalam jumlah yang cukup tinggi yaitu
tidak terdeteksi adanya asam amino histidin. Hal ini mungkin disebabkan karena
kandungan histidin pada kulit ayam sangat kecil sehingga tidak terdeteksi atau gelatin kulit
ayam memang tidak mengandung asam amino histidin. Kandungan histidin pada gelatin
tulang ayam dilaporkan 0,25% (Junianto, 2006.)
Asam amino prolin juga merupakan komponen yang cukup tinggi persentasenya
pada keenam gelatin hasil perlakuan yaitu berkisar antara 7,46%-9,87% tetapi jauh lebih
rendah dari pada kandungan prolin gelatin sapi yaitu 16,14%. Kandungan prolin tertinggi
9,87 % diperoleh pada gelatin yang diproses melalui perendaman asam laktat tanpa proses
demineralisasi menggunakan asam sulfat, dan kadar prolin terendah 7,46% ditunjukkan
gelatin hasil perendaman dengan asam sitrat setelah proses demineralisasi dengan sam
sulfat.
Asam amino essensial triptopan juga tidak terdeteksi pada gelatin hasil perlakuan
karena pada kolagen maupun gelatin secara umum tidak mengandung asam amino
triptopan. Hal inilah yang menyebabkan gelatin dikatakan sebagai protein yang kandungan
gizinya tidak lengkap. Triptopan merupakan salah satu asam amino essensial yang
dibutuhkan oleh tubuh (Glicksman, 1969). Oleh karena itu penggunaannya sebagai bahan
baku industri pangan perlu dikombinasikan dengan bahan pangan yang banyak
mengandung triptopan.
Pada penelitian ini, komposisi asam amino kekeenam produk gelatin tidak jauh
berbeda tetapi kekuatan gelnya berbeda secara sigifikan (Tabel 4.6) sehingga dapat
dikatakan komposisi asam amino gelatin kulit ayam tidak berpengaruh terhadap kekuatan
tidak hanya bergantung pada komposisi asam aminonya tetapi juga ditentukan oleh
kandungan relative dari komponen rantai protein - atau – dan aggregates dengan berat
molekul yang tinggi serta adanya kandungan fragmen protein dengan berat molekul yang
rendah. Faktor lain yang juga berpengaruh terhadap sifat fisik dan mekanik gelatin adalah
sumber atau asal dari bahan awal yang digunakan dan proses pengawetan dari bahan
mentah yang digunakan atau kesegaran dari bahan mentah yang digunakan.
4.4.7 Analisis berat molekul dengan elktroforesis menggunakan SDS_PAGE
Pada penelitian ini, fragmen pita protein produk gelatin kulit ayam broiler dianalisa
menggunakan teknik elektroforesis SDS gel poliakrilamida (SDS PAGE). Hasil yang
didapatkan dari elektroforesis yaitu berupa pita – pita protein yang terpisahkan berdasarkan
perbedaan berat molekulnya yang setara dengan panjang rantai protein. Migrasi pita protein
dalam SDS PAGE berbanding terbalik dengan berat molekulnya (panjang pita), maka
semakin besar berat molekul produk gelatin semakin lambat migrasinya sehingga posisinya
pada elektroforegram semakin di atas.
Pita protein produk gelatin kulit ayam broiler dibandingkan dengan pola protein dari
Gambar 4.7 Elektroforegram produk gelatin hasil perlakuan Keterangan:
M: Marker Protein (SDS-PAGE molecular Weight Standars Broad Range (BIORAD) A: GNAS
B: GNAA
C: GNALH
D: GNAAH
E: GNASH
F: GNAL
Berdasarkan elektroforegram hasil SDS PAGE tersebut diketahui bahwa pada
marker protein terdapat tujuh pita protein dengan berat molekul 97 kDa, 85kDa, 66kDa,
45kDa, 31kDa, 25kDa, dan 21kDa. Untuk sampel A(GASH), pita protein tidak tampak
jelas terpisah dikarenakan pita – pita yang terbentuk terlalu tipis. Pada sampel B (GNAA)
pita protein yang terbentuk pada 5 pita dengan berat molekul 97 kDa, 85 kDa, 66 kDa, 45
protein. Hal ini kemungkinan disebabkan fragmen protein yang dihasilkan memiliki berat
molekul yang rendah (berat molekul lebih rendah daripada berat molekul protein marker
yang terpendek), sehingga tidak terdeteksi dengan metode SDS PAGE. Fragmen protein
dengan berat molekul rendah tersebut kemungkinan adanya proses degradasi yang terlalu
kuat sehingga ikatan peptida pada kolagen terputus menjadi lebih pendek. Untuk Sampel D
(GNAAH) menunjukkan adanya pita protein yang terbentuk dengan berat molekul 97 kDa,
85 kDa, 66 kDa, 45 kDa, dan 35 kDa, 25kDA sama dengan yang ditunjukkan oleh sampel
B (GNAA) namun dengan pita yang lebih tebal. Untuk sampel E (GNASH) hampir sama
dengan sampel D hanya 5 pita protein yang terbentuk sangat tipis dan tidak terlalu jelas.
Demikian juga dengan sampel F (GNAL) pita protein ang terbentuk sangat tipis sehingga
tidak terlalu jelas kenampakannya.
Berdasarkan hasil elektroforegam terlihat bahwa produk gelatin kulit ayam broiler
yang memiliki berat molekul yang besar yaitu sampel D (GNAAH), hal ini ditunjukkan
dengan pita protein yang terbentuk lebih tebal bila dibandingkan dengan pita protein
produk gelatin GNASH, dan GNAL. Pada penelitian ini, tidak ditemukan pita protein
dengan berat molekul yang tinggi (200300Kda) yang merupakan komponen protein
-sheet dan -sheet, hanya pita protein dengan berat molekul 95 kDA dan 90kDa yang
menunjukkan keberadaan rantai α1 dan αβ protein dan beberapa agregates protein dengan
berat molekul yang rendah pada 66, 45, 35, dan 21 kDA. Dengan demikian dapat
dikatakan bahwa perbedaan variasi jenis asam yang digunakan berpengaruh terhadap pita
protein dan berat molekul gelatin yang dihasilkan. Pada penelitian ini proses isolasi gelatin
dengan berat molekul tertinggi dan kekuatan gel tertinggi meskipun rendemennya relatif
rendah.
4.4.8 Identifikasi Gugus FungdiProduk Gelatin dengan FTIR
Pada penelitian ini, identifikasi gugus fungsi hanya ditampilkan dan didiskusikan
untuk produk gelatin kulit ayam broiler melalui proses demineralisasi asam sulfat dengan
variasi asam dan dilakukan dengan menggunakan Spektroskopi FTIR. Gelatin seperti
umumnya protein memilki struktur yang terdiri dari karbon, hidrogen, gugus hiroksil (OH),
gugus karbonil (C=O), dan gugus amina (NH). Gelatin memiliki serapan khas, yaitu daerah
amida A pada v 3600-2300 cm-1, amida I pada v 1636-1661 cm-1, amida II pada v
1560-1335 cm-1 dan amida III pada v 1300-1200 cm-1 (Muyongga, 2004). Interpretasi spektra IR
ditunjukkan pada Tabel 4.7 dan spektra Inframerah ditampilkan pada Gambar 4.8-4.10.
Gambar 4.9. Spektra Inframerah gelatin yang diekstraksi dengan asam laktat
Dari hasil analisis spektra FT-IR dapat diketahui gugus fungsi yang terdapat pada
ketiga produk gelatin (GNAAH, GNALH, GNASH) adalah gugus N-H, O-H, C=O, dan
C-N yang merupakan gugus gugus fungsi utama pada gelatin.
BAB V SIMPULAN DAN SARAN 5.1 Simpulan
Dari penelitian yang telah dilakukan dapat disimpulkan:
1. Perbedaan jenis asam yang digunakan pada proses perendaman berpengaruh
terhadap rendemen, kekuatan gel, komposisi asam amino, dan berat molekul produk
gelatin yang dihasilkan. Perlakuan dengan asam asetat memberikan gelatin dengan
kekuatan gel tertinggi namun rendemen terendah. Perlakuan dengan asam laktat
memberikan persentase komposisi asam amino yang relatif lebih tinggi dari
penggunaan asam asetat maupun sitrat, namun memberikan kekuatan gel dan berat
molekul terendah, sedangkan perlakuan dengan asam sitrat memberikan rendemen
tertinggi, kekuatan gel dan berat molekul yang moderat.
2. Komposisi asam amino produk gelatin hasil perendaman dengan asam asetat, sitrat
dan laktat secara umum sama yaitu glisin sebagai komponen utama dengan
persentase 15,40%-20,54%, Prolin 1,46%-9,87%, glutamate 6,33%-7,53%, dan
alanin 5,48%-7,51%. Komposisi asam amino produk gelatin tidak berpengaruh
terhadap sifat mekanik kekuatan gelnya.
3. Pola pita protein produk gelatin dipengaruhi oleh jenis asam yang digunakan pada
proses perendaman. Perendaman dengan asam asetat memberikan pita protein yang