BAB II
TINAJAUN PUSTAKA
2.1 Uraian umum
2.1.1 Tanaman Sirsak (Annona muricata L.)
Indonesia terletak di daerah tropis merupakan salah satu negara penghasil buah-buahan. Bermacam buah-buahan dengan berbagai varietas, bentuk, rasa, bau dan warna yang khas telah dikenal sejak lama. Sirsak merupakan tanaman dengan tinggi pohon sekitar 5-6 m (Badrie dan Schauss, 2010).
2.1.2 Klasifikasi Tanaman Sirsak
Menurut Warisno dan Dahana (2012), klasifikasi tanaman sirsak adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta Kelas : Dicotyledoneae Ordo : Magnoliales Famili : Annonaceae Genus : Annona
Spesies : Annona muricata L. 2.1.3 Marfologi Tanaman Sirsak
cabang atau ranting juga sama dengan batangnya, namun saat masih muda berwarna hijau. Akar tanaman sirsak ada 2 jenis, yaitu akar tunggang (vertikal) dan akar serabut (horizontal), akar tunggang berfungsi untuk memperkuat berdirinya tanaman dan tumbuh kearah bawah sedangkan akar serabut memiliki fungsi untuk mencari unsur hara dan air, panjang akar tanaman sirsak dapat mencapai 1-2 m. Bunga sirsak berwarna kuning atau kehijauan, terdiri atas kelopak-kelopak bunga yang tersusun seperti membentuk kerucut, bunga sirsak dapat tumbuh pada cabang, ranting, bahkan batang. Buah sirsak memiliki bentuk dasar kerucut, tetapi bentuknya tidak beraturan, kulit buah berwarna hijau tua pada saat muda, namun berwarna kuning setelah masak, buahnya memiliki duri-duri lunak berwarna hijau yang menyelimuti seluruh buah, daging buah berwarna putih, beraroma khas, dan rasanya manis asam pada saat sudah masak. Biji sirsak berwarna hitam, lonjong, dan keras. Ujungnya memiliki bagian berwarna putih, yang merupakan titik tumbuh, biji biasanya akan tumbuh setelah disemaikan selama 2-3 minggu (Warisno dan Dahana, 2012).
2.1.4 Jenis-Jenis Tanaman Sirsak
buah nona, berbentuk bulat, daging buah berwarna kuning, bijinya banyak, rasanya manis, dan duri kulitnya lebih jarang (Zuhud, 2011).
2.1.5 Kandungan Kimia Tanaman Sirsak
Semua bagian dari tamanan sirsak mengandung senyawa aktif, buah sirsak mengandung protein, kalsium, fosfor, besi, vitamin A dan vitamin C. Batang, biji, akar dan daunnya kaya akan tanin, alkaloid, steroid/terpenoid, flavonoid, kumarin, fitosterol dan kalsium oksalat(Hariana, 2011).
2.1.6 Manfaat Tanaman Sirsak
setelah direbus, air rebusannya digunakan untuk pengobatan penyakit asma, batuk, obat penenang dan hipertensi (Warisno dan Dahana, 2012).
2.2 Mineral Fosfor
Mineral merupakan unsur yang dibutuhkan oleh tubuh manusia yang mempunyai peranan penting dalam pemeliharaan fungsi tubuh, baik pada tingkat sel, jaringan, organ, maupun fungsi tubuh secara keseluruhan. Unsur ini digolongkan kedalam mineral mikro dan makro. Mineral makro adalah mineral yang dibutuhkan dalam jumlah 100 mg sehari, misalnya natrium, klorida, kalsium, magnesium, sulfur, dan fosfor. Mineral mikro dibutuhkan kurang dari 100 mg sehari, misalnya besi, iodium, mangan dan tembaga (Almatsier, 2004).
Fosfor merupakan mineral kedua yang terbanyak didalam tubuh setelah kalsium, fosfor dan kalsium terdapat dalam jaringan tulang dan gigi, fosfor juga terdapat dalam semua sel hidup dan diperlukan untuk pelepasan energi. Fosfor mempunyai peranan dalam metabolisme karbohidrat, lemak, dan protein. Fosfor merupakan komponen esensial bagi banyak sel dan merupakan alat transport asam lemak. Fosfor berperan pula dalam mempertahankan keseimbangan tubuh. Pada umumnya bahan makanan yang mengandung banyak kalsium merupakan juga sumber fosfor, seperti susu, keju, daging, ikan, telur, dan sekitar 70% dari fosfor yang berada dalam makanan dapat diserap oleh tubuh. Penyerapan akan lebih baik bila fosfor dan kalsium dimakan dalam jumlah yang sama. Angka kecukupan fosfor rata-rata sehari adalah 400-500 mg (Almatsier, 2004).
fosfor tidak bisa dipenuhi oleh ASI (air susu ibu). Kelebihan fosfor karena makanan jarang terjadi. Bila kadar fosfor darah terlalu tinggi, ion fosfat akan mengikat kalsium sehingga dapat menimbulkan kejang (Budianto, 2009).
2.3 Metode Destruksi
2.3.1 Metode Destruksi Basah
Destruksi basah adalah perombakan sampel dengan asam-asam kuat baik tunggal maupun campuran, kemudian dioksidasi dengan menggunakan zat oksidator. Pelarut-pelarut yang dapat digunakan untuk destruksi basah antara lain asam nitrat, asam sulfat, asam perklorat, dan asam klorida. Semua pelarut tersebut dapat digunakan baik tunggal maupun campuran. Kesempurnaan destruksi ditandai dengan diperolehnya larutan jernih pada larutan destruksi, yang menunjukkan bahwa semua konstituen yang ada telah larut sempurna atau perombakan senyawa-senyawa organik telah berjalan dengan baik. Senyawa-senyawa garam yang terbentuk setelah didestruksi merupakan Senyawa-senyawa garam yang stabil dan disimpan selama beberapa hari (Raimon, 1993).
2.3.2 Metode Destruksi Kering
dilarutkan dengan pelarut asam yang encer baik tunggal maupun campuran, kemudian didekstruksi, hasil destruksi dianalisis dengan metode Spektrofotometeri Serapan Atom (Raimon, 1993).
Menurut Raimon (1993) ada beberapa faktor yang harus diperhatikan dalam hal menggunakan metode destruksi terhadap sampel, baik dengan destruksi basah atau dekstruksi kering, antara lain:
a. Sifat matriks dan konstituen yang terkandung didalamnya. b. Jenis logam yang akan dianalisis.
c. Metode yang akan digunakan untuk penentuan kadarnya.
2.4 Spektrofotometri UV-Visible
Spektrofotometri adalah pengukuran absorbansi energi cahaya oleh suatu sistem kimia pada panjang gelombang tertentu, biasanya digunakan untuk molekul dan ion organik atau kompleks dalam larutan, spektrum sinar ultraviolet dan sinar tampak sangat berguna untuk pengukuran secara kuantitatif. Sinar ultraviolet mempunyai panjang gelombang antara 200-400 nm, sementara sinar tampak mempunyai panjang gelombang 400-800 nm (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007), ada beberapa hal yang harus diperhatikan dalam analisis dengan spektrofotometri ultraviolet dan sinar tampak terutama untuk senyawa yang tidak berwarna dan yang berwarna yang akan dianalisis yaitu:
a. Pembentukan molekul yang dapat menyerap sinar UV-Visible
b. Waktu kerja (operating time)
Tujuannya adalah untuk mengetahui waktu pengukuran yang stabil. c. Pemilihan panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang yang mempunyai absorbansi maksimal.
d. Pembuatan kurva baku
Dilakukan dengan membuat larutan baku dalam berbagai konsentrasi kemudian absorbansi tiap konsentrasi diukur.
e. Pembacaan absorbansi sampel
Absorbansi yang terbaca pada spektrofotometer hendaknya terletak antara 0,2 sampai 0,6 (Gandjar dan Rohman, 2007).
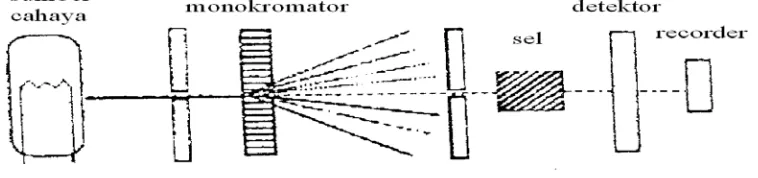
Gambar Instrumen Spektrofotometer UV-Visible
(Gandjar dan Rohman, 2007). Menurut Gandjar dan Rohman (2007), bagian-bagian instrumentasi spektrofotometer UV-Visible sebagai berikut:
a. Sumber Cahaya
b. Monokromator
Monokromator berfungsi mengubah cahaya polikromatis menjadi cahaya yang monokromatis. Alatnya dapat berupa berupa prisma atau kisi difraksi. c. Sel
Sel yang digunakan untuk daerah tampak terbuat dari kaca sedang untuk daerah ultraviolet digunakan sel kuarsa atau kaca silika. Sel tampak dan ultraviolet yang khas mempunyai panjang lintasan 1 cm, namun tersedia juga sel dengan ketebalan kurang dari 1 ml, sampai 10 cm bahkan lebih.
d. Detektor
Peranan detektor adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang.
e. Rekorder
Recorder digunakan sebagai perekam absorbansi yang dihasilkan dari pengukuran (Gandjar dan Rohman, 2007).
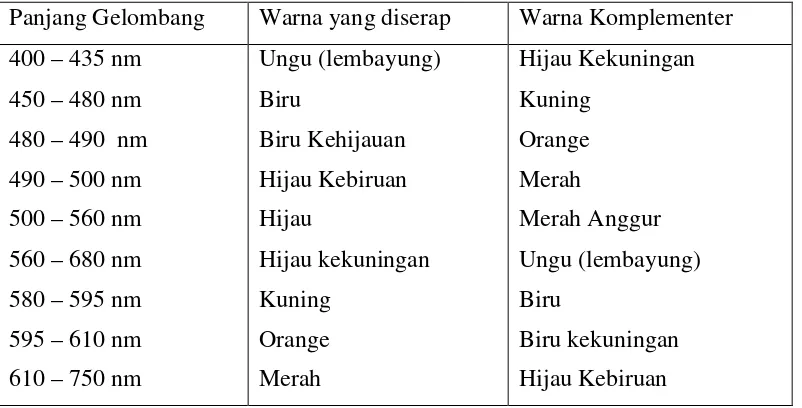
Menurut Gandjar dan Rohman (2007), warna-warna yang dihubungkan dapat dinyatakan dalam tabel dibawah ini:
2.5 Validasi Metode Analisis
Validasi adalah suatu tindakan penilaian terhadap parameter tertentu pada prosedur penetapan yang dipakai untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Suatu metode analisis harus divalidasi untuk melakukan verifikasi bahwa parameter-parameter kerjanya cukup mampu untuk mengatasi masalah analisis dan untuk menjamin bahwa metode analisis akurat, dan spesifik. Validasi metode analisis dilakukan dengan uji laboratorium, dengan demikian dapat ditunjukkan bahwa karakteristik kinerjanya telah memenuhi persyaratan untuk diterapkan dalam analisis senyawa atau sediaan yang diuji (Satiadarma, dkk., 2004).
Beberapa parameter analisis yang harus dipertimbangkan dalam validasi metode analisis adalah sebagai berikut:
a. Akurasi (kecermatan)
Akurasi (kecermatan) adalah ukuran yang menunjukkan derajat kedekatan hasil analisis dengan kadar analit sebenarnya. Akurasi dinyatakan sebagai persen perolehan kembali (recovery) analit yang ditambahkan dan dapat ditentukan melalui dua cara yaitu metode simulasi (spiked placebo recovery) dan metode penambahan bahan baku (standard addition method) (Harmita, 2004).
Metode simulasi (spiked placebo recovery) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit bahan murni kedalam suatu bahan pembawa sediaan farmasi (plasebo), lalu campuran tersebut dianalisis dan hasilnya dibandingkan dengan kadar analit yang ditambahkan (kadar sebenarnya) (Harmita, 2004).
Metode penambahan bahan baku (standard addition method) merupakan metode yang dilakukan dengan cara menambahkan sejumlah analit dengan konsentrasi tertentu pada sampel yang diperiksa, lalu dianalisis dengan metode yang akan divalidasi. Hasilnya dibandingkan dengan sampel yang dianalisis tanpa penambahan sejumlah analit. Persen perolehan kembali di tentukan dengan menentukan berapa persen analit yang ditambahkan ke dalam sampel (Harmita, 2004).
b. Presisi (keseksamaan)
Presisi (keseksamaan) merupakan ukuran yang menunjukan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Presisi dinyatakan sebagai deviasi standar relatif dan simpangan baku relatif (Nilai RSD dinyatakan memenuhi persyaratan jika tidak lebih dari 16%) (Satiadarma, dkk., 2004).
b. Batas deteksi dan batas kuantitas
Batas deteksi merupakkan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan, sedangkan batas kuantitasi merupakan kuantitasi terkecil analit dalam sampel yang masih memenuhi kriteria cermat dan seksama (Harmita, 2004).
d. Liniearitas
e. Pengujian beda nilai rata-rata
Untuk mengetahui perbedaan nilai rata-rata antar sampel dilakukan analisa statistik menggunakan uji ANOVA dengan Statistical Product Solution dengan taraf kepercayaan 95% dengan uji Tukey. Uji ini digunakan untuk menguji apakah 2 populasi atau lebih memiliki nilai rata-rata (mean) yang dianggap sama atau tidak. Analisa sesudah ANOVA atau pasca ANOVA (post hoc) dilakukan jika hipotesis nol (H0) ditolak. Namun jika hipotesis nol (H0) diterima, maka analisa