SERTA ANALISIS FISIKA-KIMIA
Oleh :
Heidi Wiratmaja
C34101048
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
SERTA ANALISIS FISIKA-KIMIA
SKRIPSI
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor
Oleh :
Heidi Wiratmaja
C34101048
PROGRAM STUDI TEKNOLOGI HASIL PERIKANAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
HEIDI WIRATMAJA. Perbaikan Nilai Tambah Limbah Tulang Ikan Tuna (Thunnus sp) Menjadi Gelatin Serta Analisis Fisika-Kimia. Dibimbing oleh MITA WAHYUNI dan MALA NURILMALA.
Ikan tuna pada umumnya dimanfaatkan untuk produksi pengalengan dan pembekuan, baik utuh maupun dalam bentuk loin beku. Produk ikan tuna beku sebagian besar hanya memanfaatkan daging ikannya saja, sedangkan sisa-sisa pemanfaatan lain berupa kepala, sirip dan tulang belum dimanfaatkan secara optimal. Saat ini kepala, sirip dan tulang hanya dibuat tepung ikan dengan nilai ekonomi yang masih rendah.
Tulang ikan tuna dapat dijadikan gelatin, karena di dalam tulang ikan tuna mengandung protein kolagen. Gelatin merupakan polipeptida yang diperoleh melalui beberapa tahapan degradatif dari protein kolagen. Proses pembuatan tulang ikan tuna menjadi gelatin digunakan HCl dengan konsentrasi 4, 5 dan 6% dan suhu ekstraksi 80, 85 dan 90 oC. Tujuan dari penelitian ini adalah mempelajari pembuatan gelatin dari tulang ikan tuna dengan menggunakan metode asam serta menganalisis sifat fisika kimia gelatin yang dihasilkan.
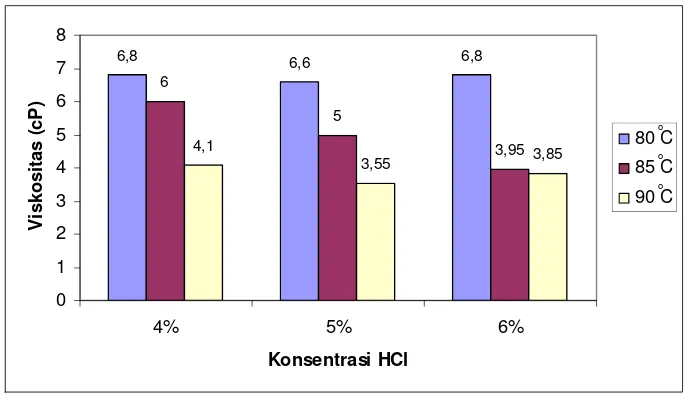
Dari kombinasi perendaman HCl 4% dengan suhu ekstraksi 80, 85 dan 90 oC dihasilkan nilai rendemen berturut-turut sebesar 3,80, 5,37 dan 6,77%, nilai pH sebesar 4,88, 4,78 dan 4,66, nilai viskositas 6,80, 6,00 dan 4,10 cp dan nilai kekuatan gel 290,00, 152,50, 72,50 bloom. Pada perendaman HCl 5% dan suhu ekstraksi 80, 85 dan 90 oC dihasilkan nilai rendemen berturut-turut sebesar 5,33, 5,91 dan 8,31%, nilai pH sebesar 4,88, 4,84 dan 4,45, nilai viskositas 6,60, 5,00 dan 3,55 cp, nilai kekuatan gel sebesar 202,50, 102,5 dan 47,50 bloom. Pada perendaman HCl 6% dengan suhu ekstraksi 80, 85 dan 90 oC dihasilkan nilai rendemen 11,14, 11,40 dan 10,31%, nilai pH sebesar 4,89, 4,47 dan 4,46, nilai viskositas sebesar 6,80, 3,95 dan 3,85 cp, nilai kekuatan gel sebesar 175,00, 82,50 dan 40,00 bloom.
Sifat Fisika-Kimia Nama Mahasiswa : Heidi Wiratmaja Nomor Pokok : C 34101048
Menyetujui,
Pembimbing I Pembimbing II
Dr.Ir. Mita Wahyuni, MS Mala Nurilmala, S.Pi, M.Si NIP. 131 789 337 NIP. 132 315 793
Mengetahui,
Dekan Fakultas Perikanan dan Ilmu Kelautan
Dr. Ir. Kadarwan Soewardi NIP. 130 805 031
Penulis dilahirkan di Bandung pada tanggal 7 Desember
1983merupakan anak kedua dari pasangan Bapak Rubino dan
Ibu Lela Dahlia.
Pendidikan Pertama di SDN Sukajadi I Bandung dan
menyelesaikan pendidikan pada tahun 1995. Pada tahun yang
sama penulis diterima di SLTPN 1 Bandung dan menyelesaikan pendidikan pada
tahun 1998. Penulis melanjutkan pendidikan di SMUN 2 Bandung dan
menyelesaikan pendidikannya pada tahun 2001.
Pada tahun 2001, penulis diterima di Institut Pertanian Bogor melalui jalur
USMI. Semasa kuliah penulis aktif sebagai pengurus Himpunan Mahasiswa
Teknologi Hasil Perikanan (Himasilkan) dan Organisasi Pencinta Alam AMAZON
Fakultas Perikanan dan Ilmu Kelautan. Selain itu penulis juga aktif sebagai asisten
luar biasa mata kuliah Avertebrata Air, Departemen Manajemen Sumberdaya
Perairan.
Penulis dinyatakan lulus di Institut Pertanian Bogor pada tanggal
20 Pebruari 2006, dengan skripsi berjudul Pembuatan dan Analisis Sifat Fisika-Kimia
i
kepada penulis, sehingga dapat menyelesaikan skripsi ini dengan baik. Shalawat dan salam kepada Nabi Muhammad SAW beserta keluarga, sahabat dan umatnya yang setia mengikuti ajarannya hingga akhir zaman.
Skripsi hasil penelitian ini disusun sebagai syarat untuk mendapatkan gelar Sarjana Perikanan dan Ilmu Kelautan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Skripsi ini merupakan studi tentang Pemanfaatan tulang ikan tuna sebagai gelatin.
Dalam kesempatan ini penulis mengucapkan banyak terima kasih kepada : 1. Dr. Ir. Mita Wahyuni, M.S dan Mala Nurilmala S.Pi, M.Si selaku dosen
pembimbing yang telah memberikan kritik dan saran dalam penelitian. 2. Bambang Riyanto, S.Pi, M.Si dan Dra. Pipih Suptijah, MBA. selaku dosen
penguji yang memberikan san dan kritikan dalam penulisan karya ilmiah. 3. Bapak, Ibu, Bram atas semangat, doa dan kasih sayang yang tiada
hentinya.
4. Keluarga Besar Prawiro dan Gandi atas nasehat dan petuah untuk menjalani hidup ini.
5. Dosen, Staf dan Laboran yang senantiasa membantu penulis dalam menyelesaikan karya kecil ini.
6. Reki, Nisa, Dias, Yulita Teman-teman yang selalu menangani segala masalah akademik, tugas dan literatur.
7. Teddy, Timor, Andiarto, Edy, Nuno, Harso, Minto, Abi, dhani, Bandel, Awan.Rekan- rekan yang Anak-anak THP 38,. Terima kasih semuanya 8. Pihak-pihak Lain yang membantu menyelesaikan skripsi ini.
Penulis menyadari dalam penulisan skripsi ini masih jauh dari sempurna. Oleh sebab itu kritik dan saran yang membangun sangat penulis harapkan.
Bogor, Pebruari 2006
ii
2.4Pembuatan Gelatin ... 9
2.5Mutu Gelatin ... 10
2.6Manfaat Gelatin... 11
3. METODOLOGI ... ...14
3.1 Waktu dan Tempat ... 14
3.2 Bahan dan Alat Penelitian ... 14
3.3 Metode Penelitian ... 14
3.3.1 Penelitian tahap pertama ... ..15
3.3.2 Penelitian tahap kedua ... 15
3.4 Analisis ... 17
3.4.1 Rendemen (AOAC,1995) ... 17
3.4.2 Kekuatan gel (Gaspar, 1998) ... 17
3.4.3 Viskositas (British Standard 757, 1975) ... 17
3.4.4 Kadar air (AOAC, 1995) ... 17
3.4.5 Kadar abu (AOAC, 1995) ... 18
3.4.6 Kadar protein (AOAC, 1995) ... 18
3.4.7 Kadar lemak (Apriyantono et.al, 1989) ... 19
3.4.8 Derajat putih (Kett Digital Whiteness Powder) ... 19
iii
3.4.13 Kandungan logam berat (Hg) (Hutagalung, 1997) ... 20
3.4.13 Komposisi asam amino (Nur et.al, 1992) ... 20
3.5 Rancangan Percobaan ... 21
4. HASIL DAN PEMBAHASAN ... ...23
4.1 Penelitian Tahap Pertama... 23
4.1.1 Rendemen gelatin ... 26
4.1.2 pH gelatin ... 27
4.1.3 Viskositas ... 29
4.1.4 Kekuatan gel ... 30
4.2 Penelitian Tahap Kedua ... 33
4.2.1 Analisis Proksimat ... 33
4.2.1.1 Kadar air ... 34
4.2.1.2 Kadar abu ... 35
4.2.1.3 Kadar lemak ... 35
4.2.1.4 Kadar protein ... 36
4.2.2 Sifat Fisika-Kimia ... 37
4.2.2.1 Titik gel ... 37
4.2.2.2 Titik leleh ... 37
4.2.2.3 Titik isoelektrik ... 38
4.2.2.4 Derajat putih ... 39
4.2.2.5 Asam amino ... 39
4.2.2.6 Kandungan logam berat (Hg) ... 41
5. KESIMPULAN DAN SARAN ... ...42
iv
Halaman 1. Sifat gelatin tipe A dan tipe B ... 8 2. Standar mutu gelatin ... 8 3. Persyaratan gelatin berdasarkan FAO ... 9 4. Aplikasi gelatin terhadap produk terhadap produk pangan
v
Halaman
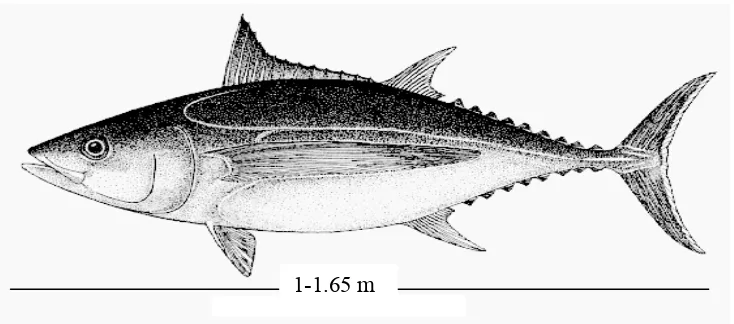
1. Ikan tuna Albacore ... 4
2. Proses pembentukan gel pada gelatin (de Man, 1997) ... 6
3. Struktur kimia gelatin (Poppe, 1992) ... 7
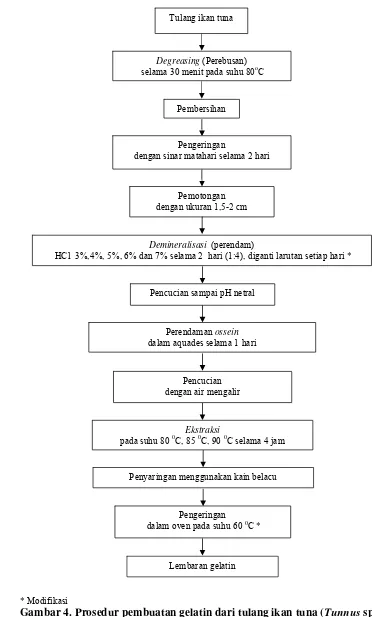
4. Prosedur pembuatan gelatin dari tulang ikan tuna (Thunnus sp) ... 16
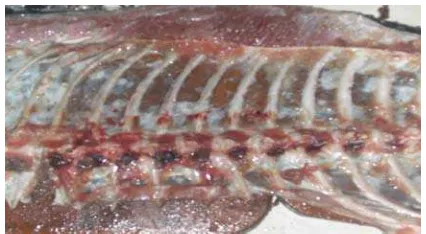
5. Tulang ikan tuna ikan tuna (Thunnus sp) bagian dada ... 23
6. Gambar gelatin dari tulang ikan tuna (Thunnus sp) ... 25
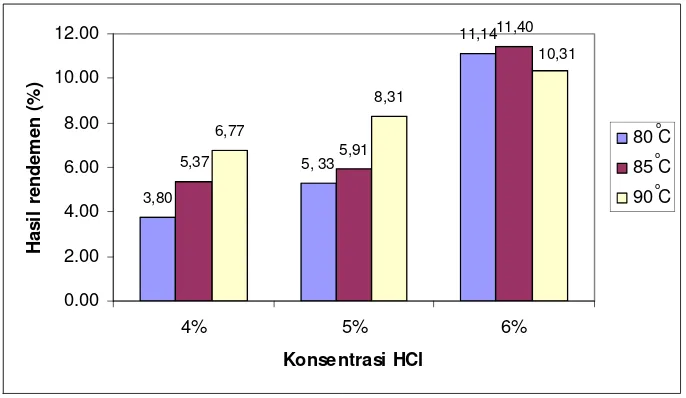
7. Histogram rendemen gelatin tulang ikan tuna (Tunnus sp) ... 26
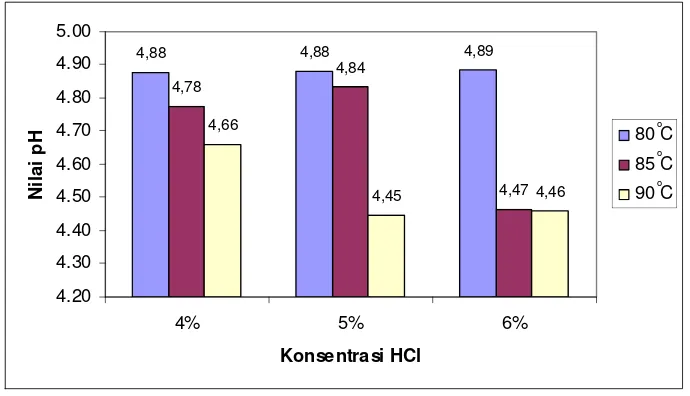
8. Histogram pH gelatin tulang ikan tuna (Thunnus sp) ... 28
9. Histogram viskositas gelatin tulang ikan tuna (Thunnus sp) ... 29
vi
Halaman
1. Grafik kekuatan gel ... 49
2. Analisis ragam faktorial rendemen gelatin ... 50
3. Analisis ragam faktorial nila pH gelatin ... 51
4. Analisis ragam faktorial viskositasgelatin ... 52
5. Analisis ragam faktorial kekuatan gel gelatin ... 53
6. Grafik pengujian asam amino standar dan sampel ... 54
7. Analisis biaya pembuatan gelatin ... 56
1. PENDAHULUAN
1.1 Latar Belakang
Ikan tuna merupakan salah satu ikan ekonomis penting Indonesia. Daerah
penyebaran ikan tuna di Indonesia meliputi Laut Banda, Laut Maluku,
Laut Flores, Laut Sulawesi, Laut Hindia, utara Irian Jaya, perairan utara Aceh,
barat Sumatera, selatan Jawa, utara Sulawesi, Teluk Tomini, dan Halmahera.
Volume ikan tuna hasil tangkapan tersebut mengalami peningkatan tiap tahunnya,
yang tentu diikuti oleh peningkatan produksi ikan tuna, dimana dari
tahun 1992-2002 mengalami kenaikan sebesar 6,55 ton (Ditjen Perikanan
Tangkap, 2004).
Ikan tuna pada umumnya dimanfaatkan untuk produksi pengalengan
dan pembekuan, baik utuh maupun dalam bentuk loin beku. Produk ikan tuna beku sebagian besar hanya memanfaatkan daging ikannya saja, sedangkan
sisa-sisa pemanfaatan lain berupa kepala, sirip dan tulang belum dimanfaatkan
secara optimal. Saat ini kepala, sirip dan tulang hanya dibuat tepung ikan.
Berdasarkan hasil wawancara pribadi dengan PT Bonecom (2005), ikan
tuna mengandung daging sebesar 45%, tulang 15%, kepala 30%, sisa kulit
dan sisik 10%. Jika didasarkan pada tingkat kenaikan produksi ikan tuna
sebesar 6,55 ton, maka limbah ikan tuna yang dihasilkan mengalami peningkatan
rata-rata sekitar 4 ton atau sekitar 1 ton akan dihasilkan limbah berupa
tulang ikan.
Tulang ikan dapat dimanfaatkan menjadi gelatin, Eastoe (1977)
menyatakan bahwa di dalam tulang terdapat kolagen sebesar 18,6% dari 19,86%
unsur organik protein kompleks. Kolagen selanjutnya dapat dibuat menjadi gelatin
melalui denaturasi panas. Berdasarkan proses pengolahannya, gelatin dapat dibagi
menjadi dua, yaitu tipe A dan tipe B. Pada pembuatan tipe A, bahan baku
direndam dengan larutan asam sehingga proses ini disebut proses asam,
sedangkan pada pembuatan tipe B, perendaman dilakukan dengan mengunakan
larutan basa, sehingga proses ini disebut proses alkali atau basa.
Kebutuhan gelatin dunia dari tahun ke tahun terus meningkat, pada
permintaan akan gelatin semakin tinggi. Penggunaan terbesar dari gelatin adalah
untuk industri makanan, yaitu sebanyak 60%. Pada tahun 2002 produksi gelatin
dunia tercatat 220.000 - 272.300 MT. Di Indonesia, kebutuhan gelatin dalam
bidang industri tidak diketahui jumlahnya secara pasti. Namun gelatin yang
digunakan industri-industri di Indonesia masih merupakan bahan impor dari
beberapa negara Eropa dan Amerika dengan harga relatif tinggi.
Secara umum fungsi gelatin untuk produk pangan adalah sebagai zat
pengental, penggumpal, pengemulsi, penstabil, pembentuk busa, menghindari
sineresis, pengikat air, memperbaiki konsistensi, pelapis tipis, pemerkaya gizi,
pengawet.
Selama ini sumber utama gelatin yang banyak dimanfaatkan adalah berasal
dari kulit dan tulang sapi atau babi. Penggunaan kulit dan tulang babi tidak
menguntungkan bila diterapkan pada produk pangan di negara-negara yang
mayoritas penduduknya beragama islam seperti Indonesia, karena babi
diharamkan untuk dimakan. Oleh karena itu, perlu dikembangkan gelatin dari
sumber hewan lain. Salah satu yang berprospek untuk dikembangkan adalah
gelatin tulang dan kulit ikan. Pembuatan gelatin dengan memanfaatan tulang ikan
patin dan menggunakan tulang ikan kakap merah sudah dilakukan. Dalam proses
pembuatannya, gelatin tulang ikan kakap merah dan tulang ikan patin
menggunakan proses pembuatan gelatin tipe A atau perendaman dengan asam,
dimana gelatin yang dihasilkan telah mendekati standar mutu gelatin yang ada
pasaran. Namun penelitian mengenai pembuatan gelatin dengan pemanfaatan
tulang ikan tuna belum pernah dilakukan. Oleh karena itu pemanfaaatan limbah
tulang ikan tuna menjadi produk gelatin menjadi sangat penting untuk dilakukan.
1.2Tujuan
Tujuan umum dari penelitian ini adalah:
1. Mengkaji metode pembuatan gelatin dari tulang ikan tuna dengan
menggunakan proses asam.
2. Menganalisis sifat fisika dan kimia gelatin dari tulang ikan tuna
2. TINJAUAN PUSTAKA
2.1Deskripsi Ikan Tuna (Thunnus sp)
Ikan tuna mempunyai tubuh seperti cerutu, dua sirip punggung, sirip depan
biasanya pendek dan terpisah dari sirip belakang, mempunyai jari-jari tambahan
(finlet) di belakang sirip dubur. Sirip dada terletak agak ke atas, sirip perut kecil, sirip ekor bercagak agak dalam dengan jari-jari penyokong menutup seluruh ujung
hipural. Tubuh ikan tertutup oleh sisik-sisik kecil berwarna biru tua dan agak
gelap pada bagian atas tubuhnya. Sebagian besar memiliki sirip tambahan yang
berwarna kuning cerah dengan pinggiran yang berwarna gelap
(Ditjen Perikanan, 1983).
Klasifikasi ikan tuna menurut Saanin (1984) adalah sebagai berikut:
Filum : Chordata
Subfilum : Vertebrata
klas : Teleostei
Subklas : Actinopterygi
Ordo : Perciformes
Subordo : Scombridae
Genus : Thunnus
Spesies : Thunnus sp
Penyebaran ikan tuna Albacore meliputi Laut Banda, Laut Maluku, Laut Flores, Laut Sulawesi, Laut Hindia, utara Irian Jaya, perairan utara Aceh,
barat Sumatera, selatan Jawa, utara Sulawesi, Teluk Tomini, dan Halmahera.
Penangkapan ikan tuna Yellow fin terletak di perairan bagian barat Samudera Pasifik tengah, Laut Banda, Laut Sulawesi, Samudera Hindia,
Selat Sunda, Laut Maluku dan barat Sumatera. (Nikijuluw, 1986)
Ikan tuna adalah jenis ikan dengan kandungan protein yang tinggi dan
lemak yang rendah. Ikan tuna mengandung protein antara 22,6-26,2%. Disamping
itu ikan tuna mengandung mineral (kalsium, fosfor, besi dan sodium), vitamin A
Sumber : www.kuuloakai.com/images/albacore_large.gif
Gambar 1. Ikan tuna albacore 2.2Kolagen
Bahan baku utama gelatin adalah kolagen, yang banyak terdapat pada
kulit, urat, tulang rawan dan tulang keras pada hewan. Kolagen merupakan
protein fibriler, yaitu protein yang berbentuk serabut. Protein ini tidak larut dalam pelarut-pelarut encer baik larutan garam, asam, basa, dan alkohol
(Winarno, 1997). Kolagen yang berarti “bahan pembentuk perekat” merupakan
komponen protein utama jaringan penghubung, yang bertindak sebagai elemen
penahan tekanan pada semua mamalia dan ikan (Glicksman, 1969).
Menurut Lehninger (1990), jaringan kolagen tersusun atas fibril kolagen
yang nampak seperti garis-garis melintang. Fibril ini terorganisasi sesuai dengan
sistem biologis jaringan tersebut. Kolagen merupakan protein yang mengandung
35% glisin dan sekitar 11% alanin serta kandungan prolin yang cukup tinggi.
Pemanasan kolagen secara bertahap akan menyebabkan struktur rusak dan
rantai-rantai akan terpisah. Berat molekul, bentuk dan konformasi larutan kolagen
sensitif terhadap perubahan temperatur yang dapat menghancurkan
makromolekulnya (Wong, 1989). Pemanasan pada suhu 40 oC belum
mengakibatkan putusnya ikatan kovalen. Ikatan kovalen yang ada pada kolagen
akan terputus saat suhu pemanasan naik menjadi 60 oC atau lebih (Johns dan
Courts 1977). Proses denaturasi struktur kolagen berlangsung relatif lambat bila
dibandingkan dengan protein lainnya.
Kolagen murni sangat sensitif terhadap reaksi enzim dan kimia. Perlakuan
alkali, kolagen juga larut dalam pelarut asam. Asam mampu mengubah serat
kolagen tripel heliks menjadi rantai tunggal, sedangkan larutan perendaman basa hanya mampu manghasilkan rantai ganda pada waktu perendaman yang sama
(jumlah kolagen yang terhidrolisis oleh larutan perendaman yang asam lebih
banyak daripada larutan basa) sehingga waktu yang diperlukan oleh larutan basa
untuk menghidrolisis kolagen menjadi lebih lama.(Bennion , 1980).
Kolagen dapat mengalami penyusutan jika dipanaskan diatas suhu
penyusutan (Ts), suhu penyusutan kolagen berkisar antara 60 – 70 oC. Pada suhu
tersebut memperpendek serat kolagen sepertiga atau seperempat dari panjang
asalnya. Suhu penyusutan (Ts) kolagen ikan adalah 35 oC. Pemecahan struktur
tersebut menjadi lilitan acak yang larut dalam air yang disebut dengan gelatin.
Jika suhu dinaikan sampai 80 oC, kolagen akan berubah menjadi gelatin
(deMan 1997).
Unit struktural pembentuk kolagen adalah tropokolagen yang mempunyai
struktur batang dengan BM 300.000, dimana di dalamnya terdapat tiga rantai
polipeptida yang sama panjang, bersama-sama membentuk struktur heliks
(Bennion, 1980).
2.3 Gelatin
Gelatin merupakan senyawa turunan yang dihasilkan dari serabut kolagen
jaringan penghubung yang dihidrolisis dengan asam atau basa (Charley, 1982).
Menurut Courts (1977), berat molekul gelatin 90.000 sedangkan rata-rata berat
molekul gelatin komersial berkisar antara 20.000-70.000.
Gelatin dapat diperoleh dengan cara denaturasi panas dari kolagen.
Pemanasan kolagen secara bertahap akan menyebabkan struktur rusak dan
rantai-rantai akan terpisah. Berat molekul, bentuk dan konformasi larutan kolagen
sensitif terhadap perubahan temperatur yang dapat menghancurkan makro
molekulnya (Wong, 1989).
Menurut deMan (1997), gelatin adalah protein larut yang diperoleh dari
kolagen tak larut. Gelatin juga didefinisikan sebagai produk yang diperoleh dari
perubahan sol-gel yang reversibel seiring perubahan suhu. Proses perubahan kolagen menjadi gelatin melibatkan tiga perubahan berikut:
1. Pemutusan sejumlah ikatan peptida untuk memperpendek rantai
2. Pemutusan / pengacauan sejumlah ikatan samping antar rantai
3. Perubahan konfigurasi rantai
Proses pembentukan gel berkaitan erat dengan gugus guanidine arginin.
Dalam pembentukan gel, gelatin didispersikan dalam air dan dipanaskan sampai
membentuk sol. Daya tarik menarik antara molekul protein lemah dan sol tersebut
berbentuk cairan, yaitu bersifat mengalir dan dapat berubah sesuai dengan
tempatnya. Bila didinginkan, molekul-molekul yang kompak dan tergulung dalam
bentuk sol mulai mengurai dan terjadi ikatan-ikatan silang antara
molekul-molekul yang berdekatan sehingga terbentuk suatu jaringan. Sol akan berubah
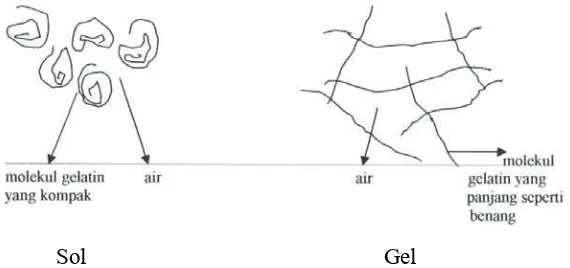
menjadi gel. Mekanisme pembentukan gel dapat dilihat pada Gambar 2.
Sol Gel
Gambar 2. Proses pembentukan gel pada gelatin (deMan 1997)
Metode pengkonversian kolagen menjadi gelatin adalah dengan cara
denaturasi kolagen dengan pemutusan ikatan hidrogen. Proses denaturasi terjadi
dengan pemanasan kolagen pada suhu 40 0C atau dengan penambahan senyawa
pemecah ikatan hidrogen pada suhu kamar atau lebih rendah, berupa pemecahan
struktur koil kolagen menjadi satu, dua, atau tiga rantai secara acak
(Hinterwaldner, 1977)
Gelatin mengandung 19 asam amino yang dihubungkan dengan ikatan
peptida membentuk rantai polimer yang panjang. Komposisi asam amino dalam
(Ward dan Courts, 1977). Susunan asam amino gelatin hampir mirip dengan
kolagen, dimana glisin merupakan asam amino yang utama (Charley, 1982).
Jenis dan komposisi asam amino pada tulang keras (teleostei) ikan patin menurut Nurilmala, 2005 antara lain sebagai berikut isoleusin 1,07%, leusin tidak
terdeteksi, lisin 1,89%, tirosin 0,09%, valin 1,34%, metionin 0,37%, sistein
0,06%, fenilalanin 2,01%, treonin 2,55%, glisin 22,97%, prolin 12,17%,
hidroksiprolin 6,25%, alanin 10,31%, arginin 8,23%, asam aspartat 4,53%, serin
2,00%, asam glutamat 9,30%, histidin 0,01%.
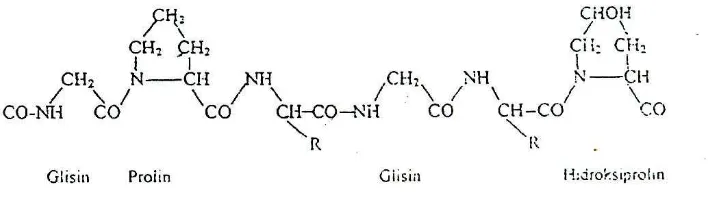
Gambar 3. Struktur kimia gelatin (Poppe, 1992)
Gelatin akan mengembang jika direndam dalam air dan menjadi lunak,
serta berangsur-angsur menyerap air 5-10 kali bobotnya. Gelatin larut dalam air
panas dan jika didinginkan akan membentuk gel. Gelatin memiliki beberapa sifat
yaitu dapat berubah secara reversibel dari bentuk sol ke gel, membengkak atau mengembang dalam air dingin, dapat membentuk film, mempengaruhi viskositas
suatu bahan dan dapat melindungi sistem koloid (Parker, 1982).
Gelatin larut dalam air, asam asetat dan pelarut alkohol seperti gliserol,
propilen glikol, sorbitol dan manitol, tetapi tidak larut dalam alkohol, aseton,
karbon, tetraklorida, benzene, petroleum eter dan pelarut organik lainnya (Viro,
1992).
Gelatin larut dalam air pada suhu 30-80 oC dan bersifat amfoter ( dapat
bersifat asam atau basa), namun hal ini sangat dipengaruhi oleh pH larutan.
Karakter amfoter pada gelatin dihasilkan oleh gugus karboksil dan amino ujung
yang terbentuk selama hidrolisis dan gugus fungsi asam amino lainnya. Selain
bersifat amfoter, gelatin juga bersifat koloid protektif yang dapat menstabilkan
Menurut Viro (1992), terdapat dua tipe gelatin berdasarkan perbedaan
proses pengolahannya. Tipe A dihasilkan melalui proses asam dengan titik
isoelektrik pada pH antara 7,5-9,0. Sedangkan tipe B dengan titik isoelektrik
4,8-5,2. Beberapa sifat gelatin tipe A dan tipe B dapat dilihat pada Tabel 1.
Tabel 1. Sifat gelatin tipe A dan tipe B
Sifat Tipe A Tipe B
Kekuatan gel (g bloom) 75-300 75-275
Viskositas (cp) 2,0-7,5 2,0-7,5
Kadar abu(%) 0,3-2,0 0,05-2,0
pH 3,8-6,0 5,0-7,1
Titik isoelektrik 9,0-9,2 4,8-5,0
Sumber: Tourtellote, 1980
Sifat fisik secara umum dan kandungan unsur-unsur mineral tertentu
dalam gelatin dapat digunakan untuk menilai mutu gelatin. Standar mutu gelatin
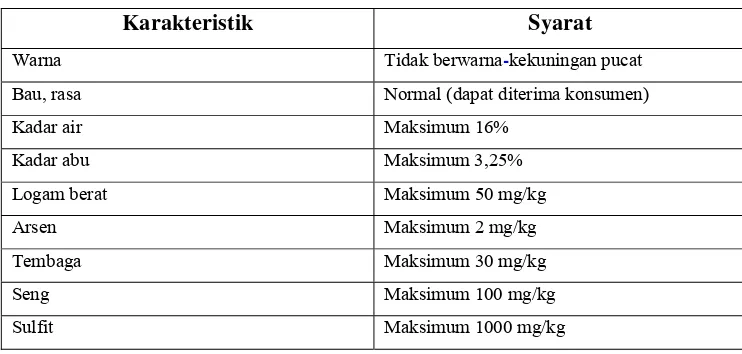
menurut SNI dapat dilihat pada Tabel 2.
Tabel 2. Standar mutu gelatin
Karakteristik Syarat
Warna Tidak berwarna-kekuningan pucat
Bau, rasa Normal (dapat diterima konsumen)
Kadar air Maksimum 16%
Kadar abu Maksimum 3,25%
Logam berat Maksimum 50 mg/kg
Arsen Maksimum 2 mg/kg
Tembaga Maksimum 30 mg/kg
Seng Maksimum 100 mg/kg
Sulfit Maksimum 1000 mg/kg
Persyaratan gelatin untuk makanan berdasarkan FAO pada Tabel 3.
Tabel 3. Persyaratan gelatin berdasarkan FAO
Parameter Persyaratan
Kadar abu Tidak lebih dari 2%
Kadar air Tidak lebih dari 18%
Belerang dioksida Tidak lebih dari 40 mg/kg
Arsen Tidak lebih dari 1 mg/kg
Logam berat Tidak lebih dari 50 mg/kg
Timah hitam Tidak lebih dari 5mg/kg
Sumber: JECFA, 2003
2.4Pembuatan Gelatin
Berdasarkan proses pengolahannya, gelatin terbagi menjadi dua yaitu tipe
A dan tipe B. Pada pembuatan tipe A, bahan baku direndam dengan larutan asam
sehingga proses ini disebut proses asam. Pada pembuatan tipe B, perendaman
mengunakan larutan basa, proses ini disebut proses alkali atau basa
(Utama, 1997).
Menurut Hinterwaldner (1997), terdapat tiga tahap proses produksi yang
utama. Tahap pertama, tahap persiapan bahan baku antara lain penghilangan komponen non kolagen dari bahan. Tahap kedua, tahap konversi kolagen
menjadi gelatin. Tahap ketiga, tahap pemurnian gelatin dengan penyaringan
dan pengeringan.
Proses penghilangan lemak dari jaringan tulang yang biasa disebut
degreasing, dilakukan pada suhu antara titik cair lemak dan suhu koagulasi albumin tulang yaitu antara 32-80 oC, sehingga dihasilkan kelarutan lemak
yang optimum (Courts, 1977).
Proses demineralisasi bertujuan untuk menghilangkan garam kalsium dan
garam lainnya dari tulang, sehingga diperoleh tulang yang sudah lumer disebut
ossein (Hinterwaldner, 1977). Menurut Court (1977) asam mampu mengubah serat kolagen triple heliks menjadi rantai tunggal, sedangkan larutan perendaman basa hanya mampu menghasilkan rantai ganda. Hal ini menyebabkan pada waktu
daripada larutan basa. Karena itu perendaman dalam larutan basa membutuhkan
waktu yang lebih lama untuk menghidrolisis kolagen.
Kisaran temperatur yang digunakan untuk ekstraksi adalah 50-100 oC atau
lebih rendah. Nilai pH ekstraksi dapat berbeda untuk setiap metode. Selanjutnya
disebutkan bahwa untuk menghilangkan zat-zat lain yang tidak larut dan dapat
mengurangi kemurnian gelatin, perlu dilakukan penyaringan
(Hinterwaldner, 1977).
Pada proses pembuatan gelatin tulang ikan kakap merah (Hadi, 2005)
menggunakan perendaman HCl dengan konsentrasi 4, 5, 6% dengan suhu
ekstraksi 80, 85, 90 oC. Proses terbaik pembuatan gelatin tulang kakap merah
menggunakan HCl 4% dengan suhu ekstraksi 80 oC dan suhu pengovenan 55 oC.
2.5Mutu Gelatin
Bahan baku tulang ikan menentukan mutu kualitas gelatin. Kesegaran
bahan baku menentukan dan mempengaruhi kualitas ossein dan gelatin. Semakin segar bahan baku maka kualitas gelatin akan semakin baik (Hinterwaldner, 1977).
Mutu gelatin sangat ditentukan oleh sifat fisik, kimia dan fungsional yang
menjadikan gelatin sebagai karakter yang unik Sifat-sifat fisik gelatin menurut
Budavari (1996) antara lain:
1. Tidak berwarna atau agak berwarna kuning transparan,
2. Rapuh
3. Tidak berbau
4. Tidak memiliki rasa
5. Berbentuk lembaran, serpihan atau tepung
6. Larut dalam air panas, gliserol dan asam asetat
7. Tidak larut dalam pelarut organik.
Menurut Poppe (1992) gelatin memiliki titik leleh di bawah 37 oC, ini
berarti gelatin dapat meleleh di dalam mulut dan mudah sekali larut. pH gelatin
terbentuk dalam larutan netral disebut titik isoelektrik. Titik isoelektrik protein
gelatin berkisar antara 4,8 - 9,4, dimana gelatin yang diproses secara asam
Kadar abu gelatin bervariasi berdasarkan jenis bahan baku dan metode
pengolahannya. Gelatin komersial memiliki kekuatan gel yang cukup bervariasi
yaitu 75 – 300 bloom (Tourtellote, 1980). Gelatin dari ikan berbeda dengan
gelatin dari sapi atau babi yaitu titik lelehnya rendah, suhu pembentuk gelnya
rendah dan viskositasnya tinggi (Leunberger, 1991).
Gelatin yang diperoleh secara basa memiliki hidroksiprolin lebih tinggi
dan memiliki tirosin yang rendah dibanding gelatin dengan proses asam.
Komposisi asam amino gelatin yang diperoleh dari kolagen ikan dan
Elasmobranchi lebih beragam dibandingkan gelatin dari sumber lainnya. Kadar prolin dan hidroksiprolin gelatin ikan lebih rendah dari mamalia dan lebih rendah
lagi pada ikan air dingin (Eastoe dan Leach, 1977).
2.6Manfaat Gelatin
Gelatin adalah protein yang mempunyai nilai gizi rendah karena pada
gelatin tidak terkandung seluruh asam amino esensial pembentuk protein secara
lengkap. Gelatin merupakan suatu protein yang tidak mengandung asam amino
triptofan oleh karena itu penggunaan gelatin lebih disukai karena sifat fisik
kimianya bukan karena nilai gizinya.
Kegunaan gelatin terutama untuk mengubah cairan menjadi padatan yang
elastis atau mengubah bentuk sol menjadi gel. Reaksi pada pembentukan gel ini
bersifat reversible kerena bila gel dipanaskan akan terbentuk sol dan bila didinginkan akan terbentuk gel lagi. Keadaan tersebut membedakan gelatin
dengan gel dari pektin, alginat, albumin telur, dan protein susu yang gelnya
irreversible (Johns, 1977).
penggunaan gelatin sudah meluas meliputi produk pangan dan non
pangan. Sebagian besar dari total produksi gelatin diaplikasikan pada industri
makanan dalam bentuk edible gelatin. Dalam pembuatan bakery, gelatin digunakan sebagai bahan penstabil dan pengisi. Pemanfaatan gelatin dalam
produk non pangan ialah industri farmasi, teknik dan kosmetik. Pada bidang
farmasi, gelatin digunakan dalam pembuatan kapsul, berperan sebagai agen
pengikat untuk tablet dan pastilles, penyamar rasa pada pil, pengganti serum,
digunakan dalam bahan pembuatan lem, kertas, cat yang berperan sebagai
pengikat, dan penstabil emulsi. Dalam industri kosmetika digunakan dalam
lipstik, shampo dan sabun.
Gelatin dapat digunakan sebagai penstabil (stabilizer), pembentuk gel (geling agent), pengikat (binder), pengental (thickner), pengemulsi (emulsifier), perekat (adhesive), dan pembungkus makanan yang bersifat dapat dimakan (edible coating) (Jones, 1977).
Gelatin sebagai pembentuk gel karena mempunyai sineresis yang rendah
dan mempunyai kekuatan gel antara 220 atau 225 gr bloom (Jones, 1977),
sehingga dapat digunakan dalam pembuatan produk jelly. Sebagai pengemulsi
gelatin bisa diaplikasikan ke dalam sirup lemon, susu, mentega, margarine, pasta ,
dan mayonnaise. Gelatin sebagai penstabil dapat digunakan dalam pembuatan es
krim dan yoghurt. Sebagai bahan pengikat, gelatin dapat digunakan dalam
Tabel 4. Aplikasi gelatin terhadap produk pangan dan non pangan berdasarkan sifat fisik-kimia
Produk fungsi Kekuatan gel
(Bloom) Type Viskositas Dosis
Gelatin gums • Gelling agent
• Tekstur
• Chewability 100-150 A/B Medium-High 0.5-3%
Marsmallows • Stabilisasi
• Gelling Agent
200-260 A/B Medium-High 2-5%
Nugget • Chewability 100-150 A/B Medium-High 2-5%
Coating • Film Forming 120-150 A/B High 0,2-1%
Youghurt • pengental
• Gelling agent
• Tekstur
200-250 A/B Medium-High 0,2-1%
Eskrim • Tekstur
Sumber :http://www.gelatin.co.za/gltn1.html#Gel-str dan www. Koshercom.org
Ket : A = Gelatin dengan Proses Asam
3. METODOLOGI
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan April 2005 sampai dengan
Agustus 2005, yang bertempat di Laboratorium Biokimia Departemen Teknologi
Hasil Perairan, Bogor, Laboratorium Pengolahan Departemen Teknologi Pangan
dan Gizi. Institut Pertanian Bogor.
3.2 Bahan dan Alat
Bahan penelitian yang digunakan, meliputi bahan utama untuk pembuatan
gelatin yaitu tulang ikan tuna albacore dibawa dengan box yang didalamnya diberi
es, tulang ikan tuna albacore diperoleh dari PT Bonecom pada bulan April, asam
klorida teknis yang didapatkan dari Toko Bratachem dan aquades. Bahan – bahan
untuk analisis yaitu asam klorida, asam sulfat, asam asetat, pelarut hexana,
natrium asetat,natrium hidroksida, etanol 95%, garam kjeldahl (CuSO4 dan
K2SO4).
Peralatan yang dibutuhkan yaitu: pisau, kompor gas, wadah plastik,
cetakan, neraca analitik, pH meter, tanur, desikator, oven, heater, thermometer, blender, peralatan mikro kjeldahl, peralatan soxhlet, cawan alumunium, cawan
porselen, alat-alat gelas, kertas saring whatman 40, kain saring, Rheoner RE3305 , Brookfield Synchro-Lectric Viscometer, Kettler Whitenes Powder.
3.3 Metode Penelitian
Penelitian ini dilakukan dalam dua tahapan, yaitu tahap pertama dan tahap
kedua. Penelitian tahap pertama berfokus pada pembuatan gelatin dengan proses
perendaman dengan asam klorida dan suhu ekstraksi. Adapun penelitian tahap
kedua berfokus pada analisis sifat fisika kimia produk gelatin yang dihasilkan.
Pembuatan gelatin dari tulang ikan tuna dilakukan dengan metode asam
yang dimodifikasi dari Hadi (2005). Tahapan utama proses pembuatan gelatin ini
adalah degrasssing (perebusan) selama 30 menit dengan suhu 80oC;
demineralisasi atau perendaman tulang ikan tuna dengan menggunakan asam klorida, dimana banyaknya tulang ikan dibandingkan dengan larutan perendaman
perendaman 2 hari, dimana tiap 24 jam larutan perendaman diganti; dan terakhir
adalah pemanasan dengan suhu berkisar antara 80-90oC. Diagram alir proses
pembuatan gelatin dapat dilihat pada Gambar 4. Adapun deskripsi selangkapnya
tahapan penelitian ini adalah :
3.3.1 Penelitian tahap pertama
Penelitian tahap pertama diawali dengan melakukan analisis proksimat
pada bahan baku tulang ikan tuna kering, yang meliputi kadar air, kadar abu,
kadar protein dan kadar lemak. Proses penelitian selanjutnya adalah pembuatan
gelatin dari tulang ikan tuna dengan perlakuan pertama pada proses
demineralisasi atau perendaman tulang ikan tuna dengan menggunakan asam klorida, dimana banyaknya tulang ikan dibandingkan dengan larutan perendaman
adalah 1: 4, dan konsentrasi asam klorida yang digunakan adalah 3, 4, 5, 6 dan 7%
v/v dengan lama perendaman 2 hari, dimana setiap 24 jam larutan perendaman
diganti dan pemanasan dengan suhu ekstraksi 80, 85 dan 90oC merupakan
perlakuan yang kedua. Untuk mengetahui perbedaan antar perlakuan dilakukan
pengamatan berupa uji fisik yang meliputi identifikasi gelatin, rendemen, pH,
viskositas, dan kekuatan gel.
3.3. Penelitian tahap kedua
Penelitian tahap kedua merupakan analisis produk gelatin yang terpilih
dari penelitian tahap pertama. Hasil analisis ini dibandingkan parameter mutunya
dengan gelatin tulang ikan kakap merah (Hadi, 2005) dan gelatin tulang ikan patin
(Nurilmala, 2004). Parameter yang dibandingkan meliputi analisis proksimat
gelatin (kadar air, abu, lemak dan protein) dan sifat fisika-kimianya meliputi
kekuatan gel, viskositas, pH, titik gel, titik leleh, titik isoelektrik, derajat putih dan
Degreasing (Perebusan) selama 30 menit pada suhu 80oC
Pembersihan
Pemotongan dengan ukuran 1,5-2 cm
Pengeringan
dengan sinar matahari selama 2 hari Tulang ikan tuna
Demineralisasi (perendam)
HCl 3%,4%, 5%, 6% dan 7% selama 2 hari (1:4), diganti larutansetiap hari *
Pencucian sampai pH netral
Perendaman ossein dalam aquades selama 1hari
Pencucian dengan air mengalir
Ekstraksi
pada suhu 80 0C, 85 0C, 90 0C selama 4 jam
Penyaringan menggunakan kain belacu
Pengeringan
dalam oven pada suhu 60 0C *
Lembaran gelatin
* Modifikasi
3.4 Analisis
3.4.1 Rendemen (AOAC, 1995)
Rendemen diperoleh dari perbandingan berat kering tepung gelatin yang
dihasilkan dengan berat bahan segar (tulang yang telah dicuci bersih). Besarnya
rendemen dapat diperoleh dengan menggunakan rumus:
Rendemen = x100%
3.4.2 Kekuatan gel (Gaspar, 1998)
Kekuatan gel dilakukan secara objektif dengan menggunakan alat Rheoner
RE3305. Tingkat kekuatan gel dinyatakan dengan satuan gf/cm2 yang berarti
besarnya gaya tekan untuk memecah deformasi produk. Sebelum digunakan alat
disetting agar sesuai dengan jenis produk yang akan diukur kekuatan gelnya
karena standar setting untuk setiap produk berbeda. Pada pengujian ini
jarak 400 x 0.01 mm, kecepatan 0.5 mm/s, chart speed 60 mm/ min, silinder probe 16 mm. Cara kerja alat ini yaitu silinder penusuk yang bediameter 16 mm tidak bergerak, meja tempat untuk meletakan sampel yang bergerak ke atas
mendekati jarum penusuk, tekanan dilakukan sebanyak satu kali hasil pengukuran
akan tercetak dalam kertas dengan bentuk Histogram, pengukuran berdasarkan
tingginya Histogram.
3.4.3 Viskositas (British Standard 757, 1975)
Larutan gelatin dengan konsentrasi 6,67% (b/b) disiapkan dengan aquades
kemudian diukur viskositasnya dengan menggunakan alat Brookfield Synchro-Lectric Viscometer. Pengukuran dilakukan pada suhu 60 0C dengan kecepatan 60 rpm. Nilai viskositas dinyatakan dalam satuan centipoises (cP).
3.4.4 Kadar air (AOAC, 1995)
Cawan porselen dikeringkan pada suhu 105 0C selama 1 jam. Kemudian
didinginkan dan ditimbang. Contoh yang akan ditentukan kadar air ditimbang
sebanyak 5 gram. Cawan yang telah berisi contoh dimasukan ke dalam oven
bersuhu 105 0C sampai beratnya konstan. Kadar air dihitung berdasarkan
(%) Kadar Air = ( ) x100%
contoh Berat
A B−
Keterangan : A= berat cawan + contoh kering (g)
B= berat cawan + contoh basah (g)
3.4.5 Kadar abu (AOAC, 1995)
Timbang sampel ± 2 gram masukan kedalam cawan porselin lalu
dipanaskan pada penangas sampai didapat arang atau sampai asap hilang dari
sampel yang dipanaskan. Contoh yang telah diuapkan airnya dimasukkan ke
dalam tanur bersuhu 600 0C, sebelumnya berat cawan kering dan berat contoh
telah diketahui. Proses penguapan dilakukan sampai semua bahan berubah warna
enjadi abu-abu, kemudian contoh ditimbang.
(%) Kadar Abu = x100%
Sampel Berat
Abu Berat
3.4.6 Kadar protein (AOAC, 1995)
Penentuan kadar protein dilakukan dengan metode mikrokjeldahl. Prinsip
analisis ini adalah menetapkan protein berdasarkan oksidasi bahan-bahan
berkarbon dan konversi nitrogen menjadi amonia. Selanjutnya amonia bereaksi
dengan kelebihan asam membentuk amonium sulfat. Setelah larutan menjadi basa,
amonia diuapkan untuk diserap dalam larutan asam borat. Jumlah nitrogen yang
terkandung ditentukan dengan titrasi HCl.
Cara penentuannya meliputi tahap destruksi, destilasi, dan titrasi.
Mula-mula sampel ditimbang sebanyak 0,5 gram, masukan dalam labu kjeldahl
kemudian ditambahkan 5 gram garam kjeldahl sebagai katalis yang berupa
campuran CuSO4.5H2O dan K2SO4, tambahkan 10 ml H2SO4 pekat. Destruksi
sampai larutan berwarna jernih, angkat labu kjeldahl dan dinginkan, setelah dingin
lakukan destilasi dengan menggunakan kjeltech sistem yang sebelumnya larutan
sampel diberi penambahan NaOH, larutan asam standar berupa asam borat dan
indikator metilenblue. Setelah larutan mencapai 200 ml lakukan titrasi dengan HCl 0,1 N sampai warna berbah menjadi biru muda.
3.4.7 Kadar lemak (Apriyantono et al., 1989)
Penentuan kadar lemak dilakukan dengan menggunakan metode soxhlet.
Prinsip analisis ini adalah mengekstrak lemak dengan pelarut dietil eter, setelah
pelarutnya diuapkan, lemak dapat ditimbang dan dihitung persentasenya. Lemak
yang dihasilkan adalah lemak kasar.
Cara penentuannya adalah dengan meletakkan 5 gram sampel yang sudah
dibungkus dengan kertas saring di alat soxhlet, kemudian pelarut dietil eter
dituang ke dalam labu lemak. Selanjutnya direfluks selama minimum 5 jam
sampai pelarut yang turun kembali ke labu lemak berwarna jernih. Pelarut yang
ada di labu lemak tersebut didestilasi, labu yang berisi hasil ekstraksi dipanaskan
dalam oven pada suhu 100 0C. Setelah didinginkan dalam desikator, labu lemak
tersebut ditimbang sampai memperoleh berat yang konstan. Berat lemak dapat
dihitung dengan rumus:
3.4.8 Derajat putih (Kett Digital Whiteness Powder)
Analisa warna dilakukan menggunakan Kett Digital Whiteness Powder C-100. Sampel dalam bentuk tepung dimasukkan kedalam cawan sampel,
selanjutnya cawan tersebut dimasukkan kedalam alat. Nilai dapat langsung dibaca
pada layer dan dinyatakan dalam persentase derajat putih. Standar derajat putih
blanko adalah 85,4 %.
3.4.9 Titik gel (Suryaningrum dan Utomo, 2002)
Larutan gelatin dengan konsentrasi 6,67% (b/b) disiapkan dengan aquades,
dan disimpan dalam tabung reaksi yang dihubungkan dengan thermometer digital,
kemudian diberikan es pada sekeliling luar bagian tabung reaksi. Titik gel adalah
suhu ketika larutan gelatin mulai menjadi gel dan suhu ini ditentukan pada saat
sensor dapat mengangkat gel dalam tabung reaksi.
3.4.10 Titik leleh ( Suryaningrum dan Utomo, 2002)
Larutan gelatin dengan konsentrasi 6,67% (b/b) disiapkan dengan aquades.
Sampel diinkubasi pada suhu 10 oC selama 17±2 jam. Pengukuran titik leleh
gelatin tersebut diletakkan goytri dan ketika goytri jatuh ke dasar gel gelatin,
maka suhu tersebut merupakan suhu titik leleh.
3.4.11. Titik isoelektrik protein (Wainewright, 1977)
Sebanyak 0,2 gr sample ditambah dengan 40 ml aquades sebagai pelarut
dengan kisaran pH 4,5-10,5 interval 0,5. Pengaturan pH dilakuakan dengan
menambahkan NaOH 0,5 N untuk menaikkan pH dan HCl 0,5 N untuk
menurunkan pH. Setelah kondisi tercapai dilanjutkan dengan pengadukan
selama 30 menit untuk menyempurnakan ekstraksi. Larutan yang dihasilkan
dipisahkan dengan bagian yang tidak larut dengan cara disentrifuse, kemudian
disaring menggunakan kertas saring Whatman. Filtrate dianalisis kadar
nitrogennya dengan metode mikrokjeldahl. Kadar nitrogen terlarut yang paling
rendah ditentukan sebagai daerah isoelektrik (pI).
3.4.12. Derajat keasaman (pH) (British Standard 757, 1975)
Sampel sebanyak 0,2 gram ditimbang dan didispersikan ke dalam 20ml
aquades pada suhu 80 oC. sampel dihomogenkan dengan magnetic stirrer, kemudian diukur derajat keasamannya pada suhu kamar dengan pH meter.
3.4.13. Kandungan logam berat (Hg) (Hutagalung, 1997)
Sampel sebanyak 2 gr dimasukan kedalam teflon beker yang memepunyai
tutup, ditambahkan 1,5 ml HClO4 dan 3,5 ml HNO3 tutup dan biarkan
selama 24 jam. Selanjutnya panaskan diatas penangas air pada suhu 60-70 oC,
selama 2-3 jam (sampai larutan jernih). Tambahkan 3 ml air suling bebas ion,
panaskan kembali hingga larutan hampir kering selanjutnya didinginkan pada
suhu ruang. Kemudian ditambahkan 1 ml HNO3 pekat dan diaduk-aduk
pelan-pelan. Selanjutnya ditambahkan 9 ml air suling bebas ion. Kemudian dilakukan
pengukuran menggunakan Atomic Absorption Spectrophotometri menggunakan nyala udara-asetilen.
3.4.14. Komposisi asam amino (Nur et al, 1992)
Sebanyak 0,2 gram sampel disiapkan dalam tabung reaksi tertutup dan
ditambahkan 5ml HCl 6N. Sampel dimasukan dalam oven dengan suhu 100 oC
selama 24 jam, selanjutnya sampel disaring dalam kertas saring Whatman 40.
dikeringkan dengan pompa vakum bertekanan 50 torr. Sampel yang telah
dikeringkan ditambahkan larutan derivat (methanol, phenyl iso tiocyanat dan
TEA) sebanyak 30 µl dan dibiarkan selama kurang lebih 20 menit. Sampel
selanjutnya diencerkan dengan 200 µl larutan pengencer natrium asetat 1 M.
Sampel siap dianalisis dengan menggunakan HPLC Water Asiociates. Kondisi HPLC pada saat dilakukan analisis:
Temperatur kolom : 38 0C
Kolom : Pico tag 3,9 X 150 nm coulomb
Kecepatan alir : Sistem linier gradient
Batas tekanan : 3000 psi
Program : Gradien
Fase gerak : Asetonitril 60%
Buffer Natrium Asetat 1 M, pH 5,75
Detektor : UV, panjang gelombang 254 nm
Konsentrasi asam amino dapat ditentukan dengan rumus:
Asam Amino (%) = x100%
BM = Berat molekul masing-masing asam amino
Fp = Faktor pengenceran
3.5 Rancangan Percobaan
Rancangan percobaan yang digunakan adalah Rancangan Acak Lengkap
Faktorial dengan dua faktor, yaitu konsentrasi HCl (4, 5 dan 6%) dan suhu
ekstraksi (80 ,85 dan 90 oC). Metode rancangan yang digunakan adalah sebagai
berikut;
Keterangan :
Yijk = Nilai hasil pengamatan dari faktor A level ke-i, faktor B level ke-j
ulangan ke-k
µ = Rataan umum
Ai = Pengaruh konsentrasi HCl
Bj = Pengaruh suhu ekstraksi
(AB)ij = Pengaruh interaksi antara konsentrasi dan suhu
∑ijk = Faktor galat (sisa)
Data selanjutnya diolah dengan menggunakan analisis ragam apabila
terjadi beda nyata pada faktor perlakuan selang kepercayaan 95%. Uji lanjut
menggunakan uji wilayah berganda Duncan menggunakan tingkat nyata yang
besarnya bergantung pada banyaknya nilai tengah yang terlibat pada setiap tahap
pengujian. Dasar pemikirannya adalah bahwa meningkatnya nilai tengah, akan
diikuti dengan mengecilnya peluang bahwa semuanya sama. Nilai tengah dihitung
dengan rumus:
Sy =
r KTS
Keterangan
Sy = total nilai tengah
KTS = kuadrat tengah sisa
R = ulangan
Untuk menghitung wilayah nyata terkecil menggunakan rumus:
Rp = q x Sy
Keterangan
Rp = wilayah nyata terkecil
4. HASIL DAN PEMBAHASAN
4.1. Penelitian Tahap Pertama
Bahan baku pada penelitian ini didapat dari perusahaan Bonecom Jakarta.
Tulang yang didapat merupakan limbah dari pengolahan loin ikan tuna, tulang
ikan tidak mengalami penanganan khusus (disimpan pada refrigerator) dari
perusahaan sehingga tidak terlalu segar, tulang tidak terlalu putih setelah di
degreasing. Tulang ikan dapat dilihat pada Gambar 5.
Gambar 5. Tulang ikan tuna (Thunnus sp) bagian dada
Pada penelitian pertama dilakukan analisis proksimat tulang ikan tuna
kering dengan tujuan untuk mengetahui kandungan protein, lemak, air dan abu
Hasil analisis proksimat selengkapnya tulang ikan tuna dapat dilihat pada Tabel 5.
Tabel 5. Proksimat tulang ikan tuna albacore
Parameter Jumlah (%)
Protein 26,02
Lemak 8,01
Abu 52,36
Air 12,57
Dari hasil analisis didapat nilai protein sebesar 26,02% sehingga tulang
ikan tuna dapat dijadikan bahan baku sebagai gelatin, karena menurut
Eastoe (1977), di dalam tulang terdapat kolagen sebesar 18,6% dari 19,86% unsur
organik protein kompleks. Kadar abu pada tulang ikan tuna sebesar 52,36%, hal
kering. Kadar lemak pada tulang ikan tuna sebesar 8,01% dan kadar air sebesar
12,57%.
Untuk mendapat gelatin dari tulang ikan tuna dilakukan beberapa tahap,
tahapan proses yang paling penting adalah pada saat demineralisasi dan ekstraksi,
pada tahap ekstraksi adalah tahap perubahan struktur kolagen menjadi gelatin.
Pada tulang ikan tuna kering dilakukan proses demineralisasi yaitu
menghilangkan mineral yang terdapat dalam tulang, proses ini akan menghasilkan
ossein. Proses demineralisasi dilakukan dengan merendam tulang dalam asam kuat, dengan tujuan supaya senyawa asam dapat memutuskan ikatan hidrogen
struktur koil kolagen lebih baik dalam waktu yang relatif singkat.
Pada penelitian ini telah dicobakan mulai dari konsentrasi 3% hingga 7%.
Konsentrasi HCl 3% belum mengubah struktur tripleheliks kolagen menjadi rantai
tunggal dan tulang masih terlalu keras dimana kandungan mineral masih cukup
tinggi sehingga ossein pada konsentrasi HCl 3% belum terbentuk secara
sempurna. Sedangkan untuk konsentrasi 7% tulang ikan menjadi hancur dan tidak
dapat dilakukan proses ekstraksi karena pengaruh asam yang cukup kuat.
Berdasarkan hasil diatas, untuk proses demineralisasi diambil perlakuan
konsentrasi HCl 4, 5 dan 6%. dengan lama perendaman selama dua hari. Hal ini
berdasarkan konsentrasi yang sering digunakan dalam proses demineralisasi
sebesar 2-6%. Perendaman selama dua hari berdasarkan pada penelitian
sebelumnya yang telah dilakukan pada gelatin dari bahan baku tulang
kakap merah (Hadi, 2005).
Tahap selanjutnya adalah ekstraksi yaitu konversi kolagen menjadi gelatin.
Ekstraksi menggunakan aquades pada suhu 80, 85 dan 90 oC selama 4 jam. Suhu
ini berada di atas suhu susut kolagen, yaitu diatas 60 oC – 70 oC
(Gross, 1961 dalam Hadi, 2005). Jika suhu ekstraksi lebih tinggi maka akan
terjadi kerusakan protein. Pemanasan akan memecahkan struktur heliks dan ikatan
peptida kolagen menjadi rantai terpisah, yang dinamakan gelatin (Courts, 1977).
Pada tahap ekstraksi dihasilkan larutan yang berwarna kuning, dan tulang terlihat
begitu lunak. Kolagen yang telah berubah menjadi gelatin dapat dirasakan atau
Larutan yang dihasilkan selanjutnya disaring dan disimpan dalam loyang
dan dimasukkan ke dalam oven pada suhu 60 oC selama 30 jam. Pengeringan
dalam oven akan menghasilkan gelatin berbentuk lembaran.
Secara fisik gelatin yang dihasilkan larut dalam air panas dan membentuk
gel ketika didinginkan pada suhu 10 oC selama ± 17 jam. Apabila gel dipanaskan
akan cair kembali karena sifat gelatin yang reversible. Berdasarkan deMan (1997)
gelatin adalah protein larut yang diperoleh dari kolagen tidak larut. Gelatin
didefinisikan sebagai produk yang diperoleh dari jaringan kolagen hewan yang
dapat didispersi dalam air dan menunjukkan perubahan sol-gel yang reversibel
seiring perubahan suhu. Hasil gelatin dari kombinasi perlakuan dapat dilihat pada
Gambar 6.
Gambar 6. Gambar gelatin dari tulang ikan tuna albacore(Thunnus sp)
Pada gambar terlihat warna pada perlakuan HCl 6% lebih cerah
dibandingkan dengan perlakuan yang lain. pada perlakuan HCL 4% terlihat lebih
kuat dibandingkan yang lainnya, pada perlakuan HCl 6% gelatin lebih mudah
patah dibandingkan dengan yang lainnya. Perbedaan-perbedaan seperti rendemen,
4.1.2 Rendemen gelatin
Rendemen merupakan salah satu parameter yang sangat penting dalam
proses pembuatan gelatin. Perhitungan rendemen dilakukan untuk mengetahui
persentase gelatin yang dihasilkan. Semakin banyak rendemen yang diperoleh
menunjukkan semakin efisien perlakuan yang diberikan. Berdasarkan hasil
penelitian, diperoleh nilai rata-rata rendemen gelatin yang berkisar
antara 3,8% - 11,4%. Hasil rendemen dalam bentuk histogran dapat dilihat pada
Gambar 7.
Gambar 7. Histogram rata-rata rendemen gelatin tulang ikan tuna (Thunnus sp)
Dari hasil penelitian terlihat kecenderungan bahwa semakin tinggi
konsentrasi asam klorida, maka rendemen yang dihasilkan makin tinggi.
Tingginya rendemen yang dihasilkan diduga karena pengaruh jumlah ion H+ yang
menghidrolisis kolagen dari rantai triple heliks menjadi rantai tunggal yaitu
gelatin lebih banyak, semakin tinggi suhu ekstraksi akan menyebabkan kolagen
terurai menjadi gelatin lebih banyak. Kecenderungan ini mencapai batasnya
apabila ion H+ yang berlebih disertai suhu yang tinggi mendenaturasi kolagen
yang terhidrolisis. Konsentrasi asam yang berlebih dan suhu yang tinggi
menimbulkan adanya hidrolisis lanjutan sehingga sebagian gelatin turut
terdegradasi dan menyebabkan turunnya jumlah gelatin. Menurut Courts (1977),
o
o
konversi kolagen menjadi gelatin dipengaruhi oleh suhu, waktu pemanasan
dan pH.
Pada perendaman tulang dengan konsentrasi HCl 4% dan suhu
ekstraksi 80 0C menghasilkan rendemen gelatin yang paling rendah yaitu sebesar
3,8%. Hal ini diduga karena rendahnya konsentrasi HCl sehingga konversi tulang
menjadi ossein tidak sempurna, sehingga ketika dilakukan ekstraksi pada
suhu 80 oC kolagen tidak terhidrolisis sempurna menjadi gelatin.
Dari hasil analisis ragam faktorial menunjukan bahwa konsentrasi
HCl (4, 5 dan 6%), suhu ekstraksi (80 ,85 dan 90 oC), dan interaksi keduanya
berbeda nyata (sig<0.05) terhadap rendemen. Hal ini menunjukan bahwa
konsentrasi HCl, suhu ekstraksi dan interaksi keduanya mempengaruhi hasil
rendemen gelatin tulang ikan tuna.
Uji lanjut menggunakan metode Duncan menunjukan bahwa hampir
semua kombinasi perlakuan memberikan pengaruh yang berbeda terhadap hasil
rendemen gelatin. Perlakuan penambahan konsentrasi HCl 6% berbeda nyata
dengan perlakuan lain. Perlakuan dengan kombinasi konsentrasi HCl 6% dan suhu
ekstraksi 85 oC merupakan perlakuan yang terbaik.
4.1.3 Nilai pH gelatin
Nilai pH gelatin adalah derajat keasaman gelatin yang merupakan salah
satu parameter penting dalam standar mutu gelatin. Pengukuran nilai pH larutan
gelatin penting dilakukan, karena pH larutan gelatin mempengaruhi sifat-sifat
gelatin yang lainnya seperti viskositas, kekuatan gel dan akan berpengaruh juga
pada aplikasi gelatin dalam produk. pH gelatin berdasarkan mutu gelatin secara
umum diharapkan mendekati pH netral. Nilai gelatin dalam histogram dapat
dilihat pada Gambar 8.
Hasil penelitian menunjukkan bahwa nilai pH gelatin berkisar
antara 4,46-4,89. Nilai ini masih memenuhi standar gelatin tipe A (gelatin dengan
proses asam) yaitu antara 3,8-6,0 (Tourtellote, 1980).
Dari hasil uji statistik ragam faktorial semua kombinasi perlakuan
konsentrasi HCl, suhu ekstraksi dan interaksi keduanya berbeda nyata (sig<0.05).
keduanya memberikan pengaruh yang berbeda terhadap nilai pH gelatin yang
Gambar 8. Histogram pH gelatin tulang ikan tuna (Thunnus sp)
Dari uji lanjut Duncan semua kombinasi perlakuan memberikan pengaruh
yang berbeda nyata. Nilai pH yang tertinggi pada kombinasi konsentrasi HCl 4%
dengan suhu 80 oC tidak berbeda nyata dengan perlakuan kombinasi konsentrasi
HCl 6% dengan suhu ekstraksi 80 oC, tetapi keduanya memberikan pengaruh yang
berbeda dengan perlakuan lain terhadap nilai pH gelatin tulang ikan tuna.
Rendahnya nilai pH pada gelatin tulang ikan tuna diakibatkan oleh
penggunaan asam kuat ( asam klorida ). Hal ini diduga bahwa masih ada sisa-sisa
asam klorida yang digunakan pada saat proses demineralisasi masih terbawa pada
saat proses ekstraksi, yang akan mempengaruhi tingkat keasaman pada gelatin
yang dihasilkan.
Berdasarkan hasil penelitian nilai rata-rata terendah terdapat pada
kombinasi konsentrasi 6% suhu 90 oC yaitu sebesar 4,46. nilai tertinggi
sebesar 4,89 terdapat pada kombinasi HCl 4% dengan suhu 80 oC. Rendahnya
nilai pH yang dihasilkan pada penelitian ini karena masih terbawanya sisa larutan
HCl pada tulang ikan dan terbawa saat ekstraksi sehingga mempengaruhi
nilai keasaman terhadap gelatin yang dihasilkan. Untuk meningkatkan nilai pH
gelatin pada saat proses penetralan dilakukan pencucian dengan air mengalir
secara berulang-ulang sehingga tulang hampir mendekati nilai pH netral (pH 7).
o
o
Gelatin dengan pH netral akan sangat baik digunakan untuk produk
daging, farmasi, fotografi, cat, dan sebagainya. Sedangkan gelatin dengan pH
rendah akan sangat baik digunakan dalam produk juice, mayonnaise, sirop rasa
asam dan sebagainya (Nurilmala, 2004). Gelatin dari tulang ikan tuna memiliki
nilai pH berkisar antara 4,45-4,46 sehingga gelatin ini cocok untuk produk-produk
asam.
4.1.4 Viskositas gelatin
Viskositas adalah daya aliran molekul dalam suatu larutan baik dalam air,
cairan organik sederhana dan suspensi encer (deMan, 1989). Stainsby (1977),
viskositas gelatin merupakan interaksi hidrodinamik antara molekul molekul
gelatin dalam larutan. Sistem koloid dalam larutan dapat meningkat dengan cara
mengentalkan cairan sehingga terjadi absorbsi dan pengembangan koloid
(Glicksman, 1969).
Dari hasil penelitian nilai rata-rata viskositas berkisar
antara 3,5-6,8 centipoise (cP). Nilai ini masih sesuai dengan standar yang
ditetapkan oleh Tourtellote (1980) yaitu 2,0-7,5. Hasil viskositas alam bentuk
Histogram dapat dilihat pada Gambar 9.
6
Gambar 9. Histogram rata-rata viskositas gelatin tulang ikan tuna (Thunnus sp)
Nilai rata-rata terendah didapat dari kombinasi konsentrasi HCl 5%
dengan suhu ekstraksi 90 oC yaitu sebesar 3,55 cP. Secara keseluruhan semakin
o
o
meningkatnya suhu ekstraksi maka semakin rendah nilai viskositasnya. Hal ini
diduga pemanasan yang tinggi mengakibatkan terjadi hidrolisis lanjutan pada
kolagen yang sudah menjadi gelatin sehingga akan memutuskan rangkaian asam
amino sehingga viskositasnya rendah. Semakin panjang rantai asam amino gelatin
maka nilai viskositas gelatin akan semakin besar (Stainsby, 1977).
Peningkatan suhu akan mengakibatkan penurunan viskositas yang
menggambarkan berkurangnya hambatan aliran fluida. Suhu tinggi akan
memutuskan ikatan antar molekul larutan membentuk unit-unit yang lebih kecil
sehingga gaya geser yang diperlukan untuk menimbulkan laju geser akan menjadi
lebih kecil, sehingga fluida lebih mudah mengalir. Peningkatan konsentrasi gelatin
dan penurunan suhu akan meningkatkan viskositas larutan gelatin (Poppe, 1992).
Viskositas gelatin dipengaruhi oleh pH gelatin, temperatur, konsentrasi
dan teknik perlakuan seperti penambahan elektrolit lain dalam larutan gelatin.
Semakin tinggi konsentrasi gelatin maka viskositasnya akan semakin tinggi
(Stainsby, 1977). Semakin besar berat molekul maka laju aliran larutan semakin
lambat dan hal akan meningkatkan nilai viskositas. Menurut Jones (1977)
viskositas gelatin akan berpengaruh pada produk akhir suatu produk.
Berdasarkan analisis ragam faktorial didapatkan bahwa konsentrasi HCl,
suhu ekstraksi dan interaksi antara keduanya berbeda nyata (sig.< 0.05). Hal ini
menunjukkan bahwa konsentrasi HCl, suhu ekstraksi dan interaksi antara
keduanya memberikan hasil yang berbeda terhadap nilai viskositas gelatin.
Dari pengujian Duncan semua kombinasi perlakuan memberikan pengaruh
yang berbeda nyata. Nilai viskositas tertinggi didapat pada kombinasi perlakuan
konsentrasi HCl 4, 5 dan 6% dengan suhu ekstraksi 80 oC yaitu sebesar 6.8 cP,
perlakuan ini berbeda nyata dengan semua perlakuan suhu yang lain.
4.1.5 Kekuatan gel
Kekuatan gel sangat penting dalam penentuan perlakuan yang terbaik,
karena salah satu sifat penting gelatin adalah mampu mengubah cairan menjadi
gel yang bersifat reversibel. Kemampuan inilah yang menyebabkan gelatin sangat
luas penggunaannya, baik dalam bidang pangan maupun non pangan.
Kekuatan gel adalah salah satu parameter dari tekstur suatu bahan dan
gel didefinisikan sebagai besarnya kekuatan yang diperlukan oleh probe untuk menekan gel sampai pada kedalaman 4 mm dengan kecepatan 0,5 mm/s.
Dari hasil penelitian menunjukkan semakin tingginya suhu ekstraksi maka
nilai kekuatan gel semakin rendah. Hal ini disebabkan semakin tingginya suhu
ekstraksi maka akan terjadinya hidrolisis lanjutan pada kolagen yang sudah
menjadi gelatin dan menyebabkan pendeknya rantai asam amino sehingga
kekuatan gelnya rendah. Hasil kekuatan gel dalam bentuk histogram dapat dilihat
dalam Gambar 10:
Gambar 10. Kekuatan gel gelatin tulang ikan tuna (Thunnus sp)
Dari Histogram di atas dapat diketahui bahwa nilai kekuatan gel berkisar
antara 40-290 bloom. Pada suhu 80 oC didapatkan nilai rata-rata tertinggi dari
semua perlakuan suhu antara 175-290 bloom dan nilai terendah pada perlakuan
suhu 90 oC yaitu berkisar antara 40-72,5 bloom, nilai ini sangat rendah dan tidak
memenuhi syarat gelatin komersial. Menurut Tourtellote (1980) kekuatan gel
standar gelatin sebesar 75-300 bloom.
Rendahnya kekuatan gel pada suhu 90 oC diduga karena terjadinya
hidrolisis lanjutan yang menyebabkan pendeknya rantai asam amino. Rendahnya
nilai kekuatan gel pada suhu 90 oC dimungkinkan rendahnya konsentrasi gelatin
dan tingginya komponen non gelatin seperti tingginya kadar abu yang dapat
menurunkan mutu gelatin.
o
o
Menurut Glicksman (1969) kekuatan gel dan viskositas dipengaruhi oleh
asam, alkali dan panas yang akan merusak struktur gelatin sehingga tidak
terbentuk. Pembentukan gel merupakan hasil ikatan hidrogen antara molekul
gelatin sehingga dihasilkan gel semi padat yang terikat dalam komponen air.
Proses pembentukan gel juga terjadi karena adanya ikatan antar rantai polimer
sehingga membentuk struktur tiga dimensi yang mengandung pelarut di dalam
celahnya. Kerangka tiga dimensi dapat mengembang karena dapat menyerap air
secara osmosis dan mempertahankan bentuknya sehingga berubah menjadi zat
padat yang elastis jika diberi tekanan.
Lemahnya kemampuan protein dalam pengikatan air akan menurunkan
daya pembentukkan gel gelatin yang terbentuk, mengingat air adalah senyawa
pelarut yang akan digunakan untuk mengisi ruangan mikrokristal dalam
pembentukan gel. Sedikitnya jumlah protein yang mempunyai kemampuan
membentuk jaringan gel mengakibatkan gel yang terbentuk mudah pecah saat
ditekan dengan probe.
Perubahan-perubahan yang terjadi selama proses pembentukkan gel
tergantung pada kandungan asam amino spesifik yang masing-masing berbeda
pada setiap spesies, komponen protein, kemampuan pembentukan gel, kondisi
pada saat ekstraksi dan perlakuan yang diberikan.
Berdasarkan analisis ragam faktorial dapat diketahui konsentrasi HCl,
suhu ekstraksi dan interaksi keduanya berbeda nyata (sig.<0.05) hal ini
menunjukan bahwa perlakuan konsentrasi HCl, suhu ekstraksi dan interaksi antara
keduanya memberikan nilai yang berbeda terhadap kekuatan gel.
Dari uji lanjut Duncan hampir semua perlakuan memberikan pengaruh
yang berbeda terhadap nilai kekuatan gel. Perlakuan konsentrasi HCl 4% dengan
suhu 80 oC merupakan perlakuan terbaik dari kekuatan gel dan berbeda dengan
kombinasi perlakuan yang lainnya.
Dari hasil diatas kekuatan gel dan viskositas memiliki korelasi positif,
dimana semakin besar nilai kekuatan gel, maka nilai viskositas semakin tinggi.
Hal ini diduga karena kekuatan gel dan viskositas keduanya dipengaruhi asam
atau alkali, temperatur, konsentrasi gelatin dan penambahan elektrolit lain dalam
Berdasarkan hasil pengujian di atas, perlakuan perendaman HCl 4%
dengan suhu ekstraksi 80 oC mempunyai nilai pH, viskositas dan kekuatan gel
yang sangat tinggi, tetapi nilai rendemen pada kombinasi perlakuan ini rendah
sehingga tidak efisien bila dilihat dari segi ekonomisnya. Pada kombinasi
perlakuan perendaman HCl 6% dengan suhu ekstraksi 80 oC memiliki nilai
viskositas dan pH yang hampir sama dengan kombinasi HCl 4% dengan suhu
ekstraksi 80 oC, kekuatan gel yang lebih tinggi dibandingkan dengan kombinasi
perlakuan perendaman HCl 5% dengan suhu ekstraksi 80 oC. Kombinasi
perlakuan perendaman HCl 6% dengan suhu ekstraksi 80 oC memiliki nilai
rendemen yang tinggi dibandingkan kombinasi perlakuan yang lain, sehingga dari
segi ekonomis perlakuan inilah yang paling ekonomis untuk digunakan.
Kombinasi perlakuan perendaman konsentrasi HCl 6% dan suhu
ekstraksi 80 oC memenuhi kriteria standar gelatin, maka diambil perlakuan ini
sebagai perlakuan yang terbaik yang akan dilanjutkan kepada penelitian utama.
4.2.Penelitian Tahap Kedua
Pada penelitian utama dilakukan pengujian lebih lanjut sifat fisika-kimia
terhadap gelatin terbaik yaitu kombinasi perlakuan perendaman HCl 6% dengan
suhu ekstraksi 80 oC. Hasil pengujian tersebut akan dibandingkan dengan gelatin
tulang ikan kakap merah (Hadi, 2005) dan tulang ikan patin (Nurilmala, 2004).
Pengujian yang dilakukan adalah analisis proksimat gelatin yang meliputi
kadar air, kadar abu, kadar protein dan kadar lemak, analisis titik gel, titik leleh,
titik isoelektrik, derajat putih dan asam amino.
4.2.1 Analisis proksimat
Gelatin tulang ikan tuna yang terpilih dilakukan analisis proksimat yang
meliputi kadar air, kadar abu, kadar lemak dan kadar protein. Hasil analisis
proksimat gelatin tulang ikan tuna, ikan kakap merah, dan ikan patin dapat dilihat
Tabel 6. Analisis proksimat gelatin tulang ikan tuna
Air merupakan komponen penting dalam suatu bahan pangan. Air dapat
berupa komponen intrasel dan ekstrasel dari suatu bahan pangan (deMan, 1989).
Air dapat mempengaruhi penampakan, tekstur, citarasa serta mutu bahan pangan
(Winarno, 1992).
Pengujian kadar air terhadap gelatin dimaksudkan untuk mengetahui
kandungan air dalam gelatin. Kadar air gelatin akan berpengaruh terhadap
daya simpan, karena erat kaitannya dengan aktivitas metabolisme yang terjadi
selama gelatin tersebut disimpan. Peranan air dalam bahan pangan merupakan
salah satu faktor yang mempengaruhi aktivitas metabolisme seperti
aktivitas enzim, aktivitas mikroba dan aktivitas kimiawi yaitu terjadinya
ketengikan dan reaksi-reaksi non enzimatik sehingga menimbulkan perubahan
sifat-sifat organoleptik dan nilai mutunya.
Hasil pengukuran kadar air dari ketiga jenis gelatin, menunjukan gelatin
dari tulang ikan tuna memiliki nilai yang lebih rendah dibandingkan ketiganya.
Hal ini diduga disebabkan oleh gelatin tulang ikan tuna lebih banyak kehilangan
air selama proses pengeringan, dimana suhu pengeringan sebesar 60 oC
selama 30 jam, suhu ini lebih tinggi dibandingkan suhu pada gelatin tulang ikan
kakap merah dan tulang ikan patin. Pada pembuatan gelatin tulang kakap merah
dan tulang patin menggunakan suhu 40 oC – 55 oC.
Nilai kadar air dari ketiga gelatin tersebut masih memenuhi standar mutu
gelatin yaitu maksimal 16% (SNI, 1995) dan standar JECFA (2003) yaitu
tuna cenderung menyerap air jika disimpan pada suhu ruang untuk mencapai titik
keseimbangan dengan kelembaban udara lingkungan. Pada kadar air 13% dan
suhu 25 oC gelatin mencapai titik keseimbangan dengan kelembaban udara
lingkungan yaitu RH 46%. (McCormick-Goodhart dalam Rusli, 2004)
4.2.1.2 Kadar abu
Abu adalah zat organik yang tidak ikut terbakar dalam proses pembakaran
zat organik. Zat tersebut diantaranya adalah natrium, klor, kalsium, fosfor,
magnesium dan belerang (winarno, 1992). Kadar abu dalam gelatin diduga
merupakan kalsium, tingginya kalsium dapat mengakibatkan warna gelatin dalam
larutan menjadi keruh (Jones, 1977).
Analisis kadar abu pada gelatin dilakukan untuk mengetahui secara umum
kandungan mineral yang terdapat dalam gelatin. Menurut Apriyantono et al.
bahwa nilai kadar abu suatu bahan pangan menunjukan besarnya jumlah mineral
yang terkandung dalam bahan pangan tersebut.
Nilai kadar abu dari ketiga jenis gelatin berbeda-beda dimana gelatin ikan
tuna mempunyai nilai 1,93, nilai ini masih memenuhi standar SNI (1995) yaitu
maksimum 3,35% dan JECFA (2003) yaitu maksimum 2%.
Besar kecilnya kadar abu ditentukan pada saat proses demineralisasi,
semakin banyaknya kalsium yang luruh maka kadar abu akan semakin rendah.
Pada saat perendaman asam klorida akan bereaksi dengan kalsium fosfat pada
tulang hal ini akan menghasilkan garam kalsium yang larut sehingga tulang
menjadi lunak. Reaksi yang terjadi adalah:
Ca3(PO4)2 + 6HCl 3CaCl2 + 2H3PO4
4.2.1.3 Kadar lemak
Penentuan kadar lemak gelatin cukup penting, karena lemak berpengaruh
terhadap perubahan mutu gelatin selama penyimpan. gelatin yang bermutu tinggi
diharapkan memiliki kandungan lemak yang rendah bahkan diharapkan tidak
mengandung lemak. Kerusakan lemak yang utama diakibatkan oleh proses
oksidasi sehingga timbul bau dan rasa tengik, yang disebut dengan proses