ABSTRAK
PENGARUH pH TERHADAP PRODUKSI ANTIBAKTERI OLEH BAKTERI ASAM LAKTAT DARI USUS ITIK
Edelina Sinaga
Penelitian ini bertujuan untuk mengetahui pengaruh variasi pH terhadap produksi antibakteri oleh Bakteri asam laktat. Penelitian ini menggunakan Rancangan Acak Lengkap pola faktorial 3X 5 (3 isolat bakteri X 5 perlakuan pH) dengan tiga kali ulangan.Faktor pertama terdiri dari pH 4, pH 5, pH 6, pH 7, pH 8, dan faktor kedua yaitu isolat bakteri B2, B7, B8, sedangkan parameter yang dilihat yaitu zonabening. Besarnya produksi antibakteri ditentukan berdasarkan besarnya diameter zona hambat terhadap Salmonella sp. Perbedaan produksi antibakteri ditentukan berdasarkan hasil analisis ragam. Perlakuan yang berpengaruh nyata dilakukan ujL lanjut BNT pada taraf 5%. Uji potensi antibakteri berupa asam pada media dengaQ pH 7 terdapat diameter zona bening terbesar dihasilkan oleh B2 sebesar 14,3 mm, kemudian pada pH 6 oleh isolat B7 sebesar 13,7 mm dan B8 sebesar 13,6 mm, sedangkan pada pH 4 terdapat diameter zona bening terkecil dihasilkan oleh B2 sebesar 8,7 mm, kemudian pada pH 4oleh isolat B7 sebesar 8,3mm dan B8 sebesar 9,1 mm.Uji potensi antibakteri bukan asam pada pH 6 terdapat diameter zona bening yang dihasilkan oleh isolat B7 sebesar 17,2 mm dan B8 sebesar 17,1 mm, kemudian pada B2 pH 7 terdapat diameter zona bening sebesar 16,7 mm, sedangkan pada pH 4 terdapat diameter zona bening terkecil dihasilkan oleh B8 sebesar 15,1 mm, kemudian pH 6 oleh isolat B2 terdapat zona bening sebesar 12,7 mm dan pada pH 5 oleh isolat B7 sebesar 11,5 mm.
PENGARUH pH TERHADAP PRODUKSI ANTIBAKTERI OLEH BAKTERI ASAM LAKTAT DARI USUS ITIK
Oleh
EDELINA SINAGA
Skripsi
Sebagai salah satu syarat untuk mencapai gelar SARJANA SAINS
Pada Jurusan Biologi
Fakultas Matematika dan Ilmu Pengetahuan Alam
JURUSAN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
PENGARUH pH TERHADAP PRODUKSI ANTIBAKTERI OLEH BAKTERI ASAM LAKTAT DARI USUS ITIK
(Skripsi)
Oleh
EDELINA SINAGA
JURUSAN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
ii A. Latar Belakang ... 1
B. Tujuan Penelitian ... 3
C. Manfaat Penelitian ... 3
D. Kerangka Pikir ...4
E. Hipotesis ...4
II. TINJAUAN PUSTAKA A. Bakteri Asam Laktat...5
B. Antibakteri ... 6
C. Produksi Antibakteri ... 7
D. Uji Antibakteri ...11
III. METODE PENELITIAN A. Waktu dan Tempat ... 13
B. Alat dan Bahan... 13
C. Metode Penelitian ... ...14
D. Prosedur Kerja ... ...14
1. Peremajaan ...14
2. Pembuatan starter ... ...14
3. Penyiapan media produksi ...15
4. Produksi antibakteri... 15
5. Preparasi antibakteri ...15
6. Uji antibakteri denganSalmonellasp...16
5. Penentuan diameter zona hambat antibakteri... ...17
iii
IV. HASIL DAN PEMBAHASAN
A. Hasil ... ...21 B. Pembahasan... ...28
V. SIMPULAN
A. Simpulan ... ...31 B. Saran ... ...31
DAFTAR PUSTAKA
DAFTAR GAMBAR
1.Cara mengukur diameter zona bening antibakteri...17 2.Diagram alir penelitian. ...18 3. Diameter zona bening ekstrak antibakteri isolat B2, B7, dan B8
dari BAL pada variasi media pH 4 – 8...22 4. Diameter zona bening ekstrak antibakteri non asam
isolat B2, B7, dan B8 dari BAL pada variasi media pH 4 – 8...26 5. Uji antibakteri isolat B2 pada pH 7 tanpa dinetralkan terhadap
Salmonella sp. ...35 6. Uji antibakteri isolat B7 pada pH 6 tanpa dinetralkan terhadap
Salmonella sp. ...36 7. Uji antibakteri isolat B8 pada pH 6 tanpa dinetralkan terhadap
Salmonella sp. ...37 8. Uji antibakteri isolat B7 pada pH 6 tanpa dinetralkan terhadap
Salmonella sp. ...38 9. Uji antibakteri isolat B8 pada pH 6 tanpa dinetralkan terhadap
Salmonella sp. ...39 10. Uji antibakteri isolat B2 pada pH 7 tanpa dinetralkan terhadap
Salmonella sp. ...40
iv
DAFTAR TABEL
Halaman 1. Uji pengaruh pH terhadap zona hambat ...23 2. Perubahan pH media selama produksi antibakteri ...25 3. Uji Pengaruh pH terhadap zona hambat (bukan asam) ...27 4. Diameter zona bening ekstrak antibakteri berupa asam
isolat B2, B7, dan pada variasi pH 4 – 8 terhadap Salmonella sp. ...41 5. Diameter zona bening ekstrak antibakteri bukan asam
MOTTO
“
The love of ALLAH is like an Ocean!
You can see the beginning, but not the end.
”
Ora et Labora
(Pray and Work)
“
Eat Failure, and you will know the taste of success.
”
Think big and act now
Your best teacher is your last mistake.
“Behind me is infinite power”
Before me is endless possibility
Around me is boundless opportunity.”
PERSEMBAHAN
Bismillahirohmanirrohim. Dengan rahmat Allah Yang Maha Pengasih lagi
Maha Penyayang, penulis persembahahkan skripsi ini sebagai tanda bakti
dan kasih sayang yang tulus kepada :
1. Bapak dan Mama yang terkasih, atas limpahan doa dan kasih sayang
yang tidak terhingga dari kalian sehingga penulis dapat mencapai gelar
sarjana.
2. Keempat Saudaraku yaitu Kak Suryani Sinaga, Adek Irwanto
Sinaga, Adek Intan Pratiwi Sinaga , dan Adek Kelvin Agus Sinaga
yang selalu mendoakan dan memberi semangat kepada penulis.
3. Sahabat sahabatku Riska, Fadilah, Putri, Cendana, Widamay,
Nora, dan Inggit .
RIWAYAT HIDUP
Penulis dilahirkan di Propinsi Lampung, Kota Bandarlampung,
Kecamatan Panjang. Tepatnya di Panjang, pidada III pada tanggal
15 September1992, sebagai anak kedua dari lima bersaudara dari
Bapak Ardi Sinaga dan Ibu Wasni Simbolon.
Pendidikan yang ditempuh penulis yaitu TK Setia Kawan, SDN 2 Panjang Utara,
SMPN 11 Bandarlampung, SMAN 6 Bandarlampung. Penulis terdaftar sebagai
mahasiswa Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam,
Universitas Lampung melalui jalur UML pada tahun 2011.
Selama menjadi mahasiswa penulis pernah menjadi Anggota Bidang Kaderisasi
(2011/2013) di Himpunan Mahasiswa Biologi (HIMBIO). Penulis juga pernah
menjadi asisten praktikum mata kuliah Mikrobiologi Umum Prodi Pendidikan
Biologi FKIP Unila, dan Mikrobiologi Pangan dan Industri Jurusan Biologi
FMIPA Unila. Pada tahun 2014 penulis melaksanakan Kerja Praktik di
SANCAWACANA
Puji Syukur Penulis ucapkan kepada Tuhan Yang Maha Esa, karena kasih dan
karunia-Nya sehingga penulis dapat menyelesaikan skripsi ini dengan baik.
Skripsi dengan judul“PENGARUH pH TERHADAP PRODUKSI
ANTIBAKTERI OLEH BAKTERI ASAM LAKTAT DARI USUS ITIK”
adalah syarat untuk memperoleh gelar sarjana sains di Universitas Lampung.
Dalam penyusunan Skripsi ini banyak pihak yang telah membantu penulis sejak
memulai kegiatan sampai terselesaikannya skripsi ini, baik bantuan secara moril
ataupun materil, untuk itu dalam kesempatan ini penulis ingin menyampaikan
ucapan terimakasih kepada :
1. Bapak Ardi Sinaga dan Ibu Wasni Simbolon sebagai orang tua penulis, yang
telah mendidik dan membesarkan penulis dengan kasih sayang yang tiada
batas, semangat, serta doa yang selalu diucapkan tiada henti kepada Tuhan
Yesus Kristus supaya penulis dapat mencapai cita-cita.
2. Ibu Dra. Christina Nugroho Ekowati, M.Si selaku Pembimbing I atas ide,
saran, motivasi, kritik, arahan, nasihat, perhatian, dan bimbingan yang telah
3. Bapak Dr.Ir. Rudy Sutrisna, M.S., selaku Pembimbing II yang telah
memberikan bimbingan, perhatian, arahan, saran, kritik, dan membantu
dengan penuh kesabaran selama proses penyelesaian skripsi penulis.
4. Bapak Dr. Sumardi, M.Si., selaku Pembahas Akademik atas bimbingan,
arahan, saran, kritik, perhatian, dukungan yang besar selama penulis
menyelesaikan skripsi dan juga selaku Pembimbing Akademik atas
dukungan, motivasi, dan bimbingan kepada penulis selama menempuh
pendidikan di Jurusan Biologi.
5. Ibu Dra. Nuning Nurcahyani, M.Sc., selaku Ketua Jurusan Biologi FMIPA
Universitas Lampung atas dukungannya sehingga penulis dapat
menyelesaikan skripsi.
6. Bapak Prof. Suharso, Ph.D., selaku Dekan FMIPA Universitas Lampung.
7. Suryani Sinaga, Irwanto Sinaga, Intan Pratiwi Sinaga, dan Kelvin Agus
Sinaga sebagai saudara–saudaraku yang telah mendoakan dan memberi
dukungan semangat kepada penulis.
9. Riska Damayanti, Putri Dhara Yunda, Fadilah Suci atas doa, kasih sayang,
kebersamaan, dan dukungan semangat kepada penulis.
10. Bapak Wawan Abdullah Setiawan, M.Si., yang telah membantu dan
mengajarkanku tentang pH meter.
11. Widamay Fresha Tarigan, Galih Cendana Nabilasani, Wayan Hernawati,
Fajrin Nuraida, Yelbi Rizki Yulian, Ambar Prameswari, dan Try Larasati
yang sudah menjadi keluarga Microholic, terimakasih untuk kekeluargaannya
dan dukungan semangat dari kalian semua.
13. Kakak dan adik tingkat di Jurusan Biologi FMIPA Unila terimakasih atas
kekeluargaan, kebersamaan, semangat, dan dukungan yang diberikan kepada
penulis.
14. Kepada semua pihak yang tidak dapat penulis tuliskan satu per satu dengan
tulus telah membantu penulis selama menyelesaikan skripsi.
Akhir kata, penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan,
akan tetapi harapan dari penulis semoga skripsi ini dapat bermanfaat bagi kita
semua.
Bandar Lampung, 20 Oktober 2015
Penulis,
1
I. PENDAHULUAN
A. Latar Belakang
Penggunaan antibiotic pada hewan ternak dilakukan untuk pengobatan, pemacu
pertumbuhan dan meningkatkan efisiensi pakan (Bogaardet al, 2000). Sampai
saat ini, Centers Diseases Control (CDC)memperkirakan sekitar 40% antibiotik
sebagai imbuhan pakandapat memacu pertumbuhan ternak tumbuh lebih besar
dan bisa mencegah terjadinya infeksi bakteri. Pemberian antibiotik secara rutin
melalui injeksi maupun oral baik dicampurdalam pakan atau air minum
memungkinkan terjadinya residu antibiotik pada daging unggas (Donkoret al.,
2011).
Hal ini disebabkan residu antibiotik di dalam daging serta produk hewan
lainnya, dapat menimbulkan ancaman potensial terhadap kesehatan konsumen
jika dikonsumsi dalam waktu yang lama, ancaman tersebut dapat berupa (1)
aspektoksikologis, yaitu residu antibiotik dapat bersifat racun terhadap hati,
ginjal, danpusat hemopoitika, (2) aspek mikrobiologis, yaitu residu antibiotik
akan menggangu keseimbangan mikroflora di dalam saluran pencernaan, (3)
aspek imunopatologis, yaitu residu antibiotik dapat menjadi faktor pemicu
timbulnya reaksi alergi dari yang bersifat ringan sampai berat dan fatal, (4)
menimbulkan gangguan pada sistem saraf dan kerusakan jaringan (Phillipset
2
Oleh karena itu, banyak peternak yang membutuhkan pengganti antibiotik semi
sintetik yang tidak menimbulkan efek samping. Salah satunya yaitu Bakteri
Asam Laktatyang sering digunakan sebagai antibakteri alami di dalam saluran
pencernaan itik untuk membunuh atau menghambat bakteri patogen.Menurut
Evanikastri (2003) Bakteri Asam Laktat memiliki kemampuan untuk
menghasilkan zat antibakteri, dan bertahan hidup selama berada pada usus
kecil merupakan syarat bakteri asam laktat sebagai probiotik. BAL
menghasilkan salah satu antibakteri yaitu nisin yang iproduksi oleh
Lactobacillussp. Nisin merupakan antibiotik berspektrum luas yang mampu
menghambat bakteri Gram negatif ataupun bakteri Gram positif.
Penelitian Usmiatiet al(2007) menyebutkan bahwa kondisi optimum produksi
bakteriosin dariLactobacillussp. yang memiliki daya hambat representatif
pada pH 5dengan nilai daya hambatbakteriosin terhadapS.thypimuriumsebesar
638,803 mm ²/ml,E.colisebesar 623,264 mm²/ml danL.monocytogenessebesar
509,434 mm²/ml.
Salah satu faktor lingkungan yang mempengaruhi produksi antibakteri yaitu
pH di dalam saluran pencernaan itik yang bervariasi. Kemampuan BAL dalam
memproduksi antibakteri untuk membunuh atau menghambat bakteri patogen
di dalam pH yang bervariasi perlu diketahui lebih lanjut.
Beberapa Penelitian yang mendukung produksi antibakteri yaituHandayani
3
Salmonellasp. Ada 3 isolat bakteri yang menghasilkan diameter daya hambat
terbesar yaitu B7 sebesar 2,75 cm, B8 sebesar 2,68 cm dan B12 sebesar 2,65
cm.
Salah satu syarat memproduksi antibakteri dipengaruhi oleh faktor lingkungan
yaitu pH sangat berpengaruh dalam produksi antibakteri sehingga perlu
dilakukan pengkajian lebih dalam menemukan pH optimum Bakteri Asam
Laktat untuk memproduksi antibakteri yang diisolasi dari usus itik (Sutrisna,
2010) terhadap bakteri patogenSalmonellasp.
Rumusan Masalah
Dari penelitian sebelumnya belum pernah diketahui pH optimumuntuk
produksi antibakteri oleh Bakteri Asam Laktat dari usus itik. Di dalam saluran
pencernaan itik memiliki pH yang bervariasi. Untuk mengetahui pH optimum
Bakteri Asam Laktat memproduksi antibakteri untuk menghambat bakteri
patogen maka diperlukan penelitian tentang pengaruh pH terhadap produksi
antibakteri oleh BAL dari usus itik.
B. Tujuan Penelitian
Tujuan penelitian ini adalah untuk mengetahui pengaruh variasi pH terhadap
produksi antibakteri oleh isolat Bakteri asam laktat.
C. Manfaat Penelitian
Melalui penelitian ini diharapkan dapat memberikaninformasi pH optimal
4
D. Kerangka Pemikiran
Bakteri Asam Laktat merupakan bakteri probiotik hidup pada saluran
pencernaan,mampu bertahan terhadap asam lambung, dan bermutualisme
dengan tubuh inangnya.Bakteri Asam Laktat menghasilkan metabolit–
metabolit yang berfungsi sebagai senyawa antimikroba antara lain asam
organik (asam laktat dan asam asetat), bakteriosin, hidrogen peroksida.Bakteri
Asam Laktat termasuk mikroorganisme heterofermentatif yang dapathidup
pada kisaran pH yang luas (Salminenet al., 2004).
pH substrat dapat berpengaruh terhadap permeabilitas membran karenapHyang
tidak sesuai dapat mengakibatkan perubahan konfigurasi sisi aktif enzim. Hal
ini dapat menyebabkan proses penyerapan nutrisi terganggu. Kelancaran
proses penyerapan nutrisi sangat diperlukan dalam metabolisme sel, termasuk
produksi antibakteri.Permeabilitas membran akan terganggu dan proton di
dalamnya dapat menjadi inaktif sehingga mempengaruhi metabolisme yang
meyebabkan proses sintesis antibakteri terhambat (Campbell et al., 2002).
Banyaknya produksi antibakteri yang dihasilkan Bakteri Asam Laktat bisa
dilihat dengan semakin besarnya zona hambat(Ray and Bhunia, 2008).
E. Hipotesis
5
II. TINJAUAN PUSTAKA
A. Bakteri Asam Laktat
Bakteri Asam laktat (BAL) yaitu kelompok bakteri gram positif, katalase
negatif yang dapat memproduksi asam laktat dengan cara memfermentasi
karbohidrat, selnya berbentuk kokus, tersusun berpasangan atau berbentuk
rantai, tidak bergerak, tidak berspora, anaerob fakultatif, bersifat non motil dan
mesofil (Ray, 2004).
Bakteri Asam Laktat yang menghasilkan dua molekul asam laktat dari
fermentasi glukosa termasuk didalam kelompok bakteri asam laktat bersifat
homofermentatif, sedangkan Bakteri Asam Laktat yang menghasilkan satu
molekul asam laktat dan satu molekul etanol serta satu molekul karbon
dioksida dikenal dalam kelompok Bakteri asam laktat bersifat
heterofermentatif(Reddyet al., 2008).
Bakteri Asam Laktat menghasilkan antibakteri berupa asam organik,
bakteriosin, metabolit primer, hidrogen peroksida, diasetil, karbondioksida,
asetaldehid dan menurunkan pH lingkungannya dengan mengeksresikan
6
Beberapa genera yang memproduksi bakteriosin danmempunyai aktivitas
hambat besar terhadap pertumbuhan beberapa bakteri patogenadalah
Lactobacillus, Lactococcus, Streptococcus,Leuconostoc,
Pediococcus,Bifidobacteriumdan Propionibacteriumterdapat di dalam saluran
pencernaan (Usmiati, 2012).
Ada 2 kelompok BAL(Prescottet al., 2002)yaitu :
1. Bakteri homofermentatif yaitu glukosa difermentasi menghasilkan asam laktat
sebagai satu-satunya produk.Contoh :Streptococcus, Pediococcus, dan
Lactobacillus.
2.Bakteri heterofermentatif yaitu glukosa difermentasikan menghasilkan asam
laktat juga memproduksi senyawa-senyawa lainnya seperti etanol, asam asetat,
dan CO
B. Antibakteri
Antibakteri adalah senyawa yang digunakan untuk mengendalikan
pertumbuhan bakteri yang bersifat merugikan. Pengendalian pertumbuhan
mikroorganisme bertujuan untuk mencegah penyebaran penyakit dan infeksi,
membasmi mikroorganisme pada inang yang terinfeksi, dan mencegah
pembusukan serta perusakan bahan oleh mikroorganisme). Faktor-faktor yang
berpengaruh pada aktivitas zat antibakteri adalah pH, suhu stabilitas senyawa,
jumlah bakteri yang ada, lamanya inkubasi, dan aktivitas metabolisme bakteri.
Antimikroba meliputi golongan antibakteri, antimikotik, dan antiviral (Nilsson,
7
Bakteri Asam Laktatmenghasilkan senyawa bersifat antibakteri yaitu
bakteriosin yang mampu membunuh atau menghambat bakteri patogen.
Beberapa genera yang memproduksi bakteriosin yaituLactobacillus,
Lactococcus, Streptococcus, Leuconostoc, Pediococcus, Bifidobacterium dan
Propionibacteriummempunyai aktivitas hambat yang besar terhadap
pertumbuhan beberapa bakteri patogen.
Secara umum bakteriosin memenuhi syarat sebagai agen biopreservatif.
Produksi bakteriosin memiliki kondisi–kondisi tertentu yaitu pH 6–7
merupakan derajat keasaaman optimal untuk produksi bakteriosin (Gautam dan
Sharma, 2009).
Mekanisme penghambatan terhadap pertumbuhan bakteri dapat berupa yaitu
antara lain (1) kerusakan dinding sel bakteri yang menyebabkan lisis atau
penghambatan terbentuknya dinding sel pada sel yang tumbuh (2) perubahan
permeabilitas membran sitoplasma yang diakibatkan oleh senyawa fenol (3)
denaturasi sel (4) penghambatan kerja enzim di dalam sel (Gautam dan
Sharma, 2009).
C. Produksi Antibakteri
1. Sintesis asam laktat
Senyawa organik berupa asam laktat dihasilkan oleh Bakteri Asam Laktat.
Proses fermentasi asam laktat dimulai dari jalur glikolisis yang menghasilkan
asam piruvat. Asam piruvat yang terdegradasi akan mengalami degradasi
8
terdegradasi dikatalisis oleh enzim asam dehidrogenase dan direduksi NADH
untuk menghasilkan ATP dan asam laktat(Pelaez dan Orue 2010).
2. Sintesis hidrogen peroksida
Hidrogen peroksida disekresikan Bakteri Asam Laktat sebagai antibakteri yang
mampu bersifat bateriostatik maupun bakterisidal. Tahapan sintesis hidrogen
peroksida dimulai dari sitokom c oksidase, kompleks transpor elektron terminal
pada rantai transpor elektron (sitokromaa3). Zat ini mengkatalisis reduksi 4
elektronO menjadiH O.O terikat ke 2 ion logan paragmagnetik di tempat
aktif.O kemudian direduksi dalam suatu langkah 2–elektron untuk
menghasilkan peroksida, sehingga reduksi satu–elektron yang tidak
menguntungkan dapat menyebabkan terbentuknya superoksida bebas dapat
dihindari. Dua elektron tambahan menyebabkan reduksi zat antara oksigen
reaktif, sehingga terbentuk 2 molH O per molO yang direduksi. Mekanisme
ini memungkinkan reaksi cara yang sangat terkontrol tanpa adanya interaksi
antara radikal bebas oksigen dan komponen mitokondria di dekatnya.
Sebagian besar oksidase di dalam sel membentuk hidrogen peroksida H O
dan bukanH O(Ouwehand dan Vesterlund, 2004).
3. Sintesis bakteriosin
Bakteriosin tersusun dari senyawa protein sintesis bakteriosin oleh Bakteri
Asam Laktat mengikuti pola sintesis protein. Sistem ini diatur oleh plasmid
DNA ekstra kromosomal dan dipengaruhi oleh beberapa faktor terutama pH.
9
bakteriosin diatur oleh adanya gen pengkode produksi dan pengkode
immunitas (Usmiati, 2012).
Ada 3 tahapan sintesis bakteriosin (Campbell et al, 2002) yaitu sebagai berikut :
DNA polymerase berperan sebagai enzim utama dalam replikasi. DNA
polymerase mensintesis DNA baru dengan arah 5 3’. DNA polymerase tidak
bisa membuat untaian DNA baru tetapi hanya menambahkan nukleotida pada 3’
-OH yang sudah ada. Pembentukkan untai baru memerlukan primer (RNA), yaitu
tempat untuk DNA polymerase dapat menempelkan nukleotida yang pertama.
Pembentukkan untai DNA baru dimulai dari 5’ 3’ akan terjadi sintesis DNA
secara bersinambungan (Leading strand), sedangkan pada untai yang lainnya akan
terjadi sintesis DNA terputus–putus (Lagging strand) karena untaian DNA
berpasangan secara anti–paralel. Replikasi dimulai pada yang disebut ori
(Origin of replication) dan berakhir pada terminator.
1. Pada proses transkripsi terjadi sintesis mRNA (messenger RNA) dari DNA
template oleh enzim RNA polymerase. RNA polymerase berikatan dengan
bagian DNA template yang disebut promotor. RNA polymerase akan bergerak
dengan arah 5’ 3’. Transkripsi yang akan dimulai disebut initiation site
dan berakhir pada termination site.
2. Pada tahap translasi terjadi proses penerjemahan ’’bahasa’’ asam nukleat
(mRNA) menjadi ’’bahasa’’ protein oleh ribosom dan tRNA. Ribosom dan
tRNA akan berikatan pada start codon di mRNA. Pada stop codon terjadi
elongasi dan berakhir. Satu segmen DNA yang mengkode suatu protein
10
Faktor–faktor yang mempengaruhi produksi antibakteri yaitu sebagai
berikut(Salminenet al., 2004):
1. pH substrat
Bakteri Asam laktat mampu bertahan pada pH dibawah 4. pH substrat yang
sesuai diperlukan untuk produksi antibakteri. Semakin rendah pH substrat
maka banyakH yang terbebas ke dalam substrat dan menempel pada
membran. Semakin tinggi pH substrat maka banyak OH yang terbebas ke
dalam substrat dan menempel pada membran. Hal ini menyebabkan sisi aktif
enzim berubah.Dengan demikian jika pH substrat tidak sesuai akan
mengganggupermeabilitas membran dan menghambat produksi antibakteri.
pH substrat yang sesuai akan menghasilkan banyak antibakteri secara
maksimal
2. Waktu inkubasi
Waktu inkubasi disesuaikan dengan pertumbuhan bakteri dalam memproduksi
antibakteri. Bakeri Asam Laktat memerlukan waktu inkubasi optimum selama
48 jam atau 3 hari untuk memproduksi banyak antibakteri.
3. Umur bakteri
Bakteri Asam Laktat hanya dapat bertahan selama 1 bulan karena tidak
menghasilkan spora. Umur bakteri sangat mempengaruhi produksi antibakteri.
Kemungkinan Bakteri Asam Laktat yang terlalu tua akan mendakati fase
kematian. Kemampuan bakteri akan berkurang untuk menyerap nutrisi
sehingga permeabilitas membran terganggu. Umur bakteri yang sesuai dapat
11
4. Suhu
Bakteri Asam Laktat mampu bertahan pada suhu 30ºC (anaerob fakultatif).
Suhu yang sesuai akan mempengaruhi banyak produksi antibakteri. Suhu
bakteri yang sesuai dapat dilihat dengan besarnya zona hambat
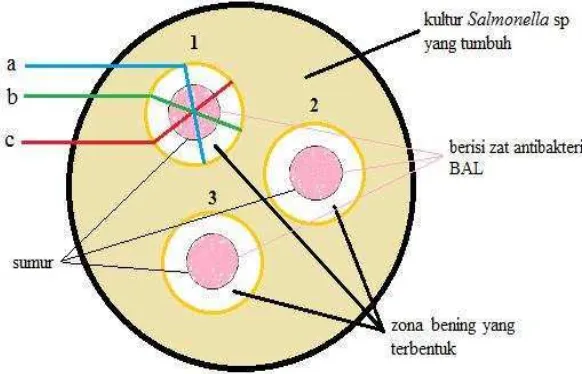
D. Uji antibakteri
Metode untuk uji antibakteri yaitu sebagai berikut :
1. Metode difusi
Metode difusi merupakan salah satu metode yang sering digunakan untuk
uji antibakteri. Metode difusi dilakukan dengan 3 cara yaitu metode
silinder, metode lubang/sumuran dan metode cakram kertas. Metode
lubang/sumuran yaitu membuat lubang pada agar
padat yang telah diinokulasi dengan bakteri. Jumlah dan letak lubang
disesuaikan dengan tujuan penelitian, kemudian lubang diinjeksikan
dengan ekstrak yang akan diuji. Setelah dilakukan inkubasi, pertumbuhan
bakteri diamati untuk melihat ada tidaknya daerah hambatan di sekeliling
lubang (Kusmayati dan Agustini, 2007).
2. Metode dilusi
Metode dilusi dibedakan menjadi dua yaitu dilusi cair (broth dilution) dan
dilusi padat (solid dilution).
a. Metode dilusi cair
Metode ini bertujuan mengukur minimum inhibitory
concencration(MH). Cara yang dilakukan adalah dengan membuat seri
12
dengan bakteri uji. Larutan uji agen antibakteri pada kadar terkecil
yang terlihat jernih tanpa adanya pertumbuhan bakteri uji ditetapkan
sebagai Kadar hambat minimum (KHM), selanjutnya dikultur ulang
pada media cair tanpa penambahan bakteri uji ataupun agen antibakteri,
dan diinkubasi selama 18-24 jam. Mediacair yang tetap terlihat jernih
setelah inkubasi ditetapkan sebagai Kadar Bunuh Minimal (KBM)
(Kusmayati dan Agustini, 2007).
b. Metode dilusi padat
Metode ini hampir sama dengan metode dilusi cair namun
13
III. METODE PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Mikrobiologi Jurusan Biologi
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
Penelitian ini dilakukan pada bulan Januari hingga Maret 2015.
B. Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini antara lain rak tabung reaksi,
mikroskop, tabung reaksi, gelas objek, tabunganaerobic jar, cawan petri,
erlenmeyer 500 ml, 250 ml, 100 ml, dan 50 ml, gelas ukur, ose, spatula,
bunsen, vortex mixer, neraca analitik, lemari es, autoklaf,laminar air flow ,
inkubator dengan suhu 37°C, mikrotube, pH meter, pipet tetes, tisu, kapas,
pinset, kertas kopi, almunium foil, dan peralatan lainnya.
Bahan-bahan yang digunakan pada penelitian ini adalah Nutrient Agar (NA),
MRS Broth, Bacterial Agar, akuades, 3 isolat bakteri dari usus itik yaitu B2,
B7, dan B8 ( koleksi Sutrisna, 2010), isolat bakteri ujiSalmonellasp. umur
14
C. Metode Penelitian
Besarnya produksi antibakteri ditentukan berdasarkan besarnya diameter zona
hambat terhadapSalmonellasp. Penelitian ini menggunakan Rancangan Acak
Lengkap pola faktorial 3X 5 (3 isolat bakteri X 5 perlakuan pH) dengan tiga
kali ulangan. Faktor pertama terdiri dari pH (4, 5, 6, 7, 8) , dan faktor kedua
terdiri dari isolat bakteri B2, B7, B8, sedangkan parameter yang dilihat yaitu
zona bening. Perbedaan produksi antibakteri ditentukan berdasarkan hasil
analisis ragam. Untuk perlakuan yang berpengaruh nyata dilakukan uji lanjut
BNT pada taraf 5%.
D. Prosedur Kerja
1. Peremajaan
Setiap isolat bakteri usus itik koleksi Sutrisna (2010) pada media cair MRS
Broth diambil 1 ml dan dibiakkan pada tabung reaksi yang berisi 9 ml
media MRS Broth steril, kemudian diinkubasi dalam anaerobic jar selama
48 jam.
2. Pembuatan starter
Bakteri yang telah diremajakan diambil sebanyak 1 ml dan dimasukkan ke
dalam 9 ml MRS Broth steril, lalu diinkubasi selama 48 jam dalam
15
3. Penyiapan zat antibakteri
3.1 MRS Broth diukur pHnya untuk dijadikan media kontrol.
3.2 20 ml MRS BrothSteril dengan ditambahkan larutan penyangga sitrat
untuk dibuat pH 4, pH 5, dan pH 6. lalu diukur dengan pH meter.
3.3 20 ml MRS Broth Steril dengan ditambahkan larutan penyangga fosfat
untuk dibuat pH 7, dan pH 8 lalu diukur dengan pH meter
4. Produksi Antibakteri
Sebanyak 4 ml starter dimasukkan ke dalam 20 ml MRS Broth Steril
pH 4, pH 5, pH 6, pH 7, dan pH 8 kemudian diinkubasi selama 48 jam.
4.1 Preparasi antibakteri
1. Antibakteri
5 ml kultur diambil sesudah inkubasi 48 jam. Kemudian masing–
masing diambil 1 ml untuk dimasukkan ke dalam microtube dan di
sentrifuge dengan kecepatan 11.000 rpm selama 10 menit. Supernatan
yang diperoleh adalah ekstrak antibakteri yang diuji dengan isolat
bakteri ujiSalmonellasp.
2 Antibakteri non asam
5 ml kultur diambil untuk diukur pHnya sesudah inkubasi 48 jam.
Sebagian diambil 5 ml kultur lalu ditambahkan NaOH 1M dengan
menggunakan pipet tetes hingga menjadi pH 7 dan sebagian diambil 5 ml
kultur lagi tetapi tidak ditambahkan NaOH . Kemudian masing–
16
sentrifuge dengan kecepatan 11.000 rpm 1selama 10 menit. Supernatan
yang diperoleh adalah ekstrak antibakteri yang diuji dengan isolat bakteri
ujiSalmonellasp.
3. Uji antibakteri denganSalmonellasp.
Sebanyak 0, ml suspensiSalmonellasp.diinokulasi secara pour plate ke
dalam cawan petri steril dan ditambahkan 20 ml media NA. Setelah
media padat dibuat sumuran dengan diameter lubang 0,7 cm. Setiap
cawan petri berisi tiga sumuran. Pada masing-masing sumuran,
dimasukkan zat antibakteri sebanyak 0,1 ml, kemudian diinkubasi dalam
inkubator suhu 40°C selama 24 jam. Kemampuan pengaruh pH terhadap
antibakteri denganSalmonellasp. ditunjukkan dengan adanya zona
bening di sekitar sumur. Semakin besar diameter zona bening yang
terbentuk, maka semakin tinggi hambat Bakteri Asam Laktat terhadap
17
4. Penentuan diameter zona hambat antibakteri (Handayani, 2014)
Diameter zona bening yang terbentuk pada setiap sumuran diukur dari
tiga sisi yang berbeda, kemudian di rata-rata (Gambar 1)
Gambar 1. cara mengukur diameter zona bening antibakteri Keterangan:
18
E. Diagram Alir Pe
1 ml
Bakteri Asam L umur 48 jam
P
Inkubasi 48 jam (anaerobic jar)
18
Penelitian
l 9 ml MRS
Broth
Laktat
4 ml
20 ml MRS Broth
PH 8 PH 7 PH 6 PH 5 PH 4 K
18
Inkubasi 48 jam (anaerobic jar)
Starter
Kontrol MRS BROTH
19
20
Bahan uj
20
Gambar 2. Diagram alir penelitian
Salmone
Inkub pada
Amati dan Catat Hasil han uji
20
onella sp.
nkubasi 24 jam pada suhu 40°C
V. KESIMPULAN
A. Kesimpulan
Berdasarkan penelitian yang telah dilakukan dapat disimpulkan bahwa :
1. Hasil penelitian menunjukkan bahwa variasi pH berpengaruhterhadap
produksi antibakteri oleh isolat B2, B7, B8 dari usus itik.
2. Isolat B2, B7, dan B8 pada pH 6–7 menunjukkan pH produksi antibakteri
terbaik.
3. Isolat B7 pada pH 6yang dinetralkan menghasilkan zona hambat terbesar
sebesar 17,2 mm, sedangkanyang tidak dinteralkan sebesar 13,70 mm. Pada
pH 4 isolat B7 yang dinetralkan menghasilkan zona hambat terkecil sebesar
14,59 sedangkan tidak dinetralkan sebesar 8,33 mm terhadapSalmonellasp.
B. Saran
Berdasarkan penelitian yang telah dilakukan maka disarankan bahwa pH 6–7
dapat digunakan sebagai pH produksi antibakteri karena mampu menghambat
Salmonelladan perlu dilakukan penelitian lanjut tentang variasi konsentrasi
antibakteri dengan pengaruh pH terhadap produksi antibakteri oleh Bakteri
✁
DAFTAR PUSTAKA
Andriani., D., W.Kurniawati. 2007. Pengaruh Asam Asetat dan Asam Laktat sebagai Antibakteri Terhadap BakteriSalmonellasp. yang Diisolasi dari Karkas Ayam.J.Seminar Nasional Teknologi Peternakan dan Veteriner 2007: 930-934.
Sweden.J. Antimicrob.Chemother. 46 (1): 146- 14.
Campbell, N.A., J.B. Reece, L.G.Mitchell. 2002.Biologi. Alih bahasa
lestari, R. et al. safitri, A., Simarmata, L., Hardani, H.W. (eds).Erlangga. Jakarta.
Cotter, P. D., and C. Hill. 2003. Surviving the Acid Test: Responses of Gram positive Bacteria to Low pH.Microbiol. Mol. Biol. Rev. 67 (3): 429-453.
Donkor, E., M. J. S. C. K Newman,. N. T. K.Tay,. D. D. E. Bannerman,and M. Olu-Taiwo. 2011. Investigation into the risk of exposure to antibiotic residues contaminating meat and egg in Ghana.FoodControl. 22:869–
873.
Gautam, N. Dan Sharma, N. 2009. Bacteriocin Safest Approach to Preserve Food Products. Indian J. Microbiol. 49(1): 204–211.
Gunawan, S.G. 2007.Farmakologi dan Terapiedisi. 5. Departemen Farmakologi dan Terapeutik. Fakultas Kedokteran, Universitas Indonesia. Jakarta. Hlm: 481-494
Bogaard, V.D., A.E., N. Bruinsma, and E.E. Stobberingh. 2000. The effect of banningavopracin on VRE carriage in the Netherlands (five abattoirs) and
Evanikastri. 2003. Isolasi dan Karakterisasi Bakteri Asam Laktat dari SampelKlinis yang Berpotensi Sebagai Probiotik. (Tesis). Institut PertanianBogor, Bogor.
✂✂
Langhout, P. 2000. New Additives for broiler chicken. Feed Mix. The International .J on feed, Nutrition and Technology9(6):24- 27.
Mojgani, N. and C. Amirnia. 2007. Kinetics of Growth and bacteriocin production in L. casei RN 78 isolated from a dairy sample in IR Iran.Int. J. Dairy sci 2(1): 1-12.
Pelaez SM, SM Orue. 2010. Feeding strategies for the control ofSalmonella in pigs.Food Sci and Technol Bulletin5(1):39-47.
Ray B & A Bhunia. 2004.Fundamental Food Microbiology. 3rdEd. Florida. CRC Press. London. New York
Ray B & A Bhunia, 2008.Fundamental of Food Microbiology Fourthed. CRC Press. London, New York.
Reddy G, M Altaf, BJ Naveena, M Venkateshwar,&EV Kumar. 2008. Amylolytic bacterial lactic acid fermentation—A review.J Elsevier-BiotechnolAdv26: 22–34.
Rostini, Iis,. 2007.Peranan Bakteri Asam Laktat (Lactobacillus
Plantarum)Terhadap Masa Simpan Filet Nila Merah pada Suhu
Rendah. Fakultas Perikanan dan Ilmu Kelautan Universitas Padjadjaran, Jatinangorng
Hendriani, R., T .S.A.F Rostinawati,. Kusuma. 2009. Penelusuran AntibakteriBakteriosin dari Bakteri Asam Laktat dalam
Yoghurt AsalKabupaten BandungBarat terhadap Staphylococcus aureusdanEscherichia coli. Laporan AkhirPenelitian Peneliti Muda (LITMUD) UNPAD. Lembaga enelitian DanPengabdian Kepada Masyarakat Universitas Padjadjaran.Jatinangor.
Kusmayati, Agustini, N.W.R. 2007. Uji Aktivitas Senyawa
48Antibakteri dariMikroalga (–53. Porphyridium cruentum).J Biod.8(1) :
Ouwehand, A.C., Vesterlund, S. 2004.Antimicrobial Components FromLactic Acid Bacteria. In Lactic Acid Bacteria: Microbiological andFunctional Aspects, ed. Salminen, S.A., Von Wright, a., ouwehand, A.C.
MarcelDekker, new york: 375-395.
Nilsson, L., Y. Chen, M.L. Chikindas, H.H. Huss, L. Gram, and T.J.
✄ ☎
Salminen, S., S. Gorbach, Y.K. Lee, dan Y. Benno. 2004. Human Studies on Probiotics : What is Scientifically Proven Today. Di dalam Salminen, S., A. von Wright, dan A. Ouwehand. (eds). 2004.Lactic Acid Bacteria :Microbiology and Functional Aspects 3nd Ed Revised and Expanded. Marcel Dekker Inc. New York.
Sari RA., R.Nofiani, P.Ardiningsih . 2012. Karakterisasi Bakteri Asam Laktat Genus Leuconostoc Dari Perkasam Ale–Ale Hasil Formulasi Skala Laboratorium. JKK1 (1): 4-20.
Surono, I.S. 2004.Probiotik Susu Fermentasi dan Kesehatan.Yayasan Pengusaha Makanan dan Minuman Seluruh Indonesia. Jakarta.
Sutrisna, R., S. Nurdjanah. 2010. Isolasi Non-starch Polysacharides Sebagai Prebiotik dan Bakteri Sebagai Probiotik Dalam Sistem Pencernaan Itik.Laporan Penelitian Hibah Bersaing. Fakultas Pertanian Universitas Lampung. Bandar Lampung.
Syabana, M. A dan Rusban T.B.. 2007.Peningkatan Daya Tahan Sate Bandeng Melalui Teknik Pengawetan Ensiling dan Asap Cair. Fakultas
Pertanian Untirta.
Sri Usmiati dan, TriMarwati. 2007. Seleksi Dan Optimasi Proses Produksi Bakteriosin Dari Lactobacillus sp. J.Pascapanen4(1) : 27- 37.
Usmiati, S. 2012. Daging Tahan Simpan dengan Bakteriosin. Warta Penelitian dan Pengembangan Pertanian34(2): 12–14.
Sujaya IN, Y.Ramona, DNM Utami, NLPSuariani, NP Widarini, KA Nocianitri ,NW Nursini. 2008a. Isolation andcharacterization of Lactic acid bacteria fromSumbawa mare milk.J Vet9:52-59.
Sujaya IN, Y.Ramona, DNM Utami, NLPSuariani, NP Widarini, KA Nocianitri ,NW Nursini.2008b. Probiotic charactrization of Lactobacillus sp. isolated from Sumbawamare milk.J Vet9:33–40.
Tensiska, 2008.Serat Makanan. Jurusan TeknologiIndustri Pangan, Fakultas Teknologi IndustriPertanian. Universitas