PEMERIKSAAN ZAT WARNA RHODAMIN B
PADA KOSMETIK JENIS PEMERAH PIPI YANG DIJUAL
DI PUSAT PASAR KOTA MEDAN
SKRIPSI
OLEH:
USWATUN HASANAH HTS NIM 050804031
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMERIKSAAN ZAT WARNA RHODAMIN B
PADA KOSMETIK JENIS PEMERAH PIPI YANG DIJUAL
DI PUSAT PASAR KOTA MEDAN
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Mencapai Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
USWATUN HASANAH HTS NIM 050804031
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
PEMERIKSAAN ZAT WARNA RHODAMIN B
PADA KOSMETIK JENIS PEMERAH PIPI YANG DIJUAL
DI PUSAT PASAR KOTA MEDAN
OLEH:
USWATUN HASANAH HTS NIM 050804031
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi
Universitas Sumatera Utara Pada Tanggal: Agustus 2010
Pembimbing I, Panitia Penguji,
Dra. Fat Aminah, M.Si., Apt. Dr. Julia Reveny, M.Si., Apt. NIP 131 569 408 NIP 130 672 239
Pembimbing II,
Dra. Fat Aminah, M.Si., Apt. NIP 131 569 408
Drs. Muchlisyam, M.Si., Apt. NIP 130 809 700
Drs. Chairul Azhar D, M.Sc., Apt NIP 131 945 348
Dra. Sudarmi, M.Si., Apt. NIP 131 283 719
Dekan,
KATA PENGANTAR
Puji dan syukur kehadirat ALLAH SWT yang telah melimpahkan rahmat,
karunia, dan ridhoNya kepada penulis sehingga penulis dapat menyelesaikan
skripsi ini dengan judul “PEMERIKSAAN ZAT WARNA RHODAMIN B
PADA KOSMETIK JENIS PEMERAH PIPI YANG DIJUAL DI PUSAT
PASAR KOTA MEDAN”. Skripsi ini diajukan sebagai salah satu syarat untuk
memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas Sumatera
Utara.
Salah satu parameter mutu kosmetik jenis pemerah pipi adalah bebas dari
penggunaan zat warna Rhodamin B, yang dinyatakan sebagai zat warna yang
dilarang penggunaannya dalam sediaan kosmetik.
Penulis menyadari bahwa skripsi ini tidak akan terwujud tanpa adanya
bantuan dari berbagai pihak, untuk itu dengan segala kerendahan dan ketulusan
hati penulis menyampaikan terima kasih yang sebesar-sebesarnya kepada:
Kedua orang tua tercinta Alm. H. Rustam Efendi Hutasuhut dan Rosmaini
Gaus dan seluruh anggota keluarga atas kasih sayang, doa, bimbingan, dan
perhatian baik moril maupun materil kepada penulis sehingga penulis dapat
berdiri tegar dalam meraih cita-cita.
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas Farmasi
Universitas Sumatera Utara.
2. Ibu Dra. Masfria, M.S., Apt., selaku Penasehat Akademik.
3. Ibu Dra. Fat Aminah, M.Si., Apt., dan Bapak Drs. Muchlisyam, M.Si., Apt.,
bimbingan, ilmu dan kesabaran serta tanggung jawab kepada penulis selama
melakukan penelitian hingga selesainya penulisan skripsi ini.
4. Ibu Dr. Julia Reveni, MSi., Apt., Bapak Drs. Chairul Azhar D, M.Sc., Apt.,
dan Ibu Dra. Sudarmi, M.Si., Apt., selaku dosen penguji yang telah
memberikan kritik, saran, dan arahan kepada penulis dalam menyelesaikan
skripsi ini.
5. Ibu Dra. Masfria, M.S., Apt., selaku kepala Laboratorium Kimia Farmasi
Kualitatif beserta staf yang telah memberikan bantuan dan fasilitas kepada
penulis selama melaksanakan penelitian.
6. Bapak Drs. Djoni Siaahan, M.M., Apt., Selaku Kepala Bidang Pangan dan
Bahan Berbahaya Balai Besar Pengawas Obat Dan Makanan RI Medan
(BPOM RI - Medan).
7. Seluruh staf pengajar dan pegawai Fakultas Farmasi yang telah memberikan
bantuan moril dan materil serta bimbingan sehingga penulis dapat
menyelesaikan skripsi ini.
Terima kasih sepenuhnya kepada abangku tersayang Zulfahmi atas segala
dukungan, do’a, dan bantuannya sehingga penulis dapat menyelesaikan skripsi ini.
Dan rekan-rekan Farmasi cuwi, kikin, anna, rina as, pipi, naya, riza, suci, winda
Tan, kak nisa,winda kir, mumu dan seluruh teman-teman Farmasi yang tidak
dapat disebutkan satu persatu khususnya stambuk 2005, untuk kebersamaan dan
dukungannya selama ini.
Penulis berharap semoga skripsi ini dapat menjadi sumbangan yang
informasi yang bermanfaat kepada masyarakat agar berhati-hati dalam memilih
kosmetik.
Penulis juga menyadari bahwa masih banyak kekurangan dalam skripsi
ini, untuk itu penulis mengharapkan kritik dan saran yang sifatnya membangun
dari para pembaca demi kesempurnaan skripsi ini.
Dengan bantuan dan dukungan yang telah penulis dapatkan akhirnya
dengan menyerahkan diri dan senantiasa memohon perlindungan Allah SWT.
Semoga amal baik dan perbuatan tersebut mendapat imbalan dari Allah SWT.
Amin Ya Robbal Alamin.
Medan, 29 Juli 2010
Penulis,
ABSTRAK
Rhodamin B merupakan pewarna yang dipakai untuk industri cat, tekstil,
dan kertas. Zat warna ini dapat menyebabkan iritasi pada saluran pernapasan dan
merupakan zat karsinogenik (dapat menyebabkan kanker) serta rhodamin dalam
konsentrasi tinggi dapat menyebabkan kerusakan pada hati. Rhodamin B merupakan zat warna sintetis berbentuk serbuk kristal, tidak berbau, berwarna
hijau, dalam bentuk larutan berwarna merah terang berpendar (berfluorescensi) .
Berdasarkan PERMENKES RI No.376/MENKES/PER/VIII/1990 dan
PERMENKES RI No. 445/MENKES/PER/V/1998 tentang zat tertentu yang
dinyatakan sebagai bahan berbahaya termasuk rhodamin B yang tidak boleh
dipergunakan untuk pemakaian kosmetik jenis lipstik, eye shadow, dan rouge.
Sehubungan dengan hasil temuan Badan Pengawas Obat dan Makanan RI
Jakarta pada tahun 2008, telah ditemukan 27 merk kosmetik yang mengandung
bahan berbahaya diantaranya adalah zat warna rhodamin B yang digunakan
sebagai salah satu pewarna termasuk juga pemerah pipi (rouge).
Berdasarkan hasil temuan Badan Pengawas Obat dan Makanan RI Jakarta
tersebut, maka penulis melakukan pemeriksaan zat warna rhodamin B pada
sediaan pemerah pipi. Pemeriksaan kualitatif rhodamin B dilakukan dengan
Kromatografi Lapis Tipis (KLT) menggunakan fase gerak n-butanol:amonia:etil
asetat (55:25:20) yang memberikan hasil positif jika menghasilkan noda berwarna
merah muda bila dilihat secara visual dan memberikan fluoresensi kuning bila
dilihat di bawah lampu UV 254 nm.
Hasil penelitian menunjukkan bahwa dari pemeriksaan kualitatif enam
belas sampel yang dianalisis yaitu Wardah (sampel kode A), Avon (sampel kode
B), Cherveen (sampel kode C), Sutsyu (sampel kode D), Chanel (sampel kode E),
MAC (sampel kode F), aubeau (sampel kode G), Louvre 1 (sampel kode H),
Cosmic (sampel kode I), Sutsyu 2 in 1 (sampel kode J), Silvie Lowrens (sampel
kode K), Louvre 2 (sampel kode L), Siellas (sampel kode M), Implora 1 (sampel
kode N), Implora 2 (sampel kode O), Aich (sampel kode P), tidak ada yang
mengandung Rhodamin B, yang berarti pemerah pipi yang di jual di sekitar Kota
Medan sudah aman dari rhodamin B.
Kata kunci :
ABSTRACT
Rhodamine-B is a coloring agent used in paint, textile, and paper industry.
This coloring agent can cause irritation in respiration tract and is a carcinogenic
(cancer-causing) substance; also, rhodamine in high concentration can cause heart
damage. Rhodamine-B is a synthetic coloring agent in crystalline powder form,
odorless, green in color, and in liquid form has bright red fluorescence.
Based on PERMENKES RI No.376/MENKES/PER/VIII/1990 and
PERMENKES RI No. 445/MENKES/PER/V/1998 about certain substances stated
as dangerous, including rhodamine-B, which must not be used in cosmetics type
lipstick, eye shadow, and rouge.
Based on the recent discovery of Badan Pengawas Obat dan Makanan RI
(Republic Indonesia’s Drug and Food Administration Bureau) Jakarta in 2008,
there were 27 cosmetic brands containing dangerous substances, among them
were rhodamine-B used as one of the coloring agent as well as rouge.
Based on mentioned discovery, the writer conducted an analysis of
rhodamine-B coloring agent in rouge preparations. The qualitative analysis of
rhodamine-B was done with Thin Layer Chromatography (TLC) method using
n-butanol:ammonia:ethyl acetate (55:25:20) as mobile phase, which gave positive
result in form of spot with pink color if observed visually, and with yellow
fluorescence if observed under 254 nm UV lamp.
The result of the research showed that from the qualitative analysis
sixteen samples analyzed, which were : Wardah (sample code A), Avon (sample
code B), Cherveen (sample code C), Sutsyu (sample code D), Chanel (sample
code E), MAC (sample code F), Aubeau (sample code G), Louvre 1 (sample code
H), Cosmic (sample code I), Sutsyu 2 in 1 (sample code J), Silvie Lowrens
(sample code K), Louvre 2 (sample code L), Siellas (sample code M), Implora 1
(sample code N), Implora 2 (sample code O), Aich (sample code P), there were no
sample containing rhodamine-B, which means that the rouge preparations sold
around Medan are safe from rhodamin B.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
HALAMAN PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... v
ABSTRAC ... vi
DAFTAR ISI ... vii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xii
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 2
1.3 Hipotesis ... 2
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Kosmetik ... 4
2.1.1 Pengertian Kosmetik ... 4
2.1.2 Penggolongan Kosmetik ... 5
2.1.3 Persyaratan Kosmetik ... 8
2.2.1 Persyaratan Kosmetik Dekoratif ... 8
2.2.2 Pembagian Kosmetik Dekoratif ... 9
2.2.3 Peranan Zat Pewarna dalam Kosmetik Dekoratif ... 9
2.2.4 Pemerah pipi ... 11
2.3 Rhodamin B ... 12
2.3.1 Struktur Molekul Rhodamin B ... 12
2.3.2 Gambar Absorpsi Rhodamin B dalam Pelarut Etanol pada λ 542.72 nm ... 12
2.3.3 Tanda-tanda Umum Terpapar Rhodamin B ... 15
2.4 Kromatografi Lapis Tipis ... 16
BAB III METODOLOGI PENELITIAN ... 20
3.1 Alat-alat ... 20
3.2 Bahan-bahan ... 20
3.3 Metode Pengambilan Sampel ... 21
3.4 Prosedur Penelitian ... 21
3.4.1 Penentuan Kualitatif Rhodamin B ... 21
3.4.1.1 Pembuatan Larutan Uji (A) ... 21
3.4.1.2 Pembuatan Larutan Baku (B) ... 21
3.4.1.3 Pembuatan Larutan Campuran (C) ... 22
3.4.1.4 Identifikasi Sampel ... 22
3.4.2 Penentuan Kuantitatif Rhodamin B ... 23
3.4.2.1 Pembuatan Larutan Induk Baku Rhodamin B ... 23
3.4.2.1.1 Larutan Induk Baku I Rhodamin B ... 23
3.4.2.2 Penentuan Panjang Gelombang Maksimum
Rhodamin B ... 23
3.4.2.3 Penentuan Operating Time ... 23
3.4.2.4 Penentuan Linieritas Kurva Kalibrasi Larutan Rhodamin B ... 24
3.4.2.5 Penetapan Kadar Rhodamin B Pada Sampel ... 24
BAB IV HASIL DAN PEMBAHASAN ... 25
4.1 Analisis Kualitatif Rhodamin B Pada Sampel ... 25
4.2. Panjang Gelombang Maksimum Larutan Rhodamin B ... 28
4.3. Penentuan Operating Time ... 29
4.4. Linieritas Kurva Kalibrasi Larutan Rhodamin B ... 29
BAB V KESIMPULAN DAN SARAN ... 31
5.1 Kesimpulan ... 31
5.2 Saran ... 31
DAFTAR PUSTAKA ... 32
DAFTAR TABEL
Halaman
Tabel 2.1. Zat Warna Yang Dinyatakan Sebagai Bahan Berbahaya ... 12
Tabel 4.1. Hasil Analisa Kualitatif Rhodamin B Pada Sampel ... 25
DAFTAR GAMBAR
Halaman
Gambar 4.1. Kurva Resapan Rhodamin B ... 28
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Contoh Perhitungan Harga Rf ... 34
Lampiran 1. Penentuan Operating Time ... 35
Lampiran 2. Data Kurva Kalibrasi Larutan Rhodamin B Pada Panjang Gelombang 544 nm ... 36
Lampiran 3. Perhitungan Persamaan Regresi ... 37
Lampiran 4. Alat Spektrofotometer ... 38
Lampiran 5. Alat Timbangan Digital ... 29
Lampiran 6. Gambar Sampel ... 40
Lampiran 7. Gambar Plat KLT 20 x 20 ... 46
Lampiran 8. Gambar Chamber ... 50
Lampiran 9. Sertifikat Pengujian BADAN POM ... 51
Lampiran 10. Metode Analisis Kosmetik ... 52
ABSTRAK
Rhodamin B merupakan pewarna yang dipakai untuk industri cat, tekstil,
dan kertas. Zat warna ini dapat menyebabkan iritasi pada saluran pernapasan dan
merupakan zat karsinogenik (dapat menyebabkan kanker) serta rhodamin dalam
konsentrasi tinggi dapat menyebabkan kerusakan pada hati. Rhodamin B merupakan zat warna sintetis berbentuk serbuk kristal, tidak berbau, berwarna
hijau, dalam bentuk larutan berwarna merah terang berpendar (berfluorescensi) .
Berdasarkan PERMENKES RI No.376/MENKES/PER/VIII/1990 dan
PERMENKES RI No. 445/MENKES/PER/V/1998 tentang zat tertentu yang
dinyatakan sebagai bahan berbahaya termasuk rhodamin B yang tidak boleh
dipergunakan untuk pemakaian kosmetik jenis lipstik, eye shadow, dan rouge.
Sehubungan dengan hasil temuan Badan Pengawas Obat dan Makanan RI
Jakarta pada tahun 2008, telah ditemukan 27 merk kosmetik yang mengandung
bahan berbahaya diantaranya adalah zat warna rhodamin B yang digunakan
sebagai salah satu pewarna termasuk juga pemerah pipi (rouge).
Berdasarkan hasil temuan Badan Pengawas Obat dan Makanan RI Jakarta
tersebut, maka penulis melakukan pemeriksaan zat warna rhodamin B pada
sediaan pemerah pipi. Pemeriksaan kualitatif rhodamin B dilakukan dengan
Kromatografi Lapis Tipis (KLT) menggunakan fase gerak n-butanol:amonia:etil
asetat (55:25:20) yang memberikan hasil positif jika menghasilkan noda berwarna
merah muda bila dilihat secara visual dan memberikan fluoresensi kuning bila
dilihat di bawah lampu UV 254 nm.
Hasil penelitian menunjukkan bahwa dari pemeriksaan kualitatif enam
belas sampel yang dianalisis yaitu Wardah (sampel kode A), Avon (sampel kode
B), Cherveen (sampel kode C), Sutsyu (sampel kode D), Chanel (sampel kode E),
MAC (sampel kode F), aubeau (sampel kode G), Louvre 1 (sampel kode H),
Cosmic (sampel kode I), Sutsyu 2 in 1 (sampel kode J), Silvie Lowrens (sampel
kode K), Louvre 2 (sampel kode L), Siellas (sampel kode M), Implora 1 (sampel
kode N), Implora 2 (sampel kode O), Aich (sampel kode P), tidak ada yang
mengandung Rhodamin B, yang berarti pemerah pipi yang di jual di sekitar Kota
Medan sudah aman dari rhodamin B.
Kata kunci :
ABSTRACT
Rhodamine-B is a coloring agent used in paint, textile, and paper industry.
This coloring agent can cause irritation in respiration tract and is a carcinogenic
(cancer-causing) substance; also, rhodamine in high concentration can cause heart
damage. Rhodamine-B is a synthetic coloring agent in crystalline powder form,
odorless, green in color, and in liquid form has bright red fluorescence.
Based on PERMENKES RI No.376/MENKES/PER/VIII/1990 and
PERMENKES RI No. 445/MENKES/PER/V/1998 about certain substances stated
as dangerous, including rhodamine-B, which must not be used in cosmetics type
lipstick, eye shadow, and rouge.
Based on the recent discovery of Badan Pengawas Obat dan Makanan RI
(Republic Indonesia’s Drug and Food Administration Bureau) Jakarta in 2008,
there were 27 cosmetic brands containing dangerous substances, among them
were rhodamine-B used as one of the coloring agent as well as rouge.
Based on mentioned discovery, the writer conducted an analysis of
rhodamine-B coloring agent in rouge preparations. The qualitative analysis of
rhodamine-B was done with Thin Layer Chromatography (TLC) method using
n-butanol:ammonia:ethyl acetate (55:25:20) as mobile phase, which gave positive
result in form of spot with pink color if observed visually, and with yellow
fluorescence if observed under 254 nm UV lamp.
The result of the research showed that from the qualitative analysis
sixteen samples analyzed, which were : Wardah (sample code A), Avon (sample
code B), Cherveen (sample code C), Sutsyu (sample code D), Chanel (sample
code E), MAC (sample code F), Aubeau (sample code G), Louvre 1 (sample code
H), Cosmic (sample code I), Sutsyu 2 in 1 (sample code J), Silvie Lowrens
(sample code K), Louvre 2 (sample code L), Siellas (sample code M), Implora 1
(sample code N), Implora 2 (sample code O), Aich (sample code P), there were no
sample containing rhodamine-B, which means that the rouge preparations sold
around Medan are safe from rhodamin B.
BAB I PENDAHULUAN 1.1 Latar Belakang
Kosmetik adalah bahan atau campuran bahan untuk digosokkan,
diletakkan, dituangkan, dipercikkan atau disemprotkan pada, dimasukkan
kedalam, dipergunakan pada badan atau bagian badan manusia dengan maksud
untuk membersihkan, memelihara, menambah daya tarik atau mengubah rupa, dan
tidak termasuk golongan obat (Wasitaatmadja, 1997).
Pemerah pipi (rouge) adalah sediaan kosmetik yang digunakan untuk
memberi warna bayangan merah wajah, zat warna yang digunakan tidak larut
dalam air, seperti misalnya besi oksida (Lesmono, M.B, dkk, 1985).
Berdasarkan hasil penelitian Badan Pengawas Obat dan Makanan RI
(BPOM RI) pada tahun 2008 telah ditemukan 27 merek kosmetik yang
mengandung bahan berbahaya yang diantaranya adalah rhodamin B (Anonimb,
2008).
Rhodamin B adalah zat warna sintetis yang biasa digunakan untuk
pewarnaan kertas, tekstil atau tinta. Zat tersebut dapat menyebabkan iritasi pada
kulit dan saluran pernafasan serta merupakan zat yang bersifat karsinogenik
(dapat menyebabkan kanker). Rhodamin B dalam konsentrasi tinggi dapat
menyebabkan kerusakan pada hati (lever) (Anonima, 2006).
Rhodamin B dengan metode Kromatografi Lapis Tipis akan memberikan
fluoresensi warna kuning jika dilihat di bawah lampu Ultra Violet 254 nm dan
berwarna merah muda jika dilihat secara visual. Penentuan kadar rhodamin B
Kromatografi Cair Kinerja Tinggi dan Spektrofotometri Sinar Tampak. Dalam
penelitian ini dilakukan pemeriksaan rhodamin B secara Kromatografi Lapis Tipis
dan Spektrofotometri Sinar Tampak (Ditjen POM, 1997).
Hasil penelitian Badan Pengawas Obat dan Makanan RI beberapa merek
pemerah pipi mengandung rhodamin B antara lain adalah merek KAI (tidak ada
nama produsen), Noubeier (produksi China), dan Cameo Make Up Kit 3 in 1
(produksi China). Dari survey yang dilakukan di pusat pasar kota Medan, ketiga
merek tersebut tidak ditemukan lagi sehingga peneliti mencurigai produsen dari
kosmetik tersebut mengganti merek dengan bahan yang sama. Selain itu, masih
terdapat pemerah pipi yang dijual dengan harga yang sangat murah, dimana pada
kemasannya menggunakan bahasa selain bahasa Indonesia dan tidak memiliki
nomor bats dan nomor register.
Berdasarkan hal tersebut peneliti tertarik untuk memeriksa rhodamin B
pada pemerah pipi yang beredar di masyarakat khususnya kota Medan.
1.2 Perumusan masalah 1. Apakah kosmetik jenis pemerah pipi bermerek yang dijual di pusat pasar
kota Medan mengandung rhodamin B.
2. Berapakah kadar rhodamin B yang disalahgunakan pemakaiannya pada
kosmetik jenis pemerah pipi.
a. Hipotesis
H0 diterima jika :
1. Pemerah pipi yang beredar di pusat pasar kota Medan masih ada yang
2. Terdapat sejumlah tertentu rhodamin B yang digunakan pada pemerah
pipi.
1.4 Tujuan Penelitian
1. Melakukan uji kualitatif rhodamin B pada pemerah pipi dengan
menggunakan metode Kromatografi Lapis Tipis (KLT).
2. Melakukan penetapan kadar rhodamin B pada pemerah pipi dengan
menggunakan metode Spektrofotometri Sinar Tampak.
1.5 Manfaat Penelitian
Memberikan informasi kepada masyarakat dan instansi yang berwenang
tentang kandungan rhodamin B dalam kosmetik jenis pemerah pipi yang dijual di
BAB II
TIJAUAN PUSTAKA
2.1 Kosmetik
2.1.1 Pengertian Kosmetik
Menurut Wall dan Jellinek, 1970, kosmetik dikenal manusia sejak
berabad-abad yang lalu. Pada abad ke-19, pemakaian kosmetik mulai mendapat
perhatian, yaitu selain untuk kecantikan juga untuk kesehatan. Perkembangan
ilmu kosmetik serta industrinya baru dimulai secara besar-besaran pada abad
ke-20 (Tranggono, ke-2007).
Kosmetik berasal dari kata kosmein (Yunani) yang berarti ”berhias”.
Bahan yang dipakai dalam usaha untuk mempercantik diri ini, dahulu diramu dari
bahan-bahan alami yang tedapat disekitarnya. Sekarang kosmetik dibuat manusia
tidak hanya dari bahan alami tetapi juga bahan buatan untuk maksud
meningkatkan kecantikan (Wasitaatmadja, 1997).
Sejak semula kosmetik merupakan salah satu segi ilmu pengobatan atau
ilmu kesehatan, sehingga para pakar kosmetik dahulu adalah juga pakar
kesehatan; seperti para tabib, dukun, bahkan penasehat keluarga istana. Dalam
perkembangannya kemudian, terjadi pemisahan antara kosmetik dan obat, baik
dalam hal jenis, efek, efek samping, dan lainnya (Wasitaatmadja, 1997).
Kosmetik adalah sediaan atau paduan bahan yang siap untuk digunakan
pada bagian luar badan seperti epidermis, rambut, kuku, bibir, gigi, dan rongga
mulut antara lain untuk membersihkan, menambah daya tarik, mengubah
badan tetapi tidak dimaksudkan untuk mengobati atau menyembuhkan suatu
penyakit (Tranggono, 2007).
2.1.2 Penggolongan Kosmetik
Penggolongan kosmetik terbagi atas beberapa golongan, yaitu :
a. Menurut Peraturan Menteri Kesehatan RI, kosmetik dibagi ke dalam 13
preparat (Tranggono, 2004) :
1. Preparat untuk bayi, misalnya minyak bayi, bedak bayi, dan lain-lain.
2. Preparat untuk mandi, misalnya sabun mandi, bath capsule, dan lain-lain.
3. Preparat untuk mata, misalnya maskara, eye-shadow, dan lain-lain.
4. Preparat wangi-wangian, misalnya parfum, toilet water, dan lain-lain.
5. Preparat untuk rambut, misalnya cat rambut, hair spray, dan lain-lain.
6. Preparat pewarna rambut, misalnya cat rambut, dan lain-lain.
7. Preparat make-up (kecuali mata), misalnya bedak, lipstik, dan lain-lain.
8. Preparat untuk kebersihan mulut, misalnya pasta gigi, mouth washes, dan
lain-lain.
9. Preparat untuk kebersihan badan, misalnya deodorant, dan lain-lain.
10.Preparat kuku, misalnya cat kuku, losion kuku, dan lain-lain.
11.Preparat perawatan kulit, misalnya pembersih, pelembab, pelindung, dan
lain-lain.
12.Preperat cukur, misalnya sabun cukur, dan lain-lain.
13.Preparat untuk suntan dan sunscreen, misalnya sunscreen foundation, dan
b. Penggolongan kosmetik menurut cara pembuatan (Tranggono, 2004) sebagai
berikut:
1. Kosmetik modern, diramu dari bahan kimia dan diolah secara modern
(termasuk di antaranya adalah cosmedic).
2. Kosmetik tradisional:
a. Betul-betul tradisional, misalnya mangir, lulur, yang dibuat dari bahan
alam dan diolah menurut resep dan cara yang turun-temurun.
b. Semi tradisional, diolah secara modern dan diberi bahan pengawet
agar tahan lama.
c. Hanya namanya yang tradisional, tanpa komponen yang benar-benar
tradisional dan diberi warna yang menyerupai bahan tradisional.
c. Penggolongan kosmetik menurut kegunaannya bagi kulit:
1. Kosmetik perawatan kulit (skin care cosmetic)
Jenis ini perlu untuk merawat kebersihan dan kesehatan kulit. Termasuk di
dalamnya:
a. Kosmetik untuk membersihkan kulit (cleanser): sabun, cleansing
cream, cleansing milk, dan penyegar kulit (freshener).
b. Kosmetik untuk melembabkan kulit (mosturizer), misalnya mosturizer
cream, night cream, anti wrinkel cream.
c. Kosmetik pelindung kulit, misalnya sunscreen cream dan sunscreen
foundation, sun block cream/lotion.
d. Kosmetik untuk menipiskan atau mengampelas kulit (peeling),
misalnya scrub ceram yang berisi butiran-butiran halus yang berfungsi
2. Kosmetik riasan (dekoratif atau make-up)
Jenis ini diperlukan untuk merias dan menutup cacat pada kulit sehingga
menghasilkan penampilan yang lebih menarik serta menimbulkan efek
psikologis yang baik, seperti percaya diri (self confident). Dalam kosmetik
riasan, peran zat warna dan pewangi sangat besar. Kosmetik dekoratif
terbagi menjadi 2 golongan (Tranggono, 2004), yaitu:
a. Kosmetik dekoratif yang hanya menimbulkan efek pada permukaan
dan pemakaian sebentar, misalnya lipstik, bedak, pemerah pipi, eyes
shadow, dan lain-lain.
b. Kosmetik dekoratif yang efeknya mendalam dan biasanya dalam baru
lama baru luntur, misalnya kosmetik pemutih kulit, cat rambut,
pengeriting rambut, dan preparat penghilang rambut.
d. Berdasarkan bahan dan penggunaannya serta maksud evaluasi produk kosmetik
dibagi menjadi 2 golongan (Ditjen POM, 2004):
1. Kosmetik golongan I adalah:
a. Kosmetik yang digunakan untuk bayi
b. Kosmetik yang digunakan disekitar mata, rongga mulut dan mukosa
lainnya
c. Kosmetik yang mengandung bahan dengan persyaratan kadar dan
penandaan
d. Kosmetik yang mengandung bahan dan fungsinya belum lazim serta
belum diketahui keamanan dan kemanfaatannya.
2. Kosmetik golongan II adalah kosmetik yang tidak termasuk ke dalam
2.1.3 Persyaratan Kosmetik
Kosmetik yang diproduksi dan atau diedarkan harus memenuhi
persyaratan sebagai berikut:
a. Menggunakan bahan yang memenuhi standar dan persyaratan mutu serta
persyaratan lain yang ditetapkan.
b. Diproduksi dengan menggunakan cara pembuatan kosmetik yang baik.
c. Terdaftar pada dan mendapat izin edar dari Badan Pengawas Obat dan
Makanan RI (BPOM RI).
2.2 Kosmetik Dekoratif
Kekhasan kosmetik dekoratif adalah bahwa kosmetik ini bertujuan
semata-mata untuk mengubah penampilan, yaitu agar tampak lebih cantik dan
noda-noda atau kelainan pada kulit tertutupi. Kosmetik dekoratif tidak perlu
menambah kesehatan kulit. Kosmetik ini dianggap memadai jika tidak merusak
kulit (Tranggono, 2007).
2.2.1 Persyaratan Kosmetik Dekoratif
Persyaratat untuk kosmetik dekoratif antara lain adalah (Tranggono, 2007):
a. Warna yang menarik.
b. Bau harum yang menyenangkan.
c. Tidak lengket.
d. Tidak menyebabkan kulit tampak berkilau.
2.2.2 Pembagian Kosmetik Dekoratif
Kosmetik dekoratif dapat dibagi dalam dua golongan, yaitu (Tranggono,
2007):
1. Kosmetik dekoratif yang hanya menimbulkan efek pada permukaan dan
pemakaiannya sebentar, misalnya bedak, lipstik, pemerah pipi, eye shadow,
dan lain-lain.
2. Kosmetik dekoratif yang efeknya mendalam dan biasanya dalam waktu lama
baru luntur, misalnya kosmetik pemutih kulit, cat rambut, dan pengeriting
rambut.
2.2.3 Peranan Zat Pewarna dalam Kosmetik Dekoratif
Dalam kosmetik dekoratif, zat pewarna memegang peranan sangat besar.
Zat warna untuk kosmetik dekoratif berasal dari berbagai kelompok :
1. Zat warna alam yang larut.
Zat ini sekarang sudah jarang dipakai dalam kosmetik. Sebetulnya dampak
zat alam ini pada kulit lebih baik dari pada zat warna sintetis, tetapi kekuatan
pewarnaanya relatif lemah, tak tahan cahaya, dan relatif mahal. Misalnya carmine
zat warna merah yang diperoleh dari dari tubuh serangga coccus cacti yang
dikeringkan , klorofil daun-daun hijau, henna yang diekstraksi dari daun Lawsonia
inermis, carotene zat warna kuning.
2. Zat warna sintetis yang larut.
Zat warna sintetis pertama kali disintetis dari anilin, sekarang benzena,
toluena, anthracene yang berfungsi sebagai produk awal bagi kebanyakan zat
warna. Sifat-sifat zat warna sintetis yang perlu diperhatikan antara lain :
b. Harus bisa larut dalam air, alkohol, minyak, atau salah satunya. Yang larut air
untuk emulsi O/W dan larut minyak untuk emulsi W/O. Yang larut air hampir
selalu juga larut dalam alkohol encer, gliserol, dan glikol. Yang larut minyak
juga larut dalam benzena, karbon tetraklorida, dan pelarut organik lainnya,
kadang-kadang juga dalam alkohol tinggi. Tidak pernah ada zat warna yang
sekaligus larut dalam air dan minyak.
c. Sifat yang berhubungan dengan pH. Beberapa zat warna hanya larut dalam pH
asam, lainnya hanya dalam pH alkalis.
d. Kelekatan pada kulit atau rambut. Daya lekat berbagai zat warna pada kulit dan
rambut barbeda-beda. Terkadang kita memerlukan daya lekat besar seperti cat
rambut, namun terkadang kita menghindarinya misalnya untuk pemerah pipi.
e. Toksisitas. Yang toksis harus dihindari, tetapi ada derajat keamanannya.
3. Pigmen alam.
Pigmen alam adalah pigmen warna pada tanah yang memang terdapat
secara alamiah, misalnya aluminium silikat, yang warnanya tergantung pada
kandungan besi oksida atau mangan oksidanya (misalnya kuning, coklat, merah
bata, coklat tua). Zat warna ini murni, sama sekali tidak berbahaya, penting untuk
mewarnai bedak-krim dan make-up sticks. Warnanya tidak seragam, tergantung
asalnya, dan pada pemanasan kuat menghasilkan pigmen warna baru.
4. Pigmen sintetis.
Dewasa ini besi oksida sintetis sering menggantikan zat warna alam.
Warnanya lebih intens dan lebih terang. Pilihan warnanya antara lain kuning,
coklat sampai merah, dan macam-macam violet.
Pigmen sintetis putih seperti zinc oxida dan titanium oxida termasuk dalam
memainkan satu peran dalam pewarnaan kosmetik dekoratif, tetapi juga dalam
preparat kosmetik dan farmasi lainnya.
Banyak pigmen sintetis yang tidak boleh dipakai dalam preparat kosmetik
karena toksis, misalnya kadmiun sulfat dan cupri sulfat.
2.2.4 Pemerah pipi
Pemerah pipi adalah sediaan kosmetik yang digunakan untuk mewarnai
pipi dengan sentuhan artistik sehingga dapat meningkatkan estetika dalam tatarias
wajah (Depkes RI, 1985).
Pemerah pipi dibuat dalam berbagai corak warna yang bervariasi mulai
dari warna merah jambu hingga merah tua. Pemerah pipi konvensional lazim
mengandung pigmen merah atau merah kecoklatan dengan kadar tinggi. Pemerah
pipi yang mengandung pigmen kadar rendah digunakan sebagai pelembut warna
atau pencampur untuk memperoleh efek yang menyolok.
Pemerah pipi dapat digunakan langsung dengan melekatkan pada kulit
pipi, tetapi dalam banyak hal lebih baik digunakan setelah sediaan alas rias, baik
sebelum maupun sesudah menggunakan bedak (Depkes RI, 1985).
Contoh formula pemerah pipi bubuk kompak
Kaolin ringan 50
Kalsium karbonat endap 50
Magnesium karbonat 50
Seng stearat 50
Talek 750
Pigmen 50
Parfum 2,0
Zat pengikat : isopropil miristat sama banyak
2.3 Rhodamin B
2.3.1 Struktur molekul rhodamin B
(Windholz, 1989)
2.3.2 Gambar Absorpsi Rhodamin B dalam Pelarut Etanol pada λ 542.75 nm.
(Aldrich, 1992)
Nama umum : Rumus Bangun Rhodamin B
Nama Kimia :
N-[9-(carboxyphenyl)-6-(diethylamino)-3H-xanten-3-ylidene]-N-ethylethanaminium chlorida
Nama Lazim : Tetraethylrhodamine; D&C Red No. 19; Rhodamine B chlorida;
C.I. Basic Violet 10; C.I. 45170
BM : 479
Pemerian : Hablur hijau atau serbuk ungu kemerahan
Kelarutan : Sangat mudah larut dalam air menghasilkan larutan merah
kebiruan dan berfluoresensi kuat jika diencerkan. Sangat mudah
larut dalam alkohol; sukar larut dalam asam encer dan dalam
larutan alkali. Larutan dalam asam kuat membentuk senyawa
dengan kompleks antimon berwarna merah muda yang larut
dalam isopropil eter (Budavari, 1996).
Penggunaan : Sebagai pewarna untuk sutra, katun, wol, nilon, kertas, tinta,
sabun, pewarna kayu, bulu, dan pewarna untuk keramik China
(Budavari, 1996).
Penggunaan rhodamin B pada makanan dan kosmetik dalam waktu lama
akan mengakibatkan kanker dan gangguan fungsi hati. Namun demikian, bila
terpapar rhodamin B dalam jumlah besar maka dalam waktu singkat akan terjadi
gejala akut keracunan rhodamin B. Bila rhodamin B tersebut masuk melalui
makanan akan mengakibatkan iritasi pada saluran pencernaan dan mengakibatkan
gejala keracunan dengan urine yang berwarna merah maupun merah muda. Selain
melalui makanan ataupun kosmetik, rhodamin B juga dapat mengakibatkan
gangguan kesehatan, jika terhidup terjadi iritasi pada saluran pernafasan. Mata
yang terkena rhodamin B juga akan mengalami iritasi yang ditandai dengan mata
kemerahan dan timbunan cairan atau udem pada mata. Jika terpapar pada bibir
dapat menyebabkan bibir akan pecah-pecah, kering, dan gatal. Bahkan, kulit bibir
Daftar tabel Peraturan Menteri Kesehatan RI No. 239/ MENKES/ PER/ V/
1985 tentang zat warna yang dinyatakan sebagai bahan berbahaya adalah sebagai
[image:30.595.121.488.183.680.2]berikut:
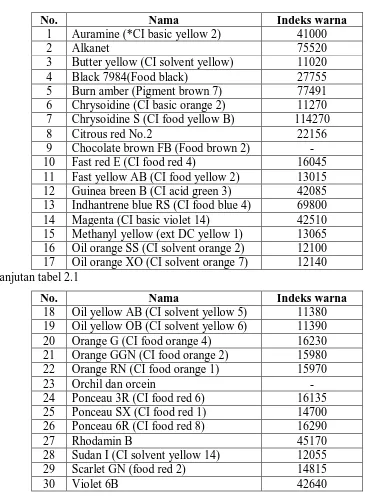
Tabel 2.1. Zat Warna Yang Dinyatakan Sebagai Bahan Berbahaya
No. Nama Indeks warna
1 Auramine (*CI basic yellow 2) 41000
2 Alkanet 75520
3 Butter yellow (CI solvent yellow) 11020 4 Black 7984(Food black) 27755 5 Burn amber (Pigment brown 7) 77491 6 Chrysoidine (CI basic orange 2) 11270 7 Chrysoidine S (CI food yellow B) 114270
8 Citrous red No.2 22156
9 Chocolate brown FB (Food brown 2) - 10 Fast red E (CI food red 4) 16045 11 Fast yellow AB (CI food yellow 2) 13015 12 Guinea breen B (CI acid green 3) 42085 13 Indhantrene blue RS (CI food blue 4) 69800 14 Magenta (CI basic violet 14) 42510 15 Methanyl yellow (ext DC yellow 1) 13065 16 Oil orange SS (CI solvent orange 2) 12100 17 Oil orange XO (CI solvent orange 7) 12140 Lanjutan tabel 2.1
No. Nama Indeks warna
18 Oil yellow AB (CI solvent yellow 5) 11380 19 Oil yellow OB (CI solvent yellow 6) 11390 20 Orange G (CI food orange 4) 16230 21 Orange GGN (CI food orange 2) 15980 22 Orange RN (CI food orange 1) 15970
23 Orchil dan orcein -
24 Ponceau 3R (CI food red 6) 16135 25 Ponceau SX (CI food red 1) 14700 26 Ponceau 6R (CI food red 8) 16290
27 Rhodamin B 45170
28 Sudan I (CI solvent yellow 14) 12055 29 Scarlet GN (food red 2) 14815
30 Violet 6B 42640
− Jika tertelan dapat menimbulkan iritasi pada saluran pencernaan dan
menimbulkan gejala keracunan serta air seni berwarna merah atau merah
muda.
− Jika terkena kulit dapat menimbulkan iritasi pada kulit.
− Jika terkena mata dapat menimbulkan iritasi pada mata, mata
kemerahan, oedema pada kelopak mata.
− Jika terhirup dapat menimbulkan iritasi pada saluran pernafasan.
(Rachdie, 2006).
2.4Kromatogarafi Lapis Tipis
Kromatografi adalah suatu nama yang diberikan untuk teknik pemisahan
tertentu. Cara yang asli telah diketengahkan pada tahun 1903 oleh Tswett, ia telah
menggunakannya untuk memisahkan senyawa-senyawa yang berwarna, dan nama
kromatografi diambil dari senyawa yang berwarna. Meskipun demikian
pembatasan untuk senyawa-senyawa yang berwarna tak lama dan hampir
kebanyakan pemisahan-pemisahan secara kromatografi sekarang diperuntukkan
pada senyawa-senyawa yang tak berwarna (Hardjono, 1985).
Pada dasarnya semua cara kromatografi menggunakan dua fase yaitu fase
diam (stationary) dan fase gerak (mobile), pemisahan-pemisahan tergantung pada
gerakan relatif dari dua fase ini. Cara-cara kromatografi dapat digolongkan sesuai
dengan sifat-sifat dari fase diam, yang dapat berupa zat padat atau zat cair. Jika
fase diam berupa zat padat maka cara tersebut dikenal sebagai kromatografi
serapan (absorption chromatography), jika zat cair, dikenal sebagai kromatografi
partisi (partition chromatography). Karena fase gerak dapat berupa zat cair atau
gas maka semua ada empat macam sistem kromatografi. Keempat macam sistem
1). Fase gerak zat cair - fase diam padat:
Dikenal sebagai kromatografi serapan yang meliputi
- Kromatografi lapis tipis
- Kromatografi penukar ion.
2). Fase gerak gas - fase diam padat :
- Kromatografi gas padat
3). Fase gerak zat cair – fase diam zat cair :
Dikenal sebagai kromatografi partisi
- Kromatografi kertas
4). Fase gerak gas – fase diam zat cair :
- Kromatografi gas – cair
- Kromatografi kolom kapiler
(Hardjono, 1985).
Semua pemisahan dengan kromatografi tergantung pada kenyataan bahwa
senyawa-senyawa yang dipisahkan terdistribusi sendiri di antara fase gerak dan
fase diam dalam perbandingan yang sangat berbeda-beda dari satu senyawa
terhadap senyawa yang lain (Hardjono, 1985).
Dari berbagai kromatografi di atas peneliti memilih kromatografi lapis
tipis karena mempunyai keuntungan yaitu, membutuhkan waktu yang lebih cepat
dan diperoleh pemisahan yang lebih baik.
Kromatografi lapis tipis (KLT) merupakan metode pemisahan dimana
yang memisahkan terdiri atas fase diam yang ditempatkan pada penyangga berupa
kromatografi adsorpsi (serapan), dimana fase diam digunakan zat padat yang
disebut adsorben (penjerap) dan fase gerak adalah zat cair yang disebut dengan
larutan pengembang. Campuran yang akan dipisahkan berupa larutan ditotolkan
berupa bercak atau pita, kemudian plat (lapisan) dimasukkan ke dalam bejana
tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak) sehingga
pemisahan terjadi selama perambatan kapiler (pengembangan). Zat penjerap pada
KLT merupakan lapisan tipis serbuk yang dilapiskan pada lempeng kaca, plastik,
atau logam secara merata (Stahl, 1985).
Dengan memakai KLT, pemisahan senyawa yang amat berbeda seperti
senyawa organik alam, senyawa organik sintetik, kompleks anorganik-organik,
dan bahkan ion anorganik, dapat dilakukan dalam beberapa menit dengan alat
yang harganya tidak terlalu mahal (Gritter, 1991).
Faktor-faktor yang mempengaruhi gerakan noda dalam kromatografi lapis
tipis yang juga mempengaruhi harga Rf :
1). Struktur kimia dari senyawa yang dipisahkan.
2). Sifat dari penyerap dan derajat aktifitasnya.
(Biasanya aktifitas dicapai dengan pemanasan dalam oven, hal ini akan
mengeringkan molekul-molekul air yang menempati pusat-pusat serapan dari
penyerap).
3). Tebal dan kerataan dari lapisan penyerap.
Meskipun dalam prakteknya tebal lapisan tidak dapat dilihat pengaruhnya, tapi
perlu diusahakan tebal lapisan yang rata. Ketidakrataan akan menyebabkan
aliran pelarut menjadi tak rata pula dalam daerah yang kecil dari plat.
Kemurnian dari pelarut yang digunakan sebagai fase gerak pada kromatografi
lapis tipis adalah sangat penting dan bila campuran pelarut diguanakan maka
perbandingan yang dipakai harus betul-betul diperhatikan.
5). Derajat kejenuhan dari uap dalam bejana pengembangan yang digunakan.
6). Teknik percobaan.
7). Jumlah cuplikan yang digunakan.
Penetesan cuplikan dalam jumlah yang berlebihan memberikan tendensi
penyebaran noda-noda dengan kemungkinan terbentuknya ekor dan efek tak
seimbang lainnya sehingga mengakibatkan kesalahan-kesalahan pada
harga-harga Rf.
8). Suhu.
Pemisahan-pemisahan sebaiknya dikerjakan pada suhu tetap, hal ini terutama
untuk mencegah perubahan-perubahan dalam komposisi pelarut yang
disebabkan oleh penguapan atau perubahan-perubahan fase.
9). Kesetimbangan.
Kesetimbangan dalam lapisan tipis sangat penting, hingga perlu
mengusahakan atmosfer dalam bejana jenuh dengan uap pelarut. Suatu gejala
bila atmosfer dalam bejana tidak jenuh dengan uap pelarut, bila digunakan
pelarut campuran, akan terjadi pengembangan dengan permukaan pelarut yang
berbentuk cekung dan fasa bergerak lebih cepat pada bagian tepi-tepi dari
BAB III
METODOLOGI PENELITIAN
Metode penelitian yang dilakukan adalah metode Deskriptif (Sudjana,
2002). Penelitian ini dilaksanakan di Laboratorium Kimia Farmasi Kualitatif
Fakultas Farmasi Universitas Sumatera Utara.
2.1 Alat-Alat
Alat-alat yang digunakan dalam penelitian ini adalah UV Mini 1240
Spektrofotometri UV Visibel (Shimadzu) yang dihubungkan dengan printer Epson
LQ 300, neraca analitis (Vibra), chamber, lampu UV 254 nm, pipa kapiler, kertas
saring whatman No. 1, penangas air, dan alat-alat gelas seperti labu ukur, pipet
volume, gelas ukur, beaker glass, erlenmeyer, corong, maat pipet, cawan penguap,
batang pengaduk, botol metanol p.a, dan botol hisap.
2.2 Bahan-bahan
Semua bahan yang digunakan pada penelitian ini berkualitas pro analisis
kecuali dinyatakan lain, yaitu metanol, plat silika gel GF 254, amonia, etil asetat,
n-butanol, rhodamin B (BPFI), pemerah pipi merek Wardah (sampel kode A),
pemerah pipi merek Avon (sampel kode B), pemerah pipi merek Cherveen
(sampel kode C), pemerah pipi merek Sutsyu (sampel kode D), pemerah pipi
merek Chanel (sampel kode E), pemerah pipi merek MAC (sampel kode F),
pemerah pipi merek aubeau (sampel kode G), pemerah pipi merek Louvre 1
(sampel kode H), pemerah pipi merek Cosmic (sampel kode I), pemerah pipi
kode K), pemerah pipi merek Louvre 2 (sampel kode L), pemerah pipi merek
Siellas (sampel kode M), pemerah pipi merek Implora 1 (sampel kode N),
pemerah pipi merek Implora 2 (sampel kode O), pemerah pipi merek Aich
(sampel kode P), air suling (Laboratorium Kimia Farmasi Kuantitatif).
2.3 Metode Pengambilan Sampel
Sampel yang digunakan kosmetik jenis pemerah pipi bermerek yang dijual
di pusat pasar kota Medan. Teknik pengambilan sampel dilakukan dengan cara
sampling purposif dan diasumsikan semua jenis merek pemerah pipi yang dijual
di kota Medan adalah homogen. Pemilihan cara pengambilan ini didasarkan atas
pertimbangan bahwa populasi sampel adalah homogen dan dianggap sebagai
sampel yang representatif (Sudjana, 2002).
2.4 Prosedur Penelitian
2.4.1 Penentuan Kualitatif Rhodamin B 2.4.1.1 Pembuatan Larutan Uji (A)
Sejumlah lebih kurang 100 mg sampel dilarutkan dengan 20 ml larutan
metanol p.a di dalam erlenmeyer, dikocok hingga larut, kemudian disaring dan
diambil filtratnya, lalu diuapkan di atas penangas air hingga diperoleh ekstrak
pekat larutan uji dimasukkan ke dalam vial 5 ml.
2.4.1.2 Pembuatan Larutan Baku (B)
Sejumlah lebih kurang 5 mg rhodamin B BPFI dilarutkan dengan 10 ml
2.4.1.3 Pembuatan Larutan Campuran (C)
Sejumlah volume yang sama larutan A dan B dicampur, kemudian
dihomogenkan.
2.4.1.4 Identifikasi Sampel
Larutan A, B dan C ditotolkan pada plat secara terpisah dan dilakukan
kondisi sebagai berikut:
Fase diam : Silika Gel GF 254
Fase gerak : n-butanol – etil asetat – amonia
( 55 : 20 : 25 )
Volume penotolan : Larutan A, B dan C masing-masing 10 µ l
Jarak rambat : 15 cm
Penampak bercak : Cahaya UV 254 nm berfluoresensi kuning.
Plat KLT berukuran 20 x 20 cm diaktifkan dengan cara dipanaskan di
dalam oven pada suhu 1000 C selama + 30 menit. Larutan A, B, dan C ditotolkan
pada plat dengan menggunakan pipa kapiler pada jarak 2 cm dari bagian bawah
plat. Jarak antara noda adalah 2 cm kemudian dibiarkan beberapa saat hingga
mengering. Plat KLT yang telah mengandung cuplikan dimasukkan ke dalam
chamber yang terlebih dahulu telah dijenuhkan. Kemudian dibiarkan fase gerak
naik sampai batas atas plat KLT lalu diangkat dan dibiarkan kering di udara. Di
2.4.2 Penentuan Kuantitatif Rhodamin B
2.4.2.1 Pembuatan Larutan Induk Baku Rhodamin B 2.4.2.1.1 Larutan Induk Baku I Rhodamin B
Ditimbang dengan seksama 50 mg rhodamin B BPFI kemudian di
masukkan dalam labu tentukur 50 ml, larutkan dengan metanol p.a hingga larut,
cukupkan volume dengan metanol p.a sampai 50 ml.
Konsentrasi Larutan Induk Baku I ml 50
mg 50
= 1 mg/ml = 1000 mcg/ml
2.4.2.1.2 Larutan Induk Baku II Rhodamin B
Dipipet 2,5 ml Larutam Induk Baku I dengan menggunakan pipet volum,
dimasukkan dalam labu tentukur 50 ml diencerkan dengan metanol p.a sampai
garis tanda.
Konsentrasi Larutan Induk Baku II ml 50 ml 5 , 2
x 1 mg/ml = 50 mcg/ml
2.4.2.2 Penentuan Panjang Gelombang Maksimum Rhodamin B
Dipipet 2 ml dari Larutan Induk Baku II dimasukkan ke dalam labu
tentukur 50 ml, cukupkan volume dengan metanol p.a sampai 50 ml (kadar 2
mcg/ml), ukur resapan pada λ 400 - 800 nm, dengan menggunakan blanko. Sebagai blanko digunakan metanol p.a.
2.4.2.3 Penentuan Operating Time
Larutan induk baku II dimasukkan dalam labu tentukur 50 ml, cukupkan
volume dengan metanol p.a hingga 50 ml. Penentuan waktu kerja kestabilan
warna merah pada sampel adalah dilakukan dengan mengukur serapan larutan di
2.4.2.4 Penentuan Linieritas Kurva Kalibrasi Larutan Rhodamin B
Larutan induk baku II dipipet dengan menggunakan maat pipet ke dalam
labu tentukur 50 ml berturut-turut dipipet 1 ; 1,5 ; 2 ; 2,5 ; 3 ml, ditambahkan
metanol p.a dan cukupkan volume sampai garis tanda kemudian di kocok
homogen. (larutan kerja ini mengandung 1 ; 1,5 ; 2 ; 2,5 ; 3 (mcg/ml) biarkan
selama 15 menit, kemudian diukur resapannya pada panjang gelombang 544 nm
menggunakan blanko.
2.4.2.5 Penetapan Kadar Rhodamin B Pada Sampel
Penetepan kadar rhodamin B pada sampel tidak dilakukan, sebab hasil
BAB IV
HASIL DAN PEMBAHASAN
4.1 Analisis Kualitatif Rhodamin B pada Sampel
Analisis sampel dilakukan dengan cara Kromatografi Lapis Tipis dengan
kondisi sebagai berikut :
Fase diam : Silika Gel GF 254
Fase gerak : n-butanol – etil asetat – amonia
( 55 : 20 : 25 )
Volume penotolan : Larutan A, B dan C masing-masing 10 µ l
Jarak rambat : 15 cm
Penampak bercak : Cahaya UV 254 nm berfluoresensi kuning
(Ditjen POM, 1997)
Hasil analisis kualitatif rhodamin B pada sampel di atas dapat dilihat pada
[image:40.595.114.512.460.747.2]tabel 3.1.
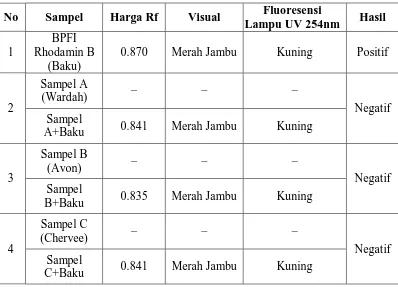
Tabel 4.1. Hasil Analisa Kualitatif Rhodamin B pada Sampel No Sampel Harga Rf Visual Fluoresensi
Lampu UV 254nm Hasil 1
BPFI Rhodamin B
(Baku)
0.870 Merah Jambu Kuning Positif
2
Sampel A
(Wardah) – – –
Negatif Sampel
A+Baku 0.841 Merah Jambu Kuning
3
Sampel B
(Avon) – – –
Negatif Sampel
B+Baku 0.835 Merah Jambu Kuning
4
Sampel C
(Chervee) – – –
Negatif Sampel
Lanjutan tabel 4.1
No Sampel Harga Rf Visual Fluoresensi
Lampu UV 254nm Hasil
5
Sampel D
(Sutsyu) – – –
Negatif Sampel
D+Baku 0.864 Merah Jambu Kuning
6
Sampel E
(Chanel) – – –
Negatif Sampel
E+Baku 0.841 Merah Jambu Kuning
7
Sampel F
(MAC) – – –
Negatif Sampel
F+Baku 0.829 Merah Jambu Kuning
8
Sampel G
(Aubeau) – – –
Negatif Sampel
G+Baku 0.835 Merah Jambu Kuning
9
Sampel H
(Louvre 1) – – –
Negatif Sampel
H+Baku 0.847 Merah Jambu Kuning
10
Sampel I
(Cosmic) – – –
Negatif Sampel
I+Baku 0.847 Merah Jambu Kuning
11
Sampel J
(Sutsyu 2in1) – – –
Negatif Sampel
J+Baku 0.841 Merah Jambu Kuning
12
Sampel K (Silvie Lowrens)
0.794 Merah Jambu Kuning
Negatif Sampel
K+Baku
0.794
0.829 Merah Jambu Kuning
13
Sampel L
(Louvre 2) – – – Negatif
Sampel
Lanjutan tabel 4.1
No Sampel Harga Rf Visual Fluoresensi
Lampu UV 254nm Hasil
14
Sampel M
(Seillas) – – –
Negatif Sampel
M+Baku 0.876 Merah Jambu Kuning
15
Sampel N
(Implora 1) 0.835 Merah Jambu Kuning
Negatif Sampel
N+Baku
0.829
0.882 Merah Jambu Kuning
16
Sampel O
(Implora 2) 0.829 Merah Jambu Kuning
Negatif Sampel
O+Baku
0.823
0.870 Merah Jambu Kuning
17
Sampel P
(Aich) 0,823 Merah Jambu Kuning
Negatif Sampel
P+Baku
0.829
0.864 Merah Jambu Kuning Keterangan : ─ = negatif
Dari tabel di atas dapat dilihat bahwa tidak ada sampel yang memberikan
hasil positif. Suatu senyawa yang mengandung rhodamin B dapat dilihat nodanya
yang jelas secara visual berwarna merah jambu dan dengan lampu UV 254 nm
memberikan fluoresensi kuning.
Selain itu, untuk mengidentifikasi suatu senyawa dapat kita lakukan
dengan melihat harga Rf-nya. Identifikasi sahih dilakukan jika senyawa yang
dianalisis dibandingkan dengan senyawa pembanding dan dengan campuran yang
terdiri atas senyawa yang dianalisis dan senyawa pembanding (cara spiking) pada
lapisan yang sama (Gritter, 1991).
Dari tabel dapat dilihat bahwa tidak ada sampel yang memberikan harga
Rf yang berdekatan dengan pembandingnya. Jadi dapat disimpulkan bahwa
4.2 Panjang Gelombang Maksimum Larutan Rhodamin B
Penentuan panjang gelombang maksimum larutan rhodamin B dilakukan
pada konsentrasi 2 ppm dengan rentang panjang gelombang 400-800 nm. Hal ini
dilakukan karena larutan rhodamin B merupakan larutan berwarna. Menurut
Sujdadi (2007), sinar tampak mempunyai panjang gelombang 400-750 nm. Selain
itu pengukuran dilakukan pada rentang tersebut karena pada panjang gelombang
maksimum kepekaannya juga maksimum dan sekitar panjang gelombang
maksimum bentuk kurva absorbansi datar dan pada kondisi tersebut hukum
Lambert-Beer akan terpenuhi (Rohman, 2007).
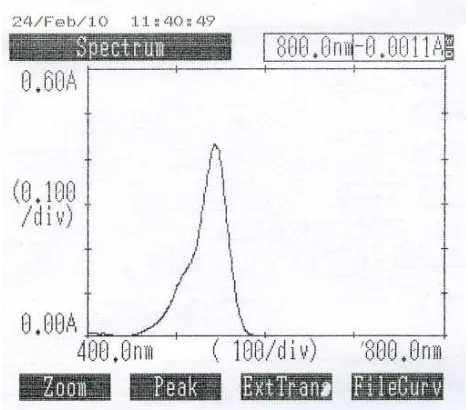
[image:43.595.194.428.389.594.2]Hasil penentuan panjang gelombang larutan rhodamin B dapat dilihat pada
gambar 3.1.
Gambar 1. Kurva Resapan Rhodamin B (Konsentrasi 2 mcg/ml)
Panjang gelombang maksimum untuk larutan rhodamin B yang digunakan
dalam penelitian ini adalah λ 544 nm. Menurut literatur panjang gelombang maksimum yang diperoleh yaitu 543,335 (Aldrich, 1992). Perbedaan panjang
Farmakope Indonesia Edisi IV yaitu 3 nm. Berarti dalam hal ini bahwa panjang
gelombang maksimum larutan rhodamin B dapat diterima sebagai analisis
rhodamin B pada sampel.
Perbedaan panjang gelombang ini kemungkinan disebabkan karena
kondisi dari alat yang digunakan, dimana spektrofotometer yang digunakan untuk
pengukuran seharusnya dikalibrasi dengan baik terhadap skala panjang
gelombang dan absorbansinya.
4.3 Penentuan Operating Time
Penentuan operating time dari rhodamin B secara Spektofotometri Sinar
Tampak dilakuan dengan selang waktu 1 menit setelah ditambahkan metanol p.a.
Dari data yang diperoleh, waktu pengukuran yang stabil dimulai dari menit ke-15
sampai menit ke-18 (Data pengamatan pada lampiran 1).
Dari data operating time yang diperoleh, diambil untuk penentuan waktu
kerja adalah data yang mempunyai kesamaan angka tiga desimal. Tidak
diperolehnya kesamaan angka empat desimal. Hal ini disebabkan kondisi alat dan
arus listrik yang tidak stabil yang mempengaruhi alat spektrofotometer.
4.4 Linearitas Kurva Kalibrasi Larutan Rhodamin B
Penentuan linearitas kurva kalibrasi larutan rhodamin B dilakukan dengan
membuat berbagai konsentrasi pengukuran yaitu 1 ; 1,5 ; 2 ; 2,5 ; 3 mcg/ml.
Tabel 4.2. Tabel Kurva Kalibrasi Rhodamin B
Linearitas kurva kalibrasi rhodamin B dapat dilihat pada gambar 3.2.
Gambar 4.2. Hasil Penentuan Kurva Kalibrasi Larutan Rhodamin B λ 544 nm. Hasil perhitungan persamaan regresi dari kurva kalibrasi diatas diperoleh
persamaan regresi Y = 0,2053 X + 0,00462 dengan koefisien korelasi (r) sebesar
0,9999 yang menunjukkan hubungan yang linier antara absorbansi dengan
konsentrasi, artinya dengan meningkatnya konsentrasi maka absorbansi juga
meningkat. Hal ini berarti terdapat 99,99% data yang memiliki hubungan linear
(Sudjana, 2002).
Penentuan kadar tidak dilakukan sebab hasil analisis kualitatif tidak
BAB IV
KESIMPULAN DAN SARAN
4.1. Kesimpulan
Bahwa dari hasil identifikasi, tidak ditemukan adanya pewarna rhodamin
B pada pemerah pipi yang berarti bahwa pemerah pipi yang beredar di Pusat Pasar
Kota Medan sudah aman dari rhodamin B.
4.2. Saran
Disarankan agar dilakukan penelitian lebih lanjut terhadap penetapan
kadar zat pewarna barbahaya lain yang beredar di pasaran secara HPLC baik
dalam betuk pemerah pipi atau bentuk sedian kosmetik lainnya.
Disarankan kepada masyarakat agar lebih berhati-hati dalam memilih
DAFTAR PUSTAKA
Anonima. (2006). Waspadai Kosmetik Murah!
Anonimb. (2008). Kenali Bahaya Kosmetik. kenali-bahaya-kosmetik/trackback.
Aldrich. (1992). Aldrich Chemical Catalogue. Milwaukee, USA: Aldrich Chemical Company.
Budavari, S. (1989). The Merck Index. Encyclopedia of chemicals, Drugs, and Biologicals. Elevent Edition. Whitehouse: Merck & Co., Inc.
Ditjen POM. (1985). Formularium Kosmetik Indonesia. Jakarta: Departemen Kesehatan RI. Hal. 189.
Ditjen POM. (1995). Farmakope Indonesia. Edisi Keempat. Jakarta: Departemen Kesehatan RI. Hal. 1061.
Ditjen POM. (1998). Permenkes RI No445/Menkes/Per/V/1998 tentang Bahan, Zat Warna, Substratum, Zat Pengawet dan Tabir Surya pada Kosmetik.Jakarta: Departemen Kesehatan RI.
Ditjen POM. (2000). Metode Analisa PPOMN. Jakarta: Departemen Kesehatan RI. Hal. 35-36.
Gritter, R.J., dan James, M.R. (1991). Pengantar Kromatografi. Terbitan kedua. Bandung: Penerbit ITB. Hal. 107, 133.
Lesmono, M.B, dkk. (1985). Kamus Istilah kosmetik. Jakarta. Pusat Pembinaan dan Pengembangan Bahasa Departemen Pendidikan dan Kebudayaan. Hal. 38.
Rohman, A. (2007). Kimia Farmasi Analisis. Cetakan Pertama. Yogyakarta: Pustaka Pelajar. Hal. 222-223, 261-262.
Sastrohamidjojo, H. (1985). Kromatografi. Edisi Pertama. Yogyakarta: Penerbit Liberty. Hal. 1-2, 35-36.
Stahl, E. (1985). Analisis Obat Secara Kromatografi dan Mikroskopi. Bandung: ITB Press. Hal. 20-25.
Tranggono, R.I.S dan Latifah, F. (2007). Buku Pegangan Ilmu Pengetahuan Kosmetik. Jakarta: Gramedia Pustaka Utama. Hal. 7-8, 93-96.
Vogel.A.I. (1994). Kimia Analisis Kuantitatif Anorganik. Cetakan Pertama. Jakarta: Penerbit EGC. Hal. 810.
Wasitaatmadja, S.M. (1997). Penuntun Ilmu Kosmetik Medik. Jakarta: Universitas Indonesia Press. Hal. 26-29, 40, 63, 122-124.
Lampiran 1. Contoh Perhitungan Harga Rf
Harga Rf =
awal titik dari depan garis jarak awal titik dari bercak pusat titik jarak
Jarak yang digerakkan oleh pelarut dari titik asal = 17
Harga Rf untuk baku pembanding = 0,976 17
6 , 16
=
Harga Rf untuk sampel I + baku pembanding = 0,929 17
15,8
=
Harga Rf untuk sampel I = 0,918 17
6 , 15
Lampiran 2. Penentuan Operating Time
Lampiran 4. Perhitungan Persamaan Regresi
No
Konsentrasi (ppm)
Absorbansi
XY X2 Y2
X Y
1 0,0000 0,0000 0,0000 0,0000 0,0000
2 1,0000 0,212 0,212 1,0000 0,0449
3 1,5000 0,316 0,474 2,2500 0,0998
4 2,0000 0,415 0,83 4,0000 0,1727
5 2,5000 0,520 1,3 6,2500 0,2704
6 3,0000 0,619 1,857 9,0000 0,3831
n=6 ∑X=10,000
0 ∑Y=2,0850
∑XY=4,673 0
∑X2
=22,500
0 ∑Y
2
= 0,9706
1,6667 0,3470
Y = ax + b
a =
(
) ( )( )
(
X)
( )
X nn Y X XY / / 2 2
∑
∑
∑
∑
∑
− − =(
) ( )(
)
(
22,5000) ( )
10 /66 / 0850 , 2 10 6730 , 4 2 − −
= 0,2053 b =
= (0,347) ─ (0,2053) (1,6667) = 0,0046
Sehingga diperoleh persamaan regresi Y = 0,2053 X + 0,0046
Untuk mencari hubungan kadar (X) dengan luas puncak (Y) digunakan pengujian
koefisien korelasi
r =
(
) ( )( )
(
)
( )
[
X X n]
[
( )
Y( )
Y n]
n Y X XY / / / 2 2 2 2
∑
∑
∑
∑
∑
−∑
∑
− −r =
(
) ( )(
)
( ) ( )
[
22,5 10 /6]
[
(
0,9706) (
2,0856)
/6]
6 / 0856 , 2 10 6730 , 4 2 2 − − −Lampiran 5. Alat Spektrofotometer
Lampiran 6. Alat timbangan digital
Lampiran 7. Gambar Sampel
Gambar 3. Pemerah Pipi Wardah (Kode Sampel – A)
Gambar 4. Pemerah Pipi Avon (Kode Sampel – B)
Gambar 6. Pemerah Pipi Sutsyu (Kode Sampel – D)
Gambar 7. Pemerah Pipi Chanel (Kode Sampel – E)
Gambar 9. Pemerah Pipi aubeau (Kode Sampel – G)
Gambar 10. Pemerah Pipi Louvre 1 (Kode Sampel – H)
Gambar 12. Pemerah pipi Sutsyu 2 in 1 (Kode Sampel – J)
[image:58.595.177.453.83.675.2]Gambar 13. Sylvie Lawrens (Kode Sampel – K)
Gambar 15. Pemerah pipi Siellas (Kode Sampel – M)
[image:59.595.179.447.81.679.2]Gambar 16. Pemerah pipi Implora (Kode Sampel – N,O)
Lampiran 8. Gambar Plat KLT 20 x 20
[image:60.595.133.488.95.483.2]X A+X A B+X B C+X C D+X D
Gambar 18. Plat A
Keterangan :
Kode X : BPFI Rhodamin B
Kode A : Wardah
Kode A+X : Wardah + BPFI Rhodamin B
Kode B : Avon
Kode B+X : Avon + BPFI Rhodamin B
Kode C : Cherveen
Kode C+X : Cherveen + BPFI Rhodamin B
Kode D : Sutsyu
X E+X E F+X F G+X G H+X H
Gambar 19. Plat B
Keterangan :
Kode X : BPFI Rhodamin B
Kode E : Chanel
Kode E+X : Chanel + BPFI Rhodamin B
Kode F : MAC
Kode F+X : MAC + BPFI Rhodamin B
Kode G : Aubeau
Kode G+X : Aubeau + BPFI Rhodamin B
Kode H : Louvre 1
X I I+X J J+X K K+X L L+X
Gambar 20. Plat C
Keterangan :
Kode X : BPFI Rhodamin B
Kode A : Cosmic
Kode A+X : Cosmic + BPFI Rhodamin B
Kode B : Sutsyu
Kode B+X : Sutsyu + BPFI Rhodamin B
Kode C : Silvie Lowrens
Kode C+X : Silvie Lowrens + BPFI Rhodamin B
Kode D : Louvre 2
X M M+X N N+X O O+X P P+X
Gambar 21. Plat D
Keterangan :
Kode X : BPFI Rhodamin B
Kode M : Siellas
Kode M+X : Siellas + BPFI Rhodamin B
Kode N : Implora I
Kode N+X : Implora I + BPFI Rhodamin B
Kode O : Implora II
Kode O+X : Implora II + BPFI Rhodamin B
Kode P : Aich