INDUSTRI
SECARA SPEKTROFOTOMETRI
KARYA ILMIAH
052401076
Rahmi Juwita Putri Daulay
PROGRAM STUDI DIPLOMA 3 KIMIA ANALIS
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENENTUAN KADAR AMMONIA LIMBAH CAIR
LABORATORIUM BALAI RISET DAN STANDARDISASI INDUSTRI SECARA SPEKTROFOTOMETRI
KARYA ILMIAH
Saya mengakui bahwa tugas akhir ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Mei 2008
NIM : 052401076
Judul : PENENTUAN KADAR AMMONIA LIMBAH CAIR LABORATORIUM BALAI RISET DAN
STANDARDISASI INDUSTRI SECARA SPEKTROFOTOMETRI
Kategori : KARYA ILMIAH
Nama : RAHMI JUWITA PUTRI DAULAY
Nomor Induk Mahasiswa : 052401076
Program Studi : DIPLOMA 3 KIMIA ANALIS
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
PENGHARGAAN
Syukur Alhamdulillah penulis sampaikan kehadirat Allah SWT atas limpahan
rahmat dan hidayahNya kepada penulis sehingga dapat menyelesaikan karya ilmiah
ini dengan baik, serta shalawat beriring salam tak lupa penulis sampaikan kepada
Junjungan Nabi Besar Muhammad SAW, yang telah memberikan Suri Teladan yang
baik kepada umat manusia.
Adapun tujuan penulisan karya ilmiah ini adalah untuk melengkapi
persyaratan penyelesaian perkuliahan di jurusan Kimia Analis Program Diploma III
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Penulis menyadari bahwa tanpa petunjuik dan bimbingan dari Dosen serta
bantuan dari pihak lain maka sulit bagi penulis untuk menyelesaikan karya ilmiah ini.
Untuk itu perkenankanlah penulis mengucapkan terima kasih kepada :
1. Ibu Dr. Rumondang Bulan Nst MS selaku Ketua Departemen Kimia Fakultas
MIPA Universitas Sumatera Utara.
2. Ibu Dra. Marpongahtun MSc selaku dosen pembimbing penulis yang telah
menyediakan waktu dan pikiran dalam memberikan pengarahan dan bimbingan
kepada penulis dalam penulisan karya ilmiah ini.
3. Ibunda tercinta Hj. Nur Abidah ,BSc, ayahanda tercinta Drs. H. M. Thoha
Daulay, MM, kakak, abang, adik, beserta keluarga yang senantiasa mendo’akan
dan memberikan semangat kepada penulis untuk menyelesaikan studi di
Universitas Sumatera Utara pada Program Diploma 3.
4. Sahabat-sahabat penulis : diyyah, Nina, Siti, Karti, Icut, cici, ratih, yuli, winda,
dan teman-teman yang lain yang tidak dapat disebutkan satu persatu yang telah
mendukung dan membantu penulis dalam penyelesaian karya ilmiah ini.
5. Seluruh Staf Pengajar dan Pegawai di Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Sumatera Utara.
Medan, 2008
DAFTAR ISI
Halaman
KATA PENGANTAR ... i
ABSTRACT ... iii
INTI SARI ... iv
DAFTAR ISI ... v
BAB 1 PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Permasalahan ... 2
1.3 Tujuan ... 2
1.4 Manfaat ... 3
BAB 2 TINJAUAN PUSTAKA ... 4
2.1 Air ... 4
2.1.1 Sifat Umum Air ... 4
2.1.2 Karakteristik Badan Air ... 5
2.1.3 Pencemaran Air ... 8
2.2 Limbah ... 9
2.2.1 Sumber Limbah Cair ... 10
2.2.2 Karakteristik Limbah Cair ... 12
2.2.3 Teknik Pengolahan Limbah Cair ... 13
2.3 Amoniak ... 16
2.5 Spektrofotometri ... 22
BAB 3 BAHAN DAN METODE ... 24
3.1 Prinsip Percobaan ... 24
3.2 Sampel ... 24
3.3 Peralatan ... 24
3.4 Bahan-bahan ... 25
3.5 Prosedur Analisa ... 25
BAB 4 HASIL DAN PEMBAHASAN ... 26
4.1 Data ... 26
4.2 Pembahasan ... 27
BAB 5 KESIMPULAN DAN SARAN ... 29
5.1 Kesimpulan ... 29
5.2 Saran ... 29
DAFTAR PUSTAKA
BAB 1
PENDAHULUAN
1.1Latar Belakang
Air merupakan sumber daya alam yang diperlukan untuk hajat hidup orang
banyak, bahkan oleh semua makhluk hidup. Oleh karena itu, sumber daya air harus
dilindungi agar tetap dapat dimanfaatkan dengan baik oleh manusia serta makhluk
hidup yang lain. Pemanfaatan air untuk sebagai kepentingan harus dilakukan secara
bijaksana,dengan memperhitungkan kepentingan generasi sekarang maupun generasi
mendatang.
Saat ini, masalah utama yang dihadapi oleh sumber daya air meliputi kuantitas
air yang sudah tidak mampu memenuhi kebutuhan yang terus meningkat dan kualitas
air untuk keperluan domestik yang semakin menurun. Kegiatan industri, domestik,
dan kegiatan lain berdampak negatif terhadap sumber daya air, antara lain
menyebabkan penurunan kualitas air. Kondisi ini dapat menimbulkan gangguan,
kerusakan, dan bahaya bagi semua makhluk hidup yang bergantung pada sumber daya
air. Oleh karena itu, diperlukan pengelolaan dan perlindungan sumber daya air secara
seksama.
Hingga saat ini, Indonesia telah memiliki Peraturan Pemerintah No. 20 tahun
1990 tentang Pengendalian Pencemaran Air dan Keputusan Menteri Negara
Lingkungan Hidup No. 51 tahun 1995 tentang Baku Mutu Limbah Cair bagi Kegiatan
yang pada dasarnya berkaitan dengan upaya pengelolaan sumber daya air dan sumber
daya alam lainnya, dalam rangka pengendalian dampak lingkungan (Effendi,H. 2003).
Amoniak (NH3), merupakan senyawa nitrogen yang menjadi NH4+ pada pH
rendah dan disebut amonium; amoniak sendiri berada dalam keadaan tereduksi.
Amoniak dalam air permukaan berasal dari seni dan tinja; juga dari oksidasi zat
organik (HaObCcNd) secara mikrobiologis, yang berasal dari air alam atau air
buangan industri dan penduduk (Alaerts, 1984).
Salah satu parameter yang terdapat dalam air adalah amoniak. Amoniak
biasanya berasal dari tinja, limbah domestik, limbah industri dan pupuk pertanian. Air
biasanya mengandung amoniak dalam jumlah yang sedikit. Kadar amoniak yang
tinggi dalam air dapat bersifat toksik, untuk itu diperlukan pengolahan dan analisis
terhadap air. Dalam hal ini kadar amoniak dalam air dapat dianalisis dengan
menggunakan alat spektrofotometer dengan panjang gelombang (λ) 425 nm
Berdasarkan hal tersebut diatas, amoniak dalam jumlah yang tinggi dapat
bersifat toksik di dalam perairan sehingga perlu dilakukan analisa kadar amoniak agar
dapat mengontrol toksisitas suatu perairan sehingga tidak merusak kehidupan biota
perairab (Effendi,H. 2003).
1.2 Permasalahan
Kadar amoniak yang melebihi standart dapat mempengaruhi kehidupan biota
perairan, untuk itu perlu dilakukan pemeriksaan apakah kadar amoniak pada limbah
cair industri telah memenuhi syarat baku mutu kualitas limbah industri menurut
1.3 Tujuan
1. Untuk mengetahui kadar amoniak dalam limbah cair laboratorium Balai Riset dan
Standardisasi Industri
2. Untuk mengetahui apakah kadar ammonia yang diperoleh telah memenuhi syarat
kualitas baku mutu limbah industri menurut keputusan menteri Lingkungan
Hidup.
1.4 Manfaat
1. Sebagai informasi dan wawasan bagi masyarakat luas dalam mengetahui cara
penentuan kadar amoniak dengan menggunakan alat spektrofotometer
2. Untuk mengetahui apakah limbah industri layak untuk dibuang ke lingkungan
BAB 2
TINJAUAN PUSTAKA
2.1 Air
Air menutupi sekitar 70% permukaan bumi, dengan jumlah sekitar 1.368 juta
km3. Air terdapat dalam berbagai bentuk, misalnya uap air, es, cairan, dan salju. Air
tawar terutama terdapat di sungai, danau, air tanah, dan gunung es. Semua badan air di
daratan dihubungkan dengan laut dan atmosfer melalui siklus hidrologi yang
berlangsung secara kontinu.
Air memiliki rumus kimia H2O, ini berarti bahwa pada setiap molekul
air memiliki ikatan kimia antara atom oksigen dengan hidrogen adalah kovalen, yang
berarti mereka melibatkan pembagian elektron secara bersama. Tetapi, pembagiannya
tidak seimbang, karena oksigen lebih rakus menarik pada elektron daripada atom
hidrogen. Sebagai akibatnya elektron molekul air mengikat atom oksigen lebih erat.
Bentuk molekul air juga suatu hal yang menarik. Ketiga atomnya tidak berjejer
lurus. Namun ikatannya mengatur sendiri dalam bentuk segitiga. Bentuk lengkungan
ini berasal dari dua pasang elektron hidrogen yang terpisah yang mengelilingi atom
oksigen. Pasangan elektron ini menolak elektron-elektron dalam ikatannya dengan
hidrogen, yang menyebabkan mereka membentuk sudut 105 derajat.
Sebuah molekul dengan ujung-ujung yang muatannya berlawanan disebut
polar. Oleh karena itu air disebut molekul kovalen polar, karena ciri bersama dari
ikatan yang tidak seimbang. Sebagaimana akan kita lihat, jenis khas dari polaritas ini
2.1.1 Sifat Umum Air
Air memiliki karakteristik yang khas yang tidak dimiliki oleh senyawa kimia
yang lain . Karakteristik tersebut adalah sebagai berikut :
a. Pada kisaran suhu yang sesuai bagi kehidupan, yakni 0oC (32oF) – 100oC, air
berwujud cair. Suhu 0oC merupakan titik beku (freezing point) dan 100o
b. Perubahan suhu air berlangsung lambat sehingga air memiliki sifat sebagai
penyimpan panas yang baik. Sifat ini memungkinkan air tidak menjadi panas
ataupun dingin dalam seketika. Sifat ini juga menyebabkan air sangat baik
digunakan sebagai pendingin mesin.
C
merupakan titik didih (boiling point) air.
c. Air memerlukan panas yang tinggi dalam proses penguapan. Penguapan
(evaporasi) adalah proses perubahan air menjadi uap air. Proses ini
memerlukan energi panas dalam jumlah yang besar. Sebaliknya, proses
perubahan uap air menjadi cairan (kondensasi) melepaskan energi panas
yang besar. Sifat ini merupakan salah satu faktor utama yang menyebabkan
terjadinya penyebaran panas secara baik di bumi.
d. Air merupakan pelarut yang baik. Air mampu melarutkan berbagai jenis
senyawa kimia. Air hujan mengandung senyawa kimia dalam jumlah yang
sangat sedikit, sedangkan air laut dapat mengandung senyawa kimia hingga
35.000 mg/liter. Sifat ini memungkinkan unsur hara (nutrien) terlarut
diangkut ke seluruh jaringan tubuh makhluk hidup dan memungkinkan
bahan-bahan toksik yang masuk ke dalam jaringan tubuh makhluk hidup
dilarutkan untuk dikeluarkan kembali. sifat ini juga memungkinkan air
digunakan sebagai pencuci yang baik dan pengencer bahan pencemar
e. Air memiliki tegangan permukaan yang tinggi. Suatu cairan dikatakan
memiliki tegngan permukaan yang tinggi jika tekanan antar-molekul cairan
tersebut tinggi. Tegangan permukaan yang tinggi menyebabkan air memiliki
sifat membasahi suatu bahan secara baik. tegangan permukaan yang tinggi
juga memungkinkan terjadinya sistem kapiler, yaitu kemampuan untuk
bergerak dalam pipa kapiler.
f. Air merupaka satu-satunya senyawa yang merenggang ketika membeku.
Pada saat membeku, air merenggang sehingga es memiliki nilai densitas
yang lebih rendah dari pada air. Dengan demikian es mengapung di air. Sifat
ini mengakibatkan danau-danau di daerah yang beriklim dingin hanya
membeku pada bagian permukaan sehingga kehidupan organisme akuatik
tetap berlangsung.
2.1.2 Karakteristik Badan Air
Badan air dicirikan oleh tiga komponen utama, yaitu komponen hidrologi,
komponen fisika-kimia, dan komponen biologi. Penilaian kualitas suatu badan air
harus mencakup ketiga komponen tersebut, yaitu :
A.
Air tawar berasal dari dua sumber, yaitu air permukaan dan air tanah. Air
permukaan adalah air yang berada di sungai, danau, waduk, rawa, dan badan air lain,
yang tidak mengalami infiltrasi ke bawah tanah. Sekitar 69% air yang masuk ke
sungai berasal dari hujan, pencairan es/salju, dan sisanya berasal dari air tanah. Air Permukaan
Air hujan yang jatuh ke bumi dan menjadi air permukaan memiliki kadar
asam, dengan nilai pH sekitar 4,2. Hal ini disebabkan air hujan melarutkan gas-gas
yang terdapat di atmosfer. Setelah jatuh ke permukaan bumi, air hujan mengalami
kontak dengan tanah dan melarutkan bahan-bahan yang terkandung di dalam tanah.
Perairan permukaan diklasifikasikan menjadi dua kelompok utama, yaitu
badan air tergenang dan badan air mengalir.
1. Perairan tergenang
Perairan tergenang meliputi danau, kolam, waduk, rawa, dan sebagainya.
Perairan tergenang, khususnya danau, biasanya mengalami stratifikasi secara vertikal
akibat perbedaan intensitas cahya dan perbedaan suhu pada kolom air yang terjadi
secara vertikal. Arus air danau dapat bergerak ke berbagai arah. Paerairan danau
biasanya memiliki stratifikasi kualitas air secara vertikal. Stratifikasi ini tergantung
pada kedalaman dan musim.
Berdasarkan intensitas cahaya yang masuk ke perairan, stratifikasi vertikal
kolom air pada perairan tergenang dikelompokkan menjadi tiga, yaitu :
a. Lapisan eufotik, yaitu lapisan yang masih mendapatkan cukup cahaya
matahari.
b. Lapisan kompensasi, yaitu lapisan dengan intensitas cahaya sebesar 1% dari
intensitas cahaya permukaan.
c. Lapisan profundal, yaitu lapisan di bawah lapisan kompensasi, dengan
intensitas cahaya sangat kecil atau bahkan tidak ada cahaya (afotik).
Tiupan aingin dan perubahan musim yang mengakibatkan perubahan intensita
cahaya matahari dan perubahan suhu dapat mengubah atau menghancurkan stratifikasi
vertikal kolom air. Fenomena perubahan stratifikasi vertikal ini dapat diamati dengan
jelas pada perairan tergenang yang terdapat di wilayah ugahari yang memiliki empat
2. Perairan mengalir
Salah satu contoh perairan mengalir adalah sungai. Sungai dicirikan oleh arus
yang searah relatif kencang, dengan kecepatan berkisar antara 0,1 – 1,0 m/detik, serta
sangat dipengaruhi oleh waktu, iklim, dan pola drainase. Pada perairan sungai,
biasanya terjadi percampuran massa air secara menyeluruh dan tidak terbentuk
stratifikasi vertikal kolom air seperti pada perairan tergenang. Kecepatan arus, erosi,
dan sedimentasi merupakan fenomena yang biasa terjadi di sungai sehingga kehidupan
flora dan fauna sangat dipengaruhi oleh ketiga variabel tersebut.
B.
Air tanah merupakan air yang berada di bawah permukaan tanah. Air tanah
ditemukan pada akifer. Pergerakan air tanah sangat lambat; kecepatan arus berkisar
antara 10 Air Tanah
-10
– 10 -3 m/detik dan dipengaruhi oleh porositas, permeabilitas dari lapisan
tanah, dan pengisian kembali air. Karakteristik utama yang membedakan air tanah dari
air permukaan adalah pergerakan yang sangat lambat dan waktu tinggal yang sangat
lama, dapat mencapai puluhan bahkan ratusan tahun. Karena pergerakan yang lama
tersebut, air tanah akan sulit untuk pulih kembali jika mengalami pencemaran.
Jika laju pengambilan air tanah pada akifer melebihi laju pengisiannya maka
akan terjadi penurunan volume air tanah dan penambahan volume udara yang
besarnya setara dengan volume air yang dikeluarkan dari akifer. Kondisi ini
memunkinkan terjadinya penurunan muka tanah. Pengambilan air tanah akan
mengubah aliran air tanah. Bersamaan dengan keluarnya air dari akifer, tekanan
hidrostatik air tanah mengalami penurunan sehingga aliran air tanah dari arah laut
Air tanah yang berasal dari lapisan deposit pasir memiliki kandungan
karbondioksida tinggi dan kandungan bahan terlarut rendah. Air tanah yang berasal
dar lapisan deposit kapur juga memiliki kadar karbondioksida yang rendah, namun
memiliki nilai TDS yang tinggi.
Air tanah biasanya memiliki kandungan besi relatif tinggi. Jika air tanah
mengalami kontak dengan udara dan mengalami oksigenasi, ion ferri pada ferri
hidroksida [Fe(OH)3
Bahan pencemar (polutan) adalah bahan-bahan yang bersifat asing bagi alam
atau bahan yang berasal dari alam itu sendiri yang memasuki suatu tatanan ekosistem
sehingga mengganggu peruntukan ekosistem tersebut. Berdasarkan cara masuknya ke
dalam lingkungan, polutan dikelompokkan menjadi dua, yitu polutan alamiah dan
polutan antropogenik. Polutan alamiah adalah polutan yang memasuki suatu
lingkungan secara alami. Polutan antropogenik adalah polutan yang masuk ke badan
air akibat aktivitas manusia, misalnya kegiatan domestik, kegiatan urban, maupun ] yang banyak terdapat dalam air tanah akan teroksidasi menjadi
ion ferro, dan segera mengalami presipitasi serta membentuk warna kemerahan pada
air. Oleh karena itu, sebelum digunakan untuk nernagai kebutuhan, sebaiknya air
tanah yang baru disedot didiamkan terlebih dahulu selama beberapa saat untuk
mengendapkan besi.
2.1.3 Pencemaran Air
Pencemaran air diakibatkan oleh masuknya bahan pencemar (polutan) yang
dapat berupa gas, bahan-bahan terlarut, dan partikulat. Pencemar memasuki badan air
dengan berbagai cara, misalnya melalui atmosfer, tanah, limpasan pertanian, limbah
kegiatan industri. Intensitas polutan antropogenik dapat dikendalikan dengan cara
mengontrol aktivitas yang menyebabkan timbulnya polutan tersebut.
Jenis-jenis Pencemar
Polutan yang memasuki perairan terdiri atas campuran berbagai jenis polutan.
Jika di perairan terdapat lebih dari dua jenis polutan maka kombinasi pengaruh yang
ditimbulkan oleh beberapa jenis polutan tersebut dapat dikelompokkan menjadi tiga
sebagai berikut :
1. Additif; pengaruh yang ditimbulkan oleh beberapa jenis polutan merupakan
penjumlahan dari pengaruh masing-masing polutan. Misalnya, pengaruh kombinasi
zinc dan kadmium terhadap ikan.
2. Synergism; pengaruh yang ditimbulkan oleh beberapa jen is polutan lebih besar
darpada penjumlahan pengaruh dari masing-masing polutan. Misalnya, pengaruh
kombinasi copper dan klorin atau pengaruh kombinasi copper dan surfaktan.
3. Antagonism; pengaruh yang ditimbulkan oleh beberapa jenis polutan saling
mengganggu sehingga pengaruh secara kumulatif lebih kecil atau mungkin hilang.
Misalnya, pengaruh kombinasi kalsium dan timbal atau zinc dan aluminium
(Effendi,H. 2003).
2.2 Limbah
Limbah cair atau air limbah adalah air yang tidak terpakai lagi, yang
merupakan hasil dari berbagai kegiatan manusia sehari-hari. Dengan semakin
bertambah dan meningkatnya jumlah penduduk dengan segala kegiatanya, maka
jumlah air limbah juga mengalami peningkatan. Pada umumnya limbah cair dibuang
kemampuan alam untuk menerima atau menampungnya, maka akan terjadi kerusakan
lingkungan (http://www.likomedia.or.id).
Limbah adalah sampah cair dari suatu lingkungan masyarakat dan terutama
terdiri dari air yang telah dipergunakan dengan hampir-hampir 0,1% daripadanya
berupa benda-benda padat yang terdiri dari zat organi dan buka organik (Mahida,
1984).
Limbah cair merupakan gabungan atau campuran dari air dan bahan-bahan
pencemar yang terbawa oleh air, baik dalam keadaan terlarut maupun tersuspensi yang
terbuang dari sumber domestik, sumber industri, dan padsa saat tertentu tercampur
dengan air tanah, air permukaan, atau air hujan.
2.2.1 Sumber Limbah Cair
Pada dasarnya limbah adalah bahan yang terbuang atau dibuang dari suatu
sumber hasil aktivitas manusia maupun proses-proses alam dan atau belum mepunyai
nilai ekonomi bahkan dapat mempunyai nilai ekonomi yang negatif. Menurut
sumber-nya limbah dapat dibagai menjadi :
1. Aktivitas bidang rumah tangga
A. Aktivitas manusia
Aktivitas manusia yang menghasilkan limbah cair sangat beraga, sesuai dengan
kebutuhan hidup manusia yang sangat beragam pula. Beberapa aktivitas manusia yang
menghasilkan limbah cair diantaranya adalah aktivitas dalam bidang rumah tangga,
perkantoran, perdagangan, perindustrian, pertanian, dan pelayanan jasa.
Sangat banyak aktivitas rumah tangga yang menghasilkan limbah cair, antara lain
mencuci kendaraan, penggunaan toliet, dan sebagainya. Semakin banyak jenis
aktivitas yang dilakukan, semakin besar volume limbah cair yang dihasilkan.
2. Aktivitas bidang perkantoran
Aktivitas perkantoran pada umumnya merupakan aktivitas penunjang kegiatan
pelayanan masyarakat. Limbah cair dari sumber ini biasanya dihasilkan dari
aktivitas kantin yang menyediakan makanan dan minuman bagi pegawai, aktivitas
penggunaan toilet, aktivitas pencucian peralatan, dan sebagainya.
3. Aktivitas bidang perdagangan
Kegiatan dalam bidang perdagangan yang menghasilkan limbah cair, yaitu
pengepelan lantai gedung, pencucia alat makan dan minum di restoran,
penggunaan toilet, pencucian pakaian, pencucian kendaraan, dan sebagainya.
4. Aktivitas bidang perindustrian
Aktivitas bidang perindustrian juga sangat bervariasi. Variasi kegiatan bidang
perindustrian dipengaruhi antara lain oleh faktor jenis bahan baku yang diolah,
jenis barang atau bahan jadi yang dihasilkan, kapasitas produksi, teknik proses
produksi yang diterapkan. Jenis aktivitas utama yang menghasilkan limbah cair
dan sifat pencemaran yang potensial.
5. Aktivitas bidang pertanian
Aktivitas bidang pertanian menghasilkan limbah cair karena digunakannya air
untuk mengairi lahan pertanian. Secara alamiah dan dalam kondisi normal, limbah
cair pertanian sebenarnya tidak menimbulkan dampak negatif pada lingkungan,
namun dengan digunakannya fertilizer serta pestisida yang kadang-kadang
dilakukan secara berlebihan, sering menimbulkan dampak negatif pada
keseimbangan ekosistem air pada badan air penerima.
Sangat banyak dan bervariasi aktivitas di berbagai jenis badan usaha pelayanan
jasa, berakibat sangat bervariasinya kuantitas serta kualitas limbah cair.
B.
Hujan merupakan aktivitas alam uang menghasilkan limbah cair yang disebut air
larian. Air hujan yang jatuh ke bumi sebagian akan merembes ke dalam tanah dan
sebagian besar lainnya akan mengalir di permukaan tanah menuju sungai, telaga, atau
tempat lain yang lebih rendah. Air larian yang jumlahnya berlebihan sebagai akibat
dari hujan yang turun dengan intensitas tinggi dan dalam waktu yang lama dapat
menyebabkan saluran air hujan teraliri dalam jumlah yang melebihi kapasitas, dan
dapat menyebabkan terjadinya banjir. Atas dasar itu, air hujan perlu diperhitungkan
dalam perencanaan sistem saluran limbah agar dapat dihindari hal-hal yang tidak
diinginkan dari adanya air hujan, baik bagi lingkungan maupun bagi kesehatan
masyarakat.
2.2.2 Karakteristik Limbah Cair
Limbah domestik terdiri dari pembuangan air kotor. Kotoran-kotoran ini
merupakan campuran yang rumit dari zat-zat bahan mineral dan organik dalam
banyak bentuk. Sampah itu juga mengandung zat-zat hidup, khususnya bakteri, virus,
dan protozoa. Kebanyakan dari bakteri itu secara relatif tidak berbahaya namun
sebagian secara positif berbahaya sebagai penyebab penyakit. Aktivitas Alam
Kadar air limbah sangat tinggi, yaitu 99% atau lebih. Benda-benda padat
dalam limbah dapat berbentuk organik maupun anorganik. Zat organik dalam limbah
terdiri dari bahan-bahan nitrogen, karbohidrat, lemak, dan sabun. Zat tersebut mudah
2.2.3 Teknik Pengolahan Limbah Cair
Berbagai teknik pengolahan air buangan untuk menyisihkan bahan polutannya
telah dicoba dan dikembangkan selama ini. Teknik-teknik pengolahan air buangan
yang telah dikembangkan tersebut secara umum terbagi menjadi 3 metode
pengolahan:
1. Pengolahan secara fisika
2. Pengolahan secara kimia
3. Pengolahan secara biologi
Untuk suatu jenis air buangan tertentu, ketiga metode pengolahan tersebut
dapat diaplikasikan secara sendiri-sendiri atau secara kombinasi.
1. Pengolahan Limbah Secara Fisika
Pada umumnya, sebelum dilakukan pengolahan lanjutan terhadap air buangan,
diinginkan agar bahan-bahan tersuspensi berukuran besar dan yang mudah mengendap
atau bahan-bahan yang terapung disisihkan terlebih dahulu. Penyaringan (screening)
merupakan cara yang efisien dan murah untuk menyisihkan bahan tersuspensi yang
berukuran besar. Bahan tersuspensi yang mudah mengendap dapat disisihkan secara
mudah dengan proses pengendapan. Parameter desain yang utama untuk proses
pengendapan ini adalah kecepatan mengendap partikel dan waktu detensi hidrolis di
dalam bak pengendap.
2. Pengolahan Limbah Secara Kimia
Pengolahan air buangan secara kimia biasanya dilakukan untuk
menghilangkan partikel-partikel yang tidak mudah mengendap (koloid), logam-logam
tertentu yang diperlukan. Penyisihan bahan-bahan tersebut pada prinsipnya
berlangsung melalui perubahan sifat bahan-bahan tersebut, yaitu dari tak dapat
diendapkan menjadi mudah diendapkan (flokulasi-koagulasi), baik dengan atau tanpa
reaksi oksidasi-reduksi, dan juga berlangsung sebagai hasil reaksi oksidasi.
3. Pengolahan Limbah Secara Biologi
Semua air buangan yang biodegradable dapat diolah secara biologi. Sebagai
pengolahan sekunder, pengolahan secara nbiologi dipandang sebagai pengolahan yang
paling murah dan efisien. Dalam beberapa dasawarsa telah berkembang berbagai
metode pengolahan biologi dengan segala modifikasinya.
Pada dasarnya, reaktor pengolahan secara biologi dapat dibedakan atas dua
jenis, yaitu:
1. Reaktor pertumbuhan tersuspensi (suspended growth reaktor);
2. Reaktor pertumbuhan lekat (attached growth reaktor).
Di dalam reaktor pertumbuhan tersuspensi, mikroorganisme tumbuh dan
berkembang dalam keadaan tersuspensi. Proses lumpur aktif yang banyak dikenal
berlangsung dalam reaktor jenis ini. Proses lumpur aktif terus berkembang dengan
berbagai modifikasinya, antara lain: oxidation ditch dan kontak-stabilisasi.
Dibandingkan dengan proses lumpur aktif konvensional, oxidation ditch mempunyai
beberapa kelebihan, yaitu efisiensi penurunan BOD dapat mencapai 85%-90%
(dibandingkan 80%-85%) dan lumpur yang dihasilkan lebih sedikit. Selain efisiensi
yang lebih tinggi (90%-95%), kontak stabilisasi mempunyai kelebihan yang lain, yaitu
waktu detensi hidrolis total lebih pendek (4-6 jam). Proses kontak-stabilisasi dapat
sehingga tidak diperlukan penyisihan BOD tersuspensi dengan pengolahan
pendahuluan.
Kolam oksidasi dan lagoon, baik yang diaerasi maupun yang tidak, juga
termasuk dalam jenis reaktor pertumbuhan tersuspensi. Untuk iklim tropis seperti
Indonesia, waktu detensi hidrolis selama 12-18 hari di dalam kolam oksidasi maupun
dalam lagoon yang tidak diaerasi, cukup untuk mencapai kualitas efluen yang dapat
memenuhi standar yang ditetapkan. Di dalam lagoon yang diaerasi cukup dengan
waktu detensi 3-5 hari saja.
Di dalam reaktor pertumbuhan lekat, mikroorganisme tumbuh di atas media
pendukung dengan membentuk lapisan film untuk melekatkan dirinya. Berbagai
modifikasi telah banyak dikembangkan selama ini, antara lain:
1. Trickling filter
2. Cakram biologi
3. Filter terendam
4. Reaktor fludisasi
Seluruh modifikasi ini dapat menghasilkan efisiensi penurunan BOD sekitar
80% - 90%. Ditinjau dari segi lingkungan dimana berlangsung proses penguraian
secara biologi, proses ini dapat dibedakan menjadi dua jenis:
1. Proses aerob, yang berlangsung dengan hadirnya oksigen;
2. Proses anaerob, yang berlangsung tanpa adanya oksigen.
Apabila BOD air buangan tidak melebihi 400 mg/l, proses aerob masih dapat
dianggap lebih ekonomis dari anaerob. Pada BOD lebih tinggi dari 4000 mg/l, proses
2.3 Amoniak
Adanya amoniak dalam air akan mempengaruhi pertumbuhan biota budi daya.
Pengaruh langsung dari kadar amonia tinggi yang belum me,matikan ialah rusaknya
jaringan insang, dimana lempeng insang membengkak sehingga fungsinya sebagai alat
pernapasan akan terganggu. Sebagai akibat lanjut, dalam keadaan kronis biota budi
daya tidak lagi hidup normal. Penyebab timbulnya amonia dalam air tambak/kolam
adalah sisa-sisa ganggang yang mati, sisa pakan, dan kotoran biota budi daya sendiri
(Sutrisno, 2006).
Amoniak (NH3) dan garam-garamnya bersifat mudah larut dalam air. Ion
Ammonium adalah bentuk transisi dari amoniak. Amoniak banyak digunakan dalam
produksi urea, industri bahan kimia (asam nitrat, amonium fosfat, amonium nitrat, dan
amonium sulfat), sertra industri bubur kertas dan kertas (pulp dan paper). Sumber
amoniak di perairan adalah pemecahan nitrogen organik (protein dan urea) dan
nitrogen anorganik yang terdapat di dalam tanah dan air, yang berasal adri
dekomposisi bahan organik (tumbuhan dan biota akuatik yang telah mati) oleh
mikroba dan jamur. Proses ini dikenal dengan istilah amonifikasi, ditunjukkan dalam
persamaan reaksi berikut:
N organik + O2 → NH3-N + O2→ NO2-N + O2 → NO3
Tinja dari biota akuatik yang merupakan limbah aktivitas metabolisme juga
banyak mengeluarkan amoniak. Sumber amoniak yang lain adalah reduksi gas
nitrogen yang berasal dari proses difusi udara atmosfer, limbah industri, dan domestik.
Amoniak yang terdapat dalam mineral masuk ke badan air melalui erosi tanah. Di -N
perairan alami, pada suhu dan tekanan normal amoniak berada dalam bentuk gas dan
membentuk kesetimbangan dengan gas amonium.
Selain terdapat dalam bentuk gas, amoniak membentuk kompleks dengan
beberapa ion logam. Amoniak juga dapat terserap ke dalam bahan-bahan tersuspensi
dan koloid sehingga mengendap di dasar perairan. Amoniak di perairan dapat
menghilang melalui proses volatilisasi karena tekanan parsial amoniak dalam larutan
meningkat dengan semakin meningkatnya pH. Hilangnya amoniak ke atmosfer juga
dapat meningkat dengan meningkatnya kecepatan angin dan suhu.
Amoniak yang terukur di perairan berupa amoniak total (NH3 dan NH4+).
Amoniak bebas tidak dapat terionisasi, sedangkan amonium (NH4+) dapat terionisasi.
Persentase amoniak bebas meningkat dengan meningkatnya nilai pH dan suhu
perairan. Pada pH atau kurang, sebagian besar amoniak akan mengalami ionisasi.
Sebaliknya, pada pH lebih besar dari 7, amoniak tak terionisasi yang bersifat toksik
terdapat dalam jumlah yang lebih banyak.
Amoniak bebas (NH3
Sumber nitrogen yang dapat dimanfaatkan secara langsung oleh tumbuhan
akuatik adalah nitrat (NO
) yang tidak terionisasi bersifat toksik terhadap
organisme akuatik. Toksisitas amoniak terhadap organisme akuatik akan meningkat
jika terjadi penurunan kadar oksigen terlarut, pH, dan suhu. Avertebrata air lebih
toleran terhadap toksisitas amoniak dari pada ikan. Ikan tidak dapat bertoleransi
terhadap kadar amoniak bebas yang terlalu tinggi karena dapat mengganggu proses
pengikatan oksigen oleh darah dan pada akhirnya dapat mengakibatkan sufokasi.
Akan tetapi, amoniak bebas ini tidak dapat dikur secara langsung.
3), amonium (NH4), dan gas nitrogen (N2). Pupuk yang
mengandung amonium, misalnya urea, berfungsi untuk menambah pasokan nitrogen
jarang ditemukan pada perairan yang mendapat cukup pasokan oksigen. Sebaliknya,
pada wilayah anoksik (tanpa oksigen) yang biasanya terdapat di dasar perairan, kadar
amoniak relatif tinggi.
Kadar amoniak pada perairan alami biasanya kurang dari 0,1 mg/liter. Kadar
amoniak bebas yang tidak terionisasi (NH3
Ada beberapa prosedur yang dikenal untuk menentukan amoniak dalam air,
yaitu metode Nessler, metode phenate, metode elektroda ammonia-selective, metode
gas kromatografi dan metode titrasi. Umumnya sebelum dianalisis dengan metode
tersebut, contoh air diatur dulu pH-nya dengan asam borat sampai 9,5. Pengaturan pH
ini dimaksudkan untuk mengurangi N dan senyawa sianat. Juga umumnya contoh air
didestilasi terlebih dahulu untuk mengurangi jumlah pengganggu. Misalnya akan ) pada perairan tawar sebaiknya tidak lebih
dari 0,2 mg/liter, perairan bersifat toksik bagi beberapa jenis ikan. Kadar amoniak
yang tinggi dapat merupakan indikasi adanya pencemaran bahan organik yang berasal
dari limbah domestik, industri, dan limpasan pupuk pertanian. Kadar amoniak yang
tinggi juga dapat ditemukan pada dasar danau yang mengalami kondisi tanpa oksigen.
Toksisitas akut amoniak yang tidak terionisasi terhadap organisme akuatik sangat
bervariasi (Effendi,H. 2003).
Amoniak digunakan dalam produksi makanan binatang dan pupuk dan di
dalam pembuatan serat, plastik, bahan ledak, kertas, dan karet. Ini digunakan sebagai
suatu pendingin, di dalam pengolahan metal, dan sebagai bahan dasar untuk
kandungan nitrogen campuran. Amoniak dan garam ammonium digunakan di dalam
bahan pembersih dan sebagai aditip makanan, dan ammonium klorida digunakan
sebagai suatu diuretic
ditentukan dengan metode Nessler atau titrasi, destilat dengan asam borat dan bila
akan dianalisis dengan metode phenat harus ditampung dengan asam sulfat. Pemilihan
metode yang mana akan dipakai harus didasarkan atas jumlah ammonia yang
terkandung dalam contoh air.
Metode Nessler dapat digunakan untuk amoniak dengan kadar 0,02 ppm.
Dengan metode ini pendahuluan dengan reagensia ZnSO4 mutlak dilakukan agar
pengotor Ca, Mg, Fe, dan S mengendap dari kkeruhan. Reagensia Nessler (campuran
HgI2 dan KI dalam larutan NaOH) dengan amoniak akan membentuk warna kuning
yang dapat diukur pada panjang gelombang 400-425 nm. Untuk kuvet 1 cm
konsentrasi NH3 – N yang dapat diukur yaitu 0,4-5 ppm. Selain itu, metode Nessler
dengan KIT ini menggunakan senyawa dengan logam berat Hg dengan pengamatan
warna secara visual baru tampak jelas bila perbedaan kadar NH3 nya 2 ppm.
Metode elektroda amoniak-selective dan gas kromatografi perlu alat khusus
dan keterampilan khusus sehingga tidak cocok untuk di lapangan yang pengukurannya
harus segera dilakukan setiap hari.
Metode phenat sebetulnya merupakan metode yang tepat bila ditinjau dari
kepekaannya yang tinggi yaitu 10 ppb tetapi kelemahannya reagensia phenat
(campuran phenol dan NaOH) ini tidak stabil. Hanya tepat pengukurannya bila
reagensia phenat dibuat setiap hari.
Metode titrasi umumnya digunakan, tetapi mempunyai kelemahan karena
terjadi deviasi yang sangat besar sehingga tidak cocok untuk diterapkan pada air
tambak/kolam yang mempunyai kadar NH3 sangat rendah. Metode titrasi sangat
cocok pada contoh air dengan amoniak 5 ppm. Walaupun demikian, metode ini tetap
Salah satu dari penentuan colorimetric untuk menentukan amoniak yang paling
tua adalah nesslerisasi. Nesslerisasi merupakan reaksi antara kalium mercuric iodida
dan amoniak untuk membentuk suatu koloidal mercuric iodid ammono-basic
merah-coklat yang kompleks:
2(HgI2 . 2KI) + 2NH3→ NH2Hg2I3 + 4KI + NH4
Kandungan campuran nitrogen organik di dalam contoh dapat diubah ke garam
ammonium dengan proses kjedahl, dan amoniak yang yang dihasilkan ditentukan
secara spectrofotometri dengan salah satu dari metoda di atas. Ini mungkin
dilaksanakan mengikuti kepindahan amoniak yang diuraikan di atas dari contoh
dengan penyulingan untuk menciri nitrogen organik dari amoniak, kalau tidak suatu
contoh aliquot yang terpisah mungkin diproses dan nitrogen organik yang ditentukan
dengan perbedaan antara yang dicerna ( amoniak yang lebih nitrogen organik) dan
belum dicernakan ( amoniak) aliquot.
I
Absorbansi diukur pada 425 nm. kalsium, magnesium, besi, dan sulfida
bertentangan dengan reaksi nesslerisasi. Sulfida mungkin diendapkan dengan
karbonat. Gangguan ion logam mungkin diatasi dengan penyulingan amoniak dari
larutan bersifat alkali ke dalam cairan asam borik sebelum nesslerisasi. Persiapan
bahan reaksi nessler adalah berdasar kepada batch demi batch variabilitas di dalam
warna, dan bahan reaksi tidak tersimpan dengan baik, sedemikian sehingga batch baru
harus sering disiapkan.
Metoda yang lain untuk menentukan amoniak adalah berdasar pada reaksi
amoniak dengan suatu zat fenol, nitroprusside, dan hipoklorit di dalam suatu medium
bersifat alkali. Absorbansi dari larutan yang dihasilkan, diukur pada 660 nm, apakah
berbanding lurus kepada konsentrasi amoniak. Kedua sistem ini mampu menentukan
Dengan metoda apapun juga, penentuan amoniak diganggu oleh kesukaran
(dalam) perolehan ( dan memelihara) reagent bebas ammonia, terutama air, dalam
kaitan dengan daya larut gas amoniak yang tinggi di dalam air dan pada fakta bahwa
penyulingan dan kolom penukar ion biasa tidak memindahkan amoniak dari air. Ini
diperlukan untuk membawa bahan reaksi yang kosong sedikitnya sehari dan tinggal
waspada untuk mencegah penggunaan konsentrasi larutan ammonium hidroksida yang
terbuka di dalam laboratorium selama pengukuran. Jika air laboratorium tercemar,
penyulingan dari larutan asam atau penggunaan penukar ion ammonia-removing
khusus harus digunakan untuk memperoleh bahan reaksi air bebas ammonia (Minear,
1984).
J. nessler di tahun 1856 pertama mengusulkan suatu larutan mercuric iodida
yang bersifat alkali di dalam kalium iodida sebagai bahan reaksi untuk penentuan
amoniak secara colorimetri. Berbagai modifikasi dari bahan reaksi sejak itu telah
dibuat. Ketika bahan reaksi nessler ditambahkan untuk melarutkan suatu larutan
garam amoniak, amoniak bebas bereaksi dengan bahan reaksi dengan cepat tetapi
tidak langsung membentuk suatu hasil orange-coklat, yang mana tersisa di dalam
larutan koloidal, tetapi flocculate sudah bertahan lama.Perbandingan colorimetri harus
dibuat sebelum flocculasi terjadi.
Reaksi dengan bahan reaksi nessler (suatu larutan kalium mercuri-iodida yang
bersifat alkali) mungkin ditunjukkan seperti persamaan reaksi berikut:
2K2(HgI4) + 2NH3→ NH2Hg2I3 + 4KI + NH4
Bahan reaksi digunakan untuk penentuan amoniak dalam larutan amoniak cair
di (dalam) air. Di hadapan unsur yang bertentangan, itu terbaik untuk memisahkan
ini juga dapat digunakan untuk penentuan nitrat dan nitrit: ini dikurangi di dalam
laruan bersifat alkali dengan campuran logam devarda ke amoniak, yang mana
dipindahkan dengan penyulingan. Prosedur ini juga dapat digunakan untuk
konsentrasi amoniak yang sama rendah seperti 0,1 mg/liter (Vogel, 1984).
2.5 Spektrofotometri
Spektrofotometri sesuai dengan namanya adalah alat yang terdiri dari
spektrometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum dengan
panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya
yang ditransmisikan atau yang diabsorbsi. Jadi spektrofotometer digunakan untuk
mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan atau
diemisikan sebagai fungsi dari panjang gelombang. Kelebihan spektrofotometer
dibandingkan fotometer adalah panjang gelombang dari sinar putih dapat lebih
terseleksi dan ini diperoleh dengan alat pengurai seperti prisma, grating ataupun celah
optis. Pada fotometer filter, sinar dengan panjang gelombang yang diinginkan
diperoleh dengan berbagai filter dari berbagai warna yang mempunyai spesifikasi
melewatkan trayek panjang gelombang tertentu. Pada fotometer filter, tidak mungkin
diperoleh panjang gelombang yang benar-benar monokromatis, melainkan suatu
trayek panjang gelombang 30 - 40 nm. Sedangkan pada spektrofotometer, panjang
gelombang yang benar-benar terseleksi dapat diperoleh dengan bantuan alat pengurai
cahaya sperti prisma. Suatu spektrofotometer tersusun dari sumber spektrum tampak
yang kontinyu, monokromator, sel pengabsorbsi untuk larutan sampel atau blanko dan
suatu alat untuk mengukur perbedaan absorbsi antara sampel dan blanko ataupun
1. Sumber: sumber yang biasa digunakan pada spektroskopi absorbsi adalah lampu
wolfram. Arus cahaya tergantung pada tegangan lampu, variasi tegangan masih
dapat diterima 0,2% pada suatu sumber DC. Lampu hidrogen atau lampu
deuterium digunakan untuk sumber pada daerah UV. Kebaikan lampu wolfram
adalah energi radiasi yang dibebaskan tidak bervariasi pada berbagai panjang
gelombang. Untuk memperoleh tegangan yang stabil dapat digunakan
transformator.
2. Monokromator : digunakan untuk memperoleh sumber sinar yang monokromatis.
Alatnya dapat berupa prisma ataupun grating. Untuk mengarahkan sinar
monokromatis yang diinginkan dari hasil penguraian ini dapat digunakan celah.
Jika celah posisinya tetap, maka prisma atau gratingnya yang dirotasikan untuk
mendapatkan λ yang diinginkan.
3. Sel Absorbsi : pada pengukuran di daerah tampak kuvet kaca atau kuvet kaca
corex dapat digunakan, tetapi untuk pengukuran pada daerah UV kita harus
menggunakan sel kuarsa karena gelas tidak tembus cahya pada daerah ini.
Umumnya tebal kuvetnya adalah 10 mm, tetapi yang lebih kecil ataupun yang
lebih besar dapat digunakan. Sel yang biasa digunakan berbentuk persegi, tetapi
bentuk silinder dapat juga digunakan. Sel yang baik adalah kuarsa atau gelas hasil
leburan serta seragam keseuruhannya.
4. Detektor : peranan detektor penerima adalah memberikan respon terhadap cahaya
pada berbagai panjang gelombang. Pada spektrofotometer, tabung pengganda
BAB 3
BAHAN DAN METODE
3.1 Bahan-bahan :
1. larutan nessler
2. Aquadest
3.2 Sampel
Sampel diambil dari tempat penampungan limbah yang berasal dari beberapa
laboratorium yang di Balai Riset dan standardisasi Industri Medan. Dimana sampel
diambil dari dua titik yang berbeda, yaitu inlet dan outlet. Sebelum sampel diambil,
terlebih dahulu diukur pH dengan menggunakan kertas pH. Lalu diambil sampel
dengan menggunakan wadah plastik tanpa adanya gelembung udara.
3.3 Peralatan
1. spektrofotometer DR 2000/2010
2. beaker glass
3. pipet volume 20 ml
4. pipet ukur
5. erlenmeyer 250 ml
3.4 Prosedur Analisa
1. Dilarutkan 100 gr HgI2 dan 70 gr KI ke dalam sedikit air.
Pembuatan larutan pereaksi nessler :
2. Dimasukkan sedikit demi sedikit ke dalam air dingin yang mengandung 160 gr
NaOH sambil terus diaduk dengan hati-hati.
3. Diencerkan sampai satu liter.
4. Disimpan dalam botol gelap dan ditempakan di tempat dingin.
1. Dioptimalkan alat spektrofotometer sesuai dengan petunjuk penggunaan alat
untuk pengujian kadar ammonium
Penentuan kalibrasi :
2. Diukur 50 ml larutan baku (standard) dan dimasukkan kedalam labu
Erlenmeyer 100 ml
3. Ditambahkan 1 ml larutan nessler, dikocok dan dibiarkan selama ± 10 menit
4. Dimasukkan kedalam kuvet pada alat spektrofotometer, dibaca dan dicatat
hasilnya
1. Dipipet 50 ml masing-masing sampel kedalam erlenmeyer 250 ml
Penentuan Kadar Ammonium
2. Ditambahkan 1 ml larutan nessler kedalam masing-masing erlenmeyer yang
telah berisi sampel
3. Didiamkan selama ±10 menit
4. Dimasukkan kedalam kuvet pada alat spektrofotometer, diukur kadar
ammonium sampel pada spektrofotometri DR 2000/2010 pada panjang
gelombang 425 nm
← Dipipet 50 ml masing-masing sampel
kedalam erlenmeyer 250 ml
← ditambahkan 1 ml pereaksi nessler
← didiamkan selama ± 10 menit Flowchart
← dimasukkan kedalam kuvet
← diukur absorbansinya pada alat
spektrofotometer DR 2000/2010 pada
panjang gelombang 425 nm
← dicatat hasil kadar amonia Sampel
Larutan kuning pucat
3.5 Prinsip Percobaan
Pereaksi Nesler (K2H4I4) bila bereaksi dengan ammonium dalam larutan basa
akan membentuk dispersi koloid yang berwarna kuning coklat. Intensitas warna
yang akan terjadi berbanding lurus dengan konsentrasi ammonium. Warna yang
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil
Dari analisa kadar amoniak yang dilakukan selama empat minggu diperoleh
hasil data analisa sebagai berikut :
4.1.1
No.
Data Analisa Kadar Amoniak dari Sampel Limbah Cair Laboratorium
BARISTAND
Tabel 4.1.1.1 Data analisa pada minggu I
Sampel NH3 – N (mg/l)
1. Inlet 4,05
2. Outlet 1,73
Tabel 4.1.1.2 Data analisa pada minggu II
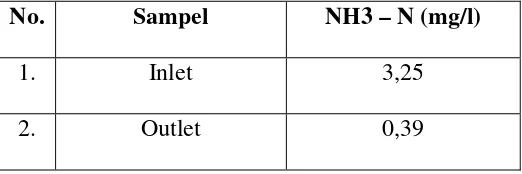
No. Sampel NH3 – N (mg/l)
1. Inlet 3,25
Tabel 4.1.1.3 Data analisa pada minggu III
No. Sampel NH3 – N (mg/l)
1. Inlet 2,6
2. Outlet 1,57
Tabel 4.1.1.4 Data analisa pada minggu IV
No. Sampel NH3 – N (mg/l)
1. Inlet 1,30
2. Outlet 1,01
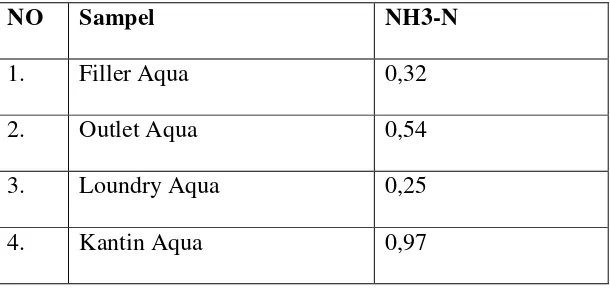
Tabel 4.1.2 Data analisa sampel Limbah Cair Industri AQUA Data Analisa Kadar Amoniak Sampel Limbah Cair Industri AQUA
NO Sampel NH3-N
1. Filler Aqua 0,32
2. Outlet Aqua 0,54
3. Loundry Aqua 0,25
4.2 Pembahasan
Limbah cair berbagai industri terutama limbah agroindustri yang berkembang
sangat pesat adalah salah satu masalah serius yang dihadapi oleh masyarakat
Indonesia. Berbagai kasus pencemaran telah sering didengar dan dilihat langsung baik
melalui surat kabar, majalah, radio, internet, TV, atau bahkan obrolan dengan teman.
Didalam implementasi persfektif penangganan limbah cair dimasa depan, kita
haruslah memandang bahwa semua sistem pengolahan limbah cair adalah industri.
Dengan memandang sistem pengolahan limbah cair sebagai industri maka diharapkan
akan meningkatkan efisiensi dan memberi perhatian lebih terhadap pemakaian bahan
dan produknya
Limbah industri sangat beragam, sesuai dengan jenis industri. Berbagai jenis
industri berpotensi mencemari lingkungan diantaranya adalah industri tekstil, cat,
penyamakan kulit, farmasi, dan industri pangan. Limbah industri pangan dapat
menim-bulkan masalah dalam penanganannya karena mengandung sejumlah besar
karbohi-drat, protein, lemak, garam-garam mineral, dan sisa-sisa bahan kimia yang
digunakan di dalam proses produksi. Contoh beberapa industri pangan yang
menghasilkan limbah seperti ini adalah produk susu, pengalengan dan pengawetan
buah-buahan dan sayuran, pengalengan dan pengawetan hasil laut, pemurnian gula,
permen, produk daging, pengawetan dan pengalengan daging, serta penggilingan
biji-bijian.
Masalah pencemaran karena buangan limbah yang tidak dikelola dengan baik
seringkali tidak hanya disebabkan oleh industri besar, tetapi juga oleh industri kecil
yang seringkali belum mempunyai fasilitas pengolah limbah. Mengingat jumlah
industri kecil yang sangat banyak dan lokasi yang menyebar, maka hal ini perlu
pengolah limbah dan adanya Keputusan Menteri Negara Kependudukan dan
Lingkungan Hidup Republik Indonesia Nomor : KEP 03/MENKLH/II/1991 tentang
Baku Mutu Limbah Cair bagi Kegiatan yang Sudah Beroperasi, seharusnya dapat
mengelola limbah yang dihasilkan dengan prosedur yang benar dan bertanggung
jawab, namun dalam pelaksanaannya masih sering terjadi pelanggaran.
Kadar amonia pada perairan alami biasanya kurang dari 0,1 mg/liter. Kadar
amonia bebas yang tidak terionisasi (NH3) pada perairan tawar sebaiknya lebih dari
0,02 mg/liter. Jika kadar amonia bebas lebih dari 0,2 mg/liter, perairan bersifat toksik
bagi beberapa jenis ikan. Kadar amonia yang tinggi dapat merupakan indikasi adanya
pencemaran bahan organik yang berasal dari limbah domestik, industri dan limpasan
pupuk pertanian. Kadar amonia yang tinggi juga dapat ditemukan pada dasar danau
yang mengalami kondisi tanpa oksigen. (Effendi, 2003)
Ada beberapa prosedur yang dikenal untuk menentukan amoniak dalam air,
yaitu metode Nessler, metode phenate, metode elektroda ammonia-selective, metode
gas kromatografi dan metode titrasi. Umumnya sebelum dianalisis dengan metode
tersebut, contoh air diatur dulu pH-nya dengan asam borat sampai 9,5. Pengaturan pH
ini dimaksudkan untuk mengurangi N dan senyawa sianat. Juga umumnya contoh air
didestilasi terlebih dahulu untuk mengurangi jumlah pengganggu. Misalnya akan
ditentukan dengan metode Nessler atau titrasi, destilat dengan asam borat dan bila
akan dianalisis dengan metode phenat harus ditampung dengan asam sulfat. Pemilihan
metode yang mana akan dipakai harus didasarkan atas jumlah ammonia yang
BAB 5
KESIMPULAN DAN SARAN
5.1Kesimpulan
Dari data analisa dan pembahasan yang telah dijelaskan di atas, maka dapat
diperoleh kesimpulan sebagai berikut :
1. Hasil analisa kadar amoniak bebas (NH3
minggu I : 1,73 mg/liter
minggu II : 0,39 mg/liter
minggu III : 1,57 mg/liter
minggu IV : 1,01 mg/liter
) yang diperoleh dari limbah cair
laboratorium Balai Riset Standardisasi Industri adalah sebagai berikut :
2. Untuk limbah cair yang berasal dari luar laboratorium (pabrik aqua) diperoleh
kadar amonia bebas sebagai berikut :
Filler Aqua : 0,32 mg/liter
Outlet Aqua : 0,54 mg/liter
Loundry Aqua : 0,25 mg/liter
Kantin Aqua : 0,97 mg/liter
3. Dari hasil analisa di atas diketahui bahwa kadar amoniak yang diperoleh masih
sesuai dengan kualitas baku mutu limbah cair industri menurut keputusan
5.2 Saran
Warna merupakan salah satu gangguan dalam analisa kadar amoniak. Oleh
karena itu, sampel air yang pekat atau berwarna sebaiknya diencerkan terlebih daulu
sebelum penambahan larutan pereaksi nessler. Hal ini dimaksudkan agar absorbansi
Alaerts, G. 1984. Metoda Penelitian Air. Surabaya: Penerbit Usaha-Nasional.
Effendi, H. 2003. Telaah Kualitas Air Bagi Pengelolaan Sumber Daya dan
Lingkungan Perairan. Yogyakarta: Kanisius.
Khopkar, S.M. 2003. Konsep Dasar Kimia Analitik. Jakarta: UI-Press.
Mahida, U.N. 1984. Pencemaran Air Dan Pemanfaatan Limbah Industri. Jakarta:
Penerbit Rajawali.
Minear, R.A. 1984. Water Analysis Volume II Inorganic Species. Part 2. Florida:
Academy Press,inc.
Soeparman. 2001. Pembuangan Tinja dan Limbah Cair. Jakarta: Penerbit Buku
Kedokteran EGC.
Sutrisno, T.C. 2006. Teknologi Penyediaan Air Bersih. Cetakan Keenam. Jakarta:
Rieneka Cipta.
Vogel, A.I. 1994. Kimia Analisis Kuantitatif Anorganik. Edisi 4. Jakarta: Penerbit