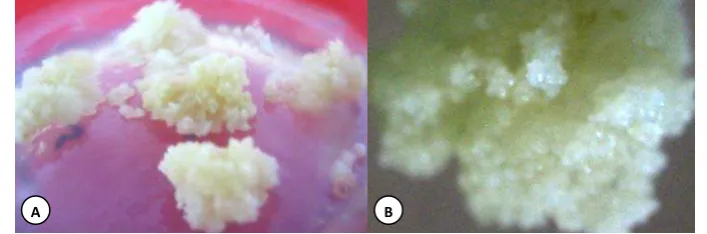
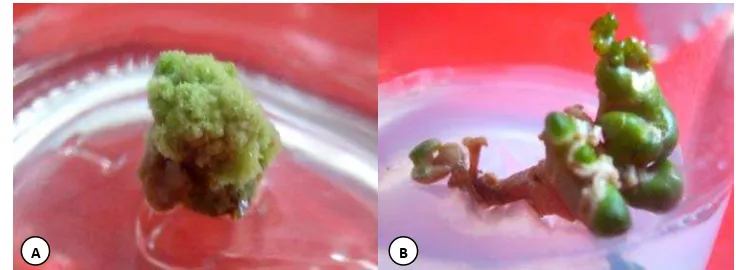
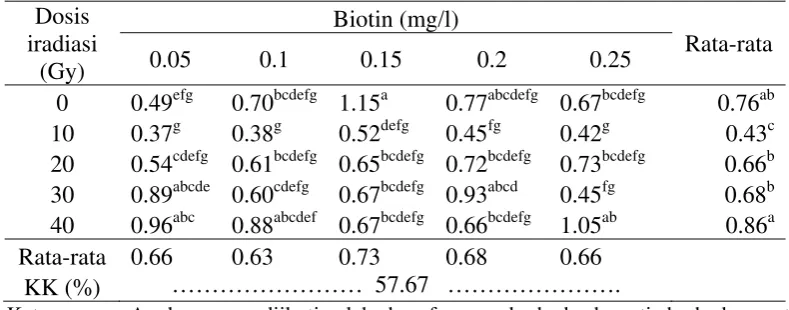
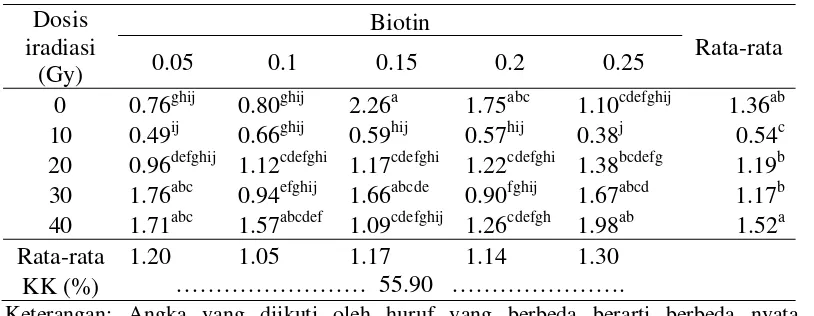
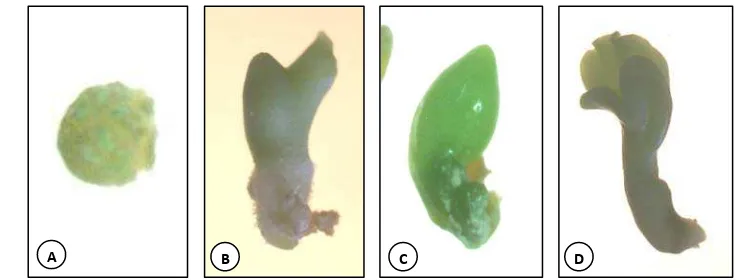
Induksi keragaman genetik dengan sinar gamma pada jeruk siam pontianak secara in vitro
Teks penuh
Gambar



Dokumen terkait
tujuan khusus penelitian ini adalah: mendapatkan metode induksi kalus embriogenik, embrio somatik dan proliferasi dari tiga varietas gandum (Dewata, Selayar dan Nias),
Percobaan ini dilakukan untuk mempelajari dosis iradiasi sinar gamma Cobalt 60 terhadap induksi keragaman genetik pada padi varietas Sintanur, mempelajari tekanan
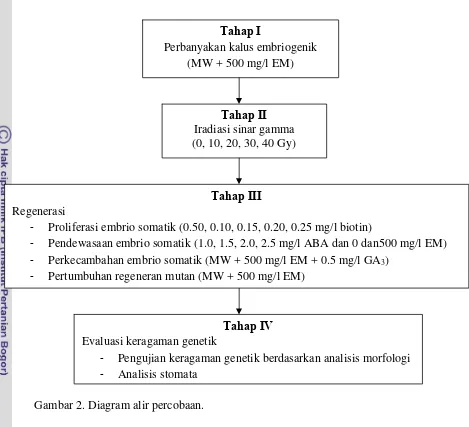
Penelitian ini terdiri atas proliferasi kalus embriogenik, pendewasaan, perkecambahan embrio somatik (ES), pertumbuhan tunas dan akar. Penelitian terdiri atas
Iradiasi sinar gamma berpengaruh nyata terha- dap diameter kalus, bobot segar kalus, dan bobot ke- ring kalus pada umur 60 dan 90 hari setelah iradiasi, sedangkan volume kalus
Iradiasi sinar gamma berpengaruh nyata terha- dap diameter kalus, bobot segar kalus, dan bobot ke- ring kalus pada umur 60 dan 90 hari setelah iradiasi, sedangkan volume kalus
Aplikasi iradiasi sinar gamma dosis rendah pada kalus embriogenik varietas Dewata yang dilanjutkan dengan seleksi in vitro ketahanan terhadap suhu tinggi
Penelitian ini terdiri dari dua percobaan yaitu 1) Iradiasi sinar gamma pada kalus embriogenik jeruk keprok SoE untuk mendapatkan nilai LD 50. 2) Seleksi untuk mendapatkan
Respon kalus lili Asiatik cv.Purple Maroon terhadap iradiasi sinar Gamma hampir sama dengan lili Oriental cv.Sorbon, yaitu semakin tinggi dosis iradiasi maka semakin rendah