EKSTRAKSI DAN ANALISIS AGAR-AGAR DARI RUMPUT LAUT Gracilaria sp. MENGGUNAKAN ASAM JAWA
SKRIPSI
Disusun Oleh: RINI SEPTI MAULI
NIM. 140704011
PROGRAM STUDI KIMIA FAKULTAS SAINS DAN TEKNOLOGI UNIVERSITAS ISLAM NEGERI AR-RANIRY
BANDA ACEH 2018 M / 1439 H
vi
KATA PENGANTAR
Puji syukur ke hadirat Allah SWT yang telah melimpahkan rahmat, hidayah dan inayah-Nya sehingga penulis dapat menyelesaikan skripsi dengan judul “Ekstraksi dan Analisis Agar-Agar dari Rumput Laut Gracilaria sp. Menggunakan Asam Jawa”. Tak lupa pula penulis kirimkan shalawat serta salam kepada junjungan Nabi Besar Muhammad SAW beserta keluarganya, para sahabatnya, dan seluruh ummatnya yang senantiasa istiqomah hingga akhir zaman. Penulisan skripsi ini bertujuan untuk melengkapi tugas-tugas dan memenuhi syarat-syarat untuk menyelesaikan pendidikan pada Universitas Islam Negeri Ar-Raniry Banda Aceh.
Penulis mengucapkan terimakasih yang sebesar-besarnya kepada semua pihak yang telah membantu penulis dalam melaksanakan penelitian dan menyelesaikan skripsi. Penulis juga banyak mendapatkan pengetahuan dan wawasan baru yang sangat berharga. Penulis juga tidak lupa mengucapkan terima kasih kepada:
Yang teristimewa kedua orang tua tercinta Azhari Mubin dan Nurlaili yang telah menjadi orang tua terhebat yang selalu memberikan motivasi, cinta, nasehat, perhatian dan kasih sayang yang tiada tara serta doa yang selalu mengiringi setiap langkah penulis.
1. Kakak Desi Aulia Purnama dan kedua adik Siti Ema Maghfirah dan M. Teguh Kurniawan yang selalu menemani dan menghibur penulis, semoga kita bisa meraih masa depan yang lebih baik dan mendapatkan semua apa yang dicita-citakan.
2. Bapak Muammar Yulian, M.Si, selaku Ketua Prodi Kimia Fakultas Sains dan Teknologi Universitas Islam Negeri Ar-Raniry Banda Aceh.
3. Sitti Saleha, M.Si, sebagai pembimbing pertama yang telah membimbing penulis dalam menyelesaikan skripsi.
4. Bhayu Gita Bhernama, M.Si, sebagai pembimbing kedua yang telah membantu penulis dan mengarahkan penulis demi kesempurnaan skripsi ini.
5. Seluruh Ibu/Bapak dosen di Prodi Kimia Fakultas Sains dan Teknologi Universitas Islam Negeri Ar-Raniry Banda Aceh.
vii
6. Sahabat-sahabat penulis yang sudah meluangkan waktu untuk membantu penulis dalam menyelesaikan penelitian dan skripsi (Cut Aoyna Maulina Najib, Nisa Ulfitri, Musauwir Ikhfar, Nasrullah dan Mahazir), sahabat-sahabat di meja diskusi yang telah mengubah pola pikir penulis serta sahabat-sahabat di meja kopi yang telah sama-sama berbagi canda dan tawa, sahabat-sahabat seperjalan yang telah berbagi pengalaman dan cerita selama perjalanan.
7. Semua teman-teman dan kawan seperjuangan angkatan 2014 yang telah memberi dukungan dan motivasi selama penelitian dan penulisan skripsi.
8. Semua pihak yang turut membantu dalam penyusunan skripsi ini.
Semoga amal baik mereka mendapatkan balasan dari Allah SWT dengan balasan yang berlipat ganda.
Penulis menyadari bahwa dengan segala keterbatasan, skripsi ini masih jauh dari sempurna, sehingga masukan dan kritikan sangat penulis harapkan demi sempurnanya skripsi ini. Akhir kata penulis berharap semoga skripsi ini dapat bermanfaat untuk semua orang khususnya untuk para pembaca dan dapat menjadi referensi dalam melaksanan penelitian dan penulisan skripsi lainnya.
Banda Aceh, 16 Januari 2019 Penulis,
viii DAFTAR ISI
Halaman
LEMBAR PERSETUJUAN ... i
LEMBAR PENGESAHAN ... ii
LEMBAR PERNYATAAN KEASLIAN ... iii
ABSTRAK ... iv
ABSTRACT ... v
KATA PENGANTAR ... vi
DAFTAR ISI ... viii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xii
BAB I PENDAHULUAN 1.1 Latar Belakang ... 1 1.2 Rumusan Masalah ... 3 1.3 Tujuan Penelitian ... 3 1.4 Manfaat Penelitian ... 3 1.5 Batasan Masalah... 4
BAB II TINJAUAN PUSTAKA 2.1 Rumput Laut Gracilaria sp. ... 5
2.2 Agar-agar... 8
2.3 Asam Jawa ... 11
2.4 Maserasi ... 12
2.5 Fourier Transform Infrared (FTIR) ... 14
BAB III METODOLOGI PENELITIAN 3.1 Waktu dan Tempat Penelitian ... 16
ix
3.2 Alat dan Bahan ... 16
3.3 Prosedur Kerja ... 17
3.4 Bagan Alir ... 20
BAB IV DATA HASIL PENGAMATAN DAN PEMBAHASAN 4.1 Data Hasil Pengamatan ... 21
4.2 Pembahasan ... 21 BAB V PENUTUP 5.1 Kesimpulan ... 33 5.2 Saran ... 33 DAFTAR PUSTAKA ... 34 LAMPIRAN ... 41 RIWAYAT HIDUP ... 49
x
DAFTAR TABEL
Halaman Tabel 2.1 Standar Mutu Agar-agar... 10 Tabel 4.1 Data Hasil Pengamatan Ekstraksi Agar-agar Praperlakuan Asam Jawa 21 Tabel 4.2 Identifikasi Gugus Fungsi Agar-agar Praperlakuan Asam Jawa ... 31
xi DAFTAR GAMBAR Halaman Gambar 2.1 G. gigas ... 6 Gambar 2.2 G. verrucosa ... 7 Gambar 2.3 G. lichenoides ... 7
Gambar 4.1 Grafik hubungan konsentrasi asam jawa dengan % rendemen ... 25
Gambar 4.2 Grafik hubungan konsentrasi asam jawa dengan kekuatan gel ... 27
Gambar 4.3 Grafik hubungan konsentrasi asam jawa dengan kadar sulfat ... 29
Gambar 4.4 Struktur penyusun agar-agar ... 32
xii
DAFTAR LAMPIRAN
Halaman Lampiran 1. Perhitungan ... 41 Lampiran 2. Foto-foto Penelitian ... 45
iv ABSTRAK Nama : Rini Septi Mauli
Program Studi : Kimia
Judul : Ekstraksi dan Analisis Agar-Agar dari Rumput Laut Gracilaria sp. Menggunakan Asam Jawa
Gracilaria sp. merupakan salah satu jenis rumput laut penghasil agar-agar. Agar-agar adalah senyawa ester asam sulfat dari senyawa galaktan, tidak larut dalam air dingin, tetapi larut dalam air panas dengan membentuk gel. Produksi agar-agar di Indonesia menggunakan metode yang melibatkan ekstraksi rumput laut dengan pelarut asam pada suhu tinggi. Penelitian ini dilakukan untuk melihat pengaruh dan kualitas agar-agar yang dihasilkan dari proses ekstraksi agar-agar-agar-agar pada perlakuan asam jawa sehingga dapat meminimalisir harga produksi agar-agar. Sampel yang digunakan adalah rumput laut Gracilaria sp. yang diperoleh dari tambak di Desa Neuhen, Kecamatan Mesjid Raya, Kabupaten Aceh Besar, dan asam jawa yang diperoleh dari Gampong Lamtrieng, Kecamatan Kuta Baro, Kabupaten Aceh Besar, Provinsi Aceh. Penelitian ini dilaksanakan pada bulan Agustus sampai September 2018 bertempat di Laboratorium Kimia Fakultas Sains dan Teknologi Universitas Islam Negeri Ar-Raniry Banda Aceh dan Laboratorium Kimia Fakultas Keguruan Ilmu Pengetahuan Universitas Syiah Kuala. Metode yang digunakan pada penelitian ini adalah metode ekstraksi secara maserasi. Pada proses ekstraksi, rumput laut Gracilaria sp. direndam dengan ekstrak asam jawa pada variasi konsentrasi yang ditentukan secara Rancangan Acak Lengkap (RAL), yaitu 5%, 10% dan 15% untuk melunakkan dinding sel rumput laut, kemudian dibersihkan dan dimasak dengan air pada suhu 90-100oC selama 90 menit. Analisis yang dilakukan terhadap agar-agar meliputi rendemen, kekuatan gel, kadar sulfat dan spektra FTIR. Hasil penelitian menunjukkan bahwa variasi konsentrasi asam jawa berpengaruh terhadap rendemen, kekuatan gel dan kadar sulfat agar-agar. Pada konsentrasi asam jawa 5%, 10% dan 15% menghasilkan nilai rendemen yang berturut-turut sebesar 28,8%, 35,35% dan 40,5%, dengan nilai kekuatan gel berturut-turut sebesar 168,28 g/cm2, 178,85 g/cm2, dan 193,24 g/cm2, sedangkan kadar sulfat agar–agar yang dihasilkan sebesar 3%, 2% dan 1,5%. Semakin tinggi konsentrasi asam jawa maka rendemen dan kekuatan gel yang dihasilkan semakin tinggi pula, sedangkan kadar sulfatnya semakin rendah. Analisa agar-agar dengan FTIR menunjukkan pita serapan C-H dari 3,6-anhidrogalaktosa yang muncul pada bilangan gelombang tertentu, agar-agar dengan konsentrasi asam jawa 5%, 10% dan 15% muncul pada bilangan gelombang 2919.56 (cm-1), 2919.24 (cm-1) dan 2916.41 (cm-1) sedangkan agar-agar komersil muncul pada bilangan gelombang 2897.61(cm-1) sehingga diduga setiap spektra perlakuan asam jawa menghasilkan senyawa yang sama yaitu agar-agar. Hasil terbaik diperoleh pada perlakuan asam jawa 15%. Hal ini menunjukkan bahwa asam jawa dapat digunakan dalam proses pembuatan agar-agar, selain harganya murah, limbahnya juga tidak merusak lingkungan.
v ABSTRACT Name : Rini Septi Mauli
Study Program : Kimia
Title : Extraction and Analysis of Agar-agar from Seaweed Gracilaria sp. Using Tamarind
Gracilaria sp. is one type of agar-producing seaweed. Agar is a sulfuric acid ester compound from galactant compounds, insoluble in cold water, but soluble in hot water by forming a gel. Agar production in Indonesia uses a method that involves extracting seaweed with acid solvents at high temperatures. This research was conducted to see the effect and quality of agar produced from the agar extraction process in the acidic treatment of Java so as to minimize the price of agar production. The sample used was seaweed Gracilaria sp. obtained from farms in Neuhen Village, Mesjid Raya Subdistrict, Aceh Besar District, and Asam Javan which were obtained from Gampong Lamtrieng, Kuta Baro District, Aceh Besar District, Aceh Province. This research was conducted from August to September 2018 at the Chemistry Laboratory of the Faculty of Science and Technology, Ar-Raniry Banda Aceh State Islamic University and the Chemistry Laboratory of the Teacher Training Faculty of Syiah Kuala University. The method used in this study is the maceration extraction method. In the extraction process, Gracilaria sp. soaked with tamarind extract at various concentrations determined by Completely Randomized Design (CRD), which is 5%, 10% and 15% to soften the seaweed cell walls, then cleaned and cooked with water at a temperature of 90-100oC for 90 minutes. Analysis carried out on agar includes yield, gel strength, sulfate content and FTIR spectra. The results showed that variations in the concentration of tamarind had an effect on the yield, gel strength and sulfate content of agar. At the concentration of tamarind acid 5%, 10% and 15% produce a yield value of 28.8%, 35.35% and 40.5% respectively, with gel strength values of 168.28 g/cm2 respectively. 178.85 g/cm2, and 193.24 g/cm2, while the agar content of sulfate was 3%, 2% and 1.5%. The higher the concentration of tamarind, the higher the yield and strength of the gel, while the lower the sulfate content. Agar analysis using FTIR showed C-H absorption band of 3,6-anhydrogalactose which appeared at certain wave numbers, agar with a concentration of java acid 5%, 10% and 15% appeared at wave number 2919.56 (cm-1), 2919.24 (cm-1) and 2916.41 (cm-1) while commercial agar appears at wave number 2897.61 (cm-1) so that it is assumed that each acidic treatment spectra produces the same compound, namely agar. The best results were obtained at 15% tamarind acid treatment. This shows that tamarind can be used in the process of making agar, besides being cheap, the waste also does not damage the environment.
1 BAB I
PENDAHULUAN
1.1Latar Belakang
Indonesia sebagai negara kepulauan dengan jumlah 17.504 pulau dan panjang garis pantai mencapai 81.000 Km memiliki potensi yang sangat besar bagi pengembangan komoditi rumput laut. Pada saat ini pengembangan industri rumput laut (alga) masih menjadi salah satu program revitalisasi Kementerian Kelautan dan Perikanan, karena komoditas rumput laut memberikan kontribusi dan penyumbang devisa negara terbesar setelah komoditas udang dan tuna. Pengembangan industri rumput laut di Indonesia memiliki prospek yang cerah. Hal ini disebabkan karena teknik pembudidayaan rumput laut yang relatif mudah dikuasai oleh masyarakat, sehingga usaha tersebut dapat dilakukan secara massal. Disamping itu, permintaan terhadap rumput laut dan produk olahannya baik di pasar domestik maupun internasional selalu menunjukkan peningkatan setiap tahunnya (Sudariastuty, 2011).
Dalam rangka peningkatan nilai tambah serta nilai jualnya, maka pengembangan usaha budidaya rumput laut harus diikuti dengan pengembangan industri pengolahannya. Potensi sumberdaya rumput laut di perairan Indonesia sangat besar, sehingga kebutuhan akan produk olahannya cukup tinggi, baik di dalam maupun di luar negeri. Sampai saat ini, hasil produksi rumput laut sebagian besar diekspor dalam bentuk kering dan hanya sebagian kecil saja yang diolah menjadi alginat, karagenan dan agar-agar. Selain diekspor dalam bentuk kering, karagenan, alginat dan agar-agar, rumput laut juga dapat diolah menjadi berbagai makanan siap saji seperti manisan, dodol, cendol, natade seaweed, selai, puding, permen jelly, dan lain-lain (Sudariastuty, 2011).
Agar-agar merupakan campuran polisakarida yang diekstraksi dari dinding sel ganggang merah (Rhodophyta), khususnya genus Gracilaria dan Gelidium. Agar-agar merupakan polisakarida kompleks yang terdiri dari agarosa dan agaropektin yang digunakan dalam penyusunan media pertumbuhan mikroba, permen dan agar jelly. Agarosa memiliki potensi pemanfaatan sebagai bahan pangan, farmasi dan industri kosmetik seperti penyedia biomassa potensial, sumber oligosakarida, antibakteri, antikanker dan antioksidan, serta dapat mempengaruhi sel-sel melanoma sehingga dapat melembabkan dan memutihkan kulit (Kobayashi, 1997).
Pengolahan rumput laut menjadi bahan baku sudah banyak dilakukan petani, akan tetapi hanya terbatas sampai rumput laut kering. Pengolahan agar-agar dari rumput laut merupakan alternatif untuk pengembangan usaha para petani. Agar-agar merupakan senyawa ester asam sulfat dari senyawa galaktan yang tidak larut dalam air dingin, tetapi larut dalam air panas dengan membentuk gel.
Perlakuan sebelum ekstraksi merupakan salah satu tahapan penting dalam pengolahan rumput laut menjadi agar-agar. Perlakuan sebelum ekstraksi yaitu proses perendaman rumput laut yang dilakukan sebelum ekstraksi untuk mempermudah proses ekstraksi, serta untuk meningkatkan mutu rendemen produk agar-agar yang dihasilkan. Perlakuan dapat dilakukan dengan menggunakan larutan alkali atau asam (Irawati, 1994). Proses perendaman dengan asam ini bertujuan untuk memecah dinding sel, sehingga agar-agar mudah diekstrak. Selain itu larutan asam tersebut diharapkan dapat menghancurkan dan melarutkan kotoran sehingga rumput laut lebih bersih. Larutan asam yang dapat digunakan adalah asam sulfat, asam asetat, asam sitrat, buah asam, dan daun asam (Winarno, 1990).
Berdasarkan penelitian yang telah dilakukan oleh Utomo & Satriyana (2006) dengan menggunakan asam asetat (CH3COOH) 3% pada ekstraksi agar-agar rumput
laut jenis Gracilaria chilensis sebagai perlakuan asam dengan jumlah air pengekstrak 20 kali berat rumput laut telah terbukti dapat menghasilkan rendemen hingga 20,21% dan kekuatan gel agar-agar yang dihasilkan sebesar 119,28 (g/cm2). Sementara berdasarkan penelitian Anjarsari, Arief & Wibowo (2005) yang menggunakan asam sulfat (H2SO4) dengan variasi pH menghasilkan rendemen agar-agar yang
berbeda-beda. Dimana dengan pH < 6,0 menghasilkan rendemen agar-agar sebesar 20,48%, pH 6,0-7,0 menghasilkan rendemen agar-agar sebesar 17,335% dan pada pH >7,0 menghasilkan rendemen agar-agar sebesar 15,567%. Hal ini menunjukkan bahwa semakin tinggi konsentrasi asam, maka semakin tinggi pula rendemen agar-agar yang dihasilkan.
Pengolahan agar-agar dari rumput laut Gracilaria sp. menggunakan asam sintetis sangat berbahaya, salah satu asam yang digunakan adalah asam sulfat. Hal ini berdasarkan Winarno (1996) yang menyatakan bahwa larutan H2SO4 sangat
berbahaya meskipun konsentrasinya 0,1% dan untuk menghilangkan larutan H2SO4
dalam proses pengolahan agar-agar dari rumput laut dilakukan perendaman dengan aquades untuk menetralkan rumput laut dengan pH 6-7. Untuk dapat mengurangi resiko akibat bahaya yang disebabkan oleh asam sintetis tersebut, perlu dilakukan
3 penelitian mengenai penggunaan asam dari bahan alam seperti asam jawa. Pengolahan agar-agar menggunakan asam jawa belum pernah dilakukan, sehingga perlu dilakukan penelitian mengenai penggunaan asam jawa dengan variasi konsentrasi terhadap pengolahan agar-agar dari rumput laut Gracilaria sp. Metode yang digunakan pada penelitian ini adalah metode ekstraksi secara maserasi. Pada proses ekstraksi, rumput laut Gracilaria sp. direndam dengan ekstrak asam jawa pada variasi konsentrasi yang ditentukan secara Rancangan Acak Lengkap (RAL), yaitu 5%, 10% dan 15% untuk melunakkan dinding sel rumput laut, kemudian dibersihkan dan dimasak dengan air pada suhu 90-100oC selama 90 menit. Analisis yang dilakukan terhadap agar-agar yang dihasilkan meliputi rendemen, kekuatan gel, kadar sulfat dan spektra FTIR.
1.2Rumusan Masalah
1. Apakah asam jawa dapat digunakan dalam proses ekstraksi agar-agar dari rumput laut Gracilaria sp.?
2. Bagaimana kualitas agar-agar hasil ekstraksi dari rumput laut Gracilaria sp. dengan menggunakan asam jawa?
1.3Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Mengetahui penggunaan asam jawa dalam proses ekstraksi agar-agar dari rumput laut Gracilaria sp.
2. Menentukan kualitas agar-agar hasil dari ekstraksi rumput laut Gracilaria sp. dengan menggunakan asam jawa.
1.4 Manfaat Penelitian
Manfaat dari penelitian ini adalah untuk memberikan informasi tentang ekstraksi agar-agar dari rumput laut Gracilaria sp. dengan menggunakan asam jawa. Penggunaan asam jawa, selain menghemat biaya, limbahnya juga tidak membahayakan lingkungan.
1.5Batasan Masalah
1. Rumput laut yang digunakan untuk penelitian ini adalah rumput laut Gracilaria sp.
2. Penelitian ini hanya membandingkan kualitas agar-agar dari rumput laut Gracilaria sp. yang menggunakan asam jawa dengan variasi konsentrasi pada proses maserasi.
3. Analisis yang dilakukan hanya melihat rendemen dari rumput laut, kadar sulfat dan kekuatan gel.
4. Identifikasi senyawa agar-agar hanya dari gugus yang muncul pada spektra yang dihasilkan dari analisis FTIR.
5 BAB II
TINJAUAN PUSTAKA
2.1Rumput Laut Gracilaria sp.
Rumput laut atau algae merupakan tumbuhan laut yang tidak dapat dibedakan antara akar, daun, dan batang, sehingga seluruh tubuhnya disebut thallus. Berdasarkan kandungan pigmen yang terdapat dalam thallus, rumput laut terdiri atas Chlorophyceae (alga hijau), Rhodophyceae (alga merah), dan Phaeophyceae (alga coklat) (Soenardjo, 2011).
Rumput laut memiliki kandungan karbohidrat, protein, sedikit lemak, dan abu yang sebagian besar merupakan senyawa garam natrium dan kalium. Selain itu, rumput laut juga mengandung vitamin-vitamin (A, B1, B2, B6, B12, dan C), betakaroten, serta mineral (kalium, kalium fosfor, natrium, zat besi, dan yodium). Beberapa jenis rumput laut mengandung lebih banyak vitamin dan mineral penting, seperti kalsium dan zat besi bila dibandingkan dengan sayuran dan buah-buahan. Beberapa jenis rumput laut juga mengandung protein yang cukup tinggi. Zat-zat tersebut sangat baik untuk dikonsumsi sehari-hari karena mempunyai fungsi dan peran penting untuk menjaga dan mengatur metabolisme tubuh manusia (Saputra, 2012).
Gracilaria merupakan salah satu marga rumput laut penghasil agar-agar atau disebut dengan agarophytes. Selain Gracilaria, rumput laut penghasil agar-agar lainnya adalah Gelidium, Pterocladia, dan Gelidiela. Pada tahun 2009 total produksi agarophytes di Indonesia mencapai 35.050 ton kering yang 81,60 % -nya (28.600 ton) diserap oleh industri nasional dan sisanya diserap industri luar negeri. Gracilaria dalam hal ini memberikan kontribusi paling besar (>90 %) untuk menyumbang bahan baku agar-agar dibandingkan dengan genus agarophytes yang lainnya. Hal ini dikarenakan Gracilaria banyak dibudidayakan di tambak-tambak, sedangkan agarophytes lainnya masih dipanen dari alam (Saputra, 2012).
Gracilaria sp. termasuk dalam kelas alga merah (Rhodophyta) dengan nama daerah yang bermacam-macam: sango-sango, rambu kasang, janggut dayung, dongidongi, bulung embulung, agar-agar karang, agar-agar jahe, blung sangu, dan lain-lain. Rumput laut marga ini memiliki banyak jenis dengan sifat-sifat morfologi dan anatomi berbeda-beda seperti: Gracilaria confervoides, Gracilaria gigas, Gracilaria lichenoides, Gracilaria crasa, Gracilaria blodgettii, Gracilaria arcuta,
Gracilaria taenioides, Gracilaria eucheumoides, dan banyak lagi. Beberapa ahli menduga bahwa rumput laut marga Gracilaria memiliki jenis yang paling banyak dibandingkan dengan rumput laut marga lainnya (Julianto & Badrudin, 2014).
Klasifikasi rumput laut marga Gracilaria sp. adalah sebagai berikut : Divisio : Rhodophyta
Kelas : Rhodophyceae Bangsa : Gigartinales Suku : Glacilariaeceae Marga : Glacilaria Jenis : Glacilaria gigas
Glacilaria verrucos
Glacilaria lichenoides. (Sudariastuty,2011).
Beberapa jenis rumput laut dari marga Gracilaria ditunjukkan pada Gambar 2.1 hingga Gambar 2.3.
7
Gambar 2.2 G. verrucosa (Sudariastuty,2011).
Gambar 2.3 G. lichenoides (Sudariastuty,2011).
Habitat rumput laut marga Gracilaria pada umumnya dapat hidup sampai 300-1000 m dari pantai, salinitas air berkisar 15-30 per mil dengan suhu air berkisar antara 20-28˚C, kedalaman air 0.5-1 meter dengan kondisi air jernih sehingga sinar matahari mampu menembus ke dalam air. Oleh karenanya jenis rumput laut Gracilaria sebaiknya dekat dengan muara sungai (Sudariastuty,2011). Kandungan agar-agar pada Gracilaria berbeda-beda menurut jenis dan lokasi pertumbuhannya, serta tergantung pada umur, bibit, lingkungan metode budidaya, panen, dan cara penanganan primer, sehingga mempunyai tingkat mutu dan harga yang berbeda beda pula. Umumnya kandungan agar-agar Gracilaria berkisar antara 16-45% (Kadi & Atmadja, 1988).
2.2Agar-agar
Agar-agar merupakan senyawa ester asam sulfat dari senyawa galaktan, tidak larut dalam air dingin, tetapi larut dalam air panas dengan membentuk gel. Agar-agar diekstraksi dari ganggang laut yang berasal dari kelompok Rhodophyceae, seperti Gracilaria dan Gelidium (Chapman & Chapman, 1980). Beberapa jenis Gracilaria yang bernilai ekonomi tinggi yang tumbuh di perairan Indonesia antara lain Gracilaria gigas, Gracilaria verrucosa, dan Gracilaria lichenoides. Fungsi utama agar-agar adalah sebagai bahan pemantap, penstabil, pengemulsi, pengisi, penjernih, pembuat gel, dan lain-lain. Beberapa industri yang memanfaatkan kemampuan membentuk gel dari agar-agar adalah industri makanan, farmasi, kosmetik, kulit, fotografi dan sebagai media penumbuh mikroba. Industri produksi agar-agar di Indonesia menggunakan metode yang melibatkan ekstraksi rumput laut dengan pelarut asam pada suhu tinggi (Anggadiredja, Zatnika, Purwoto & Istini, 2002).
Agar-agar merupakan polisakarida yang terakumulasi dalam dinding sel rumput laut penghasil agar-agar atau agarofit, oleh karenanya agar-agar yang terdapat dalam rumput laut dipengaruhi oleh musim. Semakin tua umur panen maka kandungan polisakarida yang dihasilkan semakin banyak sehingga agar-agarnya juga semakin tinggi (Syamsuar, 2006). Konsentrasi sulfat dalam agar-agar dapat dipengaruhi oleh perbedaan jenis dan asal rumput laut, metode ekstraksi, serta umur panen. Peningkatan umur panen dapat memberikan respon terhadap kandungan sulfat. Besarnya rendemen ini belum tentu sama untuk rumput laut yang sama apabila dipanen pada waktu yang berbeda (Suryaningrum, 1988).
Dinding sel perlu dipecah dengan ditambahkan asam untuk memudahkan ekstraksi. Bila tidak ada asam sulfat dapat digunakan asam asetat, asam sitrat, buah asam atau daun asam. Perendaman rumput laut dalam larutan asam dapat mempercepat waktu ekstraksi, meningkatkan rendemen agar-agar dan meningkatkan kekuatan gel agar-agar. Perendaman rumput laut dalam larutan asam bertujuan untuk mempersiapkan pemisahan agar-agar dari substansi nonagar (rumput laut). Efek musim dapat mempengaruhi rendemen dan sifat fisik dari agar (Permata, 2010).
Komponen utama agar-agar yaitu agarosa dan agaropektin. Agarosa adalah suatu polisakarida netral yang terdiri dari rangkaian D-galaktosa dengan ikatan β-1,3 dan L-galaktosa dengan ikatan α-1,4. Komponen ini tidak mengandung sulfat dan persentase agarosa dalam ekstrak agar berkisar antara 50% sampai 80%, sedangkan agaropektin adalah polimer sulfat dan bersifat lebih kompleks. Agaropektin
9 mengandung residu sulfat 3-10%, asam glukuronat dan asam piruvat. Agaropektin memiliki rantai yang hampir sama dengan rantai agarosa, tetapi beberapa residu 3,6-anhidro-L-galaktosa digantikan oleh L-galaktosa sulfat dan sebagian residu D-galaktosa digantikan oleh asetal asam piruvat (Glicksman, 1983).
Agar-agar adalah produk kering tak berbentuk (amorf) yang mempunyai sifat seperti gelatin. Molekul agar-agar terdiri dari rantai linier galaktan, yaitu polimer dari galaktosa dengan ikatan α-1,3 dan 3,6-anhidro-L-galaktosa dengan ikatan β-1,4. Dalam menyusun agar-agar, galaktan dapat berupa rantai linier yang netral, tersubstitusi dengan metal, piruvat, dan gugus sulfat. Rantai galaktan yang netral disebut agarosa, sedangkan yang tersubstitusi dengan gugus sulfat disebut agaropektin. Agarosa dan agaropektin dapat dipisahkan dengan cara pengendapan agaropektin menggunakan garam ammonium kwarterner atau propilen glikol (Glicksman, 1983).
Agar-agar bubuk merupakan komoditas yang diekspor dan beberapa pengusaha sudah mengusahakannya dalam skala industri. Di Indonesia agar-agar sudah mulai diproduksi pada tahun 1930 dan sekarang terdapat beberapa industri pengasil agar-agar. Untuk mengekspor bubuk agar-agar, mutu produk harus memenuhi persyaratan standar mutu agar-agar. Untuk sumber bubuk agar-agar di Indonesia umumnya digunakan jenis Gracilaria. Pada Tabel 2.1 dapat dilihat standar mutu agar-agar (Poncomulyo, Maryani & Kristiani, 2006).
Tabel 2.1 Standar Mutu Agar-agar
Komponen Spesifikasi
Ukuran partikel 80-100 mesh
Kadar air <18%
Kadar abu <6,99%
Logam berat <10 ppm
Arsenik <3 ppm
pH 6,8-7,0
Kelarutan Larut pada temperatur 100˚C (Poncomulyo, Maryani & Kristiani, 2006).
Agar-agar larut dalam air panas, etanolamida dan formida. Agar-agar pada suhu 32-39˚C berbentuk bekuan (solid) dan tidak mencair pada suhu di bawah 85˚C. Agar-agar merupakan agen pembentuk gel terefektif yang pernah diketahui. Gel
agar-agar dapat terbentuk dalam larutan yang sangat encer, yaitu fraksi agar-agar-agar-agar sebesar 1%. Gel agar-agar bersifat reversibel terhadap suhu, yaitu pada suhu di atas titik leleh maka fase gel akan berubah menjadi fase sol dan sebaliknya, tetapi fase transisi dari gel ke sol atau sebaliknya tidak berada pada suhu yang sama. Gel terbentuk karena pada saat dipanaskan di air, molekul agar-agar dan air bergerak bebas. Ketika didinginkan, molekul-molekul agar-agar mulai saling merapat, memadat dan membentuk kisi-kisi yang mengurung molekul-molekul air, sehingga terbentuk sistem koloid padat-cair (Rosulva, 2008).
Karakteristik gel agar-agar bersifat rigid, rapuh, mudah dibentuk dan memiliki titik cair tertentu. Keasaman (pH) sangat mempengaruhi kekuatan gel agar-agar. pH semakin menurun maka kekuatan gel agar-agar semakin lemah sampai dengan pH 2,5. Kandungan gula menghasilkan gel yang lebih keras tetapi menghasilkan tekstur yang kurang kohesif. Mekanisme pembentukan gel agar-agar adalah sebagai berikut: tiga buah atom hidrogen pada residu 3,6-anhidro-L-galaktosa memaksa molekul membentuk struktur heliks. Interaksi antar struktur heliks inilah yang menyebabkan pembentukan gel. Penggantian senyawa L-galaktosa sulfat oleh senyawa 3,6-anhidro-L-galaktosa mengakibatkan kekakuan pada struktur heliks, dari sinilah gel mulai terbentuk. Perlakuan alkali dapat mengkonversi gugus sulfat yang ada pada posisi C-6 menjadi 3,6-anhidro-L-galaktosa sehingga dapat memberikan kekuatan gel yang lebih tinggi ((Glicksman, 1983).
2.3Asam Jawa
Nama lain dari asam jawa adalah boh me (Aceh). Asam jawa sering digunakan sebagai bumbu dapur atau dibuat manisan. Tanaman asam jawa termasuk tanaman yang berbuah polong. Batang pohonnya cukup keras dan dapat tumbuh menjadi besar, serta berdaun rindang. Daun asam jawa bertangkai panjang sekitar 17 cm dan bersirip genap. Bunganya berwarna kuning kemerah-merahan. Buah polongnya berwarna coklat dengan rasa khas asam. Di dalam buah polong terdapat kulit yang membungkus daging buah dan terdapat biji yang berjumlah 2-5 yang berbentuk pipih dengan warna coklat agak kehitaman. Pada kulit bijinya mengandung phlobatanim dan bijinya mengandung albuminoid serta pati. Dalam daunnya terdapat kandungan kimia saponin, flavonoid dan tannin (Septiatin, 2008).
11 Kingdom : Plantae Divisi : Spermatophyta Kelas : Magnoliopsida Ordo : Fabales Famili : Fabaceae Genus : Tamarindus L.
Spesies : Tamarindus indica L. (Hidayah, 2016).
Tumbuhan asam jawa merupakan salah satu tumbuhan tropis. Asam jawa mengandung 15% asam sitrat. Asam organik yang dihasilkan dari buah asam jawa aman untuk digunakan pada bahan pangan. Selain mudah didapat, harga asam jawa yang terjangkau menyebabkan dapat digunakan sebagai sukuestran, meskipun daya reduksinya tidak secepat asam sitrat komersial (Edina, Sumarto & Edison, 2017). Dalam buah asam jawa terkandung beberapa kandungan kimia antara lain flavonoid, saponin, alkaloid, karbohidrat, steroid, antosian, tanin, asam askorbat, β-karoten, komponen volatil, asam tartrat, asam maleat, asam sitrat, asam suksinat, asam asetat, pektin dan gula invert (Imrawati, 2016).
Asam jawa banyak dimanfaatkan sebagai bahan pengobatan tradisional. Bagian tanaman asam jawa yang biasadigunakan untuk pengobatan antara lainadalah daun, kulit batang, daging buah dan biji (BPOM RI, 2013). Menurut identifikasi fitokimia, tanaman asam jawa mengandung flavonoid, tanin, glikosida dan saponin. Asam jawa juga mengandung protein dengan asam amino essensial, tinggi karbohidrat untuk persediaan energi, kaya akan mineral, kalium,kalsium, magnesium, dan sedikit mengandung zat besi dan vitamin A. Buah asam jawa dapat digunakan sebagai agen antiobesitas. Selain itu, buahnya dapat digunakan untuk pengobatan demam, diare, sakit perut, penyakit kuning, dan juga sebagai pembersih kulit. Kandungan flavonoid dan senyawa polifenol dalam ekstrak etanol daging buah asam jawa memiliki aktivitas sebagai antiobesitas dan antidiabetes. Flavonoid merangsang sekresi insulin dan meregenerasi kerusakan sel beta pankreas untuk antihiperglikemik. Kandungan ekstrak asam jawa, terutama daging buahnya menunjukkan aktivitas antioksidan yang paling tinggi. Antioksidan secara umum juga berpengaruh pada glukosa darah. Mekanisme antioksidan dalam antihiperglikemia yaitu mengurangi stres oksidatif pada terjadinya diabetes. Selain itu antioksidan bekerja dengan cara mengurangi glukosa dalam darah dan meningkatkan kadar insulin plasma (Hayu, Sutrisna & Devi, 2014).
2.4 Maserasi
Maserasi merupakan salah satu proses ekstraksi simplisia yang menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada suhu kamar. Metode maserasi digunakan untuk memperoleh komponen yang diinginkan dengan mengekstrak simplisia menggunakan pelarut tanpa suhu tinggi (Pratiwi, 2010). Proses maserasi sangat menguntungkan dalam isolasi senyawa bahan alam karena murah dan mudah dilakukan (Koirewoa, Fatimawali & Wiyono, 2008). Maserasi cocok untuk mengekstrak komponen-komponen yang tidak tahan akan suhu tinggi (Pratiwi, 2010). Pada perendaman sampel tumbuhan akan terjadi pemecahan dinding dan membran sel akibat perbedaan tekanan antara di dalam dan di luar sel, sehingga metabolit sekunder yang ada dalam sitoplasma akan terlarut dalam pelarut. Pelarut yang mengalir ke dalam sel dapat menyebabkan protoplasma membengkak dan bahan kandungan sel akan larut sesuai dengan kelarutannya. Lamanya waktu ekstraksi menyebabkan terjadinya kontak antara sampel dan pelarut secara lebih intensif sehingga hasilnya juga bertambah sampai titik jenuh larutan. Kontak antara sampel dan pelarut dapat ditingkatkan apabila didukung dengan adanya pengocokan agar kontak antara sampel dan pelarut semakin sering terjadi, sehingga proses ekstraksi lebih sempurna (Koirewoa, Fatimawali & Wiyono, 2008).
Sifat suatu senyawa ditentukan dari gugus fungsional yang ada. Gugus hidroksil dalam sebuah molekul menyebabkan terbentuknya ikatan hidrogen dan perubahan besar dalam sifat-sifat terutama dalam hal kelarutan. Salah satu ciri penting dari pelarut adalah tetapan dielektrik (D). Tetapan dielektrik pelarut adalah besarnya gaya yang bekerja antara muatan dalam pelarut. Tetapan ini menentukan sejauh mana tingkat kemampuan melarutkan dari pelarut. Pelarut-pelarut yang mempunyai tetapan dielektrik rendah merupakan pelarut yang baik untuk zat-zat yang non-polar dan pelarut-pelarut yang mempunyai tetapan dielektrik yang tinggi merupakan pelarut yang baik untuk zat-zat yang polar. Selain itu adanya perbedaan keelektronegatifan di dalam ikatan kovalen akan menimbulkan perbedaan muatan parsial atom-atom penyusun molekul. Perbedaan ini mengakibatkan senyawa mempunyai dipol-dipol dan senyawa bersifat polar. Senyawa yang bersifat polar akan mudah larut dalam pelarut polar sedangkan senyawa non polar akan mudah larut dalam pelarut non polar. Senyawa polar merupakan senyawa yang mempunyai momen dipol lebih besar dari pada nol. Hal ini karena molekul penyusunnya mempunyai atom tidak sejenis dan
13 bentuknya asimetris. Senyawa non-polar adalah senyawa yang mempunyai momen dipol sama dengan nol. Hal ini karena molekul penyusunnya mempunyai atom sejenis dan bentuk molekulnya simetris, sehingga titik berat muatan positif berimpit dengan muatan negatif (Effendy, 2006).
Remaserasi berarti dilakukan penambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya. Keuntungan cara penyarian dengan maserasi adalah cara pengerjaan dan peralatan yang digunakan sederhana yang mudah diusahakan (Alvicha, 2014). sedangkan kerugiannya yakni cara pengerjaannya lama, membutuhkan pelarut yang banyak dan penyarian kurang sempurna. Dalam maserasi (untuk ekstrak cairan), serbuk halus atau kasar dari tumbuhan obat yang kontak dengan pelarut disimpan dalam wadah tertutup untuk periode tertentu dengan pengadukan yang sering, sampai zat tertentu dapat terlarut. Metode ini cocok digunakan untuk senyawa yang termolabil (Rahmadani, 2015).
2.5 Fourier Transform Infrared (FTIR)
Spektroskopi inframerah merupakan teknik spektroskopi yang berguna untuk mengidentifikasi gugus fungsi. Spektrum inframerah meliputi panjang gelombang antara 2,5-1,6 µm atau setara dengan bilangan gelombang 4000-650 cm-1. Spektrum inframerah suatu senyawa dapat dengan mudah diperoleh dalam beberapa menit. Sedikit sampel senyawa diletakkan dalam instrumen dengan sumber radiasi inframerah. Spektrometer secara otomatis membaca sejumlah radiasi yang menembus sampel dengan kisaran frekuensi tertentu dan merekam pada kertas persentase radiasi yang ditransmisikan. Radiasi yang diserap oleh molekul muncul sebagai pita pada spektrum (Fauziah, 2009).
Puncak penyerapan karakteristik agarosa adalah pada bilangan gelombang 3481 cm-1 (-OH peregangan kelompok hidroksil), 1078 cm-1 (ikatan glikosidik) dan 930 cm-1 (getaran jembatan C-O-C 3,6-anhidro-L-galaktopiranosa). Karakteristik puncak penyerapan agar-agar terdapat pada 3497 cm-1 (-OH peregangan dari kelompok hidroksil). 1072 cm-1 (ikatan glikosidik), 932 cm-1 (ikatan C-O-C 3,6-anhidro-L-galaktoptranosa), 1250 cm-1 (S = O dari ester sulfat) dan 864 cm-1 ( ikatan L-galaktopirosa-6-sulfat) (Samiey & Ashoori, 2012).
Ekstrak agar-agar umumnya mempunyai gugus fungsi CH2 yang memberikan serapan pada bilangan gelombang 2960 cm-1, serapan gugus 3,6 anhidrogalaktosa pada bilangan gelombang 1070 cm-1, gugus 1,3 β-D galaktosa piranosil memberikan
serapan pada 897 cm-1, dan gugus ester sulfat menghasilkan serapan pada bilangan gelombang 1180 cm-1; 1250 cm-1; 1370 cm-1 (Sur & Guven, 2002). Fraksi agarosa umumnya mempunyai serapan pada 897 cm-1 (gugus 1,3 β-D galaktosa piranosil), serta adanya serapan 930 cm-1 dan 1070 cm-1 yang menunjukkan gugus 3,6 anhidrogalaktosa. Jumlah ikatan 3,6 anhidrogalaktosa pada agarosa lebih tinggi dibandingkan fraksi agaropektin. Fraksi agaropektin mempunyai gugus 3,6 anhidrogalaktosa yang menghasilkan serapan pada 1070 cm-1, serta serapan pada 1250 cm-1 dan 850 cm-1 yang menunjukan adanya kelompok sulfat (Balkan, Coban & Guven, 2005).
Absorban pada bilangan gelombang 2920 cmˉ¹ terkait dengan C-H yang digunakan sebagai indeks total kandungan gula karena gugus C-H tetap konstan terlepas dari perubahan rasio galaktosa terhadap 3,6-anhidrogalaktosa dan kandungan sulfat dari galaktan. Absorban pada bilangan gelombang 845 cmˉ¹ terkait dengan 3,6-anhidrogalaktosa yang juga terkait dengan kandungan galaktosa-4-sulfat pada agar-agar. Serapan pada bilangan gelombang 1250 cmˉ¹ adalah sulfat, sehingga dapat digunakan dalam perbandingan dengan absorbansi C-H pada 2920 cmˉ¹ sebagai indeks terkait sulfat total terhadap kandungan gula. Serapan 3,6 anhidrogalaktosa-2-sulfat diperoleh pada bilangan gelombang 805 cmˉ¹ (Rochas, Lahaye & Yaphe, 1986).
16 BAB III
METODOLOGI PENELITIAN
3.1Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada bulan Agustus-September 2018 bertempat di Laboratorium Kimia Fakultas Sains dan Teknologi Universitas Islam Negeri Ar-Raniry Banda Aceh dan Laboratorium Kimia Fakultas Keguruan Ilmu Pengetahuan Universitas Syiah Kuala.
3.2Alat dan Bahan
Sampel yang digunakan adalah rumput laut Gracilaria sp. yang diperoleh dari tambak didesa Neuhen, Kecamatan Mesjid Raya, Kabupaten Aceh Besar, dan asam jawa yang diperoleh dari Gampong Lamtrieng, Kecamatan Kuta Baro, Kabupaten Aceh Besar, Provinsi Aceh. Konsentrasi asam jawa ditentukan berdasarkan rancangan acak lengkap (RAL) yaitu 5%, 10% dan 15%. Bahan kimia yang digunakan untuk pembuatan agar-agar antara lain akuades (H2O), kalsium oksida (CaO) 1%, kertas
saring dan natrium hidroksida (NaOH), asam asetat (CH3COOH). Sedangkan untuk
analisis agar-agar digunakan barium klorida (BaCl2) 10 %, asam klorida (HCl) 0,2 N
dan hidrogen peroksida (H2O2) 10 %.
Alat-alat yang digunakan untuk ekstraksi agar-agar adalah gelas beaker, hotplate, magnetik stirrer, pipet tetes, gelas ukur, gelas kimia, kain saring, timbangan analitik, pH meter, spatula dan blender. Sedangkan peralatan yang digunakan untuk analisis adalah oven merek memmert, beaker glass, pipet tetes, Cary 630 FTIR Spectrometer, tanur merek Vulcan Muffle Furnace Digital D550, batang stainless steel dan rangkaian alat refluks.
3.3 Prosedur Kerja
3.3.1 Pembuatan agar-agar
Langkah-langkah pembuatan agar-agar berdasarkan Ghufran (2011) yang telah dimodifikasi adalah sebagai berikut:
1. Rumput laut dicuci dengan air sampai bersih. Kotoran yang menempel seperti lumpur, pasir, kulit kerang dan karang dihilangkan.
2. Rumput laut kemudian direndam dalam air sebanyak 20 kali berat rumput laut selama 3 hari.
3. Selanjutnya dilakukan pemucatan dengan merendam rumput laut di dalam larutan kapur tohor (CaO) 1% sambil diaduk. Setelah 1 jam, rumput laut direndam kembali selama 3 jam untuk menghilangkan kapur tohor. Rumput laut yang telah bersih dan pucat dikeringkan selama 2 hari.
4. Langkah berikutnya adalah pelembutan. Untuk lebih memudahkan ekstraksi, dinding sel dipecah dengan ditambahkan asam jawa. Rumput laut direndam dalam asam jawa dengan variasi konsentrasi 5%, 10% dan 15% selama 15 menit.. kemudian dicuci dengan merendamnya dalam air bersih selama 15
menit, kemudian ditiriskan.
5. Langkah selanjutnya adalah pemasakan. Rumput laut yang telah direndam tersebut dimasak dalam air sebanyak 40 kali berat rumput laut. Setelah mendidih (90-100˚C) ditambahkan asam asetat untuk memperoleh pH 7. Bila pH >7 maka pHnya diturunkan dengan penambahan asam asetat, dan bila pHnya <6 maka ditambahkan NaOH. Pemeriksaan pH dilakukan menggunakan pH meter. Pemasakan dilakukan selama 90 menit, dengan terus dilakukan pengadukan.
6. Untuk memperoleh agar-agar tepung, agar-agar yang telah dimasak, disaring menggunakan saringan. Cairan yang keluar ditampung dan didinginkan selama semalam pada suhu ruang. Agar-agar beku dihancurkan. Kemudian dimasukkan ke dalam alat penggiling. Hasil penggilingan adalah agar-agar tepung.
18 3.3.2 Rendemen agar-agar (AOAC, 1995)
Rendemen merupakan perbandingan antara berat agar kering dengan berat rumput laut kering. Rendeman agar dihitung dengan menggunakan rumus :
𝑅𝑒𝑛𝑑𝑒𝑚𝑒𝑛 (%) = 𝑊𝑎
𝑊𝑟 × 100%
Keterangan: Wa = berat agar kering
Wr = berat rumput laut kering. 3.3.3 Pengukuran kadar sulfat (Rahmasari, 2008)
Satu gram tepung agar-agar dimasukkan ke dalam erlenmeyer, kemudian ditambahkan 50 ml HCl 0,2 N. Erlenmeyer tersebut dipasang pada penangas tegak dan dipanaskan sampai mendidih, kemudian direfluks selama satu jam. Setelah itu, larutan ditambahkan dengan 20 ml larutan H2O2 10 % dan refluks dilanjutkan selama
2 jam sampai larutan benar-benar jernih. Larutan kemudian dipindahkan ke dalam gelas piala 600 ml, dipanaskan sampai mendidih sambil terus diaduk. 10 ml BaCl2 10
% ditambahkan ke dalam larutan kemudian endapan yang terbentuk, disaring dengan menggunakan kertas Whatman 41, lalu dicuci dengan aquades mendidih. Kertas saring dikeringkan dalam oven, kemudian diabukan pada suhu 600°C selama 6 jam dalam tanur. Abu yang diperoleh didinginkan dalam desikator dan ditimbang.
Prinsip dari pengukuran kadar sulfat adalah ion sulfat yang bereaksi dengan barium klorida dalam suasana asam akan membentuk suspensi barium sulfat, dengan reaksi
SO42- + BaCl2 → BaSO4 + 2Cl-.
Berat BaSO4 yang diperoleh ekivalen dengan kadar SO4 dalam contoh (Rosulva,
2008).
Kadar sulfat (%) = berat endapan BaSO 4 g × berat kertas saringberat sampel (g) × 100%
3.3.4 Pengukuran kekuatan gel (Distantina, 2008)
Pengukuran kekuatan gel ditentukan dengan membuat larutan agar-agar 1 gram dalam 100 mL akuades, kemudian dipanaskan sampai larut. Larutan ini dibiarkan membeku (membentuk gel) semalam pada suhu kamar dalam gelas beaker. Kemudian gelas beaker diletakkan di atas timbangan. Batang stainless steel (luas penampang = 0,05 cm) ditekan dengan tangan di atas permukaan gel sampai pecah,
dan berat maksimum dicatat. Selisih berat awal dan berat maksimum merupakan kekuatan gel untuk pecah.
3.3.5 Identifikasi agar-agar (Fauziah,2009)
Tepung agar-agar diidentifikasi dengan instrumentasi FTIR. Sedikit sampel diletakkan dalam instrument dengan sumber radiasi inframerah. Spektrometer secara otomatis membaca sejumlah radiasi yang menembus sampel dengan kisaran frekuensi tertentu dan merekam pada kertas persentase radiasi yang ditransmisikan. Radiasi yang diserap oleh molekul muncul sebagai pita pada spektrum.
20 3.4Bagan Alir
20 gram Gracilaria sp.
Perendaman menggunakan air sebanyak 400 mL selama 3 hari
Pemucatan 1 jam dengan merendam didalam larutan kapur tohor (CaO) 1 % dan kemudian direndam kembali selama 3 jam
Pengeringan dilakukan selama 2 hari
Pelembutan dengan menambahkan asam jawa 5%, 10% dan 15% selama 15 menit, kemudian direndam dalam air selama 15 menit.
Pemasakan dengan menambahkan air sebanyak 800 mL pada suhu 90-100˚C dengan pH 7 selama 90 menit dan terus diaduk.
Penyaringan dilakukan menggunakan saringan kemudian filtrat yang diperoleh didinginkan sampai membeku selama semalam pada suhu ruang.
Penepungan dilakukan dengan menggiling filtrat yang dibekukan.
21 BAB IV
DATA HASIL PENGAMATAN DAN PEMBAHASAN
4.1Data Hasil Pengamatan
Data hasil pengamatan ekstrasi agar-agar perlakuan asam jawa ditunjukkan pada Table 4.1.
Tabel 4.1 Data Hasil Pengamatan Ekstraksi Agar-Agar Perlakuan Asam Jawa Parameter Variasi Konsentrasi Asam Jawa
5% 10% 15% Rendemen (%) 28,8 % 35,35% 40,5% Kekuatan Gel (g/cm2) 168,28 178,85 193,24 Kadar Sulfat (%) 3% 2% 1,5% 4.2Pembahasan
Agar-agar adalah senyawa ester asam sulfat dari senyawa galaktan, tidak larut dalam air dingin, tetapi larut dalam air panas dengan membentuk gel. Agar-agar merupakan produk hasil dari ekstraksi dari ganggang laut yang berasal dari kelompok Rhodophyceae, seperti Gracilaria (Chapman & Chapman, 1980). Agar-agar berfungsi sebagai bahan pemantap, penstabil, pengemulsi, pengisi, penjernih, pembuat gel, dan lain-lain. Beberapa industri yang memanfaatkan sifat kemampuan membentuk gel dari agar-agar adalah industri makanan, farmasi, kosmetik, kulit, fotografi, dan sebagai media penumbuh mikroba (Distantina, 2008).
Industri produksi agar-agar di Indonesia menggunakan metode yang melibatkan ekstraksi dari rumput laut dengan pelarut asam pada suhu tinggi. Ada kecenderungan yang sering muncul pada proses ekstraksi yaitu sifat gel agar-agar menurun dengan meningkatnya rendemen agar-agar. Untuk menghindari hal itu, dikembangkan metode yaitu merendam rumput laut dengan asam dan setelah dinetralkan, rumput laut diekstraksi pada kondisi netral dengan pH 7.
Penelitian ini menggunakan asam jawa sebagai bahan alami untuk lebih memudahkan ekstraksi agar-agar dari rumput laut Gracilaria sp. Proses pembuatan agar-agar secara umum terdiri dari beberapa tahapan, yaitu pembersihan dan pencucian, perendaman dan pemucatan, pemasakan (ekstraksi), penyaringan, pendinginan dan pengeringan. Setiap tahapan dari proses pembuatan agar-agar
22 memiliki tujuan tersendiri yang dapat mempengaruhi kualitas agar-agar tersebut. Pada tahapan pembersihan dan pencucian, rumput laut dibersihkan dari kotoran-kotoran yang menempel. Selanjutnya dilakukan perendaman yang bertujuan agar rumput laut menjadi lunak sehingga proses ekstraksi dapat berjalan dengan baik.
Rumput laut direndam dalam air sebanyak 20 kali berat rumput laut selama 3 hari. Perendaman juga dilakukan untuk melanjutkan pembersihan rumput laut dari kotoran-kotoran yang mungkin masih melekat. Pemucatan dilakukan untuk memperoleh rumput laut yang berwarna putih dan bersih, serta untuk meningkatkan mutu organoleptik produk agar-agar terutama pada faktor warna. Larutan yang digunakan sebagai pemucat adalah kapur tohor (CaO) 1 % dengan lama perendaman selama 5 menit.
Penggunaan kapur tohor memiliki beberapa keuntungan yaitu harga yang murah, bau yang tidak terlalu menyengat dan waktu yang dibutuhkan untuk pemucatan singkat. Setelah proses perendaman dan pemucatan selesai, rumput laut dicuci untuk menghilangkan bahan pemucat yang selama 3 jam dan dikeringkan selama 2 hari. Rumput laut yang telah kering kemudian dilakukan perendaman kembali menggunakan asam jawa dengan variasi 5%, 10% dan 15%. Perendaman menggunakan asam jawa ini bertujuan untuk memecah dinding sel rumput laut sehingga memudahkan proses ekstraksi agar-agar dari rumput laut.
Perendaman menggunakan asam jawa membuat rumput laut semakin melunak dengan semakin tingginya konsentrasi dari asam jawa. Hal ini menunjukkan bahwa fungsi asam jawa pada perendaman adalah melunakkan dinding sel rumput laut dan menarik agar-agar keluar dari dinding sel. Dengan demikian, komponen agar-agar dalam rumput laut lebih banyak yang terekstrak pada konsentrasi asam jawa yang lebih tinggi. Hal ini sejalan dengan penelitian sebelumnya yang menunjukkan bahwa rumput laut semakin lunak dengan semakin tingginya konsentrasi asam asetat. Fungsi asam asetat pada perendaman adalah melunakkan dinding sel rumput laut sehingga komponen agar-agar dalam rumput laut lebih banyak yang terekstrak pada konsentrasi asam asetat yang lebih tinggi (Distantina, 2008).
Asam jawa sering digunakan sebagai bumbu dapur atau dibuat manisan. Asam jawa mengandung beberapa jenis asam yang bisa digunakan untuk memecahkan dinding sel rumput laut. Proses ekstraksi dengan praperlakuan asam bertujuan untuk meningkatkan rendemen agar-agar yang dihasilkan dan untuk memperpendek waktu ekstraksi (Utomo & Satriyana, 2006). Sifat asam yang dimiliki asam jawa dapat
meningkatkan kelarutan agar-agar yang tersusun dari senyawa polisakarida. Polisakarida sangat mudah terhidrolisis menjadi monosakarida (glukosa) dalam suasana asam, karena larutan asam bersifat sebagai katalis (Distantina, 2006). Dalam buah asam jawa terkandung beberapa jenis asam diantaranya asam tartrat, asam maleat, asam sitrat, asam suksinat, asam asetat. Dengan demikian, asam jawa dapat digunakan dalam proses pembuatan agar-agar dari rumput laut. Selain asam jawa mudah didapatkan, limbahnya juga tidak merusak lingkungan dan dapat meminimalisir harga produksi menjadi lebih murah.
Ekstraksi agar-agar dilakukan dengan proses perebusan menggunakan air sebanyak 40 kali dari berat rumput laut. Hal ini dikarenakan untuk memecah dinding sel rumput laut dibutuhkan luas permukaan kontak antar dinding sel dengan air pengekstrak yang besar. Ekstraksi dilakukan pada suhu 90 – 100°C selama 90 menit. Metode ekstraksi agar-agar yang bervariasi mempengaruhi rendemen dan kekuatan gel yang dihasilkan. Metode ekstraksi sangat penting untuk diperhatikan karena setiap langkah dalam proses ekstraksi mungkin akan menurunkan kualitas agar. Setelah proses ekstraksi selesai, larutan agar-agar langsung disaring dalam keadaan panas. Penyaringan bertujuan untuk menjernihkan cairan dengan cara membuang sejumlah partikel padat atau untuk memisahkan cairan dari bagian padat rumput laut dengan menggunakan saringan sehingga diperoleh filtrat agar-agar yang bersih. Kemudian filtrat yang diperoleh didinginkan pada suhu kamar selama semalaman.
Agar-agar yang telah mengeras dipotong-potong sehingga proses pengeringan berjalan efisien. Pengeringan menghasilkan agar-agar dalam bentuk lembaran. Agar-agar tersebut kemudian dihancurkan menggunakan alat pengiling. Hasil dari penggilingan berupa agar-agar dalam bentuk tepung kemudian digunakan untuk analisis. Analisis yang dilakukan terhadap tepung agar-agar yang dihasilkan meliputi rendemen, kekuatan gel, kadar sulfat dan FTIR (Spektra Fourier Transform Infrared). Pengujian dilakukan untuk mengetahui perbedaan mutu dari agar-agar yang dihasilkan.
4.2.1 Rendemen agar-agar
Rendemen merupakan salah satu parameter yang penting dalam menilai efektif atau tidaknya suatu proses produksi. Rendemen suatu bahan pangan berhubungan dengan nilai ekonomis bahan tersebut. Semakin tinggi rendemen suatu produk, maka nilai ekonomisnya juga semakin tinggi. Nilai rendemen tepung agar-agar dihitung
24 berdasarkan perbandingan berat tepung agar-agar yang dihasilkan terhadap berat rumput laut. Nilai rendemen yang dihasilkan berkisar antara 28,8-40,5%. Berdasarkan penelitian sebelumnya yang menggunakan asam sulfat pada pengolahan agar-agar menunjukkan bahwa rendemen agar-agar yang dihasilkan berkisar antara 20% sampai 25% (Anjarsari, Arief & Wibowo, 2005). Hal ini menunjukkan bahwa penggunaan asam jawa dapat meningkatkan rendemen agar-agar lebih banyak dari pada penggunaan asam sulfat. Hubungan antara konsentrasi asam jawa dan % rendemen dapat dilihat pada Gambar 4.1.
Gambar 4.1 Grafik hubungan konsentrasi asam jawa dengan % rendemen
Hasil analisis menunjukkan bahwa perlakuan asam jawa berpengaruh terhadap besarnya rendemen yang dihasilkan. Hal ini dikarenakan sifat asam dari asam jawa dapat menghidrolisis dinding sel rumput laut sehingga komponen agar-agar yang terekstrak lebih banyak dan dapat meningkatkan rendemen agar-agar.
Dinding sel rumput laut tersusun oleh polisakarida yang juga merupakan penyusun agaropektin. Polisakarida pada umumnya bersifat tidak larut dalam air, tidak berasa, dan memiliki bobot molekul yang tinggi. Salah satu polisakarida penyusun utama dinding sel rumput laut adalah selulosa (Anggraeni, Tjiptasurasa & Hartanti, 2010). Sifat asam dari asam jawa akan menghidrolisis dinding sel rumput laut yang tersusun oleh selulosa. Semakin tinggi kadar asam yang digunakan maka semakin banyak dinding sel rumput laut yang terhidrolisis sehingga menghasilkan
28,8 35,35 40,5 R² = 0,995 0 5 10 15 20 25 30 35 40 45 0% 5% 10% 15% 20% Re n d em en ( % )
rendemen agar-agar yang lebih banyak (dapat dilihat dari perlakuan rumput laut menggunakan asam jawa). Semakin banyak asam jawa yang ditambahkan pada perlakuan asam jawa maka semakin banyak rendemen agar-agar yang dihasilkan.
Permukaan dinding sel yang besar akibat hidrolisis dengan asam (asam jawa) dapat dengan mudah dilewati oleh cairan penyari (air) pada proses ekstraksi. Hal ini menyebabkan komponen agar-agar yang terdapat di dalam rumput laut lebih mudah terekstrak, sehingga dapat meningkatkan rendemen agar-agar. Rendemen dipengaruhi oleh lama dan waktu ekstraksi. Hal tersebut disebabkan semakin lama rumput laut kontak dengan panas maupun larutan pengekstrak, maka semakin banyak agar-agar yang terkumpul dan menyebabkan tingginya rendemen tepung agar-agar.
Rendemen agar-agar selain dipengaruhi cara ekstraksi, dipengaruhi pula oleh spesies, iklim, waktu pemanenan dan lokasi budidaya (Chapman & Chapman, 1980). Oleh karena itu besarnya rendemen ini belum tentu sama untuk rumput laut yang sama apabila dipanen pada waktu yang berbeda maupun ditanam pada lokasi yang berbeda. Agar-agar merupakan polisakarida yang terakumulasi dalam dinding sel rumput laut penghasil agar-agar atau agarofit, oleh karenanya kandungan agar-agar yang terdapat dalam rumput laut dipengaruhi oleh musim. Pada ekstraksi agar-agar dari rumput laut menggunakan kalsium oksida yang bertujuan untuk mengkatalisis/mempercepat laju reaksi kimia pelepasan gugus 6-sulfat dari unit galaktopiranosa yang berikatan 1,4 dengan membentuk residu 3,6-anhidrogalaktosa yang dapat mempercepat proses pembentukan struktur heliks dan dapat memberikan kekuatan gel yang lebih tinggi. Oleh karena itu, jumlah rendemennya lebih tinggi (Firdaus, Prihanto & Nurdiani, 2015).
4.2.2 Kekuatan gel agar-agar
Kekuatan gel merupakan sifat fisik agar-agar yang utama, karena kekuatan gel menunjukkan kemampuan agar-agar dalam pembentukan gel. Kekuatan gel pada penelitian ini berkisar antara 168,40-193,24 g/cm2. Berdasarkan penelitian sebelumnya kekuatan gel agar-agar hasil penelitian ini jauh lebih tinggi dari kekuatan gel agar-agar dari rumput laut Gracilaria sp. tambak sebesar 34.67 sampai 97.33 g/cm2 (Suryaningrum, Murtini, Wibowo & Suherman, 1994). Namun kekuatan gel agar-agar penelitian menggunakan asam jawa ini jauh lebih rendah dibandingkan kekuatan gel agar-agar Gracilaria verrucossa tambak yang diekstrak dengan perlakuan alkali yang menghasilkan kekuatan gel 355 g/cm2 (Utomo, 1996). Kekuatan
26 gel dari agar-agar juga tergantung pada perbandingan kadar agarosa terhadap agaropektin yang terdapat dalam molekul agar-agar. Semakin sedikit kandungan agarosa dan semakin tinggi kandungan agaropektin yang mengandung gugus sulfat maka ada kecenderungan kekuatan gelnya semakin rendah (Glicksman, 1983).
Berdasarkan standar mutu agar-agar ekspor Jepang, kekuatan gel agar-agar mutu superior sebesar > 600 g/cm2, mutu 1 sebesar > 350 g/cm2, mutu 2 sebesar >250 g/cm2 dan mutu 3 sebesar > 150 g/cm2 (Kusuma, Santosa & Pramesti, 2013). Nilai kekuatan gel yang dihasilkan pada penelitian ini sebagian besar masuk pada mutu ke 3 dengan nilai kekuatan gel >150 g/cm2.
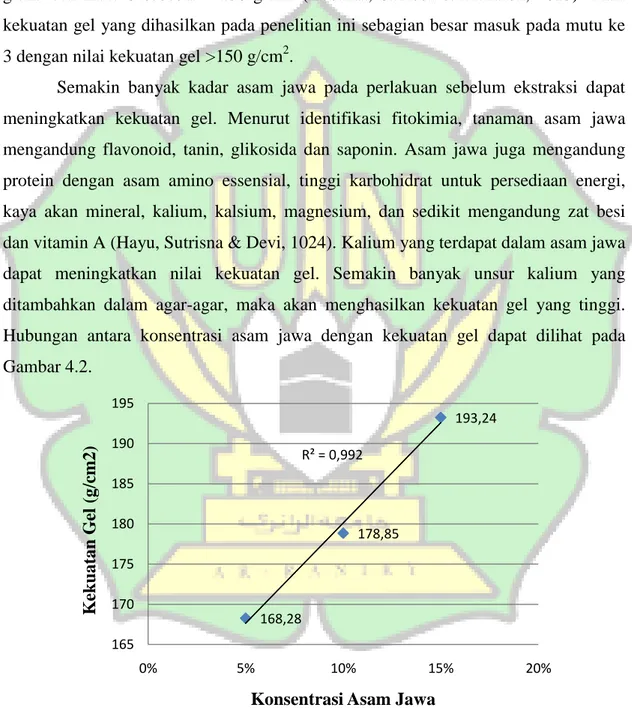
Semakin banyak kadar asam jawa pada perlakuan sebelum ekstraksi dapat meningkatkan kekuatan gel. Menurut identifikasi fitokimia, tanaman asam jawa mengandung flavonoid, tanin, glikosida dan saponin. Asam jawa juga mengandung protein dengan asam amino essensial, tinggi karbohidrat untuk persediaan energi, kaya akan mineral, kalium, kalsium, magnesium, dan sedikit mengandung zat besi dan vitamin A (Hayu, Sutrisna & Devi, 1024). Kalium yang terdapat dalam asam jawa dapat meningkatkan nilai kekuatan gel. Semakin banyak unsur kalium yang ditambahkan dalam agar-agar, maka akan menghasilkan kekuatan gel yang tinggi. Hubungan antara konsentrasi asam jawa dengan kekuatan gel dapat dilihat pada Gambar 4.2.
Gambar 4.2 Grafik hubungan konsentrasi asam jawa dengan kekuatan gel Nilai kekuatan gel agar-agar menurut SNI yaitu 150 g/cm2 (Rahmasari, 2008). Nilai kekuatan gel yang dihasilkan pada penelitian ini lebih besar nilainya dari SNI.
168,28 178,85 193,24 R² = 0,992 165 170 175 180 185 190 195 0% 5% 10% 15% 20% K ek u at an G el (g/c m 2)
Semakin tinggi konsentrasi asam jawa maka kekuatan gelnya semakin tinggi. Pada konsentrasi asam jawa 5% menghasilkan kekuatan gel sebesar 168,28 g/cm2, konsentrasi asam jawa 10% nilai kekuatan gelnya sebesar 178,85 g/cm2 dan pada konsentrasi asam jawa 15% menghasilkan kekuatan gel sebesar 193,24 g/cm2 dan telah memenuhi standar kekuatan gel SNI yaitu 150 g/cm2.
Kandungan sulfat berpengaruh terhadap kekuatan gel dari agar-agar. Semakin tinggi kandungan ester sulfat dalam agar-agar, maka kekuatan gel yang terbentuk akan semakin rendah (Chapman & Chapman,1980). Sulfat merupakan penghambat agar-agar untuk menyatu menjadi satu kesatuan ikatan sehingga apabila sulfatnya banyak maka kekuatan gelnya akan semakin rendah, begitu juga sebaliknya. Hal ini karena ester sulfat pada atom karbon keenam dari L-galaktosa (C6) menyebabkan rantai polimer membentuk suatu tekukan yang dapat menghambat proses pembentukan gel (Glicksman, 1983). Karakteristik pembentukan gel agar-agar disebabkan oleh tiga buah atom H pada residu 3,6 anhidro-L-galaktosa yang memaksa molekul-molekul untuk membentuk struktur heliks. Interaksi antar struktur heliks menyebabkan terbentuknya gel. Pergantian senyawa 3,6 anhidro-L-galaktosa oleh senyawa L-galaktosa sulfat menyebabkan kekacauan dalam struktur heliks dan dalam keadaan seperti ini kekuatan gel menjadi menurun. Adanya 3,6 anhidrogalaktosa akan menyebabkan sifat anhidrofilik dan meningkatkan pembentukan heliks rangkap sehingga terbentuk gel yang kuat (Stanley, 1987).
Semakin tua umur panen, kekuatan gel yang dihasilkan cenderung meningkat dan akan menurun setelah mencapai puncak pertumbuhan. Peningkatan kekuatan gel berbanding lurus dengan kandungan 3,6-anhidrogalaktosa. Dari hasil penelitian ini diperoleh bahwa kadar sulfat berbanding terbalik dengan kekuatan gel yang dihasilkan. Kondisi produksi mempengaruhi kekuatan gel yang dihasilkan dan kondisi produksi meliputi lokasi rumput laut tersebut dibudidayakan, akan berbeda apabila dibudidayakan di tambak dan di laut. Hal tersebut terjadi karena kualitas dari rumput laut berhubungan juga dengan kondisi lingkungan di sekitar lokasi budidaya.
Pembentukan gel merupakan fenomena penggabungan atau pengikatan silang rantai-rantai polimer sehingga membentuk suatu jala tiga dimensi bersambungan. Jala ini, dapat menangkap atau memobilisasikan air di dalamnya dan membentuk struktur yang kuat dan kaku (Fardiaz, 1986).
28 4.2.3 Kadar sulfat agar-agar
Kadar sulfat di dalam agar-agar sangat mempengaruhi kekuatan gel, karena sifat sulfat sangat hidrofilik sehingga dengan banyaknya kadar sulfat dalam agar-agar akan menurunkan kekuatan gel agar-agar (Distantina, Anggraeni & Fitri, 2008). Pada penelitian ini kadar sulfat diperoleh dengan perlakuan asam jawa berkisar antara 1,5-3%. Semakin rendah kadar sulfat yang diperoleh maka semakin baik kualitas agar-agar yang dihasilkan. Kadar sulfat agar-agar-agar-agar dalam penelitian ini relatif masih lebih rendah dibandingkan dengan penelitian sebelumnya untuk agar-agar dari rumput laut Gracilaria sp. tambak yang mengandung kadar sulfat sebesar 3.25 – 4.79% (Suryaningrum, Murtini, Wibowo & Suherman, 1994). Hubungan antara konsentrasi asam jawa dengan kadar sulfat dapat dilihat pada Gambar 4.3.
Gambar 4.3 Grafik hubungan konsentrasi asam jawa dengan kadar sulfat Nilai kadar sulfat berbanding terbalik dengan nilai kekuatan gel, dimana semakin rendah kadar sulfat maka nilai kekuatan gel akan semakin tinggi. Demikian juga sebaliknya, semakin tinggi kadar sulfat maka nilai kekuatan semakin rendah. Pada saat ekstraksi, komponen agar-agar yang berisi sulfat dikeluarkan dari sel rumput laut penghasil agar-agar. Metode ekstraksi juga berpengaruh terhadap kandungan sulfat. Proses ekstraksi dengan melakukan perlakuan basa menghasilkan kandungan sulfat yang lebih rendah dibandingkan perlakuan asam. Perlakuan basa dapat mengkatalisis gugus 6-sulfat dari unit galaktopiranosa sehingga kandungan sulfat dari agar-agar menjadi lebih rendah (Angka & Suhartono, 2000). Perlakuan asam tidak dapat mengkatalisis gugus sulfat sehingga tidak dapat menghilangkan ester
3 2 1,5 R² = 0,964 0 0,5 1 1,5 2 2,5 3 3,5 0% 5% 10% 15% 20% K ad ar S u lf at (% )
sulfat pada C6 rantai galaktosa karena asam tidak bereaksi dengan ester sulfat dan tidak membentuk garam sulfat.
Kandungan sulfat dalam rumput laut dipengaruhi oleh habitat, metode ekstraksi dan umur panen. Proses ekstraksi mempengaruhi kadar sulfat dari rumput laut (Angka & Suhartono, 2000). Sulfat pada alga penghasil agar-agar terakumulasi pada dinding sel dari alga. Sulfat terikat bersama dengan agar-agar (agarosa dan agaropektin) dan gugus sulfat disekresikan oleh badan golgi dari sel alga penghasil agar-agar (Armisen & Galatas, 2000). Pengaruh perbedaan asal dan jenis rumput laut terhadap kandungan sulfat agar-agar diduga disebabkan oleh perbedaan perbandingan jumlah agarosa dan agaropektin yang terdapat dalam molekul agar-agar. Kandungan agarosa dan agaropektin pada agar-agar bervariasi tergantung dari jenis dan asal rumput laut yang digunakan sebagai bahan baku (Guisseley, 1968).
4.2.4 FTIR agar-agar
Spektrum FTIR hasil pengukuran dapat digunakan untuk mengetahui gugus fungsi yang terdapat dalam sampel agar-agar, karena spektrum infra merah senyawa organik memiliki sifat yang khas dan mempunyai karakter spektrum yang berbeda dengan senyawa lain sehingga dapat dijadikan sebagai bukti apakah senyawa yang diperoleh dari hasil ekstraksi merupakan agar-agar atau senyawa lain. Hasil pengukuran FTIR untuk agar-agar perlakuan asam jawa dapat dilihat pada Lampiran 2.
Identifikasi gugus fungsi dari pita-pita serapan yang terdapat pada spektrum untuk agar-agar perlakuan asam jawa dapat dilihat pada Tabel 4.2
30 Tabel 4.2 Identifikasi Gugus Fungsi Agar-Agar Perlakuan Asam Jawa Bilangan
gelombang (cm-1)
Gugus fungsi Agar-agar komersial
Agar-agar Perlakuan asam jawa
5% 10% 15% 870-900 Grup sulfat C-6 α-L-galaktosa 879.66 877.36 879.75 880.39 920-950 C-O-C 3,6- anhidro-α-L-galaktosa 929.01 930.05 930.82 931.73 1000-1100 3,6 anhidrogalaktosa 1024.65 1020.82 1021.96 1023.75 1200-1300 S=O ester sulfat 1245.15 1245.40 1243.98 1243.72 2850-2970 C-H
3,6-anhidrogalaktosa 2897.61 2919.56 2919.24 2916.41
Pita-pita serapan yang muncul pada setiap spektra menghasilkan bilangan gelombang (cm-1) yang hampir sama seperti pada kemunculan gugus C-H 3,6 anhidrogalaktosa. Pada praperlakuan asam jawa 5% dan 10% gugus C-H muncul pada bilangan gelombang 2919 cm-1 dan pada praperlakuan asam jawa 15% gugus C-H muncul pada bilangan gelombang 2916 cm-1. Setiap pita-pita serapan yang muncul pada spektra menghasilkan bilangan gelombang yang tidak berbeda jauh dan spektra yang muncul menghasilkan gugus fungsi yang sama, sehingga diduga setiap spektra perlakuan asam jawa menghasilkan senyawa yang sama yaitu agar-agar. Struktur penyusun agar-agar (agarosa dan agaropektin) dan struktur molekul agar-agar ditunjukkan pada Gambar 4.4 dan gambar 4.5.
Agaropektin
Gambar 4.4 Struktur penyusun agar-agar. (Varshosaz, Zaki, Minaiyan & Banoozadeh, 2015)
Gambar 4.5 Rumus bangun Agar-Agar (Aslan, 1998)
Spektrum FTIR yang dihasilkan (Lampiran 2) berupa pita-pita serapan pada daerah panjang gelombang tertentu. Dari keempat spektrum terlihat pita-pita serapan mirip dengan bilangan gelombang yang tidak terlalu berbeda jauh. Setiap jenis ikatan yang berbeda mempunyai sifat frekuensi vibrasi yang berbeda dan jenis ikatan yang sama dalam suatu senyawa yang berbeda terletak dalam lingkungan yang sedikit berbeda, maka tidak ada dua molekul yang berbeda strukturnya akan mempunyai bentuk serapan yang tepat sama. Dengan membandingkan spektrum dari dua senyawa yang diperkirakan identik maka dapat diketahui apakah kedua senyawa tersebut identik. Pelacakan tersebut lazim dikenal dengan bentuk sidik jari dari dua spektrum tersebut. Puncak-puncak serapan di daerah sidik jari pada spektrum inframerah merupakan kekhasan untuk setiap senyawa. Daerah sidik jari berada di daerah frekuensi rendah, yaitu dari 2000-300 cm-1. Jika puncak spektrum inframerah kedua senyawa tepat sama maka dalam banyak hal kedua senyawa tersebut adalah identik.
Ekstrak agar-agar umumnya mempunyai serapan gugus fungsi CH2 pada bilangan gelombang 2960 cm-1, gugus 3,6 anhidrogalaktosa pada 1070 cm-1, gugus 1,3 β-D galaktosa piranosil pada 897 cm-1, dan gugus ester sulfat pada bilangan gelombang 1180 cm-1, 1250 cm-1, 1370 cm-1 (Sur & Guven, 2002). Fraksi agarosa umumnya mempunyai serapan pada 897 cm-1 untuk gugus 1,3 β-D galaktosa
32 piranosil, serta adanya serapan pada 930 cm-1 dan 1070 cm-1 yang menunjukkan gugus 3,6 anhidrogalaktosa, dimana ikatan 3,6 anhidrogalaktosa pada agarosa jumlahnya lebih tinggi dibandingkan fraksi agaropektin. Fraksi agaropektin mempunyai serapan gugus 3,6 anhidrogalaktosa pada bilangan gelombang 1070 cm-1, serta serapan pada 1250 cm-1 dan 850 cm-1 yang menunjukan adanya kelompok sulfat (Balkan, Coban & Guven, 2005).
33 BAB V
PENUTUP
5.1KESIMPULAN
Berdasarkan penelitian “ Ekstraksi dan Analisis Agar-Agar dari Rumput Laut Gracilaria sp. Menggunakan Asam Jawa” dapat disimpulkan bahwa:
1. Asam jawa dapat digunakan dalam proses ekstraksi agar-agar dari rumput laut Gracilaria sp. Hal ini karena asam jawa mengandung beberapa jenis asam yang dapat memecahkan dinding sel rumput laut sehingga memudahkan proses ekstraksi agar-agar.
2. Kualitas agar-agar yang dihasilkan dari perlakuan asam jawa pada konsentrasi 5% menghasilkan rendemen 28,8 % dengan nilai kekuatan gel 168,28 g/cm2 dan kadar sulfat 3%, pada konsentrasi 10% rendemen yang dihasilkan adalah 35,35% dengan nilai kekuatan gel 178,85 g/cm2 dan nilai kadar sulfat 2%, sedangkan pada konsentrasi 15% adalah hasil terbaik dengan nilai rendemen 40.5%, nilai kekuatan gel 193,24 g/cm2 dan nilai kadar sulfat 1,5%. Semakin tinggi rendemen dan kekuatan gel agar-agar yang dihasilkan maka kualitasnya semakin bagus sehingga nilai ekonomisnya juga semakin tinggi.
5.2 SARAN
Dalam penelitian ini proses pengeringan tidak menggunakan oven sehingga proses pengeringan berlangsung sangat lama karena tergantung pada kondisi matahari. Disarankan pada penelitian selanjutnya pengeringan agar-agar dilakukan menggunakan oven. Selain itu perlu dibandingkan dengan metode pembuatan agar-agar praperlakuan menggunakan basa dan perlu diketahui umur panen, habitat dan tempat budidaya dari rumput laut yang akan digunakan untuk mendapatkan mutu agar-agar yang lebih baik. Sebagai kelanjutan penelitian ini diharapkan untuk menambahkan beberapa analisis sehingga agar-agar yang didapatkan sesuai dengan SNI.