AKTIVITAS ANTIOKSIDAN EKSTRAK DAN FRAKSI KULIT BUAH MANGGIS (Garcinia mangostana L) SECARA KOLORIMETRI
Nyi Mekar Saptarini1, Ginayanti Hadisoebroto2, Budhi Kusuma2
1Fakultas Farmasi, Universitas Padjadjaran, Jl Raya Bandung Sumedang km 21 Jatinangor 45363 2Jurusan Farmasi, FMIPA, Universitas Al Ghifari, Jl Saninten 140 Bandung
Corresponding author email: mkrnyi@gmail.com
ABSTRAK
Kandungan utama kulit buah manggis (Garcinia mangostana L) adalah xanton. Xanton merupakan turunan polifenol yang memiliki aktivitas antioksidan. Tujuan penelitian ini adalah menentukan aktivitas antioksidan ekstrak etanol dan fraksi kulit buah manggis dengan metode peredaman radikal bebas 1,1-difenil-2-pikrilhidrazil (DPPH). Analisis kualitatif dilakukan dengan kromatografi lapis tipis dan analisis kuantitatif dilakukan dengan kolorimetri untuk mendapatkan nilai IC50. Hasil kualitatif menunjukkan bahwa ekstrak etanol, fraksi n-heksan,
fraksi etil asetat dan fraksi air memiliki aktivitas antioksidan. Hasil kuantitatif menunjukkan nilai IC50 ekstrak etanol, fraksi n-heksan, fraksi etil asetat, dan fraksi air adalah 13,73 ppm,
69,01 ppm, 34,50 ppm dan 16,31 ppm, secara berturut-turut.
Kata kunci: Manggis (Garcinia mangostana L), ekstrak, fraksi, antioksidan, IC50
ABSTRACT
The major mangosteen (Garcinia mangostana L) pericarp content is xanthones. Xanthones are poliphenolic derivatives which have antioxidant activity. The aim of this study was determine the antioxidant activity of ethanolic extracts and fractions of mangosteen pericarp with 1,1-diphenyl-2-picrylhydrazyl (DPPH) free radical scavenging method. Qualitative analysis was conducted by thin layer chromatography and quantitative analysis was conducted by colorimetry to obtain the IC50 values. Qualitative results showed that ethanolic extract, n-hexane fraction, ethyl acetate fraction and water fraction have antioxidant activity. Quantitative results showed the IC50 value of ethanolic extract, n-hexane fraction, ethyl acetate fraction, water fraction was 13.73 ppm, 69.01 ppm, 34.50 ppm dan 16.31 ppm, respectively.
Keywords : Mangosteen (Garcinia mangostana L), extract, fraction, antioxidant, IC50
PENDAHULUAN
Antioksidan merupakan senyawa yang dapat memperlambat atau menghambat reaksi oksidasi (Pokorny dkk, 2001). Senyawa antioksidan mengatasi dampak merugikan radikal bebas terhadap pertahanan tubuh. Radikal bebas mengalami reaksi oksidasi, sehingga menimbulkan beberapa penyakit, seperti kanker, aterosklerotik aorta dan penuaan (Kosasih dkk, 2006). Radikal bebas merupakan atom atau gugus yang memiliki satu atau lebih elektron tidak berpasangan. Radikal bebas dapat berasal dari debu, polusi maupun diproduksi sebagai hasil metabolisme normal (Septiana dkk, 2003).
Kulit buah manggis (Garcinia mangostana
L, Guttiferae) mengandung senyawa antioksidan alami, yaitu xanton. Senyawa xanton dalam manggis meliputi mangostin, mangostenol A, mangostinon A, mangostinon B, trapezifoxanton, tovofillin B, alfa mangostin, beta mangostin, garsinon B, mangostanol, flavanoid epikatekin dan gartanin (Qosim, 2007). Uji aktivitas antioksidan dengan menggunakan peroksinitrit sebagai radikal bebas diketahui bahwa gartanin, alfa mangostin dan beta mangostin merupakan senyawa yang memiliki aktivitas antioksidan terbesar (Jung et al., 2006). Penelitian ini dilakukan untuk
Seminar Nasional Farmasi (SNIFA) UNJANI
206 Peran Apoteker dalam Menjamin Mutu, Efektifitas, Keamanan pada Obat, Makanan dan Kosmetik Sebagai Upaya Meningkatkan Derajat Kesehatan Masyarakat Indonesia
menentukan aktivitas antioksidan ekstrak dan fraksi kulit buah manggis secara kolorimetri menggunakan radikal 1,1-difenil-2-pikrilhidrazil (DPPH).
METODE
Pengumpulan dan determinasi tanaman. Buah manggis diperoleh dari desa Mekarmukti, Kabupaten Ciamis. Buah memiliki diameter 65 mm, berwarna ungu kehitaman, berusia sekitar 114 hari sejak bunga mekar. Determinasi tanaman dilakukan di Laboratorium Taksonomi Tumbuhan Jurusan Biologi Fakultas MIPA Universitas Pajajaran.
Pembuatan simplisia. Kulit buah dipisahkan dari buahnya, kemudian dicuci dan diiris tipis. Irisan dikeringkan tanpa pemanasan langsung hingga bobot konstan. Simplisia dihaluskan hingga dapat melewati ayakan No. 18, kemudian ditentukan kadar airnya.
Pembuatan ekstrak. Sebanyak 200 g serbuk simplisia direndam dengan 1 L etanol 96% pada suhu ruang selama 3 x 24 jam. Setiap 24 jam dilakukan penggantian pelarut. Filtrat dipekatkan dengan rotary vaporator
dan dihitung rendemennya. Rendemen = bobot ekstrak
bobot simplisia x 100% (1) Fraksinasi. Sebanyak 7 g ekstrak dilarutkan dalam 70 mL air, dimasukkan ke dalam corong pisah dan ditambahkan 20 mL n-hexan. Corong pisah ditutup dan dikocok, kemudian didiamkan hingga terpisah. Lapisan n-hexana ditampung. Lapisan air ditambahkan lagi 20 mL n-hexan, dilakukan perlakuan yang sama sebanyak dua kali. Lapisan air ditambahkan 20 mL etil asetat dan mendapat perlakuan yang sama seperti fraksinasi n-hexan. Fraksi n-hexan, etil asetat dan air dipekatkan dan dihitung rendemennya (Desmiaty dkk, 2008).
Rendemen = bobot fraksi
bobot ekstrak x 100% (2) Skrining fitokimia. Skrining fitokimia pada simplisia, ekstrak, dan fraksi dilakukan dengan metode reaksi warna (Fransworth, 1996).
Kromatografi lapis tipis (KLT). Ekstrak etanol, fraksi n-hexan, fraksi etil asetat dan fraksi air dilarutkan dalam pelarut, kemudian ditotolkan pada pelat KLT dan dielusi dengan
n-butanol : asam asetat : air (4 :1 : 5). Penampak bercak berupa larutan DPPH 40 ppm (Desmiaty dkk, 2008).
Uji aktivitas antioksidan
a. Penentuan panjang gelombang maksimum. Sebanyak 2 ml larutan DPPH 40 ppm ditambah 1 mL etanol 96%, kemudian absorban diukur dengan spektrofotometer sinar tampak pada panjang gelombang 400-800 nm (Rahayu dkk, 2010).
b. Pengukuran aktivitas antioksidan. Sebanyak 2 mL larutan DPPH 40 ppm ditambah 1 mL sampel uji dan vitamin C, masing-masing lima variasi konsentrasi. Campuran diinkubasi selama waktu terpilih, kemudian absorban diukur pada panjang gelombang maksimum (Rahayu dkk, 2010).
c. Perhitungan IC50. Persen aktivitas antioksidan pada variasi konsentrasi sampel dan vitamin C dibuat persamaan garis. Nilai IC50 dihitung ketika % aktivitas antioksidan
sebesar 50% (Cahyana et al., 2002).
(%) akt antioksidan = abs kontrol−abs sampel
absorban kontrol x 100% (3) HASIL DAN PEMBAHASAN
Tujuan determinasi adalah memastikan kebenaran tanaman yang digunakan. Hasil determinasi menunjukkan bahwa tanaman adalah manggis (Garcinia mangostana L). Sebanyak 5 kg kulit buah manggis menghasilkan 2987 g serbuk simplisia dengan kadar air sebesar 2,3%.
Maserasi dipilih sebagai metode ekstraksi karena menggunakan suhu ruangan, sehingga tidak merusak senyawa termolabil dalam simplisia. Sebanyak 200 g simplisia menghasilkan 45,6 g ekstrak kental, dengan rendemen sebesar 22,8%. Ekstrak kental berwarna coklat kehitaman. Selanjutnya, dilakukan fraksinasi menggunakan ekstraksi cair-cair, untuk memisahkan senyawa berdasarkan polaritasnya. Rendemen fraksi n-heksan, etil asetat, dan air secara berturut-turut adalah 7,0; 28,2; dan 58,7%. Nilai rendemen menunjukkan banyaknya senyawa yang dapat terlarut dalam pelarut yang digunakan. Sebagian besar metabolit sekunder kulit buah manggis larut dalam air.
Penapisan fitokimia dilakukan untuk mengidentifikasi golongan metabolit sekunder yang ada dalam simplisia, ekstrak, dan fraksi (Tabel 1). Hasil skrining menunjukkan semua
golongan metabolit sekunder dalam simplisia dapat terekstraksi dengan cara maserasi menggunakan etanol. Semua fraksi mengandung flavonoid dan tanin. Artinya, polaritas flavonoid dan tanin dalam kulit buah manggis memiliki bersifat polar, semi polar, dan non polar.
Analisis kualitatif aktivitas antioksidan dari ekstrak, fraksi n-heksana, fraksi etil asetat dan fraksi air dengan KLT menunjukkan terbentuknya bercak kuning dengan latar belakang ungu ketika direaksikan dengan DPPH. Metabolit sekunder yang diperkirakan memiliki aktivitas antioksidan adalah flavonoid, tanin, dan polifenol. Ketiga golongan ini terdistribusi dalam ekstrak dan fraksi.
Larutan DPPH berwarna ungu, sehingga memberikan absorban maksimum pada panjang gelombang di daerah sinar tampak, yaitu 518 nm. Analisis kuantitatif aktivitas antioksidan sampel ditentukan dengan radikal DPPH secara kolorimetri. Perubahan warna radikal DPPH disebabkan oleh reaksi antara radikal bebas DPPH (ungu) dengan satu atom hidrogen yang dilepaskan senyawa dalam sampel membentuk senyawa 1,1-difenil-2-pikrilhidrazin (kuning). Absorbansi yang diukur adalah absorbansi larutan DPPH sisa yang tidak bereaksi dengan senyawa antioksidan (Josephy,1997).
Aktivitas antioksidan ekstrak, fraksi etil asetat, dan fraksi air diperkirakan berasal dari golongan flavonoid, polifenol, dan tanin. Ketiganya merupakan donor atom hidrogen untuk ditangkap oleh radikal DPPH dan berubah menjadi bentuk netralnya. Aktivitas antioksidan fraksi n-heksan diperkirakan berasal dari golongan flavanoid dan tanin. Golongan polifenol tidak terdeteksi dalam fraksi n-heksan. Hal ini disebabkan karena golongan polifenol umumnya bersifat polar dan ada dalam bentuk glikosida yang berikatan dengan suatu gula. Ekstrak, fraksi etil asetat dan fraksi air termasuk kategori antioksidan sangat kuat karena IC50 < 50 ppm.
Fraksi n-heksan termasuk kategori antioksidan kuat karena IC50 50-100 ppm (Blois, 2005). SIMPULAN
Nilai IC50 ekstrak etanol, fraksi n-heksan,
fraksi etil asetat dan fraksi air secara
berturut-turut adalah 13,73 ppm, 69,01 ppm, 34,50 ppm dan 16,31 ppm. Ekstrak, fraksi etil asetat dan fraksi air termasuk kategori antioksidan sangat kuat, sedangkan fraksi n-heksan termasuk kategori antioksidan kuat.
DAFTAR PUSTAKA
Blois, M.S. 2005. Antioxidant Determination by The Use of Stable Free Radical.
Nature 181:1191-1200.
Cahyana, M., Ekaprasada, T., Herry, A. 2002. Isolasi Senyawa Antioksidan Kulit Batang Kayu Manis (Cinnamomum
burmannii Neesex Blume), ISSN No.
0216-0781.
Departemen Kesehatan Republik Indonesia. 1978. Materia Medika Indonesia. Edisi III, Jakarta: Depkes RI. Hal 150-156, 165-167.
Departemen Kesehatan Republik Indonesia. 1979. Farmakope Indonesia. Edisi III, Jakarta: Depkes RI. Hal 29-31, 33, 649, 748.
Desmiaty, Y., Julia, R., Ika, R. 2008., Uji Aktivitas Penangkap Radikal Bebas Daun Cerme (Phyllanthus acidus (L) Skeels., Jurnal Farmasi Indonesia Vol. 4 No. 2 Juli 2008: 70-74.
Fransworth, N.R. 1996. Biological and Phytochemical Screening of Plants. Journal of Pharmaceutical Science. Volume 55 No.3. Chicago: Reheis Chemical Company. Pages 257-259, 263. Harborne, J.B. 2006. Metode Fitokimia:
penuntun cara modern menganalisis tumbuhan. Padmawinata K, Soediro I, penerjemah. Bandung : ITB Press. Terjemahan dari: Phytochemical Methods.
Houghton, P.J., Rahman, A. 1998. Laboratory Handbook for the Fractionation of Natural Extracts. Chapman and Hall, London. 40.
Josephy, P.D., 1997, Molecular Toxicology, Oxford University Press, New York, 44-103.
Jung, P., Pootakham, K., Pongpaibul, Y., Duangrat, C., dan Tharavichitkul, P., 2008. Acute and Repeated Dose 28-Day Oral Toxicity Study of Garcinia mangostana Linn. Rind Extract. CMU. J. Nat. Sci. 7 (2):199-208.
Seminar Nasional Farmasi (SNIFA) UNJANI
208 Peran Apoteker dalam Menjamin Mutu, Efektifitas, Keamanan pada Obat, Makanan dan Kosmetik Sebagai Upaya Meningkatkan Derajat Kesehatan Masyarakat Indonesia
Kosasih, E.N., Tony, S., Hendro, H. (2006). Peran Antioksidan pada Lanjut Usia. Pusat Kajian Nasional Masalah Lanjut Usia. Jakarta.
Marciniak, A., Brzeszczyńska, J., Gwoździński, K., dan Jegier, A., 2009.
Antioxidant Capacity and Physical Exercise. Biology of Sport. 26 (3):197-213.
Mardawati, E., Achyar, C.S., Marta, H. 2008. Kajian Aktivitas Antioksidan Ekstrak Kulit Manggis (Garcinia mangostana L ) Dalam Rangka Pemanfaatan Limbah Kulit Manggis Di Kecamatan Puspahiang Kabupaten Tasikmalaya. Bandung. Fakultas Teknologi Industri Pertanian Universitas Padjadjaran.
Markakis, P. 1982. Anthocyanins as Food Additives. Anthocyanins as Food Colors. Markakis, P. (ed). 1982. Academic Press. New York.
Molyneux, P. 2004. The Use of The Stable Free Radical Diphenylpicrylhydazyl (DPPH) for Estimating Antioxidant Activity. Songklanakarin Journal Science Technology. 26(2): 211-219.
Pedraza-Chaverri, J., Cárdenas-Rodríguez, N., Orozco-Ibarra, M., dan Pérez-Rojas, J.
M. 2008. Medicinal Properties of Mangosteen (Garcinia mangostana L.).
Food and Chemical Toxicology. 46:
3227-39.
Pokorny, J., Yanishlieva, N., Gordon, M. 2001, Antioxidant in Food: Practical Application, CRC Press Cambridge, New York.
Qosim, W.A. 2007. Kulit Buah Manggis Sebagai Antioksidan. Available at
http://www.pikiran-rakyat.com./cetak/2007/022007/15/kamp us/lain01.htm
Reynertson, K.A. 2007. Phytochemical Analysis of Bioactive Constituen from
Edible Myrtaceae Fruit. The City
Univercity of New York: New York.Sobir dan Poerwanto. 2007.
Mangosteen Genetics and Improvement. International Journal of Plant Breeding.
1(2): 105-11.
Zarena, A.S., Sankar, K.U. 2009. Study of Antioxidant Properties from Garcinia mangostana L. Pericarp Extract. Acta Sci. Pol.Technol. Aliment. 8 (1): 23-34.
Tabel 1. Hasil Skrining Fitokimia
Golongan Simplisia Ekstrak Fraksi
n-Heksan Etil asetat Air
Alkaloid - - - - - Flavanoid + + + + + Tanin + + + + + Polifenol + + - + + Terpenoid/ Steroid + + + - - Saponin + + - - +
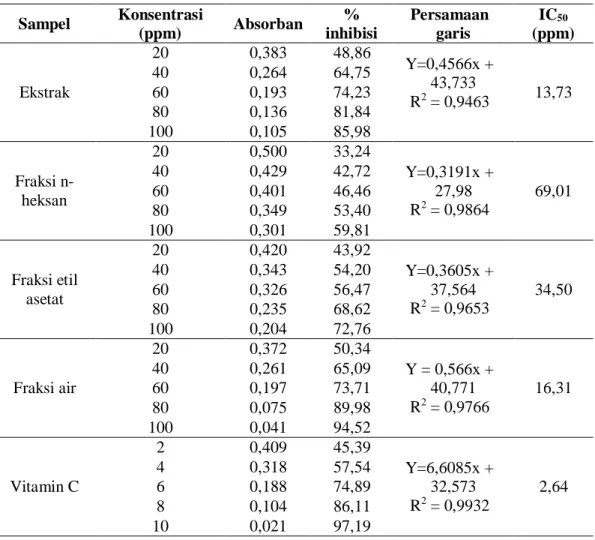
Tabel 2. Nilai IC50 Sampel dan Vitamin C Sampel Konsentrasi (ppm) Absorban % inhibisi Persamaan garis IC50 (ppm) Ekstrak 20 0,383 48,86 Y=0,4566x + 43,733 R2 = 0,9463 13,73 40 0,264 64,75 60 0,193 74,23 80 0,136 81,84 100 0,105 85,98 Fraksi n-heksan 20 0,500 33,24 Y=0,3191x + 27,98 R2 = 0,9864 69,01 40 0,429 42,72 60 0,401 46,46 80 0,349 53,40 100 0,301 59,81 Fraksi etil asetat 20 0,420 43,92 Y=0,3605x + 37,564 R2 = 0,9653 34,50 40 0,343 54,20 60 0,326 56,47 80 0,235 68,62 100 0,204 72,76 Fraksi air 20 0,372 50,34 Y = 0,566x + 40,771 R2 = 0,9766 16,31 40 0,261 65,09 60 0,197 73,71 80 0,075 89,98 100 0,041 94,52 Vitamin C 2 0,409 45,39 Y=6,6085x + 32,573 R2 = 0,9932 2,64 4 0,318 57,54 6 0,188 74,89 8 0,104 86,11 10 0,021 97,19