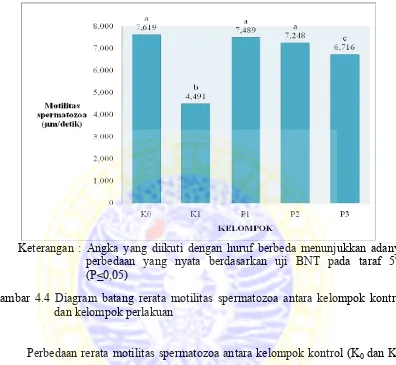
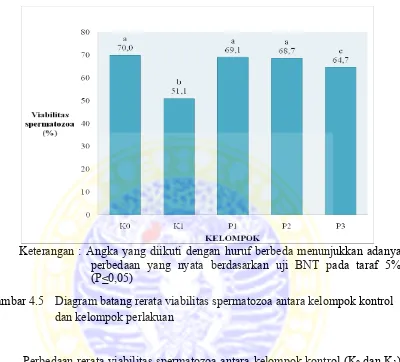
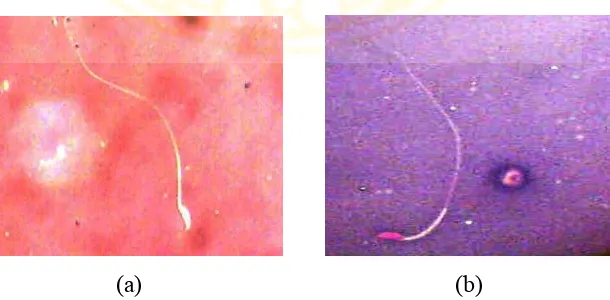
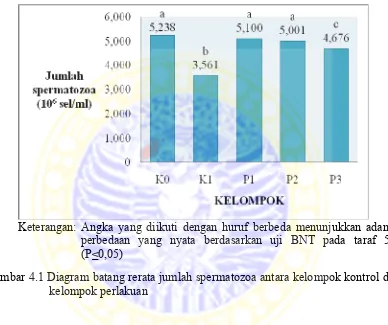
BAB IV HASIL DAN PEMBAHASAN 4.1 Hasil Penelitian 4.1.1 Pengaruh ekstrak jahe terhadap jumlah spermatozoa mencit yang terpapar 2-ME - PENGARUH EKSTRAK JAHE (Zingiber officinale Rosc.) var. Gajah TERHADAP KUALITAS SPERMATOZOA MENCIT (Mus musculus) YANG TERP
Teks penuh
Gambar
Dokumen terkait
Selain itu, adverbia totemo adalah ungkapan yang sedikit santai dan tidak ada indikasi melebih-lebihkan atau membesar-besarkan dan tidak dapat digunakan untuk
Pemantauan adalah usaha atau tindakan mengamati, mengawasi, dan memeriksa secara terstruktur perubahan kualitas tata ruang dan lingkungan yang tidak sesuai dengan
Penelitian yang dilakukan oleh Harvard Medical School (dalam Suardiman, 2011) melaporkan bahwa faktor-faktor yang memengaruhi successful aging yaitu: 1) adanya
Gambar 2.9 Hubungan tegangan menengah ke tegangan rendah dan konsumen Sistem distribusi sekunder digunakan untuk menyalurkan tenaga listrik dari.. gardu distribusi ke
Anggaran Satuan Kerja Direktorat Pembinaan Sekolah Menengah Kejuruan.. ini.
Bertambahnya beban yang bersifat induktif membutuhkan daya reaktif yang besar sehingga sumber (pembangkit listrik) harus mensuplai daya yang lebih besar. Keadaan seperti
Penentuan penerima dana BSM dengan cara manual ini dapat menyebabkan kesalahan pada saat menyeleksi, Sehigga kriteria penilaian siswa miskin yang telah di tetapkan sering terjadi
Di lain pihak, adanya asam lemak bebas yang berlebih atau kondisi hiperlipidemia juga dapat menyebabkan overproduksi ROS yang selanjutnya dapat mengakibatkan kerusakan DNA