6 mL, penetapan diulangi. Namun, jika kurang
dari atau sama dengan 0.1 mL, rerata hasilnya digunakan untuk penentuan nilai COD.
HASIL DAN PEMBAHASAN
Mikrob pada Inokulum
Inokulum yang digunakan dalam penelitian berasal dari lumpur aktif sungai Ciliwung. Pemilihan mikrob ini dikarenakan sebagian besar limbah industri maupun sisa konsumsi masyarakat dibuang ke sungai. Lumpur aktif ini lalu dikondisikan berdasarkan kondisi lingkungannya, yaitu pH 7 dan suhu 27 ºC (OECD 1995).
Lumpur aktif diaerasi, karena mikrob yang digunakan bersifat aerob. Proses aerasi dilakukan selama 7 hari untuk mematikan mikrob anaerob yang dicirikan dengan hilangnya aroma bau dari lumpur sehingga mikrob yang dihasilkan hanya mikrob aerob sesuai metode OECD (1992) dan JIS (2005). Selama aerasi dilakukan pengukuran jumlah mikrob.
Selama aerasi ditambahkan nutrisi seperti bufer fosfat dan senyawaan logam ke dalam biakan mikrob. Penambahan ini bertujuan menjaga pH larutan agar tetap karena selama pertumbuhan, mikrob akan menghasilkan senyawa asam atau basa yang dapat mengubah pH sistem sehingga dapat menurunkan populasi mikrob. Penambahan nutrisi yang lain seperti senyawaan logam ialah sebagai sumber energi bagi mikrob itu.
Mikrob yang digunakan bersifat umum sebagaimana yang terdapat di lumpur, dan bukan isolat. Hal ini disebabkan OSD yang diuji harus pada keadaan alamiah. Lumpur aktif hanya dapat bertahan selama 3 bulan. Apabila setelah 3 bulan analisis belum selesai, maka lumpur aktif tidak dapat digunakan lagi dan harus dilakukan pengambilan sampel lumpur aktif baru (OECD 1992).
Metode hitungan cawan digunakan untuk menghitung jumlah koloni yang tumbuh. Metode ini didasarkan pada anggapan bahwa setiap sel dapat hidup dan berkembang menjadi satu koloni. Jumlah koloni yang terlihat pada cawan menunjukkan jumlah organisme yang dapat hidup dan terkandung dalam sampel. Medium yang digunakan adalah NA karena dapat menumbuhkan berbagai jenis mikrob. Setelah 24 jam mikrob ditumbuhkan, hanya 1 sampai 4 cawan yang memenuhi persyaratan secara statistik.
Analisis jumlah mikrob bertujuan memastikan keberadaan mikrob dalam lumpur
dan untuk menentukan apakah lumpur memenuhi syarat untuk digunakan dalam uji. Analisis dilakukan 2 kali sesuai metode analisis yang diuji, yaitu DOC die-away dan botol tertutup, karena lumpur yang digunakan berbeda waktu pengambilannya meskipun tempat dan cara pengambilannya sama.
Pengenceran lumpur dilakukan secara desimal untuk memudahkan penentuan jumlah mikrob. Nilai berkisar antara 10-2 dan 10-7. Jumlah koloni yang dapat dihitung dalam lumpur DOC sebanyak 104 koloni pada cawan dengan konsentrasi 10-4, sementara pada botol tertutup sebanyak 182 dan 64 pada konsentrasi 10-2 dan 10-3. Nilai tersebut diambil karena jumlah koloni terbaik dalam cawan setelah masa inkubasi adalah 30 dan 300 (Fardiaz 1989). Karena itu, jumlah koloni kurang dari 30 dan lebih dari 300 tidak dimasukkan dalam perhitungan. Jumlah koloni mikrob dalam lumpur dihitung dengan mengalikan jumlah koloni dalam cawan dengan pengenceran, yakni 1.23 × 104 untuk lumpur botol tertutup dan 1.04 × 106 untuk lumpur DOC (Lampiran 7). Jumlah mikrob tersebut menunjukkan bahwa lumpur tersebut memenuhi persyaratan untuk digunakan dalam kedua metode tersebut.
Karbon Organik Terlarut (DOC) Metode DOC menganalisis penguraian bahan berdasarkan konsentrasi DOC yang dipindahkan atau hilang. Nilainya dikoreksi dengan blangko untuk meminimumkan galat.
Nilai DOC diperoleh dengan cara memasukkan nilai absorbans sebagai peubah
x ke dalam persamaan garis linear OSD dan
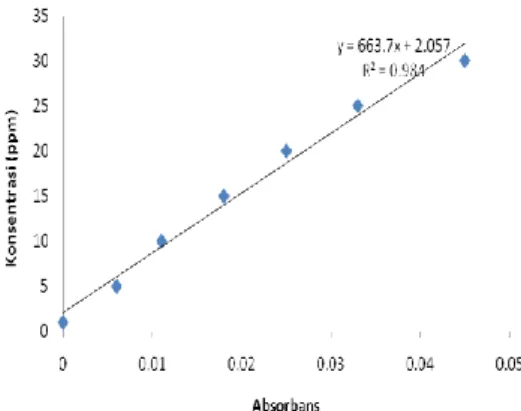
standar Na-benzoat. Tabel 2 memperlihatkan hasil pembacaan serapan Na-benzoat dan OSD. Persamaan garis linear standar dan OSD pada Gambar 1 dan 2 diperoleh berturut-turut
y = 663.7x + 2.057 serta y = 841.3x + 1.441.
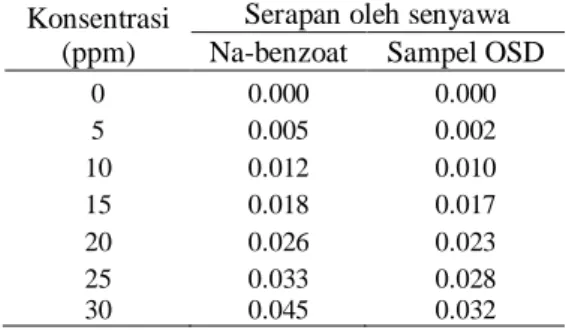
Tabel 2 Serapan Na-benzoat dan OSD pada panjang gelombang 360 nm untuk menentukan regresi linear
Konsentrasi (ppm)
Serapan oleh senyawa Na-benzoat Sampel OSD
0 0.000 0.000 5 0.005 0.002 10 0.012 0.010 15 0.018 0.017 20 0.026 0.023 25 0.033 0.028 30 0.045 0.032
7 Gambar 1 Kurva regresi linear Na-benzoat.
Gambar 2 Kurva regresi linear OSD. Secara teoretis, nilai DOC akan turun karena senyawa karbon yang terkandung akan menjadi sumber energi mikrob selama degradasi berlangsung. Nilai DOC dapat diterima jika setelah 28 hari masih tidak kurang dari 70%.
Suhu dan pH dijaga tetap konstan selama pengujian. Perubahan suhu dan pH akan menyebabkan mikrob mati dan pengujian tidak sesuai dengan OECD. Karena itu, medium mineral selain mengandung nutrisi yang dibutuhkan juga mengandung larutan penyangga untuk mempertahankan pH, sebab selama pertumbuhannya, mikrob menghasil kan senyawa asam maupun basa.
Jumlah mikrob akan terus meningkat karena dilakukan aerasi selama pengujian. Aerasi menjaga agar DO dalam metode DOC tetap selama inkubasi sehingga kemampuan mikrob lebih maksimal dalam mendegradasi bahan. Mikrob mendegradasi senyawa dengan cara memutus ikatan kimia menggunakan enzim seperti peroksidase. Tingginya DO dalam air akan menyebabkan mikrob semakin banyak menghasilkan enzim untuk mendegradasi senyawa.
Analisis DOC dilakukan dengan spektrofotometer UV. Salah satu syarat dalam analisis ini ialah sampel harus tidak berwarna dan jernih. Untuk mencegah gangguan serapan oleh mikrob pada saat pengukuran, dilakukan penyaringan dengan kertas saring 0.45 µm terlebih dahulu. Mikrob pada umumnya berukuran ≥0.45 µm. Penyaringan dapat memisahkan mikrob dari larutan sehingga serapan yang dihasilkan hanya berasal dari karbon.
Persentase penguraian standar lalu dihitung sebagai hasil bagi antara rerata hasil pengukuran pada hari yang telah ditentukan dengan rerata hasil pengukuran pada hari ke-0. Masing-masing dikoreksi dengan blangko dan nilainya tidak lebih dari 1.
Analisis penguraian bahan uji yang tidak diketahui komponen penyusunnya dilakukan melalui persamaan di bawah ini:
Corg + H2O2 CO2 + 2H+ + 2e
-Reaksi tersebut memperlihatkan bahwa DOC dapat dicari dengan anggapan oksigen bereaksi sempurna dengan karbon organik menghasilkan karbon dioksida. Karbon dioksidasi dengan oksidator kuat seperti peroksida. Peroksida dihasilkan oleh aktivitas mikrob selama inkubasi dan digunakan untuk mendegradasi senyawa. Jumlah oksigen yang digunakan dalam reaksi dapat diketahui dari COD. Nilai COD ditentukan dengan refluks tertutup pada suhu 150 ºC selama 2 jam dan dilanjutkan dengan metode titrimetri. Dalam penelitian ini diperoleh nilai COD sebesar 0.76 mg O2/mg bahan (Lampiran 8). Bahan uji
yang digunakan dalam penelitian ini ialah OSD. Perhitungan persen penguraian OSD dapat diperoleh dari nilai COD dan absorbans (Lampiran 9).
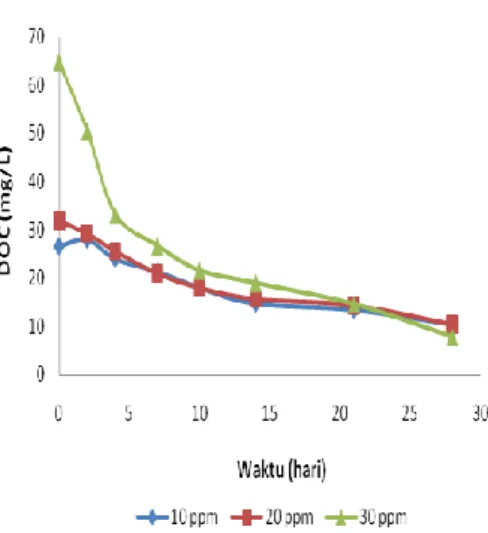
Nilai DOC Na-benzoat dengan konsentrasi 10, 20, dan 30 mg/L pada hari ke-0 berturut-turut sebesar 29.60, 31.92, dan 64.78 mg/L. Nilai ini dinyatakan sebagai konsentrasi DOC awal sebelum terurai. Konsentrasi DOC hasil penguraian setelah waktu tertentu dihitung berdasarkan konsentrasi awalnya. Nilai DOC setelah 28 hari turun berturut-turut menjadi 10.35, 10.35, dan 7.96 mg/L. Berkurangnya karbon terlarut dalam senyawa standar Na-benzoat berlangsung terus selama waktu penguraian, sebagaimana terlihat pada Gambar 3.
8 Gambar 3 Kurva hubungan DOC Na-benzoat
dengan variasi konsentrasi 10, 20,
dan 30 ppm terhadap waktu. Penurunan DOC terhadap waktu juga teramati pada OSD (Gambar 4). Nilai DOC pada OSD konsentrasi 10, 20, dan 30 mg/L setelah 28 hari diperoleh berturut-turut sebesar 1.01, 3.19, dan 3.18 mg/L, sementara DOC awal berturut-turut 5.70, 11.41, dan 17.10 mg/L.
Gambar 4 Kurva hubungan DOC OSD dengan variasi konsentrasi 10, 20, dan 30 ppm terhadap waktu.
Kurva biodegradasi diperoleh dari hubungan antara persen biodegradasi OSD dan waktu. Nilai persen biodegradasi pada metode DOC dihasilkan dari nisbah nilai DOC pada waktu t yang dikoreksi dengan blangko. Penurunan nilai DOC sejalan dengan kenaikan persen biodegradasi. Data dan contoh perhitungan persen biodegradasi dan nilai DOC dapat dilihat pada Lampiran 10.
Penentuan nilai DOC dilakukan selama 28 hari, sesuai dengan ketentuan OECD. Nilai
DOC dihitung dari absorbans yang terukur pada hari ke-0, 2, 4, 7, 10, 14, 21, dan 28. Secara teoretis nilai DOC turun sebanding dengan penurunan jumlah karbon yang terdegradasi, sebaliknya persen biodegradasi meningkat. Hal ini terjadi karena mikrob menghabiskan senyawa karbon dalam larutan selama proses degradasi berlangsung. Nilai DOC dikatakan sahih jika persen degradasi setelah 28 hari tidak kurang dari 70%.
Senyawa standar yang digunakan memiliki peran penting untuk mengetahui kemampuan inokulum mendegradasi senyawa uji. Persen biodegradasi senyawa standar harus memenuhi ketentuan AISE/CESIO (2003). Senyawa standar yang digunakan sebagai kontrol dalam penelitian ini adalah Na-benzoat.
Kurva biodegradasi standar Na-benzoat dan OSD ditunjukkan pada Gambar 5 dan 6. Persen biodegradasi Na-benzoat setelah 28 hari pada konsentrasi 10, 20, dan 30 mg/L berturut-turut sebesar 89.23, 90.28, dan 100% dan untuk OSD sebesar 82.28, 72.02 dan 81.40%. Persen biodegradasi Na-benzoat telah memenuhi ketentuan AISE/CESIO (2003), yaitu 61–95%. Secara teoretis, persen degradasi dengan metode DOC harus lebih tinggi daripada dengan metode botol tertutup karena selama inkubasi kadar DO dijaga konstan dengan aerasi sehingga kandungan oksigen tinggi dan mikrob lebih maksimal dalam mendegradasi senyawa kimia. Semakin banyak DO, akan semakin banyak karbon organik yang teroksidasi menjadi CO2 oleh
aktivitas mikrob.
Gambar 5 Persentase degradasi Na-benzoat dengan variasi konsentrasi 10,
20, dan 30 ppm terhadap waktu dengan metode DOC die-away.
9 Gambar 6 Persentase degradasi OSD dengan
variasi konsentrasi 10, 20, dan 30 ppm terhadap waktu dengan metode DOC die-away.
Botol Tertutup
Metode botol tertutup merupakan analisis penguraian bahan uji yang didasarkan pada konsumsi DO dalam air. Konsentrasi DO akan turun secara berkala selama waktu inkubasi, karena aktivitas mikrob dalam mengurai bahan uji. Dari penurunan nilai DO ini diperoleh nilai BOD.
Nilai persen biodegradasi pada metode botol tertutup dihasilkan dari hasil bagi antara nilai BOD dan nilai ThOD bahan uji. Kenaikan nilai BOD sebanding dengan kenaikan persen biodegradasi, sebaliknya nilai COD yang tinggi dapat menurunkan persen biodegradasi. Penentuan nilai BOD dilakukan selama 28 hari, sesuai dengan ketetapan pada metode botol tertutup. Penentuan nilai BOD dilakukan dari perolehan nilai DO yang terukur pada hari ke-0, 2, 4, 7, 10, 14, 21, dan 28. Secara teoretis, nilai BOD akan naik sebanding dengan penurunan nilai DO. Hal ini terjadi karena mikrob dapat menghabiskan oksigen terlarut dalam air selama proses oksidasi, hingga mencapai nol (kondisi anaerob). Nilai BOD dikatakan sahih jika oksigen yang dihabiskan pada blangko setelah 28 hari tidak melebihi 1.5 mg/L O2.
Konsentrasi residu oksigen pada botol uji setiap waktu tidak boleh di bawah 0.5 mg/L.
Senyawa standar yang digunakan pada penelitian ini adalah natrium benzoat. Rumus molekulnya C6H5CO2Na, maka nilai
ThOD-nya dapat dihitung sebesar 1.66 mg O2/mg
bahan (Lampiran 11). Nilai tersebut dihitung tanpa memperhatikan terjadinya nitrifikasi. Karena komposisi dan ukuran relatif komponen-komponen bahan uji tidak diketahui, dilakukan analisis COD pada OSD sebagai pengganti nilai ThOD (OECD 1992).
Nilai COD meningkat pada konsentrasi bahan uji yang lebih tinggi. Nilai COD yang digunakan pada pembuatan kurva biodegradasi sebesar 3.6302 mg/L O2.
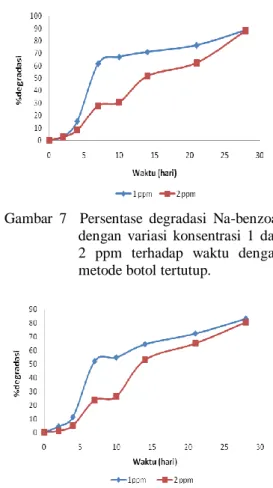
Pemilihan konsentrasi bahan yang digunakan untuk botol tertutup dibatasi oleh kelarutan oksigen dalam air dan metabolisme inokulum. Pada penelitian ini digunakan 2 konsentrasi, yaitu 1 dan 2 mg/L. Nilai persen biodegradasi Na-benzoat dengan metode botol tertutup pada kedua konsentrasi tersebut berturut-turut sebesar 88.55 dan 88.40% setelah 28 hari. Kenaikan persen biodegradasi standar Na-benzoat terhadap waktu dapat dilihat pada Gambar 7. Kedua hasil ini memenuhi ketentuan AISE/CESIO (2003), yaitu 61–95%. Hal ini menunjukkan bahwa hasil pengukuran senyawa uji dapat diterima karena senyawa standar yang digunakan dapat terdegradasi dengan baik. Nilai persen biodegradasi OSD hari ke-28 sendiri diperoleh untuk konsentrasi 1 dan 2 mg/L berturut-turut sebesar 83.13% dan 80.52% (Gambar 8 dan Lampiran 12).
Gambar 7 Persentase degradasi Na-benzoat dengan variasi konsentrasi 1 dan
2 ppm terhadap waktu dengan metode botol tertutup.
Gambar 8 Persentase degradasi OSD dengan
variasi konsentrasi 1 dan 2 ppm
terhadap waktu dengan metode botol tertutup.
10 Secara teoretis, persen degradasi dengan
metode botol tertutup lebih rendah daripada metode DOC die-away karena aerasi mikrob dilakukan hanya sebelum inkubasi. Hal ini mengakibatkan oksigen terlarut menjadi terbatas dan dapat habis oleh mikrob selama aktivitasnya. Keterbatasan oksigen ini menyebabkan aktivitas mikrob tidak maksimal dalam mendegradasi senyawa. Berdasarkan hasil analisis dengan menggunakan metode DOC die-away dan botol tertutup dapat disimpulkan bahwa metode biodegradasi DOC die-away lebih baik dalam hal mendegradasi senyawa.
SIMPULAN DAN SARAN
SimpulanPersentase penguraian Na-benzoat dengan metode DOC die-away sebesar 89.23, 90.28, dan 100% untuk konsentrasi 10, 20, dan 30 ppm, sedangkan dengan metode botol tertutup sebesar 88.55 dan 88.40% untuk konsentrasi 1 dan 2 ppm. Persentase penguraian OSD dengan metode DOC die-away sebesar 82.28, 72.02, dan 81.40% untuk konsentrasi 10, 20, dan 30 ppm serta sebesar 83.13% dan 80.52% untuk konsentrasi 1 dan 2 ppm dengan metode botol tertutup. Metode DOC die- away yang mengukur penurunan konsentrasi DOC memberikan hasil lebih baik daripada metode botol tertutup yang mengukur konsentrasi DO. Aerasi selama inkubasi pada metode DOC
die-away mengakibatkan persentase penguraian lebih baik daripada metode botol tertutup. Berdasarkan hasil yang diperoleh, OSD mudah terdegradasi di alam.
Saran
Perlu dilakukan pengujian dengan metode lain seperti TOC untuk memastikan hasil yang diperoleh.
DAFTAR PUSTAKA
[AISE/CESIO] Association International de la Savonnere de la Detergence et det Produits Entretien/ European Committee of Organic Surfactants and their Inter mediates. 2003. AISE/CESIO Observation on “Ultimate” Biodegradability and The European Detergent Legislation.
Collier KJ. 1987. Spectrophotometric determination of dissolved organic carbon
in some South Island streams and rivers.
NZ J Mar Freshwater Res 21:349-351.
[EC] European Community. 2000. Commision decision of establishing the ecological criteria for the award of the community eco-label to lubricants. Regulation (EC) No 1980/2000, 17 Jul 2000.
[EMSA] European Maritime Safety Agency 2006. Applicability of Oil Spill Dispersant Part 1. Lisbon: EMSA.
[EPA] Environmental Protection Agency. 1998. Fate, Transport, and Transformation Test Guidelines. OPPTS 835.3110 I Ready Biodegradation.
Washington.
[EPA] Environmental Protection Agency. 2009. Dissolved Organic Carbon.
http://www.epa.gov/emap/index.html [20 Feb 2009].
Fardiaz S. 1989. Analisis Mikrobiologi
Pangan. Bogor: IPB Pr.
Fardiaz S. 1992. Polusi Air dan Udara. Bogor: PAU Pangan dan Gizi.
[FEA] Federal Environmental Agency. 1999.
Classification of Substances and Mixtures into Water Hazard Classes according to the Administrative Regulation on the Classification of Substances Hazardous to Waters. Jerman: FEA.
Huet HBN. 1970. Water Quality Criteria for
Fish Life Biological Problems in Water Pollution. PHS. Publ. No. 999-WP-25.
[KLH] Kementrian Lingkungan Hidup. 2004. Keputusan Menteri Negara Lingkungan Hidup No. 51 Tahun 2004 Tentang Baku Mutu Air Laut. 2004.
[JIS] Japanese Industrial Standards. 2005.
Biodegradation Test of Chemical Substances. http://www.met.go.jp [10 Jul
2005].
Loonen H, Lindgren F, Hansen B, Karcher W, Niemelä J, Hiromatsu K, Takatsuki M, Peijnenburg W, Rorije E, Struijś J. 2006. Prediction of biodegradibility from chemical structure: Modeling of ready