Bab 4 Kesetimbangan Kimia
Teks penuh
Gambar

Garis besar
Dokumen terkait
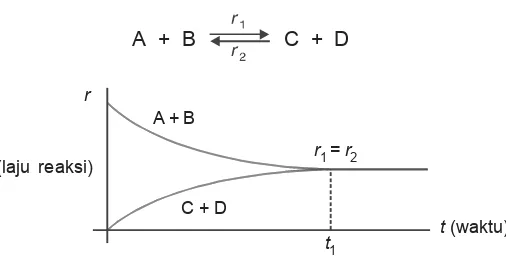
Zat-zat yang bereaksi (pereaksi) terletak di sebelah kiri tanda panah, sedangkan zat-zat hasil reaksi (produk) terletak di sebelah kanan tanda panah. Sesuai dengan hukum
Reaksi Reversible (reaksi dapat balik), yaitu reaksi yang berlangsung dua arah dimana zat hasil raksi (produk) dapat Reaksi Reversible (reaksi dapat balik),
Untuk reaksi heterogen, yakni reaksi yang melibatkan zat-zat pereaksi dengan wujud berbeda, laju reaksi dipengaruhi oleh permukaan sentuh.Semakin besar luas
rubahan katalis pada campuran reaksi yang tidak berada pada kesetimbangan akan empercepat laju reaksi maju dan reaksi balik, sehingga campuran kesetimbangan rcapai lebih cepat..
•Perubahan konsentrasi tidak akan merubah nilai tetapan kesetimbangan pada temperatur yang tetap •Jika suatu zat ditambahkan ke dalam sistem yang setimbang, kesetimbangan
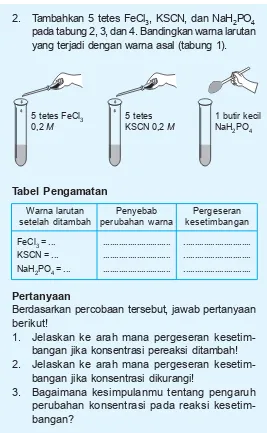
Ketika suatu reaksi kimia berlangsung, maka akan terjadi perubahan komposisi dan terbentuk zat baru yang mungkin memiliki warna yang berbeda.. Contoh reaksi kimia
zat-zat pereaksi pada kolom Reactants > Input zat-zat hasil reaksi pada kolom Products > Klik Balance > (Reaksi Setara) Untuk persamaan reaksi kimia yang melibatkan
Menurut asas Le Chatelier, agar diperoleh gas SO3 yang optimum, reaksi dilakukan pada temperatur rendah (pada temperatur rendah, kesetimbangan akan bergeser ke arah eksoterm).