BAB II
TINJAUAN PUSTAKA 2.1 Sirosis Hati
2.1.1 Definisi
Sirosis hati adalah suatu keadaan patologis yang menggambarkan stadium akhir fibrosis hati yang berlangsung progresif yang ditandai dengan distorsi arsitektur hati dan pembentukan nodulus regeneratif.Gambaran ini terjadi akibat nekrosis hepatoselular. Jaringan-jaringan retikulin kolaps disertai deposit jaringan ikat, distorsi jaringan vaskular dan regenerasi nodularis parenkim hati (Heidelbaugh J 2006, Nurdjanah S 2009)
2.1.2 Epidemiologi
Di negara maju, sirosis hati merupakan penyebab kematian terbesar ketiga setelah penyakit kardiovaskular dan kanker.Di seluruh dunia sirosis menempati urutan ketujuh penyebab kematian.Sirosis hati merupakan penyakit hati yang paling banyak ditemukan dalam ruang perawatan bagian penyakit dalam (Cheney CP 2004, Sutadi SM, 2003).Di Amerika serikat, sirosis hati menyebabkan 25000 kematian per tahun (Choudury J 2006). Sebagai akibat adanya epidemi hepatitis C, diperkirakan pada tahun 2020 proporsi pasien sirosis hati akibat hepatitis C akan berlipat ganda dari 16% menjadi 32% (Herrera JL 2008).
Di Indonesia data prevalensi sirosis hati belum ada, hanya laporan dari beberapa pusat pendidikan saja.Di RS dr Sardjito Yogyakarta jumlah pasien sirosis hati berkisar 4.1% dari pasien yang dirawat di bagian penyakit dalam dalam kurun waktu 1 tahun (2004). Di Medan, dalam kurun waktu 4 tahun dijumpai pasien sirosis hati sebanyak 819 (4%) pasien dari seluruh pasien di bagian penyakit dalam. (Nurdjanah S 2009)
2.1.3 Klasifikasi dan Etiologi
Tabel 2.1 Penyebab utama sirosis hati (idikutip darBataller 2008)
Main causes of cirrhosis Viral diseases
Hepatitis B (with or without hep. D) and Hepatitis C
Autoimmune diseases
Autoimmune hepatitis Primary biliary cirrhosis
Hepatotoxic agents
Alcohol abuse
Drugs : methotrexate, α-methyldopa,amiodarone,other
Acquired metabolic disease
Non-alcoholic fatty liver disease and steatohepatitis
Vascular diseases
Chronic right-sided heart failure
Budd-chiari syndrome (hepatic vein thrombosis)
Genetic diseases
Wilson disease Hemochromatosis
Type-IV glycogen storage disease Tyrosinemia
α1-antitripsin deficiency
Miscellaneous
2.1.4 GEJALA KLINIS
Stadium awal sirosis sering tanpa gejala sehingga kadang ditemukan pada waktu pasien melakukan pemeriksaan kesehatan rutin atau karena penyakit lain.gejala awal sirosis (kompensata) meliputi perasaan mudah lelah dan lemas, selera makan berkurang,perasaan perut kembung, mual, berat badan menurun, pada laki-laki dapat timbul impotensi, testis mengecil, buah dada membesar, hilangnya dorongan seksualitas. Bila sudah lanjut (dekompensata), gejala-gejala lebih menonjol teutama bila timbul komplikasi kegagalan hati dan hipertensi porta, meliputi hilangnya rambut badan, gangguan tidur, dan demam yang tidak begitu tinggi. Mungkin disertai adanya gangguan pembekuan darah, perdarahan gusi, epistaksis, gangguan siklus haid, ikterus dengan air kemih berwarna seperti teh pekat, muntah darah dan/atau melena, serta perubahan mental, meliputi mudah lupa, sukar konsentrasi, bingung, agitasi sampai koma (Bissel D 1996, Erlingen S 1999,Nurdjanah S 2009).
Pada sirosis hati, terdapat dua gejala klinis utama yang dapat ditemukan, yaitu kegagalan fungsi hati dan hipertensi portal (Erlingen S 1999, Sutadi SM 2003, Choudury J 2006) :
a. edema b. ikterus c. koma d. spider nevi
e. alopesia pectoralis f. ginekomastia g. kerusakan hati h. asites
i. rambut pubis rontok j. eritema palmaris k. atropi testi
l. kelainan darah (anemia,hematon/mudah terjadi perdarahan)
2. Hipertensi portal, dengan manifestasi klinis berupa : a. varises oesophagus
b. splenomegali
c. gastropati hipertensi portal d. perubahan sum-sum tulang e. caput meduse
f. asites
g. collateral veinhemorrhoid
h. kelainan sel darah tepi (anemia, leukopeni dan trombositopeni)
Tabel 2.2 Manifestasi klinis dan laboratorium pada sirosis hati (dikutip dari Choudury 2006)
2.1.5 Patogenesis
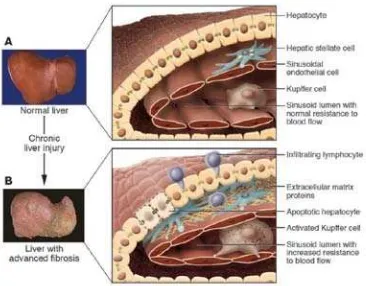
Pada kondisi normal, hati merupakan sistem filtrasi darah yang menerima darah dari vena mesenterika, lambung, limfe, dan pankreas masuk melalui arteri hepatika dan vena porta.Darah masuk ke hati melalui triad porta yang terdiri dari cabang vena porta, arteri hepatika, dan saluran empedu, kemudian masuk kedalam ruang sinusoid lobulus hati. Darah yang sudah difilter masuk ke dalam vena sentral kemudian masuk ke dalam vena hepatik yang lebih besar menuju ke vena cava inferior (Heidelbaugh 2006, Herrera 2008, Sofwanhadi R 2007).
adalah memfagosit sel hepatosit tua, debris sel, benda asing, sel tumor dan berbagai mikroorganisme (Bataller 2005).
Transformasi sel normal menjadi sel yang fibrotik merupakan proses yang sangat rumit. Terdapat interaksi antara HSC dengan sel-sel parenkimal, sitokin,
growth factor, berbagai protease matriks beserta inhibitornya dan MES.
.
Faktor-faktor yang berperan dalam terjadinya fibrosis hati antara lain : 1. Cedera hati
2. Inflamasi yang ditandai oleh
a. Infiltrasi dan aktivasi dari berbagai sel seperti : netrofil, limfosit, trombosit dan sel-sel endotelial, termasuk sel kupffer.
b. Pelepasan berbagai mediator, sitokin, growth factor, proteinase berikut inhibitornya dan beberapa jenis substansi toksik seperti reactive oxygen spesies (ROS) dan peroksida lipid.
3. Aktivasi dan migrasi sel HSC ke daerah yang mengalami cedera. 4.Perubahan jumlah dan komposisi MES akibat pengaruh HSC serta pengaruh berbagai sel, mediator dan growth factor.
5. Inaktivasi HSC, apoptosis serta hambatan apoptosis oleh berbagai komponen yang terlibat dalam perubahan MES.
Fibrosis hati adalah terbentuknya jaringan ikat yang terjadi sebagai respon terhadap cedera hati, diawali oleh cedera hati kronis yang dapat disebabkan oleh infeksi virus, ketergantungan alkohol, nonalkoholik steatohepatitis dan penyebab lainnya.
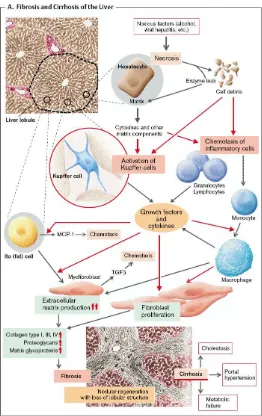
Terjadinya fibrosis pada hati dapat melalui beberapa tahap. Saat sel hepatosit yang rusak mati, maka enzim lisosom akan bocor dan mengeluarkan sitokin dari matriks ekstrasel hati (Silbernagl S 2000). Sitokin dan debris-debris sel yang mati akan mengaktifkan sel Kupffer di sinusoid hati dan menarik sel-sel inflamasi ( granulosit, limfosit dan monosit). Sebagai akibatnya akan terbentuk growth factor dan sitokin-sitokin yang akan mengubah monosit menjadi makrofag aktif dan memicu proliferasi fibroblas.
Aksi kemotaktik dari transforming growth factor β (TGF-β) dan monocyte chemotactic protein 1 (MCP-1) akan memperkuat proses di atas. Sebagai akibat berbagai interaksi kimiawi kompleks yang belum sepenuhnya difahami, produksi matriks ekstraselular akan ditingkatkan oleh myofibroblas dan fibroblas, sehingga akan menyebabkan terjadinya penumpukan kolagen, proteoglikan, dan glikoprotein. Penumpukan ini menyebabkan terjadinya fibrosis hati, yang akan menggganggu aliran darah di hati dan meningkatkan tahanan aliran darah di sinusoid.
Gambar 2.2 Patogenesis fibrosis dan sirosis hati (Silbernagl S 2000)
2.2 HIPERTENSI PORTAL
Hipertensi portal adalah peninggian tekanan dari sistem porta, dapat dakibatkan oleh penyebab sirotik atau non-sirotik. Pada awal diagnosa sirosis hati, hipertensi portal terdapat pada 60% pasien sirosis dekompensata dan pada 40% pasien sirosis kompensata. Sirosis hati adalah penyebab paling banyak dari hipertensi portal, dan mencakup 95% dari selurush kasus hipertensi portal yang ditemui di klinik (Choudury J 2006).
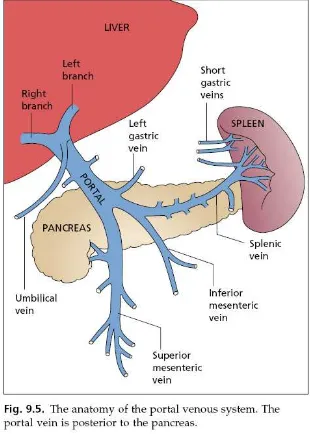
bercampur dengan darah dari arteri hepatik yang kaya oksigen, dan akan mengalami kontak dengan hepatosit. Sistem porta adalah semua sistem vena yang mengalirkan darah menuju hati yang berasal dari saluran cerna di rongga abdomen, limpa, dan kandung empedu. Vena porta masuk ke hati melalui porta hepatic, yang membagi menjadi dua bagian yang masing-masing membagi menuju tiap lobus. Vena porta merupakan penyatuan dari vena mesenterika superior dan lienalis.Vena porta terletak di anterior kaput pankreas setinggi vertebra lumbal 2, sedikit sebalah kanan garis tengah.Di dalam hati vena porta membentuk cabang yang mengaliri hati yang berjalan seiring dengan arteri hepatica.Vena mesenterika superior merupakan muara dari aliran darah vena yang berasal dari intestinal, kolon dan kaput pankreas dan kadang dari lambung melalui vena gastroepiploika kanan.Sedangkan vena lienalis merupakan muara 5-15 cabang dari vena di hilus limpa dan dari beberapa vena gastrika breves yang bermuara di sepanjang vena lienalis yang terletak di ekor dan badan pankreas.Vena menampung darah dari kaput pankreas dan vena gastroepiploika kiri yang bermuara di dekat limpa, dan darah dari mesenterika inferior yang berasal dari kolon kiri dan rectum. Kecepatan aliran vena porta mencapai 1000-1200 ml/menit dan memasok 72% kebutuhan oksigen total.
Peningkatan tekanan porta dapat terjadi akibat beberapa hal berikut : 1. Prehepatik : portal vein thrombosis
2. Posthepatic : gagal jantung kanan, perikarditis konstriktif, dll 3. Intrahepatik :
a. Presinusoid : hepatitis kronik, primary biliary cirrhosis, granuloma in schistosomiasis, tuberculosis, leukemia, dll
b. Sinusoidal : hepatitis akut, kerusakan akibat alkohol ( fatty liver, sirosis), toksin, amiloidosis, dll
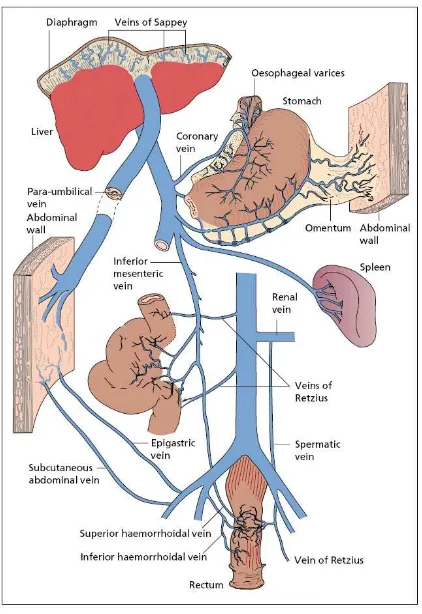
c. Postsinusoid : venous occlusive disease of the venules and small veins, Budd-chiari syndrome (obstruksi vena hati yang besar) Apabila terdapat sumbatan aliran pada sistem portal, baik sumbatan intra maupun ekstrahepatik maka akan tampak sirkulasi kolateral, sebagai upaya konsekunsi mengalihkan aliran porta ke dalam vena hepatika.
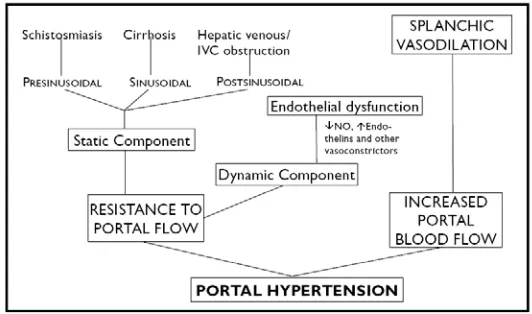
Tekanan vena porta berbanding lurus dengan jumlah aliran darah vena yang masuk dan tahanan aliran darah yang keluar dari sistem vena porta.Pada sirosis, hipertensi portal terjadi karena adanya peningkatan tahanan aliran darah pada sinusoid hati . Hal ini terjadi karena gabungan komponen statik ( akibat gangguan arsitektur hati dan fibrosis) dan komponen dinamik (akibat konstriksi sinusoid hati).
Gambar 5.Patofisiologi hipertensi portal (Choudury J 2006)
2.2. 1 Pengukuran tekanan porta
Tekanan porta dapat diukur secara langsung maupun tidak langsung.Pengukuran tekanan porta secara langsung adalah metode invasif yang jarang digunakan (Pomier-Layrargues G 2005).Metode yang paling sering digunakan untuk mengukur tekanan porta adalah dengan menentukan hepatic vein pressure gradient (HVPG), yang merupakan metode tidak langsung.
Gambar 2.6Pengukuran HVPG (dikutip dari Pomier-Layrargues 2005)
Metode tidak langsung lain yang dapat digunakan untuk mengukur tekanan porta adalah dengan splenoportografi, di mana dilakukan penusukan ke limpa secara transkutaneus dengan menggunakan needle catheter, kemudian dilakukan pengukuran tekanan intralimpa.Tekanan intralimpa ini hampir identik dengan tekanan vena porta.Tetapi, teknik ini memiliki resiko perdarahan limpa dan teknik ini sekarang tidak lagi digunakan untuk manusia, namun masih digunakan untuk hewan percobaan.
Pengukuran tekanan vena porta secara langsung jarang dilakukan karena kurang aman.Menentukan tekanan vena porta secara langsung dapat dilakukan secara percutaneous transhepatic cathetherization, secara transhepatic
pada pasien hipertensi portal intrahepatic presinusoid , misalnya idiopathic portal
hypertension, di mana HVPG mungkin normal.
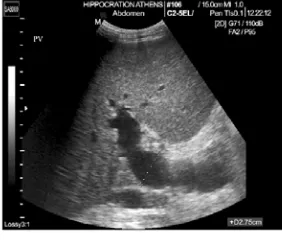
Selain mengukur tekanan vena porta, penilaian adanya hipertensi portal juga dapat dilakukan dengan menggunakan ultrasonografi. Pada USG, dapat ditemukan pelebaran vena portal, asites atau splenomegali.Diameter vena porta yang normal biasanya tidak melebihi 13 mm pada kondisi istirahat dan bernapas biasa.Pada hipertensi portal, diameter vena porta meningkat sehingga vena porta terlihat mengalami dilatasi (Bates JA 2004).Dengan USG doppler, ditemukan berkurangnya pulsatilitas pada vena hepatik dan menyempitnya vena hepatika. Baik et al (2006) menunjukkan bahwa monophasic hepatic venous flow memiliki hubungan dengan hipertensi portal berat (HVPG>15mmHg)
Gambar 2.7 Contoh USG yang menunjukkan dilatasi vena porta (2.75cm)pada pasien dengan hipertensi portal (dikutip dari Cokkinos D 2009)
Beberapa tahun belakangan, transient elastography (Fibroscan) semakin meningkat penggunaannya sebagai alat non-invasif untuk menilai derajat fibrosis hati. Beberapa studi telah meneliti hubungan fibroscan dengan hipertensi portal, di mana ditemukan bahwa fibroscan dapat secara tidak langsung memprediksi adanya hipertensi portal (Sporea I 2011) . Bureau C (2008) menilai korelasi antara HVPG dan derajat fibrosis hati menggunakan fibroscan untuk mendiagnosa hipertensi portal pada 150 pasien, di mana ditemukan cut-off point 21 kPA dapat memprediksi secara akurat keberadaan hipertensi portal pada 92% pasien.
2.3 GASTROPATI HIPERTENSI PORTAL (GHP) Definisi
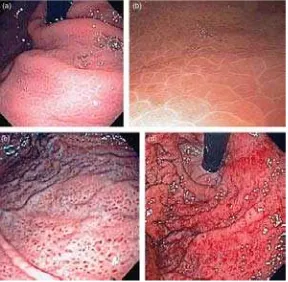
diistilahkan dengan snake-skin appearance) dengan atau tanpa red spots, pada pasien dengan hipertensi portal sirotik atau nonsirotik
Gambar 2.8 Tampilan endoskopik GHP (dikutip dari Cubillas 2010)
2.3.2 Diagnosis dan klasifikasi
Belum ada konsensus umum yang menyepakati klasifikasi endoskopis GHP. Yang paling banyak dipakai adalah klasifikasi McCormack, karena memiliki kesesuaian intra- dan inter-observer yang relatif lebih tinggi. Gold standard untuk diagnosis GHP adalah secara endoskopi (Kim MY 2010, Cubillas 2010).
Tabel 2.3. Klasifikasi GHP (dikutip dari Thuluvath PJ 2002)
McCormack et al Tanoue et al NIEC
Mild
Fine pink speckling
(scarlatina-type rash) Superficial reddening Mosaic pattern
Diffuse hemorrhagic lesion
Grade II
Severe redness and a fine
reticular pattern separating the areas of raised edematous
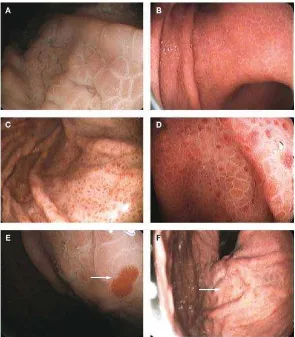
Sejak pertama dideskripsikan oleh McCormack (1985), spektrum lesi pada lambung yang konsisten dengan GHP mencakup : mosaic like-pattern, red point
Gambar 2.9 Gambaran endoskopi yang menunjukkan karakteristik utama GHP (dikutip dari Perini RF 2009)
Tabel 2.4 Karakteristik temuan endoskopis pada GHP (dikutip dari Perini RF 2009)
Biopsi pada GHP jarang dilakukan, dan pada biopsi ditemukan gambaran dilatasi pembuluh kapiler dan irregularitas vena pada mukosa dan submukosa lambung, tanpa adanya infiltrat sel inflamasi atau erosi mukosa lambung (Eleftheriadis E 2001). Studi Curvelo LA (2009) membandingkan metode diagnosis GHP secara endoskopi dan secara biopsi, dan menemukan bahwa pada kedua metode ditemukan prevalensi GHP yang cukup tinggi: 93.4% (endoskopi) dan 76.1% (biopsi).
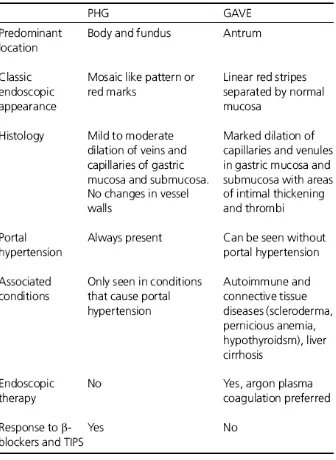
Tabel 2.5 Perbandingan antara GHP dengan GAVE
Beberapa kondisi lain juga dapat menjadi differensial diagnosis GHP. Gastritis akut (akibat obat-obatan NSAID) juga dapat memiliki gambaran endoskopis mosaic-like pattern, tetapi ciri utamanya adalah terdapatnya banyak infiltrat sel-sel inflamasi, pembuluh darah tidak berdilatasi dan hanya mengenai mukosa. Polisitemia, gastric purpura dan penyakit Osler Weber Randu juga dapat menyerupai GHP namun sangat jarang ditemukan.
2.3.3 Prevalensi
Beberapa studi melaporkan prevalensi severe GHP berkisar 9% - 46% dan
mild GHP berkisar 29% - 67%.Prevalensi GHP secara keseluruhan adalah sekitar
51%-98%.(Thuluvath 2002, Merli M 2004) Besarnya variasi GHP yang ditemukan pada berbagai studi sebelumnya kemungkinan berhubungan dengan perbedaan dalam pemilihan pasien, tidak dipakainya kriteria dan klasifikasi yang seragam dan adanya perbedaan antar- dan intra-pengamatdalam menilai lesi yang ditemukan pada endoskopi (Sarin SK 2000, LO G 2009).
dapat ditemukan pada pasien sirosis dengan varises esofagus atau varises lambung, namun korelasi langsung antara GHP dengan hipertensi portal masih kontroversial. Sedikit sekali yang diketahui mengenai hubungan antara GHP dengan prognosis pada pasien-pasien sirosis hati.
2.3.4 Patogenesis GHP
Patogenesis GHP kompleks dan memiliki banyak kontroversi.Berbagai faktor seperti aliran darah sphlanknikus, faktor humoral, gangguan lokal pada tonus pembuluh darah, dan tekanan portal telah diteliti untuk mengetahui mekanisme yang mendasari GHP.GHP diyakini sebagai kelainan vaskuler, dan berhubungan erat dengan gangguan aliran darah splanknikus. Walaupun demikian, perfusi mukosa lambung yang dideteksi dengan Doppler laser menunjukkan hasil yang berfluktuasi .Diusulkan bahwa GHP timbul karena kongesti yang diakibatkan oleh hambatan drainase darah lambung.Perubahan mukosa lambung juga dapat diakibatkan oleh peningkatan permeabilitas pembuluh darah mikro lambung yang disebabkan oleh endothelin 1, keterlibatan prostaglandin dan kelebihan nitrit oxide synthase.GHP tidak berkaitan dengan infeksi H pylori.GHP jarang terbentuk pada pasien yang memiliki varises fundus, mungkin karena adanya aliran darah kolateral yang lebih banyak (Simanjuntak LJ 2004).
Kontroversi juga terdapat pada beberapa penelitian tentang aliran darah pada mukosa lambung.Kebanyakan penelitian melaporkan adanya penurunan aliran darah mukosa lambung karena kongesti, namun ada juga beberapa penelitian melaporkan terdapatnya peningkatan aliran darah mukosa lambung pada GHP.Penelitian eksperimental oleh Imanishi menggunakan tikus sebagai model hewan menunjukkan bahwa perubahan hemodinamik karena GHP dapat menyebabkan penipisan lapisan mukus pada mukosa lambung (Eleftheriadis E 2001, Chapman RW 2007).
Sekresi asam lambung berkurang karena kerusakan terhadap ‘gastric mucosal barrier’ yang akan menyebabkan perubahan hemodinamik lokal, sehinga terjadi kongesti dan hiperemi mukosa lambung. Faktor humoral berperan dalam GHP dengan menurunkan fungsi metabolik mukosa, menurunkan respons terhadap pentagastrin, menurunkan glikoprotein mukosa, menurunkan kadar prostaglandin E2 (PGE2) dan meningkatkan sintesis nitrit oxide (NO). seluruh hal tersebut akan menurunkan asam lambung luminal dan menyebabkan penurunan respons faktor-faktor defensive terhadap stimulasi intraluminal seperti diffuse ion H, asam empedu dan penggunaan NSAID (Simanjuntak LJ 2004, Shah VH 2010).
Gambar 2.10 Patogenesis terjadinya GHP (dikutip dari Simanjuntak LJ,2004)
2.3.5 Manifestasi Klinis
severe GHP dibandingkan mild GHP. Penelitian Sarin et al (2000) melaporkan bahwa perdarahan akibat GHP terjadi pada 10 dari 86 penderita GHP (11.6%) yang dipantau selama 25 bulan. Pada studi lain, ditemukan bahwa pada pasien penyakit hati kronis, GHP dapat menyebabkan perdarahan pada 4% dari seluruh kasus perdarahan akut dan 8% dari kasus perdarahan nonvarises (Cubillas 2010).
Perdarahan mukosa lambung kronis dan anemia defisiensi besi yang berulang yang terkadang sampai membutuhkan transfusi darah adalah manifestasi klinis yang paling sering dijumpai pada penderita GHP.Perdarahan akibat GHP dapat menyebabkan kematian, tetapi GHP tidak merupakan faktor resiko independen terhadap survival pasien sirosis hati.Walaupun begitu, episode perdarahan berulang akibat GHP dapat memberikan kontribusi terhadap perburukan fungsi hati (Eleftheriadis 2001).
2.3.6 Progresi/Regresi GHP
Pada kebanyakan kasus (30-60%), kondisi GHP dijumpai tetap stabil.Namun demikian, pada beberapa kasus GHP dapat bersifat fluktuatif, di mana hal ini menunjukkan GHP merupakan suatu penyakit yang bersifat dinamis. Beberapa laporan menyatakan bahwa GHP dapat berprogresi dari mild menjadi severe pada 30% kasus, dan GHP dapat juga mengalami regresi atau bahkan menghilang pada 20% kasus (Cubillas 2010). Ligasi varises esofagus memiliki hubungan dengan progresifitas perburukan GHP yang lebih cepat, tetapi perburuan ini biasanya bersifat sementara dan dapat mengalami regresi kembali pada 44% kasus setelah ligasi varises esofagus. Studi lain menemukan bahwa hanya skor Child-Pugh yang tinggi yang memiliki hubungan dengan progresivitas GHP.
2.3.7 Penatalaksanaan dan Pencegahan GHP
portal dan aliran darah lambung.Kebanyakan pasien memuai terapi propanolol dengan dosis 20 mg dua kali sehari kemudian dosis ditingkatkan secara bertahap dengan mempertahankan denyut jantung sekitar 50-55 x/menit.Penelitian Hosking S (1987) mengevaluasi 14 pasien severe GHP yang mengalami perdarahan gastrointestinal akut dan diberikan terapi propanolol, di mana perdarahan berhenti pada 93% pasien setelah 3 hari. Ocreotide, suatu somatostatin analog (dosis 100 µg bolus dilanjutkan dengan infus 25µg/jam selama 48 jam) dilaporkan memiliki efektivitas yang tinggi (100%) untuk mengatasi perdarahan akut akibat GHP. Jika diberikan sendiri-sendiri, vasoperessin memiliki efektivitas 64% sedangkan omeprazole 59% untu mengendalikan perdarahan, tetapi jika vasopressin dan omeprazole diberikan bersama-sama, efektivitasnya adalah 88%. Belum ada penelitian yang membandingkan antara penghambat beta dengan ocreotide.
Tindakan endoskopi memiliki peranan kecil dalam penatalaksanaanperdarahan akibat GHP, karena perdarahan biasanya bersifat difus. Anti oksidan mungkin memiliki peran dalam penatalaksanaan GHP, di mana pada suatu penelitian eksperimental terhadap tikus, pemberian vitamin E oral dapat memperbaiki keadaan mukosa lambung. Transjugular intrahepatic portosystemic shunt (TIPS) dan terapi bedah (shunt surgery) tidak rutin dilakukan karena bersifat invasif namun dapat mengurangi keparahan derajat GHP.
Resiko perdarahan pada mild GHP adalah rendah, karena itu pada umumnya tidak memerlukan profilaksis primer.Namun pada pasien dengan mild GHP dan juga varises esofagus, sebaiknya diberikan propanolol sebagai profilaksis pencegahan perdarahan.Pada pasien dengan severe GHP, sebaiknya juga diberikan penghambat beta non selektif sebagai profilaksis perdarahan.
2.4 SKOR CHILD PUGH
Skor Child yang pertama, skor Child-Turcotte, melibatkan 5 variabel (bilirubin, albumin, asites, ensefalopati, dan status nutrisi) dikategorikan menjadi 3 grup dengan tingkatan keparahan penyakit (Guha 2007).
Tabel 2.7 Skor Child-Turcotte (dikutip dari Guha,2007)
A B C
Bilirubin serum (mg/dl)
<2 2-3 >3
Albumin serum (gr/dl) >3.5 3-3.5 <3
Asites - Mudah dikontrol Sulit dikontrol
Gangguan neurologi - Minimal Berat,koma
Nutrisi Sangat baik baik buruk
Skor Turcotte dimodifikasi 10 tahun kemudian dengan skor Child-Pugh dengan menggantikan status nutrisi dengan waktu protrombin atau INR dan juga nilai terendah almbumin dari 3 menjadi 2.8 gr/dl (Durand et al 2005). Variabel dari Child Pugh menggambarkan fungsi hati dalam hal sintesis (albumin dan protrombin) dan ekskresi (bilirubin).
Tabel 2.8 Skor Child-Pugh (Choudury 2006) Parameter Nilai
Ensefalopati - Derajat I-II Derajat III-IV
Child A skor 5-6; Child B skor 7-9; Child C skor 10-15
Harapan hidup 2 tahun : Child A (85%). Child B (60%), Child C (35%)
Keterbatasan pertama dari skor Child Pugh berhubungan dengan fakta bahwa 5 komponen dasar dari skor Child-Pugh telah dipilih secara empirik. Variabel-variabelnya tidak semua memiliki pengaruh independen, seperti albumin dan faktor koagulasi keduanya disintesis di hati dan keduanya saling berhubungan dengan kuat. Keterbatasan kedua mengenai nilai ambang batas dari variabel kuantitas yang belum ada bukti batasan tersebut berhubungan dengan mortalitas. Keterbatasan ketiga adalah karena pada kenyataannya faktor prognostik yang penting tidak diperhitungkan seperti adanya keterlibatan fungsi ginjal dan hipertensi portal. Terakhir Child Pugh tidak memperhitungkan penyebab sirosis, kemungkinan koeksistensi beberapa faktor dan proses kerusakan yang menetap seperti penyalahgunaan alkohol, replikasi virus hepatitis B atau C yang sedang berlangsung atau aktivitas peradangan dari hepatitis autoimun. Namun walaupun dengan berbagai keterbatasan seperti itu, skor Child Pugh masih merupakan prediktor prognosis yang kuat (Durand 2005).
2.5 Hubungan GHP dengan Sirosis Hati
Peningkatan tekanan portal dan disfungsi hati adalah penting dalam menyebabkan terjadinya GHP pada pasien sirosis hatiWalaupun hipertensi porta berperan penting dalam patogenesis GHP, tetapi peningkatan tekanan porta bukan merupakan satu-satunya faktor yang menentukan terjadinya GHP (Eleftheriadis 2010). Penelitian Sarin et al (1992) menyatakan bahwa tidak semua penderita hipertensi portal akan mangalami GHP.
Selain hipertensi portal, ada faktor-faktor lain yang berkontribusi terhadap pembentukan GHP.Terdapat beberapa bukti bahwa GHP terjadi jauh lebih sering pada pasien sirosis hati daripada non-sirosis hati (Toyonaga 1998).Tidak ada konsensus yang menyepakati hubungan antara hubungan fungsi hati pada pasien sirosis dengan GHP, namun beberapa penelitian terbaru menunjukkan bahwa insidens dan perkembangan GHP memiliki hubungan dengan fungsi hati.
keparahan GHP. Ahmed S (2010) meneliti 360 pasien sirosis hati dan mendapatkan skor Child, skor MELD, platelet/spleen ratio dan adanya varises esofagus merupakan faktor independen pada pasien dengan severe GHP, dan dapat digunakan untuk memprediksi terjadinya severe GHP. Namun pada penelitian Nashaat E (2010), ditemukan bahwa skor Child Pugh memiliki korelasi positif dengan terjadinya varises esofagus, tetapi tidak dengan GHP. Di sisi lain, Ehab et al (2010) menunjukkan bahwa prevalensi GHP meningkat sesuai dengan derajat keparahan penyakit hati, di mana 90% pasien-pasien sirosis hati dengan skor Child Pugh C dan memiliki GHP akan meninggal dalam waktu 12 bulan.