BAB 2
TINJAUAN PUSTAKA
2.1. TUMBUHAN KETAPANG (Terminalia catappa L) 2.1.1. Klasifikasi Tumbuhan Jamblang
Berdasarkan taksonomi, klasifikasi daun ketapang, hasil identifikasi tumbuhan ketapang dilaboratorium Herbarium Medanense (MEDA) Universitas Sumatera Utara adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta
Class : Dicotyledoneae
Ordo : Myrtales
Family : Combretaceae
Genus : Terminalia
Spesies : Terminalia catappa L.
Nama Lokal : Ketapang (Herbarium Medanense, 2016)
2.1.2. Morfologi Tumbuhan Ketapang
Tumbuhan ketapang (Terminalia catappa L ) merupakan tanaman asli dari Asia Tenggara yang sangat banyak tumbuh di Indonesia. Pohon Ketapang dapat tumbuh pada dataran rendah maupun dataran tinggi, di hutan primer maupun sekunder, di sepanjang sungai ataupun di daerah tepi pantai, dengan ketinggian mencapai 25 m dan diameter batang sampai 1,5 m yang tumbuh subur di daerah tropis dan subtropis.
Lemmens dan Soetjipto (1999), mendiskripsikan Tanaman Ketapang (T cattapa L. ) yaitu batangnya memiliki cabang panjang dan mendatar. Daunnya berbentuk bundar telur atau menjorong. Bunga dengan ukuran kecil, berwarna putih dan tidak bermahkota. Buah berbentuk bulat telur, waktu muda berwarna hijau dan setelah matang berwarna merah.
2.1.3.Manfaat Tumbuhan Ketapang
Pohon ketapang tidak hanya digunakan sebagai pohon peneduh melainkan memiliki banyak manfaat lain terutama pada bagian daunnya. Tanaman ketapang sering digunakan untuk ramuan tradisional. Diantaranya dapat dipergunakan untuk mengobati diare, gangguan usus , hipertensi, rematik sendi , disentri, lepra, kudis dan penyakit kulit lainnya. Bagian tumbuhan ketapang khususnya daun selain untuk obat kulit, dapat dimanfaatkan juga untuk menurunkan pH air tawar dan menyerap zat - zat kimia yang terdapat pada air tawar tersebut.
kulit batang hanya mengandung flavonoid dan saponin, pada buah hanya tanin dan steroid ( Ugwu, et al 2015)
Daun ketapang dapat digunakan sebagai antijamur dan antibakteri karena senyawa-senyawa kimia yang terkandung dalam daun ketapang tersebut merupakan senyawa yang dapat menghambat pertumbuhan maupun mematikan bakteri pathogen.
2.2. Metabolit Sekunder
Metabolit sekunder merupakan sekelompok senyawa kimia yang dijumpai diseluruh tanaman dan memiliki cirri khas untuk setiap tanaman tertentu (Manito, 1981). Senyawa metabolit sekunder umumnya mempunyai kemampuan bioaktifitas dan berfungsi sebagai pelindung tumbuhan tersebut dari gangguan hama penyakit untuk tumbuhan itu sendiri dan lingkungannya. Secara umum metabolit sekunder dalam bahan hayati dikelompokkan berdasarkan sifat dan reaksi khas suatu metabolit sekunder dengan pereaksi tertentu. Metabolit sekunder dapat dikelompokkan sebagai alkaloida, terpenoida, flavonoida, tanin, saponin dan glikosida (Harbone, 1987) Senyawa-senyawa inilah yang digunakan oleh manusia sebagai obat. Metabolisme tersebut tidak digunakan bagi pertumbuhan tanaman, akan tetapi salah satu fungsinya yaitu sebagai pertahanan terhadap mikroorganisme patogen dan juga terhadap herbivora maupun omnivora (Heldt, 1997).
Sifat-sifat utama senyawa sekunder pada tumbuhan adalah merupakan hasil proses yang kompleks dan diatur dalam jaringan tertentu pada tingkatan perkembangan tertentu.
1. Produknya dapat berbeda antar spesies, bahkan diantara organ yang berbeda
2. Sangat spesifik
2.2.1 Alkaloid
Alkaloida adalah suatu golongan senyawa organik yang terbanyak ditemukan dialam. Hampir seluruh senyawa alkaloida berasal dari tumbuh-tumbuhan dan tersebar luas dalam berbagai jenis tumbuhan. Senyawa alkaloida mengandung paling sedikit satu atom nitrogen yang biasanya bersifat basa dan dalam sebagian besar atom nitrogen ini merupakan bagian dari cincin heterosiklik. Kebanyakan alkaloid yang telah diisolasi berupa padatan Kristal dengan titik lebur yang tertentu atau mempunyai kisaran dekomposisi. Sedikit alkaloid yang berbentuk amorf dan beberapa seperti nikotin dan koniin berupa cairan. Kebanyakan alkaloid berwarna
tetapi beberapa senyawa yang kompleks, spesies aromatik berwarna ( Sastrohamidjojo, 1996).
2.2.2 Flavonoid
Senyawa flavonoid sebenarnya terdapat pada semua bagian tumbuhan termasuk daun, akar, kayu, kulit, tepung sari, bunga, buah, dan biji. Kebanyakan flavonoid ini berada didalam tumbuh-tumbuhan, kecuali alga. Namun ada juga flavonoid yang terdapat pada hewan, misalnya dalam kelenjar bau berang-berang dan sekresi lebah. Dalam sayap kupu-kupu dengan anggapan bahwa flavonoid berasal dari tumbuh-tumbuhan yang menjadi makanan hewan tersebut dan tidak dibiosintesis didalam tubuh mereka. Penyebaran jenis flavonoid pada golongan tumbuhan yang tersebar yaitu angiospermae, klorofita, fungi, briofita (Markham,1988).
Senyawa-senyawa flavonoid adalah senyawa-senyawa polifenol yang mempunyai 15 atom karbon, terdiridari dua cincin benzene yang dihubungkan menjadi satu oleh rantai linier yang terdiri dari tiga atom karbon. Senyawa-senyawa flavonoid adalah senyawa 1,3 diaril propane, senyawa isoflavonoid adalah senyawa 1,2 diaril propane, sedangkan senyawa-senyawa neoflavonoid adalah 1,1 diaril propane.
2.2.3 Tanin
Tanin merupakan senyawa kompleks biasanya campuran polifenol tidak mengkristal (tannin extracts). Tanin membentuk warna kehitaman dengan beberapa ion logam misalnya ion besi, kalsium, tembaga dan magnesium. Senyawa tanin tidak larut dalam pelarut non polar seperti eter, kloroform dan benzene tetapi mudah larut dalam air, dioksan aseton dan alkohol serta sedikit larut dalam etil asetat.
Secara struktural tanin adalah suatu senyawa fenol yang memiliki berat molekul besar yang terdiri dari gugus hidroksi dan beberapa gugus yang bersangkutan seperti karboksil untuk membentuk kompleks kuat yang efektif dengan protein dan beberapa makromolekul (Horvart, 1981). Tanin ditemukan hampir di setiap bagian dari tanaman; kulit kayu, daun, buah, dan akar (Hagerman et.al., 1998).
Tanin dibentuk dengan kondensasi turunan flavon yang ditransportasikan ke jaringan kayu dari tanaman, tanin juga dibentuk dengan polimerisasi unit kuinon (Anonymous, 2005).
Secara kimia terdapat dua jenis utama tanin yang tersebar tidak merata dalam dunia tumbuhan. Tanin terkondensasi hapir terdapaat didalam paku-pakuan dan gimnospermae, serta tersebar luas dalam angiospermae, terutama pada jenis tumbuhan berkayu. Sebaliknya, tanin yang terhidrolisiskan penyebarannya terbatas pada tumbuhan berkeping dua (Harborne, 1987).
Secara kimia terdapat 2 jenis utama tanin yaitu : 1. Tanin terhidrolisis
2. Tanin Terkondensasi
Tanin terkondensasi secara biosintesis dapat dianggap terbentuk dengan cara kondensasi katekin tunggal (galokatekin) yang membentuk senyawa dimer dan kemudian oligomer yang lebih tinggi. Tanin jenis ini biasanya tidak dapat dihidrolisis. Tanin jenis ini kebanyakan terdiri dari polimer flavonoid yang merupakan senyawa fenol. Nama lain dari tanin ini adalah proantosianidin. Proantosianidin adalah polimer dari flavonoid (Tanner et.al., 1999). Senyawa ini jika dikondensasi maka akan menghasilkan flavonoid jenis flavan dengan bantuan nukleofil berupa floroglusinol (Hagerman, 2002). Tanin terkondensasi banyak terdapat dalam paku-pakuan, gymnospermae, dan tersebar luas dalam angiospermae, terutama pada jenis tumbuhan berkayu (Robinson, 1991 dalam Sa’adah 2010).
2.2.4 Terpenoid
Kata terpenoid mencakup sejumlah besar senyawa tumbuhan, dan istilah ini digunakan untuk menunjukkan bahwa secara biosintesis semua senyawa tumbuhan itu berasal dari senyawa yang sama. Kebanyakan senyawa terpenoida terdapat bebas dalam jaringan tanaman, tidak terikat dengan senyawa-senyawa yang lain, tetapi banyak diantara mereka yang terdapat glikosida, ester dari asam organik dan dalam beberapa hal terikat dengan protein (Sastrohamidjo, 1996) Terpenoida terdiri atas beberapa macam senyawa mulai dari komponen minyak atsiri, yaitu monoterprnoida dan siskuiterpenoida yang mudah menguap (C10 dan C15) diterpenoida yang lebih sukar menguap (C20), sampai senyawa yang tidak menguap yaitu triterpenoida dan sterol (C30) serta pigmen kaotenoida (C40) (Harbone, 1987)
2.2.5 Saponin
dalam eter. Saponin paling cocok diekstraksi dengan menggunakan metanol dan etanol (Robinson, 1995).
Saponin dapat digunakan sebagai racun dan antimikroba (jamur, bakteri, dan virus). Saponi terdiri dari 2, yaitu saponin steroid dan saponin triterpenoid. Saponin memberikan hasil yang lebih baik sebagai antibakteri jika mengunakan pelarut polar seperti etanol 70%. Pada konsentrasi rendah saponin menyebabkan hemolisis sel darah merah sehingga berfungsi sebagai antibakteri (Harborne, 1987).
2.3. Ekstraksi
Ekstraksi merupakan kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak larut dengan menggunakan pelarut cair. Senyawa aktif yang terdapat dalam berbagai simplisia dapat digolongkan ke dalam golongan minyak atsiri, alkaloida, flavonoida dan lain-lain. Dengan diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut dengan cara yang tepat (Depkes RI, 2000)
Berdasarkan prinsipnya proses ekstraksi dapat berlangsung bila terdapat kesamaan dalam sifat kepolaran antara senyawa yang diekstraksi dengan senyawa pelarut. Suatu zat memiliki kemampuan terlarut yang berbeda dalam pelarut yang berbeda. Hal ini menunjukkan adanya interaksi antara zat pelarut. Senyawa polar akan larut dalam pelarut polar. Begitu juga sebaliknya. Sifat penting yang harus diperhatikan dalam pemilihan pelarut adalah selektivitas, kemampuan untuk mengekstrak, toksisitas kemudahan untuk diuapkan dan harga (Harbone, 1987)
2.4. Partisi
Metode pemisahan yang mungkin paling sederhana adalah partisi, yang banyak digunakan sebagai tahap awal pemurnian esktrak. Partisi menggunakan dua pelarut tak bercampur yang ditambahkan kedalam ekstrak tersebut , hal ini dapat dilakukan secara terus menerus dengan menggunakan dua pelarut yang tak bercampur yang kepolarannya meningkat. Partisi biasanya dilakukan melalui 2 tahap yaitu :
1. Air/ petroleum eter ringan (heksana) untuk menghasilkan fraksi non polar lapisan organik
2. Air/ diklorometan atau air/kloroform atau air/etil asetat untuk membuat fraksi agak polar dilapisan organik. Ini merupakan metode pemisahan yang mudah dan mengandalkan kelarutan bahan alam dan bukan interaksi fisik dengan medium lain (Heinrich et al, 2010)
2.5. Bakteri
Bakteri merupakan organisme yang sangat kecil (berukuran mikroskopis). Bakteri rata-rata berukuran o,5-1 µm dan panhang hingga 10 µm (1 mikron = 103 mm). Itu berarti pula bahwa jasad renik ini tipis sekali sehingga tembus cahaya. Akibatnya pada mikroskop tidak tampak jelas dan sukar untuk melihat bagian-bagiannya. Untuk melihat bakteri dengan jelas, tubuhnya perlu diisi dengan zat warna, pewarnaan ini disebut pengecatan warna (Irianto, 2006)
Walaupun terdapat berbagai jenis bakteri, tetapi hanya beberapa karakteristik bentuk sel yang ditemukan yaitu :
1. Bentuk bulat atau cocci (tunggal = coccus) 2. Bentuk batang atau bacilli (tunggal = bacillus ) 3. Bentuk spiral atau spirilli (tunggal = spirillum) 4. Bentuk koma atau vibrous (tunggal = vibrio)
Sel-sel ini dapat dijumpai dalam keadaan tunggal, berpasangan, kelompok kecil, gerombolan atau rantai (Buckle, et al.2009)
1. Bakteri Gram positif
Bakteri gram positif pada dinding selnya mendandung polisakarida yang disebut asam teikhoat yang berperan pada proses transportasi ion-ion dari dalam maupun ke luar sel (Dzen dkk., 2013). Bakteri gram positif lebih sensitif terhadap penisilin, tetapi lebih tahan terhadap perlakuan fisik dibandingkan bakteri gram negatif. Bakteri gram positif sering berubah sifat pewarnaanya sehingga menunjukkan reaksi gram variabel. Sebagai contoh, kultur bakteri gram positif yang sudah tua dapat kehilangan kemampuannya untuk menyerap pewarna violet kristal sehingga dapat berwarna merah seperti bakteri gram negatif. Perubahan tersebut dapat juga disebabkan oleh perubahan kondisi lingkungan atau modifikasi teknik pewarnaan (Fardiaz, 1992) Bakteri gram positif mempunyai struktur dinding sel yang tebal (15-80 µm) dikarenakan sel bakteri gram positif tersusun atas beberapa lapisan peptidoglikan, dan strukturnya tebal dan keras. Dinding selnya juga tersusun atas teichonic acid yang mengandung alkohol (seperti gliserol) dan posfat (Tortora, 2001)
2. Bakteri Gram Negatif
Bakteri gram negatif memiliki dinding sel yang tersusun atas satu lapisan peptidoglikan dan membran luar. Bakteri gram negatif mempunyai struktur dinding sel yang tipis (10-15µm) Kandungan peptidoglikan pada dinding selnya lebih sedikit sehingga bakteri gram negatif peka terhadap pengaruh mekanik. Dinding sel bakteri gram negatif juga mengandung lipopolisakarida, fosfolipid, lipoprotein yang berperan dalam proses masuknya bahan-bahan luar sel ke dalam sel serta menentukan sifat pewarnaan cara gram. Selain itu, lipolisakarida tersebut juga akan menghalangi terjadinya proses fagositosis dan juga bersifat toksik. Bahan toksik dari dinding sel bakteri gram negatif disebut endotoksin yang akan dilepas bila bakteri tersebut selnya rusak atau bakteri tersebut mati (Dzen dkk., 2003)
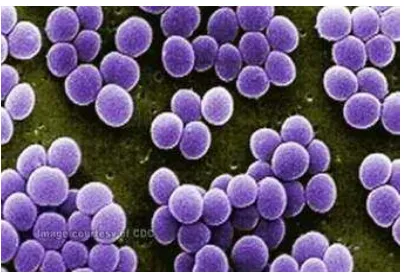
2.5.1. Staphylococcus aureus
Staphylococcus aureus (S. aureus) adalah bakteri gram positif yang
waktu pembelahan 0,47 jam. S. aureus merupakan mikroflora normal manusia. Bakteri ini biasanya terdapat pada saluran pernapasan atas dan kulit. Keberadaan S. aureus pada saluran pernapasan atas dan kulit pada individu jarang menyebabkan
penyakit, individu sehat biasanya hanya berperan sebagai karier. Infeksi serius akan terjadi ketika resistensi inang melemah karena adanya perubahan hormon; adanya penyakit, luka, atau perlakuan menggunakan steroid atau obat lain yang memengaruhi imunitas sehingga terjadi pelemahan inang.
Infeksi S.aureus diasosiasikan dengan beberapa kondisi patologi, diantaranya bisul, jerawat, pneumonia, meningitis, dan arthritits. Sebagian besar penyakit yang disebabkan oleh bakteri ini memproduksi nanah, oleh karena itu bakteri ini disebut piogenik. S. aureus juga menghasilkan katalase, yaitu enzim yang mengkonversi H2O2 menjadi H2O dan O2, dan koagulase, enzim yang menyebabkan fibrin berkoagulasi dan menggumpan. Koagulasi diasosiasikan dengan patogenitas karena penggumpalan fibrin yang disebabkan oleh enzim ini terakumulasi di sekitar bakteri sehingga agen pelindung inang kesulitan mencapai bakteri dan fagositosis terhambat.
Gambar 2.2 Bakteri Staphylococcus aureus (Nasution M, 2014)
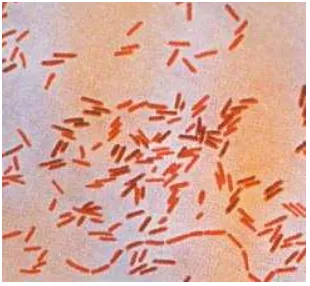
2.5.2. Salmonella typhi
membentuk koloni yang tidak berwarna. Bakteri ini tumbuh secara optimal pada suhu sekitar 35-370C. S typhi biasanya ditemukan pada jaringan limfa saluran pencernaan kemudian masuk ke dalam nodus limfa dan aliran darah. S typhi dapat menyebabkan penyakit demam tifoid (Dwidjoseputro, 1987)
Gambar 2.3. Bakteri Salmonella typhi (Pelczar, dkk, 2005)
2.5.3. Streptococcus mutan
Golongan Streptococcus mempunyai beberapa strain, tetapi yang dominan dan banyak ditemukan dalam rongga mulut manusia adalah jenis Streptococcus mutan (S. mutan). Mikroorganisme fakultatif ini dapat memetabolisme karbohidrat
dan dianggap sebagai agen etiologi terjadinya karies. Sifat karsiogenik bakteri ini terkait dengan berbagai faktor termasuk produksi konsentrasi tinggi asam dalam pembentukan plak dan glukosil transferase (GTF). S mutan merupakan bakteri gram positif, bersifat nonmotil (tidak bergerak). Memiliki bentuk kokus berbentuk bulat atau bulat telur dan tersusun dalam rantai. Bakteri ini tumbuh secara optimal pada suhu sekitar 18 ˚ - 40˚C. S mutan termasuk alfa hemolitik.
Berdasarkan penelitian longitudinal terbukti bahwa S mutan stabil dalam jumlah besar yang diasosiasikan dengan pengembangan lesi karies pada email. S mutan merupakan bakteri yang berkembang dalam plak. S mutan memiliki suatu
Keadaan ini mendukung pertumbuhan bakteri asidurik yang lain dan melarutkan enamel dan berperan penting pada pembentukan karies.
Gambar 2.4. Bakteri Streptococcus mutan (Jaweetz, dkk, 2001)
2.6. Uji Akivitas Antibakteri
Antibakteri adalah zat yang dapat mengganggu pertumbuhan atau bahkan mematikan bakteri dengan cara mengganggu metabolisme bakteri. Antibakteri hanya dapat digunakan jika mempunyai sifat toksik selektif, artinya dapat membunuh bakteri yang menyebabkan penyakit tetapi tidak beracun bagi penderitanya. Faktor - faktor yang berpengaruh pada aktivitas zat antibakteri adalah pH, Suhu stabilitas senyawa, jumlah bakteri yang ada, lamanya inkubasi dan aktivitas metabolisme bakteri (Bakhriansyah, 2008)
Aktivitas (potensi) antibakteri dapat ditunjukkan pada kondisi yang sesuai dengan efek daya hambatnya terhadap bakteri. Ada dua metode umum yang dapat digunakan yaitu Metode difusi dan Metode dilusi (Bakhriansyah, 2008) Metode difusi untuk menentukan aktifitas agen antimikroba. Piringan yang berisi agen antimikroba diletakkan pada media agar yang telah ditanami mikroorganisme yang akan berdifusi pada media agar tersebut. Area jernih mengindikasikan adanya hambatan pertumbuhan mikroorganisme oleh agen antimikroba pada permukaan media agar (Bakhriansyah, 2008).
concentration atau kadar hambat minimum, KHM) dan MBC (minimum bactericidal concentration atau kadar bunuh minimum, KBM). Cara yang dilakukan adalah dengan membuat seri pengenceran agen anti mikroba pada medium cair yang ditambahkan dengan mikroba uji. Larutan uji agen antimikroba pada kadar terkecil yang terlihat jernih tanpa adanya pertumbuhan mikroba uji ditetapkan sebagai KHM. Larutan yang ditetapkan sebagai KHM tersebut selanjutnya dikultur ulang pada media cair tanpa penambahan mikroba uji ataupun agen antimikroba dan diinkubasi selama 18-24 jam. Media cair yang tetap terlihat jernih setelah inkubasi ditetapkan sebagai KBM. Tahap selanjutnya disebut metode dilusi padat / solid dilution test. Metode ini serupa dengan metode dilusi cair namun menggunakan media padat (solid). Keuntungan metode ini adalah satu konsentrasi agen mikroba yang diuji dapat digunakan untuk menguji beberapa mikroba uji (Bakhriansyah, 2008)
Antibakteri adalah zat yang dapat mengganggu pertumbuhan atau bahkan mematikan bakteri dengan cara mengganggu metabolisme mikroba yang merugikan atau menghambat aktivitas mikroorganisme. Antibakteri hanya dapat digunakan jika mempunyai sifat toksik selektif, artinya dapat membunuh bakteri yang menyebabkan penyakit tetapi tidak beracun bagi penderitanya. Mekanisme kerja dari senyawa antibakteri diantaranya yaitu:
1. Merusak dinding sel
2. Mengganggu permeabilitas sel 3. Menghambat aktivitas enzim
4. Menghambat sintesa asam nukleat dan protein