1
Uji Antagonis Bakteri
Streptomyces
spp. terhadap Jamur
Phytophthora palmivora
BBK01 Penyebab Busuk Buah pada
Tanaman Kakao
Edy Purnomo1, Mukarlina1, Rahmawati11Program Studi Biologi, Fakultas MIPA, Universitas Tanjungpura, Jl. Prof. Dr. H. Hadari Nawawi, Pontianak Email korespondensi: purnomoedy007@gmail.com
Abstract
Black pod disease is one of the diseases in cocoa trees caused by fungi member of Phytophthora palmivora. This study aims to examine the activity of bacteria members of Streptomyces spp. in inhibiting the growth of fungus member of P. palmivora BBK01 at in vitro and in vivo antagonistic activities. The study was conducted in Microbiology Laboratory of Faculty of Mathematics and Natural Sciences of Tanjungpura University from Agust to November 2016. In vitro antagonistic activity uses dual culture methods. The isolates was examined for in vivo antagonistic effects using well method. The result of the study showed that at in vitro condition member of Streptomyces sp. SRK03 had the strongest inhibition activity against the fungus growth for 68,17% and that member of Streptomyces sp. SRK01 shows the least inhibition activity against the fungus growth for only 27,37%. At in vivo condition, the members of Streptomyces sp. SRK02, SRK03, SRK04, and SRK05 showed the strongest inhibition in the fungus growth for 100%. On the other hand, member of Streptomyces sp. SRK01 showed the lowest inhibition in the fungus growth for 79,64%.
Keywords: Phytophthora palmivora, Streptomyces spp., antagonistic examination
PENDAHULUAN
Kakao merupakan salah satu komoditas ekspor yang mampu memberikan kontribusi besar dalam upaya peningkatan devisa negara. Salah satu daerah penghasil kakao di Indonesia adalah Kalimantan Barat. Total produksi biji kakao Kalimantan Barat pada tahun 2013 sebesar 2.032 ton, namun pada tahun 2014 turun menjadi 2.007 ton (Direktorat Jendral Perkebunan, 2014). Penurunan produksi kakao tersebut disebabkan oleh banyaknya kendala yang dihadapi dalam pembudidayaan kakao. Salah satunya yaitu penyakit busuk buah yang disebabkan oleh jamur anggota spesies Phytophthora palmivora (Umayah & Purwantara, 2006).
Penyakit busuk buah dapat menurunkan kualitas dan kuantitas hasil produksi kakao. Menurut Guest (2006) penyakit busuk buah pada tanaman kakao menyebabkan kerugian yang bervariasi, yaitu antara 20-30% per tahunnya. Tingkat kerugian akan semakin besar lagi pada saat memasuki musim penghujan.
Penyakit busuk buah pada tanaman kakao hingga saat ini masih sulit untuk dikendalikan. Umumnya pembudidaya kakao memanfaatkan fungisida sintetis untuk mengendalikan jamur anggota spesies P. palmivora. Fungisida sintetis digunakan
karena sifatnya yang cepat dalam menghambat pertumbuhan jamur anggota spesies P. palmivora (Susanto, 1994). Penggunaan fungisida secara terus-menerus dapat menyebabkan jamur menjadi resisten, selain itu bahan aktif yang terkandung dalam fungisida dapat menyebabkan pencemaran terhadap lingkungan (Prapagdee et al., 2008).
Upaya pengendalian penyakit yang ramah lingkungan dapat dilakukan dengan cara pengendalian hayati, yaitu dengan memanfaatkan bakteri antagonis (Agrios, 2005). Bakteri antagonis yang berpotensi dijadikan sebagai alternatif penghambat jamur anggota spesies P. palmivora adalah bakteri anggota genus Streptomyces.
Penelitian mengenai kemampuan bakteri anggota genus Streptomyces sebagai agen pengendali pertumbuhan jamur patogen banyak dilaporkan. Menurut Raharini et al. (2012), bakteri anggota spesies Streptomyces sp. yang diujikan secara in vitro dapat menghambat pertumbuhan jamur anggota spesies Fusarium oxysporum hingga 82%. Sari et al. (2012) menambahkan bahwa, bakteri anggota spesies Streptomyces sp. dapat menghambat pertumbuhan jamur anggota spesies F. oxysporum pada tanaman tomat sebesar 75%. Menurut Papuangan (2013), bakteri anggota spesies Streptomyces sp. yang diujikan secara in
2
vitro dapat menghambat jamur anggota spesies Sclerotium rolfsii hingga 84,10%.
Penelitian mengenai peran mikroorganisme antagonis seperti bakteri isolat lokal anggota spesies Streptomyces spp. sebagai agen pengendali hayati terhadap jamur anggota spesies P. palmivora BBK01 pada tanaman kakao di Kalimantan Barat belum pernah dilaporkan. Sehingga perlu dilakukan pengkajian mengenai kemampuan agen pengendali hayati tersebut dalam menghambat pertumbuhan jamur anggota spesies P. palmivora BBK01, terutama melalui uji antagonis secara in vitro dan in vivo.
BAHAN DAN METODE Waktu dan Tempat
Penelitian ini dilaksanakan dari bulan Agustus hingga November 2016. Lokasi pengambilan sampel berada di Desa Sedau, Kecamatan Singkawang Selatan, Kota Singkawang, Kalimantan Barat. Isolasi, identifikasi serta pengujian jamur dan bakteri dilakukan di Laboratorium Mikrobiologi, Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Tanjungpura, Pontianak.
Bahan
Bahan-bahan yang digunakan terdiri atas akuades, alkohol 70%, buah kakao sehat, buah kakao yang bergejala sakit, isolat bakteri anggota spesies Streptomyces spp., isolat jamur anggota spesies P. palmivora BBK01, larutan asam laktat, media NB (Nutrient Broth), media PDA (Potato Dextrose Agar), media PDB (Potato Dextrose Broth), media PDY (Potato Dextrose Agar + extract yeast), dan siprofloksasin.
Rancangan Penelitian
Penelitian ini menggunakan Rancangan Acak Lengkap (RAL), baik untuk uji antagonis secara in vitro maupun uji antagonis secara in vivo. Uji antagonis secara in vitro dan in vivo masing-masing terdiri atas 6 perlakuan dengan 4 kali ulangan.
Prosedur Kerja
Isolasi Jamur Anggota Spesies P. palmivora Kulit buah kakao bergejala penyakit busuk buah terlebih dahulu diiris untuk mendapatkan sebagian kecil dari kulit buah. Kulit buah selanjutnya direndam dalam larutan alkohol 70% selama 3 menit, kemudian kulit buah dibilas dengan akuades steril sebanyak dua kali, masing-masing selama 2 menit. Kulit buah selanjutnya
dipindahkan ke cawan petri lalu dipotong dengan ukuran ± 1 x 1 cm. Tiga potong kulit buah kakao diletakkan di atas media PDA pada cawan petri yang telah disiapkan, kemudian cawan petri diinkubasikan selama 7 x 24 jam pada suhu ruangan (Pratama et al., 2013).
Identifikasi Jamur Anggota Spesies P. palmivora BBK01
Biakan jamur dari hasil isolasi diidentifikasi dengan melihat karakter makroskopis meliputi bentuk, tepian, dan warna koloni, serta karakter mikroskopis meliputi tipe hifa, bentuk percabangan, bentuk sporangium, bentuk klamidospora serta ada tidaknya papila pada ujung sporangium. Karakter yang tercatat dicocokkan dengan buku identifikasi Phytophthora Diseases Worldwide (Erwin & Ribeiro, 1996), dan Practical Guide to Detection and Identification of Phytophthora (Drenth & Sendall, 2001).
Uji Antagonis secara In Vitro
Pengujian mengacu pada Pratama et al. (2013), yaitu dengan metode kultur ganda (dual culture). Biakan murni isolat jamur anggota spesies P. palmivora BBK01 dan biakan murni isolat bakteri anggota spesies Streptomyces spp. diambil, masing-masing dengan ukuran 0,5 cm. Koloni jamur dan bakteri selanjutnya diletakkan pada cawan petri yang berisi media PDY secara berpasangan. Perlakuan kontrol negatif, yaitu dengan menumbuhkan koloni isolat jamur anggota spesies P. palmivora BBK01 ukuran 0,5 cm tanpa dipasangkan dengan isolat bakteri. Pengamatan dilakukan pada hari ke-7, yaitu dengan mengukur jari-jari koloni isolat jamur anggota spesies P. palmivora BBK01 yang menuju pusat antagonis dan jari-jari koloni isolat jamur anggota spesies P. palmivora BBK01 yang ada pada kontrol negatif.
Uji Antagonis secara In Vivo
Uji antagonis secara in vivo dilakukan dengan mengambil buah kakao sehat kemudian dicuci menggunakan alkohol 70% dan dibilas dengan akuades steril. Buah kakao selanjutnya diberi lubang dengan diameter 0,5 cm dan kedalaman 0,5 cm. Lubang kemudian ditutup dengan kapas yang terlebih dahulu dicelupkan pada suspensi isolat jamur anggota spesies P. palmivora BBK01 dan suspensi isolat bakteri anggota spesies Streptomyces spp. dan untuk kontrol kapas hanya dicelupkan pada suspensi isolat jamur anggota spesies P. palmivora BBK01. Buah kakao yang telah diberi perlakuan diinkubasi selama 3 x 24
3
jam pada suhu ruangan. Parameter yang diamati berupa diameter bercak yang terbentuk akibat aktivitas jamur (Umrah et al., 2009).
Perhitungan Peresentase Daya Hambat pada Uji Antagonis secara In Vitro
Penghitungan persentase daya hambat dalam uji antagonis secara in vitro menggunakan rumus:
R = (Rc - Ri) (Rc-1) x 100% Keterangan;
R = Persentase daya hambat (%)
Rc = Jari-jari koloni jamur pada kontrol (mm) Ri = Jari-jari koloni jamur menuju pusat antagonis
(mm) (Narayanasamy, 2013).
Perhitungan Peresentase Daya Hambat pada Uji Antagonis secara In Vivo
Perhitungan persentase daya hambat dalam uji antagonis secara in vivo menggunakan rumus:
DH = (DK-DP) (DK-1) x 100% Keterangan:
DH = Daya hambat (%)
DK = Diameter bercak pada kontrol (mm)
DP = Diameter bercak pada perlakuan (mm) (modifikasi Asrul, 2009).
Analisis dan Penyajian Data
Data yang diperoleh disajikan dalam bentuk gambar (foto), deskripsi dan tabel. Data yang diperoleh dari uji antagonis secara in vitro dan in vivo terlebih dahulu dianalisis menggunakan Analysis of variance (ANOVA), dan apabila data yang diperoleh hasilnya berbeda nyata, maka dilanjutkan dengan uji Duncan pada taraf 5%.
HASIL DAN PEMBAHASAN Hasil
Karakter Morfologi Isolat Jamur Anggota Spesies P. palmivora BBK01 dari Buah Kakao
Isolat jamur anggota spesies P. palmivora BBK01 yang diisolasi dari buah kakao bergejala penyakit busuk buah memiliki ciri-ciri koloni bulat, berdiameter 79,19 mm, berwarna putih (Gambar 1 a), sporangium berbentuk ovoid (oval) dengan papila (pp) di ujungnya dan pedisel (pd) di pangkalnya, serta klamidospora (kl) berbentuk bulat dengan dinding tebal (Gambar 1 b), selain itu terdapat oogonium (og) berbentuk bulat dengan dilengkapi anteridium (an) pada pangkalnya (Gambar 1 c).
a b c
Gambar 1. Isolat jamur anggota spesies P. palmivora BBK01. (a) koloni jamur isolat anggota spesies P. palmivora BBK01 pada media PDA umur 7 hari, (b) sporangium (spr) dan klamidospora (kl), (c) oogonium (og) dan anteridium (an), perbesaran 10 x 40.
Uji Antagonis secara In Vitro
Berdasarkan hasil analisis data, persentase daya hambat pada uji antagonis secara in vitro antara isolat bakteri anggota spesies Streptomyces spp.
terhadap isolat jamur anggota spesies P. palmivora BBK01 pada hari ke-7 hasilnya
berbeda-beda (F5,18 = 152,48, p = 0,000;
ANOVA). Berdasarkan uji lanjut (uji Duncan) diketahui bahwa persentase daya hambat seluruh perlakuan berbeda nyata dengan kontrol. Perlakuan P2 dan P3 hasilnya tidak berbeda nyata, namun keduanya berbeda nyata dengan perlakuan P1, P4 dan P5. Di sisi lain antara perlakuan P1, P4 dan P5, ketiganya saling berbeda nyata (Tabel 1).
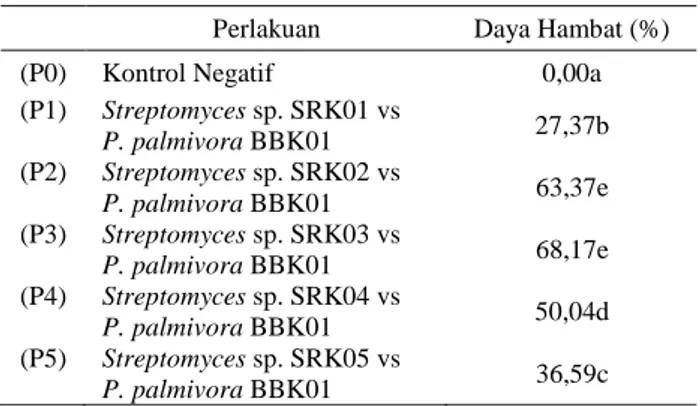
Tabel 1. Daya hambat uji antagonis secara in vitro
Perlakuan Daya Hambat (%)
(P0) Kontrol Negatif 0,00a
(P1) Streptomyces sp. SRK01 vs P. palmivora BBK01 27,37b (P2) Streptomyces sp. SRK02 vs P. palmivora BBK01 63,37e (P3) Streptomyces sp. SRK03 vs P. palmivora BBK01 68,17e (P4) Streptomyces sp. SRK04 vs P. palmivora BBK01 50,04d (P5) Streptomyces sp. SRK05 vs P. palmivora BBK01 36,59c
Keterangan: Angka yang diikuti oleh huruf yang sama menunjukkan hasil yang tidak berbeda nyata menurut uji Duncan pada taraf kepercayaan 0,05
4
Uji Antagonis secara In Vivo
Berdasarkan hasil analisis data persentase daya hambat pada hari ke-3, masing-masing perlakuan memberikan pengaruh terhadap aktivitas isolat jamur anggota spesies P. palmivora BBK01 pada buah kakao yang ditandai dengan bercak cokelat pada buah (F5,18 = 5024,25, p=0,000; ANOVA).
Hasil uji lanjut (uji Duncan) menunjukkan bahwa antara perlakuan P2, P3, P4, dan P5 hasilnya tidak berbeda nyata, namun keempatnya menunjukkan hasil yang berbeda nyata dengan perlakuan P1 dan kontrol, selain itu dari uji lanjut diketahui bahwa seluruh perlakuan (P1, P2, P3, P4, dan P5) hasilnya berbeda nyata dengan kontrol (Tabel 2).
Tabel 2. Daya hambat uji antagonis secara in vivo
Perlakuan Daya Hambat (%)
(P0) Kontrol Negatif 0,00a
(P1) Streptomyces sp. SRK01 vs P. palmivora BBK01 79,64b (P2) Streptomyces sp. SRK02 vs P. palmivora BBK01 100c (P3) Streptomyces sp. SRK03 vs P. palmivora BBK01 100c (P4) Streptomyces sp. SRK04 vs P. palmivora BBK01 100c (P5) Streptomyces sp. SRK05 vs P. palmivora BBK01 100c
Keterangan: Angka yang diikuti oleh huruf yang sama menunjukkan hasil yang tidak berbeda nyata menurut uji Duncan pada taraf kepercayaan 0,05
Pembahasan
Berdasarkan hasil karakterisasi dan identifikasi, isolat jamur anggota spesies P. palmivora BBK01 yang diisolasi dari buah kakao bergejala penyakit busuk buah memiliki ciri-ciri koloni berwarna putih, berbentuk bulat, bertipe stellate, tepian tidak rata. Secara mikroskopis terdapat klamidospora, anteridium, oogonium dan sporangium. Sporangium berbentuk ovoid, terdapat pedisel dan papila yang pendek, serta hifa senositik (tidak bersekat) (Gambar 1 a-c). Karakteristik tersebut sesuai dengan Erwin & Ribeiro (1996) serta Drenth & Sendall (2001) yang menyatakan bahwa, jamur anggota spesies P. palmivora memiliki koloni bulat, bertipe stellate atau rosaceous, tepian tidak rata, sporangium dapat berbentuk ellipsoid, ovoid atau pyriform dan terdapat pedisel serta papila yang pendek, klamidospora berbentuk bulat, hifa tak bersekat dengan percabangan simpodia.
Klamidospora isolat jamur anggota spesies P. palmivora BBK01 yang diperoleh terlihat
memiliki lapisan tebal (Gambar 1 b). Lapisan
tebal tersebut memungkinkan klamidospora resisten akan kondisi yang tidak menguntungkan. Hal tersebut diperkuat oleh Rubiyo & Amaria (2013) yang menyatakan bahwa, klamidospora jamur anggota spesies P. palmivora dapat bertahan hingga 10 bulan di dalam tanah, dikarenakan memiliki dinding sel yang tebal dan berlapis.
Berdasarkan hasil uji antagonis secara in vitro,
perlakuan P3 (Streptomyces sp. SRK03 vs P. palmivora BBK01) dan P2 (Streptomyces sp.
SRK02 vs P. palmivora BBK01) memiliki kemampuan yang sama dalam menghambat
pertumbuhan isolat jamur anggota spesies P. palmivora BBK01. Kedua perlakuan
menunjukkan persentase daya hambat yang berbeda jika dibandingkan dengan perlakuan P1 (Streptomyces sp. SRK01 vs P. palmivora BBK01), P4 (Streptomyces sp. SRK04 vs P. palmivora BBK01), dan P5 (Streptomyces sp. SRK05 vs P. palmivora BBK01). Perbedaan tersebut diduga disebabkan oleh kemampuan masing-masing bakteri anggota spesies Streptomyces spp. dalam menghasilkan senyawa penghambat pertumbuhan isolat jamur anggota spesies P. palmivora BBK01.
Bakteri strain anggota genus Streptomyces dikenal sebagai salah satu bakteri penghasil metabolit sekunder berupa antibiotik. Hasani et al. (2014) melaporkan bahwa beberapa strain bakteri anggota genus Streptomyces dapat menghasilkan antibiotik seperti vankomisin, eritromisin, tetrasiklin, streptomisin, neomisin, kanamisin, sikloserin, linkomisin, nistatin, sulfonamida, aminoglikosida, aureomisin, kloramfenikol, amfosetin B, aktinomisin, fosfomisin, dekamisin, rimfamisin, avermisin, tobramisin, spektinomisin, klindamisin, daptomisin, puromisin, novobiosin, oksitetrasiklin, klortetrasiklin, ribostamisin, platenmisin, viomisin, dimetil klortetrasiklin, spiramisin, dan sefalosporin.
Antibiotik yang dihasilkan oleh strain bakteri anggota genus Streptomyces memiliki mekanisme kerja yang berbeda-beda, yaitu dengan merusak dinding sel, mengganggu fungsi membran sel, serta mengganggu sintesis protein dan asam nukleat. Menurut Waluyo (2007) antibiotik sefalosporin, sikloserin dan vankomisin dapat merusak atau menghambat sintesis dinding sel. Antibiotik nistatin dan amfoterisin B dapat mengganggu fungsi membran sel. Antibiotik aktinomisin, eritromisin, tetrasiklin, streptomisin, neomisin, kanamisin, linkomisin, tobramisin dan
5
kloramfenikol dapat menghambat sintesis protein, sedangkan antibiotik sulfonamida dan novobiosin dapat menghambat sintesis asam nukleat.
Penelitian mengenai penggunaan antibiotik yang dihasilkan oleh bakteri anggota genus Streptomyces sebagai biokontrol terhadap mikroorganisme patogen telah banyak dilaporkan. Menurut Hwang et al. (2001), fraksi antibiotik SH1 (asam fenil asetat) dan SH2 (sodium fenil asetat) yang dihasilkan strain bakteri anggota spesies S. humidus strain S5-55 diketahui dapat menekan pertumbuhan strain jamur anggota spesies P. capsici, Pythium ultimum, R. solani, dan Saccharomyces cerevisiae. Hwang et al. (2005) melaporkan bahwa antibiotik sangivamisin yang dihasilkan oleh strain bakteri anggota spesies Streptomyces sp. A6497 mampu menghambat pertumbuhan jamur anggota spesies P. parasitica. Berdasarkan kedua penelitian di atas, diketahui bahwa bakteri anggota genus Streptomyces mampu menghambat pertumbuhan jamur anggota genus Phytophthora menggunakan antibiotik melalui mekanisme antibiosis. Menurut Soesanto (2008), antibiosis merupakan proses penghambatan pertumbuhan jamur atau bakteri akibat adanya senyawa antibiotik yang dihasilkan oleh mikroorganisme antagonis (agen biokontrol). Mekanisme penghambatan jamur patogen oleh bakteri anggota genus Streptomyces dapat pula melalui produksi enzim ekstraseluler. Menurut Prapagdee et al. (2008), enzim yang umumnya dihasilkan oleh bakteri anggota genus Streptomyces adalah enzim kitinase dan β-1.3-glukanase yang berturut-turut dapat melisiskan senyawa kitin dan glukan pada dinding sel jamur. Enzim lain yang dihasilkan oleh bakteri anggota genus Streptomyces adalah enzim protease yang berguna dalam memecah senyawa protein yang ada pada dinding sel jamur patogen (Singh & Chhatpar, 2011) dan enzim selulase yang berguna untuk melisiskan senyawa selulosa (Semédo et al., 2004). Enzim ekstraseluler bakteri anggota genus Streptomyces yang sangat penting dalam uji antagonis terhadap jamur anggota spesies P. palmivora BBK01 adalah β-1.3-glukanase dan selulase, hal ini dikarenakan menurut Semangun (2000) senyawa penyusun dinding sel pada jamur kelas Oomycetes adalah β-glukan dan selulosa. Senyawa lain yang dapat dihasilkan oleh bakteri anggota genus Streptomyces adalah senyawa siderofor. Senyawa siderofor merupakan senyawa pengkelat ion besi contohnya adalah senyawa desferrioxamine. Ion besi diketahui berperan penting bagi perkecambahan klamidospora jamur
patogen, sehingga dengan tidak adanya ion besi maka perkecambahan klamidospora jamur akan terhambat dan berakibat pada penurunan laju pertumbuhan jamur patogen. Beberapa strain bakteri anggota genus Streptomyces yang dilaporkan dapat menghasilkan senyawa siderofor adalah dari strain anggota spesies S. albovinaceus, S. caviscabies, S. griseus, S. setonii, S. virginiae, S. ambofaciens, S. coelicolor, S. lividans, dan S. viridosporus (Imbert et al., 1995; Macagnan et al., 2008).
Hasil uji antagonis secara in vivo memperlihatkan seluruh isolat bakteri anggota genus Streptomyces yang digunakan mampu menekan isolat jamur anggota spesies P. palmivora BBK01. Empat isolat yakni isolat anggota spesies Streptomyces sp. SRK02, Streptomyces sp. SRK03, Streptomyces sp. SRK04, dan Streptomyces sp. SRK05 mampu menekan isolat jamur anggota spesies P. palmivora BBK01 hingga 100% atau sama sekali tidak menghasilkan bercak cokelat pada buah kakao uji. Satu isolat yakni isolat anggota spesies Streptomyces sp. SRK01 menunjukkan adanya penghambatan sebesar 79,64%. Kondisi ini diduga disebabkan oleh kandungan bahan organik yang tinggi pada buah kakao. Menurut Mucra (2005) bahan organik pada kulit buah kakao mencapai 89,39%. Hasani et al. (2014) menambahkan bahwa bahan organik yang ada pada media pertumbuhan bakteri anggota genus Streptomyces mampu meningkatkan produksi metabolit sekunder.
Adanya kontak langsung antara isolat jamur anggota spesies P. palmivora BBK01 dan isolat bakteri anggota spesies Streptomyces spp. diduga dapat membuat jamur semakin terhambat. Chen et al. (2016) melaporkan bahwa adanya kontak antara jamur dan bakteri anggota genus Streptomyces membuat bakteri mampu melakukan mekanisme hiperparasitisme (mikoparasitisme) dengan cara membelit hifa jamur dan mengeluarkan enzim-enzim hidrolitik untuk merusak komponen penyusun hifa.
DAFTAR PUSTAKA
Agrios, GN, 2005, Plant Pathology, 5th Edition, Academic Press, New York
Asrul, 2009, ‘Uji Daya Hambat Jamur Antagonis
Trichoderma spp. dalam Formulasi Kering
Berbentuk Tablet terhadap Luas Bercak
Phytophthora palmivora pada Buah Kakao’,
6 Chen, YY, Chen, PC, & Tsay, TT, 2016, ‘The
Biocontrol Efficacy and Antibiotic Activity of
Streptomyces plicatus on the Oomycete
Phytophthora capsici’, Journal Biological
control, vol. 2, no. 11, hal. 1-27
Direktorat Jendral Perkebunan, 2014, Statistik
Perkebunan Indonesia: Kakao, Jakarta
Drenth, A & Sendall, B, 2001, Practical Guide to
Detection and Identification of Phytophthora,
CRC for Tropical Plant Protection, Australia Erwin, DC, & Ribeiro, OK, 1996, Phytophthora
Diseases Worldwide, APS Press, Minnesota
Guest, D, 2006, ‘Black Pod: Diverse Pathogens with a Global Impact on Cocoa Yield’, The American
Phytopathological Society, vol. 97, no. 12, hal.
1650-1653
Hasani, A, Kariminik, A & Issazadeh, S, 2014,
‘Streptomycetes: Characteristics and Their
Antimicrobial Activities’, International Journal of Advanced Biological and Biomedical
Research, vol. 2, no. 1, hal. 63-75
Hwang, BK, Lim, SW, Kim, BS, Lee, JY, & Moon, SS, 2001, ‘Isolation and in vivo and in vitro
Antifungal Activity of Phenylacetic Acid and Sodium Phenylacetate from Streptomyces
humidus’. J. Appl Environ Microbiol, vol. 67,
hal. 3739-3745
Hwang, EI, Yun, BS, Choi, SW, Kim, JS, Lim, SJ, Moon, JS, Lee, SH, & Kim, SU, 2005, ‘Isolation of Sangivamycin from Streptomyces
sp. A6497 and its Herbicidal Activity’,
J. Microbiol Biotechnol, vol. 15, no. 2, hal.
434–437
Imbert, M, Béchet, M, & Blondeau, R, 1995, ‘Comparison of the Main Siderophores Produced by Some Species of Streptomyces’,
Current Microbiology, vol. 31, hal. 129-133
Macagnan, D, Romeiro, RS, Pomella, AWV, & de Souza JT, 2008, ‘Production of Lytic Enzymes and Siderophores, and Inhibition of Germination of Basidiospores of
Moniliophthora (ex Crinipellis) perniciosa by
Phylloplane Actinomycetes’, J. Biol Control,
vol. 47, hal. 309–314
Mucra DA, 2005, ‘Pengaruh Pemakaian POD Cokelat sebagai Pengganti Jagung dalam Ransum terhadap Pertambahan Bobot Badan dan Efisiensi Penggunaan Ransum pada Sapi Brahman Cross’, Jurnal Peternakan, vol. 2, hal. 37-44
Narayanasamy, P, 2013, Biological Management of
Deseases of Crop, Springer, New York
Papuangan, N, 2013, ‘Aktivitas Penghambatan
Streptomyces spp. terhadap Sclerotium rolfsii
secara in vitro’, Jurnal Bioedukasi, vol. 2, no. 1, hal.185-191
Prapagdee, B, Kuekulvog, C, & Mongkulsuk, S, 2008, ‘Antifungal Potensial of Extracellular Metabolites Produce by Streptomyces
hygrospicus Against Phytophstogenic Fungi’,
International Journal of Biological Science,
vol.4, no. 5, hal. 330-337
Pratama, SW, Sukamto, S, Asyiah, IS, & Ervina, YV, 2013, ‘Penghambatan Pertumbuhan Jamur Patogen Kakao Phytophthora palmivora oleh
Pseudomonas fluorescence dan Bacillus
subtilis’, JurnalPelita Perkebunan, vol. 29, no.
2, hal. 120-127
Raharini, AO, Kawuri, R, & Khalimi, K, 2012, ‘Penggunaan Streptomyces sp. sebagai Biokontrol Penyakit Layu pada Tanaman Cabai Merah (Capsicum annum L.) yang Disebabkan oleh Fusarium oxysporum f.sp capsici’, Jurnal
Agrotrop, vol. 2, no. 2, hal. 151-159
Rubiyo, & Amaria, W, 2013, ‘Ketahanan Tanaman Kakao terhadap Penyakit Busuk Buah
(Phytophthora palmivora Butl.)’, Jurnal
Prespektif, vol. 12, no. 1, hal. 23-36
Sari, NM, Kawuri, R, & Khalimin, K, 2012,
‘Streptomyces sp. sebagai Biofungisida Patogen
Fusarium oxysporum (Schlecht) f.sp.
lycopersici (Sacc.) Snyd. Et Hans. Penyebab
Penyakit Layu pada Tanaman Tomat (Solanum
lycopersicum L.)’, Jurnal Agrotrop, vol. 2, no.
2, hal. 161-169
Semangun, H, 2000, Penyakit-Penyakit Tanaman
Perkebunan di Indonesia, Gajah Mada
University Press, Yogyakarta
Semédo, LTAS, Gomes, RC, Linhares, AA, Duarte, GF, Nascimento, RP, Rosado, AS, Margis-Pinheiro, M, Margis, R, Silva, KRA, Alviano, CS, Manfio, GP, Soares, RMA, Linhares, LF, & Coelho, RRR, 2004, ‘Streptomyces
drozdowiczii sp. nov., a Novel Cellulolytic
Streptomycete from Soil in Brazil’,
International Journal of Systematic and
Evolutionary Microbiology, vol. 54, hal.
1323-1328
Singh, AK, & Chhatpar, HS, 2011, ‘Purification, characterization and thermodynamics of antifungal protease from Streptomyces sp. A6’,
Journal of Basic Microbiology, vol. 51, hal.
424–432
Soesanto, L, 2008, Pengantar Pengendalian Hayati
Penyakit Tanaman. PT. Rajawali Grafindo
Persada, Jakarta
Susanto, 1994, Tanaman Kakao: Budidaya dan
7 Umayah, A, & Purwantara, A, 2006, ‘Identifikasi Isolat
Phytophthora Asal Kakao’, Jurnal Menara
Perkebunan, vol. 74, no. 2, hal. 76-85
Umrah, Anggraini, T, Esyanti, RR, & Aryantha, INP, 2009, ‘Antagonisitas dan Efektivitas
Trichoderma sp. dalam Menekan
Perkembangan Phytophthora palmivora pada Buah Kakao’, Jurnal Agroland, vol. 16, no.1, hal. 9-16
Waluyo, L, 2007, Mikrobiologi Umum, Universitas Muhammadiyah Malang Press, Malang