i
OPTIMASI FORMULA SINTESIS NANOSILVER MENGGUNAKAN BIOREDUKTOR EKSTRAK AIR DAUN SINGKONG (Manihot esculenta
Crantz): APLIKASI CENTRAL COMPOSITE DESIGN (CCD)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Stevani Johannes NIM : 178114056
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA 2021
ii
OPTIMASI FORMULA SINTESIS NANOSILVER MENGGUNAKAN BIOREDUKTOR EKSTRAK AIR DAUN SINGKONG (Manihot esculenta
Crantz): APLIKASI CENTRAL COMPOSITE DESIGN (CCD)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh: Stevani Johannes NIM : 178114056
FAKULTAS FARMASI UNIVERSITAS SANATA DHARMA
YOGYAKARTA 2021
vii ABSTRAK
Nanosilver merupakan partikel perak berukuran nano yang banyak digunakan sebagai antimikroba. Sintesis nanosilver dapat dilakukan dengan metode reduksi kimia. Metode reduksi kimia melibatkan reaksi redoks dari garam perak sebagai prekursor dan reduktor. Penggunaan bioreduktor dipertimbangkan karena murah, ramah lingkungan dan tidak beracun. Konsentrasi prekursor dan konsentrasi reduktor perlu dioptimasi untuk mengontrol ukuran partikel nanosilver. Penelitian ini bertujuan untuk mendapatkan formula dan area optimum sintesis nanosilver dari faktor yang dioptimasi menggunakan CCD.
Penelitian ini merupakan rancangan kuasi eksperimental menggunakan rancangan central composite design (CCD). Penelitian ini menggunakan 2 faktor sebagai variabel bebas yaitu konsentrasi AgNO3, konsentrasi ekstrak air daun
singkong. Parameter yang digunakan sebagai variabel tergantung yaitu panjang gelombang dan nilai %T. Area optimum dan analisis data dengan ANOVA menggunakan aplikasi minitab17.
Pada penelitian ini, didapatkan hasil statistik model yang signifikan berpengaruh terhadap respon dengan P-value<0,05. Area optimum formula sintesis nanosilver didapatkan menggunakan metode CCD. Solusi formula optimum yaitu konsentrasi AgNO3 1,64 mM dan konsentrasi ekstrak air daun singkong 17,61%
yang akan menghasilkan panjang gelombang 424,75 nm dan %T 95,2%. Dipilih juga 2 formula optimum dari rancangan percobaan yang telah dilakukan. Perlu dilakukan penelitian lebih lanjut terkait hubungan absorbansi dengan jumlah nanosilver yang terbentuk, validasi terhadap solusi formula optimum yang didapatkan serta memperhatikan. tahapan kritis dalam sintesis nanosilver.
viii ABSTRACT
Nanosilver is a nano-sized silver particle which is widely used as an antimicrobial. Nanosilver synthesis can be carried out by chemical reduction methods. The chemical reduction method involves the redox reaction of the silver salt as a precursor and reducing agent. The use of bioreductors is considered because they are cheap, environmentally friendly and non-toxic. The precursor concentration and the reducing agent concentration need to be optimized to control the nanosilver particle size. This study aims to obtain the optimum formula and area of nanosilver synthesis from the optimized factors using CCD.
This study is a quasi experimental design using a central composite design (CCD). This study used 2 factors as independent variables, namely the concentration of AgNO3, the concentration of water extract of cassava leaves. The parameters used as the dependent variable are the wavelength and the% T value. The optimum area and data analysis using ANOVA using the Minitab17 application.
In this study, the statistical model results were obtained which significantly affected the response with a P-value <0.05. The optimum area of the nanosilver synthesis formula was obtained using the CCD method. The optimum formula solution is 1.64 mM AgNO3 concentration and 17.61% water extract concentration of cassava leaves which will produce a wavelength of 424.75 nm and %T 95.2%. Two optimum formulas were selected from the experimental design that had been carried out. It is necessary to do further research related to the absorbance relationship with the amount of nanosilver formed, validation of the optimum formula solution obtained and pay attention. a critical stage in nanosilver synthesis.
ix DAFTAR ISI
COVER ... i
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN SKRIPSI BERJUDUL ... iv
LEMBAR PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN ... vi
ABSTRAK ... vii
ABSTRACT ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xii
PENDAHULUAN ... 1
METODE PENELITIAN ... 3
Jenis dan Rancangan Penelitian ... 3
Alat dan Bahan ... 4
Determinasi tanaman ... 4
Ekstrak air daun singkong ... 4
Uji kualitatif flavonoid rutin dengan metode KLT ... 5
Rancangan optimasi formula sintesis nanosilver ... 5
Sintesis dan purifikasi nanosilver ... 6
Penentuan panjang gelombang dan nilai transmitan nanosilver ... 6
Optimasi dan Analisis Data ... 7
HASIL DAN PEMBAHASAN ... 7
Ekstrak air daun singkong ... 7
Hasil uji KLT ekstrak air daun singkong ... 8
Proses sintesis dan purifikasi nanosilver ... 9
Hasil panjang gelombang dan %T ... 11
Hasil optimasi menggunakan rancangan CCD ... 14
KESIMPULAN ... 20
SARAN ... 20
DAFTAR PUSTAKA ... 21
LAMPIRAN ... 26
x
DAFTAR TABEL
Tabel I. Konsentrasi dan Jumlah Penimbangan Ekstrak Air Daun Singkong... 5
Tabel II. Formula Sintesis Nanosilver ... 5
Tabel III. Rancangan Penelitian Optimasi Sintesis Nanosilver 2 Faktor 5 Level Menggunakan CCD ... 6
Tabel IV. Hasil Panjang Gelombang ... 12
Tabel V. Hasil %T... 13
xi
DAFTAR GAMBAR
Gambar 2. Hasil KLT pada 366 nm ... 9
Gambar 1. Hasil KLT pada 254 nm ... 9
Gambar 3. Pembentukan Nanosilver (Mohammadlou et al., 2016) ... 9
Gambar 4. Hasil Nanosilver 400-450 nm ... 10
Gambar 5. Hasil Nanosilver <400 nm ... 10
Gambar 6. Hasil Nanosilver > 450 nm ... 11
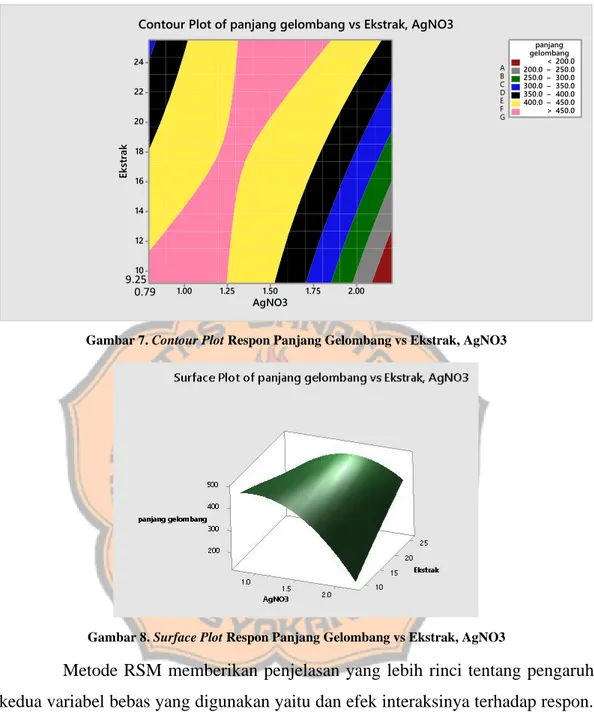
Gambar 7. Contour Plot Respon Panjang Gelombang vs Ekstrak, AgNO3 ... 16
Gambar 8. Surface Plot Respon Panjang Gelombang vs Ekstrak, AgNO3 ... 16
Gambar 9. Contour Plot Respon %T vs Ekstrak, AgNO3 ... 17
Gambar 10. Surface Plot Respon %T vs Ekstrak, AgNO3 ... 18
Gambar 11. Area superimposed contour plot ... 18
xii
DAFTAR LAMPIRAN
Lampiran 1. Hasil Determinasi Tanaman Singkong ... 26
Lampiran 2. Daun Singkong Segar, Daun Singkong Setelah Disimpan 2 Minggu dan Infusa Daun Singkong ... 27
Lampiran 3. Hasil KLT Flavonoid Rutin Ekstrak Air Daun Singkong ... 28
Lampiran 4. Serbuk AgNO3 ... 29
Lampiran 5. Hasil Nanosilver Sebelum dan Sesudah Purifikasi... 29
Lampiran 6. Endapan Sesudah Purifikasi ... 30
Lampiran 7. Hasil replikasi panjang gelombang dan %T sebelum dan sesudah purifikasi ... 31
Lampiran 8 Grafik Panjang Gelombang Sesudah dan Sebelum Purifikasi... 34
Lampiran 9. Hasil PSA ... 36
Lampiran 10. Alat dan Instrumen yang Digunakan ... 41
Lampiran 11. Hasil Analisis Respon Panjang Gelombang dengan Rancangan CCD Menggunakan Minitab17 ... 43
Lampiran 12. Hasil Analisis Respon %T dengan Rancangan CCD Menggunakan Miniab17 ... 44
1 PENDAHULUAN
Nanoteknologi telah muncul sebagai teknologi tercanggih dengan berbagai aplikasi dalam beragam bidang. Sebagian besar penelitian nanomaterials berfokus pada penelitian nanopartikel karena dapat dengan mudah disiapkan dan dilakukan (Herlekar et al., 2014). Nanopartikel merupakan material dengan ukuran panjang partikel primernya kurang dari 100nm (Masakke et al., 2015). Teknologi nanopartikel terdiri dari nanoemulsi, nanoliposom, nanofitosom, nanoetosom (Ramadon dan Mun’im, 2016) dan nanopartikel logam. Nanopartikel logam yang paling banyak diteliti adalah nanosilver karena aplikasinya yang luas sebagai antimikroba (Prasetiowati et al., 2018).
Nanosilver dapat diaplikasikan dalam kain pembalut luka, serat katun yang berfungsi menghambat pertumbuhan bakteri, semprotan antiseptik dan pelapis antimikroba untuk perangkat medis yang mensterilkan udara dan permukaan (Fabiani et al., 2019). Ukuran silver dalam skala nano menjadi pertimbangan penting karena dapat meningkatkan reaktivitas (Chuchita et al., 2018) dan luas permukaan silver sehingga meningkatkan aktivitas antibakteri (Kędziora et al., 2018). Nanosilver memiliki efek antibakteri yang luas pada berbagai bakteri gram negatif dan gram positif dan strain bakteri resisten antibiotik (Ge et al, 2014). Kemampuan antimikroba nanosilver ini belum dilaporkan adanya mikroba yang resisten terhadap silver (Ariyanta et al., 2014).
Nanosilver dapat disintesis menggunakan metode kimia, fisika dan biologi (Firdhouse dan Lalitha, 2015). Metode reduksi kimia dipilih karena merupakan metode yang mudah, cepat dan murah (Oktaviani et al., 2015). Pada sintesis nanosilver dengan metode reduksi kimia biasanya menggunakan zat pereduksi kimia cenderung beracun (Chuchita et al., 2018), tidak ramah lingkungan, mahal, dan tidak cocok untuk aplikasi biologis. Sehingga reduktor yang diperoleh dari tumbuhan dapat menjadi alternatif karena lebih tidak beracun murah, ramah lingkungan (Firdhouse dan Lalitha, 2015) serta dapat bertindak sebagai capping atau stabilizing agent (Khan et al., 2018). Bioreduktor dapat diperoleh dari tumbuhan yang metabolit sekundernya mengandung senyawa antioksidan
2
(Prasetiowari et al., 2018) seperti, flavonoid, saponin, tanin (Wendri et al., 2017), dan terpenoid, karena memiliki gugus fungsi yang mampu mendonorkan elektron (Massake et al., 2015)
Penggunaan bioreduktor dari tumbuhan dalam sintesis nanosilver sudah banyak dilakukan, diantaranya dengan ekstrak daun sambiloto (Wendri et al., 2017), daun belimbing wuluh (Prasetiowati et al., 2018), daun pelawan (Fabiani et al., 2019). Menurut penelitian Hasim et al. (2015) daun singkong memiliki memiliki aktivitas antioksidan karena mengandung senyawa polifenol seperti flavonoid dan tanin. Oleh sebab itu, daun singkong dapat digunakan sebagai bioreduktor dalam sintesis nanosilver. Flavonoid yang terkandung pada daun singkong yaitu clovin, rutin, narcissin dan nikotiflorin. Rutin dapat menjadi penanda karena kandungannya tertinggi pada daun singkong (Tao et al., 2019).
Senyawa polifenol memiliki potensial reduksi yang berbeda-beda. Flavonoid yang paling baik dalam mereduksi perak adalah rutin (+0,26 V) dan kuersetin (+0,23 V) karena memiliki potensial reduksi dibawah perak (+0,80 V) dan paling rendah dibandingkan jenis flavonoid lainnya (Terenteva et al., 2015). Selain itu, tanin memiliki potensial reduksi +0,605 (Ranoszek-Soliwoda et al., 2017). Sedangkan ion Ag+ memiliki potensial reduksi yang lebih besar dari
flavonoid dan tanin +0,80. Semakin besar nilai potensial reduksi suatu senyawa maka semakin mudah mengalami reduksi dan sebaliknya (Nasution, 2019). Sehingga flavonoid dan tanin dapat mereduksi ion Ag+ (Sari et al., 2017).
Pada sintesis nanosilver, perak nitrat (AgNO3) digunakan sebagai
prekursor karena memiliki kelarutan yang tinggi pada air (Fabiani et al, 2019), harganya lebih murah dan stabilitasnya paling stabil dibandingkan garam perak lainnya (Ge et al, 2014). Konsentrasi AgNO3 dapat mempengaruhi ukuran
nanosilver yang terbentuk (Prasetiowati et al., 2018). Dimana ketika konsentrasi AgNO3 terlalu tinggi maka agen pereduksi tidak dapat mereduksi Ag+ sepenuhnya.
Akibatnya, ukuran partikel nanosilver yang terbentuk besar (Ahmad et al.,2018). Ukuran partikel nanosilver sangat penting, karena semakin kecil ukuran partikelnya maka semakin besar aktivitas antibakterinya (Ariyanta et al., 2014). Ukuran partikel nanosilver dapat diperkirakan melalui pengukuran panjang
3
gelombang dan dapat menandakan terbentuknya nanosilver (Prasetiowati et al., 2018). Selain itu, nilai % transmitan yang mendekati 100% juga menandakan bahwa nanosilver yang terbentuk sudah berukuran nanometer (Huda dan Wahyuningsih, 2018). Ukuran partikel nanosilver dapat dikontrol dengan mengoptimasi faktor yang mempengaruhinya yaitu konsentrasi garam perak dan konsentrasi agen pereduksi (ekstrak) (Prasetiowati et al., 2018). Dimana, konsentrasi AgNO3 dan ekstrak harus seimbang agar Ag+ dan reduktor yang
tersedia dapat bereaksi semua (Ahmad et al.,2018).
Pada penelitian ini optimasi dilakukan menggunakan Central Composite Design (CCD). CCD merupakan salah satu metode response surface (Riswanti et al, 2019). CCD digunakan untuk merancang percobaan yang akan dievaluasi faktor dan responnya (panjang gelombang dan niali % transmitan) untuk mendapatkan formula sintesis nanosilver yang optimal. CCD memiliki jumlah percobaan yang lebih sedikit dengan level yang lebih banyak dibandingkan dengan desain faktorial sehingga dapat menghemat waktu, tenaga dan biaya (Riswanto et al., 2019).
Penelitian ini bertujuan mendapatkan formula dan area optimum sintesis nanosilver dari faktor yang dioptimasi menggunakan CCD. Faktor tersebut adalah konsentrasi AgNO3 sebagai oksidator dan ekstrak air daun singkong sebagai
bioreduktor. Sampai saat ini belum ada laporan mengenai pengaruh variasi konsentrasi ekstrak air daun singkong sebagai bioreduktor dan AgNO3 pada sintesis
nanosilver. Oleh karena itu, optimasi formula sintesis nanosilver dengan bioreduktor ekstrak daun singkong perlu dilakukan.
METODE PENELITIAN Jenis dan Rancangan Penelitian
Penelitian tentang optimasi formula sintesis nanosilver dengan bioreduktor ekstrak daun singkong merupakan jenis kuasi eksperimental menggunakan rancangan central composite design (CCD)
4 Alat dan Bahan
Alat-alat gelas (PYREX), vortex (Thermo), magnetic stirrer, hotplate (Thermo), spektrofotometer doeble beam UV-Vis (Shimadzu UV-Vis 1800), timbangan analitik (Mettler Toledo), pipet pump, mikropipet, sentrifugator (Thermo), water purificator (Thermo), blue tip, lampu UV 366 dan 254 nm, pipa kapiler, penggaris, chamber.
Bahan yang digunakan dalam penelitian adalah daun singkong, perak nitrat (AgNO3,) dari Merck (pro analyst grade), aqubidest, standar rutin, butanol,
asam asetat, aquadest, silika gel 60 GF254.
Determinasi tanaman
Determinasi tanaman daun singkong dilakukan oleh bagian Laboratorium Biologi Farmasi Fakultas Farmasi Universitas Gadjah Mada Yogyakarta.
Ekstrak air daun singkong
Daun singkong dari Lembaga Pendampingan Usaha Buruh Tani dan Nelayan (LPUBTN) sebanyak 1 Kilogram dicuci bersih dengan air mengalir. Daun segar tersebut diambil bagian daunnya saja. Daun singkong disimpan pada kulkas dengan suhu 6 oC selama 2 minggu. Setelah 2 minggu daun singkong dikeluarkan dari kulkas dalam keadaan layu dan bearoma tidak sedap.
Ekstraksi daun singkong menggunakan metode infundasi yang mengacu pada Hasim et al. (2015) yang dimodifikasi. Daun singkong yang sudah disimpan 2 minggu dipotong-potong sekitar 2 cm. Selanjutnya daun tersebut ditimbang lalu ditambahkan aquabidest 100 mL, dan dipanaskan dengan penangas air pada suhu 90 ºC selama 15 menit (terhitung sejak suhu mencapai 90 ºC) sambil diaduk dengan batang pengaduk. Hasil ekstraksi yang diperoleh kemudian disaring dengan kertas saring.
5
Tabel I. Konsentrasi dan Jumlah Penimbangan Ekstrak Air Daun Singkong Konsentrasi (%b/v) Jumlah (gram) Volume (mL)
9.17 9.17 100
11.57 11.57 100
17.36 17.36 100
23.15 23.15 100
25.55 25.55 100
Uji kualitatif flavonoid rutin dengan metode KLT
Fase gerak yang digunakan adalah butanol: asam asetat: air (4:1:5) dan fase diam yang digunakan yaitu silika gel 60 GF254 yang berukuran 6x10 cm yang
ditandai dengan jarak 2 cm pada batas bawah dan jarak elusi 8 cm dari batas bawah. Kemudian sampel dan pembanding rutin ditotolkan dengan pipa kapiler di batas bawah pada plat KLT GF254 tersebut. Selanjutnya dimasukkan kedalam chamber
dan dielusikan dengan fase gerak sampai tanda batas. Lalu angkat plat KLT dan diamati secara visible di bawah sinar UV 254 nm dan 366 nm lalu nilai Rf ditentukan. (Sari dan Meitisia, 2017).
Rancangan optimasi formula sintesis nanosilver Tabel II. Formula Sintesis Nanosilver
Formula Level rendah Level tinggi
AgNO3 (mM) 1 2
6
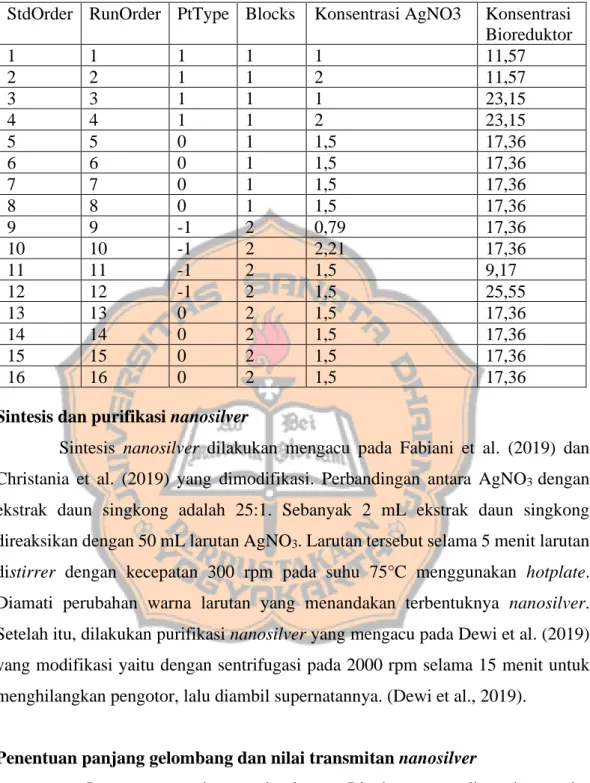
Tabel III. Rancangan Penelitian Optimasi Sintesis Nanosilver 2 Faktor 5 Level Menggunakan CCD StdOrder RunOrder PtType Blocks Konsentrasi AgNO3 Konsentrasi
Bioreduktor 1 1 1 1 1 11,57 2 2 1 1 2 11,57 3 3 1 1 1 23,15 4 4 1 1 2 23,15 5 5 0 1 1,5 17,36 6 6 0 1 1,5 17,36 7 7 0 1 1,5 17,36 8 8 0 1 1,5 17,36 9 9 -1 2 0,79 17,36 10 10 -1 2 2,21 17,36 11 11 -1 2 1,5 9,17 12 12 -1 2 1,5 25,55 13 13 0 2 1,5 17,36 14 14 0 2 1,5 17,36 15 15 0 2 1,5 17,36 16 16 0 2 1,5 17,36
Sintesis dan purifikasi nanosilver
Sintesis nanosilver dilakukan mengacu pada Fabiani et al. (2019) dan Christania et al. (2019) yang dimodifikasi. Perbandingan antara AgNO3 dengan
ekstrak daun singkong adalah 25:1. Sebanyak 2 mL ekstrak daun singkong direaksikan dengan 50 mL larutan AgNO3. Larutan tersebut selama 5 menit larutan
distirrer dengan kecepatan 300 rpm pada suhu 75°C menggunakan hotplate. Diamati perubahan warna larutan yang menandakan terbentuknya nanosilver. Setelah itu, dilakukan purifikasi nanosilver yang mengacu pada Dewi et al. (2019) yang modifikasi yaitu dengan sentrifugasi pada 2000 rpm selama 15 menit untuk menghilangkan pengotor, lalu diambil supernatannya. (Dewi et al., 2019).
Penentuan panjang gelombang dan nilai transmitan nanosilver
a. Penentuan panjang gelombang. Blanko yang digunakan yaitu aquabidest. Dilakukan pemindaian larutan sampel nanosilver yang telah dipurifikasi (Massake et al, 2015) pada rentang 400-450 nm menggunakan spektrofotometer UV-Vis (Sari et al, 2017)
7
b. Penentuan nilai transmitan. Sebanyak 100 µl larutan sampel ditambahkan 5 mL aquabidest lalu di vortex selama 1 menit. Larutan tersebut diukur absorbansinya pada panjang gelombang maksimal dengan blanko aquabidest. (Huda dan Wahyuningsih, 2018).
Optimasi dan Analisis Data
Proses optimasi dengan rancangan CCD (2 faktor dan 5 level) dan analisis data dengan ANOVA dengan taraf kepercayaan 95% dilakukan menggunakan aplikasi minitab17.
HASIL DAN PEMBAHASAN Hasil determinasi tanaman singkong
Determinasi dilakukan pada daun singkong yang diperoleh dari Lembaga Pendampingan Usaha Buruh Tani dan Nelayan (LPUBTN), Desa Pandowoharjo, Sleman DIY. Tanaman tersebut dideterminasi di Departemen Biologi Farmasi, Fakultas Farmasi, Universitas Gadjah Mada Yogyakarta. Hasil determinasi yang diperoleh menunjukkan bahwa tanaman singkong yang digunakan dalam penelitian sesuai dengan tanaman yang di maksud yaitu tanaman singkong (Manihot esculenta Crantz) (Lampiran. 1).
Ekstrak air daun singkong
Ekstrak dibuat dengan metode infundasi. Infundasi merupakan proses penyarian yang umumnya digunakan untuk menyari zat kandungan aktif yang larut dalam air. Infundasi dipilih karena sering digunakan dan sederhana (Oktavia et al., 2020). Air merupakan pelarut yang bersifat polar. Pertimbangan air dipakai sebagai pelarut karena air mudah diperoleh, murah dan stabil (Yohanes et al., 2018). Selain itu, daun singkong mengandung flavonoid rutin (Hasim, et al., 2015), saponin dan tanin (Pratiwi, 2016) yang larut dalam air. Sehingga metode infundasi cocok digunakan untuk mendapatkan senyawa-senyawa tersebut. Kandungan senyawa terbesar di ekstrak air daun singkong adalah flavonoid rutin (Tao et al., 2019),
8
sehingga flavonoid rutin digunakan sebagai perwakilan senyawa pada ekstrak ini sebagai bioreduktor sintesis nanosilver.
Hasil uji KLT ekstrak air daun singkong
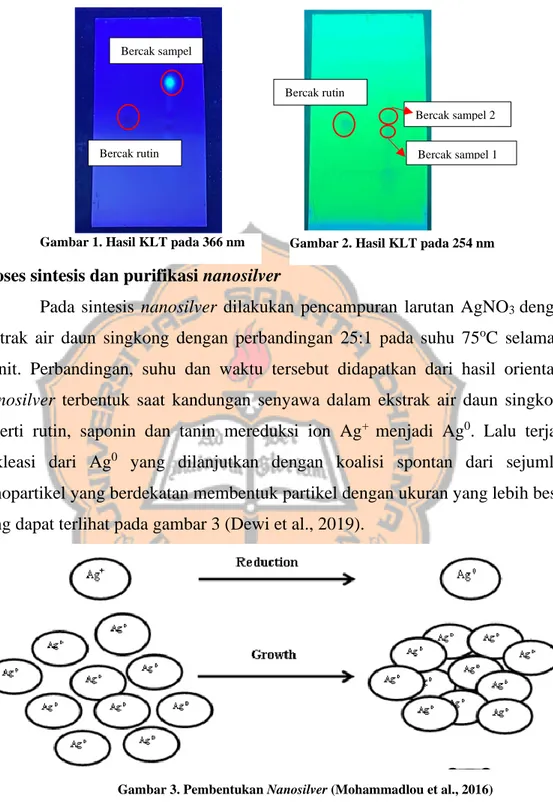
KLT merupakan metode pemisahan komponen kimia dengan prinsip adsorbs dan partisi yang ditentukan oleh fase diam dan fase gerak (Alen et al., 2017). Uji KLT ini untuk memastikan adanya flavonoid rutin pada ekstrak air daun singkong. Pada uji ini fase diam yang digunakan adala silika 60 GF254 dan fase gerak yang digunakan butanol: asam asetat: air (4:1:5) serta baku pembanding yang digunakan adalah standar rutin 0,1%. Hasil plat KLT yang diamati pada lampu UV 254 nm pada gambar 1 terlihat bahwa ekstrak daun singkong memiliki 2 bercak. Jarak migrasi standar rutin adalah 4 cm sedangkan jarak migrasi sampel bercak pertama adalah 3,5 cm dan bercak kedua 4,15 cm. Nilai Rf standar rutin 0,5 dan nilai Rf sampel bercak pertama yaitu 0,43 dan bercak kedua yatu 0,52. Sedangkan jika dilihat pada lampu UV 366 nm pada gambar 2 terdapat bercak yang berpendar pada ekstrak namun tidak berpendar pada rutin dengan jarak migrasi 6,6 cm dan nilai Rf 0,83. Nilai Rf tersebut diperoleh dengan rumus sebagai berikut:
𝑅𝑓 = 𝑗𝑎𝑟𝑎𝑘 𝑚𝑖𝑔𝑟𝑎𝑠𝑖 𝑎𝑛𝑎𝑙𝑖𝑡 𝑗𝑎𝑟𝑎𝑘 𝑚𝑖𝑔𝑟𝑎𝑠𝑖 𝑒𝑙𝑢𝑒𝑛
(Wulandari, 2011) Dilihat dari jarak elusi dan nilai Rf standar rutin dan ekstrak dapat disimpulkan bahwa rutin tidak dapat terdeteksi pada ekstrak air daun singkong. Hal ini karena jarak elusi rutin dan ekstrak yang cukup jauh. Kemungkinan hal tersebut terjadi karena kandungan rutin yang kecil pada ekstrak air daun singkong sehingga sulit terdeteksi menggunakan KLT. Sehingga disarankan untuk menggunakan metode HPLC (high performance liquid chromatography) dalam mendeteksi
9 Proses sintesis dan purifikasi nanosilver
Pada sintesis nanosilver dilakukan pencampuran larutan AgNO3 dengan
ekstrak air daun singkong dengan perbandingan 25:1 pada suhu 75oC selama 5 menit. Perbandingan, suhu dan waktu tersebut didapatkan dari hasil orientasi. Nanosilver terbentuk saat kandungan senyawa dalam ekstrak air daun singkong seperti rutin, saponin dan tanin mereduksi ion Ag+ menjadi Ag0. Lalu terjadi
nukleasi dari Ag0 yang dilanjutkan dengan koalisi spontan dari sejumlah
nanopartikel yang berdekatan membentuk partikel dengan ukuran yang lebih besar yang dapat terlihat pada gambar 3 (Dewi et al., 2019).
Gambar 3. Pembentukan Nanosilver (Mohammadlou et al., 2016)
Perubahan warna menjadi kuning kecoklatan dapat menjadi tanda terbentuknya nanosilver karena perubahan warna merupakan fenomena dari surface plasmon resonance dan reduksi ion Ag+ (Dewi et al., 2019). Surface plasmon resonance (SPR) merupakan fenomena pergerakan awan elektron yang
Bercak sampel
Bercak rutin Bercak sampel 1
Bercak sampel 2 Bercak rutin
10
dipengaruhi oleh adanya penyinaran pada koloid nanokomposit, biasanya disebut juga dengan fenomena resonansi osilasi (Rahmayani et al., 2019). Larutan nanosilver yang terbentuk menggunakan bioreduktor ekstrak air daun singkong berwarna kuning kecoklatan seperti pada Gambar 4. Larutan tersebut memiliki panjang gelombang diantara 400-450 nm. Hal tersebut dikarenakan jumlah bioreduktor yang tersedia telah mencukupi untuk mereduksi ion Ag (Chuchita et al., 2018).
Larutan yang berwarna coklat pucat seperti Gambar 5 menghasilkan panjang gelombang dibawah 400 nm. Menurut Saputra (2011), pada panjang gelombang dibawah 400 nm yang terbentuk masih Ag+ yang dapat diartikan bahwa proses reduksi kimia belum berjalan sempurna. Larutan berwarna coklat pekat sampai hitam seperti Gambar 6 menghasilkan panjang gelombang diatas 450 nm. Hal tersebut dikarenakan jumlah bioreduktor yang tersedia melebihi ion Ag+ yang tersedia sehingga Ag+ yang tereduksi sangat cepat dan menyebabkan terjadinya aglomerasi yang mengakibatkan nanosilver yang dihasilkan memiliki ukuran partikel yang besar (Chuchita et al., 2018)
Gambar 4. Hasil Nanosilver 400-450 nm
11
Purifikasi nanosilver dilakukan dengan sentrifugasi pada 2000 rpm selama 15 menit. Endapan yang terbentuk merupakan pengotor dan yang diambil adalah bagian supernatan (Dewi et al., 2019) (Lampiran 6). Selanjutnya supernatant tersebut digunakan untuk karakterisasi nanosilver. Setelah dilakukan purifikasi terjadi pergeseran panjang gelombang yang lebih panjang namun masih memenuhi target. Dilihat dari hasil uji PSA rata-rata ukuran nanosilver untuk center point (percobaan 5) sebelum dan sesudah purifikasi memiliki ukuran yang mirip (Lampiran 9). Namun panjang gelombang sebelum dan sesudah purifikasi berbeda (Lampiran 7), Menurut hasil penelitian yang pernah dilakukan Solomon et al., (2007) terkait hubungan panjang gelombang dengan ukuran partikel, dapat disimpulkan bahwa panjang gelombang yang sesuai dengan ukuran partikelnya adalah panjang gelombang sesudah purifikasi. Sehingga dapat dikatakan purifikasi yang dilakukan telah mendapatkan nanosilver yang murni.
Hasil panjang gelombang dan %T
Karakterisasi nanosilver dapat dilakukan dengan pengukuran panjang gelombang. Nanopartikel perak dapat berinteraksi secara kuat dengan panjang gelombang tertentu dari cahaya dan sifat optis unik dari material tersebut merupakan dasar dari sifat plasmonik (Ronson, 2012). Serapan absorbansi pada panjang gelombang 400-450 nm merupakan SPR nanosilver. Jika serapan absorbansi yang terbaca dibawah 400 nm merupakan panjang gelombang ion perak yang menandakan bahwa proses reduksi ion perak belum berjalan sempurna (Dewi
12
et al., 2019). Koloid nanosilver memiliki warna yang berbeda-beda berdasarkan pada absorbsi cahaya dan pancaran pada daerah cahaya tampak, frekuensi pada getaran konduksi elektron-elektron yang menjadi respon terhadap medan listrik hasil radiasi elektromagnetik. Namun, hanya elektron bebas yang memiliki resonansi plasmon pada spektrum cahaya tampak yang bisa memberikan warna yang baik (Apriandanu et al., 2014).
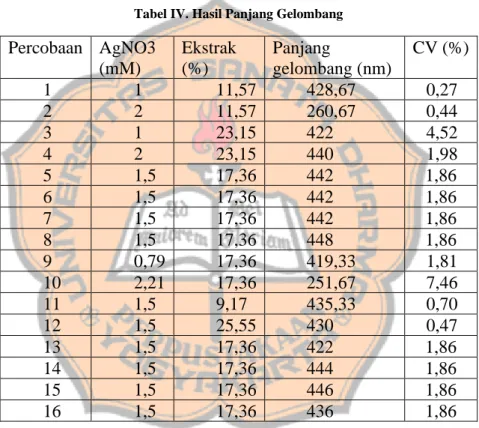
Pada penelitian ini percobaan direplikasi 2 kali (Lampiran 7). Berikut hasil rata-rata panjang gelombang:
Tabel IV. Hasil Panjang Gelombang Percobaan AgNO3 (mM) Ekstrak (%) Panjang gelombang (nm) CV (%) 1 1 11,57 428,67 0,27 2 2 11,57 260,67 0,44 3 1 23,15 422 4,52 4 2 23,15 440 1,98 5 1,5 17,36 442 1,86 6 1,5 17,36 442 1,86 7 1,5 17,36 442 1,86 8 1,5 17,36 448 1,86 9 0,79 17,36 419,33 1,81 10 2,21 17,36 251,67 7,46 11 1,5 9,17 435,33 0,70 12 1,5 25,55 430 0,47 13 1,5 17,36 422 1,86 14 1,5 17,36 444 1,86 15 1,5 17,36 446 1,86 16 1,5 17,36 436 1,86
Berdasarkan tabel hasil panjang gelombang nanosilver diatas dapat dilihat bahwa hampir semua percobaan memenuhi target panjang gelombang nanosilver yaitu 400-450 nm (Dewi et al., 2019). Pada percobaan ke 2 dan 10 panjang gelombang yang terbaca tidak memenuhi target. Hal ini terjadi karena konsentrasi garam peraknya lebih besar dari pada konsentrasi ekstrak (bioreduktor) sehingga menurut Chuchita et al. (2018), apabila reduktor yang tersedia jumlahnya belum mencukupi untuk mereduksi Ag+ menjadi Ag0 maka nanosilver yang dihasilkan sangat sedikit. Selain itu, menurut Saputra (2011), pada panjang gelombang
13
dibawah 400 nm yang terbentuk masih Ag+ yang dapat diartikan bahwa proses reduksi kimia belum berjalan sempurna.
Pada penelitian ini dilakukan replikasi 2 kali pada percobaan 1-4 dan 9-4 untuk mengurangi kemungkinan terjadinya kesalahan acak. Dari replikasi tersebut didapatkan nilai CV. Nilai CV dikatakan memenuhi syarat apabila < 10% yang artinya data memiliki presisi yang tinggi untuk setiap replikasinya (Couto et al., 2013). CV yang didapatkan pada semua percobaan memenuhi syarat sehingga dapat di katakan data yang didapatkan presisi. Namun, dapat di lihat pada tabel IV, CV yang didapatkan bervariasi. Hal tersebut dikarenakan sulit mendapatkan kondisi suhu setiap percobaan yang konstan sehingga akan mempengaruhi panjang gelombang setiap replikasinya. Pada penelitian yang dilakukan Dewi et al. (2019), peningkatan suhu akan mempengaruhi ukuran partikel yang nantinya akan berpengaruh ke panjang gelombang. Meskipun demikian, hasil yang didapakan memenuhi target panang gelombang nanosilver yaitu 400-450 nm (Dewi et al., 2019)
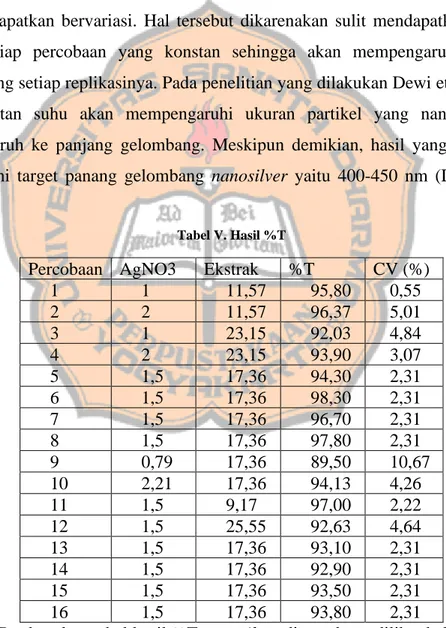
Tabel V. Hasil %T
Percobaan AgNO3 Ekstrak %T CV (%)
1 1 11,57 95,80 0,55 2 2 11,57 96,37 5,01 3 1 23,15 92,03 4,84 4 2 23,15 93,90 3,07 5 1,5 17,36 94,30 2,31 6 1,5 17,36 98,30 2,31 7 1,5 17,36 96,70 2,31 8 1,5 17,36 97,80 2,31 9 0,79 17,36 89,50 10,67 10 2,21 17,36 94,13 4,26 11 1,5 9,17 97,00 2,22 12 1,5 25,55 92,63 4,64 13 1,5 17,36 93,10 2,31 14 1,5 17,36 92,90 2,31 15 1,5 17,36 93,50 2,31 16 1,5 17,36 93,80 2,31
Berdasarkan tabel hasil %T nanosilver diatas dapat dilihat bahwa hampir semua percobaan memenuhi target %T nanosilver yaitu 91-99% (Huda dan Wahyuningsih, 2018; Deng et al., 2019). Pada percobaan ke 9, %T tidak memenuhi
14
target. Hal ini terjadi karena pada replikasi ke 1 pada pecobaan tersebut nilai %T jauh di bawah target yaitu 78,5% sedangkan replikasi lainnya memenuhi target. Sehingga saat dirata-rata hasil yang didapatkan dibawah target. Perbedaan %T yang didapatkan pada setiap replikasi dikarenakan sulit untuk mendapatkan suhu yang konstan. Suhu dapat mempengaruhi jumlah nanosilver yang terbentuk, dimana semakin tinggi suhu maka reaksi pembentukan nanosilver semakin cepat dan yang terbentuk akan semakin banyak (Lestari et al., 2019). Nilai absorbansi menunjukkan jumlah nanosilver yang terbentuk (Lestari et al., 2019), dimana semakin banyak nanosilver yang terbentuk maka nilai absorbansi akan tinggi, sedangkan nilai %T berbanding terbalik dengan absorbansi (Prasetiowati et al., 2018; Abdassah, 2017).
Nilai CV dikatakan memenuhi syarat apabila < 10% yang artinya data memiliki presisi yang tinggi untuk setiap replikasinya (Couto et al., 2013). CV yang didapatkan pada semua percobaan memenuhi syarat sehingga dapat di katakan data yang didapatkan presisi. Namun, dapat dilihat pada tabel IV, CV yang didapatkan bervariasi. Meskipun demikian, hasil yang didapatkan memenuhi target %T nanosilver yaitu 91-99% (Huda dan Wahyuningsih, 2018; Deng et al., 2019)
Hasil optimasi menggunakan rancangan CCD
Rancangan CCD pada penelitian ini digunakan untuk mengoptimasi dua faktor yaitu konsentrasi AgNO3 dan Ekstrak air daun singkong. Respon yang dilihat
adalah panjang gelombang dan %T. Rancangan CCD ini memiliki 16 run percobaan. Hasil data percobaan akan dianalisis menggunakan software Minitab 17 (Minitab, Inc, State College, PA, USA). Respon akan dievaluasi menggunakan analisis statistik ANOVA.
Model berpengaruh nyata atau signifikan jika memiliki nilai F-value>P-value dan P-F-value>P-value <0,005 (Chowdhury et al., 2016). Dari gambar 8 dapat dilihat bahwa model berpengaruh nyata atau signifikan terhadap respon tersebut secara statistik dimana memiliki P-value kurang dari 0,05 yaitu 0,000 dan F-value yang lebih besar dari P-value yaitu 14,48. Sehingga model ini dapat digunakan sebagai model optimasi. Persamaan regresi model panjang gelombang sebagai berikut:
15
453 + 242 AgNO3 – 17,6 Ekstrak – 205,7 AgNO32 – 0,085 Ekstrak2
+ 16.06 AgNO3.Ekstrak (1)
Nilai R2 yang mendekati ≥ 80% menunjukkan pengaruh variabel bebas yang signifikan terhadap respon (Purba et al., 2019). Nilai R2 yang didapatkan yaitu 90,62% yang menunjukkan bahwa faktor konsentrasi AgNO3 dan konsentrasi
ekstrak air daun singkong memberikan pengaruh sebesar 90,62% pada nilai respon panjang gelombang sedangkan sebesar 9,38% dipengaruhi faktor lain yang tidak digunakan pada model ini. Sehingga dapat disimpulkan faktor yang digunakan berpengaruh signifikan terhadap respon.
Uji lack of fit bertujuan untuk menunjukkan kesesuaian antara data yang didapatkan dari eksperimental dengan hasil data model. Uji ini dilihat dari hasil replikasi center point. Pada penelitian ini center point direplikasi sebanyak 8 kali, replikasi center point ini bertujuan untuk menyelidiki kesalahan (error) dari eksperimental (Park et al., 2012). Namun pada uji Lack of fit didapatkan P-value yang signifikan yaitu 0,001 yang menandakan bahwa data respon yang didapat tidak sesuai dengan respon yang diprediksi model (Hendrawan et al., 2016). Meskipun demikian hasil eksperimental menunjukkan sebanyak 14 percobaan memiliki panjang gelombang yang memenuhi target panjang gelombang nanosilver yaitu 400-450 nm (Dewi et al., 2019), sehingga model ini tetap dapat digunakan dalam penelitian ini (Lampiran 11).
16
Gambar 7. Contour Plot Respon Panjang Gelombang vs Ekstrak, AgNO3
Gambar 8. Surface Plot Respon Panjang Gelombang vs Ekstrak, AgNO3
Metode RSM memberikan penjelasan yang lebih rinci tentang pengaruh kedua variabel bebas yang digunakan yaitu dan efek interaksinya terhadap respon. Pada RSM terdapat Contour plot (2D) dan Surface Plot (3D). Gambar 8 menunjukkan gambaran secara 3D interaksi antara variabel bebas dengan respon. Gambar 7 merupakan contour plot yang merupakan gambaran interkasi variabel bebas dan respon secara 2D (Ahani and Khatibzadeh, 2017), dari plot tersebut menunjukkan bahwa area optimum konsentrasi AgNO3 terhadap respon panjang
gelombang yaitu terletak pada area berwarna kuning. Hal tersebut karena pada area tersebut didapatkan panjang gelombang nanosilver yang memenuhi target yaitu 400-450 nm (Dewi et al., 2019). AgNO3 Ek st ra k 2.00 1.75 1.50 1.25 1.00 24 22 20 18 16 14 12 10 > – – – – – < 200.0 200.0 250.0 250.0 300.0 300.0 350.0 350.0 400.0 400.0 450.0 450.0 gelombangpanjang
Contour Plot of panjang gelombang vs Ekstrak, AgNO3
G F E D C B A 0.79 9.25
17
Pada gambar 11 dilihat bahwa model berpengaruh nyata atau signifikan secara statistic terhadap %T dimana memiliki P-value kurang dari 0,05 yaitu 0,010 dan F-value yang lebih besar dari P-value yaitu 5,75. Nilai R2 yang didapatkan yaitu 79,31% menunjukkan bahwa faktor konsentrasi AgNO3 dan konsentrasi ekstrak air
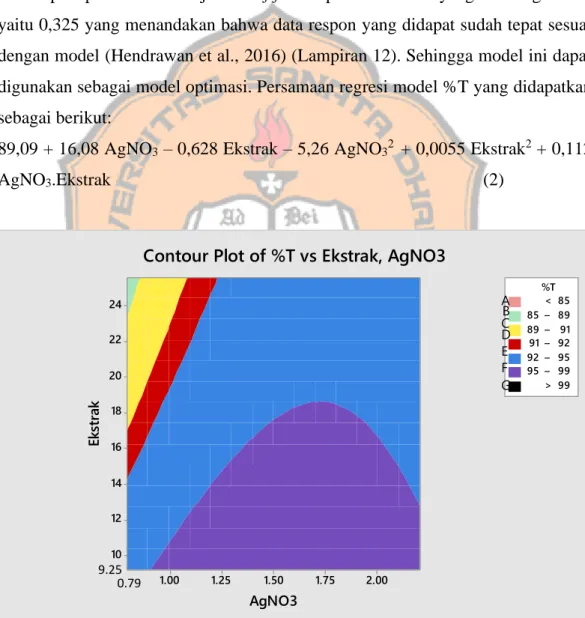
daun singkong memberikan pengaruh sebesar 79,31% pada nilai respon panjang gelombang dan sebesar 20,69% dipengaruhi faktor lain yang tidak digunakan pada model ini. Sehingga dapatkan dikatakan faktor yang digunakan cukup berpengaruh terhadap respon %T. Pada uji Lack of fit didapatkan P-value yang tidak signifikan yaitu 0,325 yang menandakan bahwa data respon yang didapat sudah tepat sesuai dengan model (Hendrawan et al., 2016) (Lampiran 12). Sehingga model ini dapat digunakan sebagai model optimasi. Persamaan regresi model %T yang didapatkan sebagai berikut:
89,09 + 16,08 AgNO3 – 0,628 Ekstrak – 5,26 AgNO32 + 0,0055 Ekstrak2 + 0,112
AgNO3.Ekstrak (2)
Gambar 9. Contour Plot Respon %T vs Ekstrak, AgNO3
AgNO3 Ek st ra k 2.00 1.75 1.50 1.25 1.00 24 22 20 18 16 14 12 10 > – – – – – < 85 85 89 89 91 91 92 92 95 95 99 99 %T
Contour Plot of %T vs Ekstrak, AgNO3
A B C G F E D 0.79 9.25
18
Gambar 10. Surface Plot Respon %T vs Ekstrak, AgNO3
Berdasarkan gambar 9 diatas dapat disimpulkan bahwa area optimum respon %T terletak pada area yang berwarna merah biru dan ungu. Hal tersebut karena pada area tersebut didapatkan respon yang memenuhi target yaitu 91-99% (Huda dan Wahyuningsih, 2018; Deng et al., 2019). Konsentrasi AgNO3 dan
ekstrak air daun singkong yang ada pada area tersebut merupakan pasangan konsentrasi yang memenuhi target. Sedangkan konsentrasi yang berada pada luar daerah tersebut merupakan pasangan konsentrasi yang tidak memenuhi target.
Gambar 11. Area superimposed contour plot
0.79 9.25
19
Gambar 12. Solusi Formula Optimum
Pada gambar 11 area yang berwarna putih menunjukkan area superimposed contour plot yang merupakan area irisan dari contour plot respon panjang gelombang dengan %T. Area tersebut merupakan area optimum konsentrasi AgNO3 dan ekstrak air daun singkong dengan respon panjang
gelombang dan %T yang memenuhi target. Pada gambar 12 menunjukkan bahwa solusi formula optimum sintesis nanosilver yang diberikan model RSM adalah pada konsentrasi AgNO3 1,64 mM dan konsentrasi ekstrak air daun singkong 17,61%.
Pada prediksi formula opitmum tersebut akan menghasilkan panjang gelombang 424,75 nm dan %T 95,20%. Nilai desirability atau ketepatan hasil solusi formula optimum tersebut yaitu 0,9703. Nilai desirability yang baik adalah mendekati 1 yang menandakan semakin tinggi nilai ketepatan solusi formula dengan respon target yang diinginkan (Nurmiah et al., 2013). Sehingga dapat disimpulkan bahwa solusi formula optimum tersebut memiliki ketepatan yang tinggi untuk mengahsilkan respon target.
Dari area formula optimum dipilih 2 formula optimum terdapat pada rancangan. Berdasarkan persamaan regresi model optimasi yang didapatkan kedua formula tersebut memiliki panjang gelombang dan %T yang memenuhi target. Kedua formula tersebut dipilih karena memiliki konsentrasi AgNO3 dan ekstrak air
20
Sehingga lebih efisien dalam bahan yang digunakan dan semakin kecil untuk terjadi interaksi yang tidak diinginkan. Kedua formula optimum dan hasil prediksi responnya dapat dilihat pada Tabel VI.
Tabel VI. Formula optimum dan prediksi responnya Formula Konsentrasi AgNO3 Konsentrasi ekstrak Panjang gelombang (nm) %T Solusi 1,64 mM 17,61%. 424,75 95,20 1 1,5 17,36 440,22 95,05 2 1,5 9,17 405,54 97,62 KESIMPULAN
1. Didapatkan area optimum formula sintesis nanosilver menggunakan metode Central Composite Design (CCD)
2. Didapatkan 3 formula optimum sintesis nanosilver yang terdiri dari solusi formula optimum yang didapatkan dengan model RSM dan 2 formula dari rancangan percobaan.
SARAN
1. Perlu dilakukan penelitian lebih lanjut terkait hubungan % Transmitan dengan ukuran partikel nanosilver yang terbentuk.
2. Mendeteksi senyawa rutin dalam ekstrak air daun singkong menggunakan metode HPLC (high performance liquid chromatography)
3. Sebaiknya ekstrak dibuat dalam 1 konsentrasi yang dapat diencerkan untuk mendapatkan variasi konsentrasi
4. Perlu dilakukan validasi terhadap solusi formula optimum yang didapatkan
5. Perlu diperhatikan untuk tahapan kritis dalam sintesis nanosilver yaitu pengendalian suhu selama proses sinesis supaya konstan
21 DAFTAR PUSTAKA
Abdassah, M., 2017. Nanopartikel dengan Gelasi Ionik. Farmaka, 15(1), 45–52. Ahani, M., Khatibzadeh, M., 2017. Optimisation of significant parameters through
Response surface methodology in the synthesis of silver nanoparticles by chemical reduction method. Micro and Nano Letters, 12(9), 705–710.
Ahmad, N., Ang, B.C., Amalina, M.A., Bong, C.W., 2018. Influence of Precursor Concentration and Temperature on The Formation of Nanosilver in Chemical Reduction Method. Sains Malaysiana, 47(1), 157–168.
Alen, Y., Agresa, F.L., YUliandra, Y., 2017. Analisis Kromatografi Lapis Tipis (KLT) dan Aktivitas Antihiperurisemia Ekstrak Rebung Schizostachyum brachycladum Kurz (Kurz) pada Mencit Putih Jantan. Jurnal Sains Farmasi dan Klinis, 3(2), 146–152.
Apriandanu, D.O.B., Wahyuni, S., Hadisaputro, S., Harjono, 2014. Sintesis Nanopartikel Perak Menggunakan Metode Poliol Dengan Agen Stabilisator Polivinilalkohol (Pva). Jurnal MIPA, 36(2).
Ariyanta, H.A., Wahyuni, S., Priatmoko, S., 2014. Preparasi Nanopartikel Perak dengan Metode Reduksi dan Aplikasinya Sebagai Antibakteri Penyebab Infeksi. Indonesian Journal of Chemical Science, 3(1), 1–6.
Chowdhury, S., Yusof, F., Faruck, M.O., Sulaiman, N., 2016. Process Optimization of Silver Nanoparticle Synthesis Using Response Surface Methodology. Procedia Engineering, 148, 992–999.
Christania, F.S., Dwiastuti, R., Yuliani, S.H., 2019. Lipid and Silver Nanoparticles Gels Formulation Of Tempeh Extract. Jurnal Farmasi Sains dan Komunitas, 16(2), 56–62.
Chuchita, Santoso, S.., Suyanta, 2018. Sintesis Nanopartikel dari Perak Nitrat dengan Tirosin Sebagai Reduktor dan Agen Pengkaping untuk Membentuk Nanokomposit Fil AgNPs-Poli Asam Laktat Sebagai Antibakteri. Berkala MIPA, 25(2), 140–153.
Couto, M.F., Peternelli, L.A., Barbosa, M.H.P., 2013. Classification of the coefficients of variation for sugarcane crops. Ciência Rural, 43(6), 957–961.
22
Deng, J., Ding, Q.M., Li, W., Wang, J.H., Liu, D.M., Zeng, X.X., Liu, X.Y., Ma, L., Deng, Y., Su, W., Ye, B., 2019. Preparation of Nano-Silver-Containing Polyethylene Composite Film and Ag Ion Migration into Food-Simulants. Journal of Nanoscience and Nanotechnology, 20(3), 1613–1621.
Dewi, K.T.A., Kartini, Sukweenadhi, J., Avanti, C., 2019. Karakter Fisik dan Aktivitas Antibakteri Nanopartikel Perak Hasil Green Synthesis Menggunakan Ekstrak Air Daun Sendok (Plantago major L.). Pharmaceutical Sciences and Research, 6(2), 69–81.
Fabiani, V.A., Putri, M.A., Saputra, M.E., Indriyani, D.P., 2019. Sintesis Nanosilver Menggunakan Bioreduktor Ekstrak Daun Pelawan (Tristaniopis merguensis) dan Uji Aktivitas Antibakter. Jurnal Kimia dan Pendidikan Kimia, 4(3), 172–178.
Firdhouse, M.J., Lalitha, P., 2015. Biosynthesis of Silver Nanoparticles and Its Applications. Journal of Nanotechnology, 2015, 1–18.
Ge, L., Li, Q., Wang, M., Ouyang, J., Li, X., Xing, M.M.Q., 2014. Nanosilver Particles in Medical Applications: Synthesis, Performance, and Toxicity. International Journal of Nanomedicine, 9(1), 2399–2407.
Hasim, Syamsul, F., Dewi, L.K., 2016. Effect of Boiled Cassava Leaves (Manihot esculenta Crantz) on Total Phenolic, Flavonoid and its Antioxidant Activity. Current Biochemistry, 3(3), 116–127.
Hendrawan, Y., Susilo, B., Putranto, A.W., Riza, D.F. Al, Maharani, D.M., Amri, M.N., 2016. Optimasi dengan Algoritma RSM-CCD pada Evaporator Vakum Waterjet dengan Pengendali Suhu Fuzzy pada Pembuatan Permen Susu. Jurnal Agritech, 36(02), 226.
Herlekar, M., Barve, S., Kumar, R., 2014. Plant-Mediated Green Synthesis of Iron Nanoparticles. Journal of Nanoparticles, 2014, 1–9.
Huda, N., Wahyuningsih, I., 2018. Karakterisasi Self-Nanoemulsifying Drug Delivery System (SNEDDS) Minyak Buah Merah (Pandanus conoideus Lam.). Jurnal Farmasi Dan Ilmu Kefarmasian Indonesia, 3(2), 49.
Kędziora, A., Speruda, M., Krzyżewska, E., Rybka, J., Łukowiak, A., Bugla-Płoskońska, G., 2018. Similarities and Differences between Silver Ions and
23
Silver in Nanoforms as Antibacterial Agents. International Journal of Molecular Sciences, 19(2), 1–17.
Khan, S.U., Saleh, T.A., Wahab, A., Khan, M.H.U., Khan, D., Khan, W.U., Rahim, A., Kamal, S., Khan, F.U., Fahad, S., 2018. Nanosilver: New Ageless and Versatile Biomedical Therapeutic Scaffold. International Journal of Nanomedicine, 13, 733–762.
Lestari, G.A.D., Suprihatin, I.E., Sibarani, J., 2019. Sintesis Nanopartikel Perak ( NPAg ) Menggunakan Ekstrak Air Buah Andaliman (Zanthoxylum acanthopodium DC.) dan Aplikasinya pada Fotodegradasi Indigosol Blue 22(5), 200–205.
Masakke, Y., Sulfikar, Rasyid, M., 2015. Biosintesis Partikel-nano Perak Menggunakan Ekstrak Metanol Daun Manggis (Garcinia mangostana L.). Jurnal Sainsmat, 4(1), 28–41.
Mohammadlou, M., Maghsoudi, H., Jafarizadeh-Malmiri, H., 2016. A review on green silver nanoparticles based on plants: Synthesis, potential applications and eco-friendly approach. International Food Research Journal, 23(2), 446– 463.
Nasution, M., 2019. Kajian Tentang Hubungan Deret Volta Dan Korosi Serta Penggunaannya Dalam Kehidupan Sehari-Hari. Seminar Nasional Teknik UISU 2019, 2(1), 251–254.
Nurmiah, S., Syarief, R., Sukarno, S., Peranginangin, R., Nurmata, B., 2013. Aplikasi Response Surface Methodology Pada Optimalisasi Kondisi Proses Pengolahan Alkali Treated Cottonii (ATC). Jurnal Pascapanen dan Bioteknologi Kelautan dan Perikanan, 8(1), 9.
Oktavia, S.N., Wahyuningsih, E., Andasari, S.D., 2020. Skrining Fitokimia Dari Infusa Dan Ekstrak Etanol 70 % Daun Cincau Hijau (Cyclea barbata Miers) 11(1), 1–6.
Oktaviani, D.T., Cahya, D., Amrullah, A., 2015. Sintesis Nano Ag dengan Metode Reduksi Kimia. Jurnal Sains dan Teknologi, 13(2), 101–114.
Park, J.-K., Lee, G.-M., Lee, C.-Y., Hur, K.-B., Lee, N.-H., 2012. Analysis of Siloxane Adsorption Characteristics Using Response Surface Methodology.
24
Environmental Engineering Research, 17(2), 117–122.
Prasetiowati, A.L., Prasetya, A.T., Wardani, S., 2018. Sintesis Nanopartikel Perak dengan Bioreduktor Ekstrak Daun Belimbing Wuluh (Averrhoa Bilimbi L.) sebagai Antibakteri. Indonesian Journal of Chemical Science, 7(2), 160–166. Pratiwi, A.P., 2016. Aktivitas Antibakteri Ekstrak Daun Singkong (Manihot
esculenta Crantz.) terhadap Shigella sp. Jurnal Kesehatan, 7(1), 161.
Purba, N.B.R., Rohman, A., Martono, S., 2019. The optimization of HPLC for quantitative analysis of acid orange 7 and sudan ii in cosmetic products using box behnken design. International Journal of Applied Pharmaceutics, 11(2), 130–137.
Rahmayani, Y., Zulhadjri, Z., Arief, S., 2019. Sintesis dan Karakterisasi Nanopartikel Perak-Tricalcium Phosphate (TCP) dengan Bantuan Ekstrak Daun Alpukat (Percea americana). Jurnal Kimia Valensi, 5(1), 72–78.
Ramadon, D., Mun’im, A., 2016. Pemanfaatan Nanoteknologi dalam Sistem Penghantaran Obat Baru untuk Produk Bahan Alam. Jurnal Ilmu Kefarmasian Indonesia, 14(2)(2), 118–127.
Ranoszek-Soliwoda, K., Tomaszewska, E., Socha, E., Krzyczmonik, P., Ignaczak, A., Orlowski, P., Krzyzowska, M., Celichowski, G., Grobelny, J., 2017. The Role of Tannic Acid and Sodium Citrate in The Synthesis of Silver Nanoparticles. Journal of Nanoparticle Research, 19(8), 273–288.
Riswanto, F.D.O., Rohman, A., Pramono, S., Martono, S., 2019. Application of Response Surface Methodology as Mathematical and Statistical Tools in Natural Product Research. Journal of Applied Pharmaceutical Science, 9(10), 125–133.
Saputra, A.H., Haryono, A., Laksmono, J.A., Hilman Anshari, D.M., 2011. Preparasi Koloid Nanosilver Dengan Berbagai Jenis Reduktor Sebagai Bahan Anti Bakteri. Jurnal Sains Materi Indonesia Indonesian Journal of Materials Science, 12(3), 202–208.
Sari, E.R., Meitisa, M., 2017. Standarisasi Mutu Ekstrak Daun Singkong ( Manihot esculenta Crantz ). Jurnal Ilmiah Bakti Farmasi, 2(1), 13–20.
25
dengan Bioreduktor Ekstrak Buah Muntingia calabura L untuk Analisis Logam Merkuri. Jurnal Pendidikan dan Ilmu Kimia, 1(1), 20–26.
Solomon, S.D., Bahadory, M., Jeyarajasingam, A. V., Rutkowsky, S.A., Boritz, C., Mulfinger, L., 2007. Synthesis and study of silver nanoparticles. Journal of Chemical Education, 84(2), 322–325.
Tao, H., Cui, B., Zhang, H., Bekhit, A.E.D., Lu, F., 2019. Identification and Characterization of Flavonoids Compounds in Cassava Leaves (Manihot esculenta Crantz) by HPLC/FTICR-MS. International Journal of Food Properties, 22(1), 1134–1145.
Tarannum, N., Divya, Gautam, Y.K., 2019. Facile Green Synthesis and Applications of Silver Nanoparticles: A state-of-the-art review. RSC Advances, 9(60), 34926–34948.
Terenteva, E.A., Apyari, V. V., Dmitrienko, S.G., Zolotov, Y.A., 2015. Formation of Plasmonic Silver Nanoparticles by Flavonoid Reduction: A Comparative Study and Application for Determination of These Substances. Spectrochimica Acta - Part A: Molecular and Biomolecular Spectroscopy, 151, 89–95.
Wendri, N., Rupiasih, N.N., Sumadiyasa, M., 2017. Biosintesis Nanopartikel Perak Menggunakan Ekstrak Daun Sambiloto: Optimasi Proses dan Karakterisasi. Jurnal Sains Materi Indonesia, 18(4), 162.
Wulandari, L., 2011. Kromatografi Lapis Tipis, Taman Kampus Presindo.
Yohanes, Khotimah, S., Ilmiawan, M.I., 2018. Uji Aktivitas Antibakteri Infusa Daun Paku Sisik Naga (Drymoglossum piloselloides L.) Terhadap Streptococcus pyogenes. Jurnal Mahasiswa PSPD FK Universitas Tanjungpura, 04(1), 1–23.
26 LAMPIRAN
27
Lampiran 2. Daun Singkong Segar, Daun Singkong Setelah Disimpan 2 Minggu dan Infusa Daun Singkong
Daun singkong segar
Daun singkong setelah disimpan 2 minggu
28
Lampiran 3. Hasil KLT Flavonoid Rutin Ekstrak Air Daun Singkong
Hasil KLT Gambar
Pengamatan secara langsung
Pengamatan dibawah lampu UV 256 nm
Pengamatan dibawah lampu UV 324 nm
29 Lampiran 4. Serbuk AgNO3
Lampiran 5. Hasil Nanosilver Sebelum dan Sesudah Purifikasi
R Sebelum Purifikasi Sesudah Purifikasi
30 1
2
Lampiran 6. Endapan Sesudah Purifikasi Endapan Setelah Sentrifugasi
31
Lampiran 7. Hasil replikasi panjang gelombang dan %T sebelum dan sesudah purifikasi
Hasil Panjang Gelombang Sesudah Purifikasi Percobaan Konsentrasi AgNO3 Konsentrasi bioreduktor R0 R1 R2 Rata-rata CV 1 1 11.57 430 428 428 428.67 0.27 2 2 11.57 262 260 260 260.67 0.44 3 1 23.15 444 412 410 422 4.52 4 2 23.15 450 434 436 440 1.98 9 0.79 17.36 428 416 414 419.33 1.81 10 2.21 17.36 262 230 263 251.67 7.46 11 1.5 9.17 438 432 436 435.33 0.70 12 1.5 25.55 430 428 432 430.00 0.47 5 1.5 17.36 442 440.25 1.86 6 1.5 17.36 442 7 1.5 17.36 442 8 1.5 17.36 448 13 1.5 17.36 422 14 1.5 17.36 444 15 1.5 17.36 446 16 1.5 17.36 436
32 Percobaan Konsentrasi AgNO3 Konsentrasi bioreduktor R0 R1 R2 Rata-rata CV 1 1 11.57 95.2 96.2 96 95.80 0.55 2 2 11.57 99.3 90.8 99 96.37 5.01 3 1 23.15 96.5 87.6 92 92.03 4.84 4 2 23.15 95.9 90.6 95.2 93.90 3.07 9 0.79 17.36 94.3 78.5 95.7 89.50 10.67 10 2.21 17.36 97.5 89.7 95.2 94.13 4.26 11 1.5 9.17 99.2 94.9 96.9 97.00 2.22 12 1.5 25.55 93.7 87.9 96.3 92.63 4.64 5 1.5 17.36 94.3 95.05 2.31 6 1.5 17.36 98.3 7 1.5 17.36 96.7 8 1.5 17.36 97.8 13 1.5 17.36 93.1 14 1.5 17.36 92.9 15 1.5 17.36 93.5 16 1.5 17.36 93.8
Hasil Panjang Gelombang Sebelum Purifikasi Percobaan Konsentrasi AgNO3 Konsentrasi bioreduktor R0 R1 R2 Rata-rata CV 1 1 11.57 426 426 410 420.67 2.20 2 2 11.57 420 420 402 414.00 2.51 3 1 23.15 436 414 402 417.33 4.13 4 2 23.15 436 418 432 428.67 2.20 9 0.79 17.36 424 414 402 413.33 2.66 10 2.21 17.36 432 416 410 419.33 2.71 11 1.5 9.17 432 422 402 418.67 3.65 12 1.5 25.55 426 414 430 423.33 1.97
33 5 1.5 17.36 428 425.75 1.49 6 1.5 17.36 416 7 1.5 17.36 432 8 1.5 17.36 432 13 1.5 17.36 416 14 1.5 17.36 428 15 1.5 17.36 428 16 1.5 17.36 426
Hasil %T Sebelum Purifikasi Percobaan Konsentrasi AgNO3 Konsentrasi bioreduktor R0 R1 R2 Rata-rata CV 1 1 11.57 90.4 92.1 94.2 92.23 2.06 2 2 11.57 90.60 91 93.8 91.80 1.90 3 1 23.15 91.10 87 90.7 89.60 2.52 4 2 23.15 87.90 86.4 88.8 87.70 1.38 9 0.79 17.36 88.70 86.2 92.6 89.17 3.62 10 2.21 17.36 90.70 86.2 92.2 89.70 3.48 11 1.5 9.17 95.40 95.4 94.5 95.10 0.55 12 1.5 25.55 84.50 83.9 94.7 87.70 6.92 5 1.5 17.36 84.60 90.28 3.51 6 1.5 17.36 88.30 7 1.5 17.36 91.00 8 1.5 17.36 93.00 13 1.5 17.36 88.40 14 1.5 17.36 94.00 15 1.5 17.36 93.20 16 1.5 17.36 89.70
34
Lampiran 8 Grafik Panjang Gelombang Sesudah dan Sebelum Purifikasi
R Sesudah sebelum
35 1
36 Lampiran 9. Hasil PSA
39 Setelah sentrifugasi
41
Lampiran 10. Alat dan Instrumen yang Digunakan
Timbangan analitik Mettler Toledo
Vortex Thermo
Spektrofotometer doeble beam UV-Vis Shimadzu 1800
42 Hot plate Thermo
43 Sentrifugator Thermo
Lampiran 11. Hasil Analisis Respon Panjang Gelombang dengan Rancangan CCD Menggunakan Minitab17
44
Lampiran 12. Hasil Analisis Respon %T dengan Rancangan CCD Menggunakan Miniab17
45 BIOGRAFI PENULIS
Penulis bernama lengkap Stevani Johannes lahir pada tanggal 11 Januari 1999. Penulis merupakan anak bungsu dari dua bersaudara pasangan Johannes dan Susan. Penulis telah menyelesaikan tugas akhir skripsi dengan judul “Optimasi Formula dan Pembuatan Nanosilver Menggunakan Bioreduktor Ekstrak Air Daun Singkong (Manihot esculenta Crantz)”. Pendidikan formal yang ditempuh penulis yakni TK Santo Tarcisius Dumai (2004-2005), SD Santo Tarcisius Dumai(2005-2011), SMP Santo Tarcisius Dumai (2011-2014), SMA Maitreyawira Batam (2014-2017), kemudian melanjutkan pendidikan Sarjana S1 di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta pada tahun 2017. Selama kuliah, penulis pernah menjadi asisten praktikum Kimia Dasar (2019), Farmakognosi Fitokimia (2019), Pharmaceutical Care Kardio Endokrin (2020). Penulis juga aktif dalam kegiatan kampus seperti menjadi panitia ketua bidang umum SICON (2019), divisi liaison officer FACTION #3 (2019), Volunteer dalam kegiaan World Diabetes Day (2017). Penulis pernah menjadi pengurus organisasi Komunitas Mahasiswa Buddhis Konghucu Dharma Viriya sebagai anggota kreasi (2018-2019).