PEMURNIAN DAN KARAKTERISASI ENZIM KATEPSIN
DARI IKAN BANDENG (Chanos chanos Forskall)
NICO DYNNAR
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
RINGKASAN
NICO DYNNAR. Pemurnian dan Karaktersisasi Enzim Katepsin dari Ikan Bandeng (Chanos chanos Forskall). Dibimbing oleh TATI NURHAYATI dan ELLA SALAMAH.
Ikan merupakan salah satu komoditas yang cepat mengalami kemunduran mutu. Kemunduruan mutu ini diakibatkan oleh adanya aktivitas bakteri dan kerja dari enzim proteolitik. Enzim ini bekerja menghidrolisis ikatan peptida pada protein. Salah satunya ialah enzim katepsin. Enzim katepsin dipercaya berperan dalam proses pelunakan daging pada ikan selama proses kemunduran mutu. Karakterisasi enzim katepsin perlu dilakukan untuk melihat faktor lingkungan apa saja yang berpengaruh terhadap aktivitas enzim katepsin, selain itu juga dengan mengkarakterisasi akan diperoleh informasi kondisi optimum enzim katepsin bekerja sehingga pada rantai penanganan ikan dapat dihindari faktor-faktor yang dapat meningkatkan kerja enzim katepsin.
Tujuan penelitian ini adalah memurnikan enzim katepsin dari ikan bandeng serta mengkarakterisasi enzim katepsin yang telah dimurnikan. Metode penelitian ini dilakukan melalui beberapa tahap. Tahap pertama yakni ekstraksi kasar daging ikan bandeng. Hasil dari ektrak kasar, lalu dipresipitasi dengan ammonium sulfat, hasilnya kemudian didialisis. Enzim yang telah dimurnikan kemudian dikarakterisasikan suhu, konsentrasi substrat, pengaruh logam, pH dan dilakukan elektroforesis SDS-PAGE dan zimogram untuk mengetahui bobot molekul enzim yang dihasilkan.
Enzim katepsin pada tahap ektraksi kasar memiliki aktivitas spesifik sebesar 0,8598 U/mg. Pemurnian lebih lanjut dengan menggunakan ammonium sulfat dengan konsentrasi sebesar 70% (b/v) didapatkan aktivitas spesifik sebesar 4,4643 U/mg. Setelah didialisis menggunakan 12 kDa selama 6 jam diperoleh aktivitas spesifik sebesar 14,4404 U/mg.
Karakterisasi katepsin dilakukan untuk mengetahui pengaruh lingkungan terhadap aktivitas dari enzim katepsin, selain itu juga untuk melihat pada titik berapa enzim katepsin bekerja secara optimal. Kondisi optimum enzim katepsin bekerja pada suhu 40 °C, pH 4, dan konsentrasi substrat 3%. Sementara keberadaan ion logam akan menghambat aktivitas enzim katepsin. Enzim Katepsin terestimasi memiliki bobot molekuk sebesar 86,87 kDa.
PEMURNIAN DAN KARAKTERISASI ENZIM KATEPSIN
DARI IKAN BANDENG (Chanos chanos Forskall)
NICO DYNNAR
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan
pada Departemen Teknologi Hasil Perairan
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
Judul Skripsi : Pemurnian dan Karakterisasi Enzim Katepsin dari Ikan Bandeng (Chanos chanos Forskall)
Nama : Nico Dynnar NRP : C34060190
Disetujui
Pembimbing I Pembimbing II
Dr. Tati Nurhayati S.Pi, M.Si Dra. Ella Salamah, M. Si NIP. 19700807 199603 2 002 NIP. 19530629 198803 2 001
Diketahui
Ketua Departemen Teknologi Hasil Perairan
Dr. Ir. Ruddy Suwandi, M.S, M. Phil NIP. 19580511 198503 1 002
KATA PENGANTAR
Puji syukur dipanjatkan ke hadirat Allah SWT, yang telah melimpahkan segenap rahmat dan karunia-Nya sehingga skripsi dengan judul Pemurnian dan
Karakterisasi Enzim Katepsin dari Ikan Bandeng (Chanos chanos Forskall) ini
dapat diselesaikan.
Skripsi ini dibuat sebagai syarat untuk memperoleh gelar sarjana perikanan pada Program Studi Teknologi Hasil Perairan di Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Banyak bantuan yang telah diberikan berbagai pihak sampai diselesaikannya laporan ini. Oleh karena itu, pada kesempatan ini disampaikan ucapan terima kasih kepada:
1. Dr. Tati Nurhayati, S.Pi, M.Si dan Ibu Dra. Ella Salamah, MS selaku komisi pembimbing, atas segala bimbingan dan pengarahannya.
2. Dr. Ir. Sri Purwaningsih, M.Si selaku dosen penguji, atas segala masukannya. 3. Dr. Ir. Ruddy Suwandi, MS selaku Ketua Departemen Teknologi Hasil Perairan,
Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
4. Dr. Ir. Agoes M. Jacoeb, Dipl.Biol selaku Ketua Komisi Pendidikan Departemen Teknologi Hasil Perairan.
5. Anna C. Erungan, MS selaku pembimbing akademik.
6. Ayah dan Ibunda tercinta, atas semua dukungan dan kasih sayang yang diberikan serta doanya selama ini.
7. Bu Ema, Ba Lastri, Silvia, Mas Epul sebagai laboran THP dan Pak Wahyu (FKH) dan Bu Dewi serta Bu Ika (PAU) yang telah banyak membantu selama penelitian. 8. Teman-teman THP 43 yang selalu memberikan kesan-kesan terindah.
9. Rekan-rekan Laboratorim Bioteknologi II atas kerjasama dan motivasi yang diberikan.
10. Kakak kelas (THP 41 dan THP 42) dan adik-adik kelas (THP 44 dan THP 45) atas semangat dan kebersamaannya.
11. Semua pihak yang telah membantu penulis selama penelitian dan penyusunan skripsi, yang tidak dapat disebutkan satu persatu.
Penulis menyadari bahwa penulisan skripsi ini masih jauh dari kesempurnaan. Oleh sebab itu, kritik dan saran yang bersifat membangun dari semua pihak sangat diharapkan. Semoga tulisan ini bermanfaat bagi semua pihak yang memerlukan.
Bogor, Januari 2011
Nico Dynnar
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 28 Agustus 1988 sebagai anak kedua dari tiga bersaudara, putra
dari pasangan Santo Dyne dan Chaironi. Penulis mengawali pendidikan di SDN Pengadilan 3 Bogor pada tahun 1994 dan menyelesaikan pada tahun 2000. Pada tahun yang sama penulis diterima di SMPN 12 Bogor dan menyelesaikan pendidikan pada tahun 2003. Penulis melanjutkan pendidikan di SMAN 2 Bogor dan selesai pada tahun 2006. Pada tahun yang sama penulis diterima di Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih mayor Teknologi Hasil Perairan pada pilihan pertamanya, dan memilih minor Manajemen Fungsional dari Departemen Manajemen sebagai pelengkapnya.
Selama perkuliahan, penulis terdaftar pada asisten luar biasa mata kuliah Avertebrata Air pada tahun ajaran 2009/2010 dan pada tahun 2010/2011, Teknologi Produk Tradisional Hasil Perairan tahun ajaran 2009/2010, Fisiologi Formasi dan Degradasi Metabolit Hasil Perairan tahun ajaran 2010/2011, keanggotan
Fisheries Processing Club (FPC), selain itu juga penulis mengikuti pelatihan Good Laboratory Practices (GLP) pada tahun 2010, pelatihan Hazard Analysis Critical Control Point (HACCP) dari Badan Pengawasan Obat dan Makanan (BPOM) –
Departemen Ilmu dan Teknologi Pangan IPB pada tahun 2008, seminar Young
Entrepreneur Awards by Commonwealth Bank pada tahun 2009. Selain itu juga pada
tahun 2003 penulis terpilih sebagai juara 3 Try Out tingkat SMP se-kota Bogor yang diselenggarakan oleh Yayasan Dharma Andhiga, dan pada tahun 2006 penulis
terdaftar sebagai peserta olimpiade kimia se-jabodetabek yang diselenggarakan oleh Institut Teknologi Indonesia. Di tempat lain penulis juga pernah terpilih sebagai 5
pemberi aspirasi terbaik pada Majalah Kereta Api edisi 40. November 2009 dengan topik aspirasi mengenai cara pemberantasan calo tiket.
I. PENDAHULUAN
1.1 Latar Belakang
Potensi lestari perikanan laut Indonesia diperkirakan sebesar 6,4 juta ton per tahun yang tersebar di perairan wilayah Indonesia dan Zona Ekonomi Ekslusif (ZEE) dengan jumlah tangkapan yang diperbolehkan sebesar 5,12 juta ton per tahun atau sekitar 80% dari potensi lestari. Potensi tersebut merupakan salah satu peluang untuk meningkatkan jumlah produksi ikan baik pada perikanan tangkap maupun perikanan budidaya. Jumlah produksi perikanan tangkap dari penangkapan ikan di laut dan di perairan umum pada tahun 2006 masing-masing sekitar 4.468.010 ton dan 301.150 ton. Produksi perikanan budidaya pada tahun 2006 mencapai 2.625.800 ton yang didominasi oleh udang 327.260 ton, rumput laut 1.079.850 ton, ikan mas 285.250 ton, bandeng 269.530 ton, nila 227.000 ton, lele 94.160 ton, gurame 35.570 ton (BRKP 2007). Data ini menggambarkan bahwa tingkat produktivitas dari ikan bandeng cukup tinggi.
Salah satu penyebab terjadinya proses kemunduran mutu ialah adanya aktivitas enzim terutama enzim proteolitik. Enzim katepsin itu sendiri merupakan salah satu enzim proteolitik yang ditemukan pada jaringan hewan yang dapat menghidrolisis protein menjadi polipeptida (Shahidi dan Botta 1994). Katepsin banyak ditemukan dalam jaringan otot ikan. Proses penurunan mutu secara enzimatis berlangsung sebagai aksi kegiatan enzim yang menguraikan senyawa kimiawi pada jaringan tubuh ikan (Ilyas 1983). Penguraian protein dalam proses enzimatis akan menyebabkan perubahan bau, tekstur, dan penampakan ikan.
Informasi mengenai kondisi optimal enzim katepsin bekerja berguna dalam proses penanganan yang tepat. Informasi ini dapat dikelola agar pada saat penanganan kondisi-kondisi lingkungan yang dapat meningkatkan kerja enzim katepsin secara optimal khususnya pada ikan bandeng dapat dihindari.
1.2 Tujuan
Tujuan dari penelitian pemurnian enzim katepsin ikan bandeng ialah: a. Memurnikan enzim katepsin dari ikan bandeng;
b. Menentukan karakter katepsin yang dihasilkan dari pemurnian enzim katepsin ikan bandeng.
II. TINJAUAN PUSTAKA
2.1 Deskripsi dan Klasifikasi Ikan Bandeng (Chanos chanos Forskall)
Ikan bandeng mempunyai ciri-ciri morfologi badan memanjang, agak pipih, tanpa scute pada bagian perutnya, mata diseliputi lendir mempunyai sisik besar pada sirip dada dan sirip perut, sirip ekor panjang dan bercagak, sisik kecil dengan tipe sikloid, tidak bergigi, sirip dubur jauh dibelakang sirip punggung (Saanin 1984). Morfologi ikan bandeng disajikan pada Gambar 1.
Gambar 1. Morfologi ikan bandeng (Erwin 2010) Klasifikasi ikan bandeng menurut Saanin (1984) adalah sebagai berikut: Filum : Chordata Subfilum : Vertebrata Kelas : Pisces Ordo : Malacopterygii Famili : Chanidae Genus : Chanos
Species : Chanos chanos
Ikan bandeng merupakan salah satu jenis ikan budidaya air payau yang potensial dikembangkan. Jenis ikan ini mampu mentolelir salinitas perairan yang luas (0-158 ppt) sehingga digolongkan sebagai ikan euryhaline. Ikan bandeng mampu beradaptasi terhadap perubahan lingkungan seperti suhu, pH, dan kekeruhan air serta tahan terhadap serangan penyakit (Ghufron dan Kardi 1997).
Ikan bandeng merupakan salah satu komoditas ekspor yang dikenal dengan sebutan milkfish. Ikan ini memiliki tubuh langsing, seperti peluru, dengan sirip ekor bercabang, ciri ini memberikan petunjuk bahwa ikan bandeng mampu berenang dengan cepat. Tubuh ikan bandeng berwarna putih keperak-perakan dan dagingnya berwarna putih susu. Ikan bandeng memiliki daerah penyebaran sangat luas, yaitu Pantai Afrika Timur sampai ke Kepulauan Tuamutu sebelah timur Tahiti dan Jepang Selatan sampai Australia Utara (Murtidjo 2002).
2.2 Enzim
Enzim ialah protein yang mengkatalisis reaksi-reaksi biokimia. Enzim biasanya terdapat dalam sel dengan konsentrasi yang sangat rendah, selain itu juga enzim mempunyai kemampuan untuk meningkatkan laju reaksi tanpa mengubah posisi kesetimbangan (Kuchel dan Gregory 2006). Enzim ikut ambil bagian dalam seluruh aktivitas yang diperlukan untuk mempertahankan kehidupan, seperti sintesis dan penguraian, eksresi, detoksifikasi, dan penyediaan energi (Shinya 2008).
Di dalam tubuh terdapat lebih dari 2500 reaksi biokimia yang berbeda dengan bantuan enzim spesifik yang sesuai untuk meningkatkan laju reaksinya. Masing-masing enzim dicirikan oleh spesifitasnya untuk substrat (reaktan) yang mirip secara biologis. Molekul-molekul lain juga dapat mengatur aktivitas enzim, molekul-molekul ini disebut efektor dan dapat bersifat sebagai aktivator, inhibitor atau keduanya (Kuchel dan Gregory 2006).
Rantai samping asam amino pada enzim mempunyai susunan tertentu yang terdapat dalam tapak aktif. Susunan tertentu inilah yang menentukan jenis molekul yang dapat diikat dan bereaksi dalam tapak tersebut. Banyak enzim memiliki molekul nonprotein kecil yang tergabung dengan atau di dekat tapak aktif yang menentukan spesifitas substrat. Molekul ini disebut kofaktor jika terikat secara non kovalen dengan protein dan disebut gugus prostetik jika terikat secara kovalen (Kuchel dan Gregory 2006).
2.2.1 Cara kerja enzim
Enzim bekerja dengan dua cara, yaitu menurut Teori Kunci-Gembok (Lock
and Key Theory) dan Teori Kecocokan Induksi (Induced Fit Theory). Menurut teori
kunci-gembok, terjadinya reaksi antara substrat dengan enzim karena adanya kesesuaian bentuk ruang antara substrat dengan sisi aktif (active site) dari enzim, sehingga sisi aktif enzim cenderung kaku. Substrat berperan sebagai kunci masuk ke dalam situs aktif, yang berperan sebagai gembok, sehingga terjadi kompleks enzim-substrat. Ikatan kompleks enzim-substrat terputus, produk hasil reaksi akan dilepas dan enzim akan kembali pada konfigurasi semula. Mekanisme teori kunci-gembok disajikan pada Gambar 2,
Gambar 2. Teori Kunci-Gembok (Stenes 1998)
Berbeda dengan teori kunci-gembok, teori induksi enzim menekankan pada enzim melakukan penyesuaian bentuk untuk berikatan dengan substrat. Hal ini bertujuan untuk meningkatkan kecocokan dengan substrat dan membuat ikatan enzim substrat lebih reaktif. Molekul enzim memiliki sisi aktif tempat melekatnya substrat dan terbentuk molekul kompleks enzim-substrat. Pengikatan substrat menginduksi penyesuaian pada enzim yang meningkatkan kecocokan dan mendorong molekul kompleks enzim-substrat (Chang 2003). Mekanisme teori kecocokan induksi disajikan pada Gambar 3,
Gambar 3. Teori kecocokan induksi (Stenes 1998)
2.2.2 Klasifikasi enzim
Sistem penamaan dan klasifikasi enzim telah diambil dari hasil persetujuan internasional dan diberi nomor kode/sandi. Pembagian didasarkan pada reaksi yang dikatalisisnya. Sistem membaginya menjadi 6 kelas utama.
Klasifikasi enzim berdasarkan atas reaksi katalisisnya (Buxbaum 2007): 1) Oksidoreduktase : Enzim yang mengkatalisis reaksi oksidasi atau reduksi
suatu substrat. Dua macam enzim yang paling utama, yakni oksidase dan dehidrogenase. Oksidase ialah enzim yang mengkatalisis reaksi antara substrat dengan molekul oksigen. Contoh: katalase, peroksidase, tirosinase, dan asam askorbat oksidase. Dehidrogenase ialah enzim yang aktif dalam pengambilan atom hidrogen dari substrat. Contoh: Enzim suksinat dehidrogenase yang memecah asam suksinat menjadi asam fumarat
2) Tranferase : Reaksi yang dikatalisisnya merupakan reaksi pemindahan gugus fungsional. Contoh: transglikosidase, transfosforilase, transaminase, dan tranasetilase.
3) Hidrolase : Enzim yang mengkatalisis reaksi hidrolisis suatu substrat atau memecah substrat dengan pertolongan molekul air. Contoh: lipase dan amilase.
4) Liase : Enzim yang aktif dalam pemecahan C-C dan C-O dengan tidak menggunakan molekul air. Contoh: enzim dekarboksilase yang memecah ikatan C-C
5) Isomerase : Jenis reaksi yang dikatalisisnya adalah pemindahan gugus di dalam molekul, menghasilkan bentuk isomer
6) Ligase : Reaksi yang dikatalisisnya merupakan reaksi pembentukan ikatan C-C, C-S, C-O, dan C-N oleh reaksi kondensasi yang berkaitan dengan penguraian ATP.
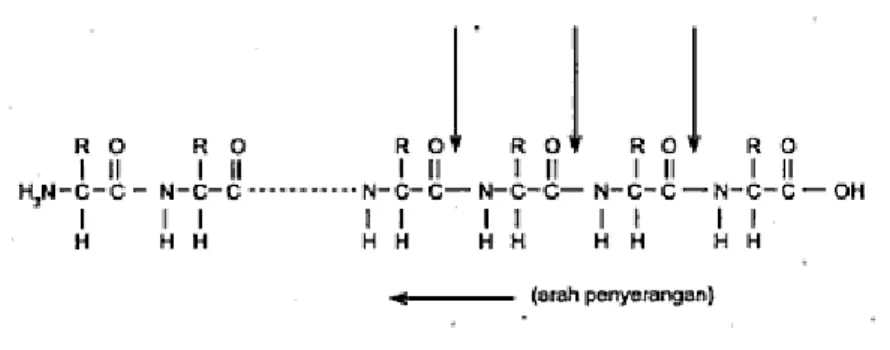
Enzim yang menghidrolisis pemutusan ikatan peptida pada protein diklasifikasikan menjadi dua kelompok besar, yaitu golongan eksopeptidase dan golongan endopeptidase. Golongan eksopeptidase mengkatalisis hidrolisis pemutusan ikatan peptida dari rantai peptida suatu protein, tempat pemutusannya dari tepi atau dari ujung, baik di ujung yang mengandung gugus karboksil maupun yang mengandung gugus amino. Golongan ini dibedakan atas karboksipeptidase dan aminopeptidase. Karboksipeptidsase mengkatalisasi hidrolisis pemutusan ikatan peptida pada rantai peptida molekul protein, dimulai dari ujung tempat gugus karboksil bebas. Tiap penyerangan atau pemutusan ikatan peptida dilepaskan sebuah asam amino (Bregman dan Futon 1996).
Gambar 4. Mekanisme pemutusan gugus karboksil oleh enzim golongan karboksipeptidase (Sumardjo 2006)
Aminopeptidase mengatalisasi hidrolisis pemutusan ikatan-ikatan peptida dari rantai peptida molekul protein, dimulai dari ujung tempat gugus amino bebas. Tiap penyerangan atau pemutusan ikatan peptida melepaskan sebuah asam amino.
Gambar 5. Mekanisme pemutusan gugus amin oleh enzim golongan aminopeptidase (Sumardjo 2006)
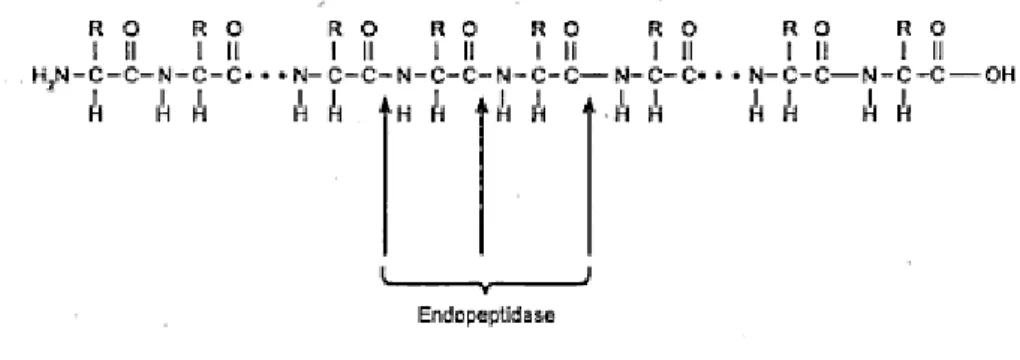
Golongan endopeptidase mengatalisasi hidrolisis pemutusan ikatan peptida dari rantai peptida suatu protein, tempat pemutusannya dari dalam atau dari tengah. Enzim ini terdiri atas satu rantai polipeptida dan dihasilkan atau diproduksi dalam bentuk nonaktif.
Gambar 6. Mekanisme pemutusan ikatan peptida oleh enzim golongan endopeptidase (Sumardjo 2006)
2.2.3 Katepsin
Katepsin merupakan salah satu enzim proteolitik yang ditemukan pada jaringan hewan termasuk ikan. Katepsin banyak ditemukan dalam jaringan otot ikan. Pada jaringan otot ikan, katepsin dan enzim penghidrolisis lainnya ditempatkan dalam organel subseluller dan dibagi dala dua tempat, yaitu pada serabut otot dan matriks ekstraselluler (Shahidi dan Botta 1994). Katepsin merupakan enzim yang menghidrolisis ikatan peptida pada protein (Salleh et al. 2006). Katepsin juga
ditemukan pada lisosom dan sel fagosit (Carreno 2000). Katepsin dikenal sebagai famili endopeptidase dan atau famili eksopeptidase. Banyak katepsin optimal pada pH asam walaupun beberapa diantaranya aktif pada pH netral (Haard 1994).
Katepsin B ditemukan secara luas pada lisosom. Katepsin B dapat diisolasi dari beberapa spesies mamalia dan berbagai jaringan, meliputi limpa, liver, kelenjar paratiroid, dan otak. Katepsin B ialah glikoprotein dengan jumlah manosa yang sangat rendah atau rendah. Katepsin H dan katepsin L ditemukan lebih banyak dibandingkan katespin B. Ketiga enzim ini dipurifikasi bersama melalui beberapa tahap sampai mereka terpisah oleh kromatografi pertukaran ion. Metode yang lebih efisien, yakni kromatografi afinitas kovalen baru untuk mempurifikasi katepsin B (Polgar 1990).
Katepsin C tidak mungkin untuk melakukan tindakannya secara utuh pada protein secara langsung, tetapi memiliki aktivitas spesifik tertinggi di antara semua peptidase lisosomal. Katepsin C mencerna lebih lanjut fragmen‐fragmen peptida yang dihasilkan dari aktivitas katepsin D (Park 2005).
Katepsin D pertama kali ditemukan pada jaringan otot daging oleh Siebert, kemudian diindentifikasikan oleh Mekinodan dan Ikeda pada tahun 1965. Katepsin D dipercaya berperan dalam pendegradasian secara signifikan pada tekstur selama penyimpanan dingin. Katepsin D juga dilaporkan merupakan salah satu katepsin penting dalam pelunakan pada post‐mortem karena katepsin D menyerang secara langsung protein pada otot yang akan menghasilkan peptida yang dapat dipecah lebih lanjut oleh katepsin lainnya (Park 2005).
Katepsin merupakan protease asam yang biasanya terletak di lisosom (DeDuve et al. 1955) dan sel fagosit tetapi juga telah ditemukan dalam retikulum sarkoplasma dari sel otot (Allen dan Goll 2003). Katepsin B mendegradasi miosin dan aktin ke bentuk yang lebih sederhana, sementara D mendegradasi baik aktin dan miosin menjadi fragmen-fragmen peptida berukuran kecil (Haard 1994).
Katepsin B dan katepsin L keduanya merupakan sistein proteinase yang kemungkinan paling penting dalam kemunduran tekstur daging (Aoki et al. 2000).
Aktivitasnya berbeda beda tiap spesies ikan. Aktivitas optimum dilaporkan pada suhu 40-50 °C dan aktivitasnya menurun dengan penurunan suhu. Secara umum bekerja pada pH 3-4 dan beberapa katepsin juga mempunyai aktivitas tinggi pada pH 6-6,5 (Kolodziejska dan Sikorsi 1996).
Aktivitas katepsin akan memberikan pengaruh pada tekstur daging ikan karena katepsin dapat menurunkan fleksibilitas sehingga daging ikan menjadi tidak elastis dan jaringan daging ikan melunak. Daging yang melunak ini merupakan salah satu sumber masalah pada industri surimi karena katepsin dapat menurunkan kemampuan pembentukan gel dalam proses pembuatan surimi dari daging ikan akibat degradasi protein miofibril yang dapat mengurangi elastisitas dan kekuatan gel surimi (Jiang 2000).
Katepsin H aktif pada pH netral, stabil terhadap panas dan menunjukkan aktivitas molekuler dengan subtrat miosin. Katepsin L merupakan jenis protease lain yang sangat aktif dalam mendegradasi protein miofibril. Aktivitas molekular dari katepsin L dengan substrat miosin adalah 10 kali lebih besar dari pada katepsin B. Katepsin L dapat mendegradasi miofibril termasuk aktin, miosin, dan tropomiosin pada pH 6,5 dan secara khusus aktif untuk troponim serta dalam pemindahan Ca dari ATPase miofibril pada pH netral (Shahidi dan Botta 1994).
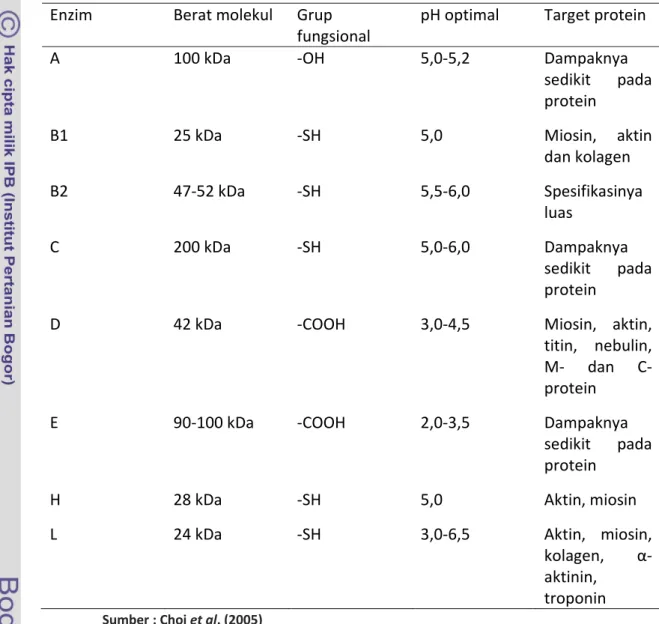
Tindakan utama katepsin H ialah aminopeptidase, dan terkadang substrat assay mengandung asam amino arginin. Katepsin H lebih toleran terhadap medium yang bersifat alkali dibandingka katepsin B (Elisabeth 1994). Tabel 1 menyajikan karakterisasi berbagai jenis katepsin.
Tabel 1. Beberapa sifat proteinase lisosomal, katepsin A‐L yang ditemukan pada otot
Enzim Berat molekul Grup fungsional
pH optimal Target protein A 100 kDa ‐OH 5,0‐5,2 Dampaknya
sedikit pada protein
B1 25 kDa ‐SH 5,0 Miosin, aktin dan kolagen B2 47‐52 kDa ‐SH 5,5‐6,0 Spesifikasinya luas C 200 kDa ‐SH 5,0‐6,0 Dampaknya sedikit pada protein
D 42 kDa ‐COOH 3,0‐4,5 Miosin, aktin, titin, nebulin, M‐ dan C‐ protein
E 90‐100 kDa ‐COOH 2,0‐3,5 Dampaknya sedikit pada protein
H 28 kDa ‐SH 5,0 Aktin, miosin
L 24 kDa ‐SH 3,0‐6,5 Aktin, miosin, kolagen, α‐ aktinin, troponin
Sumber : Choi et al. (2005)
2.2.4 Faktor-faktor yang mempengaruhi kerja enzim
Terdapat beberapa faktor yang memengaruhi kerja enzim. Faktor-faktor tersebut erat kaitannya dengan sifat enzim sebagai protein. Faktor-faktor tersebut diantaranya (Abdurahman 2008):
1) Suhu
Suhu sangat berperngaruh terhadap kerja enzim karena enzim terdiri atas protein. Semakin suhunya tinggi, reaksi kimia akan semakin cepat. Akan tetapi enzim akan mengalami denaturasi jika suhu terlalu tinggi. Enzim yang mengalami denaturasi akan mengalami perubahan konformasi dari enzim, sehingga enzim tersebut tidak aktif.
2) Derajat keasaman (pH)
Seperti protein, enzim juga bekerja dipengaruhi oleh derajat keasaman lingkungan. Setiap enzim memiliki pH lingkungan yang khas untuk mencapai aktivitas optimumnya. Di luar pH tersebut, kerja enzim akan terganggu bahkan akan terdenaturasi.
3) Zat penghambat
Kerja enzim dapat dihambat oleh zat penghambat/inhibitor. Terdapat dua jenis inhibitor yakni inhibitor kompetitif dan inhibitor non-kompetitif. Inhibitor kompetitif menghambat kerja enzim dengan cara berikatan dengan enzim pada sisi aktifnya. Inhibitor ini bersaing dengan substrat untuk menempati sisi aktif enzim. Hal ini terjadi karena inhibitor memiliki struktur yang mirip dengan substrat.
Berbeda dengan inhibitor kompetitif, inhibitor non-kompetitif tidak bersaing dengan substrat untuk berikatan dengan enzim. Inhibitor jenis ini akan berikatan dengan enzim pada sisi yang berbeda (bukan sisi aktif enzim). Jika telah terjadi ikatan enzim-inhibitor, sisi aktif enzim akan berubah sehingga substrat tidak dapat berikatan dengan enzim.
4) Konsentrasi enzim dan substrat
Pada reaksi dengan konsentrasi enzim yang lebih sedikit dibandingkan substrat, penambahan enzim akan meningkatkan laju reaksi. Peningkatan laju reaksi ini terjadi secara linear. Jika konsentrasi substart dan enzim sudah seimbang, laju reaksi akan relatif konstan. Penambahan konsentrasi substrat pada reaksi yang dikatalisis oleh enzim awalnya akan meningkatkan laju
reaksi. Akan tetapi, setelah konsentrasi substrat dinaikkan lebih lanjut, laju reaksi akan mencapai titik jenuh dan tidak bertambah lagi.
2.3 Pemurnian Protein
Pemurnian (pemekatan) protein menggunakan amonium sulfat adalah metode yang sering digunakan karena memiliki daya larut tinggi di dalam air, relatif murah, dan kestabilan protein di dalam larutan amonium sulfat (2 M – 3 M) tahan bertahun-tahun. Pemilihan amonium sulfat didasarkan pada kelarutan protein yang berinteraksi polar dengan molekul air, interaksi ionik protein dengan garam dan daya tolak menolak protein yang bermuatan sama. Kelarutan protein (pada pH dan suhu tertentu) yang meningkat akan menaikan konsentrasi garam (salting in). Penambahan garam dengan konsentrasi tertentu akan membuat kelarutan protein menurun (salting
out). Molekul air yang berikatan dengan ion-ion garam akan menyebabkan semakin
banyak terjadinya penarikan selubung air yang mengelilingi permukaan protein sehingga mengakibatkan protein saling berinteraksi, beragregasi, dan kemudian mengendap (Harris 1989).
Presipitasi protein dalam ekstrak dapat dicapai dengan penambahan garam, larutan organik, atau polimer organik, atau variasi suhu atau pH pada larutan. Agen yang sering digunakan dalam presipitasi tercantum pada Tabel 2.
Tabel 2. Agen presipitasi
Agen Tipe Karakteristik
Amonium sulfat Garam Mudah larut, stabil Sodium sulfat Garam Mudah larut, stabil
Etanol Solvent Mudah terbakar, beresiko
untuk terdenaturasi Aseton Solvent Mudah terbakar, beresiko
untuk terdenaturasi Polietilen glikol Solvent Bermuatan, tidak mudah
terbakar
Keberhasilan proses presipitasi untuk purifikasi protein tergantung pada beberapa faktor. Pertama, konsentrasi total protein harus cukup tinggi untuk cepat agregat prosedur dan hasil endapan. Konsentrasi garam yang sangat rendah, akan membuat terbentuknya agregat secara kinetis tidak akan menguntungkan, ukuran agregatnya terlalu kecil untuk dikumpulkan dengan sentrifugasi. Kedua, aktivitas protein yang diinginkan harus dijaga selama proses pengendapan, sehingga diperoleh protein aktif. Efek pengendapan yang sama akan terjadi apabila protein terdenaturasi. Konsentrasi garam yang tinggi dapat menyebabkan denaturasi protein (Pace et al. 1989 diacu dalam Marshak 1996).
Sampel protein yang telah mengendap kemudian dibersihkan dari garam pengotor dengan cara dialisis. Garam yang berlebih di dalam sampel dapat dihilangkan dengan cara menempatkan sampel di dalam kantung (membran) dialisis semipermeabel yang direndam di dalam larutan buffer. Molekul yang berukuran kecil akan keluar melalui membran, sedangkan molekul yang besar akan tertahan di dalam membran dialisis. Ukuran pori kantung dialisis yang terbuat dari bahan selulosa asetat ini dinyatakan dalam satuan dalton, yang menunjukkan berat molekul minimum yang dapat tertahan di dalam membran (Harris 1989).
2.4 Elektroforesis
Elektroforesis merupakan teknik pemisahan suatu molekul dalam suatu campuran di bawah pengaruh medan listrik (Sudjati 2008). Elektroforesis pada protein menggunakan gel poliakrilamid. Seringkali dalam pembuatan gel poliakrilamid ditambahkan sodium dodecyl sulphate (SDS) yang merupakan senyawa untuk mendisosiasikan protein menjadi subunitnya (Yuwono 2008). Protein dapat dipisahkan berdasarkan ukuran massanya dengan sistem elektroforesis gel poliakrilamid sistem tegak. Sebelumnya, campuran protein yang telah berisi SDS dipanasi. Penggunaan SDS bertujuan menyelubungi molekul protein. Penyelubungan ini menyebabkan interaksi non-kovalen terganggu sehingga molekul protein dalam struktur primer. Anion SDS berikatan dengan rantai utama dengan rasio satu molekul SDS untuk dua residu asam amino. Merkaptoetanol atau ditiotreitol juga
ditambahkan untuk mereduksi ikatan disulfida. Kompleks SDS dengan protein terdenaturasi mempunyai jumlah muatan negatif yang sebanding dengan ukuran protein. Muatan negatif yang terdapat pada ikatan SDS ini jauh lebih besar daripada muatan pada protein asli. Kompleks protein-SDS kemudian dielektroforesis, sehingga semua molekul protein bergerak menuju kutub positif. Ketika elektroforesis selesai, protein dalam gel dapat ditampakkan oleh pewarnaan dengan perak atau zat warna seperti Coomasie Blue, yang akan menampakkan beberapa pita. Coomasie blue berikatan dengan protein berdasarkan interaksi ionic antara gugus sulfit pada
Coomasie blue dengan asam amino basa, dan interaksi hidrofobik cincin Coomasie blue (Hames 2002).
Data pemurnian enzim yang diperoleh dari elektroforesis tidak selalu menunjukkan daya katalitik enzim sebenarnya karena adanya kontaminan, isoenzim, atau enzim lain dari kelas yang sama. Kekurangan ini dapat diatasi dengan meneliti aktivitas enzim sesudah elektroforesis gel. Zimogram merupakan cara menganalisa aktivitas kitinolitik yang sederhana, sensitif, dapat dikuantisasi dan fungsional (Leber dan Balkwil 1997).
III. METODOLOGI
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan April sampai Juli 2010 di
Laboratorium Bioteknologi Hasil Perairan, Laboratorium Biokimia Hasil Perairan, Laboratorium Mikrobiologi Hasil Perairan, Laboratorium Bahan Baku Hasil Perairan Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan. Laboratorium Bioteknologi Hewan, Laboratorium Kimia dan Biokimia, Ruang Pendingin, Pusat Antar Universitas. Laboratorium Terpadu Fakultas Kedokteran Hewan, Institut Pertanian Bogor.
3.2 Bahan dan Alat
Bahan yang digunakan dalam penelitian ini terdiri dari bahan utama yakni ikan bandeng dalam keadaan post-rigor, bahan-bahan untuk ektraksi kasar (buffer Tris HCl 0,1 M pH 7,4, akuades), presipitasi (ammonium sulfat teknis), dialisis (Kantong dialisis, buffer Tris HCl pH 7,4), uji aktivitas katepsin [hemoglobin (Sigma), buffer tris 0,1 pH 7,4, tirosin (Applichem), akuades, TCA 5%, folin (Merck), HCl 1 N)], uji kadar protein [pereaksi Bradford, bovine serum albumin (Applichem)].
Alat yang digunakan pada penelitian ini antara lain inkubator (Thermoline), sentrifuse suhu dingin (Himac), spektrofotometer (Yamato), pH meter, tabung dialisis, kertas saring Whatman no.1 dan erlenmeyer.
3.3 Metode Penelitian
Penelitian ini dilakukan melalui beberapa tahap, yaitu preparasi sampel berupa ikan bandeng pada tahap post-rigor yang diambil bagian dagingnya. Tahap selanjutnya yakni pemurnian enzim katepsin semi murni yang meliputi ektraksi kasar, presipitasi, dan dialisis. Tahapan metode penelitian ini dapat dilihat pada Gambar 7.
Gambar 7. Diagram alir kerja penelitian pembuatan katepsin semi murni
Ikan bandeng dalam keadaan post-rigor
Preparasi
Daging
Ekstraksi kasar
Enzim katepsin kasar Pengukuran aktivitas enzim dan kadar protein Presipitasi
(30%, 40%, 50%, 60%, 70%, 80%) (b/v)
Katepsin semi murni 1 Pengukuran aktivitas enzim dan kadar protein
Dialisis
(2 jam, 4 jam 6 jam, 8 jam)
Katepsin semi murni 2 Pengukuran aktivitas enzim dan kadar protein SDS-PAGE dan Zimogram
3.3.1 Ekstraksi katepsin kasar (Dinu et al. 2002)
Ekstraksi dilakukan dengan preparasi sampel untuk memperoleh ektrak kasar katepsin dengan cara ikan dimatikan, kemudian daging ikan dibedah dengan cepat dan dicuci untuk menghilangkan darah. Daging ikan diambil dan disuspensikan dalam akuades dengan perbandingam daging ikan dan akuades sebesar 1:1, lalu dihomogenisasi pada suhu 0 °C.
Ektrak daging hasil homogenisasi disentrifugasi pada 600xg selama 10 menit dan supernatan yang diperoleh kemudian disentrifugasi lagi pada 10000xg selama 10 menit. Pelet yang dihasilkan dari hasil sentrifugasi kemudian dilarutkan dalam buffer Tri-HCl 0,1 M pH 7,4 dengan jumlah yang sama seperti jumlah akuades tadi dan disentrifugasi pada 4000xg selama 10 menit. Supernatan (ekstrak kasar katepsin) yang diperoleh merupakan protein utama dari mitokondria dan lisosom yang siap untuk diteliti aktivitasnya lebih lanjut.
3.3.2 Presipitasi dan dialisis
Katepsin semi murni diperoleh dengan mengendapkan ektrak kasar katepsin menggunakan ammonium sulfat dengan tingkat kejenuhan 30%, 40%, 50%, 60%, 70% dan 80% (b/v). Pengendapan dilakukan dengan menambahkan garam ammonium sulfat ke dalam supernatan sedikit demi sedikit dan disentrifugasi pada 12000xg selama 30 menit.
Pelet dilarutkan dalam buffer Tris HCl 0,1 M pH 7,4. Langkah selanjutnya yakni dialisis. Dialisis dilakukan dalam buffer Tris HCl pH 7,4 menggunakan kantong selofan berukuran 12 kDa, dengan waktu dialisis 2, 4, 6, dan 8 jam. Tahap presipitasi dan dialisis ini dilakukan pada suhu ≤ 4 °C.
3.3.3 Karakterisasi katepsin
Karakterisasi dilakukan terhadap hasil dialisis dengan aktivitas spesifik yang tertinggi. Karakterisasi meliputi penentuan suhu optimum, pH optimum, pengaruh ion logam dan penentuan konsentrasi substrat optimum.
3.3.3.1 Karakterisasi suhu
Karakterisasi suhu dilakukan dengan melakukan variasi suhu inkubasi pada saat pegujian aktivitas katepsin dengan suhu20, 30, 40, 50, 60, dan 70 °C. Pada waktu pengujian, hemoglobin sebagai substratnya dibuat dengan konsentrasi 2% pH 2. Sebanyak 0,5 mL dari larutan substrat, 0,1 mL larutan buffer Tris pH 7,4 diinkubasi dengan 0,1 mL larutan enzim pada variasi suhu (20, 30, 40, 50, 60, 70 °C) selama 10 menit. Reaksi dihentikan dengan penambahan 2 mL TCA 5% (w/v). Campuran disaring dan 1 mL filtrat hasil hasil penyaringan ditambah dengan 1 mL pereaksi folin. Selanjutnya diinkubasi kembali pada suhu 37 °C selama 20 menit. Campuran kemudian diukur dengan spektrofotometer pada panjang gelombang 750 nm. Selain itu, dilakukan pula pengukuran untuk larutan blanko dan larutan standar dengan prosedur yang sama seperti larutan sampel hanya untuk larutan blanko dan larutan standar enzimnya digantikan dengan akuades dan tirosin.
3.3.3.2 Karakterisasi pH
Karakterisasi pH dilakukan dengan melakukan variasi pH buffer dan pH substrat yakni pH hemoglobin 2% dengan variasi pH yakni 2, 3, 4, 5, 6, dan 7. Pada waktu pengujian, hemoglobin sebagai substratnya dibuat dengan konsentrasi 2% dan variasi pH 2, 3, 4, 5, 6, dan 7. Sebanyak 0,5 mL dari larutan substrat, 0,1 mL larutan buffer dengan variasi pH (2, 3, 4, 5, 6, dan 7) diinkubasi dengan 0,1 mL larutan
enzim pada 37 °C selama 10 menit. Reaksi dihentikan dengan penambahan 2 mL TCA 5% (w/v). Campuran disaring dan 1 mL filtrat hasil hasil penyaringan
ditambah dengan 1 mL pereaksi folin. Selanjutnya diinkubasi kembali pada suhu 37 °C selama 20 menit. Campuran kemudian diukur dengan spektrofotometer pada panjang gelombang 750 nm. Selain itu, dilakukan pula pengukuran untuk larutan blanko dan larutan standar dengan prosedur yang sama seperti larutan sampel hanya untuk larutan blanko dan larutan standar enzimnya digantikan dengan akuades dan tirosin.
3.3.3.3 Karakterisasi konsentrasi substrat
Karakterisasi konsentrasi subtrat dilakukan dengan mengubah konsentrasi substrat hemoglobin dengan variasi konsentrasi (½%, 1%, 1 ½%, 2%, 2 ½%, 3%, 3 ½%, 4%, dan 4 ½% (b/v)). Pada waktu pengujian, hemoglobin sebagai substratnya dibuat dengan konsentrasi ½%, 1%, 1 ½%, 2%, 2 ½%, 3%, 3 ½%, 4%, dan 4 ½% (b/v) pH 2. Sebanyak 0,5 mL dari larutan substrat, 0,1 mL larutan buffer Tris pH 7,4 diinkubasi dengan 0,1 mL larutan enzim pada variasi suhu (20, 30, 40, 50, 60, 70 °C) selama 10 menit. Reaksi dihentikan dengan penambahan 2 mL TCA 5% (w/v). Campuran disaring dan 1 mL filtrat hasil hasil penyaringan ditambah dengan 1 mL pereaksi folin. Selanjutnya diinkubasi kembali pada suhu 37 °C selama 20 menit. Campuran kemudian diukur dengan spektrofotometer pada panjang gelombang 750 nm. Selain itu, dilakukan pula pengukuran untuk larutan blanko dan larutan standar dengan prosedur yang sama seperti larutan sampel hanya untuk larutan blanko dan larutan standar enzimnya digantikan dengan akuades dan tirosin.
3.3.3.4 Karakterisasi pengaruh ion logam
Karakterisasi pengaruh ion logam dilakukan dengan menambahkan ion logam monovalen (NaCl), bivalen (BaCl2 dan CaCl2), serta trivalen (AlCl3 dan FeCl3). Pada
waktu pengujian, hemoglobin sebagai substratnya dibuat dengan konsentrasi 2% pH 2. Sebanyak 0,5 mL dari larutan substrat, 0,1 mL larutan buffer Tris pH 7,4 dan 0,1 mL larutan logam(NaCl, BaCl2, CaCl2, AlCl3 dan FeCl3) diinkubasi dengan
0,1 mL larutan enzim pada 37 °C selama 10 menit. Reaksi dihentikan dengan penambahan 2 mL TCA 5% (w/v). Campuran disaring dan 1 mL filtrat hasil hasil penyaringan ditambah dengan 1 mL pereaksi folin. Selanjutnya diinkubasi kembali pada suhu 37 °C selama 20 menit. Campuran kemudian diukur dengan spektrofotometer pada panjang gelombang 750 nm. Selain itu, dilakukan pula pengukuran untuk larutan blanko dan larutan standar dengan prosedur yang sama seperti larutan sampel hanya untuk larutan blanko dan larutan standar enzimnya digantikan dengan akuades dan tirosin.
3.4 Analisis
3.4.1 Aktivitas katepsin (Dinu et al. 2002)
Aktivitas proteolitik dari katepsin diuji menggunakan hemoglobin sebagai substratnya dengan konsentrasi 2% pH 2. Sebanyak 0,5 ml dari larutan substrat, 0,1 mL buffer Tris pH 7,4 diinkubasi dengan 0,1 mL larutan enzim pada 37 °C selama 10 menit. Reaksi dihentikan dengan penambahan 2 mL TCA 5% (w/v). Campuran disaring, dan 1 mL filtrat hasil hasil penyaringan ditambah dengan 1 mL pereaksi folin. Campuran kemudian diukur dengan spektrofotometer pada panjang gelombang 750 nm. Selain itu, dilakukan pula pengukuran untuk larutan blanko dan larutan standar dengan prosedur yang sama seperti larutan sampel hanya untuk larutan blanko dan larutan standar enzimnya digantikan dengan akuades dan tirosin. Unit didefinisikan sebagai banyaknya enzim yang dapat mengubah substrat menjadi 1µmol tirosin dalam 1 menit.
Aktivitas enzim katepsin dapat dihitung dengan rumus berikut: UA = (Absorbansi sampel – absorbansi blanko) x P x 1 (Absorbansi standar – absorbansi blanko) T
Keterangan: UA = jumlah tirosin yang dihasilkan per mL enzim per menit P = faktor pengenceran
T = waktu inkubasi
3.4.2 Pengukuran konsentrasi protein (Bradford 1976)
Konsentrasi protein ditentukan menggunakan metode Bradford dengan bovine
serum albumin sebagai standar. Persiapan pereaksi Bradford dilakukan dengan cara
melarutkan 5 mg coomasive brilliant blue G-250 dalam 2,5 mL etanol 95% (v/v), lalu ditambahkan dengan 5 mL asam fosfat 85% (v/v). Jika telah larut dengan sempurna lalu ditambahkan akuades hingga 250 mL dan disaring dengan kertas saring Whatman no. 1 dan diencerkan 5 kali sesaat sebelum digunakan.
Konsentrasi protein ditentukan menggunakan metode Bradford dengan cara 0,1 mL enzim dimasukkan ke dalam tabung reaksi. Kemudian ditambahkan sebanyak
5 mL pereaksi Bradford, diinkubasi selama 5 menit dan diukur dengan spektrofotometer pada panjang gelombang 595 nm. Demikian pula untuk larutan
standar dilakukan sama seperti larutan sampel dengan konsentrasi antara 0,1-1,0 mg/mL. Tahap berikutnya adalah membuat kurva standar dengan absorbansi
sebagai ordinat (sumbu y) dan konsentrasi protein sebagai absis (sumbu x). Berdasarkan kurva tersebut dapat ditentukan konsentrasi protein dalam sampel. Tabel
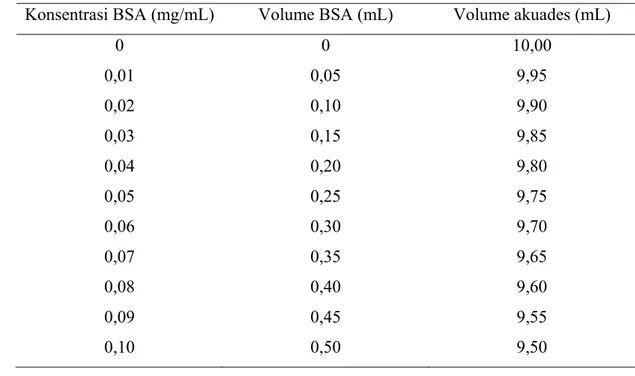
komposisi volume larutan dengan pembuatan larutan standar dengan konsentrasi 0,01-0,10 mg/ml dari larutan stok BSA konsentrasi 2 mg/ml disajikan pada Tabel 3.
Tabel 3. Pembuatan larutan standar BSA konsentrasi 0,01 – 0,10 mg/mL Konsentrasi BSA (mg/mL) Volume BSA (mL) Volume akuades (mL)
0 0 10,00 0,01 0,05 9,95 0,02 0,10 9,90 0,03 0,15 9,85 0,04 0,20 9,80 0,05 0,25 9,75 0,06 0,30 9,70 0,07 0,35 9,65 0,08 0,40 9,60 0,09 0,45 9,55 0,10 0,50 9,50
3.4.3 Penentuan berat molekul dengan SDS-PAGE dan zimogram (Laemmli 1970)
Metode SDS-PAGE yang dikerjakan dalam penelitian ini menggunakan 4% stacking gel dan 8% gel akrilamid. Konsentrasi akrilamid yang digunakan dalam analisis ini adalah 8%. Pewarnaan yang dilakukan adalah pewarnaan perak. Deteksi SDS-PAGE dilakukan dengan melepaskan gel hasil elektroforesis dari cetakan dan diukur jarak migrasi bromphenol blue. Analisis zimogram dilakukan dengan cara gel
akrilamid ditambahkan substrat hemoglobin 0,5% dan dikopolimerisasi. Komposisi pembuatan gel penahan dan pemisah SDS-PAGE dapat dilihat padaTabel 4.
Tabel 4. Komposisi gel penahan dan pemisah SDS-PAGE
Komponen Gel pemisah (8%) Gel penahan (4%) Larutan stok akrilamid 2,66 ml 0,67 ml
Buffer gel pemisah 2,5 ml - Buffer gel pengumpul - 1,25 ml
Akuades 3, 185ml 3,0 ml
APS 10% 50µl 50µl
TEMED 50µl 50µl
Pewarnaan dilakukan etelah dilakukan elektroforesis, gel untuk SDS dilarutkan dalam coomasie blue. Marker dan zimogram dipotong. Marker dilarutkan dalam coomasie blue, sedangkan zimogram dilarutkan dalam Triton-X 2,5%.
Marker, SDS dan zimogram dishaker pada suhu ruang selama 1 jam. Larutan
Triton-X pada zimogram diganti dengan buffer asetat 0,1 M pH dan diinkubasi 40 ºC selama 30 menit. SDS setelah 1 jam diinkubasi 70 ºC selama 10 menit. Pewarnaan untuk SDS dan zimogram dilakukan dengan menggunakan coomasie blue. Setelah itu dilakukan staining (metanol absolut 200 mL, asam asetat absolut 50%, dan akuades 250 mL) dan ditambakan busa untuk menyerap warna. Penentuan bobot molekul dengan SDS PAGE dilakukan dengan silver staining. Pewarnaan silver staining dilakukan sebagai berikut: Gel dilakukan perendaman dalam larutan fiksasi 25% metanol dan 15% asam asetat) selama 2 jam, kemudian dicuci dengan etanol 35% selama 3 x 20 menit. Larutan diganti dengan enhancer (0,1 g Na2S2O3.5H20 dalam
500 mL akuades) selama 2 menit. Cuci dengan dd H20 selama 3x20 detik. Larutan
silver nitrat (0,4 g AgNO3 + 700mL formaldehida dalam 200 mL akuades)
ditambahkan selama 30 menit, kemudian cuci lagi dengan ddH20 2 x 20 detik dan
ditambahkan larutan A (15 g Na2CO3 +120 mL formaldehida), dan terakhir
IV. HASIL DAN PEMBAHASAN
4.1 Pemurnian Katepsin
Pemurnian katepsin dilakukan dengan ektraksi secara kasar melalui sentrifugasi diferensiasi, presipitasi dengan garam ammonium sulfat, serta dialisis dengan menggunakan kantong dialisis berukuran 12 MWCO.
4.1.1 Ekstraksi kasar
Pemurnian katepsin diawali dengan ektraksi kasar dari daging ikan bandeng yang sudah memasuki tahap post-rigor. Pemilihan fase ini mengacu pada penelitian terdahulu yang dilakukan Fentiana (2009) yang menyatakan bahwa pada tahap
post-rigor, aktivitas katepsin berada pada aktivitas tertinggi dibandingkan pada fase-fase
sebelumnya sehingga akan meningkatkan rendemen katepsin yang dihasilkan. Pada tahap ekstraksi, pemilihan buffer Tris-HCl pH 7,4 dinilai sudah sesuai. Hal ini sesuai dengan pendapat dari Whitaker (1994) yang menyatakan bahwa ekstraksi enzim sebaiknya menggunakan buffer untuk mengontrol pH dekat dengan 7,5 dan kekuatan ion 0,1-0,5. Buffer diperlukan untuk melindungi enzim dari sejumlah besar asam yang dilepaskan dari vakuola pada saat pecahnya sel. Ekstrak kasar yang dihasilkan memiliki aktivitas spesifik sebesar 0,8598 U/mg dengan kadar protein sebesar 0,1163 mg/mL. Sentrifugasi yang dilakukan pada tahap ekstraksi kasar ialah sentrifugasi metode diferensiasi. Penelitian Toyohara et al. (1981) menyebutkan bahwa ekstrak kasar katepsin A yang berasal dari carp muscle memiliki aktivitas spesifik sebesar 0,279 U/mg.
Sentrifugasi metode diferensiasi diawali dengan sentrifugasi tingkat pertama, dimana hasil pada tingkat pertama ini pelet yang dihasilkan dibuang, kemudian pada sentrifugasi tingkat kedua supernatan kembali disentrifugasi pada kecepatan yang tinggi untuk memisahkan partikel yang berukuran sedang. Pemisahan dapat dicapai melalui sentrifugasi metode diferensiasi dapat ditingkatkan dengan mengulang resuspensi (dua atau tiga kali) pada sentrifugasi tahap ketiga, pelet yang didapatkan dihomogenisasi dengan media yang sesuai dan disentrifugasi kembali. Selanjutnya akan didapatkan supernatan dengan partikel yang kecil (Rana 2006).
Penelitian yang dilakukan Dinu et al. (2002) menyebutkan bahwa pada sentrifugasi tingkat pertama dilakukan sentrifugasi pada kecepatan 600xg selama 10 menit. Sentrifugasi tingkat kedua dilakukan sentrifugasi pada kecepatan 10000xg selama 10 menit. Sentrifugasi tahap ketiga dilakukan sentrifugasi pada kecepatan 4000xg selama 10 menit.
Prinsip dari sentrifugasi itu sendiri ialah berdasarkan fenomena bahwa partikel yang tersuspensi di dalam suatu wadah akan mengendap ke dasar wadah karena pengaruh gravitasi. Laju pengendapan tersebut dapat ditingkatkan dengan cara meningkatkan pengaruh gravitasional terhadap partikel. Hal ini dapat dilakukan dengan menempatkan tabung berisi suspensi partikel ke dalam rotor suatu mesin sentrifugasi kemudian diputar dengan kecepatan tinggi (Yuwono 2008).
4.1.2 Presipitasi
Ekstrak kasar yang diperoleh selanjutnya dipresipitasi menggunakan ammonium sulfat. Metpde presipitasi dibagi menjadi 2 grup utama, yakni (1) metode kelarutan protein dikurangi dan presipitasi dilakukan dengan mengubah beberapa sifat fisika-kimia solvent seperti pH, konstanta dielektrik, kekuatan ionik, dan tersedianya air. (2) Metode presipitasi protein yang disebabkan oleh interaksi diantara protein dan agen presipitasi (Sivasankar 2005). Pada penelitian ini metode yang dipakai untuk presipitasi ialah metode yang kedua.
Tiap presipitasi protein memiliki karakteristik pada konsentrasi reagen yang berbeda, pada ammonium sulfat persen presipitasi berselang antara 20%-100%, ini dianggap cukup untuk presipitasi (Bisswanger 2004). Presipitasi dapat dilakukan dengan penambahan garam seperti ammonium sulfat, polimer seperti polyethylene glycol (PEG), atau larutan organik seperti aseton atau alkohol (Scopes 1994 diacu dalam Kumar et al. 2003). Pada penelitian ini ammonium sulfat dipilih sebagai agen presipitasi, ammonium sulfat dipilih karena menurut Javois (1999) presipitasi dengan ammonium sulfat dianggap cepat dan murah. Aktivitas spesifik dan kadar protein setelah mengalami pengendapan dengan ammonium sulfat disajikan pada Gambar 8 dan Gambar 9.
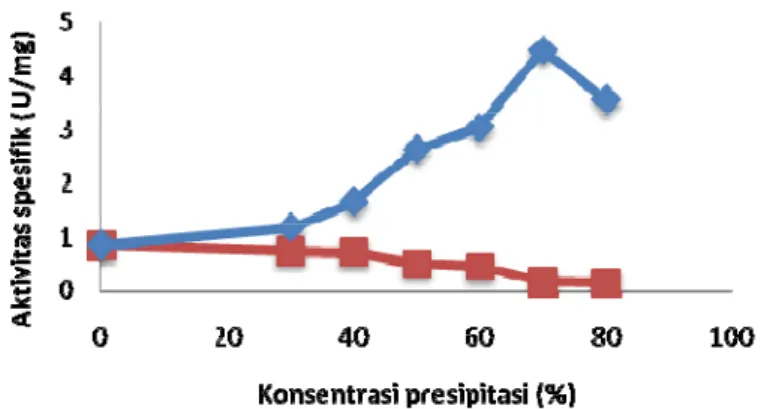
Gambar 8. Aktivitas spesifik katepsin setelah pengendapan dengan ammonium sulfat Aktivitas spesifik (pelet) Aktivitas spesifik (supernatan)
Gambar 9. Kadar protein terlarut setelah pengendapan dengan ammonium sulfat Kadar protein (pelet) Kadar protein (supernatan)
Berdasarkan Gambar 8 dapat dilihat bahwa terdapat peningkatan aktivitas spesifik pelet pada beberapa tingkat konsentrasi ammonium sulfat dan mencapai aktivitas optimum pada pelet dengan konsentrasi ammonium sulfat 70%, sementara aktivitas spesifik pada supernatan menunjukkan penurunan aktivitas spesifik. Selama proses presipitasi terjadi penurunan kadar protein dalam supernatan, dan sebaliknya terjadinya peningkatan konsentrasi dalam pelet. Kondisi ektrsaksi yang optimum ditunjukkan oleh aktivitas yang paling tinggi dalam endapan (pelet). Enzim yang dihasilkan dari presipitasi 70% memiliki aktivitas spesifik sebesar 4,4643 U/mg dengan kadar protein sebesar 0,2016 mg/mL. Penelitian Toyohara et al. (1981)
menyebutkan bahwa katepsin A yang berasal dari carp muscle pada hasil pengendapan sulfat didapatkan aktivitas spesifik sebesar 3,43 U/mg.
Kelarutan protein (pada pH dan temperatur tertentu) akan meningkat sejalan dengan peningkatan konsentrasi garam (salting in). Peningkatan kelarutan protein akan meningkatkan kekuatan ion larutan. Penambahan garam dengan konsentrasi tertentu kelarutan protein menurun (salting out). Molekul air yang berikatan dengan ion-ion garam semakin banyak yang menyebabkan penarikan selubung air yang mengelilingi permukaan protein sehingga mengakibatkan protein saling berinteraksi, beragregasi, dan kemudian mengendap (Harris 1989).
4.1.3 Dialisis
Pellet yang diperoleh dari pengendapan dengan garam ammonium sulfat (NH4)2SO4, kemudian didialisis menggunakan membran selofan berukuran 12 kDa.
Kegunaan utama dialisis ialah untuk pemekatan, pembuangan garam, dan pemurnian bahan-bahan seperti protein, hormon, dan enzim. Zat tertahan ialah berisi protein dengan ukuran molekul yang lebih besar dari ukuran pori dari Molecular Weight Cut
Off (MWCO) (Sanagi 2001). Prinsip dari dialisis ialah aplikasi preparasi enzim ke
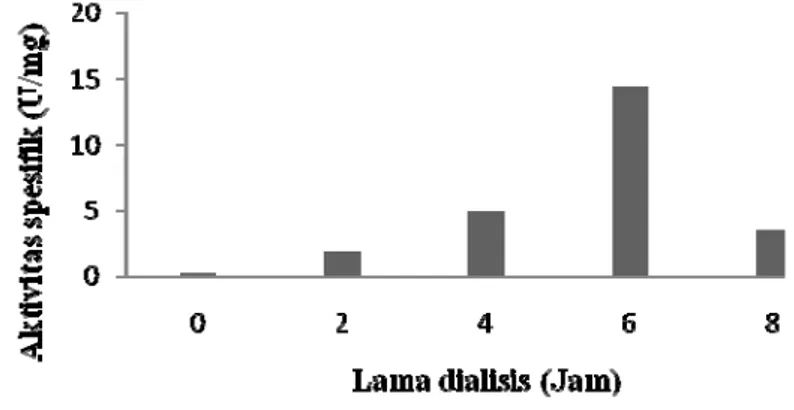
dalam kantong dialisis yang terbuat dari membran semi-permeabel yang memungkinkan molekul berukuran kecil untuk bermigrasi (Grogan 2009). Aktivitas spesifik dan kadar protein dari sampel disajikan pada Gambar 10 dan Gambar 11.
Tabel 5. Peningkatan aktivitas katepsin pada berbagai tahap pemurnian
Tahapan Volume (ml) Aktivitas
(U/ml) Kadar protein (mg/ml) Aktivitas spesifik (U/mg) Total protein (mg) Total aktivitas (U) Yield (%) Kelipatan pemurnian Ekstrak kasar 500 0,1 0,1163 0,8598 58,15 50 100 1 Presipitasi 10 0,9 0,2016 4,4643 2,02 9 0,18 5,20 Dialisis 6 2 0,1385 14,4404 0,831 12 1,33 16,80
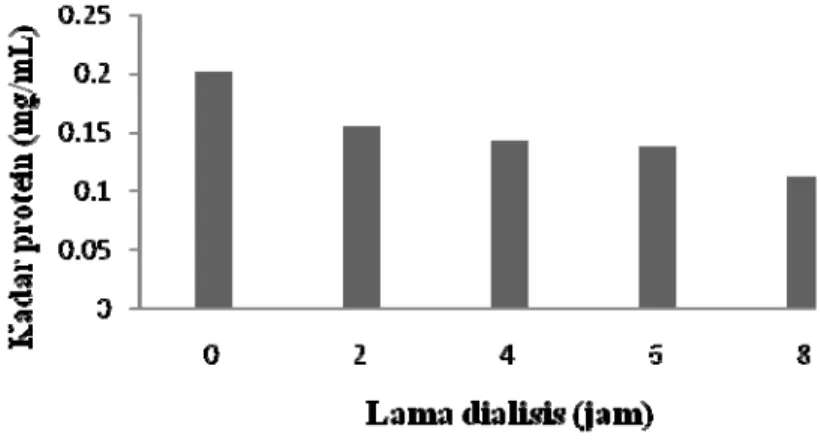
Gambar 11 Kadar protein zat terlarut setelah didialisis
Gambar 10 menunjukkan terjadinya peningkatan aktivitas spesifik pada pellet yang didialisis. Peningkatan terjadi sampai titik optimum tertentu. Pada penelitian ini titik optimum untuk proses dialisis ialah 6 jam. Enzim yang dihasilkan dari tahap dialisis memiliki aktivitas spesifik sebesar 14,4404 U/mL dengan kadar protein sebesar 0,1385 mg/mL. Gambar 11 menunjukkan bahwa kadar protein selama dialisis mengalami penurunan selama dialisis. Hal ini disebabkan karena protein-protein yang berukuran lebih kecil dari 12 kDa sudah terbuang selama dialisis.
4.2 Karakterisasi Enzim Katepsin yang Dihasilkan
Karakterisasi dilakukan untuk melihat seberapa besar pengaruh kondisi lingkungan terhadap aktivitas enzim. Karakterisasi juga dapat diketahui kondisi optimum lingkungan untuk mendapatkan enzim dengan aktivitas yang tinggi. Karakterisasi yang dilakukan pada enzim katepsin berupa konsentrasi substrat, tingkat keasaman (pH), suhu, dan pengaruh logam.
4.2.1 Tingkat keasaman (pH)
Pengikatan antara enzim dengan substrat dan reaksi katalisisnya bergantung pada interaksi antara substrat dengan rantai samping asam amino yang menyusun sisi aktif enzim (Bender 2002). Peristiwa ini harus berada pada keadaan ionisasi yang tepat untuk mengikat, dan hal ini tergantung pada pH medium.
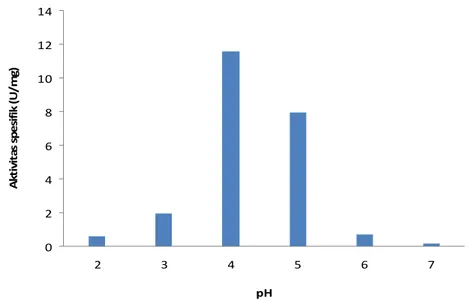
Semua reaksi enzim dipengaruhi oleh pH medium tempat reaksi terjadi. Setiap enzim memiliki pH optimum yang khas. Profil aktivitas pH enzim menggambarkan pH pada saat pemberi dan penerima proton yang penting pada sisi katalitik enzim berada pada tingkat ionisasi yang diinginkan. pH tertentu dapat menyebabkan enzim terdenaturasi yang menyebabkan enzim kehilangan aktivitas biologisnya (Lehninger 1993). Pengaruh aktivitas spesifik terhadap tingkat keasaman disajikan pada Gambar 12. 0 2 4 6 8 10 12 14 2 3 4 5 6 7 pH A kti vi ta s sp es ifik (U /m g)
Gambar 12 Pengaruh pH terhadap aktivitas spesifik katepsin
Gambar 12 memberikan informasi bahwa tingkat keasamaan berpengaruh terhadap aktivitas spesifik enzim katepsin. Enzim katepsin digambarkan memiliki aktivitas spesifik optimal pada pH 4 sebesar 11,5523 U/mg. Hal ini sesuai dengan pendapat dari Choi et al. (2005) bahwa enzim katepsin aktif pada pH asam. Sementara penelitian yang dilakukan Toyohara et al. (1981) pada carp muscle, bahwa katepsin A memiliki pH optimum 5. Sementara penelitian yang dilakukan oleh Balti et al. (2010) terhadap katepsin D yang berasal dari hepatopankreas sotong memiliki aktivitas spesifik optimum pada pH 3. Penelitian yang dilakukan oleh Krause et al. (2010) terhadap enzim katepsin D yang berasal dari daging ikan ostrich
menyebutkan bahwa katepsin D memiliki aktivitas optimal pada pH 4. Penelitian lain yang dilakukan oleh Jiang et al. (2002) terhadap katesin D ikan tongkol dan ikan bandeng, menyatakan bahwa katepsin D memiliki aktivitas tertinggi pada pH 5,04 (ikan tongkol) dan pH 4,91 (ikan bandeng).
4.2.2 Suhu
Seperti halnya reaksi kimia, tingkat enzim mengkatalisis reaksi akan meningkat sejalan dengan peningkatan suhu (Polgar 1990). Setiap enzim memiliki kisaran suhu tertentu untuk mencapai aktivitas yang optimum. Di luar kisasan suhu tersebut enzim akan tidak aktif atau aktivitasnya akan terhambat. Hal ini terjadi karena suhu menyediakan pasokan energi termal untuk memecah beberapa atraksi intramolekul grup polar (ikatan hidrogen, atraksi dipol-dipol, interaksi inonik) serta kekuatan hidropobik diantara grup non polar di dalam struktur enzim. Pengaruh suhu terhadap aktivitas spesifik enzim katepsin digambarkan pada Gambar 13.
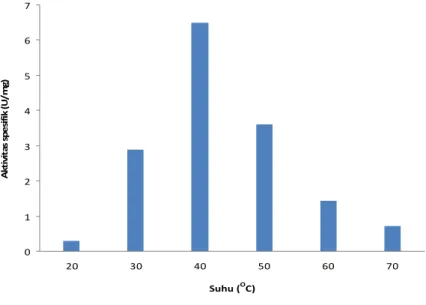
Gambar 13 Pengaruh suhu terhadap aktivitas spesifik katepsin
Berdasarkan Gambar 13 dapat dilihat bahwa peningkatan suhu akan menyebabkan peningkatan aktivitas spesifik enzim katepsin sampai pada titik tertentu. Sementara peningkatan suhu lebih lanjut akan membuat aktivitas spesifik
0 1 2 3 4 5 6 7 20 30 40 50 60 70 Suhu (OC) Akt iv it as s p es if ik (U /m g)
enzim menjadi menurun. Pada penelitian ini enzim katepsin memiliki aktivitas spesifik optimum pada suhu 40 °C dengan nilai aktivitas sebesar 6,4982 U/mg. Sementara penelitian yang dilakukan oleh Balti et al. (2010) terhadap katepsin D yang berasal dari hepatopankreas sotong memiliki aktivitas spesifik optimum pada 50 ºC. Penelitian yang dilakukan oleh Krause et al. (2010) terhadap enzim katepsin D yang berasal dari daging ikan ostrich menyebutkan bahwa katepsin D memiliki aktivitas optimal pada suhu 45 ºC. Penelitian lain yang dilakukan oleh Jiang et al. (2002) terhadap katesin D ikan tongkol dan ikan bandeng, menyatakan enzim katepsin pada ikan tongkol akan memiliki aktivitas tertinggi pada suhu 45 °C dan pada ikan bandeng pada suhu 50 °C.
Suhu yang lebih tinggi akan membuat molekul lebih sering bertabrakan. Konsep ini berlaku juga untuk tumbukan antar molekul substrat dengan enzim. Hal ini disebabkan suhu yang tinggi akan mengkatalisis reaksi enzimatis. Namun, ketika kenaikan suhu melebihi titik tertentu akan menyebabkan gangguan terhadap struktur tersier enzim. Perubahan struktur tersier pada sisi aktif akan menghambat aktivitas katalitik enzim (Stoker 2010).
4.2.3 Pengaruh logam
Pengaruh logam dilakukan untuk melihat seberapa besar pengaruh logam tertentu terhadap kerja enzim. Logam yang dipilih dalam penelitian ini ialah logam monovalen, bivalen, dan trivalent. Pengaruh logam terhadap aktivitas spesifik enzim disajikan pada Gambar 14.
0 2 4 6 8 10 12 14 16
Kontrol NaCl BaCl2 CaCl2 FeCl3 AlCl3
Logam A kt ivit as sp esif ik ( U /m g )
Gambar 14 Pengaruh logam terhadap aktvitas spesifik
Gambar 14 menunjukkan bahwa keberadaan logam sangat berpengaruh terhadap aktivitas spesifik enzim. Keberadaan logam pada enzim akan menghambat kerja enzim, sehingga aktivitas spesifik enzim akan lebih kecil jika dibandingkan dengan enzim yang tanpa adanya logam. Berdasarkan Gambar 14 didapatkan informasi bahwa ion logam divalen akan menghambat kerja enzim tertinggi, dibandingkan dengan logam monovalen maupun trivalen.
Sementara penelitian yang dilakukan oleh Balti et al. (2010) terhadap katepsin D yang berasal dari hepatopankreas sotong, menyebukan bahwa aktivitas enzim katepsin D akan meningkat oleh keberadaan ion logam Mg2+, Ni2+, Zn2+, Cu2+, Cd2+, Sr2+, and Co2+. Sementara keberadaan ion logam Na+, K+, dan Ca2+ tidak akan berpengaruh terhadap aktivitas enzim katepsin D. Penelitian lain yang dilakukan oleh Jiang et al. (2002) terhadap katesin D ikan tongkol dan ikan bandeng, menyatakan bahwa keberadaan ion logam Na+ dan K+ akan meningkatkan aktivitas katepsin D,
sementara ion logam Mg2+, Sr2+, Fe2+, dan Hg2+ akan menghambat aktivitas katepsin D.
Kerja enzim dapat dihambat oleh zat penghambat atau inhibitor. Inhibitor non-kompetitif tidak bersaing dengan substrat untuk berikatan dengan enzim. Inhibitor jenis ini akan berikatan dengan enzim pada sisi yang berbeda (bukan sisi
aktif). Jika telah terjadi ikatan enzim-inhibitor, sisi aktif enzim akan berubah sehingga substrat tidak dapat berikatan dengan enzim. Banyak ion logam bekerja sebagai inhibitor non-kompetitif (Firmansyah et al. 2007).
4.2.4 Konsentrasi substrat
Konsentrasi substrat merupakan salah satu faktor yang berpengaruh terhadap jumlah produk yang dihasilkan. Substrat dibutuhkan oleh enzim untuk berikatan dengan sisi aktif enzim sehingga akan terbentuk produk. Pengaruh konsentrasi substrat terhadap aktivitas spesifik enzim disajikan pada Gambar 15.
Gambar 15. Pengaruh konsentrasi substrat terhadap aktivitas spesifik katepsin Gambar 15 menunjukkan bahwa konsentrasi substrat berpengaruh terhadap aktivitas spesifik enzim yang dihasilkan. Jika konsentrasi substrat dinaikkan, maka aktivitas spesifik cenderung akan meningkat sampai pada titik tertentu. Konsentrasi substrat sebesar 3% merupakan konsentrasi subtrat optimal untuk enzim katepsin dengan nilai aktivitas spesifik sebesar 9,3863 U/mg.
Semakin banyak molekul substrat yang tersedia, semakin sering molekul-molekul tersebut memasuki sisi aktif molekul-molekul enzim. Akan tetapi, terdapat keterbatasan dalam memacu kecepatan reaksi dengan cara menambahkan lebih banyak lagi substrat ke suatu konsentrasi enzim yang tetap. Pada suatu titik tertentu, konsentrasi substrat itu akan menjadi cukup tinggi sehingga semua sisi aktif pada
semua molekul enzim sudah ditempati oleh substrat. Segera setelah produk meninggkalkan sisi aktif, molekul substrat yang lain akan masuk. Pada konsentrasi substrat seperti ini, enzim itu dikatakan mengalami kejenuhan, dan laju reaksi ditentukan oleh kecepatan sisi aktif mengubah substrat menjadi produk. Ketika suatu enzim telah jenuh, satu-satunya cara untuk meningkatkan produktivitas ialah menambahkan lebih banyak lagi enzim (Campbell 2002).
4.2.5 Penentuan bobot molekul
Penentuan bobot molekul dilakukan menggunakan SDS-PAGE dan zimogram. Hasil analisis menggunakan SDS-PAGE dan zimogram dapat dilihat pada Gambar 16.
(A)
(B)
Gambar 16. Hasil SDS (A) dan zimogram (B)katepsin
Penetuan bobot molekul ditentukan berdasarkan kurva standar dimana pada SDS diketahui persamaannya Y= - 1,037x + 2,112 (Gambar 17), sementara pada
zimogram diketahui persamaannya Y= - 1,384x + 2,145 (Gambar 18) dimana Y= log berat molekul marker (kDa), sedangkan x= mobilitas relatif protein (cm).
Gambar 17. Kurva standar SDS-PAGE
Gambar 18. Kurva standar zimogram
Nilai Rf sendiri merupakan jarak migrasi marker/sampel dibagi dengan nilai run nya. Data jarak migrasi marker untuk SDS maupun bobot molekul standar SDS disajikan pada Tabel 6. Tabel 6 menggambarkan bahwa protein dengan bobot molekul yang kecil akan memiliki jarak migrasi yang besar atau jauh, sementara protein dengan bobot molekul yang besar akan memiliki jarak migrasi yang kecil.
Tabel 6. Jarak migrasi dari marker SDS beserta nilai RF dan bobot molekul dari masing-masing pita
Jarak marker RF marker BM marker (kDa) Log BM
0,8 0,1818 97 1,987 1,1 0,25 66 1,820 1,8 0,409 45 1,653 2,7 0,614 30 1,477 3,3 0,75 20,1 1,303 4,2 0,955 14,4 1,158
Untuk menentukan bobot molekul sampel, pertama kali jarak migrasi sampel diukur kemudian dibagi dengan nilai run nya untuk diketahui nilai RF nya. Persamaan standar SDS kemudian digunakan untuk menentukan bobot molekul sampel, nilai RF sampel yang telah diketahui dimasukkan dalam persamaan standar SDS. Nilai Y yang didapatkan belum merupakan nilai bobot molekul sampel, untuk menentukkannya nilai Y dianti-log kan terlebih dahulu.
Teknik zimogram dapat mendeteksi protein yang masih memiliki aktivitas katalitik. Perbedaan antara SDS-PAGE dan zimogram terletak pada penambahan substrat pada gel elektroforesis. Pada pembuatan gel untuk zimogram, komposisi gel ditambahkan hemoglobin 0,5% dengan tujuan protein yang mengandung katepsin akan mendegradasi substrat hemoglobin sehingga ketika dilakukan pewarnaan diperoleh zona bening pada pita protein. Pada Tabel 7 terlihat bahwa pada ektrak kasar enzim katepsin masih mempunyai banyak band yang berarti masih banyak molekul disini, termasuk protein yang berasal dari sel dan protein pengotor lainnya. Pada tahap dialisis terlihat adanya pengurangan jumlah band protein. Hal ini berati selama proses dialisis banyak menghilangkan protein. Pada Tabel 8 terlihat bahwa enzim katepsin baru terlihat aktivitas katalitiknya pada tahap presipitasi dan dialisis, pada tahap ini enzim katepsin teridentifikasi memiliki bobot molekul 88,67 kDa.
Sementara hasil penelitian yang dilakukan oleh Balti et al. (2010) terhadap katepsin D yang berasal dari hepatopankreas sotong (Sepia officinalis) terestimasi memiliki bobot molekul 37,5 kDa. Katepsin D yang berasal dari daging ikan ostrich memiliki bobot molekul 29,1 kDa (Krause et al. 2010). Penelitian lain yang dilakukan oleh Jiang et al. (2002) terhadap katesin D ikan tongkol dan ikan bandeng, menyatakan bahwa katepsin D pada ikan tongkol terestimasi sebesar 51 kDa dan pada ikan bandeng sebesar 54 kDa.
Tabel 7. Estimasi bobot molekul protein (kDa) pada setiap tahap pemurnian Ekstrak kasar tanpa pengenceran Ektrak kasar dengan pengenceran 2X Pengendapan dengan pengenceran 2x Pengendapan dengan pengenceran 5x Pengendapan dengan pengenceran 10x Dialisis dengan pengenceran 2x Dialisis dengan pengenceran 5x Dialisis dengan pengenceran 10x 93,45 35,18 88,52 104,17 104,17 98,66 98,66 98,66 22,79 22,79 35,19 48,73 37,15 39,22 48,73 46,15 18.35 15,59 24,07 37,15 18,35 26,82 26,82 18,35 15,59 17,38 18,35 22,80 19,37 12,58 15,59 14,77 18,35 13,25 12,88
Tabel 8. Estimasi bobot molekul enzim katepsin (kDa) pada setiap tahap pemurnian
Ekstrak kasar tanpa pengencera Ektrak kasar dengan pengenceran 2X Pengendapan dengan pengenceran 2x Pengendapan dengan pengenceran 5x Pengendapan dengan pengenceran 10x Dialisis dengan pengenceran 2x Dialisis dengan pengenceran 5x Dialisis dengan pengenceran 10x - - - 86,87 86,87 86,87 86,87 86,87
V. KESIMPULAN DAN SARAN
5.1 Kesimpulan
Metode pemurnian katepsin dilakukan dengan presipitasi menggunakan ammonium sulfat 70%, kemudian didialisis menggunakan kantong dialisis berukuran 12 MWCO selama 6 jam. Pemurnian secara ekstraksi kasar didapatkan aktivitas spesifik sebesar 0,8598 U/mg dan setelah dipresipitasi dengan konsentrasi pengendapan 70% didapatkan aktivitas spesifik sebesar 4,4643 U/mg dan setelah didialisis selama 6 jam didapatkan aktivitas spesifik sebesar 14,4404 U/mg.
Karakteristik enzim katepsin yang dihasilkan yaitu mempunyai suhu dan pH optimum 40 °C dan 4, konsentrasi substrat sebesar 3%, sementara keberadaan ion logam akan mengganggu atau menghambat aktivitas enzim. Ion logam divalen akan menghambat kerja enzim tertinggi, jika dibandingkan dengan logam monovalen maupun trivalen. Enzim katepsin teridentifikasi memiliki bobot molekul sebesar 86,87 kDa
5.2 Saran
Perlu dikaji lebih dalam mengenai aktivitas spesifik enzim katepsin setelah dimurnikan lebih lanjut dengan kromatografi kolom. Pemurnian tahap dialisis perlu dikaji mengenai pengaruh frekuensi pergantian buffer terhadap aktivitas spesifik yang dihasilkan, serta disarankan pada tahap dialisis dilakukan pemilihan ukuran kantong dialisis yang lebih kecil dari 12 kDa.
DAFTAR PUSTAKA
Abdurahman D. 2008. Biologi Kelompok Pertanian. Jakarta: Grafindo Media Pratama.
Allen C, Goll MB. 2003. Lysosomal Cysteine Proteases. Oxford: Oxford University Press.
Aoki T, Yamashita T, Ueno R. 2000. Distribution of cathepsins in red and white muscles among fish species. Fisheries Science. 66(4): 776-782.
Balti F, Noomen H, Kemel J, Naima NA, Guillochon D, and Moncef N. 2010. Cathepsin D from hepatopancreas of the cuttlefish (Sepia officinalis): purification and characterization. J. Agric. Food Chem. 19:10623–10630. Bisswanger H. 2004. Practical Enzymology. Germany: Wiley-VCH.
BRKP [Badan Riset Kelautan Perikanan]. 2007. Dukungan teknologi penyediaan produk perikanan. www.litbang.deptan.go.id [12 Maret 2010].
Bradford MM. 1976. A rapid and sensitive method for quantification of microgram
quantities of protein utilizing the principle of protein dye binding.
Anal Biochem 72: 234-254.
Bregman AN, Futon C. 1996. Enzyme Technology. New York: Springer Science Business Media.
Bender DA. 2002. Introduction to Nutrition and Metabolism. Vol. 1. New York: Taylor & Francis Inc.
Buxbaum E. 2007. Fundamental of Protein Structure and Function. New York: Springer Science.
Campbell N. 2002. Biologi. Rahayu, penerjemah. Jakarta: Erlangga. Terjemahan dari:
Biology.
Careno M. 2000. Aspartic Acid Proteases as Therapeutic Targets. Germany: Wiley-VCH.
Chang R. 2003. Kimia Dasar. Jakarta: Penerbit Erlangga.
Choi, Kang,and Lanier. 2005. Surimi and Surimi Seafood. USA: CRC Press.
Dinu D, Dumitru IF, Neichifor MT. 2002. Isolation and characterization of two chatepsin from muscle of Carrassius auratus gibelio. Roum. Biotecnol. Lett. 7(3): 753-758.
Elisabeth D. 1994. Immunopharmacology of Joints and Connective Tissue. San Diego: Academic Press.
Erwin E. 2010. Milkfish. Alabama: Auburn University.
Fentiana N. 2009. Peranan Enzim Protease Jeroan ikan bandeng (Chanos chanos) dalam proses kemunduran mutu. [Skripsi]. Bogor: Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Firmansyah R, Agus M, dan Umar R. 2007. Mudah dan Aktif Belajar Biologi. Bandung: Setia Purna Inves.
Ghufron M, Kardi H. 1997. Budidaya Kepiting dan Ikan Bandeng di Tambak Sistem
Polikultur. Semarang: Dahara Prize.
Grogan G. 2009. Practical Biotransformation. Postgraduates Chemistry Series. Chichester: John Willey & Sons Ltd.
Hames BD. 2002. Gel Electrophoresis of Protein. Oxford: Oxford University Press. Harrd NF. 1994. Protein Hydrolysis in a Seafood. Glasgow: Blackie Academic and
Professional.
Harris ELV. 1989. Protein Purification Methods: A Practical Approach. England: IRS Press.
Ilyas S. 1983. Teknologi Refrigerasi Hasil Perikanan. Jakarta: CV.Paripurna.
Javois JC. 1999. Immunocytochemical Method and Protocols. New Jersey: Humana Press Inc.
Jiang ST. 2000. Enzymes and their effect on seafood texture. Haard NF dan Simpson BK, editor. Di dalam Seafood Enzymes. New York: Marcel Dekker, Inc.
Jiang ST, Her YH, Lee JJ, and Jeng HW. 2002. Comparison of the cathepsin D from mackerel (Scomber australasicus) and milkfish (Chanos chanos) muscle.
Bioscience, Biotech, Biochem. 57(4): 571-577.
Kumar A, Igor Y, Galaev, dan Bo M. 2003. Isolation and Purification Protein. New York: Marcel Dekker Inc.
Kolodziedjska I, Sikorsi ZE. 1996. Neutral and alkaline muscle proteases of marine fish and invertebrates. Journal of Food Biochemistry. 20(12): 349-363.
Kuchel P dan Gregory BR. 2006. Biokimia. Jakarta: Penerbit Erlangga.
Krause J, Shonisani C. Tshidino, Tomohisa O, Yasuharu, Vaughan, Benesh S, Muramoto K, and Ryno JN. 2010. Purification and partial characterization of ostrich skeletal muscle cathepsin D and its activity during meat maturation.
Journal Meat Science. 87(3):196-201.
Lehninger AL. 1993. Dasar-Dasar Biokimia. Jilid I. M. Thenawidjaja, penerjemah. Jakarta: Erlangga. Terjemahan dari: Principle of Biochemistry.
Laemmli UK. 1970. Cleavage of structural protein during the assembly of the heat of bacteriophag T4. Nature. 227(10): 680-685.
Leber TM, Balkwil FR. 1997. Zymogram: A Single-step Staining Method for Quantitative of Proteolytic Activity on Subtrat Gel. Anal. Biochem 249: 24-28. Marshak DR .1996. Strategies for Protein Purification and Characterization. United
States of America: Cold Spring Harbor Laboratory Press.
Murtidjo BA. 2002. Budidaya dan Pembenihan Bandeng. Yogyakarta: Penerbit Kanisius.
Park JW. 2005. Surimi and Surimi Seafood. Second edition. CRC Press. Polgar L. 1990. Mechanism of Protease Action. Florida: CRC Press.
Rana SVS. 2006. Biotechniques Theory and Practice. New Delhi: Capital Offset Press.
Saanin H. 1984. Taksonomi dan Kunci Identifikasi Ikan Jilid I dan II. Bogor: Bina Cipta.
Salleh AB, Razak CN, Zaliha RN, Basri M. 2006. New Lipases and Proteases. New York: Nova Science Publisher.
Sanagi MS. 2001. Teknik Pemisahan dalam Analisis Kimia. Melaka: Percetakan Surya.
Shahidi F dan Botta JR. 1994. Seafoods Chemistry, Processing Technology and
Quality. Glasgow: Blackie Academic and Professional.
Shinya H. 2008. The Miracle of Enzyme. Bandung: Mizan Utama.
Sivasankar A. 2005. Biotechnology and Fermentation Process. Mumbai: Rachana Enterprises.
Stenes J. 1998. Foundation of Biochemistry. New York: Plenum Press.
Stoker HS. 2010. General, Organic, and Biological Chemistry. USA: Cengage Learning.
Sudjati K. 2008. Biokimia. Jakarta: Grafindo Pratama.
Sumardjo D. 2006. Pengantar Kimia. Buku panduan kuliah mahasiswa kedokteran. Jakarta: Penerbit Erlangga.
Toyohara H, Makinodan Y, and Ikeda S. 1981. Purification and properties of carp muscle cathepsin A. Bulletin of the Japanese Society of Scientific Fisheries. 48(8): 1145-1150.
Whitaker JR. 1994. Principles of Enzymology for The Food Science. Second Edition. New York: Marcel Dekker, Inc.
Yuwono T.2008. Biologi Molekular. Jakarta: Penerbit Erlangga.