METODOLOGI PENELITIAN Bahan dan Alat
Teks penuh
Gambar
Dokumen terkait
Dalam penelitian ini dilakukan regenerasi fotokatalis Ca1-xCoxTiO3 setelah mengalami proses degradasi senyawa metilen biru dengan radiasi sinar UV.. Katalis hasil
SINTESIS PARTIKEL NANOSPERIK TiO 2 MELALUI METODE HIDROTERMAL GELOMBANG MIKRO DAN SIFAT FOTOKATALITIKNYA UNTUK DEGRADASI BIRU
Dari aplikasi menggunakan larutan metilen biru dan limbah cair industri tekstil, batubara muda berpotensi untuk digunakan sebagai adsorben zat warna.. Kata
Pemaparan gas NO 2 dengan konsentrasi yang berbeda berpengaruh pada intensitas warna kompleks yang dibentuk pada larutan penyerap KI-amilum.. Konsentrasi gas NO 2 yang
Konsentrasi zat warna RB5 yang digunakan yaitu 10 mg/l. Percobaan degradasi zat warna dilakukan dengan variasi membran SB tanpa Ag dan TiO 2 , dengan TiO 2 saja dan
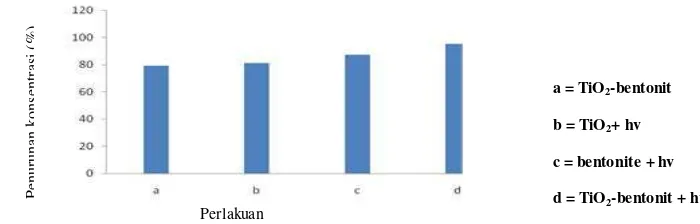
Dari penelitian yang telah dilakukan dapat disimpulkan bahwa persentase degradasi metilen biru sangat dipengaruhi oleh jumlah katalis ZnO yang ditambahkan, pH larutan
Dalam penelitian ini dilakukan regenerasi fotokatalis Ca1-xCoxTiO3 setelah mengalami proses degradasi senyawa metilen biru dengan radiasi sinar UV.. Katalis hasil
5 BAB II TINJAUAN PUSTAKA 2.1 Kajian Pustaka Penelitian yang berkaitan dengan sintesis fotokatalis yang bertujuan untuk mendegradasi zat warna metilen biru salah satunya