BAB 2
TINJAUAN PUSTAKA
2.1. Tanaman Kelapa
Tanaman kelapa tumbuh di daerah tropis. Tanaman kelapa merupakan tanaman serbaguna yang mempunyai nilai ekonomi tinggi. Seluruh bagian pohon kelapa dapat dimanfaatkan untuk kepentingan manusia. Hampir seluruh bagian pohon, dari akar, batang, daun sampai buahnya dapat digunakan untuk kebutuhan kehidupan manusia sehari-hari.
Pohon ini dapat tumbuh dan berbuah dengan baik di daerah dataran rendah dengan ketinggian 0-450 m dari permukaan laut. Pada ketinggian 450-1000 m dari permukaan laut, walaupun pohon ini dapat tumbuh, waktu berbuahnya lebih lambat, produksinya lebih sedikit dan kadar minyaknya rendah.
Ada dua pendapat mengenai asal usul kelapa, yaitu dari Amerika Selatan menurut D.F. Cook, Van Martius Beccari dan Thor Herjerdahl, dan dari Asia atau Indonesia Pasific menurut Berry, Werth, Mearil, Mayurathan, Lepesma, dan Pureseglove. Kata coco pertama kali digunakan oleh Vasco da Gama, atau dapat juga
disebut Nux Indica, al djanz al kindi, ganz-ganz, nargil, narlie, tenga, temuai, coconut. (Amin,S. 2009)
2.1.1. Buah Kelapa
Buah kelapa berbentuk bulat panjang dengan ukuran lebih kurang sebesar kepala manusia. Buah terdiri dari sabut (ekskarp dan mesokarp), tempurung (endokarp), daging buah (endosperm) dan air buah. Tebal sabut kelapa lebih kurang 5 cm dan tebal daging buah 1 cm atau lebih. (Ketaren,S. 2008)
Berat buah kelapa yang telah tua kira-kira 2 kg per butir. Buah kelapa digunakan hampir seluruh bagiannya. Daging buahnya dapat langsung dikonsumsi, bahan bumbu masakan, diproses menjadi santan kelapa, kelapa parut kering, minyak goreng atau minyak kelapa murni. Daging buah dapat dikeringkan menjadi kopra. Kopra itu dapat diproses menjadi minyak goreng, sabun, lilin, es krim, produk olekimia seperti asam lemak (fatty acid), fatty alcohol dan gliserin. (Amin, S. 2009)
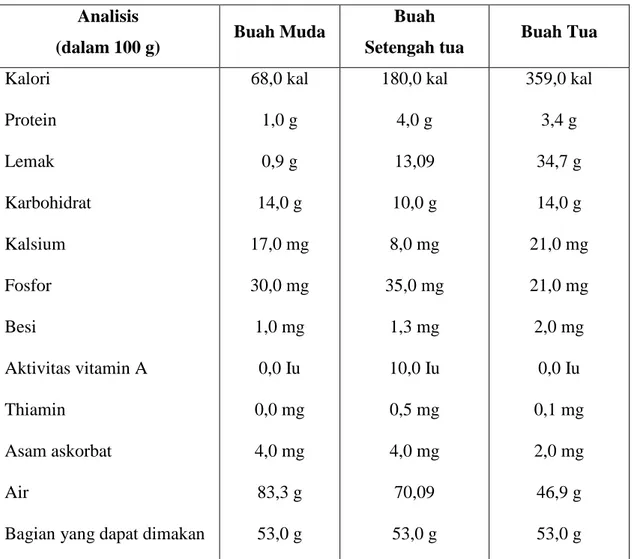
Tabel 2.1 Komposisi Kimia Daging Buah Kelapa pada Berbagai Tingkat Kematangan
Analisis
(dalam 100 g) Buah Muda
Buah
Setengah tua Buah Tua Kalori Protein Lemak Karbohidrat Kalsium Fosfor Besi Aktivitas vitamin A Thiamin Asam askorbat Air
Bagian yang dapat dimakan
68,0 kal 1,0 g 0,9 g 14,0 g 17,0 mg 30,0 mg 1,0 mg 0,0 Iu 0,0 mg 4,0 mg 83,3 g 53,0 g 180,0 kal 4,0 g 13,09 10,0 g 8,0 mg 35,0 mg 1,3 mg 10,0 Iu 0,5 mg 4,0 mg 70,09 53,0 g 359,0 kal 3,4 g 34,7 g 14,0 g 21,0 mg 21,0 mg 2,0 mg 0,0 Iu 0,1 mg 2,0 mg 46,9 g 53,0 g Sumber : Thieme,J.G. (1968) di Ketaren 2008
2.1.2. Klasifikasi Kelapa
Klasifikasi kelapa adalah :
Divisio : Spermatophyta Klas : Monocotyledoneae Ordo : Palmales
Familia : Palmae Genus : Cocos
Species : Cocos nucifera
(Suhardiman,P. 1999)
2.2. Asam Lemak
Asam-asam lemak yang biasa ditemukan di alam biasanya merupakan asam-asam monokarboksilat dengan rantai yang tidak bercabang dan mempunyai jumlah atom karbon genap. Asam-asam lemak yang ditemukan di alam dapat dibagi menjadi dua golongan yaitu, asam lemak jenuh dan asam lemak tidak jenuh. Asam-asam lemak tidak jenuh berbeda dalam jumlah dan posisi ikatan rangkapnya, dan berbeda dengan asam lemak jenuh dalam bentuk molekul keseluruhannya.
Cara penggolongan asam lemak selain asam lemak jenuh dan asam lemak tidak jenuh, dapat digolongkan menjadi asam lemak rantai pendek (Short Chain Fatty Acid), asam lemak rantai menengah (Medium Chain Fatty Acid) dan asam lemak rantai panjang (Long Chain Fatty Acid). Pada umumnya asam lemak rantai pendek mengandung C4-C10, rantai menengah mengandung C12 atau C14, dan rantai
panjang mengandung C16 atau lebih. Asam lemak dengan atom C lebih dari dua
belas tidak larut dalam air dingin maupun air panas. Asam lemak dari C4, C6, C8,
dan C10 dapat menguap dan asam lemak C12 dan C14 sedikit menguap. Garam-garam
dari asam lemak yang mempunyai berat molekul rendah dan tidak jenuh lebih mudah larut dalam alkohol daripada garam-garam dari asam lemak yang mempunyai berat molekul tinggi dan jenuh. (Winarno, F.G. 1997)
2.3. Minyak Kelapa
Minyak kelapa merupakan salah satu hasil olahan dari buah kelapa. Karenanya olahan kelapa untuk minyak kelapa mempunyai porsi yang paling besar. Di Indonesia produksi terbesar minyak kelapa dikonsumsi sebagai minyak goreng. (Palungkung,R. 1999)
Berbeda dengan minyak goreng lainnya, minyak kelapa mengandung asam lemak jenuh berantai sedang dan pendek yang tinggi, yaitu sekitar 92%. Asam lemak jenuh dalam minyak kelapa terdiri dari asam laurat dan asam kaprat. Kandungan asam laurat pada minyak kelapa sangat tinggi, yaitu mencapai 52%. Ini membuat minyak kelapa juga tergolong dalam asam laurat. Dalam tubuh, asam laurat diubah menjadi monolaurin yang mengandung antibiotik alami sehingga mampu membunuh berbagai jenis kuman, virus, mikroorganisme dengan cara merusak membran yang membungkus sel yang terdiri dari asam lemak. Selain itu, kandungan asam lauratnya setara dengan air susu ibu (ASI). Selain asam lemak jenuh, minyak kelapa juga mengandung asam lemak tak jenuh, yaitu asam palmitoleat, oleat, dan linoleat. Namun, persentasenya kecil.
Sifat yang istimewa inilah yang membuat minyak kelapa menjadi lain dari minyak goreng lainnya. Asam lemak jenuh rantai sedang pada minyak kelapa tidak menimbulkan berbagai penyakit. Hal ini dikarenakan asam lemak jenuh rantai sedang mudah diserap tubuh atau usus karena ukuran molekulnya tidak terlalu besar seperti asam lemak rantai panjang. (Sutarmi,S. 2005)
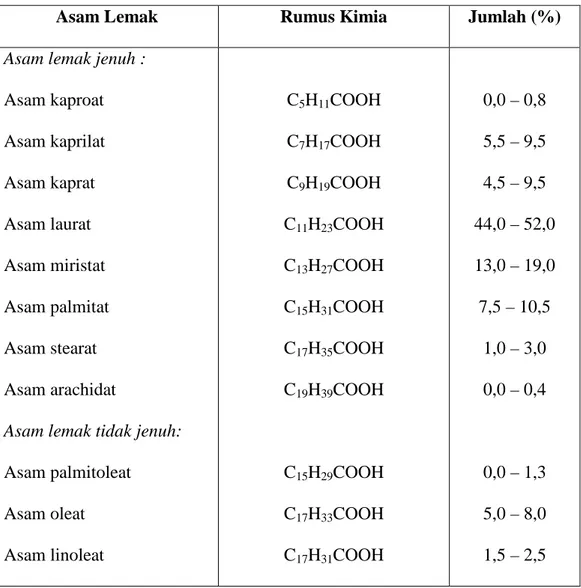
Tabel 2.2 Komposisi Asam Lemak Minyak Kelapa
Asam Lemak Rumus Kimia Jumlah (%)
Asam lemak jenuh : Asam kaproat Asam kaprilat Asam kaprat Asam laurat Asam miristat Asam palmitat Asam stearat Asam arachidat
Asam lemak tidak jenuh: Asam palmitoleat Asam oleat Asam linoleat C5H11COOH C7H17COOH C9H19COOH C11H23COOH C13H27COOH C15H31COOH C17H35COOH C19H39COOH C15H29COOH C17H33COOH C17H31COOH 0,0 – 0,8 5,5 – 9,5 4,5 – 9,5 44,0 – 52,0 13,0 – 19,0 7,5 – 10,5 1,0 – 3,0 0,0 – 0,4 0,0 – 1,3 5,0 – 8,0 1,5 – 2,5 Sumber : Thieme,J.G. (1968) di Ketaren 2008
2.4. Pengolahan Minyak Kelapa
Minyak kelapa dapat diperoleh dari daging buah kelapa segar atau dari kopra. Proses untuk membuat minyak kelapa dari daging buah kelapa segar dikenal dengan proses basah (wet process), karena pada proses ini ditambahkan air untuk mengekstraksi minyak. Sedangkan pembuatan minyak kelapa dengan bahan baku kopra dikenal dengan proses kering (dry process). (Suhardiyono,L. 1988)
2.4.1. Minyak Kelapa Komersial (RBD CNO)
Minyak kelapa komersial (RBD) dibuat dari kopra. Secara umum, pembuatan minyak kelapa dilakukan dengan mengeringkan buah kelapa melalui pemanasan yang diminimalkan, lalu dipres secara mekanik. Selanjutnya, minyak akan keluar saat pengepresan. Pembuatan minyak kelapa seperti ini biasa disebut pembuatan minyak kelapa cara kering.
Kopra merupakan daging buah kelapa yang dikeringkan. Pengeringannya bisa dilakukan dengan sinar matahari, asap, atau pembakaran. Selanjutnya, kopra dibungkus kain kemudian ditumbuk dengan menggunakan penumbuk kayu lalu direbus dalam air mendidih. Minyak akan terekstrak dan mengapung dipermukaan sehingga dapat dipisahkan dari air. Minyak kelapa yang diperoleh dengan cara ini memiliki rendemen yang rendah. Selain itu, biasanya sanitasi pengeringan kopra kurang diperhatikan. Hal ini membuat minyak yang dihasilkan tidak bisa langsung dikonsumsi. Minyak kelapa terlebih dahulu harus dimurnikan (refined), lalu diputihkan (bleaching), dan dihilangkan aromanya (deodorized).
Pada tahap refined (pemurnian) terjadi proses pemanasan yang tinggi. Tujuannya, untuk memisahkan atau menghilangkan komponen minyak yang tidak tersabunkan, sterol, klorofil, vitamin E, dan karotenoid, walaupun hanya dalam jumlah kecil. Selain itu, antioksidan alami kadarnya akan menurun dan asam lemak tak jenuhnya sebagian besar terhidrogenasi. Minyak yang terhidrogenasi mengandung trans fatty acid. (Sutarmi, 2005)
Tujuan pemurnian minyak nabati meliputi (Thieme, 1968):
- Menghilangkan asam lemak bebas (free fatty acid atau FFA) dan getah (gum) agar rasa dan kejernihannya bertambah. Prosesnya disebut netralisasi.
- Menghilangkan zat-zat pembentuk warna agar diperoleh warna yang cerah dan lebih putih. Proses penghilangan zat warna disebut pemucatan (bleaching).
- Menghilangkan semua zat yang membentuk bau. Proses penghilangan bau ini disebut proses deodorizing. (Amin,S. 2009)
Pemurnian dilakukan dengan tiga tahap, yaitu netralisasi, bleaching, dan deodorisasi.
Netralisasi
Netralisasi ialah suatu proses untuk memisahkan asam lemak bebas dari minyak atau lemak, dengan cara mereaksikan asam lemak bebas dengan basa atau pereaksi lainnya sehingga membentuk sabun (soap stock).
Pemucatan (Bleaching)
Pemucatan ialah suatu tahap proses pemurnian untuk menghilangkan zat-zat warna yang tidak disukai dalam minyak. Pemucatan ini dilakukan dengan cara mencampur minyak dengan sejumlah kecil adsorben, seperti tanah serap (fuller earth), lempung aktif (activated clay) dan arang aktif atau dapat juga menggunakan bahan kimia.
Deodorisasi
Deodorisasi adalah suatu tahap proses pemurnian minyak yang bertujuan untuk menghilangkan bau dan rasa (flavor) yang tidak enak dalam minyak. Prinsip proses deodorisasi yaitu penyulingan minyak dengan uap panas dalam tekanan
atmosfer atau keadaan vakum. Proses deodorisasi perlu dilakukan terhadap minyak yang digunakan untuk bahan pangan. (Ketaren,S. 2008)
2.4.2. Minyak Kelapa Murni (VCO)
Minyak kelapa murni (VCO) dibuat dari daging kelapa segar, bukan kopra. Bahan kimia dan pemanasan dengan temperatur tinggi tidak diperlukan untuk proses pemurnian. Hal ini berbeda dengan pembuatan minyak goreng dari kopra, dimana diperlukan bahan-bahan kimia untuk proses pemurniannya. Banyak cara yang dilakukan untuk menghasilkan VCO.
1. Proses Mekanis dan Pemanasan
Hasil pengeringan cepat daging kelapa segar kemudian dipres sehingga keluar minyaknya. Dalam proses ini dilakukan pemanasan tetapi dengan cepat dan setelah itu langsung dipres dengan alat mekanik. Metode ini sering disebut Direct Micro Expeller (DME). Ada metode ini diperoleh minyak sekitar 90% dan air 10%. Air yang terpisah dari minyak dapat diambil, sedang sedikit air yang masih ada di dalam minyak dipisahkan dengan pemanasan singkat.
Metode pemanasan adalah dengan melakukan pemanasan santan dalam keadaan vakum. Pada kondisi vakum, air dan santan dapat mendidih pada suhu sekitar 60oC. Setelah airnya menguap semua, proses dihentikan, blondo dari minyak dipisahkan. Untuk mengambil minyak dari blondo dilakukan dengan menggoreng atau dengan mengepresnya.
2. Proses Fermentasi
Metode untuk memisahkan air dari minyak meliputi penguapan, pendinginan (refrigerasi), penambahan enzim dan pemutaran mekanik (centrifuge). Proses pembuatan VCO yang paling banyak dilakukan adalah dengan metode fermentasi. Cara ini sangat sedikit menggunakan pemanasan sehingga kemurniannya lebih terjamin. Santan difermentasikan selama 12-24 jam. Selama itu telah terjadi proses pemisahan air dan minyak. Minyak yang diperoleh masih mengandung sedikit air yang dengan pemanasan sebentar saja airnya sudah akan hilang. Minyak yang diperoleh kemudian disaring.
Salah satu metode pembuatan VCO dengan fermentasi adalah menggunakan ragi tape (Saccharomyces cerevisseae) atau ragi roti. Proses pembuatan dengan fermentasi ada bermacam-macam, seperti cara pancingan atau memberikan minyak sebagai bahan pemicu pemisahan minyak dan air, dengan memutar dan mendiamkannya, agar minyak terpisah dengan air.
3. Metode Pancingan
Kelapa diparut, dibuat santan dan dibiarkan selama kurang lebih 1 jam di dalam ember plastik transparan. Krim yang diperoleh dicampur dengan minyak pancing dengan perbandingan 3 bagian krim dan 1 bagian minyak pancing. Sebagian minyak pancing digunankan VCO yang telah jadi. Campurkan dan aduk beberapa saat kemudian didiamkan selama 10-12 jam. Setelah fermentasi, campuran tersebut akan terpisah menjadi 3 lapisan, yang paling atas blondo, lapisan kedua minyak dan lapisan paling bawah adalah air. Blondo dipisahkan dari minyak dan airnya dibuang. Biarkan
minyak di tempat penampungan selama beberapa menit dan kemudian saring menggunakan kertas saring. (Amin,S. 2009)
4. Proses Pendinginan
Proses pendinginan terdiri atas dua cara pembuatan yaitu cara mixer dan cara sentrifugal. Cara mixer adalah parut daging buah kelapa dengan mesin parut. Kemudian masukkan hasil parutan ke dalam mesin pemeras tanpa mencampurkan air (menghasilkan santan). Kemudian dinginkan santan pada suhu 1oC – 10oC, mixer sampai membentuk gumpalan pada suhu 45oC (sekitar 60 menit) sampai gumpalan mencair. Setelah mencair, akan terbentuk tiga lapisan (minyak, blondo, dan air). Pisahkan minyak setelah terbentuk tiga lapisan (air, blondo, minyak). Vakum minyak pada suhu 60oC untuk mengurangi kadar air dalam minyak. Kemudian saring minyak menggunkan penyaring ukuran 400 mess dan satu mikron.
Cara sentrifugal adalah parut daging kelapa dengan mesin parut. Kemudian masukkan hasil parutan ke dalam mesin pemeras tanpa mencampurkan air (menghasilkan santan). Kemudian dinginkan santan pada suhu 1oC – 10oC. Masukkan santan dalam wadah (jangan sampai penuh). Kemudian masukkan wadah yang berisi santan dalam alat sentrifugal. Perlu diingat, kecepatan sentrifugal 700 rpm – 7000 rpm sampai terbentuk empat lapisan (tepung, air, blondo, dan minyak). Semakin tinggi kecepatan sentrifugal akan semakin cepat lapisan terpisah. Kemudian pisahkan minyak. Vakum minyak pada suhu 60oC untuk mengurangi kadar air dalam minyak. Kemudian saring minyak menggunkan penyaring ukuran 400 mess dan satu mikron. (Gani et al, 2005)
2.5. Standar Mutu Minyak Kelapa
Standar mutu merupakan hal yang penting untuk menentukan kualitas minyak yang bermutu baik. Ada beberapa faktor yang menentukan standar mutu, yaitu kandungan air dan kotoran dalam minyak, kandungan asam lemak bebas, warna, bilangan peroksida, kejernihan kandungan logam berat dan bilangan iodin.
(Ketaren,S. 2008)
2.5.1. Minyak Kelapa Komersial (RBD CNO)
Dalam praktek pemurnian minyak, pada pabrik-pabrik minyak, dilakukan dengan pemurnian secara fisik, dengan hasil yang dicapai dapat memenuhi persyaratan.
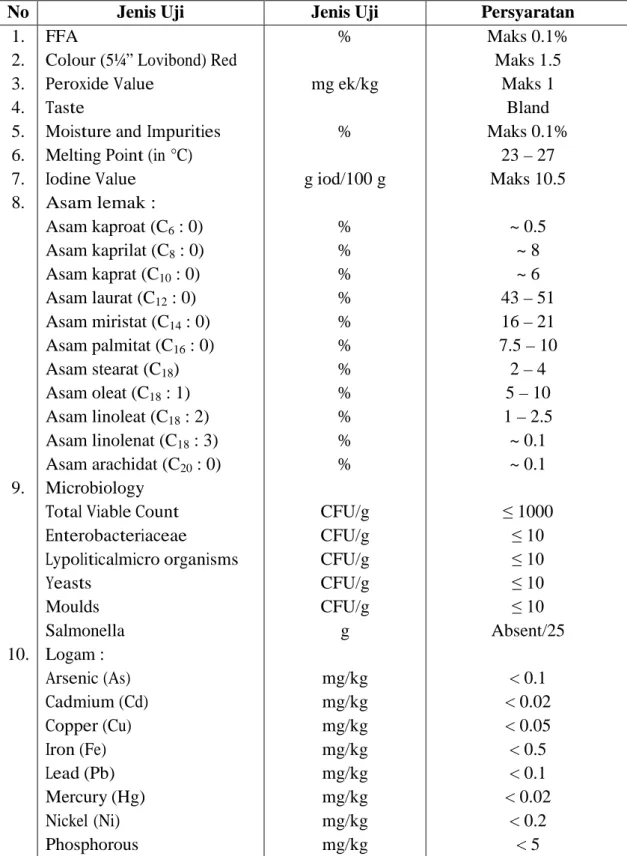
Tabel 2.3 Standar Mutu RBD Coconut Oil
No Jenis Uji Jenis Uji Persyaratan
1. 2. 3. 4. 5. 6. 7. 8. 9. 10. FFA
Colour (5¼” Lovibond) Red Peroxide Value
Taste
Moisture and Impurities Melting Point (in °C) Iodine Value Asam lemak : Asam kaproat (C6 : 0) Asam kaprilat (C8 : 0) Asam kaprat (C10 : 0) Asam laurat (C12 : 0) Asam miristat (C14 : 0) Asam palmitat (C16 : 0) Asam stearat (C18) Asam oleat (C18 : 1) Asam linoleat (C18 : 2) Asam linolenat (C18 : 3) Asam arachidat (C20 : 0) Microbiology Total Viable Count Enterobacteriaceae Lypoliticalmicro organisms Yeasts Moulds Salmonella Logam : Arsenic (As) Cadmium (Cd) Copper (Cu) Iron (Fe) Lead (Pb) Mercury (Hg) Nickel (Ni) Phosphorous % mg ek/kg % g iod/100 g % % % % % % % % % % % CFU/g CFU/g CFU/g CFU/g CFU/g g mg/kg mg/kg mg/kg mg/kg mg/kg mg/kg mg/kg mg/kg Maks 0.1% Maks 1.5 Maks 1 Bland Maks 0.1% 23 – 27 Maks 10.5 ~ 0.5 ~ 8 ~ 6 43 – 51 16 – 21 7.5 – 10 2 – 4 5 – 10 1 – 2.5 ~ 0.1 ~ 0.1 ≤ 1000 ≤ 10 ≤ 10 ≤ 10 ≤ 10 Absent/25 < 0.1 < 0.02 < 0.05 < 0.5 < 0.1 < 0.02 < 0.2 < 5 Sumber: Elbrug Global 2008
2.5.2. Minyak Kelapa Murni (VCO)
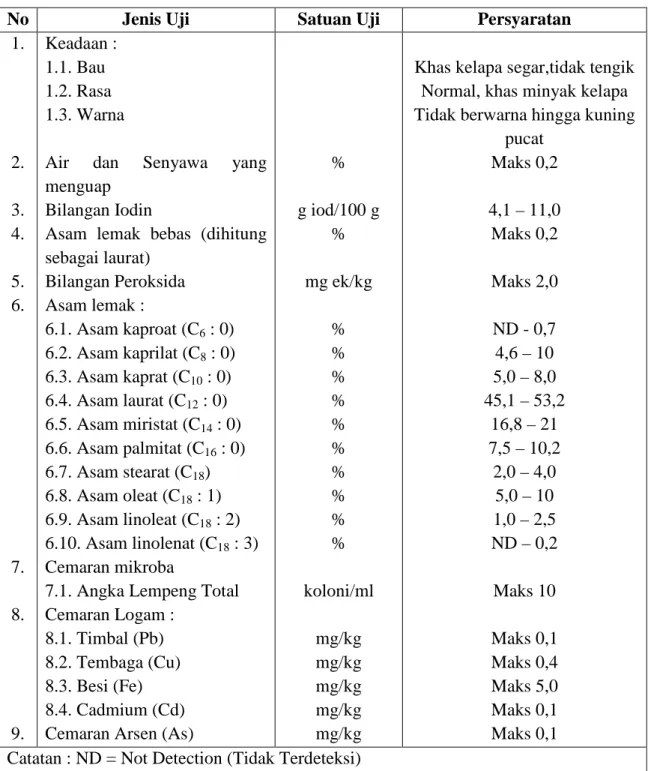
Tabel 2.4 Standar Mutu Virgin Coconut Oil (VCO)
No Jenis Uji Satuan Uji Persyaratan
1. 2. 3. 4. 5. 6. 7. 8. 9. Keadaan : 1.1. Bau 1.2. Rasa 1.3. Warna
Air dan Senyawa yang menguap
Bilangan Iodin
Asam lemak bebas (dihitung sebagai laurat) Bilangan Peroksida Asam lemak : 6.1. Asam kaproat (C6 : 0) 6.2. Asam kaprilat (C8 : 0) 6.3. Asam kaprat (C10 : 0) 6.4. Asam laurat (C12 : 0) 6.5. Asam miristat (C14 : 0) 6.6. Asam palmitat (C16 : 0) 6.7. Asam stearat (C18) 6.8. Asam oleat (C18 : 1) 6.9. Asam linoleat (C18 : 2) 6.10. Asam linolenat (C18 : 3) Cemaran mikroba
7.1. Angka Lempeng Total Cemaran Logam :
8.1. Timbal (Pb) 8.2. Tembaga (Cu) 8.3. Besi (Fe) 8.4. Cadmium (Cd) Cemaran Arsen (As)
% g iod/100 g % mg ek/kg % % % % % % % % % % koloni/ml mg/kg mg/kg mg/kg mg/kg mg/kg
Khas kelapa segar,tidak tengik Normal, khas minyak kelapa Tidak berwarna hingga kuning
pucat Maks 0,2 4,1 – 11,0 Maks 0,2 Maks 2,0 ND - 0,7 4,6 – 10 5,0 – 8,0 45,1 – 53,2 16,8 – 21 7,5 – 10,2 2,0 – 4,0 5,0 – 10 1,0 – 2,5 ND – 0,2 Maks 10 Maks 0,1 Maks 0,4 Maks 5,0 Maks 0,1 Maks 0,1 Catatan : ND = Not Detection (Tidak Terdeteksi)
2.6. Bilangan Iod
Asam lemak yang tidak jenuh dalam minyak dan lemak mampu menyerap sejumlah iod dan membentuk senyawa yang jenuh. Besarnya jumlah iod yang diserap menunjukkan banyaknya ikatan rangkap atau ikatan tidak jenuh. (Ketaren,S. 2008)
Bilangan Iod dinyatakan sebagai jumlah gram iod yang diserap oleh 100 gram minyak atau lemak. Standar ini menggambarkan beberapa metode dalam penentuan bilangan iodin pada minyak dan lemak. Penentuan bilangan iodin dapat dilakukan dengan tiga metode yaitu Metode Wijs, Hanus, dan Hulb. (Paquot,C. 1987)
2.6.1. Metode Wijs
Penambahan kedalam larutan uji dengan larutan iodin monokhlorida dalam campuran asetat dan karbon tetrakhlorida. Setelah waktu standarisasi bereaksi, maka penentuan kelebihan halogen dengan penambahan larutan kalium iodida encer dan titrasi iodin bebas tersebut dengan larutan standar natrium thiosulfat. (Paquot,C. 1987) Penentuan bilangan iodin dengan metode Wijs telah diakui Inggris dan Standar Internasional, dan ISO 3961 (1979). Ketelitian penentuan bilangan iodin dapat juga dipengaruhi oleh ketidakstabilan pereaksi Wijs yang sudah agak lama, atau larutan tiosulfat sebaiknya distandarisasi kembali dengan larutan kalium dikromat pada jangka waktu yang tetap dan juga melakukan uji blanko dengan pereaksi Wijs.
Reaksi yang terlibat adalah :
ICl + R-CH=CH-R1→ R-CHI-CHCl-R1 ICl + 2KI → KCl + KI + I2
I2 + 2Na2S2O3→ 2NaI + Na2S4O6
(Hamilton, R.J. 1986)
Pembuatan Pereaksi Wijs
Pereaksi Wijs yang terdiri dari larutan 16 gram iod monoklorida dalam 1000 mL asam asetat glasial. Cara lain yang lebih baik untuk membuat larutan ini yaitu dengan melarutkan 13 g iod dalam 1000 ml asam asetat glasial, kemudian dialirkan gas klor sampai terlihat perubahan warna yang menunjukkan bahwa jumlah gas klor yang dimasukkan sudah cukup. Pembuatan larutan ini agak sukar, dan bersifat tidak tahan lama. Larutan ini sangat peka terhadap cahaya, panas, dan udara, sehingga harus disimpan di tempat yang gelap, sejuk dan tertutup rapat.
B = Jumlah ml Na2S2O3 untuk titrasi blanko
S = Jumlah ml Na2S2O3 untuk titrasi contoh
N = Normalitas larutan Na2S2O3
G = Bobot contoh (gram)
2.6.2. Metode Hanus
Penambahan kedalam larutan uji dengan larutan iodin monobromida dalam campuran asam asetat dan karbon tetrakhlorida. Setelah waktu standarisasi bereaksi, penentuan kelebihan halogen dengan penambahan larutan kalium iodida encer dan titrasi iodin bebas tersebut dengan larutan standar natrium thiosulfat. (Paquot,C. 1987)
Pembuatan Pereaksi Hanus
Dalam cara Hanus digunakan pereaksi iodium bromida dalam larutan asam asetat glasial (larutan Hanus). Untuk membuat larutan ini, 20 gram iodium bromida dilarutkan dlaam 1000 mL alkohol murni yang bebas dari asam asetat. Jumlah contoh yang ditimbang tergantung dari perkiraan besarnya bilangan iod, yaitu sekitar 0,5 gram untuk lemak, 0,25 gram untuk minyak, dan 0,1 sampai 0,2 gram untuk minyak dengan derajat ketidakjenuhan yang tinggi. Jika ditambahkan 25 pereaksi harus ada kelebihan pereaksi sekitar 60 persen. (Ketaren,S. 2008)
2.6.3. Metode Hulb
Penambahan kedalam larutan uji dengan larutan karbon tetrakhlorida, ditambahkan berlebih larutan etanol kedalam iodin dan merkuri khlorida. Setelah waktu standarisasi bereaksi, penentuan kelebihan halogen dengan penambahan larutan kalium iodida encer dan titrasi iodin bebas tersebut dengan larutan standar natrium tiosulfat. (Paquot,C. 1987)
Pada cara Hulb digunakan pereaksi yang terdiri dari larutan 25 gram iod di dalam 500 mL etanol dan larutan 30 gram merkuri khlorida di dalam 500 mL etanol. Kedua larutan ini baru dicampurkan jika akan dipergunakan, dan tidak boleh berumur
lebih dari 48 jam. Pereaksi ini mempunyai reaktivitas yang lebih kecil dibandingkan dengan cara-cara lainnya, sehingga membutuhkan waktu reaksi selama 12 sampai 14 jam. (Ketaren,S. 2008)
2.7. Titrasi Iodometri
Titrasi iodometri dengan Na2S2O3 sebagai titrant dikenal sebagai titrasi tidak
langsung. Analat harus berbentuk suatu oksidator yang cukup kuat, karena dalam metoda ini analat selalu direduksi dulu dengan KI sehingga terjadi I2. I2 inilah yang
dititrasi dengan Na2S2O3.
Oks analat + I- Red analat + I2
2 S2O3= + I2 S4O6= + 2 I
-Reaksi S2O3= dengan I2 berlangsung baik dari segi kesempurnaannya. Selain itu,
reaksi berjalan cepat dan bersifat unik karena oksidator lain tidak mengubah S2O3=
menjadi S4O6= melainkan menjadi SO3= seluruhnya atau sebagian menjadi SO4=.
Titrasi dapat dilakukan tanpa indikator dari luar karena warna I2 yang dititrasi
itu akan lenyap bila titik akhir tercapai, warna itu mula-mula coklat agak tua, menjadi lebih muda, lalu kuning, kuning-muda, dan seterusnya, sampai akhirnya lenyap. Bila diamati dengan cermat perubahan warna tersebut, maka titik akhir dapat ditentukan dengan cukup jelas. Konsentrasi ≈ 5 x 10 -6 M yod masih tepat dapat dilihat dengan mata dan memungkinkan penghentian titrasi dengan kelebihan hanya senilai satu tetes yod 0,05 M. Namun lebih mudah dan lebih tegas bila ditambahkan amilum kedalam larutan sebagai indikator. Amilum dengan I2 membentuk suatu kompleks berwarna
terikat itu pun hilang bereaksi dengan titrant sehingga warna biru lenyap mendadak dan perubahan warnanya tampak sangat jelas. Penambahan amilum ini harus menunggu sampai mendekati titik akhir titrasi (bila yod sudah tinggal sedikit yang tampak dari warnanya yang kuning-muda). Maksudnya adalah agar amilum tidak membungkus yod dan menyebabkan sukar lepas kembali. Hal itu akan berakibat warna biru sulit sekali lenyap sehingga titik akhir tidak kelihatan tajam lagi. Bila yod masih banyak sekali bahkan dapat menguraikan amilum dan hasil penguraian ini mengganggu perubahan warna pada titik akhir. (Harjadi. 1990)