i
SINTESIS SENYAWA 4-(4'-HIDROKSI-3'-METOKSIFENIL)-4-HIDROKSIBUTAN-2-ON MELALUI REAKSI HIDRASI
TERHADAP SENYAWA HASIL SINTESIS ANTARA VANILIN DAN ASETON
SKRIPSI
Diajukan kepada
Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Negeri Yogyakarta Untuk Memenuhi
Sebagian Persyaratan Guna Memperoleh
Gelar Sarjana Sains Kimia
Oleh:
AMANDA KUMALASARI 12307144037
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGYAKARTA
iv
HALAMAN PERNYATAAN
Yang bertanda tangan di bawah ini saya:
Nama : Amanda Kumalasari
Nomor Mahasiswa : 12307144037 Program Studi : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam
Judul Penelitian : Sintesis Senyawa 4-(4'-hidroksi-3'-metoksifenil)-3- hidroksibutan-2-on melalui Reaksi Hidrasi terhadap Senyawa Hasil Sintesis antara Vanilin dan Aseton
Menyatakan bahwa penelitian ini merupakan hasil pekerjaan saya yang berjudul “Sintesis Senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on melalui Reaksi Hidrasi terhadap Senyawa Hasil Sintesis antara Vanilin dan Aseton”. Sepanjang pengetahuan saya tidak berisi materi atau data yang telah dipublikasikan atau ditulis oleh orang lain atau telah dipergunakan atau diterima sebagai persyaratan studi pada universitas atau institut lain, kecuali pada bagian-bagian yang telah dinyatakan dalam teks.
Tanda tangan dosen penguji yang tertera dalam pengesahan adalah asli. Jika tidak asli, saya siap menerima sanksi ditunda yudisium pada periode berikutnya.
Yogyakarta, 3 April 2017 Yang Menyatakan
v MOTTO
Allah tidak membebani seseorang melainkan sesuai dengan kesanggupan (Al Baqarah : 286, Al An’am : 152)
Usaha keras tak akan pernah mengkhianati hasil yang dicapai.
vi
HALAMAN PERSEMBAHAN
vii
KATA PENGANTAR
Segala puji dan syukur penulis panjatkan Kehadirat Allah SWT yang telah melimpahkan Rahmat dan Hidayah-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul “Sintesis Senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on melalui Reaksi Hidrasi terhadap Senyawa Hasil Sintesis antara Vanilin dan Aseton”.
Penulisan skripsi ini dapat terlaksana dengan lancar atas bantuan, bimbingan dan arahan dari berbagai pihak. Oleh karena itu, penulis menyampaikan ucapan terima kasih kepada yang terhormat:
1. Bapak Dr. Hartono, selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta.
2. Bapak Drs. Jaslin Ikhsan, M.App.Sc., Ph.D. selaku Ketua Jurusan Pendidikan Kimia Fakultas Matematika dan Ilmu Pengetahuan alam Universitas Negeri Yogyakarta.
3. Bapak Karim Theresih, SU selaku dosen pembimbing skripsi, dan ketua penguji yang telah memberikan bimbingan, arahan dan saran.
4. Ibu Prof. Dr. Indyah Sulistyo Arty, M.S selaku penguji utama, atas pertanyaan, kritik, dan saran yang diberikan.
5. Ibu C. Budimarwanti, M.Si. selaku penguji pendamping, atas pertanyaan, kritik, dan saran yang diberikan.
viii
7. Semua pihak yang telah membantu dan memberikan dukungan secara moral maupun material dalam penyelesaian tugas akhir skripsi ini, yang tidak dapat penulis sebut satu per satu.
Penulis menyadari bahwa laporan Tugas Akhir Skripsi ini masih banyak kekurangan, maka dari itu kritik dan saran yang bersifat membangun dari pembaca sangat penulis harapkan untuk melengkapi kekurangan dalam penyusunan laporan Tugas Akhir Skripsi ini. Semoga laporan Tugas Akhir Skripsi ini bermanfaat bagi pembaca sekalian.
Yogyakarta, 3 April 2017
ix DAFTAR ISI
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERNYATAAN... iv
MOTTO... v
HALAMAN PERSEMBAHAN... vi
KATA PENGANTAR ... vii
DAFTAR ISI ... ix
DAFTAR TABEL ... xi
DAFTAR GAMBAR... xii
DAFTAR LAMPIRAN... xiv
ABSTRAK ... xv
D. Perumusan Masalah... 3
E. Tujuan Penelitian ... 3
F. Manfaat Penelitian ... 4
x
B. Penelitian yang Relevan ... 14
C. Kerangka Berfikir... 14
BAB III. METODE PENELITIAN A. Subyek dan Obyek Penelitian ... 16
B. Alat dan Bahan ... 16
C. Prosedur Penelitian... D. Teknik Analisis Data ... 17 18 BAB IV. HASIL PENELITIAN DAN PEMBAHASAN A. Hasil Penelitian ... 19
B. Pembahasan ... 27
1. Sintesis senyawa vanilaseton ... 27
2. Hidrasi vanilaseton ... 32
BAB V. KESIMPULAN DAN SARAN A. Kesimpulan ... 40
B. Saran ... 40
DAFTAR PUSTAKA ... 41
xi
DAFTAR TABEL
Tabel 1 Karakteristik serapan infra merah dari beberapa gugus fungsional 12 Tabel 2 Data pengamatan hasil sintesis senyawa vanilin dengan aseton ... 19 Tabel 3 Daerah serapan pada senyawa hasil sintesis vanilin dan aseton .... 23 Tabel 4 Daerah serapan pada senyawa vanilin ... 24 Tabel 5 Hasil pengamatan senyawa hasil hidrasi vanilaseton ... 24 Tabel 6 Gugus fungsi yang terdapat pada senyawa hasil hidrasi
vanilaseton ... 25 Tabel 7 Serapan gugus fungsional senyawa hasil sintesis dan vanilin
dengan spektroskopi IR ... 32 Tabel 8 Perbandingan gugus karakteristik hasil sintesis dengan hasil
xii
Gambar 4 Serangan enolat pada gugus karbonil ... 7
Gambar 5 Dehidrasi aldol ... 8
Gambar 6 Reaksi hidrasi alkena ... 8
Gambar 7 Protonasi alkena ... 8
Gambar 8 Adisi nukleofil ke karbokation ... 9
Gambar 9 Proses Fragmentasi 14 Gambar 10 Senyawa hasil sintesis vanilin dan aseton ... 19
Gambar 11 Hasil KLT senyawa hasil sintesis vanilaseton ... 20
Gambar 12 Hasil TLC scanner senyawa hasil sintesis vanilaseton (kloroform:etilasetat 9:1) ... 21 Gambar 13 Hasil TLC scanner senyawa vanilin (kloroform:etilasetat 9:1) .... 21
Gambar 14 Spektrum IR senyawa hasil sintesisvanilin dan aseton ... 22
Gambar 15 Spektrum IR vanilin standar ... 23
Gambar 16 Senyawa hasil hidrasi vanilaseton ... 24
Gambar 17 Spektrum IR senyawa hasil hidrasi vanilaseton ... 25
Gambar 18 Kromatogram GC dari senyawa hasil sintesis vanilin dan aseton ... 26 Gambar 19 Spektrum massa puncak 1 senyawa hasil hidrasi vanilaseton ... 26
Gambar 20 Spektrum massa puncak 2 senyawa hasil hidrasi vanilaseton ... 27
Gambar 21 Reaksi pembentukan ion enolat dari aseton ... 28
Gambar 22 Reaksi penyerangan ion enolat terhadap gugus karbonil ... 28
Gambar 23 Pembentukan senyawa β-hidroksi keton ... 29
Gambar 24 Reaksi dehidrasi ... 29
xiii
Gambar 28 Mekanisme hidrasi 33
Gambar 29 Pembentukan senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on ...
33
Gambar 30 Pembentukan senyawa 4-(4'-hidroksi-3'-metoksifenil)-3-hidroksibutan-2-on ...
33
Gambar 31 Resonansi benzilik ... 34
Gambar 32 Fragmentasi vanilin ... 36
Gambar 33 Pembentukan enol melalui perpindahan elektron C ... 37
Gambar 34 Serangan atom oksigen terhadap proton ... 37
Gambar 35 Pelepasan proton dari gugus OH ... 37
Gambar 36 Serangan karbanion terhadap proton ... 38
xiv
DAFTAR LAMPIRAN
Lampiran 1 Perhitungan bahan ... 42
Lampiran 2 Prosedur kerja ... 43
Lampiran 3 Dokumentasi penelitian ... 45
Lampiran 4 Perhitungan Nilai Rf Kromatografi Lapis Tipis ... 47
Lampiran 5 Data Hasil TLC Scanner ... 48
Lampiran 6 Data Hasil FTIR ... 49
xv
SINTESIS SENYAWA 4-(4'-HIDROKSI-3'-METOKSIFENIL)-4- HIDROKSIBUTAN-2-ON MELALUI REAKSI HIDRASI
TERHADAP SENYAWA HASIL SINTESIS ANTARA VANILIN DAN ASETON
Oleh :
Amanda Kumalasari NIM. 12307144037
Pembimbing : Karim Theresih, SU
ABSTRAK
Tujuan dari penelitian ini adalah mensintesis senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on melalui hidrasi vanilaseton hasil sintesis vanillin dan aseton. Selain itu, juga mengidentifikasi senyawa hasil sintesis menggunakan spektrofotometer IR dan GC-MS.
Tahap pertama adalah melakukan sintesis vanilaseton yang diawali dengan mereaksikan vanillin dan aseton selama 3 jam. Selanjutnya dilakukan hidrasi senyawa vanilaseton dengan menggunakan H2SO4 95%. Identifikasi produk
sintesis dilakukan dengan KLT, spektrofotometer IR dan GCMS.
Hasil penelitian menunjukan bahwa sintesis senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on belum berhasil, hal ini dikarenakan senyawa hasil sintesis terpecah kembali menjadi bahan dasar 4-hidroksi-3-metoksibenzaldehida dan aseton.
Kata kunci: vanillin, kondensasi aldol, 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on
xvi
SYNTHESIS 4-(4'-HYDROXY-3'-METHOXYPHENYL)-4-HIDROXYBUTANE-2-ON THROUGH HYDRATION
REACTION OF SYNTHESIS COMPOUND OF VANILIN AND ACETONE
By :
Amanda Kumalasari Student Number : 12307144037 Supervisor : Karim Theresih, SU
ABSTRACT
The aim of this research was to synthesized the 4-(4'-hydroxy-3'-methoxyphenyl)-4-hydroxybutan-2-on through hydration of vanillacetone synthesis results of vanillin and acetone also to analyse the yield using IR spectrophotometer and GC-MS.
The first was synthesized the vanillacetone that begun by reacting vanillin and acetone for 3 hours. Then hydrolysed vanillacetone using 95% H2SO4. All
the yield of each product were identified using IR spectrop hotometer and GC-MS.
The results showed that the synthesis of the compound 4-(4'-hydroxy-3'-methoxyphenyl)-4-hidroksibutan-2-on had not been successful, it was because the compounds synthesized split back into the starting material 4-hydroxy-3-methoxybenzaldehyde and acetone.
1 BAB I PENDAHULUAN
A. Latar Belakang
Perkembangan ilmu kimia di zaman sekarang semakin cepat, terutama dibidang kimia organik. Banyak senyawa baru yang ditemukan dengan berbagai manfaat yang sangat berguna bagi kehidupan. Salah satu senyawa yang banyak diteliti dan dikembangkan adalah senyawa benzalaseton dan turunannya. Senyawa benzalaseton dan turunannya yang telah diteliti mempunyai manfaat sebagai antioksidan dan sebagai tabir surya (Sri Handayani, 2013; Novery Ambo, 2012).
Senyawa turunan benzalaseton dapat dibuat melalui reaksi kondensasi aldol. Kondensasi aldol adalah adisi nukleofilik dari ion enolat terhadap gugus karbonil dengan produk reaksi β-hidroksiketon atau β-hidroksialdehida, dimana senyawa enolat dan gugus karbonil yang diserang adalah dua senyawa yang sama (Fessenden, 1999).
2
dengan menggunakan reaksi kondensasi aldol antara vanilin dan aseton dengan katalis NaOH. Penggunaan katalis NaOH dengan konsentrasi yang tepat menjadi sangat penting dalam reaksi ini karena berpengaruh terhadap baik tidaknya kondensasi aldol yang terjadi (Deni Pranowo, 2010). Tahap kedua adalah dengan melakukan hidrasi hasil sintesis tahap pertama menggunakan H2SO4 95%.
Penelitian ini dilakukan untuk mensintesis senyawa vanilaseton dengan mereaksikan vanilin dan aseton melalui reaksi kondensasi aldol, kemudian senyawa vanilaseton yang terbentuk dihidrasi menggunakan H2SO4 95%
sehingga terbentuk senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on. Senyawa yang dihasilkan dari penelitian ini kemudian diidentifikasi menggunakan KLT, TLC Scanner, spektrometer infra merah, dan GC-MS.
B. Identifikasi Masalah
Berdasakan latar belakang di atas maka dapat diidentifikasi beberapa masalah sebagai berikut:
1. Katalis yang digunakan dalam sintesis senyawa vanilaseton. 2. Kondisi reaksi dalam sintesis senyawa vanilaseton.
3. Senyawa yang digunakan untuk menghidrasi senyawa vanilaseton.
3 C. Pembatasan Masalah
Berdasarkan identifikasi masalah di atas, maka masalah dalam penelitian ini dibatasi pada:
1. Katalis yang digunakan dalam proses sintesis senyawa vanilaseton adalah katalis basa yaitu natrium hidroksida.
2. Waktu pengadukan yang digunakan adalah 3 jam pada suhu kamar.
3. Senyawa yang digunakan untuk menghidrasi vanilaseton adalah H2SO4 95%.
4. Identifikasi hasil sintesis dilakukan dengan KLT (TLC scanner), spektroskopi IR, dan GC-MS.
D. Perumusan Masalah
1. Apakah senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on dapat dihasilkan melalui reaksi hidrasi terhadap senyawa hasil sintesis antara vanilin dan aseton?
2. Bagaimana hasil identifikasi senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on berdasarkan analisis dengan TLC scanner, FTIR dan GC-MS?
E. Tujuan Penelitian
Tujuan dari penelitian ini adalah
4
2. Menentukan karakterteristik dan sifat fisik senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on.
F. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan manfaat antara lain:
1. Memberi informasi mengenai cara sintesis dan identifikasi senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on dari vanilin dan aseton.
5 BAB II
TINJAUAN PUSTAKA
A. Deskripsi Teori
1. Vanilin
Senyawa 4-hidroksi-3-metoksibenzaldehida atau vanilin adalah senyawa organik aldehida fenolik dengan rumus C8H8O3. Gugus fungsional senyawa ini
meliputi aldehida, eter dan fenol. Vanilin adalah komponen utama dari ekstrak biji vanili (Ravendra, 2015). Senyawa dengan warna kristal putih ini telah banyak digunakan sebagai bahan awal untuk sintesis senyawa lain dan juga sebagai pengharum pada produk makanan, minuman dan kosmetik (Bahl, 1979). Menurut Sarifudin dalam Budimarwati (2007), vanilin dilihat dari struktur kimianya (Gambar 1), vanilin merupakan senyawa fenol tersubstitusi gugus metoksi pada posisi orto dan gugus aldehida pada posisi para, sehingga vanilin dapat dikelompokkan sebagai senyawa antioksidan.
6 2. Aseton
Aseton yang juga dikenal sebagai propanon, dimetil keton, 2-propanon, propan-2-on, dimetilformaldehida, dan β-ketopropana merupakan keton yang paling sederhana. Secara fisik, aseton berbetuk cairan yang tidak berwarna dan mudah terbakar. Aseton merupakan salah satu senyawa yang penting karena dapat digunakan untuk membuat plastik, serat, dan obat-obatan.
Aseton merupakan keton paling sederhana (Gambar 2), aseton memiliki gugus karbonil yang mempunyai ikatan rangkap dua karbon oksigen terdiri dari ikatan σ dan satu ikatan π, Aseton mempunyai atom hidrogen α bersifat asam,
oleh karena itu dapat terionisasi menghasilkan ion enolat (Wade, 2006). Sekitar 30% aseton digunakan secara langsung, sebab aseton tidak saja bercampur sempurna dengan air tetapi juga merupakan pelarut yang baik untuk banyak zat organik (resin, cat, zat warna, dan cat kuku). Sisanya digunakan untuk pembuatan bahan kimia komersial lain, termasuk bisfenol-A untuk resin epoksi (Hart, 2003: 273).
CH3 O
H3C
Gambar 2. Struktur senyawa aseton
3. Kondensai Aldol
7
molekul lebih kecil (seperti molekul air) (Fessenden, 1982: 179). Kondensasi aldol adalah adisi nukleofilik dari ion enolat terhadap gugus karbonil dengan produk reaksi β-hidroksiketon atau β-hidroksialdehida, dimana senyawa enolat dan gugus karbonil yang diserang adalah dua senyawa yang sama (Fessenden, 1999:179). Reaksi kondensasi aldol dapat berjalan melalui dua mekanisme yaitu mekanisme enol yang menggunakan katalis asam kuat dan mekanisme enolat yang menggunakan katalis basa kuat (Wade, 1999). Mekanisme pembentukan ion enolat yang menggunakan basa kuat ditunjukan pada Gambar 3 kemudian terjadi serangan nukleofil oleh ion enolat pada gugus karbonil lain yang terstabilkan oleh resonansi ditunjukkan pada Gambar 4. Produk reaksi ini adalah garam alkoksida, aldol akan terbentuk dan mengalami dehidrasi (Gambar 5) menghasilkan senyawa karbonil tak jenuh.
H
Gambar 3. Pembentukan ion enolat
H
8
Gambar 5. Dehidrasi aldol
4. Hidrasi
Dalam larutan asam kuat (seperti H2SO4 dalam air), air mengadisi suatu
ikatan rangkap dan menghasilkan alkohol (Gambar 6). Reaksi ini disebut hidrasi alkena.
Gambar 6. Reaksi hidrasi alkena
Reaksi tersebut berlangsung dalam dua tahap, tepat sama seperti adisi hidrogen halida. Tahap pertama ialah protonasi alkena dan menghasilkan karbokation (Gambar 7). Tahap kedua ialah adisi nukleofil ke karbokation itu (Gambar 8). Karena mula-mula terbentuk karbokation kedua reaksi itu tunduk pada aturan markonikov. Penataan ulang dapat terjadi jika karbokation itu dapat menjalani geseran 1,2 (dari) H atau R untuk menghasilkan karbokation yang lebih stabil. (Fessenden, 1982: 394)
C CH
R2 R + H R2C CH2R
9
Gambar 8. Adisi nukleofil ke karbokation
5. Kromatografi Lapis Tipis (KLT)
Pada kromatografi lapis tipis (KLT), fase cair berupa lapisan tipis (tebal 0,1-2mm) yang terdiri atas bahan padat yang dilapiskan kepada permukaan penyangga datar yang biasanya terbuat dari kaca, tetapi dapat pula terbuat dari polimer atau logam. Lapisan melekat kepada permukaan dengan bantuan pengikat, biasanya kalsium sulfat atau amilum (pati). Pada KLT lapisan itu biasanya berfungsi sebagai pemukaan padat yang menjerap (Gritter, 1991: 6).
10
selulosa, dan lain-lain yang mempunyai butiran sangat kecil yaitu 0,063 – 0,125 nm dilapiskan pada kaca, lembaran aluminium atau plastik dengan ketebalan tertentu (200-1500 nm) (Hardjono Sastrohamidjojo, 1991: 30).
Fasa gerak yang biasa digunakan adalah pelarut atau campuran pelarut yang dinamakan eluen. Pemilihan fasa gerak sebaiknya menggunakan campuran pelarut organik yang mempunyai polaritas serendah mungkin untuk mengurangi serapan dari komponen campuran pelarut (Hardjono Sastrohamidjojo, 1985: 31). Eluen yang digunakan merupakan suatu campuran sesederhana mungkin yang terdiri atas maksimum tiga komponen. Eluen dapat dikelompokkan ke dalam deret eluotropi berdasarkan efek elusinya. Efek elusi naik dengan kenaikan kepolaran pelarut. Tetapan dielektrik memberi informasi mengenai kepolaran suatu senyawa. Laju rambat tergantung pada viskositas eluen dan struktur lapisan, misalnya butiran adsorben (Stahl, 1985: 6). Jarak pengembangan senyawa ada kromatogram dinyatakan dengan Retordation factor (Rf).
Rf =
Faktor-faktor yang mempengaruhi gerakan noda dalam kromatograi lapis tipis yang juga mempengaruhi harga Rf adalah
11
e. Derajat kejenuhan dari uap dalam mana bejana pengembang yang digunakan.
f. Teknik percobaan.
6. Spektroskopi Inframerah (IR)
Bila sinar inframerah dilewatkan melalui cuplikan senyawa organik, maka sejumlah frekuensi diserap sedang frekuensi yang lain diteruskan/ditransmisikan tanpa diserap. Jika kita menggambar antara persen absorbansi atau persen transmitansi lawan frekuensi maka akan dihasilkan suatu spektrum inframerah (Hardjono Sastrohamidjojo, 2007:45). Spektroskopi infra merah / Infra red (IR) berkaitan dengan vibrasi molekul (Tri Panji, 2012:17)
Pada prakteknya spektroskopi inframerah diperuntukkan untuk menentukan adanya gugus-gugus fungsional utama dalam suatu sampel yang diperoleh berdasarkan bilangan gelombang yang dibutuhkan untuk vibrasi tersebut (Markham, 2009: 29). Inti atom yang terikat oleh ikatan kovalen mengalami vibrasi dan osilasi. Bila molekul tersebut menyerap radiasi inframerah akan terjadi kenaikan amplitudo vibrasi. Maka molekul akan berada dalam keadaan vibrasi tereksitasi. Panjang gelombang dari absorbsi oleh suatu tipe ikatan tertentu, tergantung pada macam vibrasi dari ikatan tersebut. Oleh karena itu, tipe ikatan yang berbeda menyerap radiasi inframerah pada panjang gelombang karakteristik yang berlainan (Fessenden, 1999).
12
misalnya karbon monoksida dalam udara dengan teknik non-dispersive spektrum infra merah memberikan puncak-puncak maksimal yang jelas sebaiknya puncak minimumnya (Khopkar, 2008: 242).
Penggunaan FTIR pada bidang kimia organik hampir menggunakan daerah dari 650-4000 cm-1. Fungsi utama dari FTIR adalah menganalisis struktur molekul, khususnya gugus fungsional seperti OH, C=O dan C=C. Serapan setiap tipe ikatan (N-H, C-H, C-X, C=O, C-O, C=C, C-N, dan sebagainya hanya diperoleh dalam bagian-bagian kecil tertentu dari vibrasi infarmerah (Hardjono Sastrohamidjojo, 1991: 46-47). Untuk menginterpretasikan spektrum inframerah secara sederhana dapat dilakukan dengan mengetahui harga dasar serapan gugus fungsional/ ikatan (Hardjono Sastrohamidjojo, 1992:14). Berdasarkan struktur senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on, maka dapat diperkirakan gugus fungsional yang akan muncul pada spektrum IR ditunjukan pada Tabel 1:
Tabel 1. Karakteristik serapan infra merah dari beberapa gugus fungsional
Jenis Vibrasi Bilangan
gelombang (cm-1) Intensitas
13 7. Spektroskopi Massa (MS)
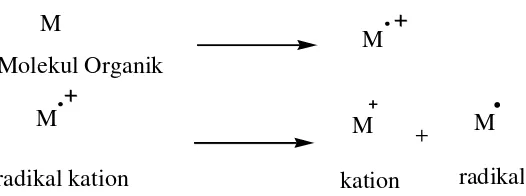
Spektroskopi massa merupakan teknik untuk mengukur massa dan berat molekul dari suatu molekul. Selain itu juga memberikan informasi yang menguntungkan mengenai struktur suatu molekul yang baru (McMurry, 2007: 415) Spektroskopi GC-MS merupakan metode yang menggabungkan dua metode analisis senyawa yaitu kromatografi gas (GC) dan spektrometri massa (MS). Kromatografi gas digunakan untuk mengetahui tingkat kemurnian dari suatu senyawa hasil sintesis (Gritter, 1991:34). Spektrum massa diperoleh dengan mengubah senyawa suatu sampel menjadi ion-ion yang bergerak cepat yang dipisahkan berdasarkan perbandingan massa terhadap muatan. Proses ionisasi menghasilkan partikel-partikel bermuatan positif dimana massa terdistribusi adalah spesifik terhadap senyawa induk (Khopkar, 2008: 403). Spektroskopi massa akan memberikan informasi massa molekul relatif (Mr) dan bagaimana proses pemecahan (fragmentasi) dari suatu molekul organik (Markham,2009)
14
radikal kation kation radikal
Gambar 9. Proses Fragmentasi
B. Penelitian yang relevan
Penelitian yang relevan yang mendukung penelitian ini adalah:
1. Penelitian yang telah berhasil dilakukan oleh Noverry Ambo (2012) yang telah mensintesis senyawa 4-(4'-hidroksi-3'-metoksifenil)-3-buten-2-on dengan bahan dasar vanilin dan aseton dengan katalis basa, diperoleh rendemen sebesar 28,37% dengan kemurnian 99,06%.
2. Penelitian yang telah berhasil dilakukan oleh Anton Cahyono (2012) yaitu mensintesis senyawa 4-(4'-hidroksi-3'-metoksifenil)-3-buten-2-on dan studi efisiensinya dengan katalis bifungsional NaOH/ZrO2-montmorillonit.
C. Kerangka Berpikir
4-15
(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on. Senyawa hasil sintesis ditentukan titik leburnya dan analisis kemurnianya menggunakan TLC scanner,
16 BAB III
METODE PENELITIAN
A. Subjek dan Objek Penelitian
1. Subjek Penelitian
Subjek penelitian ini adalah senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on.
2. Objek Penelitian
Objek penelitian ini adalah karakteristik senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on yang dihasilkan melalui reaksi hidrasi terhadap senyawa hasil sintesis antara vanilin dan aseton.
B. Alat dan Bahan Kimia
1. Alat-alat penelitian
Alat-alat yang digunakan dalam penelitian ini adalah spektrofotometer infra merah (shimadzu FTIR Prestige 21), GC-MS QP2010 SE, plat KLT silica Gel 60 GF254 merck, TLCscanner (CAMAG), timbangan analitik, satu set alat gelas.
2. Bahan-bahan penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah vanilin p.a, aseton p.a, NaOH p.a, H2SO4 95 %, HCl pekat 37 %, Na2SO4 anhidrat,
17 C. Prosedur Penelitian
1. Sintesis senyawa vanilaseton.
Prosedur sintesis senyawa vanilaseton mengadaptasi penelitian Anton Cahyono (2012). Sebanyak 0,156 gram (0,003 mol) NaOH dilarutkan dengan 0,3 ml akuades dalam gelas beker. Aseton sebanyak 0,145 gram (0,0025 mol) dimasukkan ke dalam gelas beker tersebut kemudian diaduk menggunakan
magnetic strirrer selama 30 menit. Selanjutnya, vanilin sebanyak 0,383 gram
(0,0025 mol) ditambahkan sedikit demi sedikit ke dalam gelas beker, kemudian pengadukan dilanjutkan selama 3 jam. Larutan yang terbentuk kemudian ditambahkan akuades sebanyak 10 ml dan kemudian ditambahan HCl pekat tetes demi tetes sampai terbentuk endapan berwarna kuning. Endapan yang terbentuk disaring dengan penyaring Buchner. Endapan yang diperoleh dikeringkan kemudian ditimbang dan dilakukan KLT dengan dibandingkan senyawa asal (vanilin). Hasil KLT kemudian dilakukan TLC
scanner untuk mengetahui kadar dan menghitung persen hasil. Senyawa hasil
sintesis dikarakterisasi pula dengan spektroskopi IR. 2. Hidrasi senyawa vanilaseton.
Prosedur hidrasi senyawa vanilaseton mengadaptasi Allinger et al
(1980). Ke dalam beker glass 50 ml dimasukkan 2 ml akuades dan 3-5 tetes H2SO4 95% kemudian dibiarkan selama 2 menit sambil diaduk. Kemudian ke
18
Larutan disaring diambil larutan organiknya. Lapisan organik ditambahkan Na2SO4 anhidrat untuk mengikat molekul airnya kemudian disaring. Larutan
dianalisis menggunakan FTIR dan GC-MS. D. Teknik Analisis Data
1. Data Kuantitatif
Analisis data untuk menentukan rendemen senyawa hasil sintesis adalah:
Rendemen =
x % kemurnian TLC scaner
2. Data Kualitatif
19 BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. HASIL PENELITIAN
Berdasarkan hasil penelitian yang sudah dilakukan diperoleh hasil sintesis sebagai berikut:
1. Sintesis vanilaseton
a. Hasil sintesis vanilaseton
Senyawa vanilaseton diperoleh melalui kondensasi aldol antara vanilin dan aseton dengan katalis NaOH. Hasil yang diperoleh tersaji dalam Tabel 2.
Tabel 2. Data pengamatan hasil sintesis vanilin dengan aseton
Parameter Hasil
Berat hasil sintesis 0,354 gram Bentuk hasil sintesis Serbuk Warna hasil sintesis Kuning Titik leleh hasil sintesis >140°C
Rendemen 73,75 %
Senyawa hasil sintesis tampak seperti pada Gambar 10.
20 b. Kromatogram hasil sintesis vanilaseton.
Dari identifikasi secara kromatografi lapis tipis (KLT) dengan eluen campuran dari klorofom : etil asetat (9:1). Gambar 11 menunjukkan perbandingan antara senyawa hasil sintesis vanilaseton dan senyawa vanilin pada plat KLT yang disajikan di bawah lampu UV.
Gambar 11. Hasil KLT senyawa hasil sintesis vanilaseton Keterangan:
A : Senyawa hasil sintesis vanilaseton Rf A : 0,8
B : Senyawa vanilin Rf B : 0,74
21
mengetahui tingkat kemurnian dari senyawa hasil sintesis. Hasil TLC scanner
ditunjukkan pada Gambar 12 dan Gambar 13.
Gambar 12. Hasil TLCScanner senyawa hasil sintesis vanilaseton
(Kloroform: Etilasetat 9:1)
Gambar 13. Hasil TLCScanner senyawa vanillin (Kloroform: Etilasetat
9:1)
22
menunjukkan bahwa dalam senyawa hasil sintesis benar-benar sudah bebas dari zat pengotor.
c. Spektrum IR senyawa hasil sintesis vanilaseton.
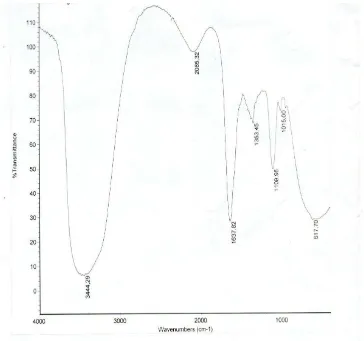
Senyawa yang didapatkan diidentifikasi strukturnya secara spektroskopi inframerah. Metode ini digunakan untuk mengetahui daerah serapan oleh gugus fungsi yang ada pada senyawa hasil sintesis. Daerah serapan tersebut terlihat pada Gambar 14 berikut:
23
Interpretasi spektrum IR di atas menunjukkan daerah serapan untuk masing-masing gugus fungsi pada senyawa hasil sintesis daerah serapan dapat dilihat pada Tabel 3 berikut.
Tabel 3. Daerah serapan pada senyawa hasil sintesis vanilin dan aseton
Daerah Serapan Gugus Fungsi
3444,29 O – H
1637,82 C = O
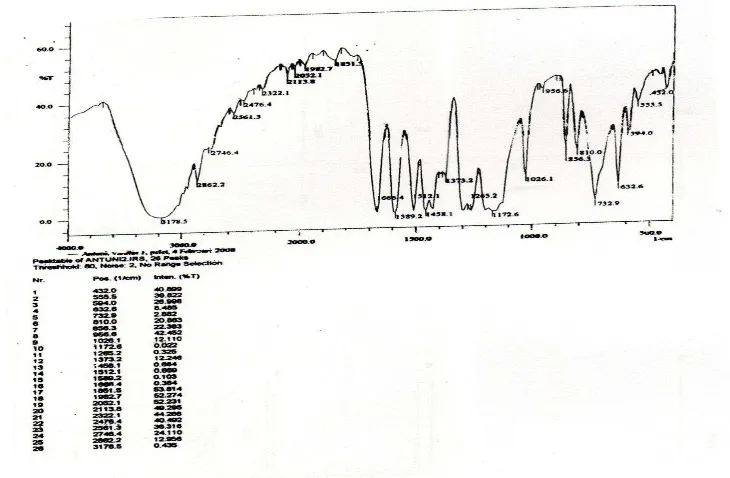
Spektrum IR senyawa hasil sintesis vanilaseton dibandingkan dengan spektrum IR vanilin, hal ini dilakukan untuk membandingkan serapan-serapan gugus fungsi yang ada dalam senyawa hasil sintesis dengan vanilin. Gambar 15 merupakan spektrum IR vanilin.
24
Berdasarkan spektrum IR tersebut, vanilin memiliki beberapa gugus fungsi seperti yang ditunjukan pada Tabel 4.
Tabel 4. Daerah serapan gugus fungsi pada senyawa vanilin
Daerah Serapan Gugus Fungsi
2746,4 dan 2862,2 CHO (aldehida)
3178,5 O-H
1666,4 C=O (keton, aldehida)
2. Hidrasi vanilaseton
a. Hasil hidrasi vanilaseton.
Hidrasi senyawa vanilaseton menggunakan H2SO4. Hasil pengamatan
pada tahap ini tersaji dalam Tabel 5 dan senyawa hasil hidrasi tampak seperti pada Gambar 16.
Tabel 5. Hasil pengamatan senyawa hasil hidrasi vanilaseton
Parameter Hasil pengamatan
Wujud Cair
Warna Larutan berwarna putih
Bau Tidak berbau
25
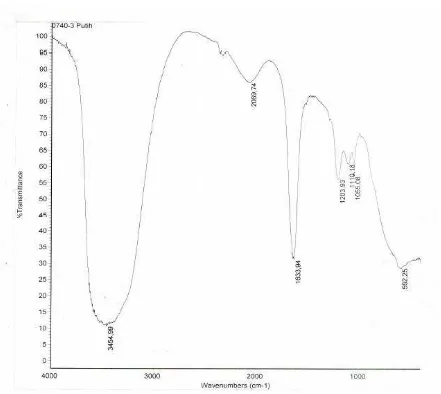
b. Spektrum IR senyawa hasil hidrasi vanilaseton.
Gambar 17. Spektrum IR senyawa hasil hidrasi vanilaseton
Tabel 6. Gugus fungsi yang terdapat pada senyawa hasil hidrasi vanilaseton
Daerah serapan Gugus fungsi
3454,99 OH
26
c. Kromatogram dan spektrum massa senyawa hasil hidrasi vanilaseton.
Berdasarkan spektrum GC-MS dapat diketahui massa serta persen kelimpahan dari suatu senyawa hasil sintesis. Hasil kromatogram GC dari senyawa hasil sintesis ditunjukkan pada Gambar 18 berikut:
Gambar 18. Kromatogram GC dari senyawa hasil sintesis vanilin dan aseton
Berdasarkan kromatogram hasil di atas terdapat dua puncak, puncak pertama dengan waktu retensi 11,100 menit dan puncak kedua dengan waktu retensi 25,331. Fragmentasi yang terjadi pada puncak 1 dan 2 ditunjukkan pada Gambar 19 dan Gambar 20.
27
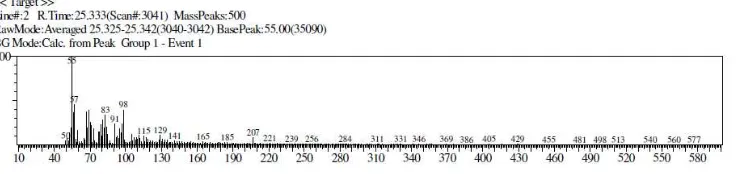
Gambar 20. Spektrum massa puncak 2 senyawa hasil hidrasi vanilaseton
B. PEMBAHASAN
1. Sintesis senyawa vanilaseton.
a. Hasil sintesis senyawa vanilaseton
Senyawa vanilaseton pada tahap ini disintesis melalui reaksi kondensasi aldol antara vanilin dan aseton dengan perbandingan mol 1:1. Katalis yang digunakan adalah basa kuat NaOH. Senyawa hasil yamg diperoleh berupa serbuk berwarna kuning, dengan rendemen sebesar 73,75% dan titik leleh >140°C. Menurut Anton Cahyono (2012), titik leleh vanilaseton yaitu 135-145°C. Sedangkan titik leleh vanilin sebesar 88-90°C, hal ini menunjukkan bahwa senyawa hasil sintesis sudah berbeda dengan bahan dasar yaitu vanilin.
28
Struktur resonansi ion enolat
+
+ H2O
Gambar 21. Reaksi pembentukan ion enolat dari aseton.
Ion enolat yang terbentuk berfungsi sebagai nukleofil. Nukleofil akan menyerang gugus karbonil pada vanilin membentuk ion alkoksida. Hal ini dikarenakan atom karbon gugus karbonil lebih bersifat elektropositif dari atom karbon lainnya. Serangan nukleofil menyebabkan ikatan π pada gugus karbonil vanilin putus dan elektron pindah ke atom oksigen dengan mekanisme berikut pada Gambar 22.
O
Gambar 22. Reaksi penyerangan ion enolat terhadap gugus karbonil.
29
dalam menjaga molekul senyawa bentuk enol pada saat kesetimbangan keto-enol. Mekanisme pembentukan senyawa β-hidroksi keton ditunjukkan pada Gambar 23.
Gambar 23. Reaksi pembentukan senyawa β-hidroksi keton
Senyawa β-hidroksi keton ini sangat mudah mengalami dehidrasi karena ikatan rangkap dalam produk berkonjugasi dengan gugus karbonil sehingga menghasilkan senyawa vanilaseton. Dehidrasi ini juga disebabkan karena ikatan rangkap distabilkan oleh konjugasi tidak hanya dengan gugus karbonil tetapi juga dengan cincin aromatik. Reaksi dehidrasi ditunjukkan pada Gambar 24.
CH
Gambar 24. Reaksi dehidrasi
30
Gambar 25. Reaksi pembentukan fenoksida
Selain menyebabkan reaksi dehidrasi aldol penambahan HCl berfungsi untuk mengembalikan fenoksida menjadi kebentuk semula yaitu vanilin seperti pada Gambar 26.
C
Gambar 26. Reaksi pengembalian fenoksida menjadi vanilin.
b. KLT senyawa hasil sintesis vanilaseton
31
asetat, sehingga senyawa hasil sintesis vanilaseton adalah senyawa yang lebih non polar dari vanilin.
Harga Rf senyawa hasil sintesis dan vanilin berturut-turut sebesar 0,8 dan 0,74. Perbedaan harga Rf antara senyawa hasil vanilaseton dan vanilin menunjukkan bahwa senyawa hasil sintesis adalah senyawa yang berbeda dari bahan dasar yaitu vanilin. Hasil uji kemurnian dengan TLC scanner
menunjukkan kemurnian sebesar 100%.
c. Identifikasi senyawa hasil sintesis vanilaseton secara spektroskopi IR
Identifikasi struktur hasil sintesis dilakukan secara spektroskospi inframerah. Tujuan dari identifikasi ini yaitu untuk mengetahui gugus-gugus fungsi yang ada di dalam sampel yang dianalisis dan untuk mengetahui apakah reaksi sudah berlangsung atau belum dengan membandingkan spektrum IR reaktan dan spektrum IR produk.
32
Tabel 7. Serapan gugus fungsional senyawa hasil sintesis dan vanilin dengan spektroskopi IR.
Gugus Fungsional Daerah Serapan (cm
-1
) Senyawa hasil sintesis Vanilin
1637,82 1656,83
aldehida - 2746,4 dan 2862,2
-OH fenolik 3444,29 3255,95
Berdasarkan data Tabel 7 senyawa hasil sintesis sudah berbeda dengan vanilin, karena pada senyawa hasil sintesis sudah tidak terdapat gugus aldehida. Hal ini menunjukkan sintesis vanilaseton sudah berlangsung.
2. Hidrasi vanilaseton.
a. Hasil hidrasi senyawa vanilaseton
OCH3
Gambar 27. Reaksi hidrasi senyawa vanilaseton
33
Gambar 28. Mekanisme hidrasi
Tahap selanjutnya karbonium A dan karbonium B diserang oleh nukleofil OH- terjadi produk reaksi 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on, dan 4-(4'-hidroksi-3'-metoksifenil)-3-hidroksibutan-2-on. Reaksi pembentukan senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on ditunjukkan pada Gambar 29, dan reaksi pembentukan senyawa 4-(4'-hidroksi-3'-metoksifenil)-3-hidroksibutan-2-on ditunjukan pada Gambar 30.
OCH3
Gambar 29. Pembentukan senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on
34
Jadi pada reaksi hidrasi vanilaseton diperoleh dua produk yaitu 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on, dan 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on, sedangkan produk yang dominan dalam reaksi ini adalah senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on. Hal ini disebabkan karena dalam mekanisme reaksi pembentukan senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on melibatkan karbonium benzilik yang terstabilkan oleh resoansi. Adapun resonansi yang terjadi adalah sebagai berikut pada Gambar 31.
OCH3
35
b. Identifikasi senyawa hasil hidrasi vanilaseton secara spektorskopi IR
Berdasarkan spektrum IR senyawa hasil hidrasi diketahui senyawa hasil hidrasi belum terbentuk, hal itu ditunjukkan oleh kemiripan spektrum antara senyawa hasil sintesis dengan senyawa hasil hidrasi. Perbandingan hasil IR antara hasil sintesis dan hasil hidrasi tersaji pada Tabel 8.
Tabel 8. Perbandingan gugus karakteristik hasil sintesis dengan hasil hidrasi
No Gugus
karakteristik
Daerah Serapan (cm-1) Hasil Sintesis Vanilin
dan Aseton
Hasil Hidrasi Vanilaseton
1 O-H 3444,29 3454,99
2 C = O 1637,82 1633,94
Berdasarkan tabel tesebut terdapat kemiripan serapan antara hasil sintesis dan hasil hidrasi, ada kemungkinan reaksi hidrasi belum berjalan atau terjadi. Untuk lebih meyakinkan bahwa sintesis berhasil atau tidak maka dilakukan identifikasi lebih lanjut dengan GC-MS.
c. Identifikasi senyawa hasil hidrasi vanilaseton dengan GC-MS
Spektroskopi GC-MS digunakan untuk menentukan molekul relatif dan persen kelimpahan dari senyawa hasil sintesis. Berdasarkan kromatogram hasil di atas terdapat dua puncak, puncak pertama dengan waktu retensi 11,100 menit dan puncak kedua dengan waktu retensi 25,331. Hidrasi senyawa vanilaseton dengan H2SO4 diharapkan menghasilkan senyawa produk dengan m/z 209. Namun dari
36
Pada spektra GC-MS menunjukkan senyawa produk dengan m/z 152. Hal ini berarti bahwa senyawa yang dikehendaki belum terbentuk. Spektra GC-MS ternyata menunjukkan spektra senyawa dasar yaitu vanillin. Gambar 32 menunjukkan kemungkinan fragmentasi senyawa vanillin.
Gambar 32. Fragmentasi vanilin
Berdasarkan data analisis di atas, dapat diketahui bahwa sintesis senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on belum berhasil. Ada kemungkinan senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on sudah terbentuk tetapi terpecah menjadi vanilin dan aseton.
37
Gambar 33. Pembentukan enol melalui perpindahan elektron C
Tahap 2: Terjadi serangan dari atom oksigen berkerapatan tinggi terhadap proton sehingga terjadi gugus OH (Gambar 34).
+ H
Gambar 34. Serangan atom oksigen terhadap proton
Tahap 3: Terjadi pelepasan proton dari gugus OH disertai pemutusan ikatan C-C maka akan terjadi 4-hidroksi-3-metoksibenzaldehida dan karbanion (Gambar 35) .
Gambar 35. Pelepasan proton dari gugus OH
38
Gambar 36. Serangan karbanion terhadap proton
Bentuk enol merupakan bentuk yang tidak stabil sehingga langsung berubah kebentuk yang lebih stabil yaitu aseton (Gambar 37).
C
Gambar 37. Kesetimbangan bentuk enol
39 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan analisis yang telah dilakukan maka dapat ditarik beberapa kesimpulan sebagai berikut:
1. Senyawa 4-(4'-hidroksi-3'-metoksifenil)-4-hidroksibutan-2-on tidak dapat dihasilkan melalui reaksi hidrasi terhadap senyawa hasil sintesis antara vanilin dan aseton.
2. Karakteristik dan sifat fisik senyawa hasil reaksi hidrasi senyawa hasil sintesis antara vanillin dan aseton berupa larutan berwarna putih yang mengandung gugus fungsi OH dan ikatan C-O, sedangkan pada spektra GC-MS menunjukkan senyawa dasar yaitu vanilin.
B. Saran
40
DAFTAR PUSTAKA
Allinger et al. 1980, Organic Chemistry Second Editions, New York : Worth Publissher Inc page : 307 – 308
Anton Cahyono. (2012). Reaksi Kondensasi Aldol Silang Antara Vanilin dan Aseton dengan Katalis Bifungsional NaOH/ZrO2-Montmorillont. Skripsi. Universitas
Negeri Yogyakarta : Jurdik Kimia FMIPA.
Budimarwanti, C. (2007). Sintesis Senyawa Benzill dari Bahan Awal Vanilin melalui Reaksi Witig dan Hidrogenasi Katalitik. Prosiding, Seminar Nasional Penelitian, Pendidikan dan Penerapan MIPA Universitas Negeri Yogyakarta. Bahl, B. S. (1979). Advanced Organic Chemistry, S. Chan and Company Ltd., New
Delhi, pp 1061 -1077.
Cahya Rotama (2011) . Reaksi Kondensasi Antara 4 – Bromoasetofenon dengan Vanilin. Skripsi. Yogyakarta : UNY
Deni Pranowo, M. Yusuf Affandi, Wahyu Candraningrum, dan M. Muchalal, (2010). Mempelajari sintesis 4-(hidroksifenil)-3-buten-2-on. Jurusan Kimia Fakultas Gajah Mada.
Fessenden, Ralph J. & Fessenden, Joan S. (1999). Kimia Organik edisi ke 3 Jilid 2. (Terjemahan A. H. Pudjaatmaka). Jakarta: Erlangga.
Fessenden, R.J & Fessenden, R.J. (1982). Kimia Organik Edisi ke 3 Jilid 2. Jakarta Erlangga.
Gritter, T. A., Bobbit, J. M., & Schwarting, A. E. (1991). Pengantar Kromatografi. Edisi kedua. (Terjemahan Kosasih Padmawinata). Bandung: Penerbit ITB. Hardjono Sastrohamidjojo. (1985). Kromatografi. Yogyakarta: Liberty.
Hardjono Sastrohamidjojo. (2007). Spektroskopi. Edisi Ketiga. Yogyakarta: Liberty. Hardjono Sastrohamidjojo. (1991). Spektroskopi. Yogyakarta: Liberty.
41
Hart, Harold., Craine, L.E., & Hart, D.J., (2003). Kimia Organik Suatu Kuliah Singkat. Edisi Kesebelas.(Alih Bahasa: Suminar Setriati Achmadi, Phd.). Jakarta : Penerbit Erlangga.
Khopkar, S.M. (2008). Konsep Dasar kimia Analitik. Jakarta : UI Press
Noverry Ambo, (2012). Sintesis Senyawa 4-(4'-Hidroksi-3'-Metoksifenil)-3-Buten-2- On Dengan Katalis Basa Serta Uji Potensinya Sebagai Tabir Surya http://eprints.uny.ac.id/9352/. Diakses pada 3 Desember 2016. Pukul 19.33.
McMurry, John. (2007). Organic Chemistry:A Biological Approach. USA: Thomson Brooks/Cole.
Markham, Sitorus. (2009). Spektroskopi Elusidasi Struktur Molekul Organik. Yogyakarta: Graha Ilmu.
Markham, Sitorus. (2010). Kimia Organik Umum. Yogyakarta : Graha Ilmu.
Tri Panji. (2012). Teknik Spektroskopi untuk Elusidasi Struktur Molekul.Yogyakarta: Graha Ilmu.
Sri Handayani, Retno Arianingrum, dan Winarto Haryadi, (2013). Aktivitas Antioksidan dan Antikanker Turunan Benzalaseton. Jurnal Penelitian Saintek
(Vol.18, No. 1). Hlm. 71-73
Stahl, Egon. (1985). Analisis Obat secara Kromatografi dan Mikroskopi. (Terjemahan Kosasih Padmawinata). Bandung: ITB.
Ravendra Kumar, P. K. Sharma, dan Prem Shanker Mishra, (2012). A Review on the Vanillin derivatives showing various Biological activities. International
Journal of PharmTech Research. No.1, 266-279.
42 Lampiran 1
Perhitungan Bahan
A. Sintesis 4-(4'-hidroksi-3'-metoksifenil)-3-buten-2-on
43 Lampiran 2
Prosedur Kerja
A. Sintesis senyawa vanilaseton
NaOH 0,156 g
Aseton 0,145 g
Gelas beker Vanilin
0,383 g
Hasil sintesis
Endapan
Ditentukan sifat fisik berupa berat, bentuk, warna, titik
leleh dan rendemen
TLC Scanner
Diidentifikasi dengan spektrofotometer IR
Distirer 3 jam
Ditambah HCl
44 B. Hidrasi senyawa vanilaseton
2 ml akudest
Gelas beker 50 ml
Disaring dan diambil lapisan organik 0,1 gram sampel
dilarutkan dalam 2m akuadest
3-5 tetes H2SO4
Lapisan organik ditambah Na2SO4 anhidrat untuk mengikat
molekul air
Diidentifikasi dengan Spektrofotometer IR dan GC-MS
Dipanaskan dengan suhu 40oC selama 5 menit
Disaring
45 Lampiran 3
Dokumentasi Penelitian
No Gambar Keterangan
1
Proses Sintesis
2
Hasil penyaringan
3
Hasil hidrasi
4
Proses pengembangan eluen
5
46 6
Spektrofotomrter infra merah (shimadzu FTIR
Prestige 21)
7
47 Lampiran 4
Perhitutang Nilai Rf Kromatografi Lapis Tipis
Secara sistematis perhitungan Rf menggunakan rumus: Rf =
Dengan, l = jarak noda dari titik awal ke titik akhir setelah proses pengembangan (cm)
Berdasarkan rumus perhitungan nilai Rf, didapatkan hasil sebagai Rf A =
= 0,8
Rf B =
48 Lampiran 5
Data Hasil TLC Scannner
A. Senyawa hasil sintesis
49 Lampiran 6
Data Hasil FTIR
51
52
Lampiran 7