Bab IV
Hasil dan Pembahasan
Hasil penelitian meliputi proses aklimatisasi, produksi AOVT (Asam Organik Volatil Total), produksi asam organik volatil spesifik (asam format, asam asetat, asam propionat, asam butirat dan asam valerat), dan penurunan COD.
IV.1 Proses Aklimatisasi
Proses aklimatisasi bertujuan untuk mendapatkan bibit yang siap bekerja untuk memproduksi asam organik volatil dari substrat yang kompleks, stillage ubi kayu.
Dalam tabel IV.1 ditampilkan komposisi stillage ubi kayu yang dipakai sebagai bahan baku dalam penelitian ini.
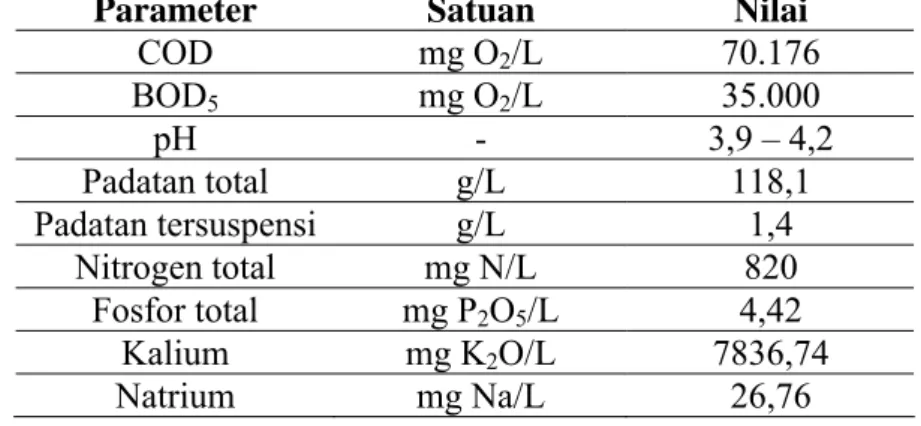
Tabel IV.1 Komposisi stillage ubi kayu
Parameter Satuan Nilai
COD mg O2/L 70.176 BOD5 mg O2/L 35.000 pH - 3,9 – 4,2 Padatan total g/L 118,1 Padatan tersuspensi g/L 1,4 Nitrogen total mg N/L 820
Fosfor total mg P2O5/L 4,42
Kalium mg K2O/L 7836,74
Natrium mg Na/L 26,76
Pada tabel IV.1 dapat dilihat bahwa nilai COD stillage ubi kayu cukup tinggi. Hal
ini yang merupakan salah satu dasar dilakukannya penelitian ini. Karena nilai COD yang tinggi menggambarkan besarnya kandungan bahan organik dalam suatu bahan. Seperti sudah disampaikan sebelumnya, bahan organik merupakan sumber nutrisi bagi mikroba dalam proses anaerobik untuk diubah menjadi asam organik volatil. Selain itu karena stillage ubi kayu merupakan limbah maka dengan diubahnya sebagian bahan organik menjadi asam organik volatil maka potensi stillage ubi kayu sebagai limbah akan berkurang. Stillage ubi kayu yang
dipakai diencerkan hingga memiliki nilai COD ± 20 g/L dengan MLSS awal 400 mg/L. Setelah kotoran sapi diaklimatisasi pada pH ± 5,6 dan suhu kamar dengan waktu sekitar 5 bulan didapatkan MLSS akhir 3000 mg/L. Stillage ubi kayu yang
sudah siap menjadi bibit akan mengalami perbedaan warna yang semula coklat keruh menjadi lebih jernih.
IV.2 Produksi Asam Organik Volatil Total
Asam organik volatil total ditentukan dengan cara mendistilasi kaldu fermentasi, selanjutnya distilat dititrasi dengan larutan basa. Konsentrasi asam total yang didapat dinyatakan sebagai konsentrasi asam asetat. Cara ini merupakan cara baku dalam penentuan konsentrasi asam organik volatil. Karena pengambilan contoh mempengaruhi volume kerja yang dipakai, maka semua hasil yang didapat dihitung dengan mengembalikan ke volume awalnya. Hasil yang didapat pada bagian pertama penelitian yang berlangsung dalam erlenmeyer bervolume kerja 1,5 L ditampilkan dalam gambar IV.1 berikut.
0,0 2,0 4,0 6,0 8,0 10,0 0,0 20,0 40,0 60,0 80,0
waktu sampling, jam
TA
OV
, g C
pH 5 pH 6 pH 7
Gambar IV.1 Produksi Asam Organik Volatil Total di erlenmeyer
Dari gambar IV.1 terlihat bahwa asam organik volatil total terbanyak diperoleh pada saat pH proses 7. Sedangkan waktu optimal produksi asam organik volatil total adalah 24 jam. Pada pH proses 5 tidak diperoleh hasil lebih rendah. Berbeda dengan hasil yang diperoleh oleh Hwang dkk (2001), pada pH 5,9 dan suhu 35°C
membutuhkan waktu 0,88 hari. Sedangkan Yang dkk (2004) melaporkan pada saat suhu 35°C dan pH 6 memerlukan waktu 2,1 hari.
Berdasar hasil yang didapat ini penelitian dilanjutkan dengan menggunakan bioreaktor skala laboratorium (Biostat) bervolume kerja 7,5 L dan pH proses yang dikendalikan dengan alat pengendali. Berbeda dengan proses yang berlangsung dalam erlenmeyer, pengaturan pH hanya secara manual. Yaitu setiap kali melakukan pengambilan contoh dilakukan pengaturan ulang pH dengan menambahkan K2CO3. Pada penelitian bagian kedua dipilih pH proses 6,5. Asam organik volatil total yang diperoleh dengan cara baku (distilasi) dapat dilihat pada gambar IV.2 berikut.
0,0 5,0 10,0 15,0 20,0 25,0 30,0 35,0 0,0 20,0 40,0 60,0 80,0
waktu sampling, jam
TAV, g C
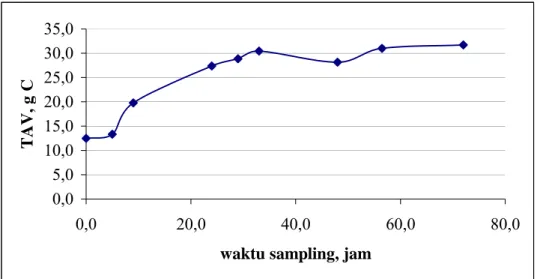
Gambar IV.2 Produksi asam organik volatil total di Biostat
Pada gambar IV.2 dapat dilihat bahwa secara keseluruhan terjadi kenaikan produksi. Waktu optimal yaitu 33 jam, sedikit lebih lama dibanding dengan hasil dari erlenmeyer pH 7,0. Perpanjangan waktu ini diduga karena bibit harus beradaptasi dengan volume kerja yang lebih besar. Hal ini nampak pada 5 jam pertama kurva menunjukkan garis datar. Setelah 5 jam, bibit sudah dapat memproduksi asam organik volatil. Tetapi tidak melebihi dari hasil yang didapat oleh Yang dkk (2004), 2,1 hari. Dari penelitian yang dilakukan oleh Nugroho dan Yustendi (2007) didapat waktu untuk menghasilkan asam organik volatil terbanyak adalah 40 jam.
Pada erlenmeyer dan Biostat terjadi perubahan bahan organik menjadi asam organik volatil. Perubahan ini dapat dinyatakan sebagai nilai yield bahan organik.
Pada erlenmeyer dan pH proses 7 didapat yield sebesar 17,9 % sedang pada
Biostat didapat 21,9 %. Rumus perhitungannya adalah sebagai berikut.
( )
100%
massa akhir AOVT massa awal AOVT
yield x
massa COD awal
−
= (IV.1)
Dalam rumus IV.1 diatas, nilai massa dinyatakan sebagai g karbon (g C). IV.3 Produksi asam organik volatil spesifik
Untuk mengetahui komposisi asam organik volatil dalam penelitian ini dilakukan analisa dengan menggunakan GC Ion DIONEX ICS 1000. Contoh yang sudah diambil harus diawetkan dulu pada pH ± 2 dan suhu 4oC sebelum dianalisa. Hasil analisa menunjukkan bahwa terdapat lima jenis asam organik volatil yaitu asam format, asam asetat, asam propionat, asam butirat dan asam valerat.
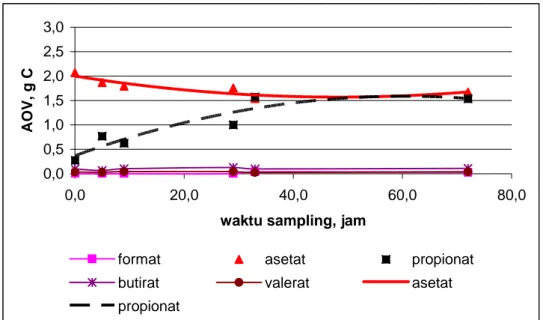
Pada penelitian dalam erlenmeyer dengan tiga variasi nilai pH proses disajikan seperti pada gambar IV.3 hingga IV.5 berikut.
0,0 0,5 1,0 1,5 2,0 2,5 3,0 0,0 20,0 40,0 60,0 80,0
waktu sampling, jam
AOV, g C
format asetat propionat
butirat valerat asetat
propionat
0,0 0,5 1,0 1,5 2,0 2,5 3,0 0,0 20,0 40,0 60,0 80,0
waktu sampling, jam
AOV
, g C
format asetat propionat butirat
valerat asetat propionat
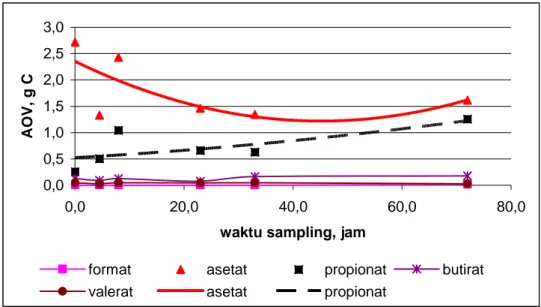
Gambar IV.4 Produksi asam organik volatil spesifik pada pH 6
0,0 0,5 1,0 1,5 2,0 2,5 3,0 0,0 20,0 40,0 60,0 80,0
waktu sampling, jam
AO
V
, g C
format asetat propionat butirat
valerat asetat propionat
Gambar IV.5 Produksi asam organik volatil spesifik pada pH 7
Seperti terlihat pada gambar IV.3 hingga IV.5 tersebut, asam asetat dan asam propionat mendominasi produk proses anaerobik. Pada proses dengan pH 5 terlihat asam asetat cenderung naik tetapi tidak securam asam propionat yang naiknya lebih tajam. Hal ini menunjukkan laju pembentukan asam asetat lebih rendah dibanding laju pembentukan asam propionat. Hasil yang serupa dinyatakan oleh Qing dan Fang, (2002) yang mendapatkan pada rentang pH 4 – 4,5 dihasilkan lebih banyak asam propionat. Sedangkan pada pH proses 6 terlihat ada fluktuasi produksi asam asetat di awal dan mulai meningkat di akhir rentang
waktu yang diambil. Berbeda dengan produksi asam propionat yang cenderung terus meningkat dan hanya mengalami sedikit penurunan. Hasil berbeda didapat oleh Qing dan Fang (2002) yang menyatakan bahwa pada rentang pH 6 – 6,5 lebih banyak dihasilkan asam asetat dan asam butirat, seperti yang juga didapat oleh Nugroho dan Yustendi (2007). Pada pH proses 7 terlihat bahwa produksi asam asetat cenderung menurun demikian juga dengan asam propionat. Tetapi sama dengan pada pH proses 5 dan 6, asam asetat dan asam propionat mendominasi produk. Hasil penelitian Hu dkk (2006) melaporkan bahwa pH 6,9 merupakan kondisi optimal untuk proses asidogenesis dan menghasikan lebih banyak asam asetat serta asam propionat. Tetapi Horiuchi dkk (2002), melaporkan pada rentang pH 5 – 7 akan didapat asam butirat dan asam asetat lebih banyak. Perbedaan yang terjadi diduga karena kondisi bibit yang dipakai pada penelitian kali ini tidak pada rentang pH mendekati 7.
Adanya asam propionat yang cenderung meningkat mengindikasikan satu hal penting. Kandungan gas H2 terakumulasi dalam erlenmeyer, hingga asam propionat tidak bisa terkonversi oleh mikroba asetogen untuk menghasilkan asam asetat. Asam propionat tetap diproduksi oleh mikroba asidogen tetapi tidak bisa diubah menjadi asam asetat.
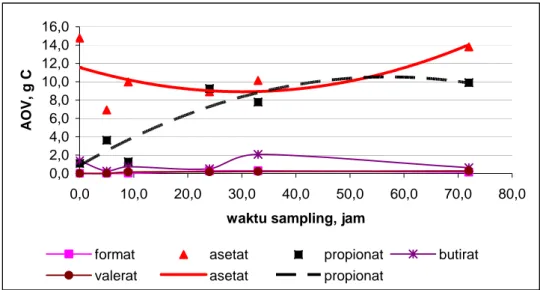
Hasil yang didapat pada proses dalam Biostat dengan volume kerja 7,5 L disajikan dalam gambar IV.6. Gambar tersebut menunjukkan hasil serupa dengan proses dalam erlenmeyer. Asam asetat dan asam propionat mendominasi produk. Laju pembentukan asam asetat cenderung meningkat demikian juga asam propionat. Terlihat jumlah asam propionat masih banyak, hal ini mengindikasikan bahwa gas H2 terakumulasi dalam Biostat.
0,0 2,0 4,0 6,0 8,0 10,0 12,0 14,0 16,0 0,0 10,0 20,0 30,0 40,0 50,0 60,0 70,0 80,0
waktu sampling, jam
AOV, g C
format asetat propionat butirat
valerat asetat propionat
Gambar IV.6 Produksi asam organik volatil spesifik di Biostat
Reaksi pembentukan asam asetat dari asam propionat (Speece, 1996) dituliskan sebagai berikut.
3 2
CH CH COO− +3H O2 ←⎯⎯⎯⎯→CH COO3 −+HCO3−+H++3H2 ΔG° = 76 kJ/mol
3 2 2
CH CH CH COO− +2H O2 ←⎯⎯⎯⎯→2CH COO3 −+2H2 ΔG° = 48,1 kJ/mol
Bila melihat nilai energi bebas Gibb’s standart nilainya positif. Karena positif maka reaksi tidak dapat berlangsung, hingga untuk membuat energi bebas Gibb’s menjadi negatif, maka tekanan parsial hidrogen harus di bawah 10-4 atm agar asam propionat bisa berubah menjadi asetat , (Speece, 1996).
Sedangkan asam butirat, bisa lebih mudah diubah menjadi asam asetat dibanding asam propionat. Karena meski nilai energi bebas Gibb’s standart masih positif tetapi tekanan parsial hidrogen yang dibutuhkan lebih tinggi, yaitu bernilai 10-3 atm.
Untuk menurunkan tekanan parsial hidrogen hingga serendah itu dapat dibantu dengan menggunakan kultur campuran antara mikroba asetogenik penghasil H2 dan mikroba metanogen pengguna H2, (Boone dkk 1980). Pada perkembangan terakhir dipakai dua buah bioreaktor yang dipasang seri, (Nie dkk, 2007). Pada bioreaktor pertama dihasilkan asam asetat, CO2 dan H2. Selanjutnya di bioreaktor kedua, CO2 dan H2 dikonversi menjadi asam asetat. Penggunaan sirkulasi gas dan
proses fedbatch di sistem bioreaktor seri tersebut juga dapat meningkatkan
konversi asam asetat, (Nie dkk, 2008). Pada penelitian kali ini ditambahkan gas nitrogen untuk mengusir sebagian besar gas H2 yang terbentuk setiap kali mengambil contoh. Selain itu dipakai pompa peristaltik untuk mensirkulasi gas nitrogen yang berfungsi sebagai pengusir (stripper) H2 yang terbentuk.
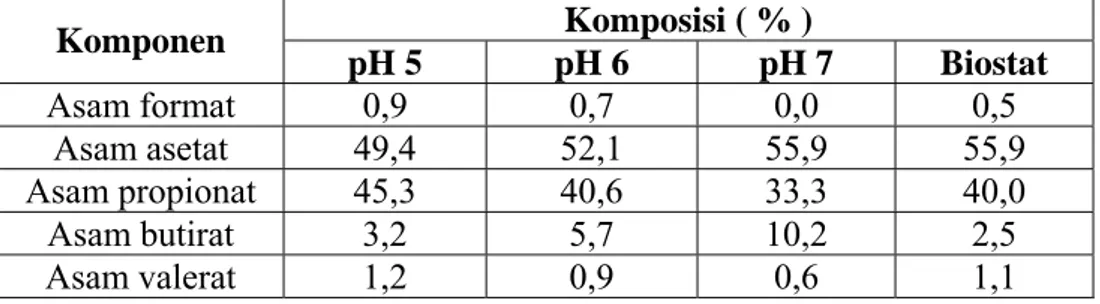
Untuk lebih jelasnya, tabel IV.3 menyajikan komposisi asam organik volatil di akhir proses pada dua bioreaktor.
Tabel IV.2 Komposisi asam organik volatil di akhir proses Komposisi ( % ) Komponen pH 5 pH 6 pH 7 Biostat Asam format 0,9 0,7 0,0 0,5 Asam asetat 49,4 52,1 55,9 55,9 Asam propionat 45,3 40,6 33,3 40,0 Asam butirat 3,2 5,7 10,2 2,5 Asam valerat 1,2 0,9 0,6 1,1
Dari tabel tersebut nampak jelas bahwa di akhir proses , asam asetat dan asam propionat yang mendominasi produk. Di semua variasi pH asam asetat diperoleh berkisar 50 % sedangkan asam propionat berkisar 40 %.
IV.4 Penurunan COD
Sesuai definisinya, COD melambangkan keberadaan senyawa organik dalam suatu bahan. Reaksi pembentukan asam organik volatil dari stillage ubi kayu akan
mengkonsumsi sebagian bahan organik yang terkandung dalam stillage ubi kayu.
Dengan sendirinya bila terbentuk asam organik volatil dari stillage ubi kayu maka
COD stillage ubi kayu akan turun.
Pada bagian pertama penelitian ini yang berlangsung dalam erlenmeyer dengan variasi pH didapat hasil yang bervariasi juga. Hal ini dapat dilihat pada gambar IV.7. Pada gambar tersebut terlihat bahwa secara keseluruhan terjadi penurunan nilai COD di ke tiga variasi pH proses. Meskipun pada waktu-waktu tertentu
terjadi kenaikan nilai COD. Sedangkan persentase penurunan nilai COD dapat dilihat pada gambar IV.8.
0,0 10,0 20,0 30,0 40,0 50,0 0,0 20,0 40,0 60,0 80,0
waktu sampling, jam
COD, g C
pH 5 pH 6 pH 7 pH 6
pH 5 pH 7
Gambar IV.7 Penurunan COD di erlenmeyer
0,0 2,0 4,0 6,0 8,0 10,0 12,0 14,0 16,0 4,0 4,5 5,0 5,5 6,0 6,5 7,0 7,5 pH % pe nur unan COD
Gambar IV.8 Persentase penurunan COD stillage ubi kayu di erlenmeyer Pada gambar IV.8 terlihat bahwa proses pada pH 6,0 memberikan hasil terbaik yaitu penurunan nilai COD sebesar 14,3 %. Nilai yang tidak terlalu besar untuk penurunan COD suatu proses penanganan limbah. Hal ini mengindikasikan selama proses tidak terjadi perubahan bahan organik menjadi metana. Perubahan yang terjadi adalah bahan organik menjadi asam organik volatil yang terlarut. Hal yang hampir sama terjadi pada proses yang berlangsung dalam bioreaktor skala laboratorium seperti dapat dilihat pada gambar IV.9 berikut.
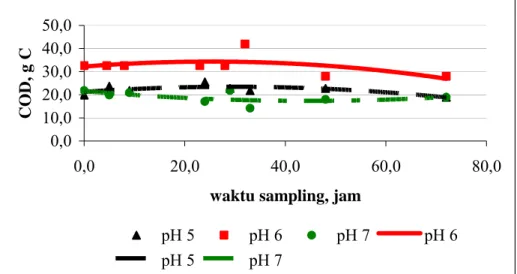
0,0 20,0 40,0 60,0 80,0 100,0 120,0 140,0 0,0 20,0 40,0 60,0 80,0
waktu sampling, jam
CO
D, g C
Gambar IV.9 Penurunan COD pada Biostat
Pada gambar IV.9 secara keseluruhan terlihat terjadi penurunan COD. Bila persentase penurunan COD dihitung didapat penurunan sebesar 36,4 %. Nilai ini masih rendah untuk suatu proses penanganan limbah, mengingat volume kerja Biostat (7,5 L) yang lebih besar dibanding erlenmeyer (1,5 L).
Mikroba yang dipakai sebagai bibit merupakan konsorsium mikroba anaerobik. Gambar IV.10 merupakan foto dari mikroba yang ditemui dalam Biostat. Pada gambar IV.10 terlihat bahwa sebagian besar mikroba merupakan bakteri (berwarna merah). Kebanyakan berbentuk batang dan bulat. Selain itu dijumpai juga spora, tetapi belum jelas asalnya, spora bakteri , ragi atau jamur. Karena
stilage ubi kayu berasal dari proses pembuatan bioetanol, maka dijumpai juga sel