94
Ekstraksi dan Pemisahan Penisilin G dari Fenilasetat dengan Teknik Membran Cair Emulsi
Imam Santoso1,2), Buchari2), Muhamad Bachri Amran2), Aminudin Sulaeman2) 1)
Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Jakarta, Jakarta 2)
Kelompok Keilmuan Kimia Analitik, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Teknologi Bandung, Bandung
e-mail: Imamsantoso_chem@yahoo.com
Diterima 11 Oktober 2006, disetujui untuk dipublikasikan 30 Mei 2007 Abstrak
Pemisahan dan pemurnian penisilin G dari asam fenilasetat (PAA) sangat sulit dilakukan karena kedua senyawa ini bersifat asam lemah dan kedua molekul senyawa tersebut dapat berubah dari satu ke lain akibat perrubahan pH larutan. Penelitian ini bertujuan untuk menentukan kondisi optimum ekstraksi dan pemindahan penisilin G dari fenilasetat. Kondisi optimum dicapai bila perbandingan volume fasa internal (Vi) terhadap volume fasa membran (Vm) 1:1; waktu pengadukan pembuatan emulsi 1 menit; kecepatan kontak, 300 rpm; waktu kontak, 15 menit; kecepatan pengadukan pembuatan emulsi 2000 rpm; waktu pendiaman emulsi 13 menit; konsentrasi larutan penisilin G dalam fasa eksternal 375 ppm; dan konsentrasi Span 80, 5 %. Pada kondisi ini penisilin G telah dapat diekstraksi dan dipisahkan dari fenilasetat dengan faktor daya pisah 19,38 dalam waktu kontak 15 menit. Dengan demikian cara ekstraksi membran cair emulsi dapat digunakan sebagai cara yang cukup efektif untuk memisahkan penisilin G dari fenilasetat.
Kata kunci: Penisilin G, Fenilasetat, Teknik membran cair emulsi
Abstract
The separation and purification of penicillin G from phenyl acetic acid (PAA) is very difficult to be carried out because the two compounds are weak acids and the two compounds can change from one to another by influence of pH. The aim of this research is to establish the optimal conditions for the extraction and separation of penicillin G from phenylacetic acid using the emulsion liquid membrane technique. The optimal conditions were ratio of internal phase volume to membrane phase volume of 1:1; time of stiring for emulsion preparation of 1 minute; emulsion contact rate of 300 rpm; emulsion contact time of 15 minutes; rate of stirring of emulsion of 2000 rpm; rest time of emulsion of 13 minutes; concentration of penicillin G as external phase 375 ppm; and concentration of surfactant 5% (v/v). At these conditions penicillin G can be extracted and separated from phenylacetic acid with a separation factor of 19.3 and a contact time of 15 minutes. Thus the technique of emulsion liquid membrane may be used as a reasonably effective method to separate penicillin G from phenylacetic acid.
Keywords: Penicillin G, Phenylacetic acid, Emulsion liquid membrane technique 1. Pendahuluan
Pada proses fermentasi, asam fenilasetat sering ditambahkan pada medium fermentasi sebagai senyawa prekursor pada pembentukan penisilin G (Lee
et al., 1994). Fenilasetat harus dipisahkan dan diperoleh
kembali dari larutan fermentasi karena sifatnya yang toksik. Oleh karena itu, pemisahan penisilin dari hasil fermentasi adalah merupakan langkah penting.
Kualitas penisilin G yang diperoleh dari hasil fermentasi sangat ditentukan oleh teknik pemisahan atau pemurnian penisilin G dengan komponen zat-zat lain yang masih tercampur dalam medium fermentasi terutama pada pemisahan asam fenilasetat yang sengaja ditambahkan sebagai prekursor.
Saat ini untuk skala industri, pemurnian penisilin G dari asam fenilasetat yang bersifat toksik masih menggunakan teknik ekstraksi pelarut. Teknik
ini relatif sederhana tetapi tidak ekonomis karena proses ekstraksi dan re-ekstraksi tidak dapat dikerjakan secara simultan dan kehilangan ekstraktan selama ekstraksi tidak dapat dihindarkan sehingga berpotensi sebagai polutan berbahaya dan kehilangan penisilin G akibat dekomposisi mencapai 10-15% (Hano et al., 1990). Dengan demikian tujuan komersial, pemisahan penisilin G dan asam fenilasetat dengan teknik ekstraksi pelarut hingga saat ini dinilai memiliki banyak keterbatasan dan tidak ekonomis (Likidis and Schugerl, 1987) akibat mudahnya senyawa tersebut terdekomposisi pada pH rendah (Reschke and Schugerl, 1984). Hal ini yang menyebabkan harga penisilin G masih relatif mahal.
Pemisahan dan pemurnian penisilin G dari asam fenilasetat (PAA) sangat sulit dilakukan karena kedua senyawa ini bersifat asam dan kedua molekul
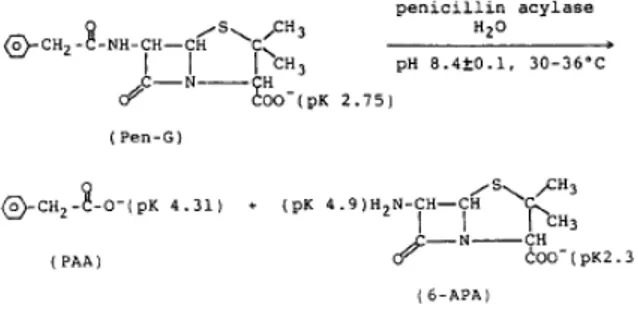
senyawa tersebut dapat berubah antara satu sama lainnya akibat adanya enzim penisilin asilase dan perubahan pH larutan seperti reaksi pada Gambar 1 (Rajendhran and Gunasekaran, 2004). Enzim penisilin asilase dapat menghidrolis dan mengubah penisilin G menjadi PAA dan asam 6-aminopenisilanat (6-APA).
Gambar 1. Reaksi hidrolisis penisilin G akibat
perubahan pH.
Adanya beberapa keterbatasan tersebut menyebabkan para ilmuwan berusaha mencari dan mengembangkan beberapa teknik pemisahan lainnya. Hingga saat ini tidak kurang dari sepuluh teknik pemisahan penisilin G telah dikembangkan. Teknik-teknik tersebut adalah Teknik-teknik mikrofiltrasi (Adikane et
al., 1999), resin penukar ion (Luuk et al., 1996),
elektrodialisis (Chen and Huang, 1995), teknik cloud
point extraction (Wang et al., 2006), teknik supported liquid membrane (Matsumoto et al., 2007), teknik
ekstraksi reaktif dalam serat berlubang (hollow-fiber) (Yang and Cussler, 2000) dan teknik emulsion liquid
membrane (Breembroek et al., 2000; Lee, 2004). Dari
beberapa teknik pemisahan yang telah dipublikasikan, hanya teknik ekstraksi reaktif dalam hollow-fiber dan teknik membran cair emulsi (emulsion liquid
membrane) yang berpotensi untuk dikembangkan ke
skala industri. Namun demikian, pembuatan
hollow-fiber yang sesuai untuk pemisahan penisilin G
membutuhkan teknologi yang lebih tinggi dari pada pembuatan emulsi membran cair (Frank, 1997) sehingga penggunaan teknik ini kurang ekonomis.
Teknik membran cair emulsi merupakan teknik yang potensial dan efektif dalam proses pemisahan di mana secara simultan terjadi reaksi di permukaan membran, antara senyawa yang akan dipisahkan pada fasa umpan dengan senyawa pembawa pada fasa organik. Hasil reaksi akan terdifusi ke fasa membran yang pada akhirnya hasil ekstraksi terkumpul dan terkonsentrasi di fasa penerima (Mok et al., 1997). Ekstraksi berjalan sangat cepat karena tebal lapisan membran yang dilewati sangat tipis dan luas permukaan yang besar per unit volume (Hano et al., 1990). Teknik ini cocok untuk pemisahan bioproduk dari hasil fermentasi jamur, terutama untuk pemisahan penisilin yang kurang stabil (Pai et al., 2002). Disamping itu, pemakaian teknik ini dapat menghemat
waktu dan mempunyai keuntungan yang lain, yaitu pemakaian pelarut yang lebih sedikit jika dibandingkan dengan ekstraksi biasa. Diharapkan, pemakaian teknik membran cair ini akan memberikan hasil pemisahan yang lebih baik.
2. Metode
2.1 Alat
Konsentrasi penisilin G dan fenilasetat hasil ekstraksi diukur dengan menggunakan High Performance Chromatography (HPLC Waters 2487, USA) dengan detektor UV dengan komposisi eluen: 0,01M NH4H2PO4:metanol = 7:3; kecepatan alir 1
mL/menit; kolom C8; panjang gelombang 225 nm. Pengukuran pH dilakukan dengan menggunakan pH meter (Hanna®). Untuk pemecah emulsi digunakan rangkaian alat dengan frekuensi 250 Hz dan tegangan 76 volt AC. Pengaduk reaktor memiliki kecepatan 100 s/d 600 rpm, sedangkan pengaduk pembuat emulsi memiliki kecepatan 1.000 s/d 10.000 rpm.
2.2. Penentuan kondisi optimum ekstraksi penisilin G dengan teknik membran cair emulsi
2.2.1 Penentuan waktu kestabilan emulsi dengan variasi perbandingan volume fasa membran (Vm) terhadap volume fasa internal (Vi)
Sebanyak 10 mL fasa membran (mengandung 5% Span 80; 0,002 M dioktilamin; kerosen:
n-butilasetat = 1:1) ditambahkan dengan 10 mL fasa
internal (bufer fosfat pH = 8), diaduk dengan pengaduk dengan kecepatan 2.000 rpm selama 1 menit. Emulsi yang terbentuk dimasukkan ke dalam gelas ukur dan diukur penurunan emulsi setiap 0, 3, 10, 15, 17, 19, 21, 30, 34, 38, 42, 45 menit. Hal yang sama dilakukan dengan menggunakan volume fasa internal 20 mL, fasa membran 10 mL, serta fasa membran 20 mL, fasa internal 10 mL.
2.2.2 Pengaruh perbandingan volume fasa internal (Vi) volume fasa membran (Vm), terhadap persen ekstraksi penisilin G
Emulsi dibuat dengan perbandingan Vm:Vi = 1:1; 1:2 dan 2:1. Ekstraksi dilakukan dengan mendis-persikan fasa emulsi dengan waktu stabil yang telah diperoleh pada langkah 2.2.1 ke fasa eksternal yang mengandung penisilin G standar 372,5 ppm dan pH bufer sitrat = 5 dengan perbandingan volume fasa emulsi:volume fasa eksternal = 1:2. Pengadukan dilakukan selama 15 menit dengan kecepatan kontak 300 rpm. Konsentrasi penisilin G dalam fasa internal diukur dengan menggunakan HPLC. Untuk menghitung persen ekstraksi digunakan persamaan:
Pen G (terekstraksi)
%E x 100%
Pen G (mula-mula)
2.2.3 Pengaruh perbandingan volume fasa emulsi (W/O) dengan volume fasa eksternal terhadap persen ekstraksi penislin G
Kondisi optimum yang diperoleh dari langkah 2.3.1 dan 2.2.2 diterapkan pada langkah ini. Variasi perbandingan volume fasa emulsi (W/O) terhadap fasa eksternal (Vemulsi:Veksternal) adalah 1:1; 1:2; 1:3; 1:4.
Persen ekstraksi penisilin G yang diperoleh dialurkan terhadap perbandingan volume fasa emulsi terhadap volume fasa eksternal. Dari kurva yang diperoleh ditetapkan harga Vemulsi:Veksternal yang memberikan
harga persen ekstraksi penisilin G tertinggi digunakan untuk penentuan kondisi optimum berikutnya.
2.2.4 Pengaruh waktu pengadukan pembuatan emulsi terhadap persen esktraksi penisilin G
Kondisi optimum yang diperoleh dari langkah 2.2.1 sampai 2.2.3 diterapkan pada langkah ini. Variasi waktu pembuatan emulsi (W/O) yang dilakukan adalah: 1, 5, 10, dan 15 menit dengan kecepatan pengadukan 2.000 rpm. Persen ekstraksi penisilin G yang diperoleh dialurkan terhadap lama pengadukan pembuatan emulsi (W/O). Dari kurva didapat kondisi optimum lama pengadukan pembuatan emulsi (W/O). Kondisi ini digunakan untuk penentuan kondisi berikutnya.
2.2.5 Pengaruh kecepatan kontak antara fasa emulsi dengan fasa eksternal selama ekstraksi terhadap persen ekstraksi penisilin G
Kondisi optimum yang diperoleh dari langkah 2.2.1 sampai 2.2.4 diterapkan pada langkah ini. Variasi kecepatan kontak yang dilakukan adalah: 100, 200, 300, 400 dan 500 rpm. Persen ekstraksi penisilin G yang diperoleh dialurkan terhadap kecepatan kontak. Kondisi optimum yang didapat kemudian digunakan untuk penentuan kondisi terbaik berikutnya.
2.2.6 Pengaruh kecepatan pengadukan pembuatan emulsi terhadap persen esktraksi penisilin G
Kondisi optimum yang diperoleh dari langkah 2.2.1 sampai 2.2.5 diterapkan pada langkah ini. Variasi kecepatan pengadukan pembuatan emulsi adalah: 1.000, 2.000 dan 3.000 rpm. Persen ekstraksi penisilin G yang diperoleh pada percobaan ini dialurkan terhadap kecepatan pengadukan. Kondisi terbaik yang didapat kemudian digunakan untuk penentuan kondisi berikutnya.
2.2.7 Pengaruh konsentrasi larutan penisilin G pada fasa eksternal terhadap persen ekstraksi penisilin G
Variasi konsentrasi larutan penisilin G yang digunakan adalah 300, 325, 350, 375, 400, 425, dan 450 ppm. Ekstraksi dan pembuatan emulsi dilakukan dengan menggunakan kondisi terbaik yang diperoleh dari percobaan sebelumnya. Persen ekstraksi penisilin G yang diperoleh dialurkan terhadap konsentrasi penisilin G. Dari kurva didapat konsentrasi penisilin G yang memberikan persen ekstraksi tertinggi. Kondisi ini digunakan untuk penentuan kondisi berikutnya. 2.2.8 Pengaruh konsentrasi span 80 terhadap persen esktraksi penislin G
Pembuatan emulsi (W/O), ekstraksi dan kondisi optimum yang diperoleh dari langkah 2.2.1 sampai 2.2.7 digunakan pada langkah ini dengan berbagai variasi konsentrasi Span 80, yaitu: 3, 4, 5, 6, dan 7% (V/V). Persen ekstraksi yang diperoleh dialurkan terhadap konsentrasi surfaktan. Konsentrasi surfaktan yang memberikan persen ekstraksi tertinggi. adalah konsentrasi surfaktan optimum.
2.3. Pemisahan penisilin G dari fenilasetat dengan teknik membran cair emulsi
Kondisi optimum yang diperoleh dari 2.2.1 sampai 2.2.8 digunakan untuk memisahkan penisilin G dari fenilasetat. Penisilin G dan fenilasetat adalah dalam keadaan tercampur yang masing-masing mengandung 372,5 ppm dan 136,5 ppm dalam 20 mL fasa umpan bufer sitrat pH = 5. Waktu kontak antara fasa emulsi dan fasa eksternal divariasikan dalam waktu yaitu: 1, 5 , 10 , 15 dan 20 menit. Setelah fasa emulsi dipisahkan dari fasa eksternal, konsentrasi penisilin G dan fenilasetat yang terdapat dalam fasa internal diukur dengan HPLC.
3. Hasil dan Diskusi
3.1 Penentuan kondisi terbaik ekstraksi penisilin G dengan teknik membran cair emulsi
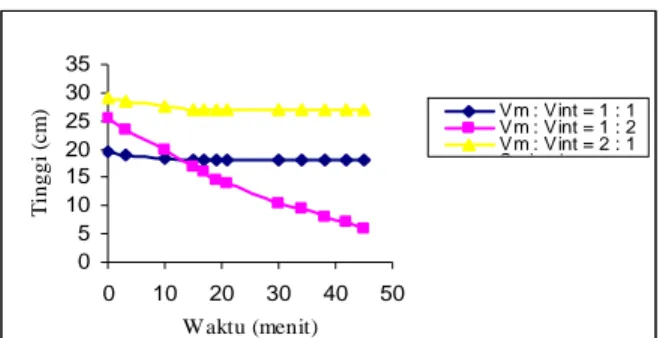
Kestabilan emulsi ditentukan melalui peng-ukuran berkurangnya tinggi emulsi terhadap lamanya waktu. Gambar 2 menunjukan bahwa komposisi fasa emulsi yang dipakai adalah komposisi Vm:Vint = 1:1. Walaupun komposisi Vm:Vint = 2:1 stabil namun konsentrasi surfaktan yang berlebih mungkin menyebabkan fasa membran menjadi rapat sehingga menghalangi transpor penisilin G. Kondisi terbaik bahwa pada komposisi Vm:Vint = 2:1 memberikan persen ekstraksi yang lebih rendah dibanding Vm:Vi = 1:1 (Tabel 1).
0 5 10 15 20 25 30 35 0 10 20 30 40 50 W aktu (menit) T inggi ( c m ) Vm : Vint = 1 : 1 Vm : Vint = 1 : 2 Vm : Vint = 2 : 1 S i 4
Gambar 2. Pengaruh kestabilan emulsi terhadap waktu. Vm = volume fasa membran, Vi = volume fasa internal.
Waktu tunggu 13 menit setelah pembuatan emulsi ditetapkan sebagai waktu stabil emulsi. Waktu tunggu tersebut digunakan untuk penentuan kondisi optimum berikutnya.
Tabel 1. Pengaruh perbandingan volume fasa internal (Vi) dengan volume fasa membran (Vm) terhadap persen ekstraksi penisilin G
Perbandingan Vm:Vi Persen ekstraksi penisilin G 1:2 82,16 1:1 94,92 2:1 26,59 Perbandingan volume fasa emulsi (W/O) dengan volume fasa eksternal yang memberikan persen ekstraksi tertinggi adalah 1:2 (Gambar 3). Pada kondisi ini emulsi terdispersi dengan baik di fasa eksternal. Seluruh butiran emulsi tersebar merata sehingga menjadikan permukaan membran luas. Jika permukaan membran luas, maka fluks akan meningkat (Lee et al., 1994). Meningkatnya fluks akan meningkatkan persen ekstraksi. Dengan perbandingan fasa eksternal yang lebih kecil, emulsi kurang terdispersi, dan permukaan fasa eksternal tertutup oleh emulsi sehingga luas permukaan berkurang dan persen ekstraksi penisilin G menurun. Perbandingan yang lebih tinggi, yaitu perbandingan di atas kondisi optimum, volume fasa eksternal menyebabkan daerah penembusan semakin berkurang sehingga menurunkan persen ekstraksi.
Persen ekstraksi penisilin G maksimum didapat pada waktu pengadukan pembuatan emulsi 1 menit (Gambar 4). Bila waktu pengadukan pembuatan emulsi dilakukan lebih dari 1 menit, maka emulsi membentuk krim sehingga tidak dapat digunakan untuk ekstraksi. 74 76 78 80 82 84 86 0 1 2 3 4 5
Perbandingan Volume ( Notas i 1 = 1 :1 ; notas i 2 = 1 : 2 ; notas i 3 = 1 : 3 ; notas i 4 = 1 : 4 ) P e rs e n E k st ra ks i P e nis ili n G ( % )
Gambar 3. Pengaruh perbandingan volume fasa emulsi (W/O) dengan volume fasa eksternal terhadap persen ekstraksi penisilin G. 0 10 20 30 40 50 60 70 80 90 0 5 10 15 20 Waktu (menit) P e rs en E k st ra ks i P e ni si li n G
Gambar 4. Pengaruh waktu pengadukan pembuatan emulsi terhadap persen ekstraksi penisilin G.
Persen ekstraksi penisilin G maksimum dicapai pada kecepatan kontak 300 rpm (Gambar 5). Apabila kecepatan kontak di bawah 300 rpm, terlihat persen ekstraksi menurun. Hal ini mungkin disebabkan ukuran butir-butir emulsi belum seragam dengan besar ukuran idealnya, akibatnya luas permukaan butiran emulsi menjadi kecil sehingga mengurangi difusi penisilin G ke dalam fasa membran (Lee et al., 1997). Jika kecepatan kontak di atas 300 rpm persen ekstraksi juga menurun. Hal ini dikarenakan sebagian butiran-butiran emulsi yang telah terisi dengan penisilin G mengalami pemecahan, akibatnya penisilin G yang telah terperangkap di dalam butiran emulsi keluar kembali ke fasa eksternal.
0 20 40 60 80 100 0 100 200 300 400 500 600 Kecepatan (rpm) P e rs en E k st ra ks i P e ni si li n G ( % )
Gambar 5. Pengaruh kecepatan kontak antara fasa emulsi dengan fasa eksternal terhadap persen ekstraksi penisilin G.
Kecepatan pengadukan pembuatan emulsi yang memberikan persen ekstraksi tertinggi adalah kecepatan 2.000 rpm (Tabel 2). Persen ekstraksi mengalami penurunan pada kecepatan pengadukan di bawah 2.000 rpm. Pengaruh ini disebabkan oleh jumlah butiran emulsi yang terbentuk belum maksimal sehingga menurunkan daya ekstraksi. Kecepatan pengadukan pembuatan emulsi di atas 2.000 rpm juga menyebabkan persen ekstraksi menurun karena emulsi mungkin pecah karena bergabung membentuk krem.
Tabel 2. Pengaruh kecepatan pengadukan pembuatan emulsi terhadap persen ekstraksi penisilin G
Kecepatan pengadukan (rpm) Persen ekstraksi penisilin G
1.000 60,42
2.000 94,19
3.000 79,63
Lama pendiaman emulsi memberikan persen ekstraksi maksimum pada waktu 3 menit (Gambar 6). Di bawah waktu 3 menit terlihat persen ekstraksi menurun. Hal ini mungkin karena ukuran butiran emulsi yang terbentuk belum ideal dan masih bertumpuk sehingga luas permukaan menjadi kecil dan akibatnya daya ekstraksi menjadi berkurang. Lama pendiaman di atas 3 menit dapat menyebabkan berkurangnya jumlah emulsi yang telah terbentuk karena butiran tersebut bergabung membentuk butiran emulsi yang lebih besar dan mengakibatkan luas permukaan menjadi kecil.
0 10 20 30 40 50 60 70 80 90 0 1 2 3 4 5 6 7 8 9 10
Lama Pen diaman Emu ls i (men it)
P e rs e n E k st ra k si P e n is ilin G ( % )
Gambar 6. Pengaruh waktu pendiaman emulsi terhadap persen ekstraksi penisilin G.
Kapasitas daya tampung fasa internal terhadap penisilin G adalah 375 ppm (Gambar 7). Pada konsentrasi fasa eksternal lebih besar dari 375 ppm persen ekstraksi terlihat menurun. Ini disebabkan oleh kapasitas daya tampung fasa internal yang terbatas. Keterbatasan daya tampung ini terjadi karena adanya kesetimbangan antara penisilin G dalam fasa internal dengan penisilin G dalam fasa eksternal. Apabila konsentrasi penisilin G dalam fasa eksternal diperbesar,
maka proses difusi akan terhenti, akibatnya persen ekstraksi menurun. 0 10 20 30 40 50 60 70 80 90 100 300 325 350 375 400 425 450
Kons entrasi Penis ilin G (ppm)
Pe rs e n E k st ra k si Pe n is il in ( G )
Gambar 7. Pengaruh konsentrasi larutan penisilin G pada fasa eksternal terhadap persen ekstraksi penisilin G.
Dari Gambar 8 terlihat bahwa persen ekstraksi penisilin G maksimum didapat pada konsentrasi Span 80 sebesar 5%. Konsentrasi Span 80 di atas 5% menyebabkan persen ekstraksi menurun. Hal ini terjadi karena pori membran menjadi lebih rapat, sehingga difusi penisilin G menjadi lebih lambat. Pada konsentrasi di bawah 5% persen ekstraksi juga me-nurun. Konsentrasi Span 80 yang rendah mengakibatkan emulsi menjadi kurang stabil, emulsi mudah pecah, dan dengan demikian penisilin G yang sudah berada di fasa internal akan kembali ke fasa eksternal. 62 64 66 68 70 72 74 76 0 1 2 3 4 5 6 7 8
Kons entras i Span 80 (%v/v)
Pe rs e n E k st ra k si Pe n is il in G ( % )
Gambar 8. Pengaruh konsentrasi span 80 terhadap persen ekstraksi penisilin G.
3.2. Pemisahan penisilin G dari fenilasetat dengan teknik membran cair emulsi.
Kemampuan suatu komponen untuk dapat tertranspor ke dalam fasa internal melalui membran cair emulsi dipengaruhi salah satunya oleh luas butiran emulsi. Oleh karena itu, faktor daya pisah pada ekstraksi secara membran cair emulsi dapat ditentukan melalui perbandingan permeabilitas masing-masing. Komponen permeabilitas adalah kemampuan suatu komponen untuk menembus fasa butiran emulsi pada luas tertentu per satuan waktu. Ungkapan permeabilitas yang digunakan adalah:
ln(C/C0) = -A/V . P.t (2)
dimana:
C = Konsentrasi setelah ekstraksi C0 = Konsentrasi mula-mula
A = Luas butiran emulsi V = Volume fasa umpan
Penentuan luas butiran emulsi dilakukan melalui pengukuran diameter butiran emulsi dengan pembesaran 100 kali (Gambar 9). Diameter butiran emulsi ± 0,1 mm sehingga butiran emulsi memiliki luas 7,85 x 10-3 mm2.
Butiran emulsi Tetesan
1mm 2 mm
Gambar 10. Waktu kontak terhadap persen ekstraksi penisilin G dan fenilasetat.
Hal yang sama juga dapat dijelaskan untuk permeabilitas penisilin G dan fenilasetat. Permeabilitas penisilin G dan fenilsetat juga menurun dan stabil pada waktu kontak 10 menit (Gambar 11). Namun demikian, permeabilitas penisilin G lebih tinggi dibanding permeabilitas fenilasetat.
Dengan memasukkan parameter luas butiran ke persamaan (2), hasil perhitungan permeabilitas dan daya pisah untuk penisilin G dan fenilasetat diperoleh dan ditunjukkan pada Tabel 3.
Gambar 9. Penentuan diameter butiran emulsi.
Tabel 3. Perhitungan Faktor Daya Pisah Penisilin G-Fenilasetat dengan Cara Perbandingan Permeabilitas pada Ekstraksi Membran Cair Emulsi
Waktu Kontak (menit)
Ppen G PFenas Daya Pisah
1 82 39 2,1 5 3,6 1,33 2,7 10 0,45 0,032 14,06 15 0,31 0,016 19,38 20 0,21 0,01 21 TR = Waktu Retensi; C = Konsentrasi; P = Permeabilitas
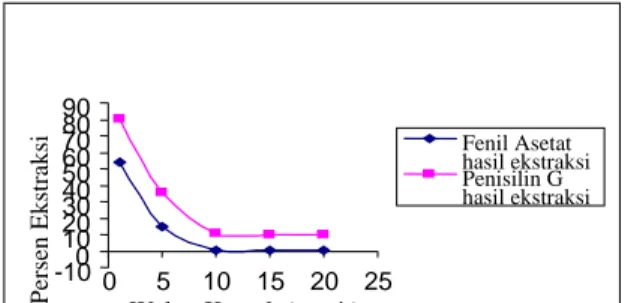
Persen ekstraksi baik penisilin G maupun fenilasetat sama-sama menurun dan penurunan terhenti pada waktu kontak 10 menit (Gambar 10). Salah satu penyebab turunnya persen ekstraksi kedua komponen tersebut adalah karena terdapatnya emulsi yang tidak stabil. Emulsi pecah ketika diaduk dengan kecepatan dan lamanya waktu pada saat kontak yang sama dengan fasa umpan. Dengan demikian, penisilin G dan fenilasetat yang sudah tertranspor di fasa internal kembali keluar ke fasa umpan. Persen ekstraksi yang terukur pada Gambar 10 adalah persen ekstraksi hasil deemulsifikasi dari emulsi yang stabil. Walaupun persen ekstraksi penisilin G dan fenilasetat cenderung menurun, tetapi persen ekstraksi penisilin G memberikan kandungan yang lebih tinggi dibanding persen ekstraksi fenilasetat.
-1 0 1 2 3 4 0 5 10 15 20 25
Waktu Kontak (menit)
P e rm eab il it as penisilin G Fenilaset at
Gambar 11. Waktu kontak terhadap permea-bilitas penisilin G dan fenilasetat.
-100 10 20 30 40 50 60 70 80 90 0 5 10 15 20 25
Waktu Kontak (menit)
Persen Ekstraksi
Fenil Asetat hasil ekstraksi Penisilin G hasil ekstraksi
Persen ekstraksi penisilin G yang lebih tinggi dari persen ekstraksi fenil asetat ini menunjukkan kemampuan penembusan penisilin G melalui butiran emulsi lebih besar dibanding fenilasetat. Jika permeabilitas penisilin G dibandingkan dengan permeabilitas fenilasetat, maka akan didapat faktor daya pisah (Gambar 12).
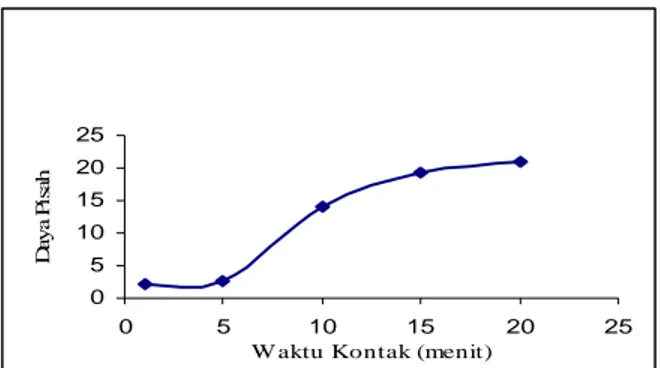
Faktor daya pisah penisilin G-fenilasetat cenderung meningkat pada waktu kontak 5 sampai 15 menit dan mendatar pada waktu kontak yang lebih lama. 0 5 10 15 20 25 0 5 10 15 20 25
W aktu Kontak (menit)
Da y a P is a h
Gambar 12. Waktu kontak terhadap faktor daya pisah penisilin G-fenilasetat.
4. Kesimpulan
Penerapan kondisi optimum pada ekstraksi pemisahan penisilin G dari fenilasetat dihasilkan faktor daya pisah 19,38. Pada kondisi ini fasa penerima (internal) lebih banyak mengandung penisilin G dibanding fenilasetat. Nilai yang diperoleh ini jauh lebih besar jika dibandingkan dengan teknik membran cair berpendukung yang dilakukan oleh peneliti lain (Lee et al. 1994) yaitu 1,8. Dengan demikian cara ekstraksi membran cair emulsi adalah cara yang cukup efektif untuk memisahkan penisilin G dari fenilasetat.
Ucapan Terimakasih
Ucapan terimakasih ditujukan kepada Direktorat Jenderal DIKTI melalui Jurusan Kimia FMIPA Universitas Negeri Jakarta yang telah mendanai penelitian ini melalui Beasiswa DUE-LIKE.
Daftar Pustaka
Adikane, H. V., R. K. Singh, and S. N. Nene, 1999, Recovery of Penicillin G from Fermentation Broth by Microfiltration, J. Membrane Sci.,
162:1-2, 119-123.
Breembroek, G. R. M., G. J. Witkamp, and G. M. Van Rosmalen, 2000, Design and Testing of an Emulsion Liquid Membrane Pilot Plant, Sep.
Sci. Technol., 35:10, 1539-1571.
Chen., S. S. W and T. C. Huang, 1995, Separation of Phenylacetic Acid, 6-Aminopenicillanic Acid and Penicillin G with Electrodialysis under
Constant Current, J. Chem. Tech. Biotechnol.,
64, 284-292.
Frank A. F., 1997, Scale-up Hollow Fiber Extractors,
Sep. Sci. Technol., 32, 573-583.
Hano, T. O., M. Matsumoto, S. Ogawa and F. Hori, 1990, Extraction of Penicillin with Liquid Surfactant Membrane, J. Chem. Eng. Japan.,
23:6, 772-775.
Lee, S. C., 2004, Comparison of Extraction Efficiencies of Penicillin G at Different W/O Ratios in the Emulsion Liquid Membrane Systems with Dilute Polymer Solutions, J. Membrane. Sci.,
237, 225-232.
Lee, S. C., K. H. Lee, G. H. Hyun and W. K. Lee, 1997, Continuous Extraction of Penicillin G by an Emulsion Liquid Membrane in a Countercurrent Extraction Column, J.
Membrane.Sci., 124, 43-51.
Lee, C. J., H. J. Yeh, W. Y Yang, and C. R. Kan, 1994, Separation of Penicillin G from Phenylacetic Acid in a Supported Liquid Membrane System, Biotechnol. Bioeng., 43, 309-313. Likidis, Z. and K. Schugerl, 1987, Reactive Extraction
and Reextraction of Penicillin with Different Carriers, J. Biotechnol., 5, 293-303.
Luuk A. M., M. van der Wielen, M. J. A. Lankveld, and K. C. A. M. Luyben, 1996, Anion Exchange Equilibria of Penicillin G, Phenylacetic Acid, and 6-Aminopenicillanic Acid versus Cl- on IRA400 Ion Exchange Resin, J. Chem. Eng. Data., 41 ,239-243. Matsumoto, M., T. Ohtani, and K. Kondo, 2007,
Comparison of Solvent Extraction and Supported Liquid Membrane Permeation using an Ionic Liquid for Concentrating Penicillin G, J. Membrane Sci., 289, 92-96. Mok, Y. S., W. K. Lee, and Y. K. Lee, 1997, Modeling
of Liquid Emulsion Membranes Facilitated by Two Carriers, Chem. Eng. J., 66, 11-20. Pai, R. A., M. F. Molone, and M. F. Doherty, 2002,
Design of Reactive Extraction Systems for Bioproduct Recovery, AIChe. J., 48:3, 514-526.
Rajendhran, J. and P. Gunasekaran, 2004, Recent Biotechnological Interventions for Developing Improve Penicillin G Acylase (Review), J.
Biosci. Bioeng., 97:1, 1-13.
Reschke, M. and K. Schugerl, 1984, Stability of Penicillin G in the Presence of Carriers and Relationships for Distribution Coefficients and Degrees of Extraction, Chem. Eng. J., 28, B1-B9.
Wang, Z., Y. Guo, D. Bao, and H. Qi, 2006, Direct Extraction of Phenylacetic Acid from Immobilised Enzymatic Hydrolysis of
Penicillin G with Cloud Point Extraction, J
Chem Technol Biotechnol, 81:560-565. Yang, C. and E. L. Cussler, 2000, Reactive Extraction
of Penicillin G in Hollow-Fiber and Hollow- Fiber Fabric Modules, Biotechnol. Bioeng.,