PETUNJUK PRAKTIKUM
KIMIA ORGANIK
DISUSUN OLEH:
TIM PRAKTIKUM KIMIA ORGANIK
PROGRAM STUDI S1 FARMASI
STIKES AL-IRSYAD AL-ISLAMMIYAH
CILACAP
2016
PETUNJUK PRAKTIKUM
KIMIA ORGANIK
DISUSUN OLEH:
TIM PRAKTIKUM KIMIA ORGANIK
PROGRAM STUDI S1 FARMASI
STIKES AL-IRSYAD AL-ISLAMMIYAH
CILACAP
2016
PETUNJUK PRAKTIKUM
KIMIA ORGANIK
DISUSUN OLEH:
TIM PRAKTIKUM KIMIA ORGANIK
PROGRAM STUDI S1 FARMASI
STIKES AL-IRSYAD AL-ISLAMMIYAH
CILACAP
DAFTAR ISI
HALAMAN JUDUL ... i
DAFTAR ISI... ii
KATA PENGANTAR.. ... iii
Percobaan I : Identifikasi Unsur dan Gugus Senyawa Organik ... 1
Percobaan II : Sintesis Metil Salisilat... 6
Percobaan III : Sintesis Asam Format... 10
Percobaan IV : Sintesis Aspirin ... 12
Percobaan V : Sintesis Yodoform ... 14
Percobaan VI : Sintesis Para-Nitroasetanilid... 16
KATA PENGANTAR
Alhamdulillahhirabbilamin, segala puji bagi Allah SWT atas ridho dan rahmad-Nya, sehingga Buku Petunjuk Praktikum Kimia Organik ini dapat disusun.
Buku petunjuk ini merupakan edisi pertama, yaitu memuat pokok materi yang akan dipratikumkan. Dengan demikian mahasiswa diharapkan akan memiliki pemahaman yang lebih mendalam terhadap materi praktikum. Buku Petunjuk Praktikum Kimia Organik ini memuat reaksi-reaksi dasar dalam kimia organik meliputi subsitutusi elektrofilik pada senyawa aromatik, reaksi terhadap asam karboksilat, esterifikasi, asetilasi, dan halogenasi pada senyawa karbonil. Selain memuat reaksi dasar diharapkan mahasiswa sekaligus memahami teknik dasar sintesa organik.
Kami menyadari sepenuhnya bahwa buku petunjuk ini masih jauh dari kesempurnaan, terutama dari segi isi dan tata letak, kritik dan saran terhadap edisi berikutnya sangat kami harapkan.
PERCOBAAN 1
IDENTIFIKASI UNSUR DAN GUGUS SENYAWA ORGANIK
A. TUJUAN PERCOBAAN
Melakukan identifikasi terhadap unsur-unsur senyawa organik (C, H, O, N, S, P, dan halogenida), gugus (Alkohol, Amina, inti benzena, Aldehid, Keton, fenol, asam karboksilat, dan ester)
B. IDENTIFIKASI UNSUR Bahan Percobaan
Campuran serbuk Castellana, senyawa yang mengandung unsur C, N, S, P, dan halogenida, reagen identifikasi.
Alat Percobaan
Pipa kapiler, tabung reaksi, spiritus, pipet tetes, drupple plate, flakon. Cara Percobaan
1. Unsur C
a. Sampel senyawa (yang mengandung unsur C) diletakkan dalam cawan porselin, dipanaskan diatas lampu spiritus nyala kecil, terbentuk warna hitam, menunjukkan adanya unsur C.
b. Dalam tabung reaksi masukkan sampel senyawa (yang mengandung unsur C), tambahkan Pb Kromat, pijarkan diatas lampu spiritus. Pada mulut tabung reaksi diletakkan pipet tetes yang berisi Ba(OH)2,
apabila cairan dalam pipet tetes menjadi keruh/endapan putih, maka ada unsur C.
2. Unsur N
a. Campurkan lebih kurang 1 bagian serbuk sampel (senyawa yang mengandung unsur N) dengan 2 bagian campuran serbuk Castellana, campur diatas kertas.
c. Saring filtratnya, masukkan dalam tabung reaksi.
d. Tambahkan beberapa tetes larutan Ferro Sulfat jenuh (akan terbentuk endapan warna hijau tua).
e. Campuran dipanaskan hingga mendidih, setelah dingin tambahkan dengan HCl 4 N dan beberapa tetes larutan FeCl4. Warna biru atau
hijau (prusian blue) yang terbentk menunjukkan adanya unsur N. 3. Unsur S
a. Campuran lebih kurang 1 bagian serbuk sampel (senyawa yang mengandung unsur S) dengan 2 bagian campuran serbuk Castellana, campur di atas kertas.
b. Masukkan campuran dalam pipa kapiler, panaskan diatas spiritus hingga membara, segera masukkan dalam flakon yang berisi aquadest, gerus dengan batang pengaduk.
c. Saring filtrat, masukkan dalam tabung reaksi.
d. Filtrat diteteskan dalam drupple plate, tambahkan larutan Natrium Nitroprusida jenuh, akan terbentuk warna merah violet.
e. Filtrat diasamkan dengan asam asetat akan terbentuk endapan hitam coklat dari Pbs.
4. Unsur P
a. Campurkan lebih kurang 1 bagian serbuk sampel (senyawa yang mengandung P) dengan 2 bagian campuran serbuk Castellana, campur diatas kertas.
b. Masukkan campuran dalam pipa kapiler, panaskan diatas spiritus hingga membara, segera masukkan dalam flakon yang berisi aquadest, gerus dengan batang pengaduk.
c. Saring filtratnya, masukkan dalam tabung reaksi.
5. Unsur Halogenida (Cl, Br, I) a. Unsur Cl (Klorida)
1) Campurkan lebih kurang 1 bagian serbuk sampel (senyawa yang mengandung usur Cl) dengan 2 bagian campuran serbuk Castellanna, campur diatas kertas.
2) Masukkan campuran dalam pipa kapiler, panaskan diatas spiritus hingga membara, segera masukkan dalam flakon yang berisi aquadest, gerus dengan batang pengaduk.
3) Saring filtratnya, masukkan dalam tabing reaksi.
4) Filtrat ditambahkan asam sulfat pekat beberapa tetes, kemudian dihangatkan. Batang pengaduk yang telah dibasahi dengan larutan amonia diletakkan diatas mulut tabung, akan terbentuk kabut putih.
5) Filtrat diasamkan dengan asam nitrat, kemudian ditambahkan larutan AgNO3, akan terjadi endapan putih. Endapan ini larut
dalam amonia encer, KCN dan Natrium tiosulfat. b. Unsur Br (Bromida)
1) Campurkan lebih kurang 1 bagian serbuk sampel (senyawa yang mengandung unsur Br) dengan 2 bagian campuran serbuk Castellanna, campur diatas kertas.
2) Masukkan campuran dalam pipa kapiler, panaskan diatas spiritus hingga membara, segera masukkan dalam flakon yang berisi aquadest, gerus dengan batang pengaduk.
3) Saring filtratnya, masukkan dalam tabung reaksi.
4) Filtrat diasamkan dengan asam nitrit, kemudian ditambahkan larutan AgNO3, akan terjadi endapan kuning pucat. Endapan ini
c. Unsur I (Iodida)
1) Campurkan lebih kurang 1 bagian serbuk sampel (senyawa yang mengandung unsur I) dengan 2 bagian campuran serbuk Castellanna, campur diatas kertas.
2) Masukkan campuran dalam pipa kapiler, panaskan diatas spiritus hingga membara, segera masukkan dalam flakon yang berisi aquadest, gerus dengan batang pengaduk.
3) Saring filtratnya, masukkan dalam tabung reaksi.
4) Filtrat diasamkan dengan asam nitrit, kemudian ditambahkan larutan AgNO3, akan terjadi endapan kuning pucat. Endapan ini
sukar larut dalam amonia encer, larut dalam amonia pekat, KCN, Natrium tiosulfat.
5) Filtrat ditambahkan K2SO4 pekat dan K2Cr2O7, letakkan segera
kertas amilum menutupi mulut tabung, akan terbentuk iod bebas yang bereaksi dengan kertas amilum menjadi berwarna biru. C. IDENTIFIKASI GUGUS
1. Gugus Alkohol
a. Alkohol primer (Etanol)
1) Sampel ditambah dengan KMnO4dan asam sulfat pekat, warna
ungu hilang.
2) Sampel ditambah dengan KMnO4dan asam sulfat pekat,
ditambahkan reagen Schiff, akan berwarna merah. b. Alkohol sekunder (Isopropanol)
Sampel ditambah aqua bromata, Natrium nitroprusida, ammonium klorida, amonia akan membentuk warna merah coklat/ungu.
2. Gugus Aldehid (benzaldehid dan glukosa)
a. Sampel dalam tabung reaksi ditambah 1 ml reagen Benedict, dipanaskan hingga terbentuk endapan merah bata.
3. Gugus Keton (Asetofenon dan fruktosa)
Sampel dalam tabung reaksi ditambah 5 tetes larutan Natrium nitroprusida, ammonium klorida dan amonia akan berwarna biru violet (ungu).
4. Gugus Amina (glisin dan parasetamol terhidrolisis)
a. Sampel dalam tabung reaksi ditambah beberapa tetes larutan Dimetilbenzaldehida HCl (DAB HCl) akan berwarna merah jingga (amina aromatik).
b. Sampel dalam tabung reaksi, ditambah beberapa tetes aseton dan Natrium nitroprusida, diamkan 5-7 menit akan berwarna merah pears (amina alifatik primer)
5. Gugus inti Benzena (benzena)
Sampel ditambah asam nitrat pekat, dinginkan, ditambah etanol, serbuk Zn dan asam klorida pekat, dinginkan, tambahkan larutan NaNO2 dan β-Naftol dalam amonia akan terbentuk cincin warna
merah.
6. Gugus Fenol (fenol)
Sampel ditambah 1 tetes larutan FeCl3 akan berwarna ungu tua, bila
ditambah etanol akan menjadi kuning. 7. Gugus asam karboksilat (asam benzoat)
Sampel ditambah etanol, ditambah asam sulfat pekat, bila perlu dengan pemanasan, akan berbau ester asetat (harum).
8. Gugus ester atau turunan asam karboksilat.
a. Sampel etil asetat ditambah larutan AgNO3, akan terbentuk
endapan perak asetat.
b. Sampel asam oksalat ditambah larutan AgNO3, akan terbentuk
PERCOBAAN 2
SINTESIS METIL SALISILAT
A. TUJUAN PERCOBAAN
Mempelajari reaksi esterifikasi dari gugus karboksil asam salisilat dengan gugus hidroksil dari methanol dalam suasana asam.
B. DASAR TEORI
Metil salisilat diperoleh dari sintesis atau maserasi dan dilanjutkan dengan destilasi uao daun Gaultheria procumbens Linne (Familia: Ericaceae) atau kulit batang betula lente Linne. Metil salisilat berupa cairan, tidak berwarna, kekuningan atau kemerahan, berbau khas dan rasa seperti gandapura. Mendidih antara 219oC dan 224oC disertai peruraian. Senyawa ini sukar larut dalam air, larut dalam etanol, dan larut dalam asam asetat glasial.
Metil salisilat digunakan sebagai analgetik untuk mengurangi rasa sakit dan sebagai antipiretik untuk mengurangi demam. Penggunaan obat ini untuk pemakaian topikal mempunyai potensi analgetik sama dengan turunan salisilat-salisilat lainnya. Metil salisilat diresorbsi baik oleh kulit dan banyak digunakan dalam obat gosok dan krim (3-10%) untuk nyeri otot, sendi, dan lain-lain.
Suatu ester asam karboksilat adalah suatu senyawa yang mengandung gugus –CO2R dengan R dapat berbentuk alkil ataupun aril. Suatu ester dapat
dibentuk dengan reaksi langsung antara asam karboksilat dan suatu alkohol. Reaksi esterifikasi berkatalis asam dan merupakan reaksi yang reversibel. Oleh karena itu, untuk menghasilkan rendemen yang besar, kesetimbangan harus digeser ke kiri (ke arah produk) dengan cara memperbesar jumlah salah satu reagen yang murah dari campuran reaksi tersebut.
Laju esterifikasi suatu asam karboksilat tergantung terutama pada hubungan sterik dari alkohol dan asam karboksilatnya. Reaksi alkohol terhadap esterifikasi sebagai berikut: ROH tersier < ROH sekunder < ROH primer < CH3OH. Kuat asam karboksilat hanya memainkan peranan kecil
dalan laju pembentukan ester. R3CCO2H < R2CHCO2H < RCH2CO2H <
CH3CO2H < HCO2H. Seperti reaksi aldehid dan keton, esterifikasi suatu asam
karboksilat berlangsung melalui serangkaian tahapan reaksi protonasi dan deprotonasi. Oksigen dan karbonil diprotonasi, alkohol nukleofilik menyerang karbon positif dan eliminasi air menghasilkan ester.
C. ALAT DAN BAHAN 1. Alat Percobaan
Asam salisilat, metanol absolute, asam sulfat pekat, natrium bikarbonat, magnesium, sulfat anhidrat.
2. Bahan Percobaan
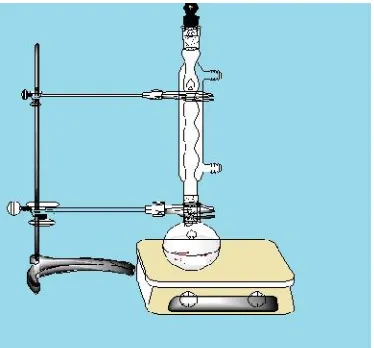
Gambar 1. Rangkaian alat refluks
D. CARA KERJA 1. Sintesis
Ke dalam labu alas bulat (LAB) 500 ml dimasukkan 14 gram asam salisilat dan ditambahkan 40,5 ml metanol absolut dan 4 ml asam sulfat pekat, dan dimasukkan 2-3 buah batu didih. LAB kemudian dihubungkan dengan pendingin tegak, direfluks selama 1,5 jam, suhu reaksi 700C-800C. 2. Isolasi
Kelebihan metanol didestilasi dengan suhu 800C (proses ini dinyatakan optimal, jika tidak ada lagi tetesan destilat (metanol dari pipa alonga), Kemudian residu (metil salisilat) yang diperoleh dituang ke corong pisah, ambil lapisan metil salisilat. Lapisan metil salisilat yang diperoleh ditambahkan larutan natrium bikarbonat, digojok-gojok, dipisahkan (diulang beberapa kali sampai netral, tidak terbentuk gelembung CO2). Cairan metil salisilat telah netral, dihitung volumenya
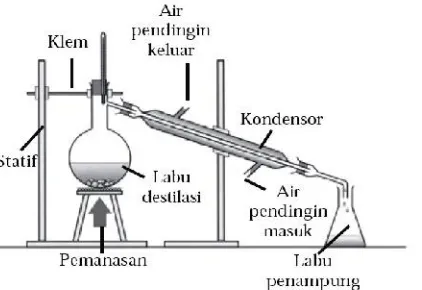
Gambar 2. Alat destilasi Gambar 3. Corong pisah 3. Pemurnian
Hasil isolasi didestilasi kembali dengan suhu 2240C, kemudian destilat ditampung dalam wadah yang kering dan bersih. Hasil sintesis disimpan dalam wadah gelap, tertutup rapat dan terlindung cahaya matahari.
4. Identifikasi hasil sintesis
PERCOBAAN 3
SINTESIS ASAM FORMAT/ASAM SEMUT
A. TUJUAN PERCOBAAN
Mengenal reaksi terhadap asam-asam karboksilat B. DASAR TEORI
Oksidasi alkohol primer biasanya menghasilkan aldehida yang dapat dioksidasi lebih lanjut menjadi asam karboksilat. Oksidator yang biasanya digunakan untuk tujuan ini adalah kalium permanganat dalam larutan netral, asam atau basa atau asam kromat.
Asam semut (secara sistematis disebut asam formay atau asam metanoat) merupakan asam karboksilat yang paling sederhana dengan rumus HCOOH atau CH2O2. Senyawa ini merupaka senyawa intermediate yang penting
dalam sintesis kimia dan terjadi secara alami. Asam format paling banyak ditemukan dalam sengat lebah dan semut.
Gambar 4. Struktur Kimia Asam Format
Sejumlah signifikan asam format dihasilkan sebagai produk samping dari pembuatan bahan kimia lain, khususnya asam asetat. Dalam percobaan ini, asam format dapat diperoleh dengan memanaskan asam oksalat dengan gliserol anhidrat dan diekstraksi dengan destilasi uap.
C. ALAT DAN BAHAN 1. Alat percobaan
Labu destilasi, pendingin liebig, erlenmeyer, lampu spiritus, termometer, statif & klem, kaki tiga & kawat kasa.
PERCOBAAN 3
SINTESIS ASAM FORMAT/ASAM SEMUT
A. TUJUAN PERCOBAAN
Mengenal reaksi terhadap asam-asam karboksilat B. DASAR TEORI
Oksidasi alkohol primer biasanya menghasilkan aldehida yang dapat dioksidasi lebih lanjut menjadi asam karboksilat. Oksidator yang biasanya digunakan untuk tujuan ini adalah kalium permanganat dalam larutan netral, asam atau basa atau asam kromat.
Asam semut (secara sistematis disebut asam formay atau asam metanoat) merupakan asam karboksilat yang paling sederhana dengan rumus HCOOH atau CH2O2. Senyawa ini merupaka senyawa intermediate yang penting
dalam sintesis kimia dan terjadi secara alami. Asam format paling banyak ditemukan dalam sengat lebah dan semut.
Gambar 4. Struktur Kimia Asam Format
Sejumlah signifikan asam format dihasilkan sebagai produk samping dari pembuatan bahan kimia lain, khususnya asam asetat. Dalam percobaan ini, asam format dapat diperoleh dengan memanaskan asam oksalat dengan gliserol anhidrat dan diekstraksi dengan destilasi uap.
C. ALAT DAN BAHAN 1. Alat percobaan
Labu destilasi, pendingin liebig, erlenmeyer, lampu spiritus, termometer, statif & klem, kaki tiga & kawat kasa.
PERCOBAAN 3
SINTESIS ASAM FORMAT/ASAM SEMUT
A. TUJUAN PERCOBAAN
Mengenal reaksi terhadap asam-asam karboksilat B. DASAR TEORI
Oksidasi alkohol primer biasanya menghasilkan aldehida yang dapat dioksidasi lebih lanjut menjadi asam karboksilat. Oksidator yang biasanya digunakan untuk tujuan ini adalah kalium permanganat dalam larutan netral, asam atau basa atau asam kromat.
Asam semut (secara sistematis disebut asam formay atau asam metanoat) merupakan asam karboksilat yang paling sederhana dengan rumus HCOOH atau CH2O2. Senyawa ini merupaka senyawa intermediate yang penting
dalam sintesis kimia dan terjadi secara alami. Asam format paling banyak ditemukan dalam sengat lebah dan semut.
Gambar 4. Struktur Kimia Asam Format
Sejumlah signifikan asam format dihasilkan sebagai produk samping dari pembuatan bahan kimia lain, khususnya asam asetat. Dalam percobaan ini, asam format dapat diperoleh dengan memanaskan asam oksalat dengan gliserol anhidrat dan diekstraksi dengan destilasi uap.
C. ALAT DAN BAHAN 1. Alat percobaan
2. Bahan percobaan
Gliserol, asam oksalat (berair kristal), pereaksi kalium permanganat, serbuk magnesium.
D. CARA KERJA
1. Di dalam labu destilasi yang telah dihubungkan dengan pendingin, panaskan campuran dari 2,5 g (BJ : 1,25 g/ml) Gliserol dan 2,5 g kristal asam oksalat yang mengandung air kristal, maka akan terjadi pengeluaran gas. Amati reaksi yang terjadi.
2. Tambahkan ke dalam labu 1,25 g asam oksalat lagi dan teruskan pemanasan. Tampunglah destilat yang terjadi dengan labu erlenmeyer. E. REAKSI TERHADAP FORMIAT
Terhadap destikat tersebut lakukan percobaan-percobaan di bawah ini: 1. Oksidasi asam semut dengan kalium permanganat
Ke dalam tabung reaksi yang berisi 2 ml larutan destilat, teteskan sedikit larutan kalium permanganat. Biarkan untuk beberapa lama dan amati reaksi yang terjadi.
2. Reduksi dengan serbuk magnesium
PERCOBAAN 4
SINTESIS ASPIRIN (ASAM ASETIL SALISILAT)
A. TUJUAN PERCOBAAN
Untuk memberikan pengenalan tentang reaksi asetilasi terhadap gugus fenol.
B. DASAR TEORI
Asam asetil salisilat yang biasa disebut aspirin, dapat digunakan sebagai obat analgesik, antipiretik, dan asnti rematik. Senyawa ini dapat disintesis di laboratorium dari asam salisilat dan asetat anhidrida yang melibatkan reaksi asetilasi gugus fenolik asam salisilat dan dikatalisis oleh asam. Reaksinya sebagai berikut:
Asetat anhidride asam salisilat Aspirin Asam asetat
Produk dipurifikasi dengan cara rekristalisasi menggunakan pelarut alkohol 96%. Kemurnian produk ditentukan dengan mudah menggunakan “spot test” untuk asam salisilat yang tidak bereaksi. Karena asam salisilat memiliki gugus fenolik, maka keberadaan asam ini menghasilkan uji yang sangat positif karena bereaksi dengan larutan besi (III) klorida (FeCl3) encer
menghasilkan larutan berwarna ungu yang kuat. Sedangkan aspirin murni tidak memberikan warna ungu.
C. ALAT DAN BAHAN 1. Alat percobaan
2. Bahan percobaan
Asam salisilat kering, asam asetat anhidrida, asam sulfat pekat, alkohol 96%, Aq.dest, Besi (III) klorida 10%.
D. CARA KERJA
Ke dalam pemanas 100 ml yang kering masukkan 5 g salisilat, 7,5 g asam asetat anhidrida (BJ: 1,08 g/ml) dan 5 tetes asam sulfat pekat. Campuran dikocok sampai terjadi pencampuran sempurna. Kemudian panaskan diatas pemanas air (suhu didalam labu dijaga ± 50-600C) sambil diaduk dengan termometer selama 15 menit.
Isolasi
Dinginkan sambil tetap diaduk dan ditambah 75 ml air, kemudian saring dengan pertolongan penghisapan.
Pemurnian
PERCOBAAN 5 SINTESIS YODOFORM
A. TUJUAN PERCOBAAN
Mempelajari reaksi halogenasi pada senyawa karbonil (substitusi α). B. DASAR TEORI
Reaksi substitusi α adalah reaksi penggantian atom H yang terletak pada Cα (atom karbon yang terikat pada atom karbon karbonil) oleh suatu elektrofil. Reaksi ini dikatalisis oleh basa ataupun asam. Senyawa karbonil akan berperan sebegai nukleofil melalui pembentukkan anion enolat (dengan katalisis basa) ataupun senyawa enol (dengan katalis asam). Dalam ini atom karbon α akan bertindak sebagai karbanion. Salah satu reaksi substitusi α adalah pembentukkan yodoform.
CH3-CO-CH3+ I2 CH3+ CH3-COONA
C. ALAT DAN BAHAN 1. Alat Percobaan
LAB, erlenmeyer, pendingin balik (refluk), penangas air, gelas arloji, pipet ukut.
2. Bahan Percobaan
Aseton (pro sintesis), etanol 99% (pro analisis), NaOH 6 N (pro analisis), kalium iodida, kaporit (CaOCl2), Aquadest.
D. CARA KERJA SINTESIS
ISOLASI
Campuran didiamkan selama 10 menit, kmudian disaring dengan saringan penghisap. Kristal dicuci 3 x dengan aquadest dingin hingga tidak bereaksi alkalis (cek dengan kertas lakmus).
PEMURNIAN
Kristal dimasukkan dalam LAB yang telah dilengkapi pendingin balik. Kemudian tambahkan alkohol hingga tepat larut sambil dipanaskan diatas penangas air. Dalam keadaan panas, larutan disaring dengan penyaring panas (corong buchner direndam dahulu dalam air panas). Filtrat didinginkan sambil digoyang-goyang hingga terbentuk kristal kembali dengan sempurna. Saring dengan corong buchner, keringkan. Hitung rendemennya.
IDENTIFIKASI
PERCOBAAN 6
SINTESIS PARA-NITROASETANILID
A. TUJUAN PERCOBAAN
Mempelajari reaksi substitusi elektrofilik kedua (nitrasi) pada senyawa aromatis asetanilida dalam sintesis para-nitroasetanilida.
B. DASAR TEORI
Senyawa aromatik adalah suatu tipe senyawa yang memperoleh penstabilan cukup banyak oleh delokalisasi elektron-π. Senyawa aromatik bersifat siklik dan datar, tiap cincin harus memiliki orbital p tegak lurus bidang cincin dan orbital-orbital p harus mengandung (4n+2) elektron-π (aturan Huckel).
Benzen atau aromatik lainnya dapat bereaksi substitusi aromatik elektrofilik. Reaksi umum substitusi elektrofilik adalah sebagai berikut:
Suatu benzen tersubstitusi dapat mengalami substitusi gugus kedua. Beberapa benzen tersubstitusi bereaksi lebih mudah dari benzennya sendiri, sementara benzen tersubstitusi lain lebih sukar bereaksi, tergantung gugus pertama merupakan gugus aktivator (misal: -NH2) atau deaktivator (misal:
-NO2). Substitusi kedua menghasilkan isomer orto dan para atau meta,
Contoh reaksi substitusi elektrofilik kedua adalah nitrasi asetanilid menghasilkan 3 isomer yaitu: 4-nitroasetanilid, 2-nitroasetanilid, dan 2,4-dinitroasetanilid. Reaksi nitrasi asetanilid sebagai berikut:
O H
N CH3 NHCOCH3NHCOCH3NHCOCH3
NO2 NO2
HNO3+ +
H2SO4
NO2NO2
Tidak seperti anilin, asetanilid menunjukkan reaktivitas yang moderat dalam substitusi elektronik aromatik. Selain itu, tidak seperti anilin, asetanilid tidak dioksidasi oleh asam nitrat. Nitrasi asetanilid secara prinsipal dapat menghasilkan orto dan para mononitroasetanilida (dengan para lebih banyak daripada orto), dan dengan sangat sedikit menghasilkan 2,4-dinitroasetanilida. Untuk mencegah dinitrasi asetanilida, campuran penitrasi asam nitrat dan asam sulfat ditambahkan dalan jumlah kecil pada larutan asetanilida, sehingga konsentrasi agen penitrasi dijaga minimum.
C. ALAT DAN BAHAN 1. Alat Percobaan
Beker glass 100 ml, termometer, gelas pengaduk, corong pisah, gelas ukur, corong buchner, kertas lakmus, alat pengukur titik lebur.
2. Bahan Percobaan
Asetanilid, natrium klorida, asam asetat glasial, asam sulfat pekat, asam nitrat pekat, etanol, dan es.
Dari campuran tersebut kemudian diambil 3 ml dengan pipet ukur dan dimasukkan ke dalam corong pisah untuk digunakan dalam sintesis para nitroasetanilid.
b. Sintesis
Di dalam beker glass 100 ml, dilarutkan 4,2 gram serbuk halus asetanilida kering ke dalam 4,3 ml asam asetat glasial (bila perlu dihangatkan untuk mempermudah pelarutan), sambil terus diaduk tambahkan 8,3 ml asam sulfat pekat (campuran reaksi akan menjadi hangat dan jernih), Kemudian, beker glass berisi campuran reaksi, dimasukkan ke dalam cairan pendingin (es dan garam NaCl), diletakkan termometer ke dalam beker glass, kemudian ditambahkan secara perlahan-lahan larutan asam penetrasi sebanyak 3 ml dengan corong pisah (penambahan asam penetrasi secara perlahan, dijaga suhu campuran reaksi kurang dari 100C). Setelah selesai penambahan asam penetrasi, beker glass berisi campuran reaksi diambil dan dibiarkan pada suhu kamar selama 30 menit.
c. Isolasi
Ke dalam campuran reaksi, dimasukkan sebanyak 30 gram crusheed ice (es batu), diamkan selama 15 menit (akan terbentuk endapan putih-kekuningan), kemudian disaring menggunakan corong buchner dengan pertolongan vakum penyedot. Residu yang diperoleh dicuci dengan aquadest dingin sampai bebas asam (cek dengan kertas lakmus biru), kemudian dikeringkan, ditimbang, dan dihitung rendemennya.
d. Pemurnian
e. Identifikasi hasil sintesis
PERCOBAAN 7
SINTESIS SENYAWA KALKON
A. TUJUAN PERCOBAAN
Mempelajari reaksi kondensasi karbonil B. DASAR TEORI
Reaksi kondenasi karbonil merupakan reaksi dua senyawa karbonil yang melibatkan kombinasi dua reaksi yaitu adisi nukleofilik dan substitusi α. Senyawa karbonil satu bertindak sebagai nukleofilik pemberi elektron, sedangkan senyawa karbonil lain bertindak sebagai elektrofil penerima elektron. Reaksi kondensasi karbonil merupakan reaksi yang sangat penting dalam kimia organik. Reaksi ini banyak terjadi dalam biokimia tubuh dan biosintesis senyawa alam.
Salah satu reaksi kondensasi karbonil yang terjadi antara aldehid dan keton dikenal dengan kondensasi aldol. Kondensasi aldol terjadi akibat dari senyawa karbonil yang memiliki hidrogen α dengan adanya suatu asam atau basa akan membentuk suatu enol atau enolat yang selanjutnya akan menyerang senyawa karbonil lain. Dengan reaksi kondensasi aldol dapat dihasilkan suatu senyawa β-hidroksi karbonil dan terhidrasi membentuk senyawa α,β-tak jenuh. Hidrogen yang berposisi α terhadap suatu gugus karbonil bersifat asam dan dapat disingkirkan oleh suatu basa kuat. Sifat keasaman hidrogen α terutama disebabkan stabilisasi resonansi dari ion enolat produknya.
C. ALAT DAN BAHAN 1. Alat Percobaan
LAB leher tiga, pendingin liebig, corong tetes, alat-alat gelas kualitas pyrex, motor pengaduk, pH meter, heating mantle, timbangan analitik,Melting Point ApparatusSMP-3, Spektrometer UV-Vis.
2. Bahan Percobaan
D. CARA KERJA a. Sintesis
Sebanyak 15 mmol asetofenon dimasukkan dalam 7,5 ml etanol dalam LAB leher tiga, diaduk selama beberapa menit pada suhu kamar. Ditambahkan 9 ml larutan NaOH 10% (45 mmol) dalam air tetes demi tetes selama beberapa menit dan 15 mmol benzaldehid. Pengadukan dilanjutkan selama 3 jam pada temperatur 20-250C.
b. Isolasi
Hasil reaksi dicuci dengan aquadest hingga pH netral (cek dengan kertas lakmus). Kristal yang diperoleh dikumpulkan dengan disaring pada corong buchner.
c. Pemurnian (rekristalisasi)
Pemurnian menggunakan metode rekristalisasi dengan cara sebagai berikut: Ditambang sebanyak 1 gram serbuk hasil isolasi kemudian dilarutkan dalam etanol secukupnya sampai tepat larut (bantu dengan pemanasan untuk menyempurnakan kelarutan). Dalam keadaan panas, ditambahkan dengan segera aquadest dingin untuk mendapatkan kristal kembali. Kristal yang diperoleh kemudian dikeringkan, dihitung
recovery-nya. d. Identifikasi
1. Analisis organoleptis meliputi warna, bau, rasa, bentuk kristal.