DETEKSI VIRUS HEPATITIS C (HCV) PADA KOMUNITAS GIGOLO SURAKARTA BERBASIS NESTED PCR PADA REGIO E1-E2
SKRIPSI
Untuk Memenuhi Persyaratan Memperoleh Gelar Sarjana Kedokteran
Sofina Kusnadi G0008171
FAKULTAS KEDOKTERAN UNIVERSITAS SEBELAS MARET
iv ABSTRAK
Sofina Kusnadi. G0008171. 2012. Deteksi Virus Hepatitis C (HCV) pada Komunitas Gigolo Surakarta Berbasis Nested PCR pada Regio E1-E2. Fakultas Kedokteran Universitas Sebelas Maret, Surakarta.
Tujuan Penelitian : Deteksi virus hepatitis C (HCV) dilakukan untuk mengetahui status infeksi HCV pada komunitas gigolo Surakarta.
Metode Penelitian : Penelitian ini bersifat eksploratif dengan pendekatan cross-sectional. Subjek penelitian adalah 30 gigolo di Surakarta yang diperoleh dengan teknik quota sampling. Wawancara terstruktur dan pengambilan sampel darah dilakukan pada tiap responden. Plasma darah kemudian dideteksi anti-HCV dengan metode particle agglutination assay. Sampel dengan anti-HCV positif kemudian dideteksi sebagian regio E1-E2 HCV dengan nested PCR.
Hasil Penelitian : Anti-HCV positif terdeteksi pada 23,3% (7/30) responden. Riwayat melakukan hubungan seksual anal dan vaginal ditemukan pada 73,4% (22/30) responden, penggunaan kondom secara inkonsisten ditemukan pada 73,3% (22/30) responden, penggunaan narkotika suntik bergantian ditemukan pada 3,3% (1/30) responden, serta riwayat tato dan tindik ditemukan pada 53,3% (16/30) responden. Sebagian regio E1-E2 HCV tidak terdeteksi pada sampel dengan anti-HCV positif.
Simpulan Penelitian : Infeksi HCV terdeteksi pada komunitas gigolo Surakarta. Data awal epidemiologi dari penelitian ini diharapkan dapat berkontribusi dalam manajemen infeksi HCV dalam kesehatan masyarakat.
Kata kunci: gigolo, Surakarta, HCV E1-E2
vii DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PENESAHAN ... ii
HALAMAN PERNYATAAN ... iii
ABSTRAK ... iv
C. Tujuan Penelitian ... 3
D. Manfaat Penelitian ... 3
BAB II. LANDASAN TEORI ... 4
A. Tinjauan Pustaka ... 4
1. Virus Hepatitis C (HCV) ... 4
2. Transmisi HCV ... 5
3. Deteksi Infeksi HCV ... 6
4. Regio E1-E2 sebagai Target Amplifikasi Nested PCR ... 7
B. Kerangka Pemikiran ... 8
BAB III. METODE PENELITIAN ... 9
A. Jenis Penelitian ... 9
B. Lokasi Penelitian ... 9
C. Subjek Penelitian ... 9
D. Teknik Pengumpulan Data ... 9
E. Rancangan Penelitian ... 10
BAB I
PENDAHULUAN
A. Latar Belakang Masalah
Virus hepatitis C (HCV) merupakan salah satu penyebab utama penyakit
hepatitis kronis, sirosis hepatis, dan karsinoma sel hepar (Drexler et al., 2009).
Lima puluh hingga 80% pasien HCV akut persisten dan 4-20% pasien dengan
hepatitis C kronis akan mengalami progresifitas penyakit menjadi sirosis hepatis
dalam waktu 20 tahun. Pasien dengan sirosis hepatis memiliki risiko 1-5% untuk
mengalami perkembangan penyakit menjadi karsinoma sel hepar (Brass et al.,
2006).
Diduga terdapat sedikitnya 170 juta penduduk dunia yang terinfeksi HCV
(Drexler et al., 2009). Prevalensi infeksi HCV tertinggi terdapat di wilayah Asia
dan Afrika (Shepard et al., 2005). Survei yang dilakukan pada populasi
masyarakat umum dan pendonor darah di berbagai provinsi di Indonesia
menunjukkan bahwa prevalensi HCV pada populasi tersebut sebesar 2,5% atau
mencakup 5,31 juta jiwa. Sekitar 45.000 kasus sirosis hepatis dan 18.000 kasus
karsinoma sel hepar terdeteksi di Indonesia setiap tahunnya (WHO, 2011).
Virus hepatitis C merupakan virus yang ditransmisikan melalui darah dan
produk darah. Faktor risiko transmisi HCV yang sering ditemukan antara lain
transfusi darah dari pendonor yang tidak ditapis terlebih dahulu, penggunaan
bersama jarum suntik, injeksi medis yang tidak aman, dan prosedur layanan
paparan terhadap darah maupun produk darah. Oleh karena itu, ada banyak jalur
transmisi HCV yang dapat terjadi. Jalur transmisi tersebut antara lain hubungan
seksual dengan pasangan yang terinfeksi HCV, prosedur kosmetik dan praktik
keagamaan atau kebudayaan seperti tato, tindik, cukur, praktik ritual, sirkumsisi,
dan akupunktur (Shepard et al., 2005).
Virus hepatitis C dapat ditransmisikan melalui hubungan seksual (Halfon et
al., 2001; Lai et al., 2004; Nakayama et al., 2005; Terrault, 2002). Individu yang
melakukan transaksi seksual memiliki frekuensi lebih tinggi dalam berhubungan
dengan banyak partner seks dan cenderung terikat dalam perilaku biseksual
dibanding masyarakat pada umumnya (Baseman et al., 1999; Weber et al., 2001;
Weber et al., 2002). Pekerja seks komersial pria atau disebut pula gigolo
merupakan pelaku transaksi seksual. Gigolo merupakan individu dengan risiko
tinggi terinfeksi HCV dan menjadi sumber infeksi HCV melalui hubungan
seksual. Berbeda dengan pekerja seks komersial wanita, gigolo dapat memiliki
partner seks tidak hanya wanita tetapi juga pria (Rissel et al, 2003). Dengan
demikian, peneliti lebih memilih gigolo dibanding pekerja seks komersial wanita
di Surakarta sebagai subjek penelitian untuk deteksi infeksi HCV. Deteksi infeksi
HCV pada komunitas gigolo ini penting untuk dilakukan agar dapat diketahui
status infeksi HCV pada komunitas tersebut dan dapat dilakukan pencegahan
meluasnya transmisi HCV pada masyarakat.
B. Rumusan Masalah
Bagaimana deteksi infeksi HCV pada komunitas gigolo di Surakarta
C. Tujuan Penelitian
1. Tujuan Jangka Pendek
Mendapatkan data status infeksi HCV pada komunitas gigolo di
Surakarta.
2. Tujuan Jangka Panjang
Mendapatkan profil epidemiologi molekuler HCV pada komunitas
risiko tinggi terinfeksi HCV melalui hubungan seksual di Surakarta.
D. Manfaat Penelitian 1. Manfaat Teoritik
Mengetahui status infeksi HCV pada komunitas gigolo di Surakarta.
2. Manfaat Aplikatif
Mendapatkan data awal status infeksi HCV pada komunitas gigolo
di Surakarta yang dapat digunakan dalam pengambilan kebijakan
kesehatan terkait infeksi HCV di Surakarta khususnya dan Indonesia pada
umumnya.
BAB II
LANDASAN TEORI
A. Tinjauan Pustaka
1. Virus Hepatitis C (HCV)
Virus hepatitis C tergolong dalam famili Flaviviridae dan
merupakan satu-satunya anggota genus Hepacivirus (Brass et al., 2006).
HCV berbentuk sferis dengan diameter 50 sampai 70 nm. HCV memiliki
struktur ikosahedral serta ber-envelope (Kato, 2001). Genom HCV berupa
ribonucleic acid (RNA) untai tunggal positif berukuran 9,6 kilo basa (kb)
dan mengandung Open Reading Frame (ORF) yang diapit oleh susunan
nukleotida yang tidak ditranslasikan (untranslated region atau UTR) pada
masing-masing ujung 5’ dan 3’ (Choo et al., 1989; Spahn et al., 2001).
Genom HCV terdiri dari regio core, E1, E2, dan p7 yang mengkode protein
struktural, serta regio NS2, NS3, NS4A, NS4B, NS5A, dan NS5B yang
akan mengkode protein non struktural (Gambar 1) (Kato, 2001).
Gambar 1. Struktur Genom Virus Hepatitis C (Kato, 2001).
2. Transmisi HCV
Virus hepatitis C dapat ditransmisikan melalui berbagai jalur.
Transmisi HCV terbanyak terjadi melalui transfusi darah dan penggunaan
bersama jarum suntik untuk narkotika (Murphy et al., 2007). Prosedur
layanan medis seperti endoskopi, perawatan gigi, dialisis, maupun operasi
dapat menjadi jalur transmisi HCV. Transmisi HCV juga dapat terjadi
melalui paparan parenteral lain seperti tato, tindik, dan akupunktur (Ishi et
al., 2001; Shepard et al., 2005; Terrault, 2002).
Virus hepatitis C dapat ditransmisikan melalui hubungan seksual
meskipun efisiensi infeksinya lebih rendah dibanding virus lain dengan
jalur transmisi serupa seperti hepatitis B virus (HBV) dan human
immunodeficiency virus (HIV) (Terrault, 2002). Ribonucleic acid (RNA)
HCV dapat dideteksi pada cairan semen, sekret vagina, dan usapan serviks
meskipun titernya rendah (Bélec et al., 2003; Leruez-Ville et al., 2000;
Manavi et al., 1999; Pekler et al., 2003). Ada beberapa laporan kasus yang
menunjukkan bahwa pasangan seksual dari individu dengan infeksi HCV
mengalami serokonversi anti-HCV dalam plasma darahnya. Dalam kasus
tersebut, berdasarkan penelusuran riwayat kesehatan, tidak ditemukan
faktor risiko transmisi HCV selain melalui jalur seksual. Pemeriksaan
terhadap genom HCV pada pasangan yang menjadi subjek studi tersebut
pun menunjukkan strain HCV yang ditemukan memiliki homologi tinggi
(Halfon et al., 2001; Lai et al., 2004; Nakayama et al., 2005). Selain itu,
HCV akut terjadi pada pasien yang memiliki riwayat kontak seksual dengan
orang lain yang memiliki status positif terinfeksi HCV sebagai satu-satunya
faktor risiko terinfeksi HCV (Terrault, 2002).
Transmisi HCV melalui hubungan seksual terjadi ketika darah atau
sekret tubuh orang yang terinfeksi HCV mengalami kontak melalui
permukaan mukosa tubuh pasangan seksualnya. Hubungan seksual tanpa
penggunaan kondom sebagai pengaman merupakan faktor risiko terjadinya
transmisi HCV (Irfan dan Arfin, 2004). Transmisi HCV lebih mudah terjadi
melalui hubungan seks anal dibanding seks vaginal karena lapisan mukosa
rektum merupakan lapisan yang tipis. Seks anal dapat menimbulkan luka
kecil pada lapisan mukosa rektum sehingga dapat terjadi kontak darah
(Hershow et al., 1998; Ndimbie et al., 1996; Thomas et al., 1995). Seks
oral, baik yang dilakukan terhadap pria (fellatio) maupun yang dilakukan
terhadap wanita (cunnilingus) dapat menjadi jalur transmisi HCV. HCV
dapat ditransmisikan melalui jalur ini jika seseorang memiliki luka di
daerah mulut, perdarahan di gusi, infeksi tenggorokan, atau terdapat darah
saat berlangsungnya aktivitas seks oral. Seseorang dengan penyakit
menular seksual lebih mudah mengalami transmisi HCV karena penyakit
tersebut menimbulkan luka pada daerah genital sehingga memungkinkan
terjadinya kontak darah (Franciscus, 2010).
3. Deteksi Infeksi HCV
Deteksi anti-HCV atau disebut juga tes serologi direkomendasikan
HCV (Moyer et al., 1999). Namun, infeksi virus dalam tubuh seseorang
dapat mengalami window period. Window period dalam infeksi HCV
merupakan masalah utama bagi keamanan darah seseorang. Selama periode
tersebut, antibodi spesifik HCV belum bisa dideteksi walaupun sebenarnya
terdapat virus dalam darah. Oleh karena itu, tes antibodi tidak mampu
mengidentifikasi status infeksi seseorang yang berada pada fase awal
infeksi HCV (Ré et al., 2005). Deteksi genom HCV merupakan
pemeriksaan yang direkomendasikan sebagai gold standard (Colin et al.,
2001). Deteksi genom dapat dilakukan melalui teknik biologi molekuler
dasar yang meliputi ekstraksi asam nukleat, polymerase chain reaction
(PCR), dan elektroforesis (Prasetyo, 2011).
4. Regio E1-E2 HCV sebagai Target Amplifikasi Nested PCR
Polymerase Chain Reaction (PCR) merupakan teknik amplifikasi
DNA selektif in vitro yang meniru fenomena replikasi DNA in vivo. Nested
PCR berarti reaksi PCR dilakukan dalam dua tahap. Tahap pertama adalah
untuk amplifikasi awal segmen DNA target, sedangkan tahap kedua
menggunakan sebagian produk PCR tahap pertama. Pasangan primer tahap
pertama berbeda dengan tahap kedua. Tahap PCR kedua bertujuan untuk
mengamplifikasi daerah bagian dalam dari daerah yang diamplifikasi PCR
tahap pertama (Prasetyo, 2011).
Dalam penelitian ini, sebagian daerah dalam regio E1-E2 HCV yang
mengandung daerah hypervariable region 1 (HVR1) dipilih sebagai target
sekuen regio HVR1 dapat mengungkapkan heterogenitas strain HCV (Ray
et al., 2000). Regio HVR1 dapat digunakan untuk menentukan genotipe
HCV dan dapat menjadi diskriminan antar tipe dan subtipe HCV (Murphy
et al., 2007).
B. Kerangka Pemikiran
Risiko transmisi HCV:
1. Riwayat hubungan seksual dengan pasangan seksual terinfeksi HCV.
2. Riwayat tidak menggunakan kondom dalam berhubungan seksual.
3. Riwayat seks anal.
4. Riwayat penggunaan bersama narkotika suntik. 5. Riwayat bertato dan bertindik.
(Hershow et al., 1998; Irfan dan Arfeen, 2004; Ishi et al., 2001;
Anti-HCV positif Anti-HCV negatif
BAB III
METODE PENELITIAN
A. Jenis Penelitian
Penelitian ini bersifat eksploratif dengan pendekatan cross-sectional.
B. Lokasi penelitian
Uji serologi plasma darah dilaksanakan di Laboratorium Mikrobiologi
Fakultas Kedokteran Universitas Sebelas Maret dan deteksi molekuler
dilaksanakan di Laboratorium Biomedik Fakultas Kedokteran Universitas Sebelas
Maret.
C. Subjek Penelitian
Subjek penelitian ini adalah komunitas gigolo di Surakarta yang
menandatangani informed consent dan surat persetujuan menjadi partisipan studi.
D. Teknik Pengumpulan Data
Teknik pengumpulan data yang digunakan dalam penelitian ini adalah
quota sampling dengan jumlah responden 30 orang.
E. Rancangan Penelitian
Sampel darah
Uji serologi aliquot plasma dengan kit Ortho HCV Ab
PA II ®
Anti-HCV negatif
Anti-HCV positif
Ekstraksi RNA HCV dari aliquot plasma darah
Sintesis cDNA HCV
Nested PCR sebagian genom E1-E2 HCV
Elektroforesis Aliquot plasma darah
Fraksinasi
Didapatkan plasma darah
F. Alat dan Bahan
1. Alat
a. spuit injeksi 5 ml
b. cool box dan cool pack
c. tabung EDTA
d. centrifuge (Eppendorf, Hamburg, Jerman)
e. tube rack
f. micropipette (P1000, P200, P10) (Gilson, Middleton, WI)
g. magnetic stirrer (Biomega, Redding, CA)
h. viral spin column
i. collection tube
j. wash tube (2 ml)
k. recovery tube (1,5 ml)
l. thermocycler (Eppendorf, Hamburg, Jerman)
m. vortex (Thermo Fisher Scientific, Worcester, MA)
n. autoclave (Hirayama, Saitama, Jepang)
o. waterbath (Thermo Fisher Scientific, Worcester, MA)
p. gel documentation (BioRad, Los Angeles, CA)
q. digital scale (Mettler Toledo, Greifensee, Switzerland)
r. aparatus elektroforesis (chamber, comb, dan power supply)
(BioRad, Los Angeles, CA)
s. refrigerator (Sharp, Osaka, Jepang)
t. deep freezer (New Brunswick Scientific, Edison, NJ)
u. class II safety cabinet (ESCO, Portland, OR)
2. Bahan
a. sampel darah
b. kit Ortho HCV Ab PA II® (Fujirebio, Tokyo, Japan)
c. kit PureLink™ Viral RNA/DNA (Invitrogen, Carlsbad, CA)
d. kit SuperScript III First-Strand Synthesis SuperMix
(Invitrogen, Carlsbad, CA)
e. primer oligonukleotida (primer forward dan primer backward)
f. nuclease-free water
g. bufer Tris-EDTA (TE) pH 8
h. loading dye
i. agarosa
j. larutan Tris-Acetate-EDTA (TAE) 1X
k. ethidium bromide (EtBr) 10 mg/ml
l. Loading quick® λ/Hind III digest, DNA-110 (Toyobo, Osaka,
Japan)
m. Loading Quick®ФX174/ Hae III (Toyobo, Osaka, Japan)
n. etanol 70% dan 96%
o. tip filter (10 ml, 200 ml, dan 1000 ml)
p. microcentrifuge tube 1,5 ml
q. tabung PCR dan cap tabung PCR
r. polypropylene (PP) tube 15 ml
s. 96 MicroWell™ Plates (Nunc, Rochester, NY)
t. tisu
u. parafilm
v. handscoen
w. masker
G. Cara Kerja
1. Preparasi Sampel
Preparasi sampel dimulai dengan mengambil darah subjek
penelitian sebanyak 5 ml dan memasukkannya ke dalam tabung EDTA.
Tabung EDTA kemudian dimasukkan ke dalam cool box yang telah diberi
cool pack. Sampel darah dalam tabung EDTA dipindahkan ke dalam
polypropylene (pp) tube lalu difraksinasi melalui sentrifugasi pada
kecepatan 3.000 rpm selama 15 menit. Setelah dilakukan fraksinasi, akan
terbentuk tiga lapisan pada sampel darah. Bagian paling atas merupakan
plasma darah, bagian tengah merupakan peripheral blood mononuclear
cells (PBMC), dan lapisan terbawah merupakan kumpulan sel darah
merah. Plasma darah diambil dengan mikropipet untuk dibuat aliquotnya
ke dalam microcentrifuge tube.
2. Uji Serologi Plasma Darah
Deteksi anti-HCV dalam plasma darah dilakukan dengan metode
particle agglutination menggunakan kit Ortho HCV Ab PA II® (Fujirebio).
Komponen kit ini terdiri dari reconstituting solution, sample diluent,
sensitized particle, lyophilized control particles, positive control, dan
dalam tabung berisi lyophilized control particles, lalu dicampur dengan
menggunakan mikropipet.
Pemeriksaan serologi dilaksanakan dengan menggunakan 96
microwell plate U shape. Well yang digunakan berjumlah tiga well untuk
setiap sampel. Reagen dimasukkan ke dalam setiap well. Well pertama
dimasukkan 75 µL sample diluent. Well kedua dan ketiga dimasukkan
masing-masing 25 µL sample diluent. Plasma darah sebanyak 25 µL
dimasukkan ke dalam well pertama lalu dicampur dengan menggunakan
mikropipet. Setelah itu dilakukan transfer antar well. Dari well pertama, 25
µL larutan diambil menggunakan mikropipet dan dimasukkan ke well
kedua lalu dicampur dengan menggunakan mikropipet. Dari well kedua,
25 µL larutan diambil dan dimasukkan ke well ketiga lalu dicampur
dengan menggunakan mikropipet. Dua puluh lima mikroliter larutan dari
well ketiga diambil lalu dibuang. Selanjutnya, 25 µ L control particle
ditambahkan ke dalam well kedua dan 25 µL sensitized particle
ditambahkan ke well ketiga. Plate kemudian digoyangkan secara perlahan,
lalu diinkubasi selama 2 jam dan kemudian dilakukan interpretasi terhadap
pola aglutinasi yang terjadi di dasar well. Apabila partikel yang
teraglutinasi menyebar secara seragam di dasar well dan dikelilingi
lingkaran merah, berarti hasil adalah positif dua (++). Jika partikel
membentuk pola cincin dengan garis terluar berbentuk kasar dan tidak
teratur serta dikelilingi lingkaran merah kecil berarti hasil adalah positif
bergaris luar halus dengan lubang di tengah. Pada hasil demikian,
pemeriksaan harus diulang. Hasil negatif (-) berarti partikel membentuk
titik di tengah dasar well dengan garis luar halus atau partikel membentuk
pola cincin dengan lubang sangat kecil di tengahnya dan bergaris luar
halus.
3. Ekstraksi asam nukleat HCV menggunakan Kit PureLink™
Viral RNA/DNA (Invitrogen, Carlsbad, CA)
Ekstraksi asam nukleat HCV dimulai dengan persiapan lisat. Dua
puluh lima mikroliter proteinase K, 200 µL plasma darah, dan 200 µ L lysis
buffer dimasukkan ke dalam microcentrifuge tube steril lalu dicampur
menggunakan vortex selama 15 detik. Selanjutnya, 250 µL etanol 100%
ditambahkan ke dalam microcentrifuge tube lalu dilakukan vortex selama
15 detik dan diinkubasi selama 5 menit pada suhu ruangan. Lisat tersebut
selanjutnya dimasukkan ke dalam viral spin column dan disentrifugasi
pada kecepatan 6.000 rpm selama satu menit. Supernatan dan collection
tube kemudian dibuang. Selanjutnya dilakukan tahap pencucian dengan
cara memasukkan 500 µL wash buffer ke dalam column lalu disentrifugasi
dan supernatan dibuang. Langkah pencucian diulang satu kali. Untuk
membuang wash buffer yang masih ada dalam spin column, dilakukan
sentrifugasi pada kecepatan 14.000 rpm selama satu menit. Spin column
dipindahkan ke dalam recovery tube berukuran 1,7 ml. Spin column
ditambahkan TE RNase DNase free water sebanyak 50 µL dan dilakukan
sentrifugasi selama satu menit pada kecepatan 14.000 rpm untuk
mengelusi asam nukleat ke recovery tube. Asam nukleat virus yang telah
diekstraksi dapat disimpan pada suhu -80oC atau digunakan langsung
untuk langkah berikutnya (Invitrogen, 2006).
4. Sintesis Complementary DNA (cDNA)
Sintesis cDNA terhadap asam nukleat yang telah diekstraksi
dilakukan dengan menggunakan kit SuperScript III First-Strand Synthesis
SuperMix (Invitrogen). Sebelum digunakan, dilakukan mix dan spin down
pada setiap reagen kit. Enam mikroliter asam nukleat, 1 µL primer random
heksamer, dan 1 µL bufer annealing dimasukkan ke dalam tabung PCR
berukuran 0,2 ml dan diinkubasi pada suhu 65oC selama lima menit.
Setelah inkubasi, campuran didinginkan pada suhu 4oC selama satu menit
dan dilakukan spin down. Kemudian, ditambahkan 10 µ l 2X First-Strand
Reaction Mix dan 2 µl SuperScript™ III/RNaseOUT™ Enzyme Mix lalu
dilakukan pipetting serta spin down. Selanjutnya campuran tersebut
diinkubasi selama 10 menit pada suhu 25oC dan dilanjutkan pada suhu
50oC selama 50 menit. Reaksi diakhiri pada suhu 85oC selama lima menit.
Setelah reaksi selesai, tabung PCR didinginkan pada suhu 4oC. Hasil
reaksi sintesis cDNA dapat disimpan pada suhu -20oC atau langsung
digunakan dalam tahap PCR (Invitrogen, 2010a).
5. Nested Polymerase Chain Reaction (PCR)
Reaksi nested PCR dilakukan dengan menggunakan kit Platinum®
Platinum® PCR SuperMix, primer hingga mencapai konsentrasi akhir
200nM, dan template DNA. Kemudian, tabung PCR yang telah ditutup
dimasukkan ke dalam thermal cycler (Invitrogen, 2010b). Kondisi PCR
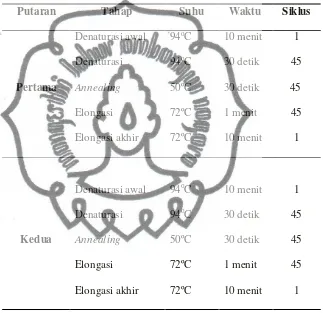
yang digunakan ditampilkan di Tabel 1.
Tabel 1. Pengaturan Kondisi PCR Sebagian Regio HCV E1-E2
Putaran Tahap Suhu Waktu Siklus
Pertama
Denaturasi awal 94oC 10 menit 1
Denaturasi 94oC 30 detik 45
45
45
Annealing 50ºC 30 detik
Elongasi 72ºC 1 menit
Elongasi akhir 72ºC 10 menit 1
Kedua
Denaturasi awal 94oC 10 menit 1
Denaturasi 94oC 30 detik 45
45
45
Annealing 50ºC 30 detik
Elongasi 72ºC 1 menit
Elongasi akhir 72ºC 10 menit 1
Primer yang digunakan dalam putaran PCR pertama adalah primer
sense Lqz188 (5’-CAY CGB ATG GCH TGG GAY ATG ATG ATG AA) dan
primer antisense Lqz187 (5’-CCY ACB ACM ACD GGG CTN GGD GTG
AAR CAR TA). Untuk putaran PCR kedua, primer yang digunakan adalah
primer sense Lqz189 (5’-TGG GAY ATG ATG ATG AAY TGG TC) dan
6. Elektroforesis
Elekroforesis dilakukan untuk analisis produk nested PCR. Untuk
elektroforesis, digunakan gel agarosa 1,5% dalam larutan
Tris-Acetate-EDTA (TAE) I X. Agarosa dibuat melalui penambahan 3 gram agarosa ke
dalam 200 ml TAE 1X dalam tabung Erlenmeyer. Agarosa dicairkan lalu
dicampur menggunakan magnetic stirrer dalam keadaan panas, kemudian
didinginkan hingga 55 ºC. EtBr ditambahkan hingga mencapai konsentrasi
0,5 µ g/ml lalu dicampur menggunakan magnetic stirrer. Agarosa
selanjutnya dituang ke dalam gel tray yang sudah dipasangi comb dan
disimpan dalam suhu kamar selama 15-20 menit hingga menjadi solid.
Setelah solid, comb diambil lalu gel diletakkan ke dalam electrophoresis
chamber dan digenangi TAE. Marker Loading Quick® λ/ Hind II sebanyak
5 µ l dimasukkan ke dalam sumur pertama gel agarosa. Sumur kedua diisi
dengan marker Loading Quick®ФX174/ Hae III sebanyak 5 µ l. Kemudian
2,5 µL produk PCR yang terlebih dahulu dicampur dengan loading dye
dimasukkan ke dalam sumur selanjutnya. Voltase yang digunakan untuk
elektroforesis adalah 100 volt selama 30 menit.
Untuk melakukan interpretasi hasil elektroforesis, gel agarosa
diambil dari bak elektroforesis lalu diletakkan ke dalam UV gel
documentation. Modus cahaya “trans UV” kemudian dipilih untuk
visualisasi DNA pada gel agarosa. Setelah itu akan didapatkan gambaran
pita DNA. Pita DNA yang terbentuk kemudian dibandingkan dengan
2011). Panjang pita DNA yang diharapkan berukuran 538 bp (Kageyama
et al., 2006).
H. Analisis Data
Data yang meliputi risiko transmisi HCV dan hasil PCR positif disajikan
secara deskriptif. Risiko transmisi HCV yang dimaksud antara lain riwayat
berhubungan seksual dengan pasangan seksual terinfeksi HCV, riwayat tidak
menggunakan kondom saat berhubungan seksual, riwayat seks anal, riwayat
penggunaan bersama jarum suntik untuk narkotika, serta riwayat bertato dan
bertindik.
BAB IV
HASIL PENELITIAN
Pengumpulan data dan spesimen darah dari 30 gigolo di Surakarta telah
dilakukan pada bulan Mei hingga Juni 2011. Data diperoleh melalui wawancara
terpimpin dengan pertanyaan yang telah divalidasi. Wawancara dilakukan secara
personal dan jawaban responden direkam dengan alat MP4 untuk kemudian
dianalisis. Spesimen darah diambil oleh tenaga kesehatan terlatih. Karakteristik
sosiodemografi gigolo di Surakarta ditampilkan pada Tabel 2.
Tabel 2. Karakteristik Sosiodemografi Gigolo di Surakarta
Dalam laporan penelitian ini, data yang disajikan secara deskriptif meliputi
riwayat berhubungan seksual dengan pasangan seksual terinfeksi HCV, riwayat
tidak menggunakan kondom saat berhubungan seksual, riwayat seks anal, riwayat
penggunaan bersama jarum suntik untuk narkotika, serta riwayat bertato dan
bertindik.
A. Riwayat Hubungan Seksual dengan Pasangan Seksual Terinfeksi HCV Pada penelitian ini tidak didapatkan responden yang memiliki riwayat
berhubungan seksual dengan pasangan seksual terinfeksi HCV.
B. Riwayat Tidak Menggunakan Kondom dalam Berhubungan Seksual Dalam melakukan hubungan seksual, 83,3% (25/30) responden
menggunakan kondom, sedangkan 16,7% (5/30) responden tidak pernah
menggunakan kondom. Kondom berbahan lateks digunakan oleh 88% (22/25)
responden. Sebanyak 12% (3/25) responden tidak mengetahui jenis kondom yang
digunakannya. Didapatkan 32% (8/25) responden menggunakan kondom secara
konsisten, sedangkan 68% (17/25) responden menggunakan kondom secara
inkonsisten.
C. Riwayat Seks Anal
Pada penelitian ini ditemukan sebanyak 73,4% (22/30) responden
melakukan hubungan seksual baik vaginal maupun anal. Didapatkan 13,3% (4/30)
responden yang melakukan hubungan seksual vaginal saja dan 13,3% (4/30) yang
melakukan hubungan seksual anal saja.
D. Riwayat Penggunaan Bersama Narkotika Suntik
responden yang memiliki riwayat tinggal di lembaga koreksional di Surakarta.
Responden tersebut pernah menggunakan narkotika suntik bersama dengan
sesama narapidana. Dalam penelitian ini, riwayat penggunaan bersama jarum
suntik untuk injeksi narkotika ditemukan pada 3,3% (1/30) responden.
E. Riwayat Bertato dan Bertindik
Berdasarkan penelitian ini, diketahui bahwa 16,7% (5/30) responden
memiliki riwayat bertato. Sebanyak 30% (9/30) responden memiliki riwayat
tindik. Ditemukan 6,7% (2/30) responden dengan riwayat tato dan tindik.
Sebanyak 46,67% (14/30) responden tidak memiliki riwayat tato maupun tindik.
Pembuatan tato dan tindik di tempat komersial dilakukan oleh 37,5% (6/16)
responden, sedangkan 62,5% (10/16) responden melakukanya di tempat
non-komersial, yaitu dilakukan sendiri di rumah atau lembaga koreksional.
Penggunaan alat tato dan tindik steril dan tidak dipakai bergantian diklasifikasikan
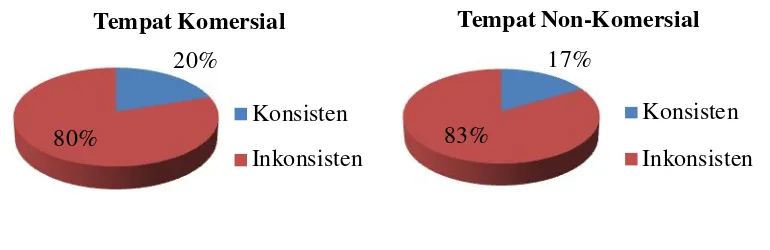
menjadi konsisten dan inkonsisten. Data tempat pembuatan tato dan riwayat
penggunan alat tato dan tindik ditampilkan pada Gambar 2.
Gambar 2. Konsistensi Penggunaan Alat Steril dan Tidak Dipakai Bergantian pada
Responden Bertato dan Bertindik 20%
80%
Tempat Komersial
Konsisten Inkonsisten
17%
83%
Tempat Non-Komersial
Konsisten Inkonsisten
F. Angka Positif HCV pada Komunitas Gigolo di Surakarta
Aliquot plasma yang didapat melalui fraksinasi dideteksi keberadaan
anti-HCV nya menggunakan kit Ortho HCV Ab PA II®. Dari pemeriksaan tersebut,
didapatkan angka anti-HCV positif sebesar 23,3% (7/30).
G. Karakteristik Responden dengan Anti-HCV Positif
Setiap responden memilki risiko paparan HCV yang berbeda berdasarkan
karakteristik yang diteliti dalam penelitian ini. Seluruh responden dengan
anti-HCV positif tidak memiliki riwayat berhubungan seksual dengan pasangan
terinfeksi HCV. Karakteristik secara lengkap terangkum dalam Tabel 3.
H. Deteksi RNA HCV pada Komunitas Gigolo di Surakarta
Dari keseluruhan sampel plasma darah dalam penelitian ini, didapatkan 7
sampel dengan anti-HCV positif. Aliquot dari 7 sampel plasma darah tersebut
kemudian diekstrak asam nukleatnya, disintesis complementary DNA
(cDNA)-nya, dan dilakukan deteksi molekuler melalui nested PCR yang mengamplifikasi
sebagian genom E1-E2 HCV. Dari 7 sampel tersebut tidak terdeteksi RNA HCV.
Visualisasi hasil hasil elektroforesis produk PCR dapat dilihat pada Gambar 3.
Gambar 3. Visualisasi Hasil Elektroforesis Produk PCR Sebagian Regio HCV E1-E2
Keterangan: Sumur 1 berisi marker Loading Quick® λ/ Hind II; Sumur 2 berisi marker Loading Quick ® ФX174/ Hae III; Sumur 3 berisi kontrol
positif produk PCR sebagian regio E1-E2 (538 bp) dengan interpretasi hasil positif; Sumur 4-10 berisi produk PCR sampel nomor 1-7
dengan interpretasi hasil negatif; Sumur 11 berisi kontrol positif produk PCR regio NS5B (328 bp)
dengan interpretasi hasil positif. 23.130 bp
9.416 bp 6.557 bp 2.322 bp 2.027 bp 1.353 bp 1.078 bp 872 bp 603 bp 271 bp
538 bp
328 bp
BAB V
PEMBAHASAN
A. Infeksi HCV dan Perilaku Seksual pada Komunitas Gigolo di Surakarta
Virus hepatitis C dapat ditransmisikan melalui hubungan seksual. Risiko
transmisi HCV melalui hubungan seksual dapat berkurang secara signifikan
melalui penggunaan kondom lateks secara benar dan konsisten. Kondom berbahan
lateks bersifat tidak permeabel terhadap agen infeksius yang terkandung dalam
sekret genital (Holmes et al., 2004; United Nations Population Fund, 2004). Pada
penelitian ini mayoritas responden yaitu 88,3% (25/30) menggunakan kondom
dalam berhubungan seksual dan 88% (22/25) di antaranya menggunakan kondom
berbahan lateks. Namun, penggunaan kondom secara konsisten hanya dilakukan
oleh 32% (8/25) responden, sedangkan 68% (17/25) responden inkonsisten.
Hubungan seksual tanpa penggunaan kondom tidak selalu menyebabkan
seseorang tertular HCV (Villena, 2006). Hal ini dikarenakan titer HCV pada
cairan semen maupun vaginal rendah, yaitu sekitar 102 kopi RNA HCV per ml.
Oleh karenanya, risiko transmisi HCV secara seksual sangat kecil jika
dibandingkan dengan agen infeksius lain seperti HBV dan HIV. Selain itu,
rendahnya tingkat transmisi HCV melalui hubungan seksual dapat disebabkan
oleh ketiadaan sel target yang tepat atau mukosa yang abnormal di traktus
genitalia untuk memulai terjadinya infeksi HCV (Terrault, 2002). Risiko terinfeksi
HCV bagi seseorang yang memiliki hubungan seksual tanpa pengaman selama 20
tahun dengan pasangan yang terinfeksi HCV adalah sebesar 2,5% (Villena, 2006).
Responden dalam penelitian ini pada umumnya melakukan hubungan
seksual baik vaginal maupun anal. Hubungan seksual anal merupakan jalur
transmisi HCV yang lebih mudah dibanding vaginal karena lapisan mukosa
anorektal lebih tipis dibanding mukosa vaginal. Hubungan seks anal dapat
menimbulkan luka pada lapisan mukosa anorektal sehingga dapat terjadi kontak
darah. Darah merupakan medium penularan HCV yang lebih baik dibanding
cairan semen. Lesi mukosa anorektal karena hubungan seksual anal dapat
berperan sebagai pintu masuk maupun sumber infeksi HCV. Dalam aktivitas seks
berkelompok, penis pasangan seksual yang melakukan insersi dapat berperan
sebagai vektor tansmisi HCV untuk pasangan reseptif. Hal ini terjadi jika kondom
tidak digunakan atau tidak diganti untuk setiap pasangan yang ada dalam aktivitas
seks berkelompok tersebut (Schmidt et al., 2011).
B. Infeksi HCV dan Paparan Parenteral Terhadap HCV pada Komunitas Gigolo di Surakarta
Paparan parenteral terhadap HCV, salah satunya penggunaan narkotika
suntik, merupakan faktor risiko kuat dalam terjadinya infeksi HCV (Murphy et
al., 2000; Sherman et al., 2001). Pada penelitian ini didapatkan 3,3% (1/30)
responden memiliki riwayat penggunaan jarum suntik secara bergantian untuk
injeksi narkotika. Selain penggunaan narkotika suntik, riwayat bertato dan
bertindik secara tidak aman juga merupakan risiko paparan parenteral lain
higienis sederhana seperti mencuci tangan, tetapi juga meliputi teknik sterilisasi
tepat terhadap peralatan yang dipakai ulang, dan menggunakan jarum sekali pakai
(WHO, 1999). Meskipun sterilisasi tidak mahal, sterilisasi dapat meningkatkan
biaya untuk setiap pembuatan tato sebesar 15% (Rauner et al., 2005). Hal ini
memungkinkan tidak dilakukannya prosedur pembuatan tato dan tindik yang
aman di tempat komersial. Pada penelitian ini, responden yang membuat tato di
tempat komersial maupun non-komersial pada umumnya inkonsisten dalam
penggunaan alat yang disterilisasi dan sekali pakai.
Lembaga koreksional (rumah tahanan dan lembaga pemasyarakatan)
merupakan tempat penting untuk transmisi virus yang ditularkan melalui darah.
Para tahanan di lembaga koreksional cenderung menggunakan jarum suntik secara
bergantian daripada menggunakan jarum suntik baru untuk injeksi narkotika.
Kegiatan tersebut merupakan faktor risiko penting untuk transmisi HCV pada
kelompok injecting drug user (IDU) (Hahn et al., 2001). Selain penggunaan
narkotika suntik, perilaku yang juga berisiko menularkan HCV di lembaga
koreksional antara lain pembuatan tato, tindik, dan kekerasan seksual (Hellard et
al., 2000). Sebanyak 3,3% (1/30) responden dengan riwayat tinggal di lembaga
koreksional yang ditemukan dalam penelitian ini, selain memiliki riwayat
penggunaan narkotika suntik, juga memiliki riwayat pembuatan tato dan
berhubungan seksual dengan sesama tahanan ketika tinggal di lembaga
koreksional.
C. Kaitan Hasil Pemeriksaan Anti-HCV dan Deteksi Molekuler RNA
HCV pada Komunitas Gigolo di Surakarta
Deteksi infeksi HCV dalam penelitian ini dilakukan dengan metode particle
agglutination assay dan nested PCR. Sampel dengan anti-HCV positif kemudian
dideteksi keberadaan RNA HCV-nya dengan PCR. PCR merupakan metode
laboratorik yang digunakan untuk mendeteksi RNA HCV yang bersirkulasi dalam
darah. Keberadaan RNA HCV mengindikasikan bahwa HCV bereplikasi aktif
(bereproduksi dan menginfeksi sel baru inang) (Carithers et al., 2000; Pawlotsky,
2002).
Pada penelitian ini didapatkan hasil deteksi molekuler negatif untuk ketujuh
responden dengan anti-HCV positif. Hasil negatif deteksi molekuler pada
penelitian ini dapat dipertanggungjawabkan karena peneliti telah melakukan
kontrol amplifikasi eksternal dan mengulang pemeriksaan.
Setelah paparan akut terhadap HCV, RNA HCV umumnya lebih dahulu
terdeteksi dalam darah mendahului munculnya antibodi terhadap HCV (Ghany et
al., 2009). RNA HCV dapat diidentifikasi dalam waktu dua minggu setelah
paparan, sedangkan anti-HCV tidak terdeteksi sebelum 8-12 minggu. Hasil negatif
palsu untuk deteksi RNA HCV dapat terjadi apabila seseorang dengan infeksi
HCV aktif mengalami viremia intermiten. Viremia intermiten berarti
didapatkannya hasil negatif pada deteksi RNA HCV yang diikuti dengan hasil
positif untuk deteksi RNA HCV berikutnya (Bruden et al., 2004; Scott et al.,
2006). Viremia intermiten dapat terjadi sekitar dua bulan sebelum infeksi HCV
fase plateau titer tinggi. Fase tersebut disebut dengan fase pre rump-up dengan
durasi yang tidak diketahui. Pada kasus demikian diperlukan pengulangan uji PCR
4-6 bulan kemudian setelah uji PCR pertama (Ghany et al., 2009).
Tidak terdeteksinya RNA HCV pada individu dengan anti-HCV positif
dapat pula menunjukkan bahwa infeksi HCV telah mengalami resolusi. Pasien
tersebut mungkin mengalami infeksi HCV di masa lalu (Gretch, 1997; Sakugawa,
1995). Pasien dengan hepatitis C yang bersifat self-limiting dapat mengalami
clearance RNA HCV dalam 12-16 minggu dari munculnya onset klinis (Mondelli
et al., 2005). Respon imun kuat dari sel T helper (Th) 1 sitopatik, sel T CD4, sel T
CD8, dan sitokin tipe 1 kemungkinan terlibat dalam clearance HCV (Mondelli et
al., 2005; Thimme et al., 2001). Setelah seseorang terinfeksi HCV, terjadi aktivasi
sel natural killer (NK) dan pemrosesan antigen virus oleh immature dendritic
cells (iDCs). Setelah maturasi, mature dendritic cells (mDCs) mengaktivasi CD4
dan sel NKT. Sel CD4 kemudian memproduksi sitokin seperti IFN-λ yang dapat
meginduksi sel T sitotoksik limfosit (CTLs). CTLs dapat mengontrol replikasi
HCV melalui pelisisan sel yang terinfeksi dan produksi sitokin yang dapat
langsung menghambat replikasi virus. Respon sel T CD4 berhubungan dengan
penurunan derajat viremia. Selain itu, akumulasi sel T CD4 spesifik HCV dalam
hepar memegang peranan penting dalam resolusi infeksi HCV. Individu dengan
respon sel CD4 spesifik HCV memiliki kemungkinan lebih untuk mengalami
resolusi infeksi HCV, sedangkan individu yang tidak memiliki respon serupa
cenderung mengalami infeksi HCV persisten (Koziel, 2005).
Resolusi spontan infeksi HCV dapat terjadi pada 30-50% kasus (Thomas et
al., 2000). Variasi genetik yang terlibat dalam respon imun berkontribusi dalam
kemampuan individu mengalami resolusi infeksi HCV. Variasi genetik pada gen
interleukin-28B (IL-28B) merupakan prediktor kuat clearance infeksi HCV
genotipe 1, baik pada individu dengan maupun tanpa pengobatan terhadap infeksi
HCV (Grebely et al., 2010; Rauch et al., 2010; Thomas et al., 2009). Terdapat
beberapa kandidat SNP pada gen IL-28B, antara lain rs4803219, rs28416813,
rs8103142, rs4803217, dan rs12979860 (Di Iulio et al., 2011). SNP pada alel
rs12979860 (kromososm 19q13) berhubungan erat dengan sustained virological
response (SVR) pada hepatitis C kronis dan resolusi spontan infeksi HCV akut.
SNP pada alel rs12979860 terletak 3 kb upstream dari gen interleukin-28B. Gen IL-28B berfungsi untuk mengkode interferon-λ3 (IFN-λ3). IFN-λ3 termasuk
dalam kelompok interferon tipe III, selain IFN-λ1 dan IFN-λ2. IFN-λ3 memiliki
aktivitas antiviral terhadap HCV genotipe 1 melalui jalur Janus kinase-signal
transducer and activator of transcription (JAK-STAT) (Robek et al., 2005;
Shiffman et al., 2009). Mekanisme kerja IFN-λ3 adalah meningkatkan ekspresi
gen yang diinduksi interferon dan meningkatkan efikasi IFN-α sehingga dapat
menghambat replikasi virus.
SNP pada alel rs12979860 berkaitan erat dengan varian pengkodean
non-sinonim dalam gen IL-28B, yaitu transisi adenine (A) oleh guanine (G) 213 basa
dari rs8103142 (213A>G) dan SNP pada rs8103142 yang menyebabkan substitusi
lysine (K) dengan arginin (R) (K70R). Perubahan 213A>G dapat mengubah
erat dengan rs12979860, yaitu transisi guanine (G) oleh cytosine (C) 37 basa dari
rs28416813 (37 G>C) dan SNP pada rs28416813 yang menyebabkan substitusi
lysine (K) dengan arginin (R) (K70R). Selain itu, genotipe rs12979860 dengan
alel C/C ditemukan lebih banyak pada individu yang mengalami clearance
spontan HCV dibanding individu dengan infeksi HCV persisten. Individu dengan
genotipe rs12979860 dengan alel C/C memiliki kemungkinan tiga kali lebih besar
untuk mengalami clearance spontan HCV dibanding individu dengan genotipe
C/T dan T/T pada alel rs12979860 (Thomas, 2009).
BAB VI
SIMPULAN DAN SARAN A. Simpulan
1. Anti-HCV positif ditemukan pada 23,3% gigolo di Surakarta.
2. Deteksi molekuler dengan nested PCR pada sebagian regio E1-E2
memberikan hasil negatif pada seluruh gigolo dengan anti-HCV positif.
3. Pada gigolo di Surakarta ditemukan 86,7% melakukan hubungan seksual anal, 73,3% menggunakan kondom secara inkonsisten, 3,3%
menggunakan narkotika suntik secara bergantian, 16,7% memiliki
riwayat bertato, 30% memiliki riwayat bertindik, dan 6,7% memiliki
baik tato maupun tindik.
B. Saran
1. Memberikan edukasi kepada komunitas gigolo di Surakarta untuk
menggunakan kondom berbahan lateks secara benar dan konsisten
dalam berhubungan seksual baik vaginal maupun anal. Selain itu,
komunitas gigolo di Surakarta juga perlu diberi edukasi bahwa
hubungan seksual anal lebih berisiko menularkan HCV dibanding
hubungan seksual vaginal.
2. Memberikan edukasi kepada komunitas gigolo di Surakarta untuk
menghindari penggunaan narkotika suntik secara bergantian, serta
penggunaan alat pembuatan tato dan tindik tanpa sterilisasi yang
3. Responden berstatus anti-HCV positif dengan RNA HCV yang tidak
terdeteksi dalam darahnya perlu diuji ulang PCR 4-6 bulan kemudian
setelah uji PCR pertama untuk memastikan status infeksi HCV.
4. Diperlukan adanya penelitian lebih lanjut mengenai variasi genetik
dan genomik yang dapat berpengaruh pada resolusi spontan infeksi
HCV.
5. Deteksi infeksi HCV perlu dilakukan pada komunitas berisiko tinggi
seperti komunitas gigolo secara berkala agar dapat dilakukan
pencegahan menyebarnya infeksi HCV ke komunitas masyarakat
yang lebih luas.