PENGEMBANGAN METODE VOLTAMMETRI LUCUTAN
UNTUK ANALISIS ASAM URAT MELALUI PELAPISAN
ELEKTRODA DENGAN POLIMER CETAKAN MOLEKUL
DEVELOPMENT OF STRIPPING VOLTAMMETRIC
METHOD FOR URIC ACID ANALYSIS THROUGH
ELECTRODE COATING WITH MOLECULAR IMPRINTING
POLYMER
Miratul Khasanah
07/263677/SPA/176
PROGRAM STUDI S3 ILMU KIMIA
JURUSAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS GADJAH MADA
YOGYAKARTA
2012
1
ANALISIS ASAM URAT MELALUI PELAPISAN ELEKTRODA DENGAN POLIMER CETAKAN MOLEKUL
oleh Miratul Khasanah NIM. 07/263677/SPA/176
I PENDAHULUAN
Asam urat di dalam tubuh merupakan hasil akhir metabolisme purin. Konsentrasi normal asam urat dalam tubuh manusia berkisar 3,5–7 mg/dL untuk pria dan 2,6–6 mg/dL untuk wanita. Tingginya konsentrasi asam urat dalam tubuh dapat mengindikasikan adanya gejala beberapa penyakit seperti diabetes, tekanan darah tinggi, penyakit ginjal dan penyakit hati, serta dapat menyebabkan kenaikan resiko terkena penyakit kardiovaskuler.Metode penentuan konsentrasi asam urat yang biasa dilakukan dalam bidang biomedis adalah spektrofotometri dengan pereaksi asam fosfotungstat atau menggunakan enzim uricase (Chen et al., 2005). Analisis asam urat dengan metode ini membutuhkan pereaksi kimia atau enzim, perlakuan sampel yang rumit sehingga memerlukan waktu analisis yang lama, jumlah sampel yang diperlukan relatif banyak, memiliki sensitivitas yang rendah dan batas deteksi yang tinggi (dalam level mM)
Pada beberapa tahun terakhir, metode voltammetri telah digunakan untuk penentuan konsentrasi dan sifat-sifat redoks suatu senyawa di dalam cairan tubuh, seperti asam urat. Pengembangan metode voltammetri untuk analisis asam urat dalam darah dan urin menjadi kajian yang sangat menarik karena keberadaan senyawa tersebut dalam sampel selalu dijumpai bersama-sama dengan senyawa elektroaktif lainnya yang sifat dan strukturnya hampir mirip.
Beberapa penelitian tentang pengembangan metode voltammetri untuk analisis asam urat melalui modifikasi elektroda padat telah dilaporkan, diantaranya menggunakan elektroda berbasis screen printed carbon (Carsol et.al., 1997), elektroda pasta karbon terlapis nafion (Zen dan Hsu 1998), elektroda Au-Pd (Matos
et al., 2000), GC–propionil kolin (Lin dan Jin, 2005), grafit-DNA (Luoet al., 2005), GC– noreepinefrin (Zare et al., 2005), GC–5-hidroksi triptofan) (Lin dan Li, 2006), pasta karbon-tionin nafion (Shahrokhian dan Ghalkhani, 2006), dan GC-CeO2(Weiet al., 2006). Dengan elektroda padat termodifikasi tersebut, analisis asam urat sangat
diganggu oleh adanya oksigen terlarut yang dihasilkan akibat penggunaan potensial oksidasi yang tinggi. Selain itu elektroda termodifikasi tersebut hanya mampu menganalisis asam urat dengan rentang konsentrasi yang relatif tinggi ( 10-8–10-3M).
Khasanah et al. (2007) melakukan analisis asam urat dalam sampel urin dan serum secara voltammetri lucutan menggunakan elektroda cair berupa hanging mercury drop (HMD). Analisis asam urat menggunakan elektroda ini menghasilkan akurasi yang tinggi (99,57–101,43%) dan batas deteksi yang rendah (3,0x10-8 M), namun sangat diganggu oleh asam askorbat karena potensial puncak keduanya berdekatan.
Pada penelitian ini dilakukan modifikasi elektroda dengan cara melapisi elektroda GC dan HMD menggunakan polimer cetakan molekul (molecular imprinting polymer, MIP) untuk analisis asam urat secara voltammetri lucutan. Dengan sistemimprintingini, akan dibentuk cetakan dengan ukuran dan bentuk yang spesifik untuk analit tertentu pada polimer yang digunakan untuk memodifikasi elektroda sehingga analisis terhadap analit tidak diganggu oleh adanya senyawa lain dalam sampel. Polimer disintesis dari monomer asam metakrilat (MAA),cross linker
etilen glikol dimetakrilat (EGDMA), inisiator 2,2’-azobis isobutironitril (AIBN) dan asam urat sebagai molekul pencetak (template).
Tujuan penelitian ini adalah menentukan perbandingan mol MAA, EGDMA dan asam urat penyususn polimer yang menghasilkan elektroda termodifikasi dengan kinerja optimum, mempelajari selektivitas elektroda termodifikasi dan menentukan validitas metode analisis. Hasil penelitian ini diharapkan dapat memberikan kontribusi yang bermakna pada perkembangan ilmu pengetahuan khususnya di bidang kimia analitik dan biomedis.
II LANDASAN TEORI
Voltammetri adalah salah satu metode elektroanalisis yang mengukur arus dalam suatu larutan sebagai fungsi potensial terpasang di bawah kondisi elektroda kerja yang terpolarisasi. Elektroda kerja merupakan komponen terpenting dalam metode voltammetri karena sensitivitas, selektivitas dan akurasi metode voltammetri salah satunya ditentukan oleh jenis elektroda kerja yang digunakan. Elektroda kerja yang biasa digunakan dalam voltammetri adalah Au, Pt, GC, grafit, HMD dan
mercury drop (MD) (El-Maali, 2004). Perkembangan teknologi di bidang voltammetri ditandai dengan pengembangan elektroda kerja yaitu dengan cara
memodifikasi elektroda melalui pelapisan senyawa tertentu di permukaan atau mencampur senyawa tertentu pada material elektroda (Wang, 200
Pada penelitian ini dilakukan modifikasi elektroda kerja dengan cara melapiskan polimer cetakan molekul ke permukaan elektroda GC dan HMD secara
electrocoating. Prinsip pembuatan polimer cetakan molekul adalah mereaksikan monomer, cross linker
sehingga terjadi kopolimerisasi antara monomer dan adanya analit target (dalam hal ini adalah asam urat) (template). Setelah terbentuk polimer, kem
jaringan polimer sehingga terbentuk suatu
terlapis pada permukaan elektroda kerja maka hanya molekul asam urat yang dapat berdifusi dan mencapai permukaan elektroda kerja. Dengan demikian modifikasi elektroda yang dilakukan pada penelitian ini akan meningkatkan selektivi
analisis asam urat.
Gambar 2.1
Pembuatan polimer dilakukan secara
non kovalen. Alasan pemilihan cara ini adalah pembentukan polimer sederhana melalui pencampuran monomer,
melalui pendekatan non kovalen sederhana dan cepat karena pada sistem non kovalen, analit berikatan dengan mon
monomer dan template
sedangkan pelepasan (ekstraksi)
serta afinitas sisi ikatan yang dihasilkan lebih tinggi ( 2005).
III METODE PENELITIAN 3.1 Bahan dan Peralatan Penelitian
Bahan kimia yang digunakan pada penelitian ini adalah asam urat (Fluka) asam askorbat (Merck), kreatin monohidrat dan kreatinin (Sigma
memodifikasi elektroda melalui pelapisan senyawa tertentu di permukaan atau mencampur senyawa tertentu pada material elektroda (Wang, 200
Pada penelitian ini dilakukan modifikasi elektroda kerja dengan cara melapiskan polimer cetakan molekul ke permukaan elektroda GC dan HMD secara Prinsip pembuatan polimer cetakan molekul adalah mereaksikan dan molekul target dengan atau tanpa bantuan inisiator, sehingga terjadi kopolimerisasi antara monomer dan cross linking monomer dengan (dalam hal ini adalah asam urat) yang bertindak sebagai cetakan Setelah terbentuk polimer, kemudian molekul target diekstraksi dari jaringan polimer sehingga terbentuk suatu template. Dengan sistem cetakan yang terlapis pada permukaan elektroda kerja maka hanya molekul asam urat yang dapat berdifusi dan mencapai permukaan elektroda kerja. Dengan demikian modifikasi elektroda yang dilakukan pada penelitian ini akan meningkatkan selektivi
Gambar 2.1 Skema reaksi pembentukan cetakan pada polimer
embuatan polimer dilakukan secara bulk polimerization melalui pendekatan . Alasan pemilihan cara ini adalah pembentukan polimer sederhana melalui pencampuran monomer,cross linkerdantemplate. Proses pembuatan polimer melalui pendekatan non kovalen sederhana dan cepat karena pada sistem non berikatan dengan monomer secara sederhana. Interaksi antara
template mudah diperoleh ketika semua komponen dicampur, sedangkan pelepasan (ekstraksi) template dari jaringan polimer mudah dilakukan serta afinitas sisi ikatan yang dihasilkan lebih tinggi (Brüggeman
METODE PENELITIAN Bahan dan Peralatan Penelitian
Bahan kimia yang digunakan pada penelitian ini adalah asam urat (Fluka) sam askorbat (Merck), kreatin monohidrat dan kreatinin
(Sigma-memodifikasi elektroda melalui pelapisan senyawa tertentu di permukaan elektroda atau mencampur senyawa tertentu pada material elektroda (Wang, 2000).
Pada penelitian ini dilakukan modifikasi elektroda kerja dengan cara melapiskan polimer cetakan molekul ke permukaan elektroda GC dan HMD secara Prinsip pembuatan polimer cetakan molekul adalah mereaksikan ekul target dengan atau tanpa bantuan inisiator, monomer dengan yang bertindak sebagai cetakan udian molekul target diekstraksi dari Dengan sistem cetakan yang terlapis pada permukaan elektroda kerja maka hanya molekul asam urat yang dapat berdifusi dan mencapai permukaan elektroda kerja. Dengan demikian modifikasi elektroda yang dilakukan pada penelitian ini akan meningkatkan selektivitas metode
Skema reaksi pembentukan cetakan pada polimer
melalui pendekatan . Alasan pemilihan cara ini adalah pembentukan polimer sederhana Proses pembuatan polimer melalui pendekatan non kovalen sederhana dan cepat karena pada sistem non omer secara sederhana. Interaksi antara mudah diperoleh ketika semua komponen dicampur, dari jaringan polimer mudah dilakukan Brüggeman, 2002; Spivak,
Bahan kimia yang digunakan pada penelitian ini adalah asam urat (Fluka), -Aldrich). Bahan
yang berfungsi sebagai monomer, cross linker dan inisiator berturut-turut adalah asam metakrilat, etilen glikol dimetakrilat dan 2,2’-azobis isobutironitril (Sigma-Aldrich). Bahan kimia lain yang digunakan adalah kloroform, dimetilformamida etanol, amonium asetat, dan asam asetat, natrium hidroksida, asam asetat, natrium asetat, natrium hidrogen fosfat dihidrat dan natrium dihidrogen fosfat dihidrat (Merck). Semua bahan kimia yang digunakan pada penelitian ini berderajat kemurnian pro analisis (p.a). Bahan lain yang digunakan adalah gas N2 (UHP/ultra high pure) dan serum kontrol Precinorm UPX 10186848, sedangkan sampel yang digunakan adalah serum dari pasien salah satu Laboratorium Patologi Klinik di wilayah Surabaya. Air yang digunakan pada penelitian ini adalah UHPwater.
Peralatan yang digunakan pada penelitian ini adalah 797 Voltammetry Computrace (MVA system-1) yang terdiri atas wadah sampel (sel voltammetri) dengan sistem tiga elektroda, pengaduk, processor unit, serta komputer (PC). Elektroda yang digunakan adalah elektroda kerja HMD (d=50 µm) dan GC (BAS MF-2012, d=3 mm), elektroda pembanding Ag/AgCl (KCl 3M) dan elektroda pembantu Pt. Peralatan yang digunakan untuk karakterisasi polimer adalah spektrofotometer FTIR (Shimadzu), SEM (JEOL tipe JSM-6360 JA), dan BET (Quantachrome NovaWin versi 2.1). Jumlah asam urat yang terekstraksi dari jaringan polimer diukur menggunakan high performance liquid chromatrography (HPLC) (Waters tipe DAD).
3.2 Prosedur Penelitian
3.2.1 Sintesis dan karakterisasi polimer
Polimer tanpa cetakan molekul (non imprinting polymer/NIP) disintesis dengan cara mencampurkan monomer, cross linker, dan larutan asam urat dengan perbandingan mol yang bervariasi yaitu 1:3:1; 2:3:1, 3:3:1, 4:3:1, 6:3:1. Polimer dengan komposisi 1:3:1 dibuat dengan cara mencampurkan 0,2153 g MAA (2,5x10-3 mol) dan 1,4868 g EGDMA (7,5x10-3 mol) dalam 10 mL kloroform, kemudian ditambahkan 0,004 g AIBN (2,5x10-5 mol). Campuran diaduk untuk melarutkan AIBN dan dipanaskan di atas hot plate pada suhu 50-60oC selama 10 menit, kemudian ditambahkan 25 mL larutan asam urat 1,0x10-1 M (2,5x10-3 mol) dan diaduk lagi. Pemanasan dilanjutkan sampai terbentuk padatan. Prosedur yang sama dilakukan untuk komposisi 2:3:1, 3:3:1, 4:3:1 dan 6:3:1. PoliMAA-ko-EGDMA disintesis dengan prosedur yang sama dengan polimer tanpa cetakan molekul namun
tanpa penambahan larutan asam urat. Polimer cetakan molekul diperoleh dengan cara melakukan ekstraksi terhadap asam urat dari jaringan polimer menggunakan amonium asetat 1 M (dalam pelarut etanol:asam asetat:air = 40:25:35) (Moral dan Mayes, 2004). Polimer (poliMAA-ko-EGDMA), polimer cetakan molekul dan polimer tanpa cetakan molekul yang telah disintesis kemudian dikarakterisasi menggunakan FTIR untuk melihat gugus fungsi, SEM untuk mengetahui porositas polimer dan adsorpsi-desorpsi N2 (BET) untuk mengetahui luas permukaan spesifik
dan distribusi ukuran diameter pori polimer (Spivak, 2005; Shiet al., 2007).
3.2.2 Modifikasi elektroda GC dan HMD dengan polimer cetakan molekul
Pada penelitian ini dilakukan pelapisan elektroda GC dan HMD dengan cetakan molekul. Pada tahap awal dilakukan optimasi potensial deposisi polimer pada elektroda GC dan optimasi waktu deposisi asam urat pada permukaan elektroda GC-cetakan molekul. Potensial deposisi divariasi dari -0,5 V sampai 1 V, sedangkan waktu deposisi asam urat divariasi mulai 30-150 detik. Potensial deposisi polimer pada permukaan elektroda HMD divariasi dari -1,6 V sampai 1 V, sedangkan waktu deposisi divariasi dari 30-180 detik. Kemudian dilakukan optimasi waktu deposisi asam urat dari 30-150 detik dan pH larutan asam urat divariasi dari 3-8. Polimer yang digunakan untuk optimasi semua parameter adalah polimer yang disintesis dengan perbandingan mol MAA, EGDMA dan asam urat = 1:3:1.
3.2.3 Uji kinerja elektroda termodifikasi
Uji kinerja elektroda GC-cetakan molekul dilakukan terhadap elektroda GC yang dilapisi dengan polimer yang disintesis dengan komposisi 1:3:1 dan 3:3:1. Uji kinerja terhadap elektroda HMD-cetakan molekul dilakukan untuk elektroda HMD yang dilapisi dengan polimer cetakan molekul yang terbuat dengan perbandingan mol MAA, EGDMA dan asam urat 1:3:1; 2:3:1; 3:3:1; 4:3:1; dan 6:3:1.
3.2.4 Pembuatan kurva baku asam urat dan uji validitas metode
Kurva baku asam urat dibuat dengan cara menganalisis larutan baku asam urat konsentrasi 6,0x10-9 M - 3,0x10-8 M menggunakan elektroda GC dan GC-cetakan molekul dan konsentrasi 1,2x10-9M – 6,0x10-10M menggunakan elektroda HMD dan HMD-cetakan molekul. Dari data yang diperoleh dibuat kurva hubungan antara konsentrasi larutan baku asam urat dengan arus yang terukur. Data pembuatan kurva baku ini selanjutnya digunakan untuk uji validitas metode meliputi linieritas,
sensitivitas, presisi (repeatability), dan batas deteksi (limit of detection) (Miller dan Miller, 1988). Uji recovery ditentukan melalui pengukuran konsentrasi asam urat pada larutan serum kontrol.
3.2.5 Uji selektivitas dan aplikasi elektroda termodifikasi
Selektivitas elektroda GC-cetakan molekul dipelajari dengan cara menambahkan asam askorbat pada analisis asam urat dengan variasi perbandingan konsentrasi asam urat dan asam askorbat 1:0,5; 1:1; 1:1,5; 1:2; 1:5; 1:10. Uji selektivitas elektroda HMD-cetakan molekul dipelajari melalui penambahan asam askorbat, kreatin dan kreatinin. Perbandingan konsentrasi asam urat dan matriks yang ditambahkan yaitu 1:0,5, 1:1, 1:2, 1:3, 1:4, dan 1:5. Selanjutnya elektroda termodifikasi cetakan molekul diaplikasikan untuk menganalisis konsentrasi asam urat dalam sampel serum.
IV HASIL PENELITIAN DAN PEMBAHASAN
4.1 Sintesis dan Karakterisasi Polimer cetakan Molekul Asam Urat
Pada penelitian ini polimer untuk pelapis elektroda disintesis dari monomer MAA dan cross linker EGDMA dalam pelarut kloroform. Penambahan senyawa
cross linkerdimaksudkan agar polimer yang terbentuk memiliki struktur yang kokoh. Polimer yang diperoleh dari penelitian ini berupa padatan yang berwarna putih. Reaksi polimerisasi MAA tergolong dalam jenis reaksi radikal, sehingga pada sintesis polimer ditambahkan inisiator pereaksi radikal yaitu AIBN. Perkiraan reaksi polimerisasi radikal MAA ditunjukkan pada Gambar 4.1.
MAA radikal MAA poliMAA
Gambar 4.1 Reaksi polimerisasi MAA
Pada pembentukan polimer cetakan molekul asam urat yang terbuat dari monomer MAA diperkirakan melibatkan ikatan hidrogen. Atom O pada gugus –C=O dalam molekul asam urat membentuk ikatan hidrogen dengan atom H dari gugus – OH dalam molekul MAA sedangkan atom O pada gugus –C=O dari molekul MAA membentuk ikatan hidrogen dengan atom H dari gugus –NH dalam molekul asam urat.
Spektra hasil karakterisasi dengan
poliMAA-ko-EGDMA telah terbentuk melalui ikatan rangkap C=C dari MAA, yang didukung dengan berkurangnya intensitas puncak spektra pada bilangan gelombang 1540 cm-1 (C=C) jika dibandingkan intensitas pada spektra MAA
urat dari jaringan polimer juga telah berhasil dilakukan yang ditandai dengan pengurangan intensitas puncak spektra C=O
dibandingkan dengan polimer tanpa cetakan molekul. juga menunjukkan bahwa
gelombang puncak gugus
tempat terjadinya ikatan hidrogen antara MAA dan asam urat.
(i)
Gambar 4.2 (i) Spektra FTIR dari (a) asam urat, (b) MAA, (c) EGDMA, (d) poliMAA-ko-EGDMA, (e)
cetakan molekul (ii) hasil analisis SEM dari polimer cetakan molekul
Dari hasil analisis
dapat disimpulkan bahwa pori polimer yang terbentuk cukup kecil (kurang dari 1 µm) dan bersifat homogen.
terlihat bahwa polimer yang telah disintesis pada penelitian ini tergolong mesopori. Distribusi ukuran diameter pori terbanyak pada polimer tanpa cetakan molekul adalah 37,71 Å dan pada polimer cetakan molekul
4.2 Modifikasi Elektroda dengan Polimer Cetakan Molekul 4.2.1 Optimasi potensial deposisi dan waktu deposisi
Hasil variasi potensial deposisi polimer ke permukaan elektroda GC menunjukkan bahwa deposisi optimum terjadi pada potensial (E
hasil karakterisasi dengan FTIR (Gambar 4.2.i) menjelaskan
EGDMA telah terbentuk melalui ikatan rangkap C=C dari MAA, yang didukung dengan berkurangnya intensitas puncak spektra pada bilangan gelombang
jika dibandingkan intensitas pada spektra MAA.
gan polimer juga telah berhasil dilakukan yang ditandai dengan pengurangan intensitas puncak spektra C=O pada polimer cetakan molekul, jika dibandingkan dengan polimer tanpa cetakan molekul. Data spektra FTIR
bahwa tidak terjadi pergeseran yang bermakna pada bilangan gelombang puncak gugus –NH (3300 cm-1) dan –C=O (1700 cm-1) yang merupakan tempat terjadinya ikatan hidrogen antara MAA dan asam urat.
(ii)
Spektra FTIR dari (a) asam urat, (b) MAA, (c) EGDMA, (d) EGDMA, (e) polimer cetakan molekul, dan (f) polimer tanpa
(ii) hasil analisis SEM dari polimer cetakan molekul
alisis permukaan polimer menggunakan SEM (Gambar
dapat disimpulkan bahwa pori polimer yang terbentuk cukup kecil (kurang dari 1 µm) dan bersifat homogen. Dari analisis polimer menggunakan adsorpsi
terlihat bahwa polimer yang telah disintesis pada penelitian ini tergolong mesopori. stribusi ukuran diameter pori terbanyak pada polimer tanpa cetakan molekul adalah
dan pada polimer cetakan molekul adalah 38,02 Å.
Modifikasi Elektroda dengan Polimer Cetakan Molekul Optimasi potensial deposisi dan waktu deposisi
variasi potensial deposisi polimer ke permukaan elektroda GC menunjukkan bahwa deposisi optimum terjadi pada potensial (Ed) -0,4 V.
menjelaskan bahwa EGDMA telah terbentuk melalui ikatan rangkap C=C dari MAA, yang didukung dengan berkurangnya intensitas puncak spektra pada bilangan gelombang . Ekstraksi asam gan polimer juga telah berhasil dilakukan yang ditandai dengan pada polimer cetakan molekul, jika Data spektra FTIR tersebut ergeseran yang bermakna pada bilangan ) yang merupakan
Spektra FTIR dari (a) asam urat, (b) MAA, (c) EGDMA, (d) molekul, dan (f) polimer tanpa (ii) hasil analisis SEM dari polimer cetakan molekul
menggunakan SEM (Gambar 4.2.ii) dapat disimpulkan bahwa pori polimer yang terbentuk cukup kecil (kurang dari 1 µm) Dari analisis polimer menggunakan adsorpsi-desorpsi N2
terlihat bahwa polimer yang telah disintesis pada penelitian ini tergolong mesopori. stribusi ukuran diameter pori terbanyak pada polimer tanpa cetakan molekul adalah
variasi potensial deposisi polimer ke permukaan elektroda GC 0,4 V. Pada saat
pemindaian ke arah potensial positif teramati adanya puncak pada potensial Ep=1,966
V (vs Ag/AgCl). Pelapisan polimer pada permukaan elektroda HMD dilakukan pada potensial kerja -1,0 V. Pada potensial terpasang tersebut diperoleh potensial puncak pada -0,423 V. Hal ini menunjukkan bahwa pada saat proses lucutan terjadi reaksi oksidasi dan elektroda berfungsi sebagai anoda. Dengan demikian proses analisis asam urat secara voltammetri pada penelitian ini tergolong dalam voltammetri lucutan anodik. Reaksi deposisi dan lucutan asam urat pada permukaan elektroda disajikan pada Gambar 4.3.
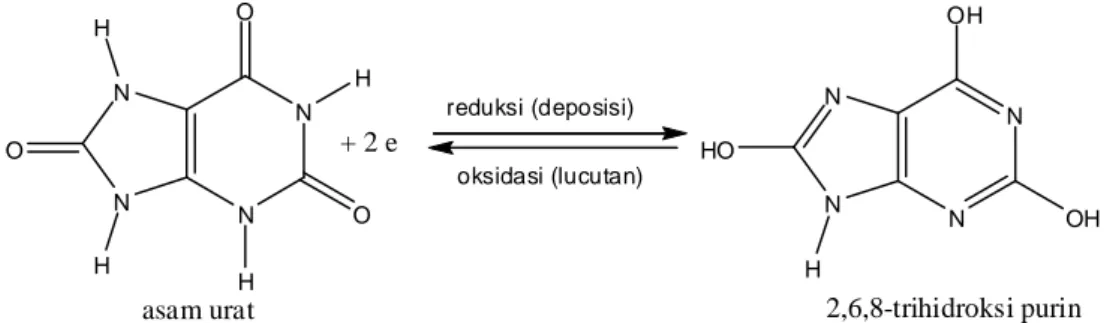
N N N N O O O H H H H asam urat N N N N OH OH HO H +2 e 2,6,8-trihidroksi purin reduksi (deposisi) oksidasi (lucutan)
Gambar 4.3 Reaksi deposisi dan lucutan asam urat pada permukaan elektroda
Beberapa penelitian menyebutkan bahwa puncak oksidasi asam urat menggunakan elektroda padat teramati pada kisaran potensial 0,3-0,6 V (Strochkova
et al., 1997; Zenet al.,1998; Huanget al., 2006, Renet al., 2006; Huanget al., 2010). Tingginya potensial puncak yang diperoleh dari penelitian ini kemungkinan disebabkan oleh adanya respon elektroda terhadap spesi lain yang dihasilkan dari proses kimia asam urat.
Pada potensial tinggi (E > 1,229 V) dimungkinkan terjadinya puncak oksigen dari hasil analisis terhadap larutan bermedia air (aqueous). Oksigen terlarut dalam larutan yang bersifat asam memiliki potensial reduksi sebesar +1,229 V (Bard dan Faulkner, 1980). Oksigen tersebut akan menutupi permukaan elektroda dan menghalangi kontak antara molekul asam urat dengan permukaan elektroda. Namun pada penelitian ini diperoleh hubungan yang linier antara konsentrasi asam urat dengan nilai arus puncak asam urat, sedangkan di sisi lain, besarnya konsentrasi oksigen terlarut adalah tetap. Dengan demikian puncak yang dihasilkan pada potensial tersebut bukan didominasi oleh puncak oksigen. Pada potensial di atas 1,2 V, terjadi reaksi oksidasi irreversibel terhadap elektroda GC dan menghasilkan gugus karbonil (C=O) (Zenet al., 1998). Pada potensial tersebut memungkinkan terjadinya interaksi (ikatan hidrogen) antara gugus C=O hasil dari oksidasi permukaan elektroda
GC dengan gugus –NH dari asam urat. Hal ini menyebabkan asam urat lebih mudah terdeposisi pada permukaan elektroda GC dan menghasilkan respon arus. Namun demikian karena permukaan elektroda GC terlapisi oleh polimer yang memiliki gugus -COOH maka jumlah gugus C=O yang dihasilkan oleh proses oksidasi dari elektroda GC jauh lebih kecil dan diabaikan terhadap jumlah gugus C=O yang berasal dari polimer yang terlapis pada permukaan elektroda GC.
Pada pelapisan elektroda HMD dengan potensial negatif, diperoleh nilai arus yang semakin bertambah dengan semakin negatifnya potensial pelapisan. Namun demikian dari hasil pengamatan secara visual, pada potensial yang lebih kecil dari -1,2 V terjadi pembesaran ukuran tetes merkuri sehingga bertambah besarnya respon arus diyakini disebabkan oleh semakin banyaknya asam urat yang terdeposisi akibat dari semakin luasnya permukaan elektroda HMD. Bertambah besarnya ukuran tetes merkuri ini mempengaruhi stabilitas elektroda, sehingga pada potensial -1,6 V nilai arus yang dihasilkan adalah nol, karena elektroda HMD jatuh (menetes) sebelum terjadi proses lucutan asam urat.
Waktu deposisi adalah waktu yang disediakan untuk terakumulasinya polimer ke permukaan elektroda. Semakin lama waktu deposisi maka akan semakin banyak jumlah polimer yang terlapis pada permukaan elektroda (Wang, 2000). Pelapisan polimer ke permukaan elektroda diharapkan hanya menghasilkan lapisan tunggal (monolayer). Dengan demikian analit akan dengan mudah berdifusi melalui pori polimer menuju ke permukaan elektroda HMD.
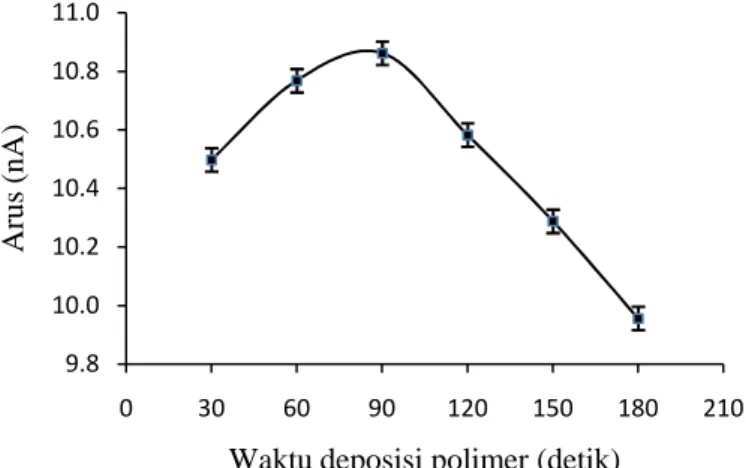
Gambar 4.4 Kurva hubungan antara arus puncak asam urat dan waktu deposisi ke permukaan elektroda HMD
Kurva hubungan antara waktu deposisi polimer ke permukaan elektroda terhadap arus yang terukur (Gambar 4.4) memperlihatkan bahwa perubahan waktu deposisi relatif tidak berpengaruh terhadap arus yang terukur. Namun demikian untuk
9.8 10.0 10.2 10.4 10.6 10.8 11.0 0 30 60 90 120 150 180 210 A ru s (n A )
waktu deposisi 30-90 detik terlihat bahwa semakin lama waktu deposisi menyebabkan kenaikan arus yang terukur. Sebaliknya untuk waktu deposisi di atas 90 detik teramati arus yang terukur semakin mengecil dengan bertambahnya waktu. Fenomena di atas dapat dijelaskan sebagai berikut. Semakin lama waktu pelapisan akan menyebabkan semakin tebal lapisan polimer yang terbentuk (multilayer) pada permukaan elektroda, sehingga pori cetakan asam urat yang terdapat pada lapisan polimer pertama tertutup oleh lapisan berikutnya. Dengan demikian asam urat dalam larutan sulit berdifusi menembus permukaan elektroda (kontak antara asam urat dengan permukaan elektroda HMD terhalang). Pada penelitian ini diambil waktu deposisi 60 detik, dengan pertimbangan efisiensi waktu dan pada waktu deposisi tersebut harga koefisien variasi (presisi) yang diperoleh dari hasil pengulangan pengukuran juga paling kecil.
Hasil penelitian tentang pengaruh pH larutan menunjukkan bahwa terjadi peningkatan nilai arus pada rentang pH 3-5, sedangkan pada pH 6 terjadi penurunan nilai arus secara drastis. Hal ini dapat dijelaskan sebagai berikut. Asam urat memiliki harga pKa sebesar 5,75. Pada larutan yang memiliki pH kurang dari nilai pKa-nya,
asam urat berada dalam bentuk molekul asam urat netral. Pada pH tersebut molekul asam urat dikelilingi oleh proton (H+ dari larutan asam), sehingga akan mudah menuju elektroda HMD yang dikondisikan sebagai katoda. Dengan demikian arus yang teramati tinggi (Zen et al., 1998). Pada pH lebih besar dari 6, asam urat berada dalam bentuk anion dan sebagian kecil berada dalam bentuk spesies tereduksi sebagai 2,6,8-trihidroksi purin (Huang et al., 2010). Anion asam urat tidak dapat menempel pada permukaan elektroda HMD karena terjadi tolakan antara ion urat dan elektroda HMD yang dikondisikan sebagai katoda. Dengan demikian pada pH basa tidak ditemukan arus dan potensial puncak asam urat. Dari data yang diperoleh terlihat bahwa arus mencapai harga maksimum pada pH kerja 4-5.
4.2.2 Uji kinerja elektroda termodifikasi untuk analisis asam urat
Analisis asam urat dengan elektroda murni menghasilkan arus yang terbesar bila dibandingkan dengan menggunakan elektroda yang termodifikasi poliMAA-ko-EGDMA, polimer cetakan molekul maupun polimer tanpa cetakan molekul. Berkurangnya arus yang diperoleh dari analisis asam urat menggunakan elektroda termodifikasi polimer tersebut menandakan bahwa polimer yang terbuat dari monomer MAA bersifat tidak konduktif. Lapisan polimer yang menutupi permukaan
elektroda mengurangi luas area elektroda yang dapat digunakan untuk terdeposisinya asam urat sehingga menurunkan sinyal arus yang terukur saat proses lucutan (Chenet al., 2009). Elektroda GC yang dilapisi dengan polimer tanpa cetakan molekul yang disintesis dengan perbandingan mol 1:3:1 menunjukkan kinerja yang lebih bagus dibandingkan elektroda GC yang dilapisi polimer yang disintesis dengan perbandingan mol 3:3:1.
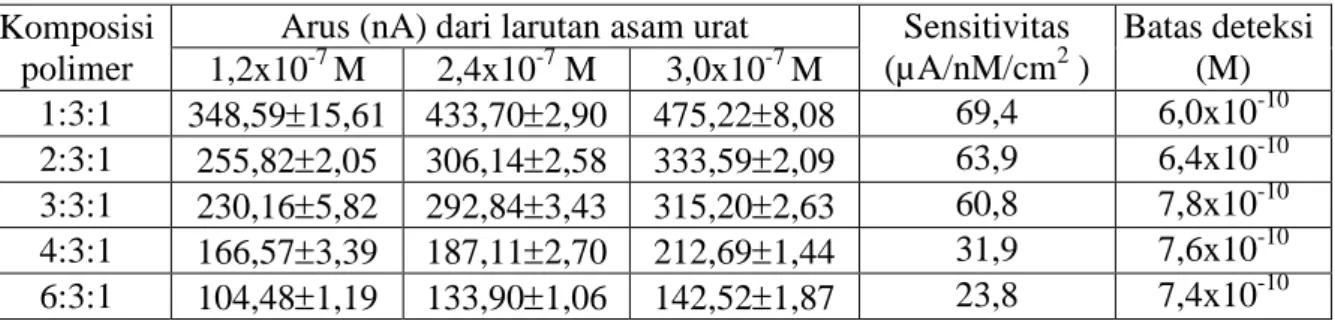
Data pada Tabel 4.1 memperlihatkan bahwa penambahan jumlah monomer (MAA) tidak dapat memperbaiki kinerja polimer yang terbentuk bahkan memperburuk/menurunkan sensitivitas. Hal ini dapat dilihat dari semakin rendahnya arus yang terukur seiring dengan semakin tingginya jumlah monomer. Pada penelitian ini penambahan jumlah monomer tidak diiringi dengan penambahan jumlah cross linker, sehingga penambahan jumlah monomer menyebabkan penurunan perbandingan mol monomer (M) terhadapcross linker(X).
Tabel 4.1 Pengaruh komposisi pembuatan polimer pada hasil analisis asam urat menggunakan elektroda HMD-cetakan molekul
Komposisi polimer
Arus (nA) dari larutan asam urat Sensitivitas (µA/nM/cm2) Batas deteksi (M) 1,2x10-7M 2,4x10-7M 3,0x10-7M 1:3:1 348,5915,61 433,702,90 475,228,08 69,4 6,0x10-10 2:3:1 255,822,05 306,142,58 333,592,09 63,9 6,4x10-10 3:3:1 230,165,82 292,843,43 315,202,63 60,8 7,8x10-10 4:3:1 166,573,39 187,112,70 212,691,44 31,9 7,6x10-10 6:3:1 104,481,19 133,901,06 142,521,87 23,8 7,4x10-10
Keterangan : komposisi polimer = perbandingan mol MAA, EGDMA dan asam urat pada pembuatan polimer, n = 5
Rendahnya perbandingan mol monomer dan cross linker tersebut menyebabkan jaringan polimer yang terbentuk kaku (rigid) dan dapat mempertahankan sifat serta letak sisi ikatan karena hanya sedikit mengalamiswelling
dalam pelarut air (Shi et al., 2007). Di sisi lain, penambahan jumlah monomer tanpa diiringi penambahan jumlahcross linkertidak menyebabkan penambahan jumlah sisi ikatan yang dapat digunakan untuk pengenalan terhadap analit sehingga tidak dapat memperbaiki kinerja analitik elektroda. Dengan turunnya rasio (perbandingan) cross linker dan monomer akan membatasi jumlah monomer yang dapat terikat silang sehingga sisi ikatan pada polimer cetakan molekul yang terbentuk juga turun. Kelebihan jumlah monomer akan menambah jumlah ikatan non-spesifik yang mengakibatkan turunnya sensitivitas dan selektivitas cetakan molekul (Spivak, 2005;
Shi et al., 2007). Dengan demikian, semakin banyak jumlah mol MAA pada sintesis polimer dalam penelitian ini menyebabkan semakin kecilnya sensitivitas elektroda termodifikasi. Polimer yang disintesis dengan perbandingan mol 1:3:1 juga menunjukkan kinerja terbaik sebagai bahan pelapis elektroda HMD.
Ekstraksi asam urat dari jaringan polimer dilakukan dengan cara merendam serbuk polimer di dalam larutan amonium asetat 1 M (dalam asam asetat:metanol:air = 40:25:35) sambil diaduk (Moral dan Mayes, 2004). Percobaan ini dilakukan terhadap polimer yang dibuat dengan perbandingan mol MAA, EGDMA dan asam urat = 1:3:1. Hasil analisis menggunakan kromatografi cair kinerja tinggi (HPLC) menunjukkan bahwa dengan satu kali ekstraksi menggunakan 20 mL amonium asetat 1 M selama 20 menit diperoleh konsentrasi asam urat 2,8x10-4M, sedangkan dengan 4 kali ekstraksi masing-masing dengan 5 mL amonium asetat 1 M selama 5 menit diperoleh konsentrasi asam urat 3,1x10-4 M. Dari hasil tersebut disimpulkan bahwa dengan ekstraksi sebanyak satu kali, sudah cukup memberikan ruang kepada analit asam urat untuk memasuki pori polimer saat analisis secara voltammetri karena konsentrasi asam urat yang digunakan/dianalisis berada pada level nM.
(i) (ii)
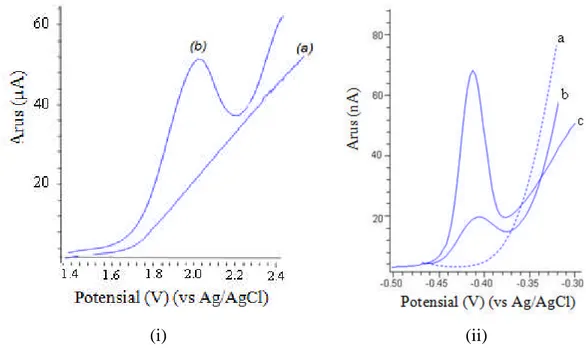
Gambar 4.5 Voltammogram pulsa diferensial hasil analisis larutan (a) blanko,
(b) asam (a) blanko, (b) asam urat 3,0x10-8 M, (c) asam urat 2,4x10-7 M
menggunakan elektroda (i) GC-cetakan molekul dan (ii) HMD-cetakan molekul
Hasil penelitian (Gambar 4.5) menunjukkan bahwa tidak ditemukan puncak voltammogram hasil analisis larutan blanko menggunakan elektroda termodifikasi cetakan molekul, dengan demikian dapat disimpulkan bahwa asam urat yang masih tertinggal di dalam jaringan polimer tidak mengganggu proses analisis karena tidak
memberikan puncak arus. Voltammogram tersebut juga menjelaskan bahwa dengan satu kali ekstraksi terhadap asam urat yang terjebak dalam polimer telah dapat menghasilkan jumlah ruang cetakan yang mencukupi untuk masuknya asam urat dari larutan sampel selama proses analisis.
4.2.3 Kurva baku asam urat
Pengembangan suatu metode analisis dimaksudkan untuk memperbaiki kelemahan metode analisis yang sudah ada dan mendapatkan metode baru dengan kinerja yang lebih bagus. Salah satu kriteria untuk menyatakan bahwa suatu metode itu bagus adalah tingkat validitas metode. Beberapa parameter yang dapat digunakan untuk mengukur validitas metode diantaranya adalah rentang konsentrasi analit yang dapat diukur, sensitivitas, presisi, akurasi dan batas deteksi. Pada penelitian ini telah dilakukan pembuatan kurva baku dari hasil pengukuran arus terhadap sederetan larutan baku asam urat secara voltammetri lucutan.
Elektroda GC Elektroda HMD
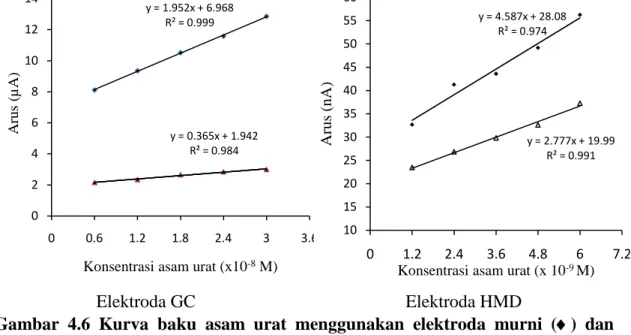
Gambar 4.6 Kurva baku asam urat menggunakan elektroda murni () dan elektroda termodifikasi cetakan molekul ()
Keempat kurva baku pada Gambar 4.6 memiliki nilai intersep (intersep tidak bernilai nol) yang menandakan terjadinya arus latar (non-faradaik) saat analisis. Arus tersebut salah satunya timbul akibat adanya perpindahan muatan partikel secara terus menerus di lingkungan bermuatan listrik (proses migrasi). Arus yang diharapkan terukur pada analisis secara voltammetri adalah arus difusi, yaitu arus yang timbul akibat adanya gradien konsentrasi. Arus migrasi dapat dikurangi dengan penambahan elektrolit pendukung dengan konsentrasi tinggi (100 kali konsentrasi analit). Pada
y = 1.952x + 6.968 R² = 0.999 y = 0.365x + 1.942 R² = 0.984 0 2 4 6 8 10 12 14 0 0.6 1.2 1.8 2.4 3 3.6 A ru s (µ A )
Konsentrasi asam urat (x10-8M)
y = 4.587x + 28.08 R² = 0.974 y = 2.777x + 19.99 R² = 0.991 10 15 20 25 30 35 40 45 50 55 60 0 1.2 2.4 3.6 4.8 6 7.2 A ru s (n A )
penelitian ini digunakan elektrolit pendukung berupa bufer dengan konsentrasi sekitar 10-3M. Bufer tersebut memiliki sifat sebagai elektrolit lemah, sehingga tidak mampu menekan arus migrasi. Arus non-faradaik juga menandakan lambatnya proses reduksi-oksidasi gugus karbonil dari asam urat pada permukaan elektroda (Zen,et al., 1998). Adanya gugus karbonil (polar) pada permukaan elektroda juga dapat meningkatkandouble layer capacitanceyang menyebabkan tingginya arus latar.
4.2.4 Uji selektivitas
Hasil uji selektivitas elektroda GC menunjukkan bahwa keberadaan asam askorbat sedikit menurunkan arus asam urat. Hal ini disebabkan oleh ikut menempelnya asam askorbat di permukaan elektroda GC pada potensial yang dipasang untuk mendeposisikan asam urat (Shahrokhian dan Ghalkhani, 2006). Dengan menggunakan elektroda GC, keberadaan asam askorbat dengan konsentrasi sama dengan asam urat menyebabkan penurunan arus asam urat sebesar 14,20%. Namun jika menggunakan elektroda GC-cetakan molekul hanya menyebabkan penurunan arus sebesar 2,03%. Dengan demikian dapat disimpulkan bahwa elektroda GC-cetakan molekul mempunyai selektivitas yang jauh lebih tinggi daripada elektroda GC. Selektivitas yang tinggi tersebut disebabkan oleh bentuk cetakan pada polimer yang hanya sesuai untuk asam urat.
Pada penelitian ini juga telah dipelajari selektivitas elektroda HMD-cetakan molekul terhadap asam urat melalui penambahan senyawa yang memiliki struktur mirip dengan asam urat yaitu asam askorbat, kreatin dan kreatinin. Analisis asam urat secara voltammetri lucutan menggunakan elektroda HMD-cetakan molekul relatif tidak diganggu oleh asam askorbat. Keberadaan asam askorbat dengan konsentrasi hingga 333 kali konsentrasi asam urat ternyata hanya mampu menurunkan respon arus sebesar 6,5%, sedangkan jika menggunakan elektroda HMD, keberadaan asam askorbat dengan konsentrasi sama dengan asam urat dapat menurunkan respon arus sebesar 24,96%. Hal ini menunjukkan bahwa dengan sistem pelapisan polimer cetakan molekul pada permukaan elektroda, selektivitas elektroda terhadap molekul asam urat menjadi jauh lebih tinggi dibandingkan jika analisis dilakukan menggunakan elektroda HMD. Keberadaan cetakan pada permukaan elektroda HMD hanya cocok dengan struktur analit asam urat yang dianalisis, sehingga keberadaan asam askorbat dengan konsentrasi sangat tinggi sekalipun relatif tidak mempengaruhi analisis asam urat. Dengan sistem HMD-cetakan molekul ini, analisis asam urat
dalam sampel serum dapat dilakukan tanpa gangguan dari asam askorbat karena konsentrasi asam askorbat dalam sampel serum hanya sekitar 45,8 µM atau kira-kira sepersepuluh konsentrasi asam urat (Chenet al., 2010).
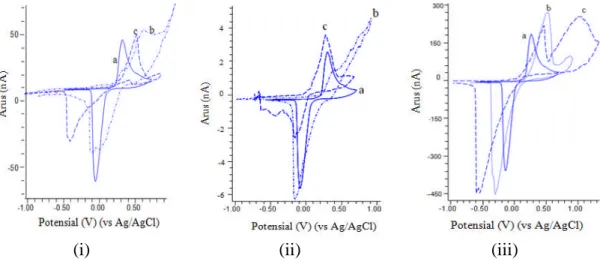
(i) (ii) (iii)
Gambar 4.7 Voltammogram siklis (a) asam urat, (b) matriks (i = asam askorbat, ii = kreatin dan iii = kreatinin), dan (c) campuran asam urat dan matriks
Senyawa lain yang selalu dijumpai dalam serum adalah kreatin dan kreatinin. Keberadaan kreatin nampak menaikkan respon arus pada analisis asam urat menggunakan HMD, tetapi untuk HMD-cetakan molekul kenaikannya tidak signifikan. Kreatin memiliki struktur terbuka yang berbeda dengan struktur asam urat, namun kreatin memiliki gugus –NH dan –COOH yang sebagaimana dimiliki oleh asam urat. Secara perhitungan volume molekul kreatin sedikit lebih kecil jika dibandingkan dengan asam urat. Jika dilihat dari voltammogram siklis Gambar 4.7.ii.b, maka hampir tidak ditemukan puncak anodik pada kreatin dan hanya diperoleh puncak yang landai pada potensial sekitar (Ep) 0,48 V. Dari voltammogram siklis campuran antara asam urat dan kreatin (Gambar 4.7.ii.c) dapat dilihat bahwa terjadi penambahan tinggi puncak asam urat, sedangkan puncak kreatin tidak nampak. Gangguan yang disebabkan oleh kreatin pada analisis asam urat secara voltammetri lucutan menggunakan HMD-cetakan molekul jauh lebih rendah jika dibandingkan menggunakan elektroda HMD ( 5% untuk perbandingan mol asam urat dan kreatin =1:10).
Penambahan kreatinin menyebabkan penurunan respon arus asam urat. Dengan menggunakan elektroda HMD analisis asam urat sangat diganggu oleh kreatinin. Keberadaan kreatinin dengan konsentrasi yang sama dengan konsentrasi asam urat menurunkan respon arus sebesar 15,88%, sedangkan dengan HMD-cetakan molekul keberadaan kreatinin dengan konsentrasi hingga 5 kali konsentrasi
asam urat hanya menurunkan arus sebesar 1,73%. Dengan demikian, elektroda HMD-cetakan molekul terbukti sangat selektif terhadap asam urat yang berada dalam sampel yang mengandung kreatinin.
Secara hipotesis, ukuran (volume) kreatinin juga lebih kecil jika dibandingkan dengan molekul asam urat, sehingga dimungkinkan molekul ini dapat memasuki pori cetakan molekul asam urat. Namun karena muatan formal –NH pada kreatinin berbeda dengan –NH pada asam urat menyebabkan senyawa ini tidak mengganggu analisis asam urat. Berdasarkan strukturnya, kreatinin bersifat basa sehingga pada saat analisis berlangsung, asam urat akan tereduksi lebih dulu dibandingkan kreatinin.
4.2.5 Ujirecoverydan aplikasi elektroda untuk analisis asam urat dalam serum
Pada penelitian ini untuk mengetahuirecoveryasam urat digunakan larutan uji berupa sampel serum untuk elektroda GC-cetakan molekul dan serum kontrol untuk elektroda HMD-cetakan molekul menggunakan teknik kurva baku. Recovery yang diperoleh dari penelitian ini adalah 99,6% untuk elektroda GC-cetakan molekul; 97,6% untuk elektroda HMD dan 89,6% untuk elektroda HMD-cetakan molekul.
Untuk lebih memahami gangguan matriks, selanjutnya dilakukan aplikasi metode untuk analisis asam urat dalam sampel serum menggunakan elektroda HMD dan HMD-cetakan molekul dan hasilnya dibandingkan dengan hasil analisis menggunakan spektrofotometri.
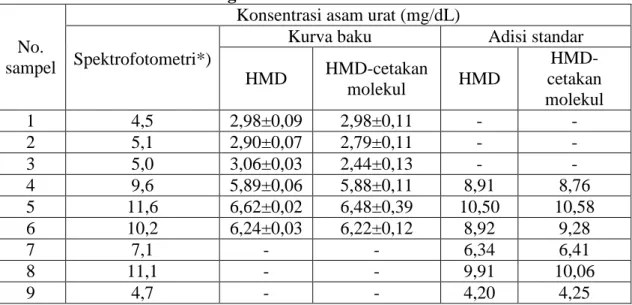
Tabel 4.2 Hasil analisis asam urat dalam sampel serum secara spektrofotometri dan voltammetri lucutan dengan teknik kurva baku
No. sampel
Konsentrasi asam urat (mg/dL) Spektrofotometri*)
Kurva baku Adisi standar HMD HMD-cetakan molekul HMD HMD-cetakan molekul 1 4,5 2,98±0,09 2,98±0,11 - -2 5,1 2,90±0,07 2,79±0,11 - -3 5,0 3,06±0,03 2,44±0,13 - -4 9,6 5,89±0,06 5,88±0,11 8,91 8,76 5 11,6 6,62±0,02 6,48±0,39 10,50 10,58 6 10,2 6,24±0,03 6,22±0,12 8,92 9,28 7 7,1 - - 6,34 6,41 8 11,1 - - 9,91 10,06 9 4,7 - - 4,20 4,25
Data pada Tabel 4.2 menunjukkan bahwa hasil analisis asam urat dalam sampel serum secara voltammetri lucutan dengan teknik kurva baku jauh lebih rendah
dari hasil analisis menggunakan spektrofotometri. Hal ini sekali lagi membuktikan bahwa matriks yang berada dalam sampel serum sangat mengganggu analisis asam urat. Selanjutnya dilakukan uji recovery menggunakan teknik adisi standar. Dengan teknik ini diperolehrecoverysebesar 102,5% untuk elektroda HMD dan 95,7% untuk elektroda HMD-cetakan molekul. Nilai recovery metode analisis asam urat menggunakan HMD-cetakan molekul yang diperoleh secara adisi standar ini jauh lebih bagus jika dibandingkan dengan nilai recovery yang diperoleh menggunakan teknik kurva baku. Hal ini secara jelas menunjukkan adanya gangguan yang berasal dari matriks sampel.
Data Tabel 4.2 menjelaskan bahwa konsentrasi asam urat yang diperoleh dari analisis sampel serum baik menggunakan elektroda HMD maupun HMD-cetakan molekul lebih rendah (sekitar 10%) jika dibandingkan konsentrasi yang diperoleh menggunakan metode spektrofotometri (Hitachi-analyzer) yang selama ini dianggap sebagai metode baku di bidang medis. Penyimpangan tersebut masih dalam batas toleransi yang dapat diterima di dalam metode analisis karena rentang keberterimaan hasil analisis untuk konsentrasi level ppm (10-4 M) adalah 80-110% (Traverniers et al., 2004). Dengan demikian metode analisis asam urat secara voltammetri lucutan yang dikembangkan pada penelitian ini disarankan untuk digunakan sebagai metode alternatif pada analisis asam urat dalam sampel serum di bidang medis.
4.2.6 Perbandingan kinerja elektroda
Dari hasil pembahasan sub bab sebelumnya telah dapat dilihat bahwa elektroda termodifikasi cetakan molekul memberikan kinerja/validitas yang lebih tinggi dibandingkan elektroda tanpa modifikasi. Secara lengkap validitas metode analisis asam urat secara voltammetri lucutan yang dikembangkan ini ditampilkan pada Tabel 4.3.
Jika dibandingkan dengan elektroda GC, metode analisis asam urat menggunakan elektroda GC-cetakan molekul memiliki sensitivitas yang lebih rendah. Hal ini menunjukkan bahwa polimer cetakan molekul yang terbuat dari MAA bersifat tidak konduktif. Jika tebal lapis difusi () adalah 100 µm (Wang, 2000), nilai D yang diperoleh pada analisis menggunakan elektroda GC adalah 1,4x10-6 cm2/detik, sedangkan dengan GC-cetakan molekul adalah 2,6x10-7 cm2/detik. Nilai D yang diperoleh menggunakan elektroda GC-cetakan molekul lebih rendah dari nilai D pada analisis menggunakan elektroda GC maupun elektroda Au termodifikasi
single-walled carbon nanotube (Huang, et al., 2006). Nilai batas deteksi yang diperoleh menggunakan elektroda GC pada penelitian ini jauh lebih kecil jika dibandingkan hasil yang diperoleh dari penelitian sebelumnya (Zareet al., 2005; Lin dan Jin, 2005; Zareet al., 2006; Renet al., 2006; Lin dan Li, 2006; Weiet al., 2006).
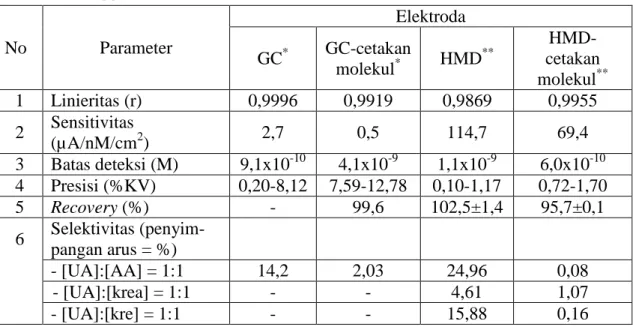
Tabel 4.3 Perbandingan validitas metode analisis asam urat secara voltammetri lucutan menggunakan elektroda berbasis GC dan HMD
No Parameter Elektroda GC* GC-cetakan molekul* HMD ** HMD-cetakan molekul** 1 Linieritas (r) 0,9996 0,9919 0,9869 0,9955 2 Sensitivitas (µA/nM/cm2) 2,7 0,5 114,7 69,4 3 Batas deteksi (M) 9,1x10-10 4,1x10-9 1,1x10-9 6,0x10-10 4 Presisi (%KV) 0,20-8,12 7,59-12,78 0,10-1,17 0,72-1,70 5 Recovery(%) - 99,6 102,5±1,4 95,7±0,1 6 Selektivitas (penyim-pangan arus = %) - [UA]:[AA] = 1:1 14,2 2,03 24,96 0,08 - [UA]:[krea] = 1:1 - - 4,61 1,07 - [UA]:[kre] = 1:1 - - 15,88 0,16 Keterangan :
*) rentang konsentrasi pengukuran =6,0x10-9M sampai 3,0x10-8M **) rentang konsentrasi pengukuran =1,2x10-9M sampai 6,0-10-9M
[UA] =konsentrasi asam urat, [AA] =konsentrasi asam askorbat, [krea] =konsentrasi kreatin, [kre] = konsentrasi kreatinin, - = tidak ditentukan
Dengan mengasumsikan tebal lapis difusi adalah 100 µm, maka nilai D yang diperoleh menggunakan elektroda HMD adalah sebesar 5,2x10-6 cm2/detik. Nilai D yang diperoleh menggunakan elektroda HMD-cetakan molekul ini adalah 2,6x10-6 cm2/detik. Nilai batas deteksi yang diperoleh pada analisis asam urat secara voltammetri lucutan baik menggunakan elektroda HMD maupun HMD-cetakan molekul 105 kali lebih rendah jika dibandingkan dengan nilai batas deteksi yang diperoleh menggunakan metode spektrofotometri yang selama ini digunakan di bidang medis yaitu 1,2x10-5 M. Nilai batas deteksi tersebut juga lebih rendah dari nilai batas deteksi hasil penelitian sebelumnya yang juga menggunakan elektroda termodifikasi cetakan molekul namun dengan monomer yang berbeda (Prasad et al., 2007; Patel et al., 2009; Chen et al., 2010). Begitu pula dengan batas deteksi yang diperoleh menggunakan elektroda GC-cetakan molekul dengan polimer yang sama. Dengan batas deteksi yang sangat rendah ini dapat disimpulkan bahwa metode
voltammetri lucutan menggunakan elektroda HMD-cetakan molekul sangat cocok untuk digunakan pada analisis asam urat dalam sampel serum yang ukuran sampelnya sangat kecil (dalam orde mikroliter).
Presisi suatu metode dikatakan memenuhi syarat keberterimaan jika nilai KV lebih kecil dari 2/3KVHorwitz. Berdasarkan data pada Tabel 4.4, diperoleh presisi yang
memenuhi syarat keberterimaan (KVHorwitz untuk konsentrasi level ppb atau 10-9 M
adalah 45%). Nilairecovery yang diperoleh dari penelitian ini juga memenuhi syarat keberterimaan (recovery untuk konsentrasi 10-4 M adalah 80-110%) (Harmita, 2004; Taverniers,et al., 2004; Workman dan Mark, 2006).
Ditinjau dari waktu yang dibutuhkan untuk sekali analisis sampel serum, metode voltammetri membutuhkan waktu yang relatif lebih pendek dibandingkan metode spektrofotometri. Analisis asam urat dengan metode spektrofotometri membutuhkan waktu sekitar 10 menit, sedangkan dengan metode voltammetri menggunakan elektroda HMD hanya membutuhkan waktu sekitar 2 menit dan dengan elektroda HMD-cetakan molekul membutuhkan waktu sekitar 4 menit. Di sisi lain, metode analisis asam urat secara spektrofotometri membutuhkan pereaksi kimia atau enzim tertentu, dengan demikian membutuhkan biaya yang lebih mahal dibandingkan metode voltammetri. Analisis asam urat secara spektrofotometri membutuhkan sampel yang jauh lebih banyak (skala mL) dibandingkan dengan metode voltammetri (skala L) karena metode voltammetri memiliki batas deteksi 105kali lebih rendah dibandingkan metode spektrofotometri.
4.3 Mekanisme Reaksi yang Terjadi pada Elektroda HMD-Cetakan Molekul
Mekanisme reaksi yang terjadi pada permukaan elektroda HMD-cetakan molekul telah dipelajari dengan cara melakukan analisis asam urat secara voltammetri siklis dengan berbagai nilai laju pindai () yaitu 29,5; 59; 100; 118 dan 129,5 mV/detik. Dari Gambar 4.8 diperoleh informasi bahwa voltammogram siklis asam urat menunjukkan Epa = +300 mV dan Epc +19,0 mV, sehingga harga Ep yang
diperoleh sebesar 281 mV, sehingga reaksi yang terjadi termasuk reaksi tidak reversibel (Ep> 212 mV) (Bard dan Faulkner, 1980; Gosser, 1993). Hubungan linier
antara ipa dengan menggambarkan bahwa proses yang terjadi pada permukaan
Gambar 4.8 Voltammogram siklis asam urat pada berbagai laju pindai
Nilai ipa/ipc pada berbagai laju pindai adalah kurang dari 1. Di sisi lain, kurva
pada Gambar 4.9 menunjukkan bahwa ipa merupakan fungsi 1/2 dan melengkung ke
arah sumbu 1/2. Hal ini menandakan bahwa reaksi yang terjadi pada permukaan elektroda HMD-cetakan molekul adalah reaksi transfer elektron yang diikuti oleh reaksi kimia (EC).
Gambar 4.9 Kurva hubungan antara ipadengan1/2
Dari data Epa dan log v diperoleh gambaran bahwa Epamerupakan fungsi dari
log . Hal ini menjelaskan bahwa reaksi kimia berlangsung semi cepat. Mekanisme reaksi yang terjadi pada permukaan elektroda HMD-cetakan molekul dinyatakan dengan Persamaan 4.1 (Wang, 2000).
y = -0.493x2+ 16.64x - 28.06 R² = 0.995 40 50 60 70 80 90 100 110 4 5 6 7 8 9 10 11 12 ipa (nA ) 1/2
Ox+ ne Red Z (4.1)
Pada saat deposisi, asam urat (Ox) mengalami reduksi menjadi 2,6,8-trihidroksi purin (Red) seperti yang dijelaskan pada Gambar 4.3. Sebagian asam urat yang tereduksi menjadi 2,6,8-trihidroksi purin tersebut berubah menjadi spesies lain (Z) dan pindah dari permukaan elektroda. Reaksi perubahan tersebut berjalan semi cepat, sehingga sebagian 2,6,8-trihidroksi purin lainnya secara reversibel berubah lagi menjadi asam urat saat pemindaian kembali.
V KESIMPULAN DAN SARAN 5.1 Kesimpulan
Dari hasil penelitian dan pembahasan yang telah diuraikan maka dapat diambil beberapa kesimpulan sebagai berikut.
Polimer cetakan molekul yang disintesis dengan perbandingan mol MAA, EGDMA dan asam urat 1:3:1 memberikan kinerja terbaik sebagai bahan pelapis untuk memodifikasi elektroda HMD pada analisis asam urat secara voltammetri lucutan. Hasil karakterisasi terhadap polimer cetakan molekul menunjukkan bahwa ekstraksi asam urat dari jaringan polimer telah berhasil dilakukan. Cetakan molekul memiliki rongga yang homogen dengan ukuran cukup kecil (0,1 µm). Setelah proses ekstraksi asam urat dari jaringan polimer, terjadi sedikit perbedaan distribusi ukuran polimer dari 37,71 Å menjadi 38,02Å.
Polimer yang terbuat dari monomer MAA bersifat non kunduktif. Semakin lama waktu deposisi polimer mengakibatkan turunnya kinerja elektroda termodifikasi. Pelapisan polimer cetakan molekul pada elektroda GC mencapai optimum pada potensial deposisi -0,4 V (vs Ag/AgCl), sedangkan pada elektroda HMD diperoleh potensial kerja -0,8 sampai -1,0 V (vs Ag/AgCl) dengan waktu deposisi masing-masing 60 detik. Waktu deposisi asam urat yang paling baik terjadi selama 60 detik, pada larutan dengan pH 4-5. Semakin lama waktu yang disediakan untuk tahap deposisi asam urat, respon voltammetrik saat lucutan juga semakin tinggi.
Analisis asam urat secara voltammetri lucutan menggunakan elektroda GC-cetakan molekul (komposisi pembuatan polimer 1:3:1) menghasilkan linieritas kurva kalibrasi (r) 0,9919 (rentang konsentrasi 6,0x10-9M – 3,0x10-8M). Sensitivitas yang diperoleh adalah 0,5 µA/nM/cm2, presisi 7,59-12,78% dan batas deteksi 4,1x10-9M, sedangkanrecoverymetode dapat mencapai 99,6% (n=3). Adapun analisis asam urat
secara voltammetri lucutan menggunakan elektroda HMD-cetakan molekul menghasilkan linieritas 0,9955 (rentang konsentrasi 1,2x10-9 M – 6,0x10-9 M). Sensitivitas yang diperoleh adalah 69,4 µA/nM/cm2, presisi 0,72-1,70%, batas deteksi 6,0x10-10M, sedangkan recovery yang diperoleh adalah 95,7% (n=2). Batas deteksi metode analisis asam urat yang diperoleh dari penelitian ini 104-105kali lebih rendah dibandingkan metode spektrofotometri yang biasanya digunakan dalam bidang medis.
Analisis asam urat menggunakan elektroda GC-cetakan molekul relatif tidak diganggu oleh asam askorbat. Di sisi lain, keberadaan asam askorbat, kreatin dan kreatinin juga tidak mengganggu analisis asam urat menggunakan elektroda HMD-cetakan molekul. Analisis asam urat dalam sampel serum menggunakan elektroda GC-cetakan molekul dan HMD-cetakan molekul secara umum memberikan hasil sedikit lebih rendah dibandingkan hasil analisis menggunakan metode spektrofotometri.
5.2. Saran
Berdasarkan hasil penelitian ini maka diajukan saran sebagai berikut.
1. Dilakukan penelitian tentang pelapisan elektroda GC dan HMD dengan polimer konduktif untuk analisis asam urat secara voltammetri lucutan agar diperoleh sinyal arus yang lebih tinggi.
2. Dilakukan penelitian pengaruh senyawa lain yang terdapat dalam serum selain asam askorbat, kreatin dan kreatinin pada analisis asam urat secara voltammetri lucutan menggunakan elektroda GC dan HMD termodifikasi cetakan molekul.
DAFTAR PUSTAKA
Bard, A.J. and Faulkner, L.R., 1980, Electrochemical Methods: Fundamentas and Applications, John Wiley and Sons, New York.
Brüggeman, O., 2002, Molecularly imprinted materials – receptors more durable than nature can provide, Advanced in Biochemistry Engineering/Biotechnology, Springer Verlag, Germany.
Carsol, M-A., Volpe, G. and Mascini, M., 1997, Amperometric detection of uric acid and hypoxanthine with xanthine oxidase immobilized and carbon paste screen-printed electrode. Aplication for fish freshness determination,Talanta, 44, 2151-2159.
Chen, J.C., Chung, H.H., Hsu, C.T., Tsai, D.M., Kumar, A.S. and Zen, J.M., 2005, A disposable single-use electrochemical sensor for the detection of uric acid in human whole blood,Sens. ActuatorsB, 110, 364-369.
Chen, P., Nien, P., Wu, T., Lin, C. and Ho, K., 2009, Fabrication of molecularly imprinted polymer by self-assembling monolayer mediator system,Anal. Chim. Acta, 643, 38-44.
Chen, P., Vittal, R., Nien, P., Liou, G. and Ho, K., 2010, A novel molecularly imprinted polymer thin film as biosensor for uric acid,Talanta, 80, 1145-1151. El-Maali, N. A., 2004, Voltammetric analysis of drugs,Biochemistry, 64, 99-107. Gosser, D.K., 1993, Cyclic Voltammetry: Simulation and Analysis of Reaction
Mechanisms, VCH Publisher Inc, New York.
Harmita, 2004, Petunjuk pelaksanaan validasi metode dan cara perhitungannya,
Majalah Ilmu Kefarmasian, 1 (3), 117-135.
Huang, X, Im H., Yarimaga, O., Kim, J., Lee, D., Kim, H. and Choi, Y., 2006, Direct Electrochemistry of uric acid at chemically assembled carboxylated single-walled carbon nanotubes netlike electrode,J. Phys. Chem. B, 110, 21850-21856. Huang, S., Liao, H. and Chen, D., 2010, Simultaneous determination of
norepinephrine, uric acid, and ascorbic acid at a screen printed carbon electrode modified with polyacrylic acid-coated multi-wall carbon nanotubes, Biosens. Bioelectron., 25, 2351-2355.
Khasanah, M., Supriyanto, G., Handajani, U.S., Fitriana, M. and Asmaningrum, W., 2007, Analysis of uric acid in urine and serum with voltammetry stripping using hanging mercury drop electrode,Proceeding of ICOWOBAS,Unair, Surabaya, p. 307-311.
Lin, X. and Li, Y, 2006, Monolayer covalent modification of 5-hydroxytryptophan on glassy carbon electrode for simultaneous determination of uric acid and ascorbic acid,Electrochim. Acta, 51, 5794-5801.
Lin, X. and Jin, G., 2005, Monolayer modification on glassy carbon electrode by using propionylcholine for selective detection of uric acid, Electrochim. Acta, 50, 3210 – 3216.
Luo, J.W., Zhang, M. and Pang, D.W, 2005, Selective and sensitive determination of uric acid at DNA-modified graphite powder microelectrodes, Sens. ActuatorsB, 106, 358-362.
Matos, R.C., Augelli, M.A., Lago, C.L. and Angnes, L., 2000, Flow injection analysis-amperometric determination of ascorbic and uric acids in urine using arrays of gold microelectrodes modified by electrodeposition of palladium,Anal. Chim. Acta, 404, 151-157.
Miller, J.C. and Miller, J. N., 1988, Statistics for Analytical Chemistry, 3rd edition, Ellis Horwood Ltd., New York.
Moral, N.P. and Mayes, A.G., 2004, Comparative study of imprinted polymer particles prepared by different polymerisation methods, Anal. Chim. Acta, 504, 15-21.
Patel, A.K., Sharma, P.S. and Prasad, B.B., 2009, Electrochemical sensor for uric acid based on a molecularly imprinted polymer brush grafted to tetraethoxysilane derived sol-gel thin film graphite electrode, Mater. Sci. Eng. C, 29 (5), 1545-1553.
Prasad, B.B., Sharma, P.S. and Lakshmi, D., 2007, Molecularly imprinted based solid-phase extraction combined with molecularly imprinted polymer-based sensor for detection of uric acid,J. Chromatogr. A, 1173, 18–26.
Ren, W., Luo, H. Q. and Li, N.B., 2006, Simultaneous voltammetric measurement of ascorbic acid, epinephrine and uric acid at glassy carbon electrode modified with caffeic acid,Biosens. Bioelectron.,21, 1086-1092.
Shahrokhian, S. and Ghalkhani, M., 2006, Simultaneous voltammetric detection of ascorbic acid and uric acid at a carbon-paste modified electrode incorporating thionine-nafion ion-pair as an electron mediator, Electrochim. Acta, 51, 2599-2606.
Shi, X., Wu, A., Qu, G., Li, R. and Zhang, D., 2007, Development and characterisation of MIP based on MAA for selective recognition of drug,
Biomaterials, 28, 3731-3749.
Spivak, D.A., 2005, Optimization, evaluation an characterization of molecularly imprinted polymers,Advanced Drug Delivery Reviews, 57, 1779-1794.
Strochkova, E.M., Tur’yan, Ya.I., Kuselman, I., and Shenhar, A., 1997, Simultaneous voltammetric determination of uric and ascorbic acid in urine,Talanta, 44, 1923-1928.
Traverniers, I., De Loose, M., and Van Bockstaele, E., 2004, Trends in quality in the analytical laboratory. II. Analytical method validation and quality assurance,
Trends Anal. Chem., 23 (8), 535-552.
Wang, J., 2000,Analitical Electrochemistry, Wiley-VCH, Canada.
Wei, Y., Li, M., Jiao, S., Huang, Q, Wang, G and Fang, B., 2006, Fabrication of CeO nanoparticles modified glassy carbon electrode and its application for electrochemical determination of uric acid and ascorbic acid simultaneously, Electrochim. Acta, 52, 766-772.
Workman, J.Jr. and Mark, H., 2006, Limitation in analytical accuracy, part I: Horwitz’s trumpet,Spectroscopy, 21 (9), 18-24.
Zare, H.R., Memarzadeh, F., Ardakani, M.M., Namazian, M. and Golabi, S.M., 2005, Norepinephrine-modified glassy carbon electrode for simultaneous determination of ascorbic acid and uric acid,Electrochim. Acta, 50, 3495-3502. Zare, H.R., Rajabzadeh, N., and Ardakani, M.M., 2006, Voltammetric studies of an
oracet blue modified glassy carbon electrode and its application for the simultaneous determination of dopamine, ascorbic acid and uric acid, J. Electroanal. Chem., 589, 60 – 69.
Zen, J. and Hsu, C., 1998, A selective voltammetric method for uric acid detection at Nafion-coated carbon paste electrode,Talanta,4, 1363-1369.
Zen, J., Jou, J. and Ilangovan, G., 1998, Selective voltammetric method for uric acid detection using pre-anodized Nafion-coated glassy carbon electrodes, Analyst, 123, 1345-1350.