PENGARUH pH DAN RASIO COD:N
DENGAN BAHAN BAKU LIMBAH INDUSTRI ALKOHOL (VINASSE)
Gita Khaerunnisa (L2C009027) dan Ika Rahmawati (L2C009090)
Jurusan Teknik Kimia, Fakultas Teknik, Universitas Diponegoro
Jln. Prof. H. Soedarto, S.H.,
Pembimbing: Dr. Ir. Budiyono, M. Si
Limbah industri etanol, yaitu vinasse merupakan salah satu sumber yang berpotens
menjadi biogas. Penelitian ini dilakukan untuk mengkaji potensi limbah vinasse dan perbandingan nutrisi yang dibutuhkan untuk mendapatkan biogas dengan hasil yang optimum.
dalam digester volume 5L, dioperasikan pada suhu kamar dan pH netral dengan me perbandingan COD:N 800:7,
vinasse, rumen, serta NH4HCO
pengaruh pH, perbandingan COD:N dan penggunaan nutrisi
yang optimum dalam menghasikan biogas adalah pada pH 7 atau hanya dilakukan penetralan di awal. Produksi biogas optimum dihasilkan pada perbandingan
(0,96 ml biogas/mg TS COD)
TS COD) pada campuran vinasse, rumen, NH NH4HCO3 menghasilkan biogas lebih banyak dib
Kata kunci: biogas; COD:N
Industrial waste ethanol, which
was conducted to assess the potential of biogas with optimum results
temperature and neutral pH mixture, rumen, urea and vinasse
taken from this research are influence of pH, ratio of COD:N and nutrition to biogas production. The optimum condition of pH in producing biogas is at 7.
ratio of COD: N: P 800:7 is equal to
rumen, urea and 3839 ml (13,73 ml biogas/mg due to the comparison easier
and NH4HCO3 produces more maintain the pH range so that
Key Words: biogas; COD:N
1. Pendahuluan
Seiring dengan krisis energi di dunia, banyak penelitian dapat terbarukan (renewable resources
tebu (sugar cane) yang mendorong cukup banyaknya industri gula dan industri etanol. Industri
berkembang di Indonesia. Namun, yang menjadi permasalahan baru adalah limbah yang dihasilkan dari produksi etanol.
Limbah vinasse merupakan limbah hasil penyulingan yang memiliki daya polusi tinggi dan nilai pemupukan yang tinggi. Kekuatan po
organik dan memiliki BOD (Biological Oxygen Demand
karena itu, limbah vinasse ini tidak dapat langsung dibuang ke lingkungan karen atau pengurangan kadar logam dan nonorganik pada limbah vinasse tersebut.
PENGARUH pH DAN RASIO COD:N TERHADAP PRODUKSI BIOGAS
DENGAN BAHAN BAKU LIMBAH INDUSTRI ALKOHOL (VINASSE)
Gita Khaerunnisa (L2C009027) dan Ika Rahmawati (L2C009090)
Jurusan Teknik Kimia, Fakultas Teknik, Universitas Diponegoro
S.H., Tembalang, Semarang, 50239, Telp/Fax: (024)7460058
Pembimbing: Dr. Ir. Budiyono, M. Si
Abstrak
Limbah industri etanol, yaitu vinasse merupakan salah satu sumber yang berpotens
. Penelitian ini dilakukan untuk mengkaji potensi limbah vinasse dan perbandingan nutrisi yang dibutuhkan untuk mendapatkan biogas dengan hasil yang optimum. Percobaan dilakukan dalam digester volume 5L, dioperasikan pada suhu kamar dan pH netral dengan me
800:7, 900:7, 1000:7 pada campuran vinasse, rumen, urea dan juga campuran HCO3 dalam waktu 30hari. Respon yang diambil pada penelitian ini adalah pengaruh pH, perbandingan COD:N dan penggunaan nutrisi terhadap produksi biogas. Kondisi pH yang optimum dalam menghasikan biogas adalah pada pH 7 atau hanya dilakukan penetralan di
Produksi biogas optimum dihasilkan pada perbandingan COD:N 800:7 yaitu sebesar ) pada campuran vinasse, rumen, urea dan 3839 ml (
pada campuran vinasse, rumen, NH4HCO3. Sementara campuran vinasse, rumen, serta menghasilkan biogas lebih banyak dibanding campuran vinasse, rumen dan
COD:N; vinasse; urea; NH4HCO3
Abstract
which vinasse is one potential source to be processed into
the potential of vinasse waste and comparison nutrients needed results. Experiments conducted in the digester volume 5L
pH by varying the ratio of COD: N: P 800:7, 900:7, vinasse mixture , rumen, and NH4HCO3 within 30 days
taken from this research are influence of pH, ratio of COD:N and nutrition to biogas production. The optimum condition of pH in producing biogas is at 7. Production of biogas produced at the
is equal to 280 ml (0,96 ml biogas/mg TS COD) in a mixture of 13,73 ml biogas/mg TS COD) in a mixture of vinasse
easier bacteria decompose organic compounds. While vinasse more biogas than vinasse mixture, rumen, urea may be so that the bacteria can survive.
COD:N; vinasse; urea; NH4HCO3
Seiring dengan krisis energi di dunia, banyak penelitian dilakukan untuk mencari energi alternatif yang renewable resources). Indonesia memiliki banyak keanekaragaman hayati, di antaranya adalah tebu (sugar cane) yang mendorong cukup banyaknya industri gula dan industri etanol. Industri
berkembang di Indonesia. Namun, yang menjadi permasalahan baru adalah limbah yang dihasilkan dari produksi
Limbah vinasse merupakan limbah hasil penyulingan yang memiliki daya polusi tinggi dan nilai pemupukan yang tinggi. Kekuatan polusinya mencapai 100 kali lebih kuat daripada limbah domestik, kaya bahan
Biological Oxygen Demand) dan COD (Chemical Oxygen Demand
karena itu, limbah vinasse ini tidak dapat langsung dibuang ke lingkungan karena rendahnya kemampuan degradasi atau pengurangan kadar logam dan nonorganik pada limbah vinasse tersebut. Beberapa peneliti terdahulu telah
1
TERHADAP PRODUKSI BIOGAS
DENGAN BAHAN BAKU LIMBAH INDUSTRI ALKOHOL (VINASSE)
Gita Khaerunnisa (L2C009027) dan Ika Rahmawati (L2C009090)
Jurusan Teknik Kimia, Fakultas Teknik, Universitas Diponegoro
Tembalang, Semarang, 50239, Telp/Fax: (024)7460058
Limbah industri etanol, yaitu vinasse merupakan salah satu sumber yang berpotensi untuk diolah . Penelitian ini dilakukan untuk mengkaji potensi limbah vinasse dan perbandingan Percobaan dilakukan dalam digester volume 5L, dioperasikan pada suhu kamar dan pH netral dengan memvariasikan pada campuran vinasse, rumen, urea dan juga campuran Respon yang diambil pada penelitian ini adalah terhadap produksi biogas. Kondisi pH yang optimum dalam menghasikan biogas adalah pada pH 7 atau hanya dilakukan penetralan di yaitu sebesar 280 ml (13,17 ml biogas/mg . Sementara campuran vinasse, rumen, serta anding campuran vinasse, rumen dan urea.
be processed into biogas. This study nutrients needed to obtain 5L, operated at room , 1000:7 on vinasse 30 days. Respons which taken from this research are influence of pH, ratio of COD:N and nutrition to biogas production. The produced at the optimum a mixture of vinasse, vinasse, rumen, NH4HCO3
vinasse mixture, rumen, be due NH4HCO3 to
dilakukan untuk mencari energi alternatif yang Indonesia memiliki banyak keanekaragaman hayati, di antaranya adalah tebu (sugar cane) yang mendorong cukup banyaknya industri gula dan industri etanol. Industri-industri ini cukup berkembang di Indonesia. Namun, yang menjadi permasalahan baru adalah limbah yang dihasilkan dari produksi
Limbah vinasse merupakan limbah hasil penyulingan yang memiliki daya polusi tinggi dan nilai lusinya mencapai 100 kali lebih kuat daripada limbah domestik, kaya bahan Chemical Oxygen Demand) yang tinggi. Oleh a rendahnya kemampuan degradasi Beberapa peneliti terdahulu telah
melakukan penelitian yang berkaitan dengan pembuatan biogas, di antaranya Cortella dan da Porto (2002) melakukan penelitian pemurnian etanol dengan mengaplikasikan McCabe
dirancang dengan menggunakan 10 tray untuk mendapatkan etanol 80% berat. Stampe dkk. (1983) melakukan penelitian yang mempelajari konsumsi energi pada farm
kolom bagian stripping pada 94,4oC, 95
(2010) melakukan penelitian yang bertujuan untuk mempelajari performa dari biore
Sludge Blanket) untuk mengkonversi limbah cair vinasse menjadi biogas dan material Bioreaktor diinokulasi dengan 4 L lumpur aktif dari biorea
Dari penelitian terdahulu, metode yang digunakan memerlukan investasi yang besar. Oleh karena itu diperlukan kombinasi metode yang efektif dan murah untuk menangani limbaah
karakteristik dari limbah tersebut.
Penelitian ini dilakukan untuk me
optimum serta untuk mengetahui biogas yang dihasilkan setiap harinya.
2. Bahan dan Metode Penelitian
Bahan yang digunakan dalam penelitian ini adalah vinasse, rumen, urea, Vinasse didapatkan dari Desa bekonang, Solo, Jawa Tengah.
Alat yang digunakan pada p
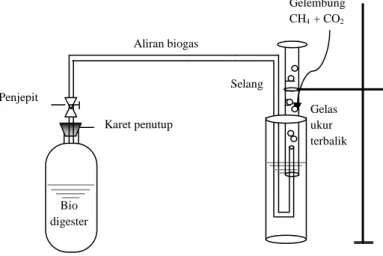
Gambar 1. Gambar Rangkaian Alat
Penetralan pH dilakukan dengan menambahkan larutan NaOH 1N dan pengukuran pH dilakukan dengan menggunakan pH meter elektrik. Pengukuran biogas dilakukan setiap 2 hari sekali.
3. Hasil dan Pembahasan
a. Pengaruh pH terhadap Produksi Biogas Penjepit Bio digester Selang Aliran biogas Karet penutup 0 50 100 150 200 250 300 350 0 10 20 A k u m u la si P ro d u k si B io g a s (m l) Hari ke COD:N 800:7 pH 7 COD:N 1000:7 pH 7 COD:N 900:7 pH kontrol
melakukan penelitian yang berkaitan dengan pembuatan biogas, di antaranya Cortella dan da Porto (2002) elitian pemurnian etanol dengan mengaplikasikan McCabe-Thiele pada kolom distilasi yang dirancang dengan menggunakan 10 tray untuk mendapatkan etanol 80% berat. Stampe dkk. (1983) melakukan penelitian yang mempelajari konsumsi energi pada farm-scale distillation, dengan cara menghitung suhu, pada C, 95 oC dan 95,6oC serta menghitung energi yang dibutuhkan. Soeprijanto dkk. (2010) melakukan penelitian yang bertujuan untuk mempelajari performa dari bioreaktor UASB (Upflow
Sludge Blanket) untuk mengkonversi limbah cair vinasse menjadi biogas dan material
Bioreaktor diinokulasi dengan 4 L lumpur aktif dari bioreaktor UASB. Bioreaktor ini dioperasikan pada volume 9 L. tode yang digunakan memerlukan investasi yang besar. Oleh karena itu diperlukan kombinasi metode yang efektif dan murah untuk menangani limbaah vinasse dengan terlebih dahulu mempelajari
Penelitian ini dilakukan untuk mengetahui pH dan perbandingan nutrisi terbaik untuk menghasilkan biogas optimum serta untuk mengetahui biogas yang dihasilkan setiap harinya.
Bahan dan Metode Penelitian
Bahan yang digunakan dalam penelitian ini adalah vinasse, rumen, urea, NH4HCO Vinasse didapatkan dari Desa bekonang, Solo, Jawa Tengah.
Alat yang digunakan pada penelitian ini dapat digambarkan secara umum seperti pada gambar berikut:
Gambar 1. Gambar Rangkaian Alat
Penetralan pH dilakukan dengan menambahkan larutan NaOH 1N dan pengukuran pH dilakukan dengan Pengukuran biogas dilakukan setiap 2 hari sekali.
Pengaruh pH terhadap Produksi Biogas Selang Gelas ukur terbalik Gelembung CH4 + CO2
Percobaan dilakukan dalam digester volume 5L dan dioperasikan pada suhu kamar dengan memvariasikan perbandingan
dilakukan pada 12 tangki. Tangki 1, 2, 3 berisi vinasse, rumen, dan urea dengan perbandingan COD:N sebesar 800:7, 900:7
pH awal 7. Tangki 4, 5, 6 berisi vinasse, rumen, dan urea dengan perbandingan
900:7, serta 1000:7 dengan pH awal 7 dan setiap empat hari sekali digester tersebut akan dibuka untuk dilakukan penetralan pH. Tangki 7, 8, 9 berisi vinasse, rumen, serta buffer NH
perbandingan COD:N sebesar 1000:7 dengan pH awal 7.
12 berisi vinasse, rumen, serta buffer NH dengan perbandingan COD:N
serta 1000:7 dengan pH awal 7 dan setiap empat hari sekali digester tersebut akan dibuka untuk dilakukan penetralan pH. 20 30 40 Hari ke-COD:N 900:7 pH 7 COD:N 800:7 pH kontrol COD:N 1000:7 pH kontrol
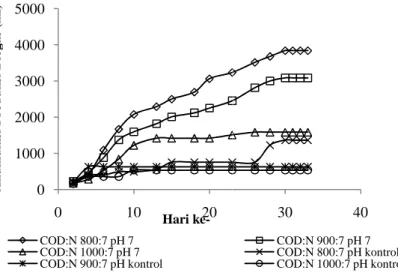
Gambar 2 menunjukkan pengaruh pH terhadap produksi biogas pada campuran vinasse
tambahan sumber Volume biogas yang campuran vinasse
tidak dinetralkan lebih banyak dibandingkan biogas dar dinetralkan. Volume biogas drastis pada hari ke
setelah itu akumulasinya konstan sudah tidak terbentuk biogas.
Gambar 2
produksi biogas dalam waktu 30 hari. Pada gambar dapat dilihat, bahwa biogas paling banyak diproduksi apabila menggunakan pH yang dinetralkan hanya pada awal reaksi saja.
2
melakukan penelitian yang berkaitan dengan pembuatan biogas, di antaranya Cortella dan da Porto (2002) Thiele pada kolom distilasi yang dirancang dengan menggunakan 10 tray untuk mendapatkan etanol 80% berat. Stampe dkk. (1983) melakukan lation, dengan cara menghitung suhu, pada C serta menghitung energi yang dibutuhkan. Soeprijanto dkk. ktor UASB (Upflow Anaerobic Sludge Blanket) untuk mengkonversi limbah cair vinasse menjadi biogas dan material-material sederhana. tor UASB. Bioreaktor ini dioperasikan pada volume 9 L. tode yang digunakan memerlukan investasi yang besar. Oleh karena itu diperlukan dengan terlebih dahulu mempelajaringetahui pH dan perbandingan nutrisi terbaik untuk menghasilkan biogas
HCO3, NaOH, dan aquades.
enelitian ini dapat digambarkan secara umum seperti pada gambar berikut:
Penetralan pH dilakukan dengan menambahkan larutan NaOH 1N dan pengukuran pH dilakukan dengan Percobaan dilakukan dalam digester volume 5L dan dioperasikan pada suhu kamar dengan memvariasikan perbandingan COD:N yang dilakukan pada 12 tangki. Tangki 1, 2, 3 berisi rumen, dan urea dengan perbandingan 900:7, serta 1000:7 dengan pH awal 7. Tangki 4, 5, 6 berisi vinasse, rumen, dan urea dengan perbandingan COD:N sebesar 800:7, dengan pH awal 7 dan setiap empat hari sekali digester tersebut akan dibuka untuk dilakukan penetralan pH. Tangki 7, 8, 9 berisi vinasse, rumen, serta buffer NH4HCO3 dengan sebesar 800:7, 900:7, serta dengan pH awal 7. Sedangkan tangki 10, 11, 12 berisi vinasse, rumen, serta buffer NH4HCO3
COD:N sebesar 800:7, 900:7, dengan pH awal 7 dan setiap empat hari sekali digester tersebut akan dibuka untuk
menunjukkan pengaruh terhadap produksi biogas pada
vinasse dan rumen dengan tambahan sumber nitrogen dari urea. Volume biogas yang dihasilkan dari vinasse, rumen dan urea yang dinetralkan lebih banyak kuantitasnya ogas dari campuran yang Volume biogas meningkat drastis pada hari ke-8 dan ke-10, namun akumulasinya konstan karena sudah tidak terbentuk biogas.
Gambar 2 menunjukkan akumulasi iogas dalam waktu 30 hari. Pada dilihat, bahwa biogas paling diproduksi apabila menggunakan etralkan hanya pada awal
Gambar 2 Grafik pengaruh pH terhadap produksi biogas pada campuran vinasse, rumen dan urea
Sedangkan produksi biogas
yang dinetralkan tiap empat hari. Biogas yang dihasilkan pada kondisi biogas/mg TS COD.
Sebagaimana diketahui bahwa salah satu tahap dalam dekomposisi bahan organik anaerobik adalah tahap asidogenesis dan asetogenesis. Pada tahap ini terbentuk asam lemak volatil yang akan menurunkan pH dalam reaktor. Keseluruhan proses anaerobik terjadi pada
peka terhadap pH, tetapi pH dalam reaktor tidak harus dikendalikan secara ketat.
Pengaturan pH dapat dilakukan dengan menjaga umpan tidak terlalu asam serta mengendalikan jumlah
pencampuran agar kesetimbangan reaksi antara tahap asidogenik dan metanogenik terjaga dengan baik. Pada kondisi tanpa bantuan penyeimbang pH, maka pada nilai pH dibawah 6 aktivitas bakteri metan akan mulai terganggu dan bila mencapai 5,5 aktivitas bakterial akan terhenti sam
dipengaruhi oleh jumlah asam lemak volatil (VFA), ammonia, CO dihasilkan.
Faktor pH sangat berperan pada dekomposisi anaerob karena pada rentang pH yang tidak se
tidak dapat tumbuh dengan maksimum dan bahkan dapat menyebabkan kematian. Pada akhirnya kondisi ini dapat menghambat perolehan gas metana. Derajat keasaman yang optimum bagi kehidupan mikroorganisme adalah 6,8 7,8 (Simamora dkk, 2006).
Pertumbuhan bakteri penghasil gas metana akan baik
sampai 7. Nilai pH terbaik untuk suatu digester yaitu sekitar 7,0. Apabila nilai pH di bawah 6,5, maka aktivitas bakteri metanogen akan menurun dan apabila nil
Darwis, 1990). Bila proses fermentasi berlangsung dalam
otomatis berkisar antara 7 – 8,5. Jika pH lebih tinggi dari 8,5 akan mengakibatkan pengar populasi bakteri metanogen, sehingga akan mempengaruhi laju pembentukan biogas dalam reaktor.
Pada botol 4, 5, 6, 10, 11, dan 12, campuran dinetralkan mencapai pH 7 dan akan dinetralkan kembali setiap empat hari sekali. Sedangkan 6 bot
penetralan pH selama penelitian.
Pengolahan limbah secara biologis dibedakan menjadi dua proses, yaitu proses aerobik dan proses anaerobik. Pada proses aerobik, berlangsungnya proses
proses anaerobik justru sebaliknya karena oksigen akan menghambat jalannya proses.
Di dalam reaktor biogas, terdapat dua jenis bakteri yang sangat berperan, yakni bakteri asidogenik dan bakteri metanogenik. Kedua jenis bakteri ini perlu eksis dalam jumlah yang berimbang. Bakteri
memanfaatkan bahan organik dan memproduksi metan dan gas lainnya dalam siklus hidupnya pada kondisi anaerob. Mereka memerlukan kondisi tertentu dan sensitif terhada
keasaman dan jumlah material organik yang akan dicerna. Terdapat beberapa spesies metanogenik dengan berbagai karateristik. Bakteri ini mempunyai beberapa sifat fisiologi yang umum, tetapi mempunyai morf
seperti Methanomicrobium, Methanosarcina
Pada tahap pembentukan gas metana, bakteri yang berperan adalah bakteri metanogenesis. Bakteri metanogenesis akan memanfaatkan hasil dari tahap kedu
Gambar 3 menunjukkan pengaruh pH terhadap produksi biogas pada campuran vinasse dan rumen dengan tambahan sumber nitrogen dari NH4HCO3. Dari gambar dapat diketahui bahwa volume biogas dengan pH 7, akumulasi volumenya lebih banyak daripada biogas yang dihasilkan dari campuran yang dinetralkan setiap empat hari sekali. yang dihasilkan pada kondisi COD:N 800:7 dan pH 7 adalah 13,17 ml biogas/mg TS COD.
Derajat keasaman (pH) menunjukan sifat asam atau basa pada suatu bahan. Derajat keasaman merupakan suatu ekspresi dari konsentrasi ion hidrogen, [H+] yang besarannya dinyatakan dalam minus logaritma dari konsentrasi ion hidrogen, yaitu:
pH = - log [H+]
Grafik pengaruh pH terhadap produksi biogas pada
Sedangkan produksi biogas terendah yang ditunjukkan dengan gradien garis yang paling kecil adalah pada pH dinetralkan tiap empat hari. Biogas yang dihasilkan pada kondisi COD:N 800:7 dan pH 7 adalah
Sebagaimana diketahui bahwa salah satu tahap dalam dekomposisi bahan organik anaerobik adalah tahap asidogenesis dan asetogenesis. Pada tahap ini terbentuk asam lemak volatil yang akan menurunkan pH dalam reaktor. Keseluruhan proses anaerobik terjadi pada pH antara 6 – 8. Walaupun bakteri pembentuk metana sangat peka terhadap pH, tetapi pH dalam reaktor tidak harus dikendalikan secara ketat.
Pengaturan pH dapat dilakukan dengan menjaga umpan tidak terlalu asam serta mengendalikan jumlah setimbangan reaksi antara tahap asidogenik dan metanogenik terjaga dengan baik. Pada kondisi tanpa bantuan penyeimbang pH, maka pada nilai pH dibawah 6 aktivitas bakteri metan akan mulai terganggu dan bila mencapai 5,5 aktivitas bakterial akan terhenti sama sekali. Konsetrasi pH di dalam reaktor ini sangat
dipengaruhi oleh jumlah asam lemak volatil (VFA), ammonia, CO2 dan kandungan alkalinitas bikarbonat yang
Faktor pH sangat berperan pada dekomposisi anaerob karena pada rentang pH yang tidak se
tidak dapat tumbuh dengan maksimum dan bahkan dapat menyebabkan kematian. Pada akhirnya kondisi ini dapat menghambat perolehan gas metana. Derajat keasaman yang optimum bagi kehidupan mikroorganisme adalah 6,8
mbuhan bakteri penghasil gas metana akan baikbila pH bahan berada pada keadaan (basa) yaitu 6,5 sampai 7. Nilai pH terbaik untuk suatu digester yaitu sekitar 7,0. Apabila nilai pH di bawah 6,5, maka aktivitas bakteri metanogen akan menurun dan apabila nilai pH di bawah 5,0, maka fermentasi akan terhenti (Yani dan Darwis, 1990). Bila proses fermentasi berlangsung dalam keadaan normal dan anaerobik, maka pH akan secara
8,5. Jika pH lebih tinggi dari 8,5 akan mengakibatkan pengar populasi bakteri metanogen, sehingga akan mempengaruhi laju pembentukan biogas dalam reaktor.
Pada botol 4, 5, 6, 10, 11, dan 12, campuran dinetralkan mencapai pH 7 dan akan dinetralkan kembali setiap empat hari sekali. Sedangkan 6 botol yang lain, campuran dinetralkan pada awal proses dan tidak dilakukan
Pengolahan limbah secara biologis dibedakan menjadi dua proses, yaitu proses aerobik dan proses anaerobik. Pada proses aerobik, berlangsungnya proses sangat tergantung dari adanya oksigen, sedangkan dalam proses anaerobik justru sebaliknya karena oksigen akan menghambat jalannya proses.
Di dalam reaktor biogas, terdapat dua jenis bakteri yang sangat berperan, yakni bakteri asidogenik dan genik. Kedua jenis bakteri ini perlu eksis dalam jumlah yang berimbang. Bakteri
memanfaatkan bahan organik dan memproduksi metan dan gas lainnya dalam siklus hidupnya pada kondisi anaerob. Mereka memerlukan kondisi tertentu dan sensitif terhadap lingkungan mikro dalam reaktor seperti temperatur, keasaman dan jumlah material organik yang akan dicerna. Terdapat beberapa spesies metanogenik dengan berbagai karateristik. Bakteri ini mempunyai beberapa sifat fisiologi yang umum, tetapi mempunyai morf
Methanosarcina, Metanococcu, dan Methanothrix (Haryati, 2006).
Pada tahap pembentukan gas metana, bakteri yang berperan adalah bakteri metanogenesis. Bakteri metanogenesis akan memanfaatkan hasil dari tahap kedua yaitu asetat, format, karbondioksida, dan hidrogen sebagai
0 1000 2000 3000 4000 5000 0 10 20 A k u m u la si P ro d u k si B io g a s (m l) Hari ke-COD:N 800:7 pH 7 COD:N 1000:7 pH 7 COD:N 900:7 pH kontrol menunjukkan pengaruh pH terhadap produksi biogas pada campuran dan rumen dengan tambahan sumber . Dari gambar dapat diketahui bahwa volume biogas dengan pH 7, akumulasi volumenya lebih banyak daripada biogas yang dihasilkan dari campuran yang dinetralkan setiap empat hari sekali. Biogas yang dihasilkan pada kondisi COD:N 800:7 l biogas/mg TS COD.
Derajat keasaman (pH) menunjukan sifat asam atau basa pada suatu bahan. Derajat keasaman merupakan suatu ekspresi dari konsentrasi ion hidrogen, [H+] yang besarannya dinyatakan dalam minus logaritma dari konsentrasi ion
(1) Gambar 3 Grafik pengaruh pH terhad
campura vinasse, rumen, dan NH4HCO3
3
terendah yang ditunjukkan dengan gradien garis yang paling kecil adalah pada pHCOD:N 800:7 dan pH 7 adalah 0,96 ml
Sebagaimana diketahui bahwa salah satu tahap dalam dekomposisi bahan organik anaerobik adalah tahap asidogenesis dan asetogenesis. Pada tahap ini terbentuk asam lemak volatil yang akan menurunkan pH dalam 8. Walaupun bakteri pembentuk metana sangat Pengaturan pH dapat dilakukan dengan menjaga umpan tidak terlalu asam serta mengendalikan jumlah
setimbangan reaksi antara tahap asidogenik dan metanogenik terjaga dengan baik. Pada kondisi tanpa bantuan penyeimbang pH, maka pada nilai pH dibawah 6 aktivitas bakteri metan akan mulai terganggu dan a sekali. Konsetrasi pH di dalam reaktor ini sangat dan kandungan alkalinitas bikarbonat yang
Faktor pH sangat berperan pada dekomposisi anaerob karena pada rentang pH yang tidak sesuai, mikroba tidak dapat tumbuh dengan maksimum dan bahkan dapat menyebabkan kematian. Pada akhirnya kondisi ini dapat menghambat perolehan gas metana. Derajat keasaman yang optimum bagi kehidupan mikroorganisme adalah
6,8-bila pH bahan berada pada keadaan (basa) yaitu 6,5 sampai 7. Nilai pH terbaik untuk suatu digester yaitu sekitar 7,0. Apabila nilai pH di bawah 6,5, maka aktivitas
ai pH di bawah 5,0, maka fermentasi akan terhenti (Yani dan keadaan normal dan anaerobik, maka pH akan secara 8,5. Jika pH lebih tinggi dari 8,5 akan mengakibatkan pengaruh yang negatif pada populasi bakteri metanogen, sehingga akan mempengaruhi laju pembentukan biogas dalam reaktor.
Pada botol 4, 5, 6, 10, 11, dan 12, campuran dinetralkan mencapai pH 7 dan akan dinetralkan kembali ol yang lain, campuran dinetralkan pada awal proses dan tidak dilakukan
Pengolahan limbah secara biologis dibedakan menjadi dua proses, yaitu proses aerobik dan proses sangat tergantung dari adanya oksigen, sedangkan dalam
Di dalam reaktor biogas, terdapat dua jenis bakteri yang sangat berperan, yakni bakteri asidogenik dan genik. Kedua jenis bakteri ini perlu eksis dalam jumlah yang berimbang. Bakteri-bakteri ini memanfaatkan bahan organik dan memproduksi metan dan gas lainnya dalam siklus hidupnya pada kondisi anaerob. p lingkungan mikro dalam reaktor seperti temperatur, keasaman dan jumlah material organik yang akan dicerna. Terdapat beberapa spesies metanogenik dengan berbagai karateristik. Bakteri ini mempunyai beberapa sifat fisiologi yang umum, tetapi mempunyai morfologi yang beragam
(Haryati, 2006).
Pada tahap pembentukan gas metana, bakteri yang berperan adalah bakteri metanogenesis. Bakteri a yaitu asetat, format, karbondioksida, dan hidrogen sebagai
30 40
COD:N 900:7 pH 7 COD:N 800:7 pH kontrol COD:N 1000:7 pH kontrol
substrat untuk menghasilkan metana, karbondioksida, sisa
bakteri obligat anaerobik dan sangat sensitif terhadap perubahan lingkungan. Berbeda dangan bakteri asidogenesis dan asetogenesis, bakteri metanogenesis termasuk dalam genus
mempunyai struktur morfologi yang sangat berbeda molekul yang berbeda dengan bakteri lain.
Produksi biogas akan lebih optimum jika fermentasi anaerobik yang dilakukan benar
tanpa oksigen (O2). Sehingga pada penelitian dengan pH kontrol yang dilakukan tiap empat hari sekali tidak dapat menghasilkan biogas dengan optimum. Kondisi yang memungkinkan masuknya oksigen pada reaktor adalah ketika dilakukannya pengambilan sampel bahan dari dala
terdapat pada reaktor. Solusi yang mungkin bisa dilakukan adalah dengan memperbaiki desain sistem reaktor ketika pengambilan sampel, agar kemungkinan masuknya oksigen dikurangi, yaitu dengan sistem bu
lubang sampel.
Pada hasil terlihat bahwa setelah hari ke 13 sudah tidak dihasilkan biogas. Hal itu karena pH pada botol 1 hingga 6 sudah mengalami penurunan hingga
menurun dan di saat nilai pH mencapai di bawah 5,0, maka fermentasi terhenti sehingga biogas tidak dihasilkan kembali. Penurunan pH dapat dilihat pada g
Dari gambar tersebut dapat dilihat bahwa pada hari ke
sehingga fermentasi terhenti dan tidak dapat dihasilkan biogas. Nilai pH yang terlalu asam da aktivitas mikroorganisme penghasil metana. Sedangkan pada campuran
dapat terbentuk pada hari ke-13 karena NH
pada kondisi netral. Seperti diketahui bahwa bakteri metanogenik memiliki karakteristik antara lain membutuhkan kondisi anaerob, menghasilkan enzim
yaitu 5-7 (Weimer et al., 1999; Peres et al., 2002). b. Pengaruh Perbandingan
Chemical Oxygen Demand
dibutuhkan oleh oksidator (misal kalium dikhromat) untuk mengoksidasi seluruh
anorganik yang terdapat dalam air (MetCalf & Eddy, 2003). Mikroba membutuhkan udara dalam mendegradasi substrat, dimana protein dihidrolisis menjadi asam
sederhana, dan lemak dihidrolisis menjadi asam
anorganik cukup besar, maka oksigen terlarut di dalam air dapat mencapai nol sehingga tumbuhan air, ikan hewan air lainnya yang membutuhkan oksigen tidak memungki
Dari hasil terlihat bahwa pada perbandingan
sebesar 280 ml (0,96 ml biogas/mg TS COD), sementara pada perbandingan COD:N 900:7 dan 1000:7 biogas optimum hanya diperoleh sebesar 250 ml (0,857 ml
COD). Dari gambar 3, produksi biogas optimum yang diperoleh juga terdapat pada perbandingan
yaitu sebesar 3839 ml (13,17 ml biogas/mg TS COD), sementara pada perbandingan COD:N 900:7 dan 100 biogas optimum hanya diperoleh sebesar 3088 ml (10,589 ml biogas/mg TS COD), dan 1586 ml (5,44 ml biogas/mg TS COD). Perbandingan COD:N 800:7
bakteri lebih mudah menguraikan senyawa
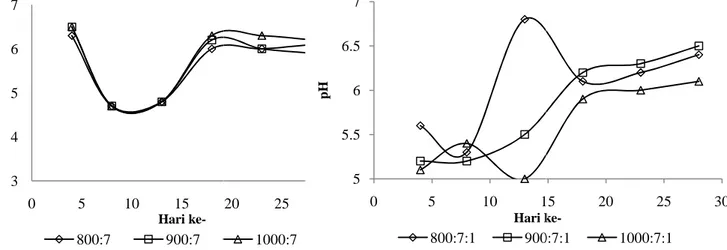
diperoleh hasil biogas yang paling kecil yang menandakan bahwa penurunan COD juga kecil pula. Sedikitnya 3 4 5 6 7 0 5 10 15 p H Hari ke-800:7 900:7
Gambar 4 Grafik pH harian campuran dan urea
substrat untuk menghasilkan metana, karbondioksida, sisa-sisa gas seperti H2S dan air. Bakteri ini merupakan bakteri obligat anaerobik dan sangat sensitif terhadap perubahan lingkungan. Berbeda dangan bakteri asidogenesis dan asetogenesis, bakteri metanogenesis termasuk dalam genus Archaebacter yaitu kelompok bakteri yang i struktur morfologi yang sangat berbeda-beda (heterogen), sifat biokimia yang umum, dan sifat biologi molekul yang berbeda dengan bakteri lain.
Produksi biogas akan lebih optimum jika fermentasi anaerobik yang dilakukan benar
). Sehingga pada penelitian dengan pH kontrol yang dilakukan tiap empat hari sekali tidak dapat menghasilkan biogas dengan optimum. Kondisi yang memungkinkan masuknya oksigen pada reaktor adalah ketika dilakukannya pengambilan sampel bahan dari dalam reaktor. Sampel bahan diambil dari lubang sampel yang terdapat pada reaktor. Solusi yang mungkin bisa dilakukan adalah dengan memperbaiki desain sistem reaktor ketika pengambilan sampel, agar kemungkinan masuknya oksigen dikurangi, yaitu dengan sistem bu
terlihat bahwa setelah hari ke 13 sudah tidak dihasilkan biogas. Hal itu karena pH pada botol 1
hingga 6 sudah mengalami penurunan hingga di bawah 6,5, yang menyebabkan aktivitas bakteri metanogen
menurun dan di saat nilai pH mencapai di bawah 5,0, maka fermentasi terhenti sehingga biogas tidak dihasilkan kembali. Penurunan pH dapat dilihat pada gambar berikut ini:
tersebut dapat dilihat bahwa pada hari ke-13, pH campuran mencapai nilai di bawah 5 sehingga fermentasi terhenti dan tidak dapat dihasilkan biogas. Nilai pH yang terlalu asam da
aktivitas mikroorganisme penghasil metana. Sedangkan pada campuran vinasse, rumen, dan NH
13 karena NH4HCO3 merupakan buffer yang yang digunakan untuk menjaga
pada kondisi netral. Seperti diketahui bahwa bakteri metanogenik memiliki karakteristik antara lain membutuhkan kondisi anaerob, menghasilkan enzim Silanase actinobacteria dan hanya dapat hidup pada kisaran pH yang sempit
1999; Peres et al., 2002).
Pengaruh Perbandingan COD:N Terhadap Produksi Biogas
Chemical Oxygen Demand (COD) atau kebutuhan oksigen kimiawi merupakan jumlah oksigen yang dibutuhkan oleh oksidator (misal kalium dikhromat) untuk mengoksidasi seluruh material baik organik maupun anorganik yang terdapat dalam air (MetCalf & Eddy, 2003). Mikroba membutuhkan udara dalam mendegradasi substrat, dimana protein dihidrolisis menjadi asam-asam amino, karbohidrat dihidolisis menjadi gula
k dihidrolisis menjadi asam-asam berantai pendek. Jika kandungan senyawa organik dan anorganik cukup besar, maka oksigen terlarut di dalam air dapat mencapai nol sehingga tumbuhan air, ikan
hewan air lainnya yang membutuhkan oksigen tidak memungkinkan hidup.
terlihat bahwa pada perbandingan COD:N 800:7 produksi biogas mampu mencapai optimum sebesar 280 ml (0,96 ml biogas/mg TS COD), sementara pada perbandingan COD:N 900:7 dan 1000:7 biogas optimum hanya diperoleh sebesar 250 ml (0,857 ml biogas/mg TS COD) dan 208 ml (0,713 ml biogas/mg TS
produksi biogas optimum yang diperoleh juga terdapat pada perbandingan
3839 ml (13,17 ml biogas/mg TS COD), sementara pada perbandingan COD:N 900:7 dan 100 biogas optimum hanya diperoleh sebesar 3088 ml (10,589 ml biogas/mg TS COD), dan 1586 ml (5,44 ml biogas/mg
800:7 menghasilkan biogas yang optimum, karena pada perbandingan tersebut bakteri lebih mudah menguraikan senyawa-senyawa organik. Sedangkan pada perbandingan
diperoleh hasil biogas yang paling kecil yang menandakan bahwa penurunan COD juga kecil pula. Sedikitnya
20 25 30 1000:7 5 5.5 6 6.5 7 0 5 10 15 p H Hari ke 800:7:1 900:7:1
Grafik pH harian campuran vinasse, rumen, Gambar 5 Grafik pH harian campuran
dan NH4NCO
4
S dan air. Bakteri ini merupakan bakteri obligat anaerobik dan sangat sensitif terhadap perubahan lingkungan. Berbeda dangan bakteri asidogenesis yaitu kelompok bakteri yang beda (heterogen), sifat biokimia yang umum, dan sifat biologiProduksi biogas akan lebih optimum jika fermentasi anaerobik yang dilakukan benar-benar pada kondisi ). Sehingga pada penelitian dengan pH kontrol yang dilakukan tiap empat hari sekali tidak dapat menghasilkan biogas dengan optimum. Kondisi yang memungkinkan masuknya oksigen pada reaktor adalah ketika m reaktor. Sampel bahan diambil dari lubang sampel yang terdapat pada reaktor. Solusi yang mungkin bisa dilakukan adalah dengan memperbaiki desain sistem reaktor ketika pengambilan sampel, agar kemungkinan masuknya oksigen dikurangi, yaitu dengan sistem buka-tutup otomatis pada
terlihat bahwa setelah hari ke 13 sudah tidak dihasilkan biogas. Hal itu karena pH pada botol 1
di bawah 6,5, yang menyebabkan aktivitas bakteri metanogen akan menurun dan di saat nilai pH mencapai di bawah 5,0, maka fermentasi terhenti sehingga biogas tidak dihasilkan
13, pH campuran mencapai nilai di bawah 5 sehingga fermentasi terhenti dan tidak dapat dihasilkan biogas. Nilai pH yang terlalu asam dapat menghambat , rumen, dan NH4HCO3 biogas masih merupakan buffer yang yang digunakan untuk menjaga pH tetap pada kondisi netral. Seperti diketahui bahwa bakteri metanogenik memiliki karakteristik antara lain membutuhkan dan hanya dapat hidup pada kisaran pH yang sempit
(COD) atau kebutuhan oksigen kimiawi merupakan jumlah oksigen yang material baik organik maupun anorganik yang terdapat dalam air (MetCalf & Eddy, 2003). Mikroba membutuhkan udara dalam mendegradasi asam amino, karbohidrat dihidolisis menjadi gula-gula asam berantai pendek. Jika kandungan senyawa organik dan anorganik cukup besar, maka oksigen terlarut di dalam air dapat mencapai nol sehingga tumbuhan air, ikan-ikan dan
produksi biogas mampu mencapai optimum sebesar 280 ml (0,96 ml biogas/mg TS COD), sementara pada perbandingan COD:N 900:7 dan 1000:7 biogas biogas/mg TS COD) dan 208 ml (0,713 ml biogas/mg TS produksi biogas optimum yang diperoleh juga terdapat pada perbandingan COD:N 800:7 3839 ml (13,17 ml biogas/mg TS COD), sementara pada perbandingan COD:N 900:7 dan 1000:7 biogas optimum hanya diperoleh sebesar 3088 ml (10,589 ml biogas/mg TS COD), dan 1586 ml (5,44 ml biogas/mg menghasilkan biogas yang optimum, karena pada perbandingan tersebut nyawa organik. Sedangkan pada perbandingan COD:N 1000:7 diperoleh hasil biogas yang paling kecil yang menandakan bahwa penurunan COD juga kecil pula. Sedikitnya
15 20 25 30
Hari
ke-900:7:1 1000:7:1
Grafik pH harian campuran vinasse, rumen,
penyisihan COD karena oleh beberapa hal, yaitu bahan organik pada tahap asidifikasi dirombak menjadi asam yang selanjutnya dirombak menjadi metana pada tahap metanasi. Semakin besar bahan organik yang dirombak menjadi asam (VFA) dan melebihi kemampuan bakt
sehingga proses metanasi terhambat dan penyisihan COD kurang maksimal
c. Pengaruh Penambahan Nutrisi terhadap Volume Biogas
Gambar 6 di atas menunjukkan pengaruh dari penggunaan dihasilkan. Dari gambar tersebut, dapat dijelaskan
lebih banyak daripada menggunakan
Urea dipilih sebagai sumber nitrogen karena mudah dicerna oleh berbagai mikroorganisme. Selain itu, urea yang berisi nitrogen menjadi sumber nutrisi bagi pertumbuhan mikroorganisme. Akan tetapi,
menghambat produksi metana (Anunputtikul, 2004). Dari hasil penelitian yang dapat dilihat pada
urea menunjukkan hasil yang tidak maksimal. Hal ini karena rasio C/N pada limbah su
yang bagus untuk pertumbuhan mikroorganisme sehingga penambahan urea menyebabkan kadar N dalam umpan semakin besar, sehingga kadar C/N semakin kecil. Kadar C/N yang relatif kecil tidak baik untuk proses pembentukan biogas karena akan meningkatkan emisi nitrogen sebagai amonium yang dapat menghalangi perkembangan bakteri. Oleh karena itu, perlu ada alternatif lain yang digunakan sebagai nutrisi sumber nitrogen.
Pada proses pembentukan biogas sering terjadi penurunan pH yang cukup dr
disebabkan oleh pembentukan asam yang terlalu cepat. Selain pembentukan asam juga karena pembentukan gas hidrogen, karbondioksida, dan beberapa VFA seperti asam propionate dan butirat. pH yang rendah mampu menyebabkan mikroorganisme pembentuk biogas yaitu bakteri metanogenesis (bakteri rumen) berada dalam kondisi inaktif (Vicenta et al., 1984)
Di samping itu, agar bakteri metanogenik mampu tumbuh dan berkembang dengan baik diperlukan penambahan buffer ke dalam digester untuk mening
yang juga berfungsi sebagai buffer untuk meningkatkan alkalinitas selama proses fermentasi berlangsung.
Tingkat keasaman maupun basa pada froses fermentasi dinyatakan dengan pH. Kebanyakan bakteri metanogenesis mempunyai pH optimum mendekati netral (Jones et al., 1987). pH optimum dalam produksi biogas berada dalam rentang 6,8-7,2 dengan batasan rentang operasi tanpa hambatan yang signifikan sekitar 6,5
1t al., 1987; Bunchueydee, 1984; Haga
pH antara 6,5-8,2 (Buyukkamaci dan filibeli, 2004).
Pembentukan biogas yang lebih besar pada proses fermentasi 2 tahap hidrolisa terlebih dahulu yang merupakan
yang lebih sederhana yaitu disakarida dan monosakarida sehingga akan oleh bakteri asetogenik dan juga proses pembentukan metan oleh bakteri dijumpai pada fermentasi 1 tahap, sehingga akan terjadi pembentukan
yang terlalu cepat inimenyebabkan banyaknya bakteri metanogenesis yang mati karena tidak tahan
0 1000 2000 3000 4000 5000 800:7 V o lu m e B io g a s (m l) Perbandingan COD:N vinasse, rumen, urea
Gambar 6 Grafik Penambahan Urea dan Biogas
penyisihan COD karena oleh beberapa hal, yaitu bahan organik pada tahap asidifikasi dirombak menjadi asam yang selanjutnya dirombak menjadi metana pada tahap metanasi. Semakin besar bahan organik yang dirombak menjadi asam (VFA) dan melebihi kemampuan bakteri metanogen untuk merombak mengakibatkan akumulasi asam sehingga proses metanasi terhambat dan penyisihan COD kurang maksimal (sitasi).
Pengaruh Penambahan Nutrisi terhadap Volume Biogas
di atas menunjukkan pengaruh dari penggunaan sumber nitrogen terhadap volume biogas yang dihasilkan. Dari gambar tersebut, dapat dijelaskan bahwa produksi biogas dengan menggunakan NH
lebih banyak daripada menggunakan urea.
Urea dipilih sebagai sumber nitrogen karena mudah dicerna oleh berbagai mikroorganisme. Selain itu, urea yang berisi nitrogen menjadi sumber nutrisi bagi pertumbuhan mikroorganisme. Akan tetapi,
menghambat produksi metana (Anunputtikul, 2004).
Dari hasil penelitian yang dapat dilihat pada gambar 6 didapatkan bahwa vinasse
urea menunjukkan hasil yang tidak maksimal. Hal ini karena rasio C/N pada limbah sudah berada pada komposisi yang bagus untuk pertumbuhan mikroorganisme sehingga penambahan urea menyebabkan kadar N dalam umpan semakin besar, sehingga kadar C/N semakin kecil. Kadar C/N yang relatif kecil tidak baik untuk proses kan meningkatkan emisi nitrogen sebagai amonium yang dapat menghalangi perkembangan bakteri. Oleh karena itu, perlu ada alternatif lain yang digunakan sebagai nutrisi sumber nitrogen.
Pada proses pembentukan biogas sering terjadi penurunan pH yang cukup dr
disebabkan oleh pembentukan asam yang terlalu cepat. Selain pembentukan asam juga karena pembentukan gas hidrogen, karbondioksida, dan beberapa VFA seperti asam propionate dan butirat. pH yang rendah mampu me pembentuk biogas yaitu bakteri metanogenesis (bakteri rumen) berada dalam kondisi Di samping itu, agar bakteri metanogenik mampu tumbuh dan berkembang dengan baik diperlukan penambahan buffer ke dalam digester untuk meningkatkan alkalinitasnya. Oleh karena itu digunakan
untuk meningkatkan alkalinitas selama proses fermentasi berlangsung.
Tingkat keasaman maupun basa pada froses fermentasi dinyatakan dengan pH. Kebanyakan bakteri tanogenesis mempunyai pH optimum mendekati netral (Jones et al., 1987). pH optimum dalam produksi biogas
7,2 dengan batasan rentang operasi tanpa hambatan yang signifikan sekitar 6,5
1t al., 1987; Bunchueydee, 1984; Haga et al., 1979). Bakteri metanogenesis terkadang dapat tumbuh pada rentang 8,2 (Buyukkamaci dan filibeli, 2004).
Pembentukan biogas yang lebih besar pada proses fermentasi 2 tahap disebabkan karena adanya proses merupakanproses degradasi senyawa kompleks yaitu polisakarida menjadi senyawa lebih sederhana yaitu disakarida dan monosakarida sehingga akanmempermudah proses pembentukan asam oleh bakteri asetogenik dan juga proses pembentukan metan oleh bakteri metanogenesis. Proses tersebut tidak dijumpai pada fermentasi 1 tahap, sehingga akan terjadi pembentukanasam yang terlalu cepat. Pembentukan asam
menyebabkan banyaknya bakteri metanogenesis yang mati karena tidak tahan
900:7 1000:7
Perbandingan COD:N
vinasse, rumen, urea vinasse, rumen, NH4HCO3
Grafik Penambahan Urea dan NH4HCO3 terhadap Volume
Bahan
oleh mikroorganisme tanpa oksigen menghasilkan beberapa jumlah metana. Kurangnya elemen khusus yang diperlukan untuk pertumbuhan mikroorganisme akan membatasi produksi biogas. Nutrisi di
karbon dan nitrogen (perkiraan 20 (Anunputtikul, 2004).
perlu dilakukan penambahan nutrisi, dalam hal ini urea dan NH
suplai nutrisi. Kuantitas urea dan NH4HCO3 yang ditambahkan disesuaikan dengan nilai COD bahan dan perbandingan variabel
diinginkan.
5
penyisihan COD karena oleh beberapa hal, yaitu bahan organik pada tahap asidifikasi dirombak menjadi asam yang selanjutnya dirombak menjadi metana pada tahap metanasi. Semakin besar bahan organik yang dirombak menjadi eri metanogen untuk merombak mengakibatkan akumulasi asamerhadap volume biogas yang bahwa produksi biogas dengan menggunakan NH4HCO3 jauh
Urea dipilih sebagai sumber nitrogen karena mudah dicerna oleh berbagai mikroorganisme. Selain itu, urea yang berisi nitrogen menjadi sumber nutrisi bagi pertumbuhan mikroorganisme. Akan tetapi, kekurangan urea dapat
vinasse yang diberi tambahan dah berada pada komposisi yang bagus untuk pertumbuhan mikroorganisme sehingga penambahan urea menyebabkan kadar N dalam umpan semakin besar, sehingga kadar C/N semakin kecil. Kadar C/N yang relatif kecil tidak baik untuk proses kan meningkatkan emisi nitrogen sebagai amonium yang dapat menghalangi perkembangan bakteri. Oleh karena itu, perlu ada alternatif lain yang digunakan sebagai nutrisi sumber nitrogen.
Pada proses pembentukan biogas sering terjadi penurunan pH yang cukup drastis di awal proses yang disebabkan oleh pembentukan asam yang terlalu cepat. Selain pembentukan asam juga karena pembentukan gas hidrogen, karbondioksida, dan beberapa VFA seperti asam propionate dan butirat. pH yang rendah mampu me pembentuk biogas yaitu bakteri metanogenesis (bakteri rumen) berada dalam kondisi Di samping itu, agar bakteri metanogenik mampu tumbuh dan berkembang dengan baik diperlukan katkan alkalinitasnya. Oleh karena itu digunakan NH4HCO3 untuk meningkatkan alkalinitas selama proses fermentasi berlangsung.
Tingkat keasaman maupun basa pada froses fermentasi dinyatakan dengan pH. Kebanyakan bakteri tanogenesis mempunyai pH optimum mendekati netral (Jones et al., 1987). pH optimum dalam produksi biogas 7,2 dengan batasan rentang operasi tanpa hambatan yang signifikan sekitar 6,5-7,6 (Anglo et al., 1979). Bakteri metanogenesis terkadang dapat tumbuh pada rentang
disebabkan karena adanya proses proses degradasi senyawa kompleks yaitu polisakarida menjadi senyawa mempermudah proses pembentukan asam metanogenesis. Proses tersebut tidakakan asam yang terlalu cepat. Pembentukan asam menyebabkan banyaknya bakteri metanogenesis yang mati karena tidak tahandengan suasana
Bahan organik yang diuraikan oleh mikroorganisme tanpa oksigen, akan menghasilkan beberapa jumlah metana. Kurangnya elemen khusus yang diperlukan untuk pertumbuhan mikroorganisme akan membatasi produksi biogas. Nutrisi ditandai dengan rasio karbon dan nitrogen (perkiraan 20-30:1) (Anunputtikul, 2004). Oleh karena itu, perlu dilakukan penambahan nutrisi, dalam hal ini urea dan NH4HCO3 sebagai suplai nutrisi. Kuantitas urea dan yang ditambahkan disesuaikan dengan nilai COD bahan dan perbandingan variabel COD:N yang
asam. Terjadinya penurunan pH ini diatasi dengan penambahan
range pH agar bakteri dapat bertahan.
4. Kesimpulan
Hasil penelitian di atas menunjukkan
dinetralkan di awal tanpa penetralan harian. Sedangkan diantara variabel perbandingan dan 1000:7, yang dapat menghasilkan biogas dengan optimal adalah variabel
Biogas yang dihasilkan pada kondisi
hari. Selain itu, dari penelitian ini dapat diketahui bahwa nutrisi yang baik sebagai sumber nitrogen adalah NH4HCO3 , juga sekaligus berperan sebagai
Ucapan Terima Kasih
Terima kasih disampaikan kepada
Laboratorium Pengolahan Limbah Teknik Kimia Universitas Diponegoro.
Daftar Pustaka
Anunputtikul, W., Rodtong, S., Investigation of The
of the 15th Annual Meeting of The Thai Society for Biotechnology and JSPS Thailand, 2004, p. 70.
Ayu, Audra and Vinsencia Dyan. 2010. Biogas Production Using Anaerobic Biodigester Effluent With Ruminant Bacteria as Biocatalyst.
Faculty, Diponegoro University. Semarang. Buren, A. 1979. A Chinese Biogas Manual.
Cortella, Giovanni and Carla Da Porto. 2003. Spirits Originating From Fermented Grape
Dahuri, D. 2007. Sampah Organik, Kotoran Kerbau Sumber Energi 2007)
Engler CR., dkk. 2000. Economics and Environmental Impact of Biogas Production as a Manure Management Strategy. http://tammi.tamu.edu/Engler2.pdf
Fardiaz, S. 1990 . Fisiologi Fermentasi
Fry, L. J. 1974. Practical Building of Methane Power Plants for Rural Energy Independence Santa Barbara: California.
Gijzen HJ. 1987. Anaerobic Digestion of Cellulatic Waste by Rumen Derived Process Hambali E, dkk. 2007. Teknologi Bioenergi
Haq PS dan Soedjono ES. 2009. Lingkungan. FTSP-ITS: Surabaya.
Indartono, Yuli Setyo. 2006. Reaktor Biogas Skala Kecil/Menengah. April 2007)
Indira. 2007. Laju Produksi CH4
http://digilib.itb.ac.id. (3 Mei 2007) Judoamidjojo, M. dan A. A. Darwis. 1990.
Bogor.
Nandiyanto, A. B. D. dan F. Rumi. 2006. Biogas Sebagai Peluang Pengembangan Energi Alternatif. jepang.org/article.php?d=199
Padmono, Djoko. 2007. Kemampuan Alkalinitas Kapasitas Fixed Bed. Pusat Teknologi Lingkungan. Jakarta.
Prasetio B. 2010. Optimasi porduksi xilitol oleh sel amobil candida tropicalis melalui fermentasi batch. Fakultas Matematika dan Ilmu Pengetahuan A
Sahidu, S. 1983. Kotoran Ternak Sebagai Sumber Energi Salomon, K. R. dan Silva Lora, E.E. 2009.
Sources of Biogas in Brazil.
Sathianathan, M. A. 1975. Biogas Echiefemens and Challanges. 1992. Mempelajari Cara Pembuatan Biogas Melalui Proses ’Rumen Derived Anaerobic Digestion’ (RURAD).
Pertanian, Fakultas Teknologi
Soeprijanto,dkk. 2010. Pengolahan Vinasse dari Air Limbah Industri Alkohol menjadi Biogas dengan Menggunakan Bioreaktor UASB. Jurnal Purifikasi, Vol.11 No. 1 hal.11
asam. Terjadinya penurunan pH ini diatasi dengan penambahan NH4HCO3 yang bertujuan untuk mempertahankan
pH agar bakteri dapat bertahan.
di atas menunjukkan bahwa pH yang baik untuk produksi biogas adalah pH 7 a dinetralkan di awal tanpa penetralan harian. Sedangkan diantara variabel perbandingan COD:N
, yang dapat menghasilkan biogas dengan optimal adalah variabel 800:7.
Biogas yang dihasilkan pada kondisi COD:N 800:7 dan pH 7 adalah 13,73 ml biogas/mg COD selama 30 Selain itu, dari penelitian ini dapat diketahui bahwa nutrisi yang baik sebagai sumber nitrogen adalah
, juga sekaligus berperan sebagai buffer yang dapat mengatasi penurunan pH pada awal pros
Terima kasih disampaikan kepada
Dr
. Ir. Budiyono, M. Si selaku dosen pembimbing dan Staf Laboratorium Pengolahan Limbah Teknik Kimia Universitas Diponegoro.Investigation of The Potential Production of Biogas from Cassava Tuber of the 15th Annual Meeting of The Thai Society for Biotechnology and JSPS
Ayu, Audra and Vinsencia Dyan. 2010. Biogas Production Using Anaerobic Biodigester
Effluent With Ruminant Bacteria as Biocatalyst. Thesis. Chemical Engineering Department, Technical Faculty, Diponegoro University. Semarang.
A Chinese Biogas Manual. Intermediate Technology Publications Ltd. London.
tella, Giovanni and Carla Da Porto. 2003. Design of a Continuous Distillation Plant for The Production of Spirits Originating From Fermented Grape. Journal Of Food Engineering 58: 379.
Dahuri, D. 2007. Sampah Organik, Kotoran Kerbau Sumber Energi Alternatif. http://www.energilipi.go.id
Engler CR., dkk. 2000. Economics and Environmental Impact of Biogas Production as a Manure Management http://tammi.tamu.edu/Engler2.pdf. (2 Mei 2011)
Fisiologi Fermentasi. Pusat Antar Universitas - IPB. Bogor.
Practical Building of Methane Power Plants for Rural Energy Independence
Anaerobic Digestion of Cellulatic Waste by Rumen Derived Process. Den Haag: Bibliotech. Teknologi Bioenergi. Jakarta: Agromedia Pustaka.
Haq PS dan Soedjono ES. 2009. Potensi lumpur tinja manusia sebagai penghasil biogas. ITS: Surabaya.
Indartono, Yuli Setyo. 2006. Reaktor Biogas Skala Kecil/Menengah. http://www.indeni.org/content/view/63/48/
dari Degradasi Sampah Kota Secara Anaerob dengan Variasi Temperatur. http://digilib.itb.ac.id. (3 Mei 2007)
Judoamidjojo, M. dan A. A. Darwis. 1990. Teknologi Fermentasi. Pusat Antar Universitas Bioteknologi
B. D. dan F. Rumi. 2006. Biogas Sebagai Peluang Pengembangan Energi Alternatif. jepang.org/article.php?d=199 (25 April 2007)
Kemampuan Alkalinitas Kapasitas Penyangga (Buffer Capacity) dalam Sistem Anaerobik Pusat Teknologi Lingkungan. Jakarta.
Prasetio B. 2010. Optimasi porduksi xilitol oleh sel amobil candida tropicalis melalui fermentasi batch. Fakultas Matematika dan Ilmu Pengetahuan Alam. IPB, Bogor.
Kotoran Ternak Sebagai Sumber Energi. Dewaruci Press. Jakarta.
Salomon, K. R. dan Silva Lora, E.E. 2009. Estimate of the Electric Energy Generating Potential for Different Sources of Biogas in Brazil. Biomass and Bioenergy 33 (2009) page 1101-1107
Sathianathan, M. A. 1975. Biogas Echiefemens and Challanges. 1992. Mempelajari Cara Pembuatan Biogas Melalui Proses ’Rumen Derived Anaerobic Digestion’ (RURAD). Skripsi. Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor. Bogor.
Pengolahan Vinasse dari Air Limbah Industri Alkohol menjadi Biogas dengan Menggunakan Jurnal Purifikasi, Vol.11 No. 1 hal.11-20.
6
yang bertujuan untuk mempertahankan
bahwa pH yang baik untuk produksi biogas adalah pH 7 atau pH yang COD:N yaitu 800:7, 900:7,
dan pH 7 adalah 13,73 ml biogas/mg COD selama 30 Selain itu, dari penelitian ini dapat diketahui bahwa nutrisi yang baik sebagai sumber nitrogen adalah
yang dapat mengatasi penurunan pH pada awal proses.
selaku dosen pembimbing dan Staf
Potential Production of Biogas from Cassava Tuber, Abstracts of the 15th Annual Meeting of The Thai Society for Biotechnology and JSPS-NRCT Symposium,
Ayu, Audra and Vinsencia Dyan. 2010. Biogas Production Using Anaerobic Biodigester From Cassava Starch Chemical Engineering Department, Technical
Intermediate Technology Publications Ltd. London.
Plant for The Production of . Journal Of Food Engineering 58: 379.
http://www.energilipi.go.id (26April
Engler CR., dkk. 2000. Economics and Environmental Impact of Biogas Production as a Manure Management
Practical Building of Methane Power Plants for Rural Energy Independence. Standard Printing . Den Haag: Bibliotech.
nghasil biogas. Jurusan Teknik http://www.indeni.org/content/view/63/48/. (21
dari Degradasi Sampah Kota Secara Anaerob dengan Variasi Temperatur.
. Pusat Antar Universitas Bioteknologi - IPB.
B. D. dan F. Rumi. 2006. Biogas Sebagai Peluang Pengembangan Energi Alternatif.
http://io.ppi-Penyangga (Buffer Capacity) dalam Sistem Anaerobik Prasetio B. 2010. Optimasi porduksi xilitol oleh sel amobil candida tropicalis melalui fermentasi batch. Skripsi.
Estimate of the Electric Energy Generating Potential for Different Sathianathan, M. A. 1975. Biogas Echiefemens and Challanges. 1992. Mempelajari Cara Pembuatan Biogas . Departemen Teknologi Industri
Stampe. S , dkk. 1983. Energy Consumption 355.
Sttafford, D. A., D. L. Hawkes., dan R. Homton. 1980. Press, Inc. Florida.
Sulaeman D. 2007. Pengomposan: Salah Satu Alternatif P http://agribisnis.Deptan.go.id/Pustaka/dede. (24
Tchobanoglous, G. dan Burton, F.L.
McGraw Hill, New York, pp.1334. Wahyuni. 2009. Biogas. Jakarta: Penebar Swadaya.
Weismann U. 1991. Anaerobic Treatment of Industrial Wastewater. Institut fur Verhahrentechni Yani M dan Darwis AA. 1990. Diktat Teknologi Biogas. Pusat Antar Universitas Bioteknologi
Energy Consumption of a Farm-Scale Ethanol Distillation System
Sttafford, D. A., D. L. Hawkes., dan R. Homton. 1980. Methan Production From Waste Organic Matter
Sulaeman D. 2007. Pengomposan: Salah Satu Alternatif Pengolahan Sampah Organic http://agribisnis.Deptan.go.id/Pustaka/dede. (24 April 2007)
Tchobanoglous, G. dan Burton, F.L. (1991). Wastewater Engineering: Treatment, Disposal and Reuse, third edition. McGraw Hill, New York, pp.1334.
Wahyuni. 2009. Biogas. Jakarta: Penebar Swadaya.
Weismann U. 1991. Anaerobic Treatment of Industrial Wastewater. Institut fur Verhahrentechni Yani M dan Darwis AA. 1990. Diktat Teknologi Biogas. Pusat Antar Universitas Bioteknologi
7
Scale Ethanol Distillation System. Energy in Agriculture 2: Methan Production From Waste Organic Matter. CRC engolahan Sampah Organic(1991). Wastewater Engineering: Treatment, Disposal and Reuse, third edition.
Weismann U. 1991. Anaerobic Treatment of Industrial Wastewater. Institut fur Verhahrentechnik, Berlin. Yani M dan Darwis AA. 1990. Diktat Teknologi Biogas. Pusat Antar Universitas Bioteknologi-IPB. Bogor