BAB II
TINJAUAN PUSTAKA
2.1 UraianTumbuhan Lidah Mertua
2.1.1 Sistematika Tumbuhan
Menurut Chase, dkk (2009), sistematika dari tumbuhan lidah mertua adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Kelas : Monocotyledonae Ordo : Asparagales Suku : Asparagaceae Genus : Sansevieria
Spesies : Sansevieria trifasciata
2.1.2 Nama Lain
Di Indonesia, tumbuhan ini umumnya di kenal dengan sebutan lidah mertua. Nama daerah dari tumbuhan lidah mertua, yaitu ki kolo, letah menyawak (Sumatera), nanas belanda (Sunda), pacing towo (Jawa) dan mandafika (Madura) (Utami, 2008).
2.1.3 Morfologi
permukaan daun berwarna hijau dengan garis-garis bergelombang horizontal dan tepi daun berwarna kuning cerah, panjang 5-175 cm, lebar 4-9 cm. Bunga majemuk dalam tandan dengan panjang 30-80 cm. Kuntum bunga 3-8 kuntum berkumpul membentuk bulir, berwarna hijau muda, harum dan mekar sepanjang malam. Buah buni, berbiji 1-3, bulat dengan diameter 3 mm dan berwarna merah tua (Dalimartha, 2007).
2.1.4 Kandungan Kimia dan Kegunaan
Bagian tumbuhan yang digunakan sebagai bahan obat adalah daun. Daun lidah mertua mengandung saponin dan polifenol (Dalimartha, 2007). Daun lidah mertua digunakan untuk mengobati flu, batuk, kekurangan vitamin C, bisul, borok, bengkak (memar) dan penyubur rambut (Dalimartha, 2007; Hariana, 2007).
2.2 Metode Ekstraksi
Ekstraksi adalah proses penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak larut dengan pelarut cair. Tujuan utama dari ekstraksi adalah untuk mendapatkan atau memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan. Zat aktif yang terdapat dalam simplisia tersebut dapat digolongkan ke dalam golongan minyak atsiri, alkaloid, flavonoid dan lain-lain (Ditjen POM. 2000).
Menurut Ditjen POM (2000), ada beberapa metode ekstraksi yang sering digunakan yaitu cara dingin dan cara panas.
2.2.1 Cara Dingin
Ekstraksi menggunakan pelarut dengan cara dingin terdiri dari: a. maserasi
Maserasi adalah penyarian simplisia dengan cara perendaman menggunakan pelarut disertai sesekali pengadukan pada temperatur kamar. Maserasi yang dilakukan pengadukan secara terus menerus disebut maserasi kinetik sedangkan yang dilakukan penambahan ulang pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
b. perkolasi
Perkolasi adalah proses penyarian simplisia menggunakan alat perkolator dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus menerus sampai diperoleh perkolat.
2.2.2 Cara Panas
Ekstraksi menggunakan pelarut dengan cara panas terdiri dari: a. refluks
Refluks adalah proses penyarian simplisia pada temperatur titik didihnya menggunakan alat dengan pendingin balik dalam waktu tertentu dimana pelarut akan terkondensasi menuju pendingin dan kembali ke labu.
b. digesti
temperatur 40 - 50°C. c. sokletasi
Sokletasi adalah proses penyarian menggunakan pelarut yang selalu baru, dilakukan dengan menggunakan alat khusus (soklet) dimana pelarut akan terkondensasi dari labu menuju pendingin, kemudian jatuh membasahi sampel. d. infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 15 menit.
e. dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 30 menit.
2.3 Toksisitas
Toksisitas adalah kemampuan suatu zat asing dalam menimbulkan kerusakan pada organisme baik saat digunakan atau saat berada dalam lingkungan (Priyanto, 2009). Menurut Wisaksono (2002), toksisitas adalah potensi bahan kimia untuk meracuni tubuh orang yang terpapar.
ditentukan dosis penggunaannya demi keamanan pemakainya (OECD, 2008).
Penelitian toksisitas konvensional pada hewan coba sering mengungkapkan serangkaian efek akibat pajanan toksikan dalam berbagai dosis untuk berbagai masa pajanan. Penelitian toksikologi biasanya dibagi menjadi tiga kategori (Lu, 1994):
a. uji toksisitas akut dilakukan dengan memberikan bahan kimia yang sedang diuji sebanyak satu kali atau beberapa kali dalam jangka waktu 24 jam.
b. uji toksisitas jangka pendek (dikenal dengan subkronik) dilakukan dengan memberikan bahan kimia berulang-ulang, biasanya setiap hari, selama jangka waktu kurang lebih tiga bulan untuk tikus dan satu atau dua tahun untuk anjing. c. uji toksisitas jangka panjang dilakukan dengan memberikan bahan kimia berulang-ulang selama masa hidup hewan coba atau sekurang-kurangnya sebagian besar dari masa hidupnya, misalnya 18 bulan untuk mencit, 24 bulan untuk tikus dan 7-10 tahun untuk anjing dan monyet.
Efek toksik dari uji toksisitas sangat bervariasi dalam sifat, organ sasaran, maupun mekanisme kerjanya. Semua efek toksik terjadi karena interaksi biokimiawi antara toksikan dengan struktur reseptor tertentu dalam tubuh. Sifat efek toksik pun dapat berbeda-beda. Beberapa efek toksik yang dapat ditimbulkan antara lain (Lu, 1994):
a. efek lokal dan sistemik
sistemik terjadi hanya setelah toksikan diserap dan tersebar ke bagian lain tubuh. Umumnya toksikan hanya mempengaruhi satu atau beberapa organ saja.
b. efek berpulih dan nirpulih
Efek toksik disebut berpulih (reversibel) jika efek itu dapat hilang dengan sendirinya. Sebaliknya, efek nirpulih (ireversibel) akan menetap atau justru bertambah parah setelah pajanan toksikan dihentikan. Efek nirpulih di antaranya karsinoma, mutasi, kerusakan saraf dan sirosis hati.
c. efek segera dan tertunda
Efek segera yaitu efek yang timbul segera setelah satu kali pajanan, sedangkan efek tertunda timbul beberapa waktu setelah pajanan.
d. efek morfologis, fungsionalis dan biokimiawi
Efek morfologis berkaitan dengan perubahan bentuk luar dan mikroskopis pada morfologi jaringan. Efek fungsionalis biasanya berupa perubahan berpulih pada fungsi organ sasaran. Efek biokimiawi adalah efek toksik yang tidak menyebabkan perubahan morfologis.
2.3.1 Uji Toksisitas Akut
Tabel 2.1 Parameter dasar pengujian toksisitas akut
Spesies Tikus lebih disukai pada uji oral dan inhalasi, kelinci lebih disukai pada uji secara dermal
Umur Dewasa
Jumlah Hewan 5 jenis setiap jenis kelamin per level dosis
Dosis Tiga level dosis yang direkomendasikan, pemberian secara dosis tunggal selama 24 jam untuk uji oral dan dermal dan 4 jam untuk uji inhalasi
Waktu Pengamatan 14 hari
(Gupta dan Bhardwaj, 2012) Prinsip uji toksisitas akut yaitu sediaan uji dalam beberapa tingkat dosis diberikan pada beberapa kelompok hewan uji dengan satu dosis per kelompok, kemudian dilakukan pengamatan terhadap adanya efek toksik dan kematian. Hewan yang mati selama percobaan dan yang hidup sampai akhir percobaan diotopsi untuk dievaluasi adanya gejala-gejala toksik (BPOM RI., 2014). Tujuan toksisitas akut adalah untuk mendeteksi toksisitas dari suatu zat, menentukan organ sasaran dan kepekaan spesies, memperoleh informasi bahaya setelah pemaparan suatu zat secara akut dan untuk memperoleh informasi awal yang dapat digunakan untuk merancang uji toksisitas selanjutnya serta untuk memperoleh nilai LD50 suatu sediaan (BPOM RI., 2014).
Penelitian uji toksisitas akut sebagian besar dirancang untuk menentukan dosis letal median (LD50) toksikan. LD50 didefinisikan sebagai “dosis tunggal
suatu bahan yang secara statistik diharapkan akan membunuh 50% hewan coba”. Pengujian ini juga dapat menunjukkan organ sasaran yang mungkin dirusak dan efek toksik spesifiknya, serta memberikan petunjuk tentang dosis yang sebaiknya digunakan dalam pengujian yang lebih lama (Lu, 1994). LD50 adalah dosis
menghasilkan kematian 50% dari populasi di bawah kondisi yang ditentukan dari tes atau LC50 merupakan konsentrasi perkiraan, dalam lingkungan hewan yang
terpapar, yang akan membunuh 50% dari populasi di bawah kondisi yang ditentukan dari tes (Hodgson dan Levi, 2000).
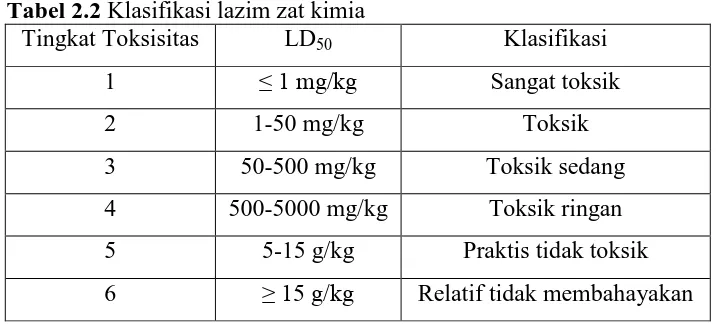
Nilai LD50 sangat berguna untuk hal-hal sebagai berikut:
a. klasifikasi lazim zat kimia sesuai dengan toksisitas relatifnya dapat dilihat pada Tabel 2.2 (BPOM RI., 2014):
Tabel 2.2 Klasifikasi lazim zat kimia
Tingkat Toksisitas LD50 Klasifikasi
1 ≤ 1 mg/kg Sangat toksik
2 1-50 mg/kg Toksik
3 50-500 mg/kg Toksik sedang
4 500-5000 mg/kg Toksik ringan 5 5-15 g/kg Praktis tidak toksik 6 ≥ 15 g/kg Relatif tidak membahayakan
b. evaluasi dampak keracunan yang tidak sengaja; perencanaan penelitian toksisitas subkronik dan kronik pada hewan, memberikan informasi tentang mekanisme toksisitas, pengaruh umur, seks, faktor penjamu dan faktor lingkungan lainnya dan variasi respons antar spesies dan antar strain hewan; memberikan informasi tentang reaktivitas suatu populasi hewan (Lu, 1994).
2.3.2 Uji Toksisitas Subkronik
Tujuan toksisitas subkronik oral pada rodensia adalah untuk memperoleh informasi (BPOM RI., 2014):
a. efek toksik zat yang tidak terdeteksi pada uji toksisitas akut.
b. efek toksik setelah pemaparan sediaan uji secara berulang dalam jangka waktu tertentu.
c. dosis yang tidak menimbulkan efek toksik (No Observed-Adverse Effect-Level/NOAEL).
d. mempelajari adanya efek kumulatif dan efek reversibilitas setelah pemaparan sediaan uji secara berulang dalam jangka waktu tertentu.
Pengamatan yang dilakukan dalam pengujian toksisitas subkronis adalah pengamatan pada awal pemberian senyawa meliputi penampakan fisik (kematian, membran mucus, kulit dan lain sebagainya), konsumsi makanan, berat badan, respon neurologi, kelakuan yang tidak normal, pernafasan, ECG, EEG, hematologi, pemeriksaan darah, urin. Pengamatan pada akhir pengujian meliputi nekropsi dan histologi (Hodgson dan Levi, 2000).
2.3.3 Uji Toksisitas Kronik
Uji toksisitas kronik oral adalah suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji secara berulang sampai seluruh umur hewan. Perlu dilakukan uji toksisitas kronik mengingat pemakaian obat seringkali memerlukan waktu yang relatif panjang, bahkan mungkin sepanjang masa hidup si pemakai (OECD, 2008).
memerlukan waktu yang lebih lama dan melibatkan kelompok yang lebih besar dari hewan pada uji toksisitas subkronik (Gupta dan Bhardwaj, 2012). Pada tikus, paparan kronik biasanya 6 bulan sampai 2 tahun. Untuk hewan selain tikus biasanya selama satu tahun tetapi mungkin lebih lama (Cassaret dan Doull, 2008).
2.4 Pengujian In Vivo
Pengujian secara in vivo adalah pengujian yang dilakukan dengan menggunakan hewan percobaan untuk mengetahui metabolisme suatu senyawa di dalam tubuh. Hewan percobaan yang digunakan pada percobaan secara in vivo harus dari jenis mamalia, karena hasilnya dapat diterapkan pada manusia. (Retnomurti, 2008). Mencit sebagai hewan percobaan sangat praktis digunakan untuk penelitian yang bersifat kuantitatif karena sifatnya yang mudah berkembangbiak. Selain itu, dalam bidang peternakan mencit tidak membutuhkan biaya yang mahal, efisien dalam waktu, dan kemampuan reproduksi tinggi dengan waktu yang singkat (Hadriyanah, 2008).
Sistem taksonomi mencit adalah sebagai berikut (Pribadi, 2008). Kingdom: Animalia
Filum: Chordata Subfilum: Vertebrata Kelas: Mamalia Ordo: Rodentia Famili: Muridae Genus: Mus
Mencit memiliki beberapa data biologis, diantaranya (Retnomurti, 2008): Lama hidup: 1-2 tahun
Lama produksi ekonomis: 9 bulan Lama hamil: 19-21 hari
Umur dewasa: 35 hari Umur dikawinkan: 8 minggu
Berat dewasa: 20-40 gram (jantan); 18-35 gram (betina)
2.5 Hati
2.5.1 Anatomi Hati
Hati adalah organ terbesar yang terdapat di dalam tubuh kita, letaknya di rongga perut di sebelah kanan bawah diafragma. Hati berwarna merah tua dan beratnya ± 1,5 kg. Hati terbagi dalam dua belahan utama, kanan dan kiri. Permukaan atas berbentuk cembung dan terletak di bawah diafragma, permukaan bawah tidak rata dan memperlihatkan lekukan yang disebut fisura tranversus (Irianto, 2004).
Hati tersusun oleh beberapa tipe sel, yaitu: a. hepatosit
Sel-sel ini merupakan 70% dari semua sel di hati dan 90% dari berat hati total. Hepatosit tersusun dalam unit-unit fungsional yang disebut asinus atau lobules. Setiap lobules memiliki sebuah vena sentral (vena terminalis) dan traktus portal yang terletak di perifer.
b. sel duktus biliaris
hepar, dengan ukuran dan garis tengahnya secara bertahap membesar. c. sel vaskular
Hati memiliki pendarahan ganda. Organ ini menerima darah melalui arteri hepatika dan vena porta. Arteri hepatika dan vena porta masuk ke hati di porta hepatis lalu bercabang menjadi pembuluh yang lebih halus berjalan sejajar sampai mencapai vena sentralis.
d. sinusoid
Sinusoid hati adalah saluran darah yang melebar dan berliku-liku, sinusoid hati dipisahkan dari hepatosit dibawahnya oleh spatium perisinusoideum (disse) subendotelial. Akibatnya, zat makanan yang mengalir di dalam sinusoid memiliki akses langsung melalui dinding endothelial yang tidak utuh dengan hepatosit. Struktur dan jalur sinusoid yang berliku di hati memungkinkan pertukaran zat yang efisien antara hepatosit dan darah. Selain sel endotel, sinusoid hati juga mengandung makrofag, yang disebut sel kuppfer (macrophagocytus stellatus), terletak di sepanjang sinusoid.
e. kandung empedu
Kandung empedu adalah organ kecil berongga yang melekat pada permukaan bawah hati. Empedu diproduksi oleh hepatosit dan kemudian mengalir melalui kanalikuli dan disimpan di dalam kandung empedu (Eroschenko, 2004).
meninggalkan hati melalui vena hepatika yang mengalir menuju vena kava inferior (Underwood, 1994).
2.5.2 Fungsi Hati
Organ hati terlibat dalam metabolisme zat makanan serta sebagian besar obat dan toksikan (Lu, 1994). Hati mempunyai fungsi yang sangat banyak dan kompleks yang penting untuk mempertahankan hidup (Husadha, 1996) yaitu: a. fungsi pembentukan dan eksresi empedu
Hal ini merupakan fungsi utama hati yaitu mengeksresikan sekitar satu liter empedu setiap hari. Garam empedu penting untuk pencernaan dan absorbsi lemak dalam usus halus.
b. fungsi metabolik
Hati berperan penting dalam metabolisme karbohidrat, lemak, protein, vitamin dan juga memproduksi energi. Hati mengubah ammonia menjadi urea untuk dikeluarkan melalui ginjal dan usus.
c. fungsi pertahanan tubuh
Hati mempunyai fungsi detoksifikasi dan perlindungan yang dilakukan oleh enzim-enzim hati untuk melakukan oksidasi, reduksi, hidrolisis atau konjugasi zat yang kemungkinan membahayakan dan mengubahnya menjadi zat yang secara fisiologis tidak aktif. Fungsi perlindungan dilakukan oleh sel kupffer yang terdapat di dinding sinusoid hati.
2.5.3 Biokimia Hati
Hati mampu mengsekresikan enzim - enzim transaminase saat selnya mengalami gangguan. Transaminase merupakan indikator yang peka pada
a. ALT (alanin aminotransferase)
Enzim ini mengkatalis pemindahan satu gugus amino antara lain alanin dan α-ketoglutarat menjadi glutamate dan piruvat yang bersifat reversibel.
Terdapat banyak di hepatosit dan konsentrasinya relatif rendah di jaringan lain. Aktivitas normal dalam darah 5 – 35 U/L pada manusia (Husadha, 1996), pada mencit adalah 25 – 200 IU/L (Hall, 2007). ALT lebih sensitif dibandingkan AST (Sacher dan Person, 2002).
b. AST (aspartat aminotransferase)
Enzim ini berfungsi sebagai katalisator reaksi antara asam aspartat dan asam α-ketoglutarat menjadi glutamate dan oksalasetat yang bersifat reversibel.
AST terdapat lebih banyak di jantung dibandingkan di hati, selain itu enzim ini juga terdapat di otot rangka, otak dan ginjal. Aktivitas normal dalam darah 10 – 40 U/L dan meningkat tajam apabila terjadi infark miokardium (Husadha, 1996). Enzim ini kurang spesifik untuk penyakit hati (Gaze, 2007).
Ketika sel hati mengalami kerusakan, enzim transaminase tersebut berada di dalam darah, sehingga dapat diukur aktivitasnya. Hal ini disebabkan karena terjadi kerusakan pada struktur dan fungsi membran sel hati, aktivitas ALT lebih dini dan lebih cepat meningkat dari aktivitas AST (Widmann, 1995).
2.5.4 Gangguan Fungsi Hati Akibat Zat Toksik
Jenis-jenis kerusakan hati yang disebabkan oleh zat toksik antara lain (Lu, 1994):
a. steatosis (perlemakan hati)
b. kolestasis
Kolestasis bersifat akut dan lebih jarang ditemukan jika dibandingkan steatosis dan nekrosis. Contoh penyebabnya yaitu klorpromazin dan eritromisin laktobionat.
c. karsiogenesis
Karsinoma hepatoseluler adalah jenis neoplasma ganas yang paling umum pada hati. Contoh penyebab karsiogenesis seperti vinil klorida, aflaktosin dan dioksin.
d. nekrosis
Nekrosis adalah kematian hepatosit. Nekrosis dapat bersifat sentral atau perifer, dan biasanya nekrosis merupakan kerusakan akut. Beberapa zat kimia telah dilaporkan dan terbukti sebagai penyebab nekrosis hati. Nekrosis hati merupakan suatu manifestasi toksik yang berbahaya, tetapi tidak selalu kritis karena mempunyai kapasitas yang luar biasa untuk pertumbuhan kembali. Contoh penyebab nekrosis hati yaitu karbon tetraklorida (CCl4), kloroform, isoniazida dan
parasetamol. Nekrosis hati oleh parasetamol bersifat sentrilobular. e. sirosis
Sirosis ditandai oleh adanya septa kolagen yang tersebar di sebagian besar hati. Pada sebagian besar kasus, sirosis disebabkan nekrosis sel tunggal karena kurangnya mekanisme perbaikan sehingga terjadi fibroblastik dan pembentukan jaringan parut. Penyebab sirosis yang paling penting adalah penggunaan kronis alkohol.
f. hepatitis yang mirip hepatitis virus
dapat dibedakan dari hepatitis virus. Pada umumnya, obat itu mempunyai ciri-ciri berikut:
i. kerusakan hati semacam itu tidak dapat diperlihatkan pada hewan. ii. tampaknya beberapa efek pada manusia tidak berkaitan dengan dosis. iii. masa laten sangat beragam.
iv. toksisitas hanya muncul pada beberapa individu yang rentan. v. gambaran histopatologi lebih beragam.
vi. biasanya pasien memperlihatkan tanda-tanda hipersensitivitas lain dan kadang- kadang bereaksi terhadap suatu dosis tantangan.