DIALISIS LARUTAN GARAM MENGGUNAKAN MEMBRAN
KITOSAN TERMODIFIKASI POLI(VINIL ALKOHOL)
DENGAN POLI(ETILENA GLIKOL) SEBAGAI POROGEN
RIKI ARIWANDA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2006
DIALISIS LARUTAN GARAM MENGGUNAKAN MEMBRAN
KITOSAN TERMODIFIKASI POLI(VINIL ALKOHOL)
DENGAN POLI(ETILENA GLIKOL) SEBAGAI POROGEN
RIKI ARIWANDA
Skripsi
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2006
Judul : Dialisis Larutan Garam Menggunakan Membran Kitosan Termodifikasi Poli(vinil alkohol) dengan Poli(etilena glikol) sebagai Porogen
Nama : Riki Ariwanda NIM : G44201056
Disetujui
Pembimbing I Pembimbing II
Drs. Ahmad Sjahriza Dra. Sri Mulijani, MS
NIP 131 842 413 NIP 131 950 978
Diketahui
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Dr. Ir. Yonny Koesmaryono, M.S.
NIP 131 473 999
PRAKATA
Alhamdulillah, segala puji dan syukur penulis ucapkan kepada Allah SWT atas rahmat
dan karunia-Nya karya ilmiah ini berhasil diselesaikan. Karya ilmiah ini berjudul Dialisis Larutan Garam Menggunakan Membran Kitosan Termodifikasi Poli(vinil alkohol) dengan Poli(etilena glikol) sebagai Porogen. Penelitian ini dilaksanakan mulai bulan Desember 2005 hingga Juni 2006 di Laboratorium Kimia Fisik dan Lingkungan Departemen Kimia Institut Pertanian Bogor.
Terimakasih penulis ucapkan kepada Bapak Drs. Ahmad Sjahriza dan Ibu Dra. Sri Mulijani, MS selaku pembimbing yang telah membimbing dan memberikan masukkan serta pengarahan kepada penulis. Penulis juga mengucapkan terima kasih kepada almarhumah Mama, Papa, Widya, Angga, dan seluruh keluarga atas segala dukungan moril, materil, waktu, tenaga, doa, dan kasih sayangnya. Ucapan terima kasih juga disampaikan kepada Budi Arifin, S.Si, Rahmat, dan Dwi atas diskusi-diskusi dan bantuannya selama penelitian, Mas Heri, Pak Nano, Pak Mail, Mbak Ai, Pak Sabur, dan semua laboran, teknisi atas bantuan dan kerjasamanya, rekan-rekan satu Lab: Manuara, Dyah, dan Eka atas semangat dan kerjasamanya. Penulis juga mengucapkan terima kasih kepada teman-teman kimia: Mas Indra, Dedy, Joe, Nazer, dan Peris atas dorongan dan motivasinya bagi penulis. Terima kasih juga kepada Red House Permai Family (Anton, Zaim, dan Wisnu) atas bantuan, kerjasama, dan keceriaan yang terjalin.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat
.
RIWAYAT HIDUP
Penulis dilahirkan di Payakumbuh pada tanggal 11 November 1983 sebagai anak pertama dari tiga bersaudara dari pasangan Azhar Azis dan Elmiati (almarhumah). Tahun 2001 penulis lulus dari SMU Negeri 2 Payakumbuh dan pada tahun yang sama lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui jalur Ujian Masuk Perguruan Tinggi Negeri (UMPTN) pada Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA).
Selama mengikuti perkuliahan, penulis pernah mengikuti kegiatan Praktik Lapangan di Bagian Pemurnian Sera dan Diagnostik PT Bio Farma (Persero), Bandung dengan judul Pemurnian Serum Anti Bisa Ular Polivalen Ankystrodon rhodostoma, Bungarus
fasciatus dan Naja sputatrix (ABN). Selain itu penulis juga aktif di berbagai kegiatan
akademik dan non akademik. Penulis pernah menjadi asisten praktikum Kimia Dasar II, Kimia Organik Tingkat Persiapan Bersama, Kimia Organik II, Kimia Fisik I, Kimia Fisik II, Kimia Fisik TPG, dan Kimia Pangan.
DAFTAR ISI
Halaman
DAFTAR TABEL...viii
DAFTAR GAMBAR ...viii
DAFTAR LAMPIRAN... ix
PENDAHULUAN ... 1
TINJAUAN PUSTAKA ... 1
Kitin dan Kitosan ... 1
Glutaraldehida ... 2 Poli(vinil alkohol)... 2 Poli(etilena glikol) ... 2 Membran... 2 Pencirian Membran... 3 Dialisis ... 3
BAHAN DAN METODE ... 3
Bahan dan Alat ... 3
Metode Penelitian ... 4
HASIL DAN PEMBAHASAN... 5
Membran Kitosan Termodifikasi... 5
Pengaruh Waktu terhadap Dialisis... 5
Pengaruh Jenis Membran terhadap Dialisis... 5
Pengaruh Laju Alir terhadap Dialisis ... 6
Dialisis untuk Larutan Garam yang Berbeda... 7
SIMPULAN DAN SARAN... 8
Simpulan... 8
Saran ... 8
DAFTAR PUSTAKA ... 8
DAFTAR TABEL
Halaman
1 Parameter mutu kitosan ... 2
2 Faktor-faktor yang mempengaruhi tingkat permeasi ... 3
3 Komposisi PVA dan PEG untuk setiap jenis membran ... 4
4 Tebal membran berdasarkan jenis... 5
DAFTAR GAMBAR
Halaman 1 Struktur kimia kitin dan kitosan... 12 Struktur glutaraldehida... 2
3 Struktur PVA ... 2
4 Struktur PEG... 2
5 Sel dialisis ... 4
6 Skema rancangan aliran counter-current pada proses dialisis ... 4
7 Hubungan konsentrasi dengan waktu dialisis pada MD1 dengan ragam laju alir umpan dan permeat 20:20 (×10 mL/menit) ... 5
8 Hubungan konsentrasi dengan waktu dialisis NaCl dengan ragam laju alir umpan dan permeat 20:20 (×10 mL/menit) ... 6
9 Hubungan antara konsentrasi dan waktu dialisis KCl pada MD1 dengan beragam laju alir larutan umpan dan permeat ... 7
10 Hubungan konsentrasi dengan waktu dialisis pada MD3 dengan ragam laju alir umpan dan permeat 40:20 (×10 mL/menit) ... 7
DAFTAR LAMPIRAN
Halaman
1 Diagram alir penelitian ... 11
2 Hasil pengukuran kurva standar larutan NaCl dan KCl... 12
3 Data dialisis larutan garam dengan membran kitosan... 13
PENDAHULUAN
Udang merupakan salah satu hasil perikanan Indonesia yang banyak dikonsumsi oleh masyarakat. Selain dikonsumsi, udang juga banyak dimanfaatkan dalam dunia indus- tri sebagai salah satu komoditas ekspor non-migas. Limbah udang berupa bagian kepala dan kulit dapat dimanfaatkan sebagai sumber bahan baku pembuatan kitin dan kitosan yang berdaya guna dan bernilai tinggi di berbagai bidang industri modern, seperti farmasi, biokimia, kosmetika, industri kertas, industri pangan, dan industri tekstil.
Kitosan dapat digunakan sebagai bahan pembuat membran karena mempunyai gugus hidroksil dan amino yang reaktif dan tahan terhadap pelarut organik, dan kitosan dapat larut dalam asam organik encer seperti asam asetat encer (Aryanto 2002). Membran umum digunakan untuk memisahkan suatu molekul dari molekul-molekul yang lain dalam suatu larutan, diantaranya dalam proses dialisis seperti pemurnian protein, pemurnian pelarut, dan hemodialisis. Kitosan dapat dijadikan sebagai salah satu alternatif bahan dasar pembuat membran semipermeabel yang digunakan pada proses dialisis.
Penggunaan membran kitosan sering diiringi dengan modifikasi, antara lain berupa penambahan bahan atau polimer yang dapat membentuk tautan silang dengan molekul kitosan, seperti glutaraldehida atau genipin. Membran kitosan termodifikasi diharapkan dapat memiliki ciri-ciri yang lebih baik seperti peningkatan kestabilannya (Jin et al. 2004).
Membran kitosan pada penelitian ini akan dimodifikasi dengan menambahkan poli(vinil alkohol) (PVA) sebagai bahan pembentuk struktur semi-interpenetrating network (semi-IPN) karena sifat mekaniknya yang baik (Hassan & Peppas 2000). Penambahan PVA akan meningkatkan kekuatan membran kito- san. Menurut Nisa (2005), semakin tinggi konsentrasi PVA yang ditambahkan, membran yang dihasilkan akan semakin tebal.
Selain penambahan PVA, juga dilakukan penambahan glutaraldehida sebagai agen per- tautan silang, dan penambahan poli(etilena glikol) (PEG) sebagai porogen untuk mem- bentuk dan menyeragamkan pori-pori mem- bran (Yang et al. 2001).
Penelitian ini bertujuan untuk mempelajari perilaku dan karakter membran kitosan termo- difikasi pada proses dialisis larutan garam. Hipotesis penelitian ini adalah membran kitosan termodifikasi dapat digunakan untuk proses dialisis.
TINJAUAN PUSTAKA Kitin dan Kitosan
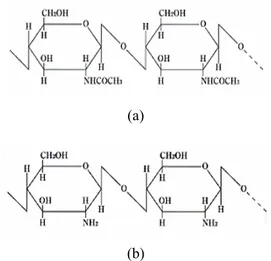
Kitin adalah biopolimer polisakarida turunan selulosa dengan rantai linear yang tersusun dari unit-unit berulang 2-asetamido-2-deoksi-D-glukopiranosa yang dihubungkan melalui ikatan glikosidik β(1→4). Kitin banyak terdapat pada invertebrata darat dan laut (Thatte 2004).
Pemutusan gugus asetil (deasetilasi) kitin oleh basa kuat menghasilkan kitosan (Sigma-Aldrich 1999). Kitin dan kitosan dapat dibedakan dari derajat deasetilasinya. Derajat deasetilasi kitosan biasanya berkisar antara 70–95%, bergantung pada metode yang digu- nakan dalam pembuatannya (Li et al. 1992). Gambar 1 menunjukkan struktur molekul kitin dan kitosan.
Salah satu metode yang digunakan untuk menentukan derajat deasetilasi adalah spektroskopi inframerah. Metode tersebut memiliki kelebihan antara lain analisis yang dilakukan relatif cepat dan tidak memerlukan contoh yang murni. Selain itu ketelitiannya tinggi dengan kisaran derajat deasetilasi contoh yang luas bila dibandingkan dengan teknik titrimetri atau metode spektroskopi lainnya (Baxter et al. 1992). Derajat deasetila- si kitosan yang dapat dijadikan membran anta- ra 77% sampai 85%. Selain derajat deasetila- si, kadar abu, kadar air, dan viskositas juga merupakan parameter yang penting bagi kito- san seperti terlihat pada Tabel 1.
(a)
(b)
Gambar 1 Struktur molekul kitin (a) dan kitosan (b) (Thatte 2004).
Tabel 1 Parameter mutu kitosan
Parameter Nilai Ukuran partikel Serpihan sampai bubuk
Kadar air ≤10%
Kadar abu ≤2%
Derajat deasetilasi ≥70% Warna larutan Jernih Viskositas: 1% kitosan (cps) Rendah <200 Medium 200-799 Tinggi 800-2.000 Ekstra tinggi >2.000 Sumber: Manullang (1997). Glutaraldehida
Glutaraldehida (Gambar 2) merupakan agen pertautan silang yang sering digunakan dalam polipeptida dan protein karena aktivi- tasnya yang tinggi. Glutaraldehida juga digu- nakan sebagai agen pertautan silang dengan PVA dan beberapa polisakarida lainnya seper- ti asam heparin, asam hialuronat, dan kitosan (Wang et al. 2004). Glutaraldehida merupakan senyawa yang umum digunakan dalam modi- fikasi protein dan polimer. Glutaraldehida mempunyai rumus molekul C5H8O2 dengan
bobot molekul sebesar 100.1 g/mol, titik didih sebesar 100 °C, titik lebur -15 °C, pH 3.2–4.2, serta berupa larutan berwarna kuning yang larut dalam air, alkohol, dan benzena (BASF 1999).
Gambar 2 Struktur glutaraldehida (Wang et al. 2004).
Poli(vinil alkohol)
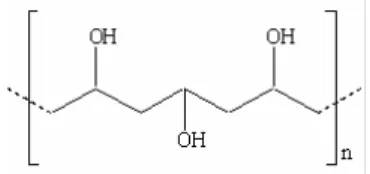
PVA (Gambar 3) memiliki struktur kimia yang sederhana dengan gugus hidroksil yang tidak beraturan. Monomernya, yaitu vinil alkohol, tidak berada dalam bentuk stabil, tetapi berada dalam keadaan bertautomerisasi dengan asetaldehida (Wang et al. 2004). PVA industri biasanya merupakan campuran dari beberapa tipe stereoregular yang berbeda (isotaktik, ataktik, dan sindiotaktik). Mutu PVA industri yang baik ditentukan oleh derajat hidrolisisnya. Semakin tinggi derajat hidrolisis, kelarutannya akan semakin rendah (Hassan & Peppas 2000).
Dalam pembuatan hidrogel kitosan-PVA, PVA dilarutkan dalam larutan kitosan pada
suhu 80 °C selama lima menit. Kombinasi kitosan-PVA dengan glutaraldehida sebagai agen pertautan silang menghasilkan struktur hidrogel semi-IPN. Hidrogel yang terbentuk dari kombinasi tersebut memiliki nisbah pem- bengkakan dan penyusutan yang tinggi, peka terhadap perubahan pH, serta mudah terurai secara alami (Wang et al. 2004).
Gambar 3 Struktur PVA (Csustan 1999).
Poli(etilena glikol)
PEG (Gambar 4) merupakan molekul sederhana dengan struktur molekul linear atau bercabang. Pada suhu ruang, PEG dengan bobot molekul di bawah 700 berbentuk cair, sedangkan yang memiliki bobot molekul 700– 900 berbentuk semipadat, dan PEG dengan bobot molekul lebih dari 900 berbentuk padatan. PEG larut dalam air dan beberapa pelarut organik seperti toluena, aseton, metanol, dan metil klorida tetapi tidak larut dalam heksana dan hidrokarbon alifatik yang sejenis (Fadillah 2003).
Interaksi konsentrasi PEG dengan selulosa asetat menunjukkan pengaruh yang sangat nyata terhadap ukuran pori-pori membran (Fadillah 2003). Fluks membran akan bertam- bah dengan bertambahnya konsentrasi PEG dan dengan berkurangnya konsentrasi selulosa asetat.
H O
H O
Gambar 4 Struktur PEG (Wikipedia 2006).
Membran
Membran adalah lapisan semipermeabel berupa padatan polimer tipis yang menahan pergerakan bahan tertentu (Scott & Hughes 1996). Menurut Osada & Nakagawa (1992), membran merupakan lapisan semipermeabel tipis yang dapat digunakan untuk memisah- kan dua komponen dengan cara menahan dan melewatkan komponen tertentu melalui pori-pori.
Membran dapat disiapkan dengan menggunakan beberapa metode antara lain
pelelehan, pengepresan, track-etching, dan pembalikan fase. Pembalikan fase adalah proses pengubahan polimer dari bentuk larutan menjadi bentuk padatan secara terkendali. Proses pemadatan sangat sering diawali dengan perpindahan polimer dari suatu cairan (pelarut) ke cairan lainnya (non-pelarut). Fase dengan konsentrasi polimer yang tinggi dalam larutan akan membentuk padatan atau matriks membran, sedangkan fase dengan konsentrasi polimer yang rendah akan membentuk pori-pori (Mulder 1996).
Pencirian Membran
Membran dapat dicirikan berdasarkan struktur maupun fungsinya. Beberapa ciri membran antara lain ketebalan, kandungan air, permeabilitas, ukuran pori, distribusi ukuran pori, dan beberapa sifat fisik dan kimianya. Membran juga dapat dicirikan berdasarkan koefisien difusi, rejeksi zat terlarut, fluks, potensial membran, jumlah pelarut yang dipindahkan melewati membran, dan volume elektroosmotik.
Dialisis
Dialisis diartikan sebagai pergerakan zat terlarut melewati membran semipermeabel dari larutan berkonsentrasi tinggi pada salah satu sisi membran menuju sisi lainnya yang memiliki konsentrasi yang lebih rendah (Baker 2004). Dialisis menggunakan membran semipermeabel yang melewatkan ion dan molekul kecil, tetapi menghalangi partikel koloid yang berukuran besar (Hunt 2003). Dialisis lazim digunakan pada bidang kedokteran sebagai metode pencucian darah pada pasien yang mengalami kerusakan ginjal.
Dialisis menggunakan suatu membran semipermeabel untuk memisahkan spesies berdasarkan perbedaan tingkat difusi pada membran. Larutan umpan yang berisi zat terlarut yang akan dipisahkan dialirkan pada satu sisi membran, dan pelarut dialirkan pada sisi membran yang lain. Beberapa pelarut juga dapat berdifusi-silang melewati membran dengan arah yang berlawanan, yang akan mengurangi kinerja dialisis karena terjadi pengenceran larutan umpan.
Dalam praktiknya dialisis digunakan un- tuk memisahkan spesies yang mempunyai per- bedaan ukuran dan juga mempunyai perbeda- an tingkat difusi yang besar. Fluks zat terlarut bergantung pada perbedaan konsentrasi pada membran. Oleh karena itu, dialisis ditandai dengan tingkat fluks yang lebih rendah dibandingkan dengan proses membran lain
seperti osmosis balik (reverse osmosis) atau ultrafiltrasi, yang tergantung pada tekanan yang diberikan.
Proses dialisis zat terlarut terjadi pada permukaan membran, dengan perbedaan kon- sentasi dari larutan yang berada di kedua sisi membran. Proses ini dipengaruhi oleh bebera- pa peubah seperti suhu, viskositas, dan tingkat pencampuran larutan.
Pergerakan zat terlarut melewati membran semipermeabel adalah hasil dari gerakan mo- lekul secara acak. Sebagai molekul terlarut dalam gerakan larutan, maka akan terjadi tum- bukan dari waktu ke waktu antara molekul zat terlarut dan membran serta antar molekul zat terlarut itu sendiri sampai mereka berdifusi.
Tingkat perpindahan zat terlarut melewati membran semipermeabel sebagian besar ber- gantung pada bentuk, muatan, dan ukuran zat terlarut. Ukuran zat terlarut sangat berhubung- an dengan bobot molekul. Permeasi zat terla- rut melewati membran semipermeabel dalam larutan berbanding terbalik dengan bobot mo- lekul. Faktor-faktor yang memengaruhi ting- kat permeasi dapat dilihat pada Tabel 2.
Tabel 2 Faktor-faktor yang mempengaruhi tingkat permeasi
Pengaruh terhadap tingkat permeasi
Parameter
Menaikkan Menurunkan Perbedaan
konsentrasi Besar Kecil
Ukuran molekul Kecil, berbentuk bola Besar, berbentuk serat
Temperatur Tinggi Rendah
Ketebalan membran Tipis (<20 µm) Tebal (>20 µm) Luas permukaan
membran Besar Kecil
Sumber: McPhie (1971).
BAHAN DAN METODE Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini antara lain kitosan dengan derajat deasetilasi 77.81%, akuades, asam asetat 1% (v/v), larutan NaOH 1 M, PVA (BM=72000), glutaraldehida 33.30 µM, PEG (BM=6000), NaCl, dan KCl. Alat-alat yang digunakan adalah alat-alat kaca, sel dialisis, pompa, pengaduk magnetik, neraca analitik, pemanas, lempeng kaca, dan plastik polietilena.
Metode Penelitian
Bagan alir penelitian ini dapat dilihat secara garis besar pada Lampiran 1. Penelitian ini dilakukan dalam beberapa tahapan yaitu pembuatan larutan kitosan 3% (b/v) dalam asam asetat 1% (v/v), dilanjutkan dengan pembuatan dope membran yang terdiri dari campuran larutan kitosan tersebut, PVA (2.5 dan 5.0%), PEG (2.5 dan 5.0%), dan glutaraldehida 33.30 μM. Kemudian dilanjut- kan dengan pencetakan membran (metode pembalikan fase) dan proses dialisis larutan garam pada membran yang telah terbentuk.
Pembuatan larutan kitosan 3% (b/v)
Sebanyak 3 gram kitosan dilarutkan ke dalam asam asetat 1% (v/v). Campuran diaduk dengan pengaduk magnetik sampai seluruh kitosan larut sampai menjadi larutan kental jernih kekuningan.
Pembuatan dope
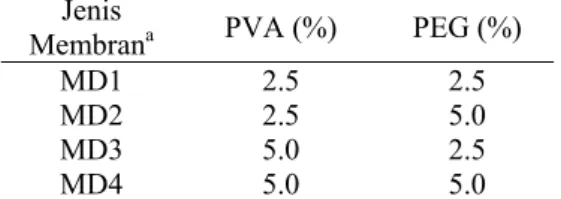
PVA dimasukkan ke dalam larutan kitosan 3% (b/v) dalam gelas piala dan diaduk dengan pengaduk magnetik sambil dipanaskan pada suhu 80 °C selama lima menit untuk me- larutkan semua PVA. Digunakan ragam kon- sentrasi PVA 2.5 dan 5.0% (b/v). Selama pemanasan, gelas piala ditutup dengan plastik polietilena. Setelah didinginkan pada suhu ruang, ditambahkan PEG, juga dengan ragam konsentrasi 2.5 dan 5.0% (b/v), ke dalam campuran kitosan-PVA sambil diaduk selama 30 menit sampai semua PEG larut. Terakhir, glutaraldehida 25% (v/v) ditambahkan ke dalam setiap campuran dengan konsentrasi akhir glutaraldehida 33.30 μM, dan diaduk selama 30 menit sampai semuanya bercampur. Setelah itu, setiap campuran (dope) ditutup dengan plastik polietilena dan didiamkan selama 12 jam untuk menghilangkan gelem- bung udara dari dalamnya. Komposisi PVA dan PEG untuk setiap jenis membran ditun- jukkan pada Tabel 3.
Tabel 3 Komposisi PVA dan PEG untuk setiap jenis membran
Jenis
Membrana PVA (%) PEG (%)
MD1 2.5 2.5 MD2 2.5 5.0 MD3 5.0 2.5 MD4 5.0 5.0 a MD = membran dialisis Pencetakan membran
Setiap dope yang sudah terbebas dari gelembung-gelembung udara kemudian dice- tak di atas permukaan lempeng kaca yang berukuran 20 cm × 15 cm dengan cara dituang ke atasnya sampai diperoleh lapisan tipis yang rata. Cetakan tersebut kemudian diuapkan se- lama 12 jam lalu dicelupkan ke dalam NaOH 1 M dalam wadah berukuran 30 cm × 20 cm selama 2–3 jam. Membran yang telah tercetak dilepaskan dari permukaan lempeng kaca dan dicuci dengan akuades untuk menghilangkan NaOH. Membran dibentuk dengan ukuran 20 cm × 5 cm kemudian disimpan dalam akuades sampai proses dialisis dilakukan.
Proses dialisis
Membran yang terbentuk ditempatkan dalam alat dialisis. Larutan garam dengan konsentrasi 0.10 M dialirkan pada salah satu sisi membran sebagai aliran umpan, sementara pada sisi lainnya dialirkan larutan garam dengan konsentrasi 0.01 M sebagai aliran per- meat. Proses dialisis menyebabkan zat terlarut akan berdifusi dari aliran larutan garam yang konsentrasinya lebih tinggi melewati mem- bran menuju aliran larutan garam yang kon- sentrasinya lebih rendah. Dilakukan peragam- an terhadap laju alir larutan umpan (20 dan 40 × 10 mL/menit) dengan permeat dibiarkan te- tap (20 × 10 mL/menit). Kemudian dilihat pengaruh peragaman terhadap proses dialisis yang berlangsung. Garam yang melintasi membran selama dialisis diperoleh dengan ca- ra menghitung konsentrasi larutan garam yang ada pada kedua sisi membran setiap lima me- nit selama satu jam dengan metode kondukto- metri. Gambar 5 dan 6 berturut-turut memper- lihatkan sel dialisis dan rancangan percobaan dialisis yang dilakukan.
Gambar 5 Sel dialisis.
Gambar 6 Skema modul aliran counter- current pada proses dialisis.
HASIL DAN PEMBAHASAN Membran Kitosan Termodifikasi
Pembentukan membran dengan penam- bahan PVA 5.0% (b/v) berlangsung lebih mu- dah, dengan produk membran yang diperoleh lebih baik dan lebih kuat dibandingkan dengan membran yang dibentuk dari penam- bahan PVA 2.5% (b/v). Hal tersebut menun- jukkan bahwa sifat mekanik PVA mampu menstabilkan membran yang dibentuknya (Hassan & Peppas 2000). Membran yang ter- bentuk beragam ketebalannya (Tabel 4). Hal tersebut dikarenakan perbedaan konsentrasi PVA dan PEG yang ditambahkan serta proses pencetakan.
Tabel 4 Tebal membran berdasarkan jenis Jenis Membrana Tebal (μm)
MD1 74 MD2 79 MD3 86 MD4 92
a MD = membran dialisis
Pengukuran ketebalan membran memper- lihatkan bahwa membran dengan konsentrasi PVA yang lebih tinggi akan lebih tebal daripada membran yang dibentuk dengan konsentrasi PVA lebih rendah. Konsentrasi PVA yang tinggi membuat dope membran lebih kental dan karena itu, lebih sulit dicetak.
Membran yang terbentuk memiliki struktur semi-IPN dari campuran kitosan-PVA dengan glutaraldehida sebagai agen pertautan silang (Nisa 2005). Tautan silang terbentuk antara rantai-rantai kitosan sementara pada rantai-rantai PVA tidak terbentuk tautan silang. Tautan silang yang terjadi berupa ikatan kovalen koordinasi antara gugus amino (-NH2) dari rantai kitosan dan atom karbon
pada gugus aldehida dari glutaraldehida (Wang et al. 2004).
Pengaruh Waktu tehadap Dialisis
Hasil pengukuran kurva standar hubungan antara konsentrasi dengan konduktivitas mem- berikan persamaan y = 102781x – 65.342 un- tuk NaCl dan y = 122049x – 82.548 untuk KCl (Lampiran 2). Persamaan ini digunakan untuk menghitung konsentrasi NaCl dan KCl selama proses dialisis.
Dialisis akan terus berjalan seiring dengan bertambahnya waktu hingga tercapai keadaan setimbang antara konsentrasi-konsentrasi la- rutan garam di kedua sisi membran. Terjadi- nya gejala ini dikarenakan dialisis mengguna-
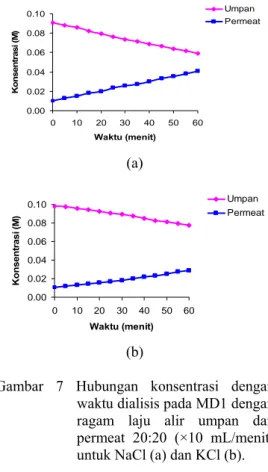
kan prinsip difusi sederhana. Zat terlarut akan berpindah dari larutan yang konsentrasinya le- bih tinggi menuju larutan dengan konsentrasi yang lebih rendah melewati pori-pori mem- bran kitosan. Gejala ini ditunjukkan oleh Gambar 7. 0.00 0.02 0.04 0.06 (a) (b)
Gambar 7 Hubungan konsentrasi dengan waktu dialisis pada MD1 dengan ragam laju alir umpan dan permeat 20:20 (×10 mL/menit) untuk NaCl (a) dan KCl (b). Nilai konsentrasi garam pada larutan um- pan terus turun seiring dengan bertambahnya waktu. Sebaliknya, konsentrasi garam pada permeat terus bertambah. Proses dialis ini akan terus berlangsung sampai saat tidak ada lagi perubahan konsentrasi yang terjadi baik pada larutan umpan maupun permeat.
Dari waktu ke waktu konsentrasi naik atau turun dengan stabil. Dengan kata lain, proses dialisis berlangsung secara bertahap dengan perpindahan zat terlarut berlangsung stabil se- tiap satuan waktunya. Tidak terjadi perpindah- an zat terlarut secara spontan dalam jumlah besar pada suatu waktu, tetapi sangat kecil pada waktu yang lain.
Pengaruh Jenis Membran terhadap Dialisis
Setiap jenis membran yang berbeda tentu saja akan memberikan pengaruh yang berbeda terhadap proses dialisis. Hal ini disebabkan membran dengan jenis yang berbeda automa- tis akan tersusun dari komposisi bahan penyu-
0. s i (M ) 08 0.10 0 10 20 30 40 50 60 Waktu (menit) Kons entra Umpan Permeat 0.00 0.02 0.04 0.06 0.08 0.10 0 10 20 30 40 50 60 Waktu (menit) K o n sen tr as i (M ) Umpan Permeat
sun yang berbeda baik secara kualitatif atau kuantitatif. Gambar 8 menunjukkan pengaruh berbagai jenis membran terhadap proses dialisis.
(a)
(b)
(c)
(d)
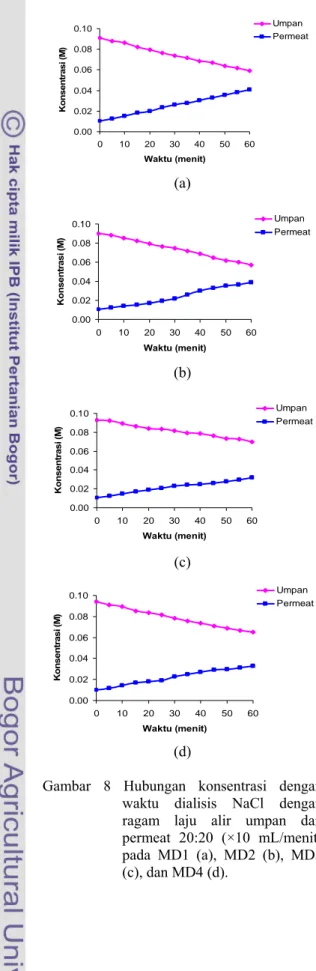
Gambar 8 Hubungan konsentrasi dengan waktu dialisis NaCl dengan ragam laju alir umpan dan permeat 20:20 (×10 mL/menit) pada MD1 (a), MD2 (b), MD3 (c), dan MD4 (d).
MD1 dan MD2 yang terbentuk dari pe- nambahan PVA dengan konsentrasi 2.5% (b/v) dan merupakan membran yang tipis. Ka- rena itu, proses dialisis akan berlangsung lebih cepat pada kedua jenis membran tersebut dibandingkan dengan pada MD3 dan MD4 yang tersusun dari PVA dengan konsentrasi 5.0% (b/v). Ketebalan membran merupakan salah satu faktor yang mempengaruhi dialisis. Semakin tebal membran yang harus dilewati zat terlarut pada proses dialisis, dialisis akan berjalan lebih lambat. Sebagaimana terlihat pada Gambar 8, penurunan konsentrasi larutan umpan dan kenaikan konsentrasi permeat NaCl lebih tajam pada MD1 dan MD2 dibandingkan dengan pada MD3 dan MD4. Hal yang sama juga berlaku untuk larutan KCl. 0.00 0.02 0.04 0.06 0.08 0.10 0 10 20 30 40 50 60 Waktu (menit) K onsent rasi ( M ) Umpan Permeat 0.00 0.02 0.04 0.06 0.08 0.10 0 10 20 30 40 50 60 Waktu (menit) K o n s e n tr a s i (M ) Umpan Permeat
Pengaruh penambahan PEG pada setiap jenis membran untuk proses dialisis terlihat jelas dengan membandingkan MD3 dengan MD4. MD3 dan MD4 dibentuk dengan kon- sentrasi PVA yang sama, tetapi dengan kon- konsentrasi PEG yang berbeda. Dialisis pada MD3 [konsentrasi PEG lebih rendah 2.5% (b/v)] berlangsung lebih lambat dibandingkan dengan MD4 [konsentrasi PEG 5.0% (b/v)]. Gejala ini dapat dilihat dari gradien kurva penurunan konsentrasi umpan atau kenaikan konsentrasi permeat untuk kedua membran tersebut. MD3 (Gambar 8c) memiliki gradien 4.0×10-4 M/menit untuk penurunan konsentra-
si umpan dan 3.0×10-4 M/menit untuk kenaik-
an konsentrasi permeat, sedangkan MD4 (Gambar 8d) memiliki gradien berturut-turut 5.0×10-4 M/menit dan 4.0×10-4 M/menit untuk
kedua hal di atas.
0.00 0.02 0.04 0.06 0.08 0.10 0 10 20 30 40 50 60 Waktu (menit) K onsent rasi (M ) Umpan Permeat
Hal ini dapat terjadi karena PEG yang di- tambahkan ke dalam dope pada saat pemben- tukan membran akan hilang pada saat pence- cetakan dan pencucian membran, dengan meninggalkan pori pada membran itu. Semakin tinggi konsentrasi PEG yang ditam- bahkan, pori yang terbentuk akan semakin banyak. Semakin banyak pori yang terbentuk, dialisis tentu saja akan berjalan lebih cepat karena zat terlarut akan mempunyai lebih banyak jalan untuk melewati membran.
0.00 0.02 0.04 0.06 0.08 0.10 0 10 20 30 40 50 60 Waktu (menit) Konsentrasi (M ) Umpan Permeat
Pengaruh Laju Alir pada Dialisis
Skema counter-current memungkinkan untuk dilakukannya peragaman laju alir larutan umpan dan permeat. Laju alir umpan dan permeat yang digunakan didapat memengaruhi kecepatan dialisis (Gambar 9).
Gambar 9 Hubungan antara konsentrasi dan waktu dialisis KCl pada MD1 dengan beragam laju alir larutan umpan dan permeat.
Dialisis yang dilakukan dengan laju alir larutan umpan dan permeat 40:20 (×10 mL/menit) berlangsung lebih cepat dibanding- kan dengan dialisis yang dilakukan dengan pada variasi 20:20 (×10 mL/menit). Sebagai- mana terlihat pada Gambar 9, penurunan kon- sentrasi larutan umpan dan kenaikan konsen- trasi permeat KCl pada MD1 lebih tajam pada 40:20 (×10 mL/menit). Gejala yang sama juga ditunjukkan pada MD2, MD3, dan MD4 serta larutan NaCl pada semua jenis membran. Data selengkapnya disajikan pada Lampiran 3. Dengan laju alir yang lebih cepat, larutan umpan mempunyai energi lebih besar daripada permeat. Energi tersebut dapat mem- buat zat terlarut dari larutan umpan bergerak lebih cepat melewati membran.
Laju alir yang lebih cepat juga mengaki- batkan pergerakan molekul-molekul zat terla- rut di dalam larutan umpan menjadi lebih ce- pat. Semakin cepat gerakannya, tumbukan antar molekul zat terlarut maupun antara mo- lekul zat terlarut dan permukaan menjadi se- makin banyak. Hal ini akan membuat proses dialisis berlangsung lebih cepat. Secara teore- tis, semakin besar perbedaan laju alir terse- but, laju dialisis akan semakin besar.
Dialisis untuk Larutan Garam yang Berbeda
Proses dialisis untuk larutan yang berbeda akan memberikan hasil yang berbeda pula. Tingkat perpindahan zat terlarut melewati membran semipermeabel sebagian besar bergantung pada bentuk, muatan, dan ukuran zat terlarut. Ukuran zat terlarut sangat berhubungan dengan bobot molekul.
Ukuran molekul memengaruhi seberapa cepat molekul tersebut dapat bergerak melalui pori-pori membran. Apabila ukuran molekul mendekati atau melebihi ukuran pori-pori membran, jalan zat terlarut untuk melewati
membran akan dihambat sepenuhnya atau sebagian. Dengan kata lain, molekul yang memiliki ukuran atau bobot molekul lebih besar akan lebih lambat melewati membran pada proses dialisis (Hunt 2003). Gambar 10 menunjukkan perbandingan laju dialisis antara dua larutan garam yang berbeda yaitu NaCl dan KCl. 0.00 0.02 0.04 0.06 0.08 0.10 0 10 20 30 40 50 60 Waktu (menit) K ons ent rasi (M ) Umpan 20:20 (x10 mL/menit) Permeat 20:20 (x10 mL/menit) Umpan 40:20 (x10 mL/menit) Permeat 40:20 (x10 mL/menit) 0.00 0.02 0.04 0.06 0.08 0.10 0 10 20 30 40 50 60 Waktu (menit) K o n sen tras i (M ) Umpan Permeate (a) 0.00 0.02 0.04 0.06 0.08 0.10 0 10 20 30 40 50 60 Waktu (menit) Kon s ent ra si ( M ) Umpan Permeat (b)
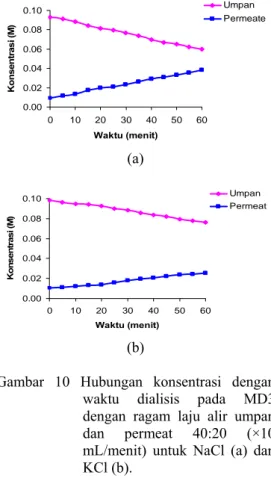
Gambar 10 Hubungan konsentrasi dengan waktu dialisis pada MD3 dengan ragam laju alir umpan dan permeat 40:20 (×10 mL/menit) untuk NaCl (a) dan KCl (b).
Proses dialisis larutan KCl (BM=74.5) melewati membran kitosan termodifikasi berlangsung lebih lambat dibandingkan dengan larutan NaCl (BM=58.5). Hal yang sama juga berlaku untuk MD1, MD2, dan MD4. Data selengkapnya diberikan pada Lampiran 4. Hal ini terdeteksi dari penurunan dan kenaikan konsentrasi NaCl pada larutan umpan dan permeat yang lebih besar dibandingkan dengan KCl dalam waktu yang sama. Larutan NaCl memberikan kemiringan garis sebesar 6.0×10-4 M/menit dan 5.0×10-4
M/menit berturut-turut untuk penurunan konsentrasi umpan dan kenaikan konsentrasi permeat pada MD3 dengan variasi laju alir umpan dan permeat 40:20 (×10 mL/menit). Sementara itu, larutan KCl memiliki kemiringan berturut-turut sebesar 4.0×10-4
M/menit dan 3.0×10-4 M/menit pada kondisi
SIMPULAN DAN SARAN Simpulan
Membran kitosan yang terbentuk dari penambahan PVA dengan konsentrasi lebih tinggi memiliki sifat mekanik yang lebih baik. Membran kitosan-PVA yang dibuat bisa digunakan untuk proses dialisis. Dialisis akan terus berjalan seiring dengan bertambahnya waktu.
Dialisis berjalan lebih cepat pada membran yang terbentuk dari penambahan PVA dengan konsentrasi lebih rendah. Membran yang terbentuk dengan penambahan konsentrasi PEG lebih tinggi lebih mudah dilewati zat terlarut dan proses dialisis akan berjalan lebih cepat. MD4 dapat digunakan sebagai lapisan semipermeabel yang baik dibandingkan dengan MD1, MD2, dan MD3 untuk dialisis larutan garam NaCl dan KCl.
Laju alir larutan umpan dan permeat juga mempengaruhi kecepatan dialisis. Dialisis yang dilakukan dengan ragam laju alir larutan umpan dan permeat 40:20 (×10 mL/menit) berlangsung lebih cepat apabila dibandingkan dengan 20:20 (×10 mL/menit) pada semua jenis membran yang dibuat terutama pada MD1.
Zat terlarut dengan ukuran molekul atau bobot molekul lebih besar (KCl) akan lebih lambat melewati membran dibandingkan dengan zat terlarut dengan molekul lebih kecil (NaCl).
Saran
Perilaku dan karakter membran kitosan termodifikasi pada proses dialisis dalam penelitian ini difokuskan terhadap waktu, jenis membran, laju alir umpan dan permeat, dan molekul dengan konsentrasi yang berbeda, sedangkan masih ada faktor lain yang mempengaruhi proses dialisis yaitu temperatur, viskositas, dan tingkat pencampuran larutan.
Zat terlarut dengan ukuran molekul lebih besar perlu diuji proses dialisisnya pada membran kitosan termodifikasi untuk mengetahui ukuran molekul maksimal yang dapat melewati membran kitosan termodifi- kasi pada proses dialisis. Diperlukan pengaturan ketebalan dan besar pori-pori membran untuk mengendalikan proses dialisis yang berlangsung.
DAFTAR PUSTAKA
Aryanto AY. 2002. Pemanfaatan kitosan dari limbah kulit udang (crustacea) sebagai bahan untuk pembuatan membran [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor. Baker RW. 2004. Membrane Technology and
Applications. London: Wiley.
BASF. 1999. Glutaraldehide-50%. New Jersey: BASF.
Baxter A, Dillon M, Taylor KD, Roberts GAF. 1992. Improved Method for IR Determination of the Degree of N-Acetylation of Chitosan. Biomacromol 14: 166-169.
Csustan. 1999. The Structure and Properties of Polymers. http://wwwchem.csustan. edu/CHEM2000/EXP2/bkg.htm [10 April 2006].
Fadillah F. 2003. Pengaruh penambahan PEG terhadap karakterisasi membran selulosa asetat [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Hassan CM, Peppas NA. 2000. Structure and aplication of poli(vinyl alcohol) hidrogel produced by conventional crosslinking or by freezing/thawing methods. Adv Polym Sci 153:37-38.
Hunt A. 2003. A-Z Chemistry. London: McGraw-Hill.
Jin J, Song M, Hourston DJ. 2004. Novel chitosan-based film cross-linking by genepin with improved physical properties. Biomacromol 5:165-168.
Koros WJ, Ma YH, Shimidzu T. 1996. Terminology for Membranes and Membrane Processes (IUPAC Recommendation 1996). Internat Pure and Appl Chem 68:1479-1489.
Li Q, Dunn ET, Grandmaison EW, Goosen MFA. 1992. Applications and properties of chitosan. Di dalam: Goosen MFA, editor. Applications of Chitin and Chitosan. Lancaster: Technomic. Hlm 3-21.
Manullang EH. 1997. Optimasi proses pembuatan kitin dari limbah udang (Penaid sp.) dengan menggunakan bahan teknis [skripsi]. Bogor: Fakultas Perikanan, Institut Pertanian Bogor.
McPhie P. 1971. Dialysis. Meth Enzymol 22:23-33.
Meloan CE. 1999. Chemical Separations: Principles, Techniques, and Experiments. London: J Wiley.
Mulder M. 1996. Basic and Principles of Membrane Technology. London: Kluwer. Nisa K. 2005. Karakteristik fluks membran
kitosan termodifikasi poli(vinil alkohol) dengan variasi poli(etilena glikol) sebagai porogen [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Osada Y, Nakagawa T. 1992. Membrane Science and Technology. New York: Marcel Dekker.
Scott K, Hughes R. 1996. Industrial Membrane Separation Technology. London: Blackie Academic and Professionals.
Sigma-Aldrich. 1999. Search result for: 9012-76-4. http://www.sigma-aldrich.com [16 Agustus 2004].
Thatte MR. 2004. Synthesis and antibacterial assessment of water-soluble hydrophobic chitosan derivatives bearing quaternary ammonium functionality. [dissertation]. India: The Louisiana State University. Wang H, Fang Y, Yan Y. 2001. Surface
modification of chitosan membranes by alkane vapor plasma. Mater Chem 11:911-918.
Winkipedia. 2006. Polyethylene glycol. http://en.wikipedia.org/wiki/Polyethylene glycol [10 April 2006].
Yang L, Hsiao WW, Chen P. 2001. Chitosan-cellulose composite membrane for affinity purifications of biopolymers and immunoadsorption. J Membr Sci 5084: 1-13.
Lampiran 1 Diagram alir penelitian
Kitosan (3 gram)
Pelarutan dalam asam asetat 1% (b/v)
PVA (2.5 dan 5.0%)
Larutan kitosan 3% glutaraldehida
PEG (2.5 dan 5.0%)
Dope membran (variasi jenis membran)
Pencetakan membran
Perendaman dalam NaOH 1 M
Membran
Pencucian membran dengan akuades
Penyimpanan membran dalam akuades
Lampiran 2 Hasil pengukuran kurva standar larutan NaCl dan KCl
Standar NaCl
Konsentrasi NaCl (M) Konduktivitas (µmhos)
0.10 10000 0.08 8400 0.06 6300 0.04 3790 0.02 1980 0.01 1000 y = 102781x - 65.342 R2 = 0.9967 0 2000 4000 6000 8000 10000 12000 0.00 0.02 0.04 0.06 0.08 0.10 Konsentrasi (M) K o n d u kt ivi tas ( μ mh o s) Standar KCl
Konsentrasi KCl (M) Konduktivitas (µmhos)
0.10 11900 0.08 10000 0.06 7400 0.04 4450 0.02 2380 0.01 1210 y = 122049x - 82.548 R2 = 0.9967 0 2000 4000 6000 8000 10000 12000 14000 0.00 0.02 0.04 0.06 0.08 0.10 Konsentrasi (M) K o n d u kt ivi tas ( μ mh o s)
Lampiran 4 Kurva data perubahan konsentrasi pada proses dialisis
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.10 0 5 10 15 20 25 30 35 40 45 50 55 60 Waktu (menit) K o n se n tr as i (M ) umpan (20:20) permeat (20:20) umpan (40:20) permeat (40:20)Hubungan antara waktu dan konsentrasi pada proses dialisis larutan NaCl pada MD1 dengan variasi laju alir
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.10 0 5 10 15 20 25 30 35 40 45 50 55 60 Waktu (menit) K o n sen tr asi ( M ) umpan (20:20) permeat (20:20) umpan (40:20) permeat (40:20)
Hubungan antara waktu dan konsentrasi pada proses dialisis larutan NaCl pada MD2 dengan variasi laju alir
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.10 0 5 10 15 20 25 30 35 40 45 50 55 60 Waktu (menit) K o n se n tr as i (M ) umpan (20:20) permeat (20:20) umpan (40:20) permeat (40:20)
Hubungan antara waktu dan konsentrasi pada proses dialisis larutan NaCl pada MD3 dengan variasi laju alir
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.10 0 5 10 15 20 25 30 35 40 45 50 55 60 Waktu (menit) K onsent rasi ( M ) umpan (20:20) permeat (20:20) umpan (40:20) permeat (40:20)
Hubungan antara waktu dan konsentrasi pada proses dialisis larutan NaCl pada MD4 dengan variasi laju alir
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.10 0 5 10 15 20 25 30 35 40 45 50 55 60 Waktu (menit) K onsent rasi ( M ) umpan (20:20) permeat (20:20) umpan (40:20) permeat (40:20)
Hubungan antara waktu dan konsentrasi pada proses dialisis larutan KCl pada MD1 dengan variasi laju alir
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.10 0 5 10 15 20 25 30 35 40 45 50 55 60 Waktu (menit) K o n sen tr asi ( M ) umpan (20:20) permeat (20:20) umpan (40:20) permeat (40:20)
Hubungan antara waktu dan konsentrasi pada proses dialisis larutan KCl pada MD2 dengan variasi laju alir
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.10 0 5 10 15 20 25 30 35 40 45 50 55 60 Waktu (menit) K o n sen tr asi ( M ) umpan (20:20) permeat (20:20) umpan (40:20) permeat (40:20)
Hubungan antara waktu dan konsentrasi pada proses dialisis larutan KCl pada MD3 dengan variasi laju alir
0.00 0.01 0.02 0.03 0.04 0.05 0.06 0.07 0.08 0.09 0.10 0 5 10 15 20 25 30 35 40 45 50 55 60 Waktu (menit) K o n sen tr asi ( M ) umpan (20:20) permeat (20:20) umpan (40:20) permeat (40:20)
Hubungan antara waktu dan konsentrasi pada proses dialisis larutan KCl pada MD4 dengan variasi laju alir