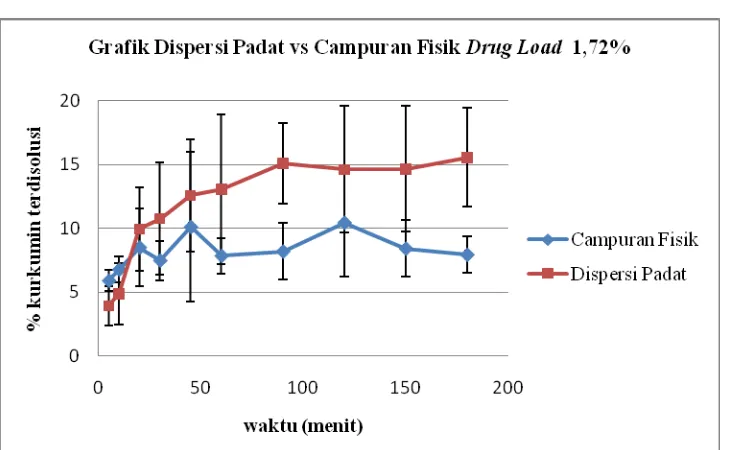
Pengaruh proporsi drug load terhadap disolusi dispersi padat vacuum dried isolat ekstrak rimpang kunyit (Curcuma domestica C-95)-Gom Guar - USD Repository
Teks penuh
Gambar

Dokumen terkait
Dalam konteks ini, peran pengawas pemilu adalah mengawasi setiap tahapan pemilu berlangsung dengan benar baik dari sisi proses maupun hasil, termasuk mengawasi
BPR Jatim adalah Perseroan Terbatas yang didirikan berdasarkan Peraturan Daerah Provinsi Jawa Timur Nomor 10 Tahun 2000 tentang Penggabungan dan Perubahan Bentuk Badan
PT Wijaya Karya – PT Jaya Konstruksi Manggala Pratama – Proyek Jalan Pangkalan Lada Berdasarkan Perjanjian Kerjasama Operasi, pada tanggal 21 Pebruari 2008 dari notaris Achmad
(4) Hasil analisis Threats (Ancaman) dalam penerapan 8 SNP pada SMP Negeri 2 Dolopo adalah perencanaan, sosialisasi, pelaksanaan dan evaluasi serta tindak lanjut yang tidak
Berdasarkan 2(dua) kelompok data tersebut, jika nilai rata-rata pada kolom G (sel G4) digunakan sebagai acuan, maka fungsi database yang tepat untuk mengisi data predikat seperti
Penerapan Model Inkuiri Terbimbing Berbantuan Media Animasi Komputer untuk Meningkatkan Motivasi dan Hasil Belajar Matematika Siswa Kelas V di SD Negeri 2
Kompetensi Bermain Gitar Elektrik Anggota Komunitas Rumah Gitar Mahasiswa Upi Divisi Gitar Klasik.. Universitas Pendidikan Indonesia | Repository.Upi.Edu |
Simpulan peneliti bahwa penerapan model inkuiri terbimbing berbantuan media barang bekas dapat meningkatkan keterampilan guru dalam mengajar, pemahaman konsep