BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1.Hasil Penapisan Fitokimia Air Kelapa
Uji penapisan fitokimia bertujuan untuk mengetahui beberapa kandungan fitokimia pada air kela pa, seperti alkaloid, flavonoid, tanin, saponin, steroid, dan fenolik. Hasil yang diperoleh adalah keempat air kelapa yang digunakan menunjukkan hasil negatif pada identifikasi alkaloid, flavonoid, saponin, dan steroid, sedangkan pada identifikasi tanin menunjukkan hasil yang positif (Tabel 4.1).
Tabel 4.1 Hasil Uji Penapisan Fitokimia
Keterangan: - = negatif; + = positif
Identifikasi alkaloid menunjukan hasil negatif karena tidak adanya endapan jingga coklat (Gambar 4.1). Identifikasi flavonoid yang dilakukan tidak memperlihatkan warna merah, sehingga kandungan flavonoidnya negatif (Gambar 4.2). Identifikasi tanin dikatakan positif karena tampak warna kuning kehijauan (Gambar 4.3). Identifikasi saponin menunjukkan hasil negatif sebab tidak timbul busa ketika dilakukan pengocokan (Gambar 4.4). Identifikasi steroid dikatakan negatif karena tidak tampak warna biru dan hijau (Gambar 4.5).
Fitokimia
Sampel Air Kelapa
Alkaloid Flavonoid Tanin Saponin Steroid
Air kelapa obat hijau - - + - -
Air kelapa obat coklat - - + - -
Air kelapa hijau - - + - -
Gambar 4.1 Identifikasi alkaloid (a) kelapa obat kuning; (b) kelapa obat hijau; (c) kelapa kuning; (d) kelapa hijau
Gambar 4.2 Identifikasi flavonoid (a) kelapa obat kuning; (b) kelapa obat hijau; (c) kelapa hijau; (d) kelapa kuning
Gambar 4.3 Identifikasi tanin (a) kelapa obat hijau; (b) kelapa obat kuning; (c) kelapa kuning; (d) kelapa hijau
a b c d
a b c d
Gambar 4.4 Identifikasi saponin (a) kelapa kuning; (b) kelapa obat kuning; (c) kelapa obat hijau; (d) kelapa hijau
Gambar 4.5 Identifikasi steroid (a) kelapa kuning; (b) kelapa hijau; (c) kelapa obat kuning; (d) kelapa obat hijau
4.1.2.Hasil Uji Efektivitas Antimikroba dan Pengukuran Zona Hambat
Kemampuan air kelapa muda menghambat pertumbuhan bakteri uji ditandai dengan terbentuknya zona bening di sekitar kertas cakram (Gambar 4.9, 4.10,
dan 4.11). Zona bening yang terbentuk diukur diameternya menggunakan jangka sorong. Data hasil pengukuran tersebut kemudian dianalisis menggunakan ANOVA, dan menunjukkan hasil bahwa antar perlakuan mempunyai pengaruh yang berbeda. Pada bakteri uji S.typhi dan Shigella sp. mempunyai pengaruh
a b c d
nyata, tetapi tidak berbeda nyata pada bakteri uji E.coli (Lampiran 2). Data diuji lebih lanjut menggunakan uji Duncan Multiple Range Test (DMRT) dengan hasil seperti tercantum dalam Tabel 4.2, Gambar 4.6, 4.7, dan 4.8.
Tabel 4.2 Hasil Uji Daya Hambat Antimikroba Air Kelapa Muda, Obat Diare, dan Aquades Terhadap Pertumbuhan Bakteri S. typhi, E. coli, dan Shigella sp.
Perlakuan
Diameter zona hambat pada bakteri (cm)
S. typhi E. coli Shigella sp.
Obat diare Lodia 0.953±0.206 b 0.827±0.015 1.233±0.101 b Kelapa Hijau 1.233±0.699 b 0.84±0.05 0.663±0.025 c Kelapa Obat Kuning 0.803±0.038 b 0.807±0.038 0.923±0.198 bc Kelapa Kuning 1.287±0.123 b 0.837±0.04 0.657±0.051 c Kelapa Obat Hijau 1.887±0.178 a 0.973±0.169 1.663±0.484 a Aquades 0,00 ±0,000 c 0.833±0.098 0.727±0.132 c Angka yang diikuti huruf sama tidak berbeda bermakna pada Duncan 5%
Gambar 4.6 Diagram BatangDiameter Zona Hambat Bakteri S. typhi
0.0
Gambar 4.7 Diagram BatangDiameter Zona Hambat Bakteri E. coli
Gambar 4.8 Diagram BatangDiameter Zona Hambat Bakteri Shigella sp.
Berdasarkan analisis DMRT yang telah dilakukan (Tabel 4.2), hasil menunjukkan bahwa perlakuan obat diare Lodia, kelapa hijau, kelapa obat kuning, dan kelapa kuning menunjukkan tidak berbeda nyata dalam mempengaruhi pertumbuhan bakteri S.typhi. Perlakuan kelapa obat hijau berbeda nyata terhadap semua perlakuan dan menunjukkan diameter yang terbesar yaitu 1,887 cm
Diameter Zona Hambat bakteri E. coli
0.0
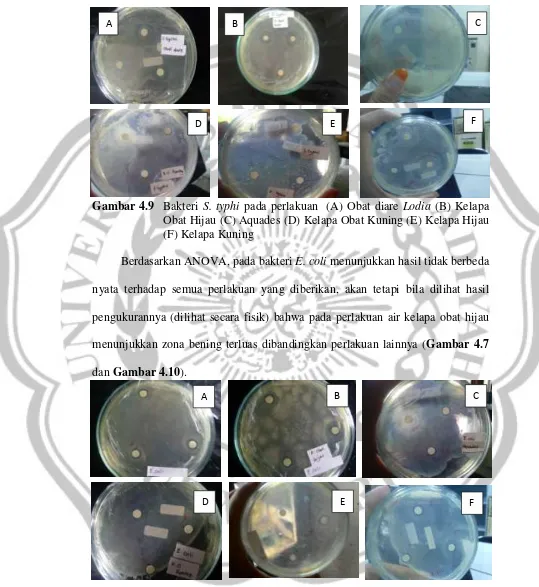
Gambar 4.9 Bakteri S. typhi pada perlakuan (A) Obat diare Lodia (B) Kelapa Obat Hijau (C) Aquades (D) Kelapa Obat Kuning (E) Kelapa Hijau (F) Kelapa Kuning
Berdasarkan ANOVA, pada bakteri E. coli menunjukkan hasil tidak berbeda nyata terhadap semua perlakuan yang diberikan, akan tetapi bila dilihat hasil pengukurannya (dilihat secara fisik) bahwa pada perlakuan air kelapa obat hijau menunjukkan zona bening terluas dibandingkan perlakuan lainnya (Gambar 4.7
dan Gambar 4.10).
Gambar 4.10 Bakteri E. coli pada perlakuan (A) Obat diare Lodia (B) Kelapa Obat Hijau (C) Aquades (D) Kelapa Obat Kuning (E) Kelapa Hijau (F) Kelapa Kuning
A
A B C
D E F
B
D
C
Berdasarkan Tabel 4.2 pada perlakuan kelapa obat hijau dengan perlakuan yang lain menunjukkan hasil yang berbeda nyata dalam mempengaruhi pertumbuhan bakteri Shigella sp. Pada perlakuan kelapa obat hijau mempunyai diameter zona hambat tertinggi yaitu sebesar 1,663 cm (Gambar 4.8 dan
Gambar 4.11).
Gambar 4.11 Bakteri Shigella sp. pada perlakuan (A) Obat diare Lodia (B) Kelapa Obat Hijau (C) Aquades (D) Kelapa Obat Kuning (E) Kelapa Hijau (F) Kelapa Kuning
4.2. Pembahasan
4.2.1.Penapisan Fitokimia Air Kelapa
Berdasarkan hasil uji penapisan fotokimia pada semua air kelapa yang digunakan dalam penelitian, metabolit sekunder yang ada pada air kelapa adalah tanin (Tabel 4.1). Hasil penelitian menunjukkan hasil yang sama dengan teori yang dikemukakan oleh Kurniati (2010), air kelapa muda mengandung tanin atau antidotum (antiracun). Kusumaningrum (2010) mengatakan bahwa tanin mempunyai rasa sepat dan juga bersifat antibakteri dan astringent.
A B C
Dari hasil penelitian tampak adanya perubahan warna pada semua air kelapa yang diujikan. Akan tetapi warna yang tampak setelah pengujian adalah kuning kehijauan bukan warna hujau kehitaman (Gambar 4.3). Diduga karena kadar tanin yang ada pada air kelapa rendah, sehingga ketika dilakukan pengujian tidak tampak warna hijau kehitaman.
Perubahan warna terjadi ketika penambahan FeCl3 yang bereaksi dengan salah satu gugus hidroksil pada senyawa tanin, penambahan FeCl3 pada ekstrak uji menghasilkan warna hijau kehitaman yang menunjukkan mengandung senyawa tanin (Nirwana et al, 2015) atau hijau violet (Masitoh, 2011). Terjadinya pembentukan warna ini karena terbentuknya senyawa kompleks antara logam Fe dan tanin. Senyawa kompleks terbentuk karena adanya ikatan kovalen koordinasi antara ion atau atom logam dengan atom non logam (Latifah, 2015).
4.2.2.Pembahasan Uji Efektivitas Antimikroba
Berdasarkan hasil penelitian yang telah dilakukan diperoleh hasil bahwa air kelapa muda mampu menghambat pertumbuhan bakteri E. coli, Salmonella typhi, dan Shigella sp. Tanda adanya daya hambat air kelapa muda ditunjukkan dengan adanya zona bening pada daerah sekitar kertas cakram (Gambar 4.9, 4.10, 4.11). Zona bening tersebut menunjukkan bahwa tidak ada pertumbuhan bakteri, artinya bakteri mengalami kematian, diduga karena zat yang terkandung dalam larutan uji.
diameter zona hambat secara berturut-turut 0,953 cm, 0,827 cm, dan 1,233 cm (Tabel 4.2).
Hal tersebut diduga karena komposisi dari obat diare. Bahan aktif dari Lodia adalah Loperamide HCl. Lodia merupakan obat antibiotik untuk diare (Anonim, 2018). Ada beberapa mekanisme kerja antibiotik menurut Pratama (2013), yaitu dengan menghambat sintesis dinding sel bakteri, bekerja langsung pada membran sel mikroorganisme, meningkatkan permeabilitas dan menyebabkan kebocoran senyawa intraseluler, mengganggu fungsi subunit ribosom 30S atau 50S untuk menghambat sintesis protein secara reversibel, berikatan pada subunit ribosom 30S dan mengganggu sintesis protein, mempengaruhi metabolisme asam nukleat bakteri, dan menahan enzim-enzim penting dari metabolisme folat.
Lain halnya dengan Muhlisin (2018), yang mengatakan bahwa Loperamide
merupakan obat antimotilitas. Menurut Samiadi (2018) cara kerja Loperamide
adalah dengan memperlambat gerak usus dan membuat feses menjadi lebih padat.
Loperamide juga digunakan untuk mengurangi jumlah cairan yang keluar pada pasien yang dilakukan ileostomi, dan untuk mengobati diare pada orang dengan penyakit radang usus.
lebih tinggi dibandingkan kelapa jenis lainnya sehingga khasiatnya lebih cepat terasa oleh tubuh.
Mekanisme penghambatan tanin terhadap bakteri adalah dengan merusak membran sel, inaktivasi enzim-enzim esensial, dan dekstruksi fungsi material genetik (Kusumaningrum, 2012). Mekanisme kerja tanin sebagai antibakteri adalah menghambat enzim reverse transkriptase dan DNA topoisomerase sehingga sel bakteri tidak dapat terbentuk (Nuria et al., 2009). Tanin memiliki aktifitas antibakteri yang berhubungan dengan kemampuannya untuk menginaktifkan adhesin sel mikroba juga menginaktifkan enzim, dan menggangu transport protein pada pada lapisan dalam sel (Cowan, 1999).
mengalami lisis. Hal ini diakibatkan peristiwa osmosis yaitu perpindahan air dari lingkungan hipotonis ke hipertonis. Akibatnya sel akan mengembang dan lama kelamaan pecah.